Вирус эпштейн барра у детей жить здорово
Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела (Ат) к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80–100% взрослых [3, 13]. Заболеваемость острой формой ЭБВИ (ОЭБВИ) в различных регионах мира колеблется от 40 до 80 случаев на 100 тыс. населения [2]. Хроническая форма ЭБВИ (ХЭБВИ) развивается у 15–25% лиц после ОЭБВИ [1, 5, 15]. Установлена роль ВЭБ в развитии злокачественных новообразований, аутоиммунных заболеваний и синдрома хронической усталости [3, 5, 14, 15]. Все это свидетельствует об актуальности проблемы ЭБВИ.
ВЭБ, открытый в 1964 г. M. Epstein и Y. Barr, относится к γ-герпес-вирусам [3]. ВЭБ имеет в своем составе 3 антигена: капсидный (VCA), ранний (EA) и ядерный (EBNA). Своеобразие патологического процесса при ЭБВИ определяется способностью ВЭБ к трансформации В-лимфоцитов, пожизненной персистенции в организме человека, индукции вторичного иммунодефицитного состояния (ИДС), аутоиммунных реакций, злокачественных опухолей [1, 3, 5, 12].
Источник заражения ВЭБ — больные манифестными и бессимптомными формами. 70–90% лиц, перенесших ОЭБВИ, выделяют вирус в последующие 1–18 мес. Пути передачи ВЭБ: воздушно-капельный, контактно-бытовой, парентеральный, половой, вертикальный. ОЭБВИ характеризуется эпидемическими подъемами 1 раз в 6–7 лет, чаще регистрируется в возрасте от 1 до 5 лет, в организованных коллективах [4, 7, 9].
Входные ворота для ВЭБ — слизистая оболочка верхних дыхательных путей: вирус проникает в лимфоидную ткань, инфицирует В-лимфоциты, развивается поликлональная активация В-лимфоцитов, диссеминация возбудителя в составе В-лимфоцитов, синтез антител (Ат) в ответ на антигенную стимуляцию снижен. В первую очередь ВЭБ поражает лимфоидные органы (миндалины, печень, селезенку).
Следующий этап — образование клона сенсибилизированных цитотоксических CD8-клеток, последовательный синтез Ат к VCA-, EA- и EBNA-антигенам вируса. Вследствие нарушения иммунного ответа, функциональной активности факторов врожденной резистентности (нейтрофилов, макрофагов, NK-клеток, системы интерферона) формируется вторичное ИДС [2–4, 12].
Иммунный статус 109 больных ОЭБВИ в возрасте от 5 до 14 лет в нашей работе выявил признаки активации Т-клеточного звена иммунной системы — повышение количества Т-лимфоцитов (CD3), цитотоксических Т-лимфоцитов (CD8), клеток с маркерами поздней активации (HLA-DR); поликлональную активацию В-лимфоцитов — увеличение количества CD20-клеток, иммуноглобулинов (Ig) IgA, IgM, IgG, циркулирующих иммунных комплексов (ЦИК). Обнаружены признаки угнетения иммунной системы: нормальное содержание Т-хелперов (CD4), снижение иммунорегуляторного индекса CD4/CD8, количества естественных киллерных клеток NK (CD16), повышение готовности иммунокомпетентных клеток к апоптозу (CD95). Наблюдалась активация кислородзависимого метаболизма нейтрофилов и редукция его адаптационных возможностей.
У трети обследованных детей (33,9%) ОЭБВИ протекала в форме микст-инфекции с цитомегаловирусами (ЦМВ), вирусами простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2). При бактериологическом исследовании мазков из ротоглотки у 41,3% пациентов выделены Streptococcus (S.) viridans, у 11,9% — Candida albicans, у 8,2% — Staphilococcus (Staph.) epidermidis, у 6,4% — S. pyogenes, у 2,7% — Klebsiella (Kl.) pneumoniae, у 41,3% — ассоциация бактерий. У 43,1% пациентов — серологические маркеры активной формы хламидийной инфекции, у 30,3% — микоплазмоза.
Возможны следующие исходы ОЭБВИ: латентная инфекция, ХЭБВИ, ИДС, онкологические, аутоиммунные заболевания, синдром хронической усталости [5, 8, 10, 11]. Переход в ХЭБВИ связан с комплексом неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушением нейроиммунноэндокринной регуляции, генетической предрасположенностью.
Проведенное нами обследование 60 детей в возрасте от 5 до 14 лет с ХЭБВИ показало, что в этой группе у 86,7% матерей имел место отягощенный акушерский анамнез; у 83,3% детей обнаружены перинатальная и постнатальная патология ЦНС, ЛОР-органов и др.
В иммунном статусе больных ХЭБВИ выявлено увеличение содержания антагониста интерлейкина-1 (ИЛ-1RA), недостаточная активация иммунокомпетентных клеток (уменьшение HLA-DR) и повышение их готовности к апоптозу (увеличение CD95). Отмечалось нарушение функциональной активности Т-хелперов 1 типа (Th1) (снижение содержания интерферона γ (ИФН γ)); уменьшение общего пула Т-клеток (CD3), количества лимфоцитов с рецепторами к ИЛ-2 (CD25) и NK-клеток (CD16); содержание цитотоксических CD8-лимфоцитов было повышено. Сохранение маркеров репликации ВЭБ на протяжении длительного времени в этой группе свидетельствовало о нарушении элиминации вируса; при этом отмечались повышение функциональной активности Th2, поликлональная активация В-лимфоцитов (CD20), повышение содержания IgA, IgM, IgG, ЦИК, снижение уровня хемотаксического фактора нейтрофилов (ИЛ-8), изменение их метаболизма.
Нарушения иммунного статуса приводили к активации условно-патогенной микрофлоры, вирусных и грибковых инфекций. В микробном спектре слизистой ротоглотки пациентов с ХЭБВИ выделены S. Viridans (30%), Candida albicans (28,3%), Staph. Epidermidis (25%), S. Pyogenes (20%), Kl. Pneumoniae (8,4%), ассоциация бактерий (41,7%); у 28,3% — серологические маркеры активной формы хламидиоза, у 26,7% — микоплазмоза. У 90% пациентов заболевание протекало в форме микст-инфекции с участием герпес-вирусов: ВЭБ + ЦМВ, ВЭБ + ВПГ-1, ВПГ-2.
Классификация. Общепринятая классификация заболевания отсутствует; рекомендуем использовать разработанную нами рабочую классификацию ЭБВИ.
- По периоду возникновения: врожденная, приобретенная.
- По форме: типичная (инфекционный мононуклеоз), атипичная: стертая, бессимптомная, висцеральная.
- По тяжести: легкая, среднетяжелая, тяжелая.
- По течению: острая, затяжная, хроническая.
- По фазе: активная, неактивная.
- Осложнения: гепатит, разрыв селезенки, менингоэнцефалит, полирадикулонейропатия, миокардит, синусит, отит, гемолитическая анемия, тромбоцитопения, нейтропения, панкреатит и др.
- Микст-инфекция.
Примеры оформления диагноза:
- Осн.: Приобретенная ЭБВИ, типичная тяжелая форма (инфекционный мононуклеоз), острое течение, активная фаза. Осл.: Острый гепатит.
- Осн.: Приобретенная ЭБВИ, висцеральная форма (менингоэнцефалит, гепатит, нефрит), тяжелое хроническое течение, активная фаза. Осл.: острая печеночно-почечная недостаточность. Сопp.: Респираторный хламидиоз (ринофарингит, бронхит, пневмония).
Клиническая картина острой ЭБВИ впервые была описана Н. Ф. Филатовым (1885) и Е. Пфейфером (1889). Инкубационный период длится от 4-х дней до 7 нед. Полный симптомокомплекс формируется к 4–10-му дням болезни [4, 7].
Нами обследованы 109 детей с ОЭБВИ. У большинства пациентов заболевание начинается остро, с повышения температуры тела и появления симптомов интоксикации; реже отмечается постепенное начало: несколько дней наблюдается недомогание, слабость, вялость, снижение аппетита. Температура тела субфебрильная или нормальная. Ко 2–4-му дням болезни температура достигает 39–40 °С; лихорадка и симптомы интоксикации могут сохраняться в течение 2–3 и более недель.
Тонзиллит — наиболее частый и ранний симптом ОЭБВИ, сопровождается увеличением миндалин до II-III степени. Лакунарный рисунок подчеркнут за счет инфильтрации ткани миндалин или сглажен из-за лимфостаза. На миндалинах — налеты желтовато-белого или грязно-серого цвета в виде островков, полосок. Они исходят из лакун, имеют шероховатую поверхность (напоминают кружево), легко снимаются без кровоточивости, растираются, не тонут в воде. Характерно несоответствие размера налета и степени увеличения регионарных ЛУ. При фибринозно-некротическом характере налетов в случае их распространения за пределы миндалин необходим дифференциальный диагноз с дифтерией. Налеты на миндалинах исчезают, как правило, через 5–10 дней.
Гепатомегалия может быть обнаружена с первых дней болезни, однако чаще выявляется на второй неделе. Нормализация размеров печени происходит в течение полугода. У 15–20% больных в качестве осложнения развивается гепатит.
Спленомегалия относится к поздним симптомам, встречается у большинства больных. Нормализация размеров селезенки происходит в течение 1–3 нед.
Экзантема при ОЭБВИ появляется на 3–14-й дни болезни, имеет полиморфный характер — пятнистая, папулезная, пятнисто-папулезная, розеолезная, мелкоточечная, геморрагическая. Определенной локализации нет. Сыпь наблюдается в течение 4–10 дней, иногда оставляет пигментацию. У детей, получавших ампициллин или амоксициллин, сыпь появляется чаще (90–100%).
Гематологические изменения включают лейкоцитоз (10–30 х 10 9 /л), нейтропению с палочкоядерным сдвигом влево, увеличение количества лимфоцитов, моноцитов, атипичных мононуклеаров до 50–80%, повышение СОЭ до 20–30 мм/час. Характерный гематологический признак — атипичные мононуклеары в количестве 10–50%: они появляются к концу первой недели заболевания, сохраняются в течение 1–3 нед.
Хроническая ЭБВИ является исходом ОЭБВИ или развивается как первично-хроническая форма [2, 5, 8, 10, 11, 15]. Нами обследовано 60 детей с ХЭБВИ, клиника которой включала хронический мононуклеозоподобный синдром и полиорганную патологию. У всех пациентов обнаружены лимфопролиферативный синдром (генерализованная лимфаденопатия, гипертрофия небных и глоточной миндалин, увеличение печени и селезенки) и признаки хронической интоксикации (длительный субфебрилитет, слабость, снижение аппетита и др.). Вследствие развития ИДС наблюдались острые инфекции респираторного тракта и ЛОР-органов с обострениями до 6–11 раз в год: ринофарингиты (28,3%), фаринготонзиллиты (91,7%), аденоидиты (56,7%), отиты (11,7%), синуситы (20%), ларинготрахеиты (18,3%), бронхиты (38,3%), пневмонии (25%). Обращала внимание высокая частота полиорганной патологии, обусловленная длительной репликацией ВЭБ, вторичным ИДС, аутоиммунными реакциями (патология ЦНС; хронический гастрит, дискинезия желчевыводящих путей; кардиальный синдром, артралгии).
В последние годы описана врожденная ЭБВИ. Установлено, что риск ее при первичной ЭБВИ во время беременности составляет 67%, при реактивации — 22%. Клиника врожденной ЭБВИ сходна с ЦМВИ.
Установлена роль ВЭБ в развитии онкологических заболеваний и паранеопластических процессов — лимфомы Беркетта, назофарингеальной карциномы, лимфогранулематоза, опухолей желудка, кишечника, слюнных желез, матки, лейкоплакии языка и слизистой ротовой полости, а также ряда аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена, лимфоидного интерстициального пневмонита, хронического гепатита, увеита и др. [3, 5, 14, 15]. ВЭБ, наряду с вирусами герпеса человека 6 и 7 типов, является этиологическим фактором синдрома хронической усталости и наиболее частой причиной (15%) развития длительной лихорадки неясного генеза.
Диагностика ЭБВИ основана на учете групп риска, ведущих клинических синдромов и данных лабораторного исследования [8–11]. К группам риска у матери относят отягощенный анамнез, маркеры герпес-вирусных инфекций и др., у ребенка — перинатальное поражение ЦНС, аллергический фенотип, ИДС, маркеры герпес-вирусных инфекций и др. Ведущими клиническими синдромами ЭБВИ являются мононуклеозоподобный, общеинфекционный синдромы, экзантема, синдром полиорганной патологии.
В обязательный стандарт диагностики ЭБВИ входят клинический анализ крови, общий анализ мочи, биохимическое исследование крови, бактериологическое исследование слизи ротоглотки и носа, серологические маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм, УЗИ органов брюшной полости, консультация ЛОР-врача, по показаниям — рентгенография придаточных пазух носа, органов грудной клетки, ЭКГ. Дополнительный стандарт диагностики (в специализированном лечебно-профилактическом учреждении): маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм методом полимеразной цепной реакции (ПЦР), иммунограмма второго уровня, консультация иммунолога, по показаниям — коагулограмма, морфологическая картина стернальной пункции, консультация гематолога, онколога.
Методом иммуноферментного анализа (ИФА) определяют Ат к антигенам ВЭБ, что позволяет осуществить лабораторную диагностику ЭБВИ и определить период инфекционного процесса.
Ат класса IgM к VCA появляются одновременно с клиникой ОЭБВИ, сохраняются в течение 2–3 мес, повторно синтезируются при реактивации ВЭБ. Длительная персистенция высоких титров этих Ат характерна для ХЭБВИ, ВЭБ-индуцированных опухолей, аутоиммунных заболеваний, ИДС.
Ат класса IgG к EA достигают высокого титра на 3–4-й нед ОЭБВИ, исчезают через 2–6 мес. Они появляются при реактивации, отсутствуют при атипичной форме ЭБВИ. Высокие титры Ат данного класса выявляют при ХЭБВИ, ВЭБ-индуцированных онкологических и аутоиммунных заболеваниях, ИДС.
Ат класса IgG к EBNA появляются через 1–6 мес после первичной инфекции. Затем их титр уменьшается и сохраняется в течение всей жизни. При реактивации ЭБВИ происходит повторное увеличение их титра.
Большое значение имеет исследование авидности Ат класса IgG (прочности связывания антигена с Ат). При первичной инфекции сначала синтезируются Ат с низкой авидностью (индекс авидности (ИА) менее 30%). Для поздней стадии первичной инфекции характерны Ат со средней авидностью (ИА — 30–49%). Высокоавидные Ат (ИА — более 50%) образуются через 1–7 мес после инфицирования ВЭБ.
Серологическими маркерами активной фазы ЭБВИ являются Ат IgM к VCA и Ат IgG к EA, низкая и средняя авидность Ат IgG к маркерам неактивной фазы, Ат IgG к EBNA.
Материалом для ПЦР служат кровь, ликвор, слюна, мазки со слизистой ротоглотки, биоптаты органов и др. Чувствительность ПЦР при ЭБВИ (70–75%) ниже, чем при других герпесвирусных инфекциях (95–100%). Это связано с появлением ВЭБ в биологических жидкостях лишь при иммуноопосредованном лизисе инфицированных В-лимфоцитов.
На основании опыта лечения 169 детей с ЭБВИ нами разработан стандарт лечения этого заболевания.
Базисная терапия: охранительный режим; лечебное питание; противовирусные препараты: вироцидные препараты — инозин пранобекс (Изопринозин), аномальные нуклеозиды (Валтрекс, Ацикловир), Арбидол; препараты ИФН — рекомбинантный ИФН α-2β (Виферон), Кипферон, Реаферон-ЕС-Липинт, интерфероны для в/м введения (Реаферон-EC, Реальдирон, Интрон А, Роферон А и др.); индукторы ИФН — Амиксин, сверхмалые дозы антител к γ-ИФН (Анаферон), Циклоферон, Неовир. По показаниям: локальные антибактериальные препараты (Биопарокс, Лизобакт, Стопангин и др.); системные антибактериальные препараты (цефалоспорины, макролиды, карбапенемы); иммуноглобулины для внутривенного введения (Иммуновенин, Габриглобин, Интраглобин, Пентаглобин и др.); витаминно-минеральные комплексы — Мульти-табс, Вибовит, Санасол, Киндер Биовиталь гель и др.
Интенсификация базисной терапии по показаниям:
Симптоматическая терапия.
При лихорадке — жаропонижающие препараты (парацетамол, ибупрофен и др.); при затруднении носового дыхания — назальные препараты (Изофра, Полидекса, Називин, Виброцил, Адрианол и др.); при сухом кашле — противокашлевые препараты (Глаувент, Либексин), при влажном кашле — отхаркивающие и муколитические препараты (АмброГЕКСАЛ, бромгексин, ацетилцистеин и др.).
В течение нескольких лет для лечения ЭБВИ мы с успехом применяем схему комбинированной этапной этиотропной терапии, в которую входят инозин пранобекс (Изопринозин) и рекомбинантный интерферон α-2β (Виферон) (рис. 1, 2). Инозин пранобекс (Изопринозин) подавляет синтез вирусных белков и тормозит репликацию широкого спектра ДНК- и РНК-содержащих вирусов, в том числе ВЭБ [3]. Препарат обладает иммунокорригирующей активностью — модулирует иммунный ответ по клеточному типу, стимулирует продукцию Ат, цитокинов, ИФН, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток; предохраняет пораженные клетки от поствирусного снижения синтеза белка. Инозин пранобекс (Изопринозин) назначался по 50–100 мг/кг/сут внутрь в 3–4 приема. Проводили три курса лечения по 10 дней с интервалом 10 дней. Рекомбинантный ИФН α-2β (Виферон) тормозит репликацию вирусов за счет активации эндонуклеазы, разрушения вирусной матричной РНК [6]. Препарат модулирует иммунный ответ, способствует дифференцировке В-лимфоцитов, стимулирует выработку цитокинов, повышает функциональную активность макрофагов, нейтрофилов и NK-клеток. Входящие в его состав природные антиоксиданты (витамины Е и С) стабилизируют клеточные мембраны. Препарат назначали по пролонгированной схеме (В. В. Малиновской и соавт., 2006) [6].
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p Рис. 2. Механизмы этиопатогенетического действия комбинации инозина пранобекса (Изопринозина) и рекомбинантного интерферона α-βb (Виферона) при Эпштейна-Барр вирусной инфекции у детей
Комбинированная терапия при ОЭБВИ способствовала модуляции иммунного ответа по клеточному типу (увеличение CD3-, CD4-, CD8-, CD16- и HLA-DRT-лимфоцитов). Снижалась готовность иммунокомпетентных клеток к апоптозу (CD95). Отмечались стимуляция выработки IgA, переключение синтеза Ат с IgM на IgG, снижение содержания ЦИК, улучшались показатели метаболизма нейтрофилов.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону

Самые распространенные среди детей заболевания — вирусные. Причина в том, что иммунитет ребенка еще недостаточно крепкий, незрелый, и ему не всегда бывает легко противостоять многочисленным угрозам извне. Но если о гриппе и ветрянке сказано и написано много, да и с корью мамам все более-менее понятно, то есть в этом мире вирусы, одни названия которых нагоняют на родителей священный ужас.
Один из таких малоизученных и очень часто встречающихся — вирус Эпштейна-Барр. О нем довольно часто спрашивают известного педиатра и телеведущего Евгения Комаровского.


Что это такое
ВЭБ — вирус Эпштейна Барр. Один из самых распространенных вирусов на планете. Впервые был найден в образцах опухолей и описан в 1964 году английским профессором Майклом Эпштейном и его ассистенткой Ивонной Барр. Это вирус герпеса четвертого типа.
По медицинской статистике, следы перенесенной инфекции обнаруживаются в анализах крови половины детей в возрасте 5-6 лет и у 97% взрослых, причем сами они об этом зачастую даже не догадываются, ведь у большинства людей ВЭБ протекает незаметно, без симптомов.

Самая излюбленная среда обитания вируса — лимфоциты, таким образом он поражает иммунную систему ребенка. Чаще всего эта микроскопическая частица-паразит вызывает цитомегаловирус, инфекционный мононуклеоз, лимфогранулематоз, гепатит, герпес, лимфому Беркитта и ряд других малоприятных диагнозов. Вакцины от этого недуга еще не изобретено, так как на разных стадиях своего развития вирус кардинально меняет свой белковый состав и лучшие ученые умы за ним просто не успевают.


Инфицирование может произойти во время переливания крови и ее компонентов, через общие с больным вещи и игрушки, а также вирус передается от зараженной матери через плаценту плоду во время беременности. ВЭБ легко распространяется воздушно-капельным путем, а также от донора к реципиенту во время трансплантации костного мозга.



Инкубационный период -от 1 до 2 месяцев, после чего у детей развиваются яркие симптомы, свойственные многим вирусным инфекциям.
Впрочем, не так страшен сам вирус со сложным названием, сколько то, что его последствия совершенно непредсказуемы. Он может пройти совершенно не заметно у одного ребенка, а у другого станет причиной развития тяжелых состояний и даже онкологических заболеваний.

Комаровский о ВЭБ
А теперь послушаем доктора Комаровского об инфекционном монокулезе.
Симптомы, которые позволяют заподозрить у ребенка ВЭБ, довольно размыты:
- Раздражительность, плаксивость, повышенная капризность и частая беспричинная усталость.
- Легкое или более заметное увеличение лимфатических узлов. Чаще всего — подчелюстных и заушных. Если инфекция протекает тяжело — по всему телу.
- Отсутствие аппетита, проблемы с пищеварением.
- Сыпь.
- Высокая температура (до 40,0).
- Боли в горле (как при ангине и фарингите).
- Сильная потливость.
- Небольшое увеличение размеров печени и селезенки. У ребенка это может проявляться ноющими болями в животе.
- Желтушность кожных покровов. Этот симптом встречается крайне редко.

Комаровский подчеркивает, что на основании одних только жалоб и наличия тех или иных симптомов поставить диагноз нельзя, поскольку состояние ребенка будет напоминать и ангину, и энтеровирус, и лимфогранулематоз.


Симптомы при заболевании могут отличаться
Что такое инфекционный мононуклеоз
Ученый Майкл Эпштейн со своей аспиранткой Ивонной Барр в 1964 году впервые описали этот вирус. Первоначальное научное название Epstein-Barr virus было изменено в 1979 году на Human herpesvirus 4, а в 2016 еще раз, теперь его название звучит Human gammaherpesvirus 4.
Передается этот вирус несколькими способами:
- воздушно-капельным;
- контактно-бытовым;
- парентеральным, минуя пищеварительный тракт;
- половым;
- вертикальным, от матери к плоду.
Часто ни врачи, ни родители не замечают появление этого вируса у ребенка, заболевание протекает в большинстве случаев довольно легко. У взрослых симптомы более тяжелые, проявляется типичный инфекционный мононуклеоз.
Диагностика
Заболевание очень многоликое. Проявляться может по-разному, искажать общую картину течения сопутствующих заболеваний, обязателен забор крови для подтверждения наличия вируса.
Основными причинами назначения гемолитического исследования являются такие состояния:
- тонзиллит;
- увеличение лимфоузлов;
- лихорадка;
- увеличенные печень или селезенка.
Специфические антитела в крови помогают определить наличие вируса Эпштейна-Барр. О наличии острой инфекции расскажет обнаруженный IgM. О контакте, но отсутствии острого болезненного процесса сообщит IgG положительный. Повышение лейкоцитов в крови и СОЭ, наличие мононуклеаров в биохимическом анализе, а также УЗИ печени и селезенки могут подтвердить заболевание. В первую очередь требуется сдать анализ крови.
Симптомы
Развиваться болезнь может постепенно или с появлением острых симптомов:
- высокая температура от 38 градусов;
- лихорадка;
- озноб или потливость выше нормы;
- головные боли;
- ломота и мышечные боли;
- неприятные ощущения в горле, особенно при сглатывании.
Это состояние может сопровождать ребенка довольно долго, до месяца, при этом температура может появляться и пропадать. Отек лимфоузлов, в частности на затылке, под челюстями, на задней части шеи является также признаком, говорящем о возможном проявлении вируса. Они могут болеть довольно долго, до нескольких лет, если не пройти необходимую терапию, возможно даже увеличение их количества.
Инфекционный мононуклеоз может проявляться в виде:
- ангины, характеризующейся покраснением, появлением зернистости слизистой, кровоизлияний на поверхности, фолликулярной гиперплазией;
- характерной мононуклеозной сыпи;
- увеличении печени или селезенки, больше распространено у взрослых, но зафиксировано также у детей.
Возможно проявление других болезней, таких как тонзиллит, бронхит или трахеит, а также пневмония или желтуха. Нет единой картины развития вирусной инфекции, многое зависит от возраста, иммунитета, наличия других болезней.
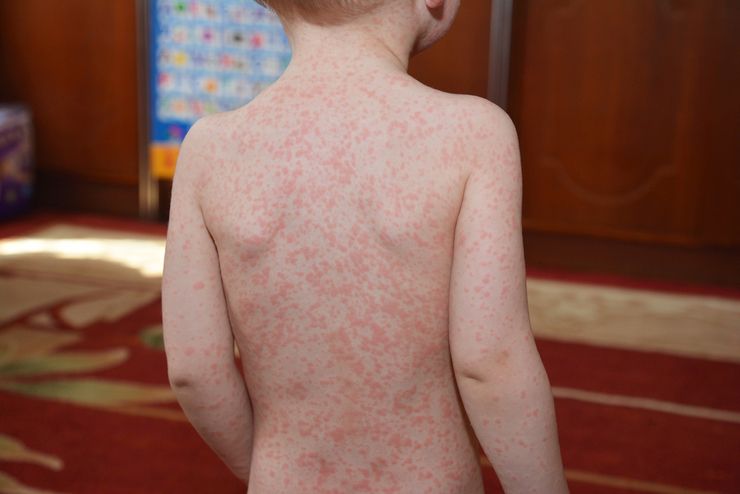
Один из симптомов – появление сыпи
Вирус Эпштейна-Барр у детей может сопровождаться бессонницей, поносом, головокружением, болями в животе. Инкубационный период 7–21 дней – норма для этого заболевания.
Лечение
Конкретной терапии по герпесоподобному вирусу Эпштейна-Барр у детей нет. Используется симптоматическая терапия и поддерживающая.
Запрещается использовать ацетилсалициловую кислоту или аспирин, а также медикаменты, содержащие парацетамол.
В большинстве случаев лечение проводится в домашних условиях, показания к госпитализации:
- гипертермия 39,5С;
- интоксикация, сопровождающаяся рвотой, диареей, мигренями;
- присоединение других заболеваний, появление осложнений;
- полиаденит с возможной асфиксией.
Вирус Эпштейна-Барр должен быть дифференцирован с вирусными и бактериальными болезнями респираторного характера, в том числе дифтерией или краснухой, лейкозом и другими, протекающими со сходными симптомами. Предписано соблюдать постельный режим, необходимо обеспечить максимальный покой, дробное диетическое питание. Прогулки на свежем воздухе осуществимы при более легком течении болезни, физические нагрузки и возможность переохлаждения должны быть исключены.
Эффективность лечения проверяется назначением анализов, сдавать их следует после выздоровления.
Могут ли быть осложнения?
Частым осложнением является присоединение другого заболевания. Самым опасным считается разрыв селезенки вследствие ее отека и увеличения. Такие случаи фиксируются у 0,1% больных, они несут угрозу жизни, требуется срочная операция.
Повторный инфекционный процесс может начаться в связи с появлением стафилококков или стрептококков. Кроме этого, могут развиться следующие заболевания:
- менингоэнцефалит;
- интерстициальная пневмония;
- печеночная недостаточность;
- гепатит;
- анемия;
- неврит;
- кардиологические болезни.
При своевременной терапии общий прогноз вполне благоприятен. Переход заболевания в хроническую форму возможен при неправильной диагностике либо при несоблюдении назначений врача.
Считается, что вирус Эпштейна-Барр может спровоцировать развитие онкологических болезней. При этом болеть не обязательно, достаточно быть носителем вируса. Клинически подтверждено, что резкое снижение иммунитета способно привести к таким последствиям, однако подобных случаев довольно мало.
Практически полгода после лечения ребенка могут сопровождать высокая утомляемость и необходимость в более частом отдыхе. Лучше устраивать ребенку дневной сон независимо от возраста, ограждать от эмоциональных нагрузок, снизить физическую активность. В период восстановления после болезни плановая вакцинация приостанавливается.
Профилактика
На сегодняшний день не существует специальных средств, которые могли бы защитить от заболевания вирусом Эпштейна-Барр. После выздоровления человек продолжает выделять в окружающую среду вирус, потому карантин не предусмотрен.
Главными профилактическими действиями считаются:
- полноценный рацион;
- регулярные занятия спортом, закаливание;
- поддержание режима дня;
- снижение уровня стресса;
- употребление витаминных комплексов при необходимости.
Регулярное посещение педиатра поможет своевременно обнаружить заболевание, в другом случае последствия могут быть самыми плачевными. Профилактические консультации докторов узкоих специальностей избавят от осложнений.
Читайте также:


