Вирусная нагрузка при cin
В борьбе с COVID-19 медики во всем мире платят высокую цену. Несмотря на защитную одежду и маски, врачи и медсестры более подвержены заражению, чем большинство людей, а также имеют высшее вероятность тяжелого течения болезни.
Почему так происходит пишет британская газета The Telegraph.
Вирусная нагрузка – это количество вируса, которое есть в организме человека.
С медицинской точки зрения это значит, какой объем вируса находится в крови или плазме. Термин “вирусная нагрузка” обычно используется, когда речь идет о ВИЧ: пациенты, чьи состояния хорошо контролируются и находятся на правильном лечении, имеют неопределяемую вирусную нагрузку, что означает, что они не могут передать болезнь другим.

“Инфекционная доза” – это количество вируса, которое должно попасть в организм, чтоб человек заболел. В случае с вирусом гриппа людям для заболевания нужно совсем небольшое количество частиц. Касательно COVID-19 ученые еще не знают, какая должна быть доза, но она, вероятно, будет относительно небольшой из-за большого количества заболевших людей.
Согласно исследованию двух других коронавирусов (SARS и MERS), если человек получит более высокую дозу вируса, то болезнь будет протекать более тяжелее.

“Исходя из предыдущей работы по коронавирусам SARS и MERS, мы знаем, что воздействие более высоких доз связано с худшим исходом, и это может касаться и COVID-19”, – отметил профессор микробиологии и инфекции в Университете Бирмингема Виллем ван Шайк.
“В случае с респираторными вирусами – тяжело заболел ли ты или просто простудился – иногда определяется количеством вируса, который на самом деле попал в ваше тело и начал заражение. Все дело в размерах “армий на каждой стороне битвы”, очень большая армия вирусов трудна для сражения армии нашей иммунной системы”, – подчеркнула глава департамента инфекционных заболеваний в Имперском колледже Лондона профессор Венди Барклай.
Возраст и наличие у человека основного заболевания также играют роль в тяжести и исходе заболевания.

Фото: The Telegraph
Может показаться, что уровни вирусной нагрузки влияют на людей по-разному.
Врачи, изучающие вспышку в Ломбардии на севере Италии, осмотрели более 5000 человек и сравнили мазки из носа тех, у кого были симптомы, с теми, у кого не было. Они не обнаружили различий в вирусной нагрузке между двумя группами – однако, по их словам, поскольку они изучали лишь небольшое количество людей без симптомов, они не могли сделать четкие выводы.
Работники здравоохранения, которые контактируют непосредственно с пациентами, подвергаются особенно высокому риску, и именно поэтому врачи и медсестры так обеспокоены из-за нехватки средств индивидуальной защиты таких, как перчатки, очки и маски.
Такая нехватка является проблемой во всем мире, и во Франции врачи подают в суд на правительство за то, что оно не сумело накопить средства защиты.
Кроме того, люди, которые ухаживают за больными дома, также подвергаются риску. Именно поэтому Всемирная организация здравоохранения рекомендует в случае заболевания COVID-19 спать в отдельной комнате и по возможности использовали другую ванную комнату и туалет.
По словам научного сотрудника по системной биологии Лондонской школы гигиены и тропической медицины, доктора Эдварда Паркера, в то время как пациенты, которые явно больны и представляют риск, низкие дозы вируса также могут быть вредными из-за их кумулятивного эффекта.
“Исследования на мышах также показали, что повторное воздействие низких доз может быть таким же заразным, как разовая высокая доза. В общем, для нас крайне важно ограничить все возможные воздействия COVID-19, будь то люди с высокой степенью симптомов, кашляющих большими количествами вируса, или люди с бессимптомным течением, у которых небольшие количества”, – говорит он.
Исследование, проведенное на девяти пациентах с легкими симптомами, показало, что период, когда они были наиболее заразными пришелся на первую неделю после появления первых симптомов. Отмечается, что пациенты выделяют чрезвычайно большое количество вируса на ранней стадии.
Этот очень высокий показатель помогает объяснить, почему вирус так быстро распространился по всему миру.
Около 5000 работников здравоохранения в Италии и 3000 в Китае заразились этой болезнью. В Великобритании пока неизвестно, сколько работников здравоохранения заразилось, хотя многие сотрудники заболели – они могли подхватить заболевание в течение своей повседневной жизни, а не непосредственно от пациента.
В Украине среди госпитализированных пациентов с коронавирусом COVID-19 есть 26 медицинских работников.
- В Украине по состоянию на утро подтверждено 804 случая заражения коронавирусом COVID-19. За сутки было зафиксировано 135 новых случаев.
- По оценкам Всемирной организации охраны здоровья в течение ближайших нескольких дней количество заболевших COVID-19 превысит 1 млн.
ДИСПЛАЗИЯ ШЕЙКИ МАТКИ – ЭТО ПРЕДРАКОВЫЙ ПРОЦЕСС, ХАРАКТЕРИЗУЮЩИЙСЯ НАРУШЕНИЕМ СОЗРЕВАНИЯ МНОГОСЛОЙНОГО ПЛОСКОГО ЭПИТЕЛИЯ В РЕЗУЛЬТАТЕ ДЛИТЕЛЬНОЙ ПЕРСИСТЕНЦИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА.
Синонимы: цервикальная интраэпителиальная неоплазия (CIN), плоскоклеточное интраэпителиальное поражение (SIL).
Если коротко, дисплазия шейки матки — это заболевание, которое в будущем может привести к раку. Вероятность этого тем выше, чем выше степень дисплазии. К дисплазии 1 степени (CIN 1, LSIL) относят любые изменения эпителия, порой даже минимальные и субъективные. Это позволяет взять женщину под контроль и не допустить прогрессирования процесса. На практике, для диагностики дисплазии 1 степени достаточно поражение эпителиальных клеток вирусом папилломы человека. Опасаться этого не стоит! Легкая степень дисплазии самостоятельно проходит у 70% женщин в течение нескольких лет. За это время собственная иммунная система уничтожает вирус и заболевание регрессирует. Обычно дисплазия 1 степени требует только наблюдения, в части случаев может назначаться прижигание. Дисплазия 2 и 3 степени (CIN 2-3, HSIL) — это уже предопухолевый процесс с высоким риском, поэтому требует серьезного лечения. В таких случаях показана широкая эксцизия или конизация шейки матки. Диагностировать дисплазию эпителия можно с помощью мазка на цитологию или биопсии. В принятии решения и тактике лечения важную роль играет тест на ВПЧ.
Подробнее читайте ниже, а также посмотрите комментарии, там Вы найдете ответы на свои вопросы.
Основной причиной развития дисплазии шейки матки является вирус папилломы человека, а именно его онкогенные штаммы — 14 серотипов, среди которых наиболее важными являются 16 и 18. Зрелый многослойный плоский эпителий, покрывая наружную часть шейки, создает непреодолимую преграду для вируса. Единственным же уязвимым местом является граница с железистым эпителием у наружного зева, называемая зоной трансформации . При эрозии (эктопии) шейки матки зона трансформации смещается на наружную часть шейки матки, что создает предпосылки для инфицирования.
Более 80% случаев дисплазии и рака шейки матки развивается именно в зоне трансформации.
Большинство женщин переносит ВПЧ-инфекцию без каких либо изменений со стороны организма. В течение нескольких лет иммунная система самостоятельно избавляется от вируса. Однако 10% женщин не могут уничтожить вирус, который в свою очередь встраивается в ДНК эпителиальных клеток и модифицирует их, приводя к опухолевой трансформации. Это может быть связано как с индивидуальной предрасположенностью, так и с иммунодефицитом или длительными стрессами. Также известно, что курение способствует снижению специфического иммунитета против ВПЧ.
Дисплазия шейки матки — это качественное изменение клеток плоского эпителия, которое указывает на возможное начало опухолевой трансформации.
Различают несколько степеней дисплазии шейки матки по тяжести, что обычно выражается в числовых значениях от 1 до 3. Каждая степень отражает прогноз патологического процесса и позволяет выбрать соответствующий алгоритм лечения. Так, дисплазия 1 степени имеет низкий потенциал к малигнизации и в большинстве случаев самостоятельно регрессирует в течение нескольких лет без какого-либо вмешательства. В противоположность, дисплазия 3 степени в течение одного года обязательно трансформируется в рак и требует уже специализированного хирургического лечения.

Прогрессирование дисплазии шейки матки
В международной практике термин “дисплазия шейки матки” имеет различные синонимы. Наиболее широко распространена аббревиатура CIN – цервикальная интраэпителиальная неоплазия, что означает развитие неоплазии (новообразования) в пределах эпителиального пласта. В отличие от рака, CIN не обладает способностью к инвазивному росту и метастазированию. На этом этапе можно предотвратить развитие злокачественной опухоли.
1) LSIL (low grade squamous intraepithelial lesion) — плоскоклеточное интраэпителиальное поражение легкой степени. LSIL соответствует CIN 1 или дисплазии 1 степени.
| Pap class System 1954 | Классификация ВОЗ 1956 | Классификация Bethesda 1988 |
| Class | Дисплазия/CIN (ЦИН — цервикальная интраэпителиальная неоплазия) | SIL (плоскоклеточное интраэпителиальное поражение) |
| Class 3 | Дисплазия 1 степени/CIN 1 | LSIL — плоскоклеточное интраэпителиальное поражение легкой степени |
| Class 4 | Дисплазия 2 степени/CIN 2 | HSIL — плоскоклеточное интраэпителиальное поражение тяжелой степени |
| Дисплазия 3 степени/CIN 3 | ||
| Рак in situ (рак в пределах эпителиального пласта, без инвазивного роста) |

Первым методом в диагностике дисплазии шейки матки чаще всего является мазок на онкоцитологию . Это скрининговый метод для обследования большого количества женщин. Является самым простым и безопасным для женщины, однако не самым точным. Чувствительность метода составляет 60-70%, и только трехкратное исследование позволяет с высокой точностью определить или опровергнуть дисплазию эпителия. Кроме этого у молодых женщин часто бывают ложно-отрицательные результаты, когда дисплазия может быть пропущена; а у пожилых женщин часты ложно-положительные результаты, когда мазок показывает наличие дисплазии, в то время как более качественные методы ее исключают.
При определении LSIL в мазке необходимо только лишь активное наблюдение. Под этим диагнозом подразумеваются клеточные изменения с низким потенциалом опухолевой трансформации. К LSIL относятся различные дегенеративные изменения клеток при раздражении, воспалении или вирусном поражении. Гинеколог, получив такое заключение может порекомендовать проведение кольпоскопии с последующей точечной биопсией.
При наличии HSIL в мазке на цитологию проведение кольпоскопии с гистологическим подтверждением становится обязательным!
Кольпоскопия — это метод осмотра наружной поверхности шейки матки с помощью специального микроскопа. Кольпоскопия является достаточно субъективным методом диагностики, сильно зависящим от опыта и умения врача. Кольпоскопические картины дисплазии шейки матки размыты и очень часто ее можно спутать с банальными физиологическими процессами, такими как плоскоклеточная метаплазия, вирусным поражением или лейкоплакией. Несмотря на это, кольпоскопия позволяет определить подозрительные места на шейке матки и взять биопсию — участок ткани для дальнейшего гистологического исследования.
К кольпоскопическим признакам дисплазии относятся: ацетобелый эпителий, йод-негативные зоны, изъеденность или нерегулярность эпителиального покрова, атипичные сосуды, мозаика, пунктация, контактная кровоточивость и др. Гинеколог должен оценить не только степень, но и скорость наступления тканевой и сосудистой реакции при обработке уксусной кислотой или йодом.
Цель кольпоскопии — это определить анатомическую локализацию зоны трансформации, что имеет решающее значение для дальнейшей тактики диагностики и лечения.
Биопсия является “золотым” стандартом диагностики дисплазии и рака шейки матки. Гистологическое исследование позволяет определить качество плоского эпителия и степень его созревания. Биопсия может быть точечной, получаемой с помощью специального инструмента — конхотома, или широкой (эксцизионной), получаемой с помощью электропетли.
Изменения при дисплазии 1 степени обычно носят характер цитопатического действия вируса папилломы человека. В эту категорию так же относят остроконечную и плоскую кондиломы. Морфологические изменения при CIN 1 (LSIL) включают: нарушение стратификации плоского эпителия преимущественно в базальных отделах, нарушение поляризации клеток относительно базальной мембраны, единичные делящиеся клетки, незначительный дискариоз, а также признаки вирусного поражения — койлоцитарную атипию в поверхностных отделах эпителия, дискератоз, пара- и гиперкератоз эпителия.

Патологическая эпидермизация желез с CIN III
Морфологические изменения при CIN 2-3 (HSIL) носят уже неопластический характер, а цитопатическое действие вируса может проявляться слабо. Нарастает клеточная атипия, которая затрагивает весь пласт плоского эпителия с минимальными признаками созревания. Клетки активно делятся, замещая нормальный эпителий цервикальных желез, в ряде случаев пролиферирующий плоский эпителий может замещать выстилку цервикального канала. Характерно обилие как нормальных, так и патологических митозов.
Тяжелая дисплазия шейки матки отличается от рака отсутствием инвазивного роста.
Тест на ВПЧ помогает в диагностике дисплазии шейки матки и выборе тактики лечения в сложных ситуациях.
ВПЧ тест рекомендуется делать женщинам после 25 лет, поскольку имеется большая вероятность, что инфекция уже длительное время персистирует в организме и могла вызвать какие-либо изменения в шейке. В более молодом возрасте при нормальном мазке на цитологию ВПЧ-тистирование не дает полезной информации.
С возрастом ВПЧ-тестирование приобретает все большую значимость. К примеру, при наличии 16 или 18 штаммов ВПЧ у 50 летней женщины можно с высокой вероятностью утверждать, что у нее уже имеется тяжелое интраэпителиальное поражение эпителия. Мазок на цитологию менее эффективен в данном случае. Женщине тот час может рекомендоваться диагностическая биопсия и выскабливание цервикального канала.
Тактика лечения и ведения пациенток с дисплазией зависит от гистологического заключения, кольпоскопической картины, типа зоны трансформации, возраста и планирования беременности. Основными методами являются абляция (прижигание), или эксцизия (удаление тканей). Эти методы могут проводиться с помощью различных инструментов, использующих низкие или высокие температуры, электро-, лазеро- или радиоволновую энергию.
По западным протоколам LSIL необходимо динамически наблюдать. Так как LSIL обладает низким злокачественным потенциалом и часто регрессирует самостоятельно, женщине рекомендуется проходить цитологическое исследование не менее 2 раз в год. В отечественной медицине часто рекомендуют абляцию (прижигание), хотя это не всегда оправдано. С прижиганием связывают некоторое повышение риска невынашивания беременности. Однако, часть авторов, опровергает это.
Наиболее оптимальным является радиоволновая абляция Сургитроном. Патологический эпителий и подлежащая строма выпариваются радиоволнами, после чего пораженная зона эпителизируется заново. Минусом абляции является отсутствие материала для последующего гистологического исследования, плюсом — сохранение анатомического строения шейки матки и небольшое количество осложнений.
HSIL обладает высоким злокачественным потенциалом, поэтому в данном случае показано удаление патологически изменненых тканей. Обычно, рекомендуется широкая эксцизионная биопсия или конизация шейки матки — это конусообразное удаление тканей, включающая наружную часть шейки матки и ткани вокруг цервикального канала. Весь удаленный материал отправляется на гистологическое исследование для подтверждения и уточнения диагноза. В удаленном материале гистолог оценивает края резекции, так как важно, чтобы патологический эпителий был удален в пределах здоровых тканей. При наличии в краях резекции патологии, или глубоком поражении цервикального канала, а также наличии инвазивного роста может быть принято решение об ампутации шейки матки.
Изредка, если женщина молода и планирует беременность, допускается лечение HSIL абляцией. Это возможно только лишь в случае 1 или 2 типа зоны трансформации при кольпоскопии, когда гинеколог видит глазом все измененные ткани и может обеспечить полную их абляцию. Если зона трансформации смещена глубоко в цервикальный канал — показана только глубокая конизация или ампутация шейки матки.
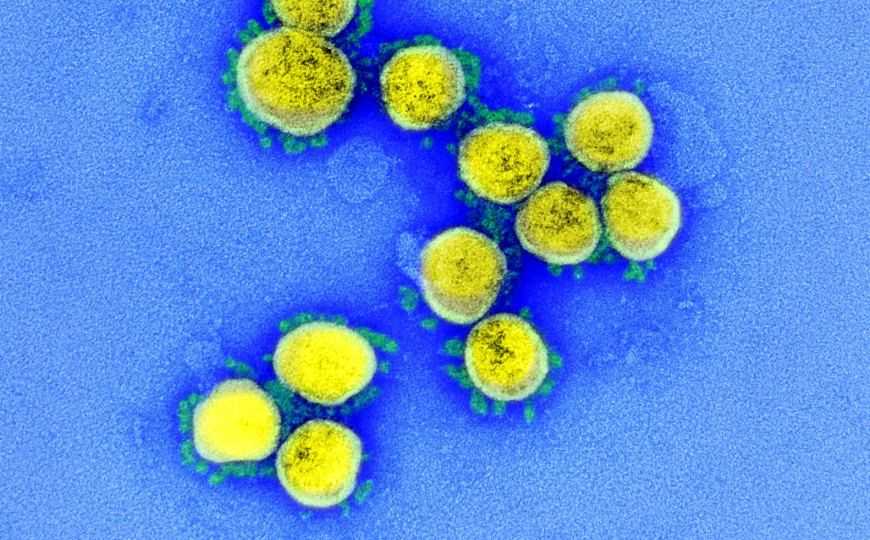
Исследователи из Германии под руководством Кристиана Дростена (клиника Шарите, Берлин) и Клеменса Вендтнера (клиника Швабинг, Мюнхен) выполнили подробный вирусологический анализ для девяти взрослых из Мюнхена, принадлежащих к одному кластеру эпидемиологически связанных случаев, со сравнительно умеренными симптомами COVID-19. Все они заболели после 23 января, о контакте с инфицированной женщиной из Китая стало известно 27 января (подробнее на PCR.news).
У девяти человек с диагнозом COVID-19 и нетяжелыми респираторными симптомами анализировали мазки из носоглотки, ротоглотки, образцы мокроты, а также образцы стула, крови и мочи. РНК вируса выявляли методом ОТ-ПЦР.
Авторы сообщают о больших количествах вируса в верхних дыхательных путях в течение первой недели после появления симптомов (с пиком около 4-го дня: 7,11*10 8 копий РНК). (Сходные результаты недавно опубликовали исследователи из Гонконга.)
Присутствие вирусной РНК не всегда означает, что в образце есть жизнеспособный вирус. Однако исследователям удалось выделить инфекционную форму вируса из образцов, взятых из горла и мокроты пациентов вплоть до восьмого дня с момента появления симптомов (к этому времени симптомы обычно ослабевают). Кроме того, способность вируса к репликации подтверждали с помощью ОТ-ПЦР, выявляющей субгеномную мРНК вируса (sgRNA) в клинических образцах. Эта РНК присутствует только внутри клетки, но не упаковывается в вирионы, следовательно, ее присутствие говорит о том, что вирус поражает клетки больного.
Можно сделать вывод, что в первую неделю заболевания пациент выделяет значительные количества вируса. А у двух пациентов с некоторыми признаками начинающейся пневмонии высокий уровень вируса в мокроте сохранялся до десятого и одиннадцатого дня. Вирусная РНК обнаруживалась в мокроте и после окончания симптомов. Эти результаты важно иметь в виду, когда принимается решение о выписке. (Еще одно недавнее исследование на ту же тему.)
Успешное обнаружение вирусной РНК в мазках из горла и носа отличает новый коронавирус от возбудителя атипичной пневмонии SARS-CoV: ее возбудителя далеко не всегда удавалось выявить таким путем, например, в одном исследовании позитивными оказались лишь 38 из 98 образцов пациентов из Гонконга. В этом может быть причина и более эффективного распространения SARS-CoV-2 воздушно-капельным путем в начале заболевания.
Авторы упоминают интересную гипотезу, согласно которой SARS-CoV-2 активнее поражает ткани горла, потому что его S-белок, в отличие от S-белка SARS-CoV, имеет сайт расщепления человеческой протеазой фурином. Такое расщепление необязательно для проникновения в клетку, но облегчает его; возможно, поэтому новый коронавирус более успешно поражает ткани с низкой плотностью рецепторов ACE2.
Интересно, что ни один из пациентов не был коинфицирован малоопасными сезонными коронавирусами, вирусами гриппа и другими возбудителями респираторных заболеваний.
Сероконверсия (появление антител к вирусному белку) у 50% пациентов была зарегистрирована на 7-й день, на 14-й день — у всех. Резкой элиминации вируса после сероконверсии авторы не наблюдали, скорее начиналось медленное, но устойчивое снижение вирусной нагрузки в мокроте. Этот факт стоит учесть разработчикам вакцин против SARS-CoV-2, которым важно добиться сильного иммунного ответа.
Вирус не был выявлен в образцах крови или мочи. Авторы также не обнаружили реплицирующейся формы вируса в образцах стула (хотя концентрации вирусной РНК и в них были высокими и у шести из девяти пациентов РНК обнаруживалась до трех недель, как и в мокроте). Отсутствие вирусной репликации в образцах кала — аргумент против фекального пути передачи; однако здесь необходимы дополнительные исследования.
Таким образом, наиболее эффективно SARS-CoV-2 выделяется в верхних дыхательных путях на ранней стадии, когда симптомы легкие и не кажутся угрожающими. Дальнейшие исследования покажут, способно ли увеличение вирусной нагрузки у пациента после первой недели сигнализировать об обострении болезни, предполагают авторы.
Исследователи также секвенировали полные вирусные геномы у пациентов и у всех нашли одну и ту же нуклеотидную замену, что подтверждало эпидемиологические данные об их принадлежности к одному кластеру. При этом у первого пациента замена присутствовала только в образце из глотки, в мокроте был вирус с изначальным вариантом последовательности. Это говорит о том, что размножение вируса в глотке и легких может идти независимо.
ДИСПЛАЗИЯ ШЕЙКИ МАТКИ – ЭТО ПРЕДРАКОВЫЙ ПРОЦЕСС, ХАРАКТЕРИЗУЮЩИЙСЯ НАРУШЕНИЕМ СОЗРЕВАНИЯ МНОГОСЛОЙНОГО ПЛОСКОГО ЭПИТЕЛИЯ В РЕЗУЛЬТАТЕ ДЛИТЕЛЬНОЙ ПЕРСИСТЕНЦИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА.
Синонимы: цервикальная интраэпителиальная неоплазия (CIN), плоскоклеточное интраэпителиальное поражение (SIL).
Если коротко, дисплазия шейки матки — это заболевание, которое в будущем может привести к раку. Вероятность этого тем выше, чем выше степень дисплазии. К дисплазии 1 степени (CIN 1, LSIL) относят любые изменения эпителия, порой даже минимальные и субъективные. Это позволяет взять женщину под контроль и не допустить прогрессирования процесса. На практике, для диагностики дисплазии 1 степени достаточно поражение эпителиальных клеток вирусом папилломы человека. Опасаться этого не стоит! Легкая степень дисплазии самостоятельно проходит у 70% женщин в течение нескольких лет. За это время собственная иммунная система уничтожает вирус и заболевание регрессирует. Обычно дисплазия 1 степени требует только наблюдения, в части случаев может назначаться прижигание. Дисплазия 2 и 3 степени (CIN 2-3, HSIL) — это уже предопухолевый процесс с высоким риском, поэтому требует серьезного лечения. В таких случаях показана широкая эксцизия или конизация шейки матки. Диагностировать дисплазию эпителия можно с помощью мазка на цитологию или биопсии. В принятии решения и тактике лечения важную роль играет тест на ВПЧ.
Подробнее читайте ниже, а также посмотрите комментарии, там Вы найдете ответы на свои вопросы.
Основной причиной развития дисплазии шейки матки является вирус папилломы человека, а именно его онкогенные штаммы — 14 серотипов, среди которых наиболее важными являются 16 и 18. Зрелый многослойный плоский эпителий, покрывая наружную часть шейки, создает непреодолимую преграду для вируса. Единственным же уязвимым местом является граница с железистым эпителием у наружного зева, называемая зоной трансформации . При эрозии (эктопии) шейки матки зона трансформации смещается на наружную часть шейки матки, что создает предпосылки для инфицирования.
Более 80% случаев дисплазии и рака шейки матки развивается именно в зоне трансформации.
Большинство женщин переносит ВПЧ-инфекцию без каких либо изменений со стороны организма. В течение нескольких лет иммунная система самостоятельно избавляется от вируса. Однако 10% женщин не могут уничтожить вирус, который в свою очередь встраивается в ДНК эпителиальных клеток и модифицирует их, приводя к опухолевой трансформации. Это может быть связано как с индивидуальной предрасположенностью, так и с иммунодефицитом или длительными стрессами. Также известно, что курение способствует снижению специфического иммунитета против ВПЧ.
Дисплазия шейки матки — это качественное изменение клеток плоского эпителия, которое указывает на возможное начало опухолевой трансформации.
Различают несколько степеней дисплазии шейки матки по тяжести, что обычно выражается в числовых значениях от 1 до 3. Каждая степень отражает прогноз патологического процесса и позволяет выбрать соответствующий алгоритм лечения. Так, дисплазия 1 степени имеет низкий потенциал к малигнизации и в большинстве случаев самостоятельно регрессирует в течение нескольких лет без какого-либо вмешательства. В противоположность, дисплазия 3 степени в течение одного года обязательно трансформируется в рак и требует уже специализированного хирургического лечения.

Прогрессирование дисплазии шейки матки
В международной практике термин “дисплазия шейки матки” имеет различные синонимы. Наиболее широко распространена аббревиатура CIN – цервикальная интраэпителиальная неоплазия, что означает развитие неоплазии (новообразования) в пределах эпителиального пласта. В отличие от рака, CIN не обладает способностью к инвазивному росту и метастазированию. На этом этапе можно предотвратить развитие злокачественной опухоли.
1) LSIL (low grade squamous intraepithelial lesion) — плоскоклеточное интраэпителиальное поражение легкой степени. LSIL соответствует CIN 1 или дисплазии 1 степени.
| Pap class System 1954 | Классификация ВОЗ 1956 | Классификация Bethesda 1988 |
| Class | Дисплазия/CIN (ЦИН — цервикальная интраэпителиальная неоплазия) | SIL (плоскоклеточное интраэпителиальное поражение) |
| Class 3 | Дисплазия 1 степени/CIN 1 | LSIL — плоскоклеточное интраэпителиальное поражение легкой степени |
| Class 4 | Дисплазия 2 степени/CIN 2 | HSIL — плоскоклеточное интраэпителиальное поражение тяжелой степени |
| Дисплазия 3 степени/CIN 3 | ||
| Рак in situ (рак в пределах эпителиального пласта, без инвазивного роста) |

Первым методом в диагностике дисплазии шейки матки чаще всего является мазок на онкоцитологию . Это скрининговый метод для обследования большого количества женщин. Является самым простым и безопасным для женщины, однако не самым точным. Чувствительность метода составляет 60-70%, и только трехкратное исследование позволяет с высокой точностью определить или опровергнуть дисплазию эпителия. Кроме этого у молодых женщин часто бывают ложно-отрицательные результаты, когда дисплазия может быть пропущена; а у пожилых женщин часты ложно-положительные результаты, когда мазок показывает наличие дисплазии, в то время как более качественные методы ее исключают.
При определении LSIL в мазке необходимо только лишь активное наблюдение. Под этим диагнозом подразумеваются клеточные изменения с низким потенциалом опухолевой трансформации. К LSIL относятся различные дегенеративные изменения клеток при раздражении, воспалении или вирусном поражении. Гинеколог, получив такое заключение может порекомендовать проведение кольпоскопии с последующей точечной биопсией.
При наличии HSIL в мазке на цитологию проведение кольпоскопии с гистологическим подтверждением становится обязательным!
Кольпоскопия — это метод осмотра наружной поверхности шейки матки с помощью специального микроскопа. Кольпоскопия является достаточно субъективным методом диагностики, сильно зависящим от опыта и умения врача. Кольпоскопические картины дисплазии шейки матки размыты и очень часто ее можно спутать с банальными физиологическими процессами, такими как плоскоклеточная метаплазия, вирусным поражением или лейкоплакией. Несмотря на это, кольпоскопия позволяет определить подозрительные места на шейке матки и взять биопсию — участок ткани для дальнейшего гистологического исследования.
К кольпоскопическим признакам дисплазии относятся: ацетобелый эпителий, йод-негативные зоны, изъеденность или нерегулярность эпителиального покрова, атипичные сосуды, мозаика, пунктация, контактная кровоточивость и др. Гинеколог должен оценить не только степень, но и скорость наступления тканевой и сосудистой реакции при обработке уксусной кислотой или йодом.
Цель кольпоскопии — это определить анатомическую локализацию зоны трансформации, что имеет решающее значение для дальнейшей тактики диагностики и лечения.
Биопсия является “золотым” стандартом диагностики дисплазии и рака шейки матки. Гистологическое исследование позволяет определить качество плоского эпителия и степень его созревания. Биопсия может быть точечной, получаемой с помощью специального инструмента — конхотома, или широкой (эксцизионной), получаемой с помощью электропетли.
Изменения при дисплазии 1 степени обычно носят характер цитопатического действия вируса папилломы человека. В эту категорию так же относят остроконечную и плоскую кондиломы. Морфологические изменения при CIN 1 (LSIL) включают: нарушение стратификации плоского эпителия преимущественно в базальных отделах, нарушение поляризации клеток относительно базальной мембраны, единичные делящиеся клетки, незначительный дискариоз, а также признаки вирусного поражения — койлоцитарную атипию в поверхностных отделах эпителия, дискератоз, пара- и гиперкератоз эпителия.

Патологическая эпидермизация желез с CIN III
Морфологические изменения при CIN 2-3 (HSIL) носят уже неопластический характер, а цитопатическое действие вируса может проявляться слабо. Нарастает клеточная атипия, которая затрагивает весь пласт плоского эпителия с минимальными признаками созревания. Клетки активно делятся, замещая нормальный эпителий цервикальных желез, в ряде случаев пролиферирующий плоский эпителий может замещать выстилку цервикального канала. Характерно обилие как нормальных, так и патологических митозов.
Тяжелая дисплазия шейки матки отличается от рака отсутствием инвазивного роста.
Тест на ВПЧ помогает в диагностике дисплазии шейки матки и выборе тактики лечения в сложных ситуациях.
ВПЧ тест рекомендуется делать женщинам после 25 лет, поскольку имеется большая вероятность, что инфекция уже длительное время персистирует в организме и могла вызвать какие-либо изменения в шейке. В более молодом возрасте при нормальном мазке на цитологию ВПЧ-тистирование не дает полезной информации.
С возрастом ВПЧ-тестирование приобретает все большую значимость. К примеру, при наличии 16 или 18 штаммов ВПЧ у 50 летней женщины можно с высокой вероятностью утверждать, что у нее уже имеется тяжелое интраэпителиальное поражение эпителия. Мазок на цитологию менее эффективен в данном случае. Женщине тот час может рекомендоваться диагностическая биопсия и выскабливание цервикального канала.
Тактика лечения и ведения пациенток с дисплазией зависит от гистологического заключения, кольпоскопической картины, типа зоны трансформации, возраста и планирования беременности. Основными методами являются абляция (прижигание), или эксцизия (удаление тканей). Эти методы могут проводиться с помощью различных инструментов, использующих низкие или высокие температуры, электро-, лазеро- или радиоволновую энергию.
По западным протоколам LSIL необходимо динамически наблюдать. Так как LSIL обладает низким злокачественным потенциалом и часто регрессирует самостоятельно, женщине рекомендуется проходить цитологическое исследование не менее 2 раз в год. В отечественной медицине часто рекомендуют абляцию (прижигание), хотя это не всегда оправдано. С прижиганием связывают некоторое повышение риска невынашивания беременности. Однако, часть авторов, опровергает это.
Наиболее оптимальным является радиоволновая абляция Сургитроном. Патологический эпителий и подлежащая строма выпариваются радиоволнами, после чего пораженная зона эпителизируется заново. Минусом абляции является отсутствие материала для последующего гистологического исследования, плюсом — сохранение анатомического строения шейки матки и небольшое количество осложнений.
HSIL обладает высоким злокачественным потенциалом, поэтому в данном случае показано удаление патологически изменненых тканей. Обычно, рекомендуется широкая эксцизионная биопсия или конизация шейки матки — это конусообразное удаление тканей, включающая наружную часть шейки матки и ткани вокруг цервикального канала. Весь удаленный материал отправляется на гистологическое исследование для подтверждения и уточнения диагноза. В удаленном материале гистолог оценивает края резекции, так как важно, чтобы патологический эпителий был удален в пределах здоровых тканей. При наличии в краях резекции патологии, или глубоком поражении цервикального канала, а также наличии инвазивного роста может быть принято решение об ампутации шейки матки.
Изредка, если женщина молода и планирует беременность, допускается лечение HSIL абляцией. Это возможно только лишь в случае 1 или 2 типа зоны трансформации при кольпоскопии, когда гинеколог видит глазом все измененные ткани и может обеспечить полную их абляцию. Если зона трансформации смещена глубоко в цервикальный канал — показана только глубокая конизация или ампутация шейки матки.
Читайте также:


