Вирусные гепатиты кафедра инфекционных болезней
Научная деятельность кафедры инфекционных болезней
Научно-исследовательская работа на кафедре проводится с первых дней её создания. В первые годы работы кафедры были определены следующие основные направления научных исследований: бактериальные менингиты, дифтерия, острые кишечные инфекции.
В последние годы происходит смещение научных интересов на изучение проблем вирусных гепатитов, ВИЧ-инфекции: методы прогнозирования неблагоприятных исходов вирусных гепатитов, персонификация лечения гепатитов В, С, ко-инфекции ВИЧ/вирусные гепатиты, гепатита С с атипичным серологическим профилем и гепатита неуточненной этиологии. Изучаются особенности пространственно-временных проявлений эпидемического процесса ВИЧ-инфекции. Проводятся исследования патогенеза поражений головного мозга и по разработке методов диагностики и лечения бактериальных менингитов, генерализованной бактериальной инфекции.
Ежегодно сотрудники кафедры выступают на международных конференциях, съездах, симпозиумах. Динамика сделанных сотрудниками кафедры докладов на различных уровнях представлена на рис. 1.
Рис. 1. Количество докладов, выполненных сотрудниками кафедры за последние 5 лет.
Следует обратить внимание, что в структуре докладов (рис.2) имеется тенденция к увеличению выступлений на международном и республиканском уровнях (2016-2017 гг. – до 66,6%).
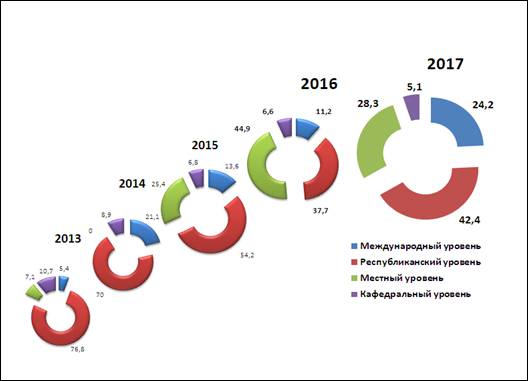
Рис. 2. Структура докладов, сделанных сотрудниками кафедры за последние 5 лет.
Количество публикаций за год в среднем составляет около 80 с ростом числа статей, опубликованных в центральных журналах, включенных в Перечень российских рецензируемых, которые рекомендованы ВАК для публикации результатов диссертаций на соискание ученой степени кандидата и доктора медицинских наук. На рис. 3 приведена динамика публикаций за последние 5 лет.
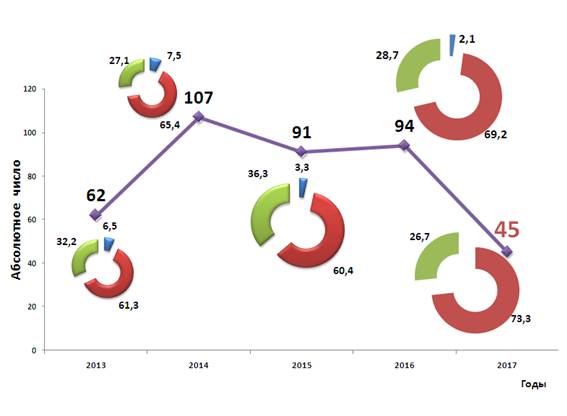
Рис 3. Количество публикаций, сделанных сотрудниками кафедры за последние 5 лет. Обозначения те же (см. рис 2).
В рамках кафедральных НИР все исследования проводятся комплексно с межинститутским взаимодействием. Сотрудники кафедры выполняют исследования по хоздоговорной тематике и в рамках государственных грантов, Федеральных целевых программ, научных школ.
Изучение исходов хронического гепатита В, основанное на анализе генетических факторов человека, в сочетании с методами определения вирусной нагрузки и геновариантов HBV, позволит оптимизировать тактику ведения больных с различными вариантами хронической HBV-инфекции.
Другим подходом прогнозирования неблагоприятных исходов ХГ является оценка показателей клеточного состава крови больных ХГ. В результате исследований получены новые данные о патогенезе хронического вирусного гепатита С в соответствии со стадиями фиброзных изменений в печени. Преимуществом разработанной методики является возможность ее применения в клинической практике на базе стационаров и центров, оснащенных иммунологическими лабораториями. Предложено проводить ежегодный мониторинг клеточного состава крови у больных с верифицированным диагнозом хронического гепатита С по определенному алгоритму.
В 2015 г. проведено генотипирование 239 образцов РНК больных ХГС (как получавших, так и не получавших противовирусную терапию (ПВТ) и 200 образцов РНК людей контрольной группы для определения SNP - rs738409 гена PNPLA3, rs2248814 гена NOS2A, rs2072324 гена NOS2A, rs11234870 гена FZD4, rs12980275 и rs12980275 гена IL-28B в ПЦР с использованием олигонуклеотидов собственной разработки. Проведен анализ данных пациентов с ХГС без цирроза печени, закончивших комбинированную терапию (пегилированным интерфероном и рибавирином) с длительностью 24 недели в соответствии с выявленным генотипом HCV.
В группе пациентов, закончивших комбинированную ПВТ, дополнительно проведен анализ полиморфизмов rs12979860 и rs8099917 гена человека ИЛ-28В, являющимся предиктором эффективности ПВТ. Благоприятный по отношению к эффективности ПВТ генотип СС выявлен у 36% больных. Генотип GG, ассоциирующийся с низким уровнем ответа на терапию, выявлен в 6% случаев. Выявлено преобладание генотипа СТ rs12979860 (48%), и только в 16% случаев - генотип ТТ. Частота встречаемости генотипов ТТ и ТG rs8099917 гена ИЛ-28В составила 58% и 36%, соответственно. Носительство благоприятного генотипа СС полиморфизма rs12979860 гена ИЛ-28В у пациентов с отсутствием УВО зарегистрировано лишь у 2 пациентов (11, 8%), генотип СТ был выявлен у большинства пациентов (64,7%), в 23,% случаев выявлен генотип ТТ. Частота достижения УВО была статистически значимо выше у больных с достижением быстрого вирусологического ответа (БВО) по сравнению с его отсутствием (р=0,0263), 94%больных с отсутствием ответа на ПВТ не достигли БВО. В группе с отсутствием УВО статистически достоверно чаще встречаются больные, инфицированные генотипом 1 HCV (78%,14/18), и пациенты с исходно высоким уровнем виремии (>8х10 5 МЕ/мл).
С целью выявления возможных генетически детерминированных факторов эффективности ПВТ было проведено сопоставление предварительных результатов исхода ПВТ с особенностями генома HCV. Всего секвенировано и проанализировано 66 фрагментов из NS5B области (размером в среднем около 300 пар оснований), 31 фрагмент из 5’UTR/core области (размером в среднем около 450-600 пар оснований), 41 полноразмерный ген core (573 пар оснований). В результате филогенетического анализа фрагмента NS5B области генома 66 изолятов идентифицированы восемь субтипов HCV: 1a, 1b, 2a, 2b, 2c, 2k, 3a и 3b. У тридцати двух изолятов наблюдалось полное совпадение результатов генотипирования. В то же время, 32 изолята (7 от пациентов с ХГС и 25 от пациентов с коинфекцией ВИЧ/HCV), отнесенные к генотипу 2 на основе коммерческих-тест систем, по NS5B области принадлежали к субтипу 1b. Филогенетический анализ показал, что все 32 изолята входили в монофилетическую группу, сформированную изолятами рекомбинантной формы RF2k/1b (RF2k/1b). Для верификации их принадлежности к RF2k/1b, у 21 из 32 был секвенирован фрагмент 5’UTR/core области генома. Анализ нуклеотидных последовательностей подтвердил, что все они по этой области принадлежали к субтипу 2k. Наличие значительного пула изолятов RF2k/1b позволяет по результатам филогенетического анализа NS5B области генома идентифицировать рекомбинантную форму RF2k/1b.
Типирование вариантов HCV с использованием коммерческих тест-систем российского производства и результатов генотипирования на основе анализа фрагментов NS5B и core областей генома подтвердило невозможность идентификации в клинической лабораторной практике RF2k/1b, которая при использовании тест-систем типируется как генотип 2. Особенностями строения рекомбинантной формы RF2k/1b является принадлежность всех структурных генов к субтипу 2k, а неструктурных генов, к субтипу 1b. Впервые выявлен тренд существенного увеличения доли RF2k/1b в структуре циркулирующего генотипа 2 HCV на территориях г. Москва и г. Санкт-Петербург, которая стала достигать 37-45% и 67% в основной популяции населения и среди людей ко-инфицированных ВИЧ соответственно.
Установлено, что ни у одного пациента (n=5), инфицированного RF2k/1b, с опытом ПВТ в прошлом, не был достигнут УВО. В группе больных, инфицированных генотипом 2 HCV, закончивших лечение в рамках настоящего исследования (n=7), у двух пациентов выявлен рекомбинантный вариант RF2k/1b, и только у этих пациентов ПВТ была не эффективна. В отсутствии рекомбинантного варианта при генотипе 2 HCV в 100% достигнут успех лечения, а при его наличии в 100% терапия была неуспешной.
Полученные результаты позволяют констатировать, что необходимо включить в клиническую лабораторную практику обязательное субтипирование всех изолятов генотипа 2 на основе анализа фрагмента NS5B области генома, что позволит оптимизировать схему ПВТ и повысит её эффективность.

В исследования, посвященные проблеме ВИЧ/СПИДа, сотрудники кафедры включились с конца 90-х годов XX столетия. Изучение клинических и эпидемиологических аспектов позволило вскрыть особенности проявлений эпидемического процесса ВИЧ-инфекции, что учтено при совершенствовании системы эпидемиологического надзора, а исследования особенностей течения инфекционного процесса при ВИЧ/СПИДе позволили повысить качество жизни ВИЧ-инфицированных людей.
Работа по совершенствованию диагностики и лечения сопутствующей патологии (инфекционной и хирургической) у ВИЧ-инфицированных была проведена в рамках ГрантаРФФИ; 09-02-00836-а.
Роль и значение этих факторов риска неоднозначны. Ведущее значение принадлежит социальным факторам.
Сопоставление стандартизованных коэффициентов возрастной структуры смертности населения г. Москвы и возрастной структуры смертности среди ВИЧ-инфицированных показало, что основной возрастной группой, в которой отмечена наибольшая смертность от ВИЧ-инфекции была группа трудоспособного возраста, т.е. смертность при ВИЧ-инфекции вносит существенный вклад в общую смертность трудоспособного населения (избыточная смертность), уменьшая трудовой ресурс и вызывая депопуляцию населения в социально-значимой возрастной группе населения.
Причинами летального исхода при ВИЧ/СПИДе могут быть как квазиэндогенные, так и экзогенные несвязанные с основным заболеванием.
Детальный анализ эндогенных и квазиэндогенных причин смерти ВИЧ-инфицированных позволяет констатировать, что принятая форма врачебного свидетельства о смерти не отражает в полной мере комплекс причин, приведших к летальному исходу при болезни, вызванной ВИЧ. При наличии у больного ко-инфекции, например, туберкулез, вирусные гепатиты В, С, в первую часть свидетельства может быть внесена только одна из перечисленных выше нозологических форм.
Учитывая вышеприведенные обстоятельства, становится очевидным необходимость комплексного анализа смертности среди ВИЧ-инфицированных с обязательным учетом возраста, пола умерших, пути заражения с выделением причин наступления смерти.
Изучение динамики проявлений эпидемического процесса на различных этапах развития эпидемии ВИЧ-инфекции позволило определить тенденции распространения ВИЧ в индикаторных социальных и возрастных группах населения. Было условно выделено IV периода, которые различались интенсивностью динамики заболеваемости, трендом хода эпидемического процесса и ведущим путем передачи ВИЧ. Начиная с 2005 по 2017 г. в Российской Федерации стал отмечаться новый постепенный рост показателя заболеваемости ВИЧ-инфекцией (четвертый период).
Группой риска инфицирования ВИЧ остаются люди в возрасте 30 - 40 лет. Отмечена тенденция смещения заболеваемости ВИЧ-инфекцией на более старшие возрастные группы. Удельный вес вновь выявленных случаев ВИЧ-инфекции в группе 40-50-летних мужчин вырос с 13,6% в 2012 г. до 21,1% в 2016 г., а среди женщин – с 11% в 2012 г. до 17% в 2016 г.
Установлено, что имеется доминирование рискованной модели сексуального поведения среди учащейся молодежи. Среднее количество половых партнеров с начала половой жизни составило 4,8±0,3 у мужчин (ДИ 95%от 1 до 9,9) и 3,5±0,5 у женщин (ДИ 95%от 1 до 18). Принимая во внимание кумулятивный эффект, на связь не менее чем с тремя половыми партнерами приходилось 60,3%, то есть это каждый 2, и каждый 5 имел половые контакты не менее чем с 6 половыми партнерами. Выявлено, что имеется негативная тенденция роста опасности заражения ИППП, так как более половины респондентов имели в анамнезе переболевание ИППП, причем во время болезни 32,8% вступали в половые контакты и в 20% случаев не использовали профилактические средства защиты. Обращено внимание на то, что в 32,4% случаев имели место случайные половые связи с 3-5 половыми партнерами за последний год, а в 60,3% случаев число половых партнеров с начала половой жизни было более трех.
У большинства пациентов с синдромом генерализованной лимфаденопатии инфекционной природы она была обусловлена микобактериями (66,7%). На втором месте по частоте развития синдрома лимфаденопатии была цитомегаловирусная инфекция (25.5%) и реже она регистрировалась при токсоплазмозе (в 5,8% случаев). Генерализованная туберкулёзная лимфаденопатия с наибольшей частотой выявлялась у ВИЧ-инфицированных пациентов на стадии 4В этой болезни (73,5%) и в три раза реже на стадии 4Б (23,5%). Фактором риска развития генерализованной лимфаденопатии было падение числа CD4+ лимфоцитов ниже 100 клеток/мкл. Результаты работы позволяют обосновать целесообразность использования отобранных критериальных значений для прогнозирования рисков развития лимфаденопатии у ВИЧ-инфицированных, что повысит эффективность диагностическх мероприятий и применения схем АРВТ.
Доказано, что при БГМ происходит увеличение в СМЖ содержания белка, преимущественно за счет al- и а2-глобулиновых фракций, которые являются белками ранней фазы гнойного воспаления и элиминируются из СМЖ при эффективном лечении к 7-10 дням. Уровень этих фракций существенно выше при осложненном течении болезни, что позволяет использовать эти показатели для ранней диагностики БГМ, оценки тяжести течения и эффективности терапии. Установлено повышение уровня D-димера фибрина в СМЖ при БГМ, обусловленное лизисом фибринозно-гнойного экссудата. Уровень D-димера при динамическом исследовании зависел от этиологии менингита и эффективности терапии, что позволило рекомендовать данный показатель для ранней диагностики менингита и оценки эффективности лечения.
В процессе работы установлена важная роль в саногенезе при БГМ автономной иммунной системы ЦНС, которая проявляется в отличие от серозных и невоспалительных поражений ЦНС повышением количества Т-лимфоцитов (CD3+), в основном за счет увеличения числа цитотоксических Т-лимфоцитов (CD3+/CD8+), снижением естественных киллеров (CD16+/CD56+), снижением ИРИ, резким повышением ИЛ-1/3 и появлением IgG в СМЖ.
Динамическое наблюдение за пациентами с БГМ различной этиологии позволило установить, что наиболее распространенными являются менингиты менингококковой, пневмококковой, гемофильной этиологии и с 2008 г. - увеличение числа больных менингитами стафилококковой, клебсиеллезной и листериозной этиологии, что позволило ввести в обязательное исследование СМЖ методом ПЦР использование тест-систем для обнаружения фрагментов генома стафилококка (качественно и количественно), листерий и клебсиеллы в режиме реального времени в комплексе с бактериологическим методом.
На основе результатов проведенных исследований разработаны клинико-лабораторные алгоритмы для ранней дифференциальной диагностики БГМ с серозными вирусными менингитами и не воспалительными заболеваниями ЦНС.
2 и 3 марта 2020 года на лекции будет проведен первый этап олимпиады по вакцинации, по результатам которого будут отобраны основные участники на 2 и 3 туры
В целях ликвидации академических задолжностей на кафедре инфекционных болезней 26 февраля и 2 марта 2020 года состоится промежуточная аттестация для студентов, имеющих академические задолжности по инфекционным болезням, по итогам предыдущего семестра. Время приема академических задолжностей с 16:00.
В 2019 г. кафедра инфекционных болезней ФГБОУ ВО "Казанский государственный медицинский университет" (КГМУ) Минздрава России празднует замечательную дату - 35 лет назад начал свою работу на кафедре известный врач, педагог, ученый, профессор Вильдан Хайруллаевич Фазылов.

Вильдан Хайруллаевич родился в Республике Узбекистан. С 1966 по 1972 г. учился в Иркутском государственном медицинском институте. Уже в студенческие годы Вильдан Хайруллаевич увлекся научно-исследовательской работой и за время практической деятельности врача неоднократно выступал с научными докладами на конференциях областного и республиканского уровня, имел научные публикации в различных сборниках, посвященных проблемам энтеровирусных инфекций, дисбиоза кишечника при вирусных гепатитах. Талантливого и добросовестного врача-инфекциониста Лениногорской центральной районной больницы заметила главный инфекционист Минздрава ТАССР, заведующая кафедрой, профессор Диляра Шакировна Еналеева.
В 1984 г. Вильдан Хайруллаевич был приглашен работать на кафедру инфекционных болезней Казанского государственного медицинского института. Под руководством Д.Ш. Еналеевой Вильдан Хайруллаевич активно продолжил свою научную работу и в 1990 г. защитил кандидатскую диссертацию на тему "Состояние сосудисто-тромбоцитарного гемостаза и коррекция его нарушений при роже". В 1996 г. была успешно защищена докторская диссертация на тему "Нарушения гемостаза и иммунитета при формировании рецидивов рожи, их терапевтическая коррекция".
С 1995 по 2017 г. профессор В.Х. Фазылов заведовал кафедрой инфекционных болезней, продолжал научное направление кафедры - изучение этиопатогенеза и совершенствование методов специфической корригирующей терапии нарушений гемостаза и иммунных дисфункций у инфекционных больных. В рамках этого научного направления под его руководством защищены 2 докторских и 24 кандидатских диссертации.
В 2003 г. издана монография "Хронические вирусные гепатиты В и С" в соавторстве с Д.Ш. Еналеевой и А.С. Созиновым, в 2011 и 2015 г. она переиздана с дополнениями. Вильдан Хайруллаевич - автор раздела в коллективной монографии Сибирского отделения Российской академии медицинских наук (СО РАМН) и Научно-исследовательского института эпидемиологии и микробиологии СО РАМН "Хантавирусы и хантавирусные инфекции", изданной во Владивостоке в 2003 г. В 2004 г. увидело свет учебно-методическое пособие для студентов факультета социальной работы "Инфекционные болезни", рекомендованное Учебно-методическим объединением (УМО) по образованию в области социальной работы. За последние 5 лет издано 16 учебно-методических пособий, из них 3 с грифом УМО, 2 с грифом Федерального института развития образования.
Вильдан Хайруллаевич ежегодно участвует во всероссийских и международных научно-практических конференциях, в работе Европейской и Американской ассоциаций по изучению болезней печени. За последние 5 лет им опубликовано 160 научных работ, из них 40 статей в журналах, рекомендованных Высшей аттестационной комиссией РАН, 6 статей в журналах, представленных в Scopus/EMBASE. Профессор В.Х. Фазылов имеет авторское свидетельство № 1679686 "Антисептическое средство, повышающее барьерно-защитные функции кожи и слизистых оболочек", патент на изобретение № 2159080 "Способ диагностики развития холе-стаза при острых вирусных гепатитах".
Профессор В.Х. Фазылов успешно сочетает научную деятельность с активной общественной работой в рамках КГМУ Минздрава России, Республики Татарстан и на федеральном уровне. В течение 5 лет был ученым секретарем диссертационного совета К 208.034.01 при КГМУ Минздрава России, остается членом диссертационных советов при КГМУ Минздрава России и ФГБОУ ВО "Башкирский государственный медицинский университет" Минздрава России. Ежегодно участвует в работе диссертационных советов других вузов РФ. Вильдан Хайруллаевич - председатель предметно-проблемной комиссии КГМУ Минздрава России по диагностике, лечению и профилактике инфекционных болезней, член научно-консультативного совета Центральной научно-исследовательской лаборатории, член экспертного совета Учебноме-тодической комиссии при Минздраве России по специальности "лечебное дело", член Учебно-методической комиссии по инфекционным болезням Координационного совета по области образования "Здравоохранение и медицинские науки" (УМК), внештатный эксперт Республиканского центра судебной медицины Минздрава Республики Татарстан, эксперт страховой компании "Ак Барс-мед" по Республике Татарстан, до 2009 г. был внештатным главным инфекционистом Управления здравоохранения г. Казани.
В течение многих лет В.Х. Фазылов являлся членом редакционного совета "Казанского медицинского журнала", продолжает сотрудничать в редакционных советах журналов "Практическая медицина", "Инфекционные болезни: новости, мнения, обучение" (журналы входят в Перечень российских рецензируемых научных журналов, рекомендованных Министерством высшего образования и науки Российской Федерации для публикации результатов диссертаций на соискание ученой степени кандидата и доктора наук), а также "Журнала инфекционной патологии" (Ассоциация инфекционистов и госпитальных эпидемиологов Иркутской области).
В 2007 г. В.Х. Фазылов награжден дипломом III степени "Лучший преподаватель 2007 года". В 2013 и 2014 гг. на расширенных заседаниях УМК по инфекционным болезням был одобрен опыт работы кафедры по использованию рейтинговой системы контроля знаний студентов по инфекционным болезням в КГМУ Минздрава России.
Много сил и энергии В.Х. Фазылов уделяет и практическому здравоохранению. В последние 15 лет под его руководством активно разрабатываются и внедряются в практику здравоохранения Республики Татарстан методы диагностики и лечения хронических вирусных гепатитов, в том числе сочетанной инфекции с вирусом иммунодефицита человека. В 2000 г. по инициативе кафедры и под руководством В.Х. Фазылова продолжает успешно функционировать гепатологический кабинет при консультативно-диагностическом отделении Республиканской клинической инфекционной больницы. На его базе научная группа совместно с практическими врачами изучает аспекты патогенеза и клиники я хронических вирусных гепатитов с разработкой современных методов их диагностики и терапии.
Профессор В.Х. Фазылов имеет почетное звание "Заслуженный врач Республики Татарстан". В 2012 г. за многолетнюю и плодотворную научно-практическую работу Указом Президента Республики Татарстан ему присуждено почетное звание "Заслуженный деятель науки Республики Татарстан".
Вильдан Хайруллаевич Фазылов - человек большой эрудиции, обладающий высочайшими организаторскими способностями, талантливый ученый, профессионал своего дела. Его врачебная, научная и педагогическая деятельность - один из ярких примеров истинной преданности медицинской науке.
Коллектив кафедры инфекционных болезней КГМУ Минздрава России, заведующая, доктор медицинских наук, профессор И.М. Хаертынова и коллектив кафедры инфекционных болезней Казанской государственной медицинской академии - филиал ФГБОУ ДПО "Российская медицинская академия непрерывного профессионального образования" Минздрава России от всей души поздравляют Вильдана Хайруллаевича с этой знаменательной датой, выражают огромную благодарность за многолетний труд, желают крепкого здоровья и дальнейших творческих успехов.
Студенты, получившие неудовлетворительную оценку на экзамене, будут допущены к пересдаче только во время дополнительной промежуточной аттестации!
18 января состоится дополнительный день сдачи экзамена для студентов, пропустивших по уважительной причине день сдачи экзамена его группы (при себе иметь форму 22)
Вирусный гепатит А (ВГА, болезнь Боткина) – острая вирусная антропонозная болезнь с фекально-оральным механизмом передачи возбудителя, характеризующаяся развитием паренхиматозного гепатита и доброкачественным циклическим течением.
Этиология : вирус гепатита А – РНК-содержащий пикорнавирус
Эпидемиология : источник - больной всеми формами ВГА, лица с иннапарантной инфекцией, механизм передачи – фекально-оральный (при употреблении инфицированной воды и пищи, через грязные руки); наиболее восприимчивы к ВГА дети
Патогенез : внедрение ВГА в организм через слизистые ЖКТ --> гематогенный занос в гепатоциты --> влияние ВГА на ряд биохимических процессов в гепатоцитах, усиление перекисного окисления липидов --> цитолиз гепатоцитов с массивным поступлением в кровь печеночных ферментов, высвобождением антигенов вируса --> активация иммунной системы, интенсивной антителообразование --> элиминация вируса.
Клиническая картина ВГА:
1. инкубационный период (в среднем 15-30 дней)
2. преджелтушный период (4-7 дней):
- начало заболевания может протекать в нескольких клинических вариантах:
а) гриппоподобный – острое начало с быстрого повышения температуры до 38-39°С, часто с ознобом, в течении 2-3 дней, жалобы на головную боль, боли в мышцах и суставах, иногда небольшой насморк, болезненные ощущения в ротоглотке
б) диспепсический – постепенное начало со снижения или исчезновения аппетита, боли и тяжесть в подложечной области или правом подреберье, тошнота, рвота, иногда учащение стула до 2-5 раз/сут
в) астеновегетативный – постепенное начало со снижения работоспособности, слабости, сонливости, раздражительности, головной боли, головокружений
г) смешанный – сочетание признаков нескольких синдромов
- отечность и обложенность языка, пальпаторно увеличение, уплотнение и повышение чувствительности печени, часто увеличение селезенки
- за 2-3 дня до появления желтушности склер и кожных покровов темнеет мочи, испражнения становятся более светлыми (гипохоличными)
3. желтушный период (в среднем около 2 нед):
- появляется вначале желтушность склер, слизистых ротоглотки, затем и кожи; интенсивность желтухи быстро нарастает, достигая максимума на 5-7 день, цвет мочи становится все более темным, испражнения бесцветными (ахоличными); желтуха держится 4-5 дней, затем кал постепенно темнеет, моча светлеет, интенсивность желтухи быстро падает (дольше всего сохраняется желтушность склер)
- характерны нормализация температуры тела, уменьшение астеновегетативных и диспепсических проявлений к моменту появления желтухи (дольше всего могут сохраняться общая слабость, снижение аппетита, чувство тяжести в правом подреберье)
- печень увеличена, выступает из подреберья на 2-4 см, уплотнена, с закругленным краем, чувствительным при пальпации
- характерны брадикардия, нормальное или несколько сниженное АД, ослабленный 1-ый тон сердца на верхушке
- в ОАК: лейкопения, нейтропения, относительный лимфо- и моноцитоз, нормальная или замедленная СОЭ
- в БАК повышено содержание общего билирубина (в основном за счет прямого), резко нарастает активность аминотрансфераз (особенно АлАТ), увеличены показатели тимоловой пробы, снижен протромбиновый индекс
- при серологическом исследовании крови определяются анти-HAV IgM
4. период реконвалесценции (1-3 мес) – быстро улучшается общее состояние, ослабевают признаки нарушения пигментного обмена (исчезает желтушность кожи и слизистых, моча и кал приобретают обычную окраску, постепенно нормализуется БАК)
Циклическое течение наблюдается в 90-95% случаев , в 5% болезнь приобретает волнообразный характер в виде одного или двух обострений (обычно в пределах 1-3 мес от начала болезни), при этом усиливаются признаки, характерные для разгара ВГА (ухудшается общее состояние, усиливаются неприятные ощущения в области печени, исчезает аппетит, темнеет моча, обесцвечивается кал, нарастает интенсивность желтушности кожи, повышается активность АлАТ). ВГА заканчивается, как правило, полным выздоровлением, хронизации не бывает .
В зависимости от тяжести течения процесса выделяют:
а) легкую форму ВГА – слабо выраженные симптомы интоксикации или их отсутствие, малая выраженность желтухи и ее быстрое исчезновение через 2-3 нед, билирубинемия не превышает 100 мкмоль/л, протромбиновый индекс более 60%, быстрая нормализация АлАТ в течение 1 мес
б) среднетяжелую форму ВГА – умеренно выраженные симптомы интоксикации, умеренная гепатомегалия, исчезновение желтухи через 3-4 нед, билирубинемия от 100 до 200 мкмоль/л, протромбиновый индекс 50-60%, нормализация АлАТ в течение 1,5 мес
в) тяжелую форму ВГА – резко выраженные симптомы интоксикации (нарастающая общая слабость, сонливость, головокружение, анорексия вплоть до отвращения к пище, повторная рвота и др.), яркая желтушность кожи, исчезновение желтухи через 4 нед и более, билирубинемия выше 200 мкмоль/л, протромбиновый индекс менее 50%, нормализация АлАТ через 1,5 мес и более
г) фульминантную форму ВГА - быстрое, в течение часов - суток, развитие острой печеночной энцефалопатии с печеночной комой и летальным исходом; характерны высокие показатели активности аминотрансфераз, при этом АсАТ преобладает над АлАТ
1) данные эпидемиологического анамнеза (пребывание в очаге ВГА за 15-30 дней до заболевания), особенности клинической картины (острое начало, короткий преджелтушный период, диспепсические и астеновегетативные явления, быстрое развитие желтухи с улучшением общего состояния)
2) общеклинические исследования: ОАК (лейкопения, нейтропения, относительный лимфомоноцитоз, замедление СОЭ), БАК (билирубинемия чаще не выше 100 мкмколь/л, раннее и длительное повышение АлАТ), ОАМ (положительная качественная реакция на уробилин и желчные пигменты)
3) серологические исследования методом ИФА (выявление анти-HAV IgM в течение первых 2-3 нед болезни и/или четырехкратное и более выраженное нарастание титра анти-HAV IgG, взятых в желтушном периоде болезни и в периоде реконвалесценции)
1. При легких и среднетяжелых формах – полупостельный режим, при тяжелых – постельный; диета № 5, пища механически и химически щадящая, без экстрактивных веществ, подается в теплом виде
2. Строгое соблюдение гигиены полости рта и кожи, при зуде - протирание кожи р-ром пищевого уксуса (1:2), 1% р-ром ментолового спирта, горячий душ на ночь
3. Дезинтоксикационная терапия: в/в капельные инфузии 0,5-1,5 л 5% р-ра глюкозы, полиионных р-ров, гемодеза, реополиглюкина, форсированный диурез под контролем суточного баланса жидкости
4. Противовирусные ЛС при доброкачественном течении ВГА не показаны
5. При выраженном холестазе, отсутствии пигментного криза в течении недели от начала желтушного периода - энтеросорбенты (полифепан, билигнин, угольные гранулированные сорбенты), экстракорпоральная детоксикация (гемосорбция, плазмаферез, плазмосорбция и др.), при налии длительной постгепатитной гипербилирубинемии – фенобарбитал.
6. Ферментые препараты (панкреатин, креон, мезим форте, фестал, панзинорм, юниэнзайм) для усиления пищеварительной функции желудка и поджелудочной железы; при запорах – слабительные растительного просхождения, магния сульфат внутрь.
7. Гепатопротекторы в течение 1-3 мес: производные силимарина (легален, карсил, силимар), препараты из экстрактов растений (гепалив, гепатофальк, гепабене), эссенциале.
8. Иммунокорригирующая терапия: препараты тимуса (тималин, тимоген, тактивин), ИЛ-2 / ронколейкин
8. Лечение признаков печеночной недостаточности и печеночной энцефалопатии (см. вопрос 191)
Вирусный гепатит Е (ВГЕ) – острая вирусная антропонозная инфекционная болезнь с фекально-оральным механизмом передачи (преимущественно водным путем), острым циклическим течением и частым развитием печеночной энцефалопатии у беременных.
Этиология : вирус ГЕ – РНК-содержащий вирус.
Эпидемиология : источник – больные любыми формами ВГЕ, механизм заражения – фекально-оральный (чаще через воду); характерны взрывообразные водные вспышки заболевания в эндемичных районах каждые 7-8 лет
Патогенез : сход с патогенезом ВГА, вирус ГЕ обладает прямым цитопатическим эффектом на гепатоциты
Клиническая картина – протекает как ВГА, но имеет некоторые отличия:
- инкубационный период чаще около 1 мес
- преджелтушный период короткий (5-6 дней), без лихорадочной реакции, с выраженными диспепсическими проявлениями (отсутствие аппетита, тошнота, рвота, тяжесть и различной интенсивности ноющие боли в правом подреберье, у трети больных – диарея), синдромом общей интоксикации
- с появлением желтухи синдром общей интоксикации не уменьшается, всегда имеется значительное увеличение печени, потемнение мочи и ахолия кала, возможны холестатические формы желтухи с выраженным кожным зудом
- у женщин во 2-ой половине беременности часто протекает злокачественно по фульминантному типу с быстрым развитием массивного некроза печени и острой печеночной энцефалопатии, ДВС-синдромом, ОПН
Диагностика : как при ВГА + серологическое исследование (выявление анти-HEV IgM), лечение : как при ВГА.
Читайте также:


