Вирусы поражающие иммунную систему
14 октября 2013
- 19908
- 16,4
- 2
- 4
Распространенность СПИДа в мире на 2009 год.

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Обратная транскрипция осуществляется вирусным белком обратной транскриптазой [31]. Обратная она потому, что обычно в клетке все наоборот — информация переносится с ДНК на РНК (а с РНК — в последовательность аминокислот белков). РНК по сравнению с ДНК очень нестабильна, и поэтому для ВИЧ характерна огромная скорость мутации — в десятки тысяч раз быстрее, чем для человека. Если скорость нейтральных мутаций для ДНК составляет у различных видов и для различных генов в среднем меньше 10 −9 замен на сайт в год, то скорость мутирования генетического материала РНК-вирусов — около 10 −3 замен на сайт в год (у гена env ВИЧ: 10 −2 –10 −3 замен на сайт в год [21]). Это одна из причин, почему иммунная система не может справиться с ВИЧ — он слишком быстро изменяется.
Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
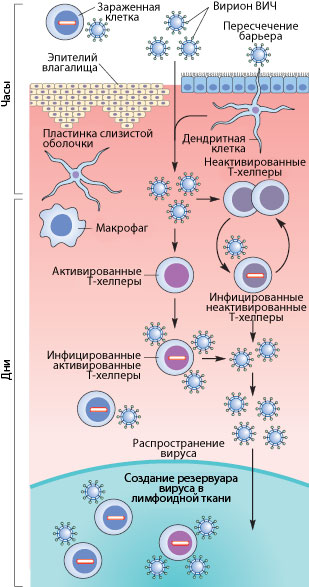
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
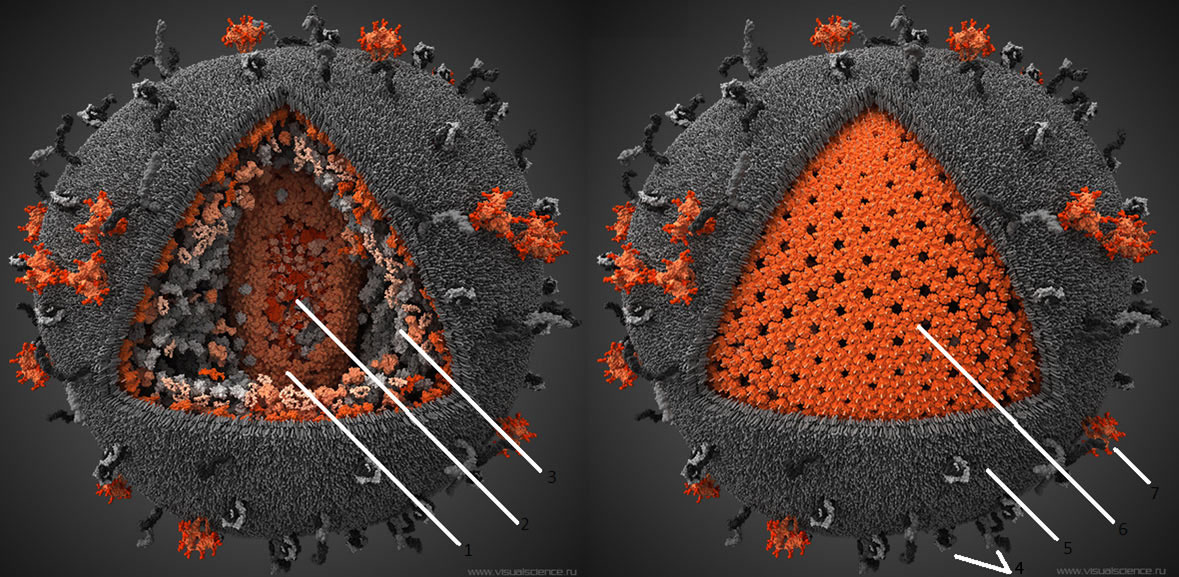
10000 нуклеотидов в каждой. Всего геном включает девять генов, которые в результате альтернативного сплайсинга кодируют 15 различных белков. 3 — Различные белки, захваченные вирусом из хозяйской клетки. 4 — Человеческие белки, обычно находящиеся на поверхности мембраны клеток. Захваченые в результате отпочковывания, они увеличивают вирулентность вируса. 5 — Внешняя оболочка ВИЧ, ведущая свое происхождение от цитоплазматической мембраны клетки, от которой когда-то отпочковался вирион. 6 — Матрикс, образованный тримерами белка р17. 7 — Тримерные комплексы белков gp120 и gp41, при помощи которых вирус проникает в клетку. На поверхности среднего вириона насчитывается около 20 таких тримеров. Чтобы увидеть рисунок в полном размере, нажмите на него.
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Пост скопирован с Яндекс Дзена:
Со временем вирусы мутируют в лёгкую форму и живут с нами, во многом даже помогая организму. Пример тому - коронавирус долго жил мирно в животных. Сейчас он просто перепрыгнул на человека. Ему нужно время, чтобы снизить свою активность и перестать убивать нас, то есть его среду обитания.
Начну с того, что вирусы всегда находятся в нашем организме, и мы от этого не умираем!* Среда обитания людей - "организм" Земля, среда обитания вирусов - организм человека. И люди, и вирусы могут чрезмерно паразитировать в своей среде, или нет. Если да, то организм перестаёт жить. Такова природа жизни.
Наш иммунитет, если он работает как надо, не даёт бесконтрольно паразитировать вирусам. А работает он как надо почти у всех людей.
Если вы здоровы, молоды и уверены, что ваш защитник иммунитет справится, то укрепляйте его(закаляйтесь и т. п.), а не мешайте ему таблетками и прочим. Ничего лишнего, природа уже обо всём позаботилась.
Коронавирус не хочет нас убивать. Ему просто нужно местечко для существования. Его цель размножиться. Но он может делать это слишком активно, что его среда обитания, организм, гибнет.
*например, много людей переносят туберкулёз, но не в форме прямо болезни-болезни
В эти дни, когда у вас много свободного времени, постарайтесь сделать что-то полезное, неважно что, неважно насколько.
Статья написана после просмотра этого видео:

Лимоны из солнечного Узбекистана
Сегодня был в магазине Глобус. Имбиря вообще нет, лимоны только одного сорта по цене мраморной говядины.

Вирусы. Часть 2 и 3
часть 2. Чужой внутри нас.
Человек — вершина эволюции. Десятки тысяч лет эффективного приспособления привели нас на вершину пищевой цепи. Насколько непоколебимо наше положение? Блага цивилизации позволили создать значительное конкурентное преимущество над другими видами. Но за пределами видимого мира, которым верховодит наш научно-технический прогресс, скрывается еще один, неведомый глазу микромир, где превосходство человека не так очевидно. Это самое густонаселенное место планеты, мириады обитателей которого не прочь поживиться за наш счет. Кто победит в этой борьбе, тот и будет править всем. Станет ли мы пищей, либо сможем диктовать правила -- это зависит от нашей иммунной системы.
Городские улицы. Бесконечные вереницы вечно спешащих горожан изо дня в день идут по знакомым маршрутам. Утром в тесном метро и автобусах, вечером -- в парках и скверах. Работа -- развлечения -- дом. Каждое мгновение жизни нас окружают десятки тысяч невидимых обитателей -- бактерии, водоросли, дрожжи, простейшие, споры грибов и вирусы. В здании популярного торгового центра или большого офиса может распологаться до 20 тысяч микроорганизмов на 1 кубический метр воздуха. На улице -- около 5 тысяч. На ферме или за городом -- до 2 миллионов микроорганизмов на 1 куб.м. Их настолько много, что они даже внутри нас. И многие из этих незваных гостей абсолютно не против такого соседства. На человеке эффективно паразитирует более тысячи различных видов микроорганизмов. Их самые любимые места -- кисти рук и заушные впадины, а также полость рта (около 20% от всех обитателей). Все это разнообразие жизни на человеке называют микробиомом кожи. По нему можно определить образ жизни и наше место обитания. Всю микрофлору, обитающую на человеке, разделяют на постоянную – резидентную (около 90 % обитателей), факультативную (условно-патогенную) – около 9,5 % и случайную (транзиторную) – 0,5 %. За тысячелетия совместной жизни резидентная микрофлора вполне научилась сосуществовать с нами, не причиняя очевидного ущерба, либо даже выполняя полезные функции. С остальными 10% все не так однозначно.
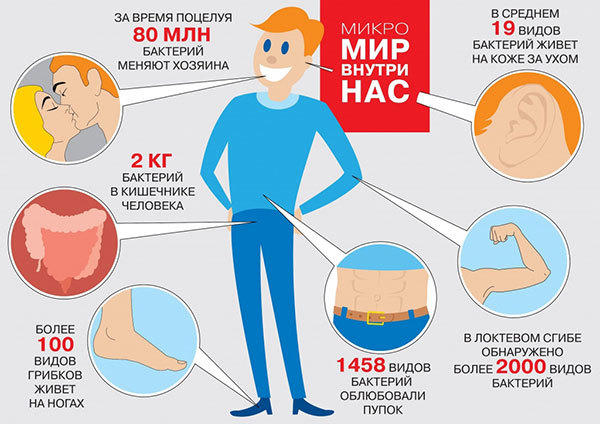
Все микроорганизмы, паразитирующие на нашем теле, принято разделять на две категории -- внеклеточные и внутриклеточные. Как не сложно догадаться, к внеклеточным паразитам относятся микроорганизмы, которые не могут проникнуть внутрь нашей клетки -- это крупные бактерии, грибки, токсины и даже другие животные. Они стремятся поселиться на нашей коже, либо в каких-нибудь органах и тканях, перемещаясь по телу благодаря системе кровообращения. Для борьбы с ними мать-природа создала достаточно эффективные механизмы -- кожный гомеостаз и гуморальный иммунитет.
Иммунитет — одна из самых древних систем, присущих живым организмам, возникшая более миллиарда лет назад, задолго до разделения животных и растений на отдельные царства. Первыми микроорганизмами, обладающими иммунной системой, на данный момент, считаются социальные амебы Dictyostelium discoideum. История ее появления достаточно интересна.
Социальные амебы Dictyostelium discoideum представляют собой организмы, образующиеся при слиянии одиночных амеб, которые при недостатке еды сползаются вместе и формируют плазмодий более чем из 100 тыс. клеток. При этом примерно 20% клеток жертвуют собой, чтобы создать плодоножки, а 80% становятся спорами. Около 1% сохраняет свои фагоцитарные функции и становятся иммунной системой, используя фагоцитоз (процесс захвата и переваривания клеткой твердых частиц) и сетки ДНК для уничтожения бактерий, которые поставили бы под угрозу выживание единого организма.
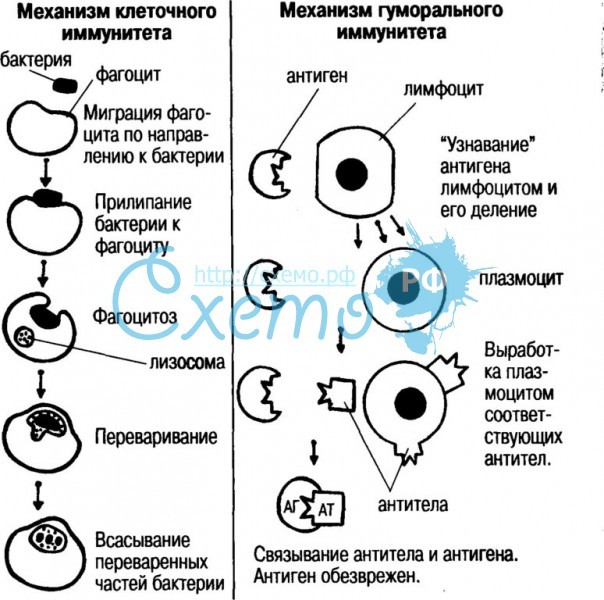
Фагоцитоз является основой клеточного иммунитета -- одной из двух основных форм иммунного ответа, наравне с гуморальным, присущим живым организмам в целом, и человеку в частности .
Кожный покров является первым барьером на пути микроорганизмов. Переднюю линию обороны на нем составляют уже обитающие там резидентные микроорганизмы. Наша кожа -- слишком густонаселенной место и ее постоянные жители отнюдь не в восторге от мысли, что им приедятся потесниться, вступают с пришельцами в ожесточенное противостояние. Если они не справляются, приходит черед кожного гомеостаза. Данный иммунный механизм изучен достаточно слабо, но мы знаем, что кожа полагается на непрерывное удаления мертвых клеток.
Если внеклеточные паразиты все же попадают в наш организм, проникая через повреждения кожи и слизистые оболочки, при дыхании или с едой, в бой вступает гуморальный иммунитет. В общем понимании, он представляет собой естественную реакцию организма на раздражитель (бактерии, грибки, токсины, животные-паразиты), попавший в кровь. Если опустить все детали и сильно обобщить, то говоря о работе гуморального иммунитета, мы подразумеваем создание антител, направленных на уничтожение инородного материала (антиген) в кровотоке. В этом нам помогают группы белков, гликопротеинов и полипептидов, выполняющих ферментативные, рецепторные и сигнальные функции:

Кроме внеклеточных патогенов, нам постоянно приходится сталкиваться с еще одним видом внешней угрозы -- внутриклеточным. Вирусы - это внутриклеточные паразиты, не проявляющие за пределами живой клетки никаких своих свойств. Проникнув в клетку, вирус изменяет в ней обмен веществ, направляя всю ее деятельность на производство вирусной нуклеиновой кислоты и белков, чтобы начать процесс репликации -- производства собственных копий. В организме среднестатистического жителя планеты Земля одновременно обитает от 5 до 15 вирусов. Они могут жить в клетках организма от нескольких часов до 7 дней, активно размножаясь и никак не давая о себе знать. Такие вирусы называют "спящими", а период их незаметного нахождения в организме "инкубационным".
Жар, кашель, светобоязнь, головная боль и слабость — это далеко не полный список симптомов самого распространенного заболевания в истории человечества — ОРВИ (острая респираторно-вирусная инфекция). Это группа заболеваний, вызванных вирусами, куда включают грипп (типа A, B и С), парагрипп, аденовирусную инфекцию и другие вирусные инфекции верхних дыхательных путей.
ОРЗ (острое респираторное заболевание) -- широкое понятие, включающее в себя заболевания верхних дыхательных путей, вызванные бактериями и вирусами. Когда же мы говорим об ОРВИ, то речь всегда идёт только о вирусной инфекции. На раннем этапе симптомы ОРВИ вирусного происхождения и ОРЗ бактериального происхождения зачастую очень похожи. При этом ОРВИ, будучи вирусной инфекцией, на поздних этапах своего течения проявляется, как правило, более выраженными симптомами: высокой температурой, ознобом, сильной головной болью, болями в мышцах и суставах
Часть 3. Незримый страж. Врожденный иммунитет.
Взаимодополняющая работа клеточного и гуморального иммунитета является гарантией нашей выживаемости в борьбе с вирусами и другими микроорганизмами. Но для начала разберемся, как работает наш иммунитет.
Основой человеческого иммунитета является костный мозг. Именно там образуются иммунные клетки, в дальнейшем поступающие в места своего хранения -- лимфатические узлы, селезенку и другие органы. Нейтрофилы и моноциты создаются в своем окончательном варианте и сразу отправляются в кровь. Но есть такие клетки, которым приходится проделать более долгий путь. Речь идет о лимфоцитах, которые выходя из костного мозга поступают в еще один важный орган иммунной системы -- тимус.
Тимус — это вилочковая железа, образование, которое лежит на сердце и осуществляет функцию по отбору лучших лимфоцитов. Дело в том, что лимфоциты в одинаковой мере способны реагировать как на клетки собственного организма, так и на чужеродные микроорганизмы. Поэтому тимус уничтожает все лимфоциты, которые чересчур сильно реагируют на свое. Так запускается природный механизм отрицательной селекции, в результате работы которого гибнет около 95% созданных костным мозгом лимцофитов.
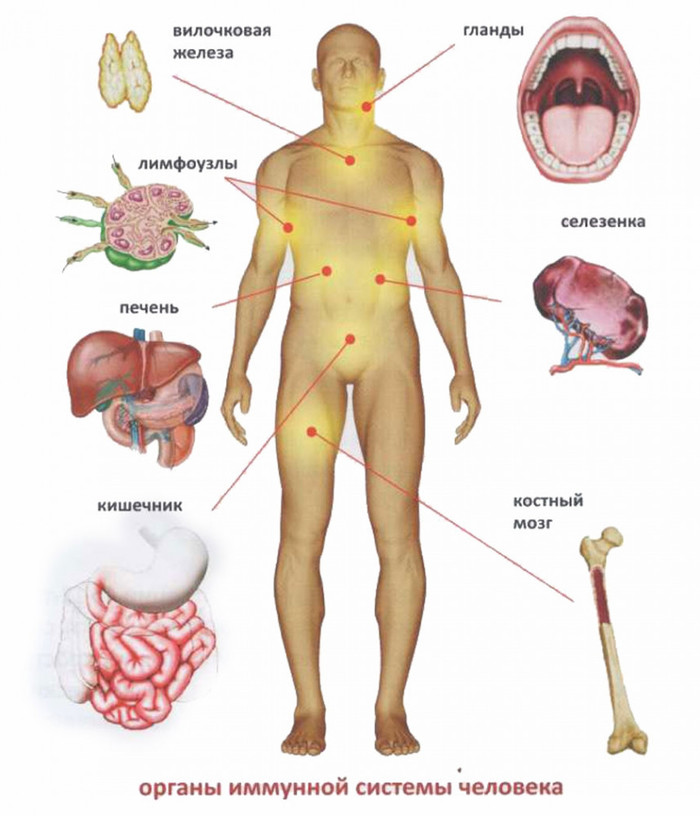
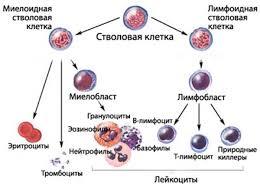
Что происходит, когда патоген попадает в наш организм? Все защитные факторы нашего организма можно разделить на врожденные (неспецифические или наследственные) и приобретенные (адаптивные). Первые представляют собой глубокий пласт иммунной системы, сформированный в процессе эволюции. Он защищает нас с самого рождения и позволяет не болеть рядом заболеваний, присущих животным и растениям (например, чумка собак или грибковые поражения растений). Врожденный иммунитет представляет собой первую линию защиты, моментально вступая в бой и позволяя выиграть время, чтобы наше тело смогло изучить геном патогена и выработать специфические антитела. Первыми удар принимают клетки-разведчики -- дендриты.
Один тип дендритных клеток позволяет вирусам проникнуть в свою структуру и начать процесс репликации -- воспроизводства вирусного РНК/ДНК. В то же время другой тип дендритных клеток подхватывает эти фрагменты и использует их для обучения Т-клеток иммунитета борьбе с этим вирусом. При этом, главной загадкой дендритных клеток является то, что при этом они не гибнут и не заражаются, как это происходит с обычными клетками.
Пока адаптивный иммунитет готовит на основе данных, полученных от дендритов, специфические антитела, способные бороться именно с этим видом микроорганизмов, врожденная иммунная система всеми силами старается выиграть время и не дать агрессору разгуляться. На переднем краю обороны оказываются фагоциты. Фагоциты -- большущие (по меркам микромира) клетки-пожиратели, которые регулярно защищают наш организм от внеклеточных бактерий, неправильно работающих клеток организма и отходов клеточной жизнедеятельности. Их главное оружие -- поедание врага. Заключенная в фагоцит бактерия (они способны поглотить любое вещество) погибает в течении нескольких минут. Фагоциты эффективны против внеклеточных бактерий, но против вирусов слабы, т.к. вирусы орудуют в собственных клетках организма. Поэтому основную нагрузку по борьбе с вирусом принимают лимфоциты, уничтожающие зараженные клетки, в то время как фагоциты выводят из организма их остатки.
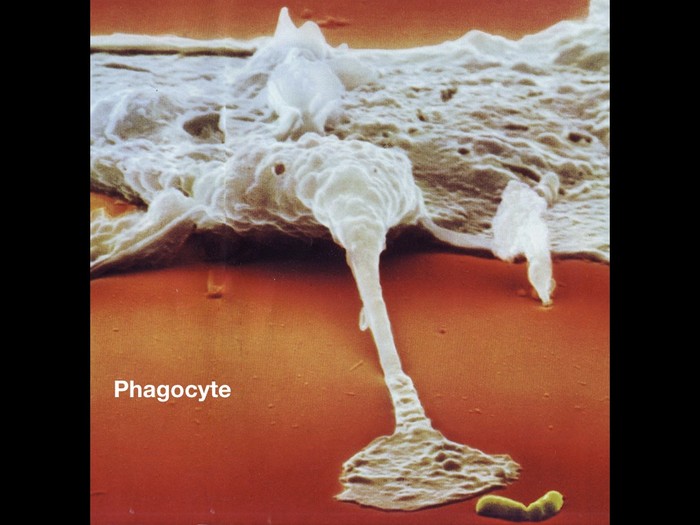
Рядом с фагоцитами, плечом к плечу, идут "система комплимента" и "естественные киллеры".
Система комплемента — комплекс сложных белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов (расщепляют пептидную связь между аминокислотами в белках), предназначенная для гуморальной защиты организма от действия чужеродных агентов в кровотоке.
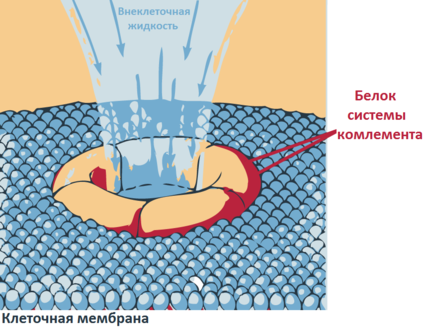
Простыми словами, система комплемента работает следующим образом: определенные белки прикрепляются к чужеродным клеткам и начинают делать в них дырки (лизис), разрушая оболочку. Если фагоциты являются частью клеточного врожденного иммунитета, то система комплимента относится к гуморальному врожденному иммунитету. Система комплемента может действовать тремя различными способами:
1) через хемотаксис: различные компоненты (факторы) комплемента могут привлекать иммунные клетки, которые атакуют бактерии и пожирают их (фагоцитируют)
2) через лизис: компоненты комплемента присоединяются к бактериальным мембранам, в результате чего образуется отверстие в мембране и бактерия лизируется (разрушается)
3) через опсонизацию: компоненты комплемента присоединяются к бактерии, в результате чего образуется метка для узнавания фагоцитирующими клетками (например, макрофагами и лейкоцитами), имеющими рецепторы к компонентам комплемента
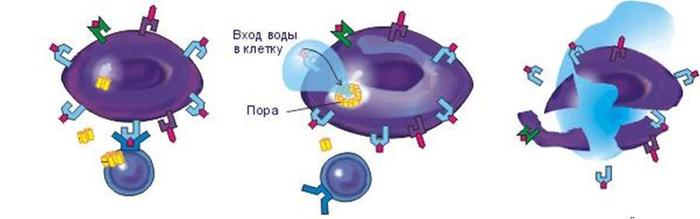
Следующие герой -- естественный киллер (NK) -- клетки врожденного иммунитета, способные убивать опухолевые клетки или клетки, зараженные вирусами. Они образуются из клеток-предшественников (рождаются в костном мозге) в различных тканях и органах (лимфатических узлах, селезенке, печени, кишечнике, тимусе, матке и других). Естественные киллеры важны для защиты от внутриклеточных инфекций, например вирусов, и для защиты от опухолей. Если этот механизм защиты нарушен, люди страдают рецидивирующими вирусными инфекциями, у них повышена вероятность возникновения опухолей. Механизм их работы таков:
В качестве ядов естественные киллеры используют несколько белков: перфорин, гранзим и гранулизин. Киллер образует герметичный контакт с клеткой-жертвой и внутрь этого герметичного просвета между клетками выделяет яд, который убивает неправильную клетку. Сама клетка-киллер защищена от этого яда. В качестве ядов естественные киллеры используют несколько белков: перфорин, гранзим и гранулизин.
Перфорин встраивается во внешнюю мембрану клетки-жертвы и образует в мембране поры, через которые проходят гранзим и гранулизин. Они входят в клетку, включают ее механизм апоптоза — самоликвидации. В течение 10–20 минут клетка переварит свое содержимое до простейших молекул и упакует эти безопасные останки в небольшие мешочки, которые охотно съедят фагоциты. Так очень аккуратно, не навредив соседним, здоровым клеткам, инфицированная или опухолевая клетка самоликвидируется по команде клетки-киллера. Естественный киллер — серийный убийца, он может поразить 30–40 клеток-мишеней подряд.
Как естественные киллеры находят клетки, которые надо убить? Дело в молекулярных витринах (молекулах MCH).
Каждая клетка организма представляет на своей поверхности элементы того, что синтезируется внутри клетки. Это необходимо, чтобы иммунитет мог обнаружить любые болезненные изменения в каждой клетке организма — признаки чужих, инфекционных молекул или собственные молекулы, существенно измененные в результате мутаций. Довольно часто инфицированные и опухолевые клетки прячут признаки болезни, не показывая на поверхности молекулы-витрины. Сенсоры естественных киллеров следят за тем, чтобы на поверхности каждой клетки организма обязательно были представлены молекулы-витринки. Отсутствие или существенное снижение количества MHC-молекул (витринок) на клетке рассматривается естественным киллером как признак, достаточный для смертного приговора.
Живем в кольце врагов — вирусы, бактерии и прочая зараза, которая то и дело переходит в наступление, превращает здоровых людей в больных, убивает. Зловредный коронавирус Covid-19 — свежий тому пример.
Коронавирус против человечества: новые инфекции усиливают наш иммунитет
Казалось бы, человечество давно должно было бы исчезнуть, пав в неравных боях с инфекционными заболеваниями. Но оно до сих пор живо. Почему?
- Все эпидемии, как и любые войны, рано или поздно заканчиваются, - говорит Павел Воробьев, доктор медицинских наук, профессор, председатель правления Московского городского научного общества терапевтов. - И нынешняя не исключение. Скоро пойдет на убыль. Если уже не пошла.
И это, по словам ученого, не столь уж удивительно. По крайней мере, для него. Поскольку относительно мирное наше сосуществование с вирусами и бактериями предопределено природой. Геном человека примерно на половину состоит из ДНК вирусов, которые встраивалась туда в процессе эволюции. А бактерий в нашем организме больше, чем клеток самого организма. Разнообразные микробы помогают переваривать пищу, вырабатывают всякие полезные вещества, укрепляют иммунитет.
С бактериями, которые, иной раз перемещаясь из привычных мест обитания в несвойственные им, начинают вредоносную деятельность, вступают в борьбу защитные силы самого организма и антибиотики, созданные человеком. Бактерии сопротивляются, вырабатывая устойчивость к антибиотикам и атакам защитных сил, но пока проигрывают в этом противостоянии. Выработанный в итоге иммунитет побеждает болезнь. Если организм, конечно, не слишком истощен, не испорчен прожитыми годами и нехорошими излишествами.

Попытки убить вирус физически не самые действенные. Иммунитет - надежнее.
- Создается впечатление, будто бы так оно и есть на самом деле, - отвечает ученый.
КОШМАРЫ МИНУВШИХ ДНЕЙ
Самые страшные вирусные эпидемии в истории человечества
Испанский грипп 1918 года: от 50 до 100 миллионов жертв

Заразившимися "испанкой" были переполнены госпитали.
Скептики сходство эпидемий отрицают, уверяя, что вирусы — прежний и нынешний — хоть и родственники, но все-таки очень разные. Равно, как и заболевания ими вызванные.

Болели "испанкой" не долго: 3 дня - и освобождали место для вновь прибывших.
Оспа: от 300 до 500 миллионов жертв в ХХ веке

Оспа "косила" людей с глубокой древности.
Оспу победила вакцинация. Самый последний случай заболевания зафиксирован в 1978 году. Тогда заразилась британская женщина, работавшая медицинским фотографом. Заразилась в вирусной исследовательской лаборатории. И умерла.
СПИД: около 35 миллионов жертв с начала эпидемии
Синдром приобретенного иммунного дефицита (СПИД) вызывают вирусы иммунного дефицита человека ( ВИЧ ). Считается, что поражать людей они начали с 60-х годов прошлого века - мутировали из тех, которые жили в африканских обезьянах.

СПИД еще не побежден: эпидемия продолжается.
О первых случаях заболевания СПИДОМ заговорили в 1981 году после того, как в США объявили о 30 случаях. Сам вирус был выявлен и изучен в 1983 году. В 2008 году ученые, сделавшие открытие, получили Нобелевскую премию. На удивление, и ВИЧ похож на коронавирус — тоже эдакий шарик с пупырышками.
Первоначально считалось, что СПИД поражает исключительно геев и наркоманов. В итоге же оказалось, что никто не застрахован.
ЭТО БЫЛО НЕДАВНО
Свиной грипп 2009 года: примерно 500 тысяч жертв
Похоже, что 11 лет назад проявил себя мутировавший в очередной раз H1N1. Происхождение этого штамма, способного передаваться от человека к человеку, неизвестно. Но заболевание впервые приобрело массовый характер в Мексике и США.
Летом 2009 года ВОЗ объявила свиной грипп пандемией и присвоила ему шестой - наивысший - уровень опасности.

Вирус свиного гриппа может. где-нибудь "отсидеться", мутировать и опять напасть на людей.
Симптомы свиного гриппа и обычного совпадают — головная боль, жар, кашель, насморк. Вирусы внешне похожи, как все те, которые погубили почти миллиард человек по всему миру.
Читайте также:


