Актуальные проблемы герпесвирусных инфекций

Герпетическая инфекция – инфекция, вызываемая герпесвирусами, для которой характерно поражение кожи, слизистых, глаз, нервной системы.
Инфекция, вызванная герпесвирусами, распространена повсеместно. Инфицированность населения очень высокая. По данным Всемирной организации здравоохранения (ВОЗ) герпесвирусная инфекция занимает второе место среди вирусных заболеваний человека, уступая лишь гриппу.
Восприимчивость к инфекции всеобщая, независимо от пола и возраста.
Подъемы заболевания регистрируются в осенне-зимний период.
Проведенные за последние 10 лет эпидемиологические исследования показали, что к 15-летнему возрасту инфицировано 80% детей, а к 30 годам 90% населения имеют антитела к вирусам того или иного типа.
Возбудитель инфекции – вирус герпеса, включающий более 70 представителей, из которых наибольшую патогенность для человека имеют вирусы простого герпеса 1 и 2 типа (ВПГ 1 или ВПГ 2), вирус ветряной оспы, опоясывающего герпеса, цитомегаловирус (ЦМВ), вирус Эпштейна-Барр, вирус герпеса человека 6 типа, вирус герпеса человека 7 типа.
Попадая в клетку – вирус вызывает ее гибель. В отдельных клетках вирус может сохраняться длительное время, но при последующей активации вируса, клетка погибнет.
Считается, что ВПГ–1 чаще поражает дыхательные пути, а ВПГ-2 - урогенитальную систему, но, несмотря на это, роль ВПГ-1 в развитии генитального герпеса увеличивается.
Вирусы простого герпеса неустойчивы к действию физических и химических факторов, легко разрушаются под действием ультрафиолетовых и рентгеновских лучей, чувствительны к этиловому спирту, эфиру. При низких температурах (-20-70 о С) вирус сохраняется десятилетиями.
Источники инфекции – вирусоносители и больные с различными формами болезни.
Пути передачи инфекции:
- Половой (наиболее значимый);
- Гематогенный;
- Воздушно-капельный;
- Контактно-бытовой (через игрушки, предметы обихода, одежду).
Факторами передачи вируса являются: слюна, кровь, слезная жидкость, сперма, секрет влагалища и цервикального канала, различные органы и ткани, используемые при трансплантации, моча, медицинский инструментарий.
Попадает вирус в организм через поврежденные участки кожи и слизистой, затем, в месте внедрения вируса происходит размножение вирусных частиц. Первичное инфицирование вызывает латентную (скрытую, вялотекущую) инфекцию.
Клиническая картина.
Клинические проявления герпетической инфекции отличаются значительным разнообразием. Они зависят от локализации поражения, распространенности, состояния иммунной системы, типа вируса, а также от механизма заражения.
По локализации поражения:
- Кожа – простой герпес, герпетиформная экзема;
- Слизистые оболочки ротоглотки – стоматит, фарингит, тонзиллит;
- Верхние дыхательные пути – острое респираторное заболевание;
- Глаза – кератоконъюнктивит;
- Урогенитальный тракт – уретрит, цистит, вульвовагинит;
- Нервная система – менингит, энцефалит, менингоэнцефалит;
- Внутренние органы – гепатит, гломерулонефрит, пневмония.
Генитальный герпес развивается у молодых людей после начала половой жизни. Первичный генитальный герпес отличается более тяжелым и продолжительным течением. Высыпания обильные и занимают большую площадь поражения. При первичном генитальном герпесе отмечается повышение температуры, общая слабость, раздражительность. В области гениталий появляются везикулезные высыпания, сохраняющиеся до 8 суток.
Влияние вируса простого герпеса на беременность и роды.
Первичное инфицирование и рецидивы во время беременности могут привести к мертворождению, выкидышам, а также к формированию пороков у плода. Наиболее опасно заражение в третьем триместре.
При первичном инфицировании матери во время беременности инфицирование плода происходит в 5% случаев. Чаще всего инфицирование ребенка происходит во время родов (85%) или после родов (10%).
Инфицирование ребенка ВПГ во время родов может стать причиной последующего развития герпетической инфекции новорожденного.
Основную опасность представляет выделение вируса со слизистой половых органов в момент родов. Выделение вируса может сопровождаться высыпаниями в области половых органов, а может и не сопровождаться никакими симптомами.
Последствия герпесвирусной инфекции для ребенка:
- распространение вируса по всему организму с поражением головного мозга, легких, печени, надпочечников, кожи, глаз, ротовой полости;
- поражение ЦНС (снижение аппетита, судороги, повышенная возбудимость);
- поражение кожных покровов, слизистой оболочки глаз, рта.
Профилактика герпесвирусной инфекции:
Важным принципом профилактики этого заболевания является прекращение близких контактов с больным человеком в период обострения.
- не пользоваться чужими предметами личной гигиены;
- больной герпесвирусной инфекцией должен иметь отдельную посуду и пользоваться личным полотенцем;
Для того чтобы не допустить распространения заболевания на другие части тела рекомендуется:
- губы, пораженные высыпаниями, не трогать;
- наносить противовирусные средства на места высыпания следует ватной палочкой, руками нельзя;
- сдирать корочки и выдавливать пузырьки запрещается;
- если вы носите контактные линзы ни в коем случае нельзя смачивать их слюной.
- пользоваться чужой косметикой и давать кому-то свою категорически запрещено. В магазине перед покупкой не рекомендуется пользоваться тестерами.
Профилактика ВПГ-1 сводится к соблюдению общих правил предупреждения респираторных заболеваний. Профилактика ВПГ-2 соответствует профилактике инфекций передающихся половым путем (использование презервативов во время половых контактов), использование антисептических растворов после полового акта.
Профилактика инфицирования во время беременности:
- исключить половые контакты с партнером, у которого имеются герпетитческие высыпания;
- в третьем триместре беременности воздержаться от половых контактов, если у партнера когда-либо имели место быть герпетические высыпания.
Укрепление иммунитета.
Профилактика обязательно должна быть направлена на укрепление иммунитета, ведь при его ослаблении заболевание обязательно даст о себе знать снова. Переутомления, плохое питание, вредные привычки – все это может стать повторной причиной развития герпеса. Именно поэтому такие ситуации важно не допускать.
Прежде всего, обратите внимание на работу своего желудочно-кишечного трака, ведь все иммунные процессы берут свое начало именно отсюда. Деятельность его будет нормальной только при полноценной работе желчного пузыря.
Ослабнуть иммунитет может при длительном приеме лекарственных препаратов, особенно антибиотиков. По возможности их нужно заменять иными средствами. Так, например, для повышения иммунитета может применяться настойка эхинацеи, купить ее можно в аптеке. Отвар шиповника также оказывает укрепляющее действие на организм.
Главный метод, позволяющий повысить иммунитет – правильное питание. Поэтому если на ваших губах постоянно появляется герпес следует обратить внимание на свой рацион питания.
Должны присутствовать следующие продукты:
- фрукты и овощи в свежем виде;
- молочные продукты;
- морепродукты;
- мясо, но кроме говядины;
- яйца и прочее.
Не забывайте о сое, пивных дрожжах, они также полезны как при профилактике, так и в момент лечении. Есть также и те продукты, употреблять которые ни в коем случае нельзя: сахар, говядина, орехи.
Человеку, в период обострения, то есть когда появляются высыпания, рекомендуется больше времени проводить дома, ведь в этот момент есть большая опасность для окружающих.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Герпесвирусы широко распространены в человеческой популяции. После первичного инфицирования вирусы герпесгруппы переходят в латентное состояние и пожизненно персистируют в организме. При неблагоприятных условиях и снижении местного или системного иммунитета может происходить реактивация инфекции, что обусловливает развитие воспаления чаще всего на местном уровне. Разнообразие клинических форм герпесвирусных инфекций постоянно поддерживает научный интерес как в области изучения их патофизиологии, так и в области поиска эффективной противовирусной терапии. Особенно актуально это для β- и γ-герпесвирусов, т. к. группа α-герпесвирусов изучена достаточно хорошо.
Цель исследования: определить эффективность валацикловира в отношении репликации вируса Эпштейна – Барр (ВЭБ), вируса герпеса человека 6 типа (ВГЧ-6), цитомегаловируса (ЦМВ) в ротоглотке у часто болеющих взрослых с хроническими воспалительными заболеваниями верхних дыхательных путей (ВДП).
Материал и методы: нами амбулаторно обследованы 80 пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП. Всем пациентам проводились микробиологическое исследование мазков из ротоглотки и оценка вирусной нагрузки в смешанной слюне и цельной крови вне периода обострения. Пациенты получали терапию валацикловиром по схеме 500 мг 3 р./сут в течение 14 дней. Контроль вирусной нагрузки в биоматериале проводился после окончания лечения.
Результаты и обсуждение: микробный пейзаж ротоглотки часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой. В смешанной слюне обнаруживалась ДНК ВЭБ, ВГЧ-6, но не ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлялась. Применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у часто болеющих взрослых.
Выводы: целесообразно провести дальнейшие исследования по определению режима дозирования и оценке клинической эффективности ациклических нуклеозидов в лечении ВЭБ-инфекции.
Ключевые слова: герпесвирусы, вирус Эпштейна – Барр, вирус герпеса человека, цитомегаловирус, часто болеющие взрослые, вирусная нагрузка, валацикловир.
Для цитирования: Щубелко Р.В., Зуйкова И.Н., Шульженко А.Е. Герпесвирусные инфекции человека: клинические особенности и возможности терапии. РМЖ. 2018;8(I):39-45.
Human herpesviruses infections: clinical features and opportunities of therapy
R.V. Shubelko 1 , I.N. Zuykova 2 , A.E. Shulzhenko 2
1 JSC "K+31", Moscow
2 “National Research Center — Institute of Immunology” Federal Medical-Biological Agency of Russia, Moscow
Herpesviruses are widely spread among the human population. After the primary infection, the herpesviruses become latent and persistent in the human body for life. Adverse conditions and a low local or systemic immunity may reactivate the infection, which causes the inflammation, usually at the local level. The variety of clinical forms of herpesviruses infections constantly supports scientific interest both in the field of studying their pathophysiology and in the search for effective antiviral therapy. This is especially important for β- and γ-herpesviruses, since the α-herpesvirus group has been studied rather well.
Aim: to determine the efficacy of valacyclovir for replication of the Epstein-Barr virus (EBV), human herpesvirus type 6 (HHV-6), cytomegalovirus (CMV) in the oropharynx in frequently ill adults with chronic inflammatory diseases of the upper respiratory tract.
Patients and Methods: 80 patients with frequent recurrences of chronic inflammatory diseases of the upper respiratory tract were examined outpatiently. All patients underwent microbiological examination of swabs from the oropharynx and the viral load in mixed saliva and whole blood not in exacerbation period was assessed. Patients received valacyclovir therapy according to the scheme 500 mg x 3 times a day for 14 days. Control of viral load in the biomaterial was carried out after the end of treatment.
Results and Discussion: out of the period of exacerbation the oropharynx microflora in frequently ill adults is represented mainly by a normal or conditionally pathogenic microflora. EBV DNA, HHV-6, but not CMV DNA, were detected in the mixed saliva. The DNA of the herpesvirus was not detected in the blood samples of these patients. The use of valacyclovir in a dose
of 500 mg 3 times a day significantly reduces the replication of EBV in the oropharynx in frequently ill adults.
Conclusions: it is advisable to conduct further studies to determine the dosage regimen and evaluate the clinical efficacy of acyclic nucleosides in the treatment of EBV infection.
Key words: herpes viruses, Epstein-Barr virus, human herpes virus, cytomegalovirus, frequently ill adults, viral load, valacyclovir.
For citation: Shubelko R.V., Zuykova I.N., Shulzhenko A.E. Human herpesviruses infections: clinical features and opportunities of therapy // RMJ. 2018. № 8(I). P. 39–45.
В статье рассмотрены клинические особенности и возможности терапии герпесвирусных инфекции человека. Определена эффективность валацикловира в отношении репликации вируса Эпштейна – Барр, вируса герпеса человека 6 типа, цитомегаловируса.
Только для зарегистрированных пользователей
Методические указания для студентов к практическому занятию № 6.
Тема: Лабораторная диагностика герпесвирусных инфекций.
Цель: Изучение лабораторной диагностики герпесвирусных инфекций.
Модуль 3. Общая и специальная вирусология.
Содержательный модуль 16. Специальная вирусология.
Тема 6:Лабораторная диагностика герпесвирусных инфекций.
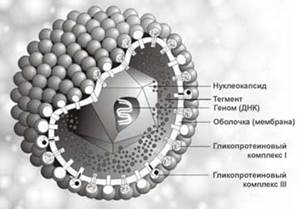
Актуальность темы:
Вирус простого герпеса – одна из самых распространенных вирусных инфекций человека, характеризующаяся лихорадочным состоянием и пузырьковыми высыпаниями, которые чаще всего локализуются на коже и слизистых оболочках. Важными особенностями герпетической инфекции являются пожизненное носительство вируса и частые рецидивы болезни.
Вирусная природа простого герпеса установлена в 1912 г. У. Грютером.
(Трёхмерное изображение вируса герпеса).
Герпесвирусы и вызываемые ими заболевания
| Типы вирусов герпеса | Вызываемые заболевания |
| ВПГ-1 (вирус простого герпеса типа 1) | Поражение: кожи, слизистой оболочки ротовой полости, конъюнктивы или роговицы глаза, энцефалиты |
| ВПГ-2 (вирус простого герпеса типа 2) | Поражение слизистых оболочек гениталий, у новорожденных - центральной нервной системы |
| ВЗВ (вирус ветрянки) | Ветряная оспа, опоясывающий лишай, постгерпетическая невралгия; язвенно-некротическая форма опоясывающего герпеса - СПИД-индикаторный признак заболевания |
| ЦМВ (цитомегаловирус) | Патологии новорожденных; осложнения после трансплантации органов и костного мозга: интерстициальная пневмония, гастроинтестинальные расстройства, гепатиты |
| ВЭБ (вирус Эпштейна-Барра) | Инфекционный мононуклеоз, лимфома Беркитта, рак носоглотки |
| ВГ-6 | Вирус, вызывающий фатальные интерстициальные пневмонии и инфекционные розеолы новорожденных |
| ВГ-7 | Вирус, выделенный от больных с синдромом хронической усталости |
| ВГ-8 | Вирус, выделенный из биоптата больного саркомой Капоши, ассоциированный с лимфопролиферативными заболеваниями |
| Примечание. ВГ - вирус герпеса. |
Таксономия, морфология, химический состав. Возбудитель простого герпеса - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Simplexvirus. По морфологии и химическому составу не отличается от вирусов ветряной оспы и опоясывающего герпеса.

Культивирование. Вирус простого герпеса (ВПГ) культивируют в куриных эмбрионах, культурах клеток и организме лабораторных животных. На хорионаллантоисной оболочке куриных эмбрионов вирус образует мелкие белые плотные узелки-бляшки; в зараженных культурах - вызывает цитопатический эффект: образование гигантских многоядерных клеток с внутриядерными включениями.
Антигенная структура. Вирус содержит ряд антигенов, связанных как с внутренними белками, так и с гликопротеидами наружной оболочки. Последние являются основными иммуногенами, индуцирующими выработку антител и клеточный иммунитет. Существует два серотипа вируса: ВПГ типа 1 и ВПГ типа 2.
Резистентность. Вирус может выживать на поверхности предметов при комнатной температуре в течение нескольких часов, чувствителен к УФ-лучам, обычным дезинфицирующим средствам, жирорастворителям, термолабилен.
Восприимчивость животных. Вирус простого герпеса патогенен для многих животных, у которых вызывает энцефалит при введении возбудителя в мозг или местный воспалительный процесс при заражении в глаз. В естественных условиях животные не болеют.
Эпидемиология. Простой герпес - одна из самых распространенных инфекций, которая поражает различные возрастные группы людей, чаще в осенне-зимний период. Отмечаются спорадические случаи заболевания, иногда небольшие вспышки в семьях, детских коллективах, больницах. Эпидемий не наблюдается.
Источником инфекции являются больные и носители. Основной механизм передачи - контактный, аэрогенный. Заражение происходит при попадании вирусов на поврежденные кожные покровы или слизистые оболочки.
Эпидемиология герпеса, вызванного вирусами типов 1 и 2, различна. ВПГ типа 1 передается через слюну, зараженные слюной руки и предметы быта, а ВПГ типа 2 - половым путем. Возможно заражение плода через плаценту.
Патогенез и клиническая картина. По клиническим проявлениям различают первичный и рецидивирующий герпес. Входными воротами возбудителя при первичной герпетической инфекции являются поврежденные участки кожи и слизистых оболочек рта, глаз, носа, мочеполового тракта, где вирусы репродуцируются. Затем по лимфатическим сосудам вирусы попадают в кровь и заносятся в различные органы и ткани.
Инкубационный период при первичном герпесе составляет в среднем 6-7 дней. Заболевание начинается с жжения, зуда, покраснения, отека на ограниченных участках кожи и слизистых оболочек, затем на этом месте появляются пузырьковые высыпания, наполненные жидкостью. Иногда заболевание сопровождается повышением температуры тела и нарушением общего состояния. При подсыхании пузырьков рубцов не образуется. Первичный герпес у новорожденных протекает тяжело и нередко заканчивается смертью. Однако у большинства людей первичная инфекция остается нераспознанной, так как протекает бессимптомно.
После первичной инфекции (явной и бессимптомной) 70-90 % людей остаются пожизненными носителями вируса, который сохраняется в латентном состоянии в нервных клетках чувствительных ганглиев. Нередко у носителей появляются рецидивы болезни в результате переохлаждения, перегревания, менструации, интоксикации, различных инфекционных заболеваний, стрессов, нервно-психических расстройств. Для рецидивирующего герпеса характерны повторные высыпания на коже и слизистых оболочках, нередко в тех же местах. Наиболее частой локализацией рецидивирующего герпеса, вызванного ВПГ типа 1, являются губы, крылья носа, полость рта, конъюнктива глаз. ВПГ типа 2 поражает мочеполовую систему и вызывает герпес новорожденных. Доказана роль ВПГ типа 2 в развитии рака шейки матки. Сравнительно редко встречаются генерализованные формы рецидивирующего герпеса, в частности поражения нервной системы и внутренних органов.
Иммунитет. В результате первичной герпетической инфекции в организме образуются сывороточные и секреторные антитела, которые обусловливают иммунитет к первичному герпесу, но не препятствуют сохранению вируса и возникновению рецидивов. Рецидивирующий герпес возникает при высоком уровне антител к вирусу герпеса. Основное значение в развитии рецидивирующего герпеса имеет состояние клеточного иммунитета.
Лабораторная диагностика. Материалом для исследования являются содержимое герпетических пузырьков, слюна, соскобы с роговой оболочки глаза, кровь, цереброспинальная жидкость, в летальных случаях . кусочки головного и спинного мозга.
Экспресс-диагностика заключается в обнаружении гигантских многоядерных клеток с внутриядерными включениями в мазках-отпечатках из высыпаний, окрашенных по Романовскому-Гимзе. Для дифференциации от других вирусов, принадлежащих к этому семейству, используют РИФ, ИФА, РИА, ПЦР. Выделение вируса проводят на куриных эмбрионах, культуре клеток и на лабораторных животных (мыши-сосунки), идентифицируют вирус с помощью РИФ или РН. В последние годы в диагностике простого герпеса начали применять моноклональные антитела, что дает возможность определить серотип вируса. Для серодиагностики заболевания используют РСК, РН, РИФ, ИФА.
Специфическая профилактика и лечение. Для профилактики тяжелых форм рецидивирующего герпеса в период ремиссии применяют многократное введение инактивированной, культуральной герпетической вакцины. Вакцинация, а также применение иммуномодуляторов, например реаферона, удлиняют межрецидивный период и облегчают течение последующих рецидивов. В остром периоде с лечебной целью используют химиотерапевтические препараты (виразол, ацикловир, оксолиновую, тебро-феновую, флореналовую мази, бонафтон), интерфероны и индукторы интерферона.
Вирус цитомегалии

Цитомегалия - инфекционное заболевание, возбудителем которого является цитомегаловирус (ЦМВ) Cytomegalovirus hominis (от греч. cytys - клетка, megas - большой). Вирус вызывает цитомегаловирусную инфекцию человека, характеризующуюся поражением почти всех органов (преимущественно слюнных желез) с образованием в них гигантских клеток с внутриядерными включениями, протекающую в различных формах - от бессимптомного носительства до тяжелой генерализованной формы, заканчивающейся летальным исходом.
Вирус впервые выделен К. Смитом в 1956 г.
Таксономия, морфология, антигенная структура. Возбудитель цитомегалии - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Cytomegalovirus.
Морфология, химический состав типичны для семейства герпесвирусов. Диаметр вирусной частицы (вириона) около 180 нм. В центре вириона находится двенадцатигранный нуклеокапсид, содержащий генетическую информацию - двухнитевую ДНК-вируса. Установлено 2 антигенных серотипа вируса.
Резистентность. Вирус термолабилен, чувствителен к дезинфицирующим средствам и жирорастворителям.
Эпидемиология. Цитомегаловирусная инфекция широко распространена на земном шаре. Источником вируса является больной человек или носитель. Вирус выделяется со слюной, мочой, секретами организма, реже фекалиями. Предполагается, что ведущий механизм передачи инфекции - контактно-бытовой, возможны аэрогенный и фекально-оральный механизмы передачи. Цитомегаловирус обладает высокой способностью проникать через плаценту (вертикальная передача), вызывая внутриутробную патологию плода.
Патогенез и клиническая картина. Патогенез не вполне выяснен. Инфекция связана с длительным носительством вируса, который в латентном состоянии сохраняется в слюнных железах, почках и других органах. Активация латентной инфекции происходит при иммунодефицитных состояниях, иммунодепрессивной терапии. Вирус поражает ЦНС, костный мозг, почки, печень, клетки крови. У беременных женщин цитомегалия может приводить к недоношенности, мертворождению, развитию аномалий у плода.
Иммунитет. У больных независимо от клинической формы инфекции, а также у носителей образуются антитела, которые, однако, не препятствуют сохранению вируса в организме и выделению его в окружающую среду. Интенсивность развития болезни находится под контролем клеточной иммунной системы хозяина.
Лабораторная диагностика. Обследованию на цитомегалию в первую очередь подлежат дети с поражением ЦНС и врожденными уродствами, а также женщины с неблагополучно протекающей беременностью. Исследуемый материал - слюна, моча, мокрота, цереброспинальная жидкость, кровь, пунктат печени.
Специфическая профилактика и лечение. Разработана живая аттенуированная вакцина. Для лечения применяют химиотерапевтические препараты (ганцикловир, фоскорнет натрия), иммуномодуляторы, интерферон.
Не нашли то, что искали? Воспользуйтесь поиском:

В Клиническом отделении №3 г. Кисловодска добавлены услуги УЗИ-диагностики
Среди семейства Herpesviridae к человеческим патогенам относятся вирус простого герпеса 1 типа (ВПГ-1) и 2 типа (ВПГ-2), вирус зостер, герпесвирус человеческий типа 6 (ВГЧ-6), цитомегаловирус человеческий (ЦМВ), вирус Эпштейна-Барр, герпесвирусы 7 и 8 типа.
Вирус герпеса человека (вирус простого герпеса) 1 типа (ВПГ-1) - наиболее часто вызывает поражения слизистой оболочки полости рта, глаз и кожи (орофациальный герпес, его рецидивирующую форму - herpes labialis) и значительно реже - поражение гениталий, а также герпетический энцефалит и пневмонит.
Вирус герпеса человека (вирус простого герпеса) 2 типа (ВПГ-2) - вызывает поражение гениталий, неонатальный герпес, диссеминированный герпес.
Вирус герпеса человека 3 типа (ВГЧ-3) или вирус varicella zoster - вызывает ветряную оспу и опоясывающий лишай.
Вирус герпеса человека 4 типа (ВГЧ-4) или вирус Эпштейна-Барр - вызывает инфекционный мононуклеоз, лимфому Беркитта, ворсистую лейкоплакию языка, назофарингеальную карциному, В-клеточную лимфому, синдром хронической усталости и иммунной депрессии.
Единственный резервуар инфекции - человек. Основной путь передачи - воздушно-капельный, реже трансмиссивный или половой.
В раннем возрасте инфекцию сопровождают стёртые проявления, либо она бывает вообще бессимптомной; первичное инфицирование в подростковом или более старшем возрасте может вызвать заболевание, известное как инфекционный мононуклеоз. Патогенез инфекционного мононуклеоза включает репликацию вируса в верхних отделах дыхательных путей и ассоциированной лимфоидной ткани с развитием местных воспалительных реакций и лихорадочного состояния. Возбудитель индуцирует появление популяции реактивных Т-клеток (атипичные лимфоциты), а также поликлональную активацию В-клеток и их дифференцировку в плазмоциты, секретирующие гетерофильные AT с низким аффинитетом к вирусу, но реагирующие с различными субстратами, включая эритроциты различных животных. При этом геном вируса может сохраняться в В-лимфоцитах в латентной форме. Значительно реже выявляют хроническую персистенцию вируса, известную как реактивированная хроническая ВЭБ-инфекция.
Состояние представлено множеством форм и встречается достаточно редко; среди них чаще наблюдают синдром хронического мононуклеоза (характерны жалобы на постоянную слабость при наличии или отсутствии каких-либо изменений лабораторных показателей). Хроническая активная ВЭБ инфекция обычна для пациентов с иммунодефицитами (наиболее часто со СПИДом и реципиентов трансплантатов). Наиболее часто проявляется прогрессирующим лимфопролиферативным заболеванием либо лимфомами ЦНС. Способность возбудителя вызывать злокачественную трансформацию клеток даёт основание предполагать участие вируса (как коканцерогена) в развитии болезней злокачественного роста, таких как африканские формы лимфомы Беркетта, карцинома носоглотки у мужчин некоторых этнических групп Южного Китая, а также саркома Капоши у пациентов со СПИДом.
Механизмы развития злокачественных трансформаций, индуцированных вирусом Эпштейна-Барр, связаны со способностью инфицировать В-лимфоциты и нарушать их дальнейшую дифференцировку; при этом часть вирусного генома экспрессируется в инфицированных лимфобластах.
Диагностика: обнаружение атипичных мононуклеаров в крови, серологические методы, ПЦР.
Лечение: при инфекционном мононуклеозе, как правило, симптоматическое; вирус чувствителен к ряду противогерпетических препаратов.
Вирус герпеса человека 5 типа (ВГЧ-5) - вызывает ЦМВ-инфекцию (врожденные повреждения ЦНС, ретинопатии, интерстициальный пневмонит, гепатит, энтероколит при СПИДе, цитомегалия при иммунодефиците и трансплантации органов).
Вирус проникает в организм через слюну при поцелуях и через секреты гениталий при половых контактах, через грудное молоко и при использовании нестерильного шприца, при трансплантации органов и переливании донорской крови, при использовании донорской спермы и яйцеклеток. Предполагают, что главным хранилищем вирусов являются мононуклеарные фагоциты - моноциты и макрофаги, а так же эпителиоциты слюнных желез и почечных канальцев, гепатоциты и некоторые другие клетки.
Заражение цитомегаловирусом может произойти ещё в период внутриутробного развития плода. Необходимым условием заражения плода является вирусемия беременных. Если плод заразился этим вирусом в утробе матери, то это будет врождённая цитомегаловирусная инфекция. У таких детей может быть желтуха, увеличиваются печень и селезёнка, могут быть тяжёлые врождённые пороки, иногда несовместимые с жизнью. Инфекция может протекать и бессимптомно, но у 5-25% таких детей в последующие несколько лет может наблюдаться снижение слуха, нарушения психики, могут появиться аномалии глаз. Если ребёнок заражается во время или через небольшой промежуток времени после рождения, то он плохо прибавляет в весе, у него может развиться гепатит, анемия, появиться сыпь.
В подростковом возрасте цитомегаловирусная инфекция может проявить себя в виде мононуклеоза. При этом заболевании поднимается температура, появляются боли в мышцах, развивается быстрая утомляемость. У людей с иммунодефицитом инфекция протекает обычно тяжело.
Цитомегаловирусная инфекция является частым спутником СПИДа. При этом поражаются многие внутренние органы, что может закончиться смертью больного. Основные симптомы: лихорадка, недомогание, отсутствие аппетита, боли в мышцах, кашель. При поражении тонкого кишечника могут возникать язвы, которые, в свою очередь могут кровоточить или перфорировать (в стенке желудка или кишечника появится сквозное отверстие). Ретинит (поражение сетчатки глаза), вызванный цитомегаловирусом, может привести к слепоте. У человека с нормальным иммунитетом цитомегаловирусная инфекция никак себя не проявляет и может не давать о себе знать всю жизнь. После пересадки органов и костного мозга активная цитомегаловирусная инфекция обычно развивается в первые четыре месяца после операции и очень часто является причиной заболеваний, и даже смерти реципиентов. Источником инфекции может стать реактивация собственного ЦМВ или повторное заражение реципиента через донорские органы, переливание крови и ее компонентов. Существует предположение, что ЦМВ-инфекция играет определённую роль в патогенезе острых и хронических реакций трансплантата против хозяина.
Лечение: современные противогерпетические препараты - ациклические нуклеозиды - обладают высокой специфичностью и неплохо себя зарекомендовали в лечении цитомегаловирусных инфекций. В последние годы обнаружены штаммы ЦМВ, имеющие двойную устойчивость к ганцикловиру и фоскарнету.
Вирус герпеса человека 6 типа (ВГЧ-6) - вызывает острые поражения кожи у детей раннего возраста (ложную краснуху - внезапную экзантему (эритема новорожденных)), синдром хронической усталости и иммунной депрессии у взрослых.
ВГЧ-6 (В-лимфотропный герпесвирус) впервые выделен в 1986 году Salahuddin в США из лимфоцитов периферической крови больных с лимфопролиферативными и иммунодефицитными заболеваниями. Основные инфицированные клетки - Т-лимфоциты. Кроме того поражаются мегакариоциты, глиобласты, В-лимфоциты. ВГ-6 имеет последовательность, гомологичную ЦМВ.
Первичное инфицирование происходит в первые годы жизни, далее следует бессимптомная сероконверсия и вирусоносительство. Реактивация вируса происходит у вышеперечисленных больных, причины до конца не выяснены. Не всякое нарушение иммунной системы сопряжено с активацией ВГ-6. У пациентов с трансплантированной почкой, которым проводилась иммуносупрессивная терапия, титр антител оставался нормальным. Можно считать, что активация ВГ-6 - это результат избирательного поражения лишь определенных субпопуляций Т-лимфоцитов, контролирующих уровень размножения вируса.
Не выявлено общих нуклеотидных последовательностей с другими человеческими герпесвирусами, нет перекрестной реакции антител. Пути передачи общие с ЦМВ и ВЭБ. Антитела регистрируются у 26% взрослых людей, среди детей до 4 лет - у 94-100%.
- В-клеточная лимфома. В 80-90% случаев В-клеточных лимфом в трансформированных клетках выделяют интегрированные фрагменты ДНК, гомологичные геному вируса, что даёт основания рассматривать его как возможный этиологический агент.
- Exanthema subitum (roseola infantum). Розеола детская (внезапная), или ложная краснуха - острая вирусная инфекция детей младшего возраста, вызванная ВГ-6; характерны внезапный подъём температуры, лихорадка (иногда с судорогами) и критическое разрешение через несколько дней с появлением пятнисто-папулёзной сыпи.
- Синдром хронической усталости. Относительно недавно выделен в самостоятельную нозологическую единицу; основание для установления этиологической роли ВГ-6 - выявление специфических антител в сыворотке пациентов. Однако это положение остаётся предметом дискуссии, т.к. эти антитела можно выявить у 90% здоровых лиц.
Диагностика: выделение на культуре клеток, иммунологические методы, микроскопия.
Лечение: лечение симптоматическое, получены данные об эффективности ганцикловира.
Этиологическая роль еще двух типов - ВГЧ-7 и ВГЧ-8 точно не установлена, хотя полагают, что ВГЧ-7 ассоциирован с лимфопролиферативными заболеваниями, а ВГЧ-8 - с саркомой Капоши. (29)
Свойства ВГЧ-7: растет медленно, лишь на CD4 лимфоцитах человека, которые имеют клеточные рецепторы к этому вирусу. Вирус определяется в периферической крови и слюне. Очень часто у людей с вирусом герпеса 7 типа выделяют вирус герпеса 6 типа.
Является возможной причиной синдрома хронической усталости (Chronic Fatigue Syndrome, CFS). Полагают, что вирус герпеса человека 7 типа может быть причиной лимфопролиферативных заболеваний.
Проявления заболевания: синдром хронической усталости можно заподозрить по совокупности ряда признаков: беспричинная слабость, повышенная плаксивость; высокая утомляемость; повышенный уровень тревожности; депрессии; нарушение сна (фазы засыпания). На утро чувство разбитости; температура 36,9-37,3 гр. Цельсия в течение 6 месяцев; беспричинное увеличение лимфоузлов - лимфоаденопатия.
Диагностика: полимеразная цепная реакция (ПЦР), иммуноферментный анализ (ИФА); иммунограмма, на которой можно отметить: снижение NK (естественные киллеры), увеличение CD8 лимфоцитов, ЦИК, IgG; анализ личности больного (симуляция).
Лечение: симптоматическое. Проводится невропатологом или психиатром. Заключается в противовирусной терапии и лечении, направленном на укрепление иммунитета.
Профилактика: не разработана.
Вирус герпеса 8 типа (ВГ-8, HHV8)
ДНК этого вируса постоянно обнаруживается в ткани СПИД-ассоциируемой саркомы Капоши, в то время как в нормальной ткани соседних участков не выявляется. Было установлено, что HHV8 связан со всеми типами саркомы Капоши, включая эндемическую у африканцев, классическую у пожилых людей средиземноморья и трансплантат-связанную. Показано, что за 3-10 лет развитию саркомы Капоши предшествует инфекция, вызванная HHV8. С помощью ПЦР одни авторы вирус обнаруживали в семенной жидкости и сперме, хотя другие этого не подтвердили. HHV8 был выявлен в эндотелиальных клетках, циркулирующих CD20+ лимфоцитах (В-клетки), носовом секрете, бронхоальвеолярной леважной жидкости у больных с легочной локализацией саркомы Капоши.
Клиника. Классическая форма проявляется в виде локализованных узлов коричнево-красного - синюшно-красного цвета с локализацией преимущественно на коже нижних конечностей. Выделяют следующие стадии заболевания: кожные проявления, локализованное торпидное течение (классическое), кожные проявления, локализованное агрессивное течение с увеличением или без увеличения лимфатических узлов (африканский локализованный агрессивный вариант), генерализованные кожные проявления и/или поражение лимфатических узлов (африканская лимфаденопатия и эндемический вариант), висцеральные проявления (эпидемический вариант).
По новым данным известно, что существует вертикальная передача ВГЧ-8 от матери ребенку. Исследователи изучили вертикальную передачу герпесвируса, ассоциированного с саркомой Капоши, от 89 серопозитивных матерей к новорожденным детям. Из 89 детей только у 2 был обнаружен вирус герпеса 8 типа. (39)
Согласно этим новым данным предполагается, что KSHV может передаваться во время беременности, но это возникает очень редко. Тем не менее, исследователи рекомендуют сообщать беременным женщинам о возможном риске передачи вируса и, не исключено, даже скринировать на наличие KSHV во время беременности женщин из групп риска. Однако матери должны быть предупреждены, что KSHV - только фактор риска развития саркомы Капоши, и это не означает, что вирус герпеса 8 типа - единственный фактор, обязательно приводящий к развитию саркомы Капоши.
Исследователи отмечают, что пока недостаточно информации о том, каким образом передается вирус от матери к ребенку, но полагают, что, вероятнее всего, KSHV передается преимущественно во время или после родов, а наибольшая концентрация герпесвируса, ассоциированного с саркомой Капоши, отмечается в слюне.
В некоторых лаборатория сейчас уже доступны раздельные анализы на антитела к ВПГ-1 и ВПГ-2. Единственный типоспецифический белок на поверхности ВПГ-2 - гликопротеин G-2 - используется в ИФА для обнаружения ВПГ-2 - специфических IgG и IgM. Очень высокая чувствительность (95-99%) и специфичность (100%) были достигнуты с помощью этих типоспецифических серологических тестов. Необходимое время - 4-6 часов.
Рекомендуется проведение повторного исследования (2-4 раза в течение 5-7 дней) материала из различных очагов инфекции (на 18-20 дни менструального цикла) для повышения выявляемости ВПГ.
Для точной диагностики необходимо исследовать как АГ + АТ, так и иммунный статус. Наличие интерферона в сыворотке крови более 2 ЕД говорит об острой инфекции.
Читайте также:


