Артрит энцефалит коз опасен ли для людей
Артрит-энцефалит коз — (АЭК), симптомокомплекс, характеризующийся развитием демиелинизирующего энцефалита, прогрессирующего артрита и интерстици-альной пневмонии. Болезнь, известная также как лейкоэнцефаломиелит-артрит коз.
Предполагается, что болезнь распространена широко, так как симптомокомплекс поражения 3-систем органов (ЦНС, суставов, легких) у коз уже описан в некоторых странах. Инфекция широко известна во Франции. Чаще вирус встречается в районах интенсивного козоводства — Европе, Австралии, США. При этом только у 1—2 % инфицированных животных поражается ЦНС и до 30—40 % (в последствии) — суставы. В Мексике обнаружили вирусные частицы ВАЭК при клиническом, серологическом, патологическом, иммуногистохимическом и ультраструктурном исследовании молочных коз. Изучали ткани после гибели животных. Исследовали синовиальные мембраны, легкие и молочные железы от коз с клинической характеристикой заболевания и содержанием специфических антител.
Болезнь широко поражает козлят в возрасте 1—5 месяцев. По клиническим признакам АЭК похож на синдром висны-маэди у овец. В ранних сообщениях эта болезнь была представлена как маэди или ППО по аналогии с аденоматозом овец, проявляется атаксией, гиперстезией, иногда лихорадкой, прогрессирующими парезами конечностей, перерастающими в параличи. Процесс чаще начинается с задних конечностей и распространяется на передние. Животные часто погибают с картиной тетраплазии. Присоединяются явления пневмонии и воспаления суставов. Яркий клинический признак — увеличение объема путового сустава. Картина крови, как правило, без изменений, иногда может наблюдаться лимфопения. В цереброспинальной жидкости отмечается плеоцитоз, в основном за счет мононуклеарных клеток, и увеличение количества белка. Течение болезни — несколько недель, исход — летальный.
Патоморфологические изменения у естественно и экспериментально инфицированных животных локализуются в ЦНС, суставах и легких. В ЦНС изменения выявляют в белом веществе головного и спинного мозга и мозжечке. Наиболее выраженные поражения чаще обнаруживаются в шейных и грудных отделах спинного мозга. Микроскопически поражения характеризуются образованием плотных периваску-лярных муфт из мононуклеарных клеток, формированием лимфоцитарных инфильтратов, пролиферации глии и выраженной первичной демиелинизацией. В тяжелых случаях участки нервных клеток замещаются глиальными рубцами. В суставах обнаруживается гиперплазия синовиальных клеток, лимфопитарная и плазмоклеточная инфильтрация. При прогрессировании болезни нарастают дегенеративные изменения, такие как фиброз, некроз, и минерализация синовильных оболочек, появляются периартикулярные коллагенозные структуры. В легких — изменения, аналогичные наблюдаемым при маэди у овец: интерстициальная пневмония, гиперплазия пери-бронхиальной лимфоидной ткани.
Вирус пребывает в латентном состоянии в предшественниках макрофагов и начинает реплицироваться в период их дифференциации. На процесс репликации вируса влияют вирусные AT и цитокины. AT к гликопротеинам одних лентивирусов нейтрализуют вирус, в то время как AT к гликопротеину других вирусов соединяются с вирионами, но не нейтрализуют их. Образовавшиеся в таких случаях комплексы вирус - АТ связываются с Fc-рецепторами макрофагов и способствуют проникновению вирусов в клетки. После проникновения в ткани инфицированные макрофаги взаимодействуют с лимфоцитами и индуцируют воспалительный каскад с дальнейшей продукцией цитокинов, которые усиливают экспрессию AT класса II — главного комплекса гистосовместимости и пролиферацию лимфоцитов В и CY. Патологический процесс, по-видимому, усиливается образованными комплексами: вирусный гликопротеин — Ig.
Вирус относится к семейству Retroviridae, близок, но не идентичен вирусу висны-маэди. По многим свойствам сходен с вирусом висны-маэди овец. Вирус, изолированный от больных коз, обладает свойствами, характерными для ретровирусов. Вирус содержит 60—70S РНК и РНК-зависимую ДНК-полимеразу, а в инфицированных вирусом культурах клеток обычно обнаруживают вирусные частицы, морфологически характерные для ретровирусов. В градиенте сахарозы его плотность составляет 1,15 г/см3, т. е. идентична плотности вируса висны-маэди.
Морфогенез вируса АЭК идентичен морфогенезу вируса висны-маэди: частицы типа С ретровируса диаметром 100—120 нм почкуются на плазменных мембранах инфицированных клеток. Почкующаяся частица содержит электронноплотную внутреннюю структуру, имеющую форму полумесяца. После созревания частицы отпочковываются в межклеточное пространство; зрелые экстрацеллюлярные вирионы имеют отчетливый промежуточный слой, электронноплотное центрально расположенное ядро.
Структурные белки АЭК очень похожи на белки вируса висны-маэди овец, а их АГ детерминанты перекрестно реагируют со структурным полипептидом рЗО вируса висны-маэди. Эти вирусы в РИД неразличимы, поэтому некоторые исследователи считают, что вирус АЭК является вариантом вируса висны-маэди овец, хотя, как установлено, они различаются по критерию гомологичности нуклеотидных последовательностей генома и являются двумя различными представителями семейства ретровирусов. Гомологичные участки геномов этих вирусов, были выявлены в районах gag и pol и небольшой области гена env, контролирующих групповую специфичность, определяемую близкими в АГ-отношении внутренними белками двух вирусов. Негомологичные участки, такие как большая область гена env, могут представлять уникальные последовательности нуклеотидов, определяющие штаммовую специфичность и клеточный тропизм. Таким образом, полученные данные хорошо коррелируют с результатами сравнительного изучения биологических свойств, указанных вирусов.
Устойчивость не изучена. Прототипные шт. — К 1514, 1736—81, 2150—81. Вышеприведенные данные о родстве вируса АЭК с возбудителем висны-маэди, вызывающим у козлят в возрасте 2—4 месяцев пневмонию и поражение ЦНС, а у взрослых особей — артрит, чаще путового сустава, подтверждаются рядом исследователей. Данный вирус более связан с вирусом висны, чем с вирусом ВИЧ. Вирус кодирует белок Rev, необходимый для эффективной репликации его в культуре клеток. Поверхностный гликопротеин gp 135 вируса АЭК формируется в результате посттрансляционной модификации гликозилированного gp 155. Установлена частичная гомология генома ВИЧ с геномами лентивирусов домашних животных: висны-маэди, АЭЕ и ИНАН. Наиболее выраженная гомология обнаружена с геномом вируса висны-маэди. Исходя из имеющихся данных о последовательностях, проведен филогенетический анализ лентивирусов мелких жвачных для фрагментов из областей env, pol, gag и LTR Дивергенция между фрагментами варьировала от 16 % в областях gag и pol до 22 % в env и 35 % в LTR. Существует как негативный, так и позитивный дарвиновский отбор в генах исследуемых лентивирусов. При построении филогенетических деревьев по относительной скорости замен применительно к позиции кодонов выявлены интересные взаимоотношения между лентивирусами овец и коз. В целом дифференцировано, как минимум, 6 разных экотипов (clades) без четкого разделения штаммов, выделенных от коз (вирус артрита-энцефалита коз) и овец (вирус маэди-висна). Филогенетические деревья, построенные на основе фрагментов из разных кодирующих областей, хорошо согласовались между собой, равно как и с деревьями, построенными с использованием других методов филогенетического реконструирования. Таким образом, получены убедительные свидетельства существования и эпидемиологического значения межвидовой трансмиссии.
Экспериментальная инфекция воспроизводится на ягнятах 1,5-месячного возраста, у которых развиваются артриты и продуцируются вирусоспецифические AT. С этой целью кровь от молодых серонегативных коз центрифугируют в растворе фи-кола с последующей адгезией в лунках пластиковых плашек, выделяют моноциты. Последние инфицируют in vitro вирусом и инокулируют козам в дозе по 105 клеток/животное. Спустя 3 месяца инфицированных животных обрабатывают гексаметазоном. Обработка обостряет течение инфекции. После ее проявления у всех коз, | инфицированных чужими моноцитами, обычно развиваются артриты и в крови появляются инфицированные моноциты; в группе коз, зараженных собственными моноцитами, только у одной из трех отмечали обострение инфекции. Таким образом, реакция хозяина на инфицированные вирусом клетки является основным фактором, определяющим экспрессию вируса АЭК. Вирус АЭК размножается in vitro в культурах клеток козьего происхождения, а также, как и изоляты вируса висны-маеди, в культурах клеток овец. Предполагают, что козлята заражаются внутриутробно или немедленно после рождения. Вирус АЭК обнаружен в молоке и молозиве инфицированных коз. Совместное содержание ягнят со взрослыми козами, инфицированными вирусом АЭК, не вело к развитию болезни у ягнят в течение 15 месяцев наблюдения. Однако вирус АЭК передается с молоком не только козлятам, но и ягнятам.
Профилактика и меры борьбы. Средства специфической профилактики АЭК не разработаны. Поэтому меры борьбы сводятся к проведению ветеринарно-санитарных мероприятий, выявлению и выбраковке больных и серопозитивнях животных. Рекомендуется изолированное содержание потомства инфицированных коз и вскармливание козлят молоком КРС или молоком коз из благополучных хозяйств. Совместное содержание коз и овец может неблагоприятно влиять на попытки искоренения двух болезней, вызываемыхретровирусами, т. е. артрита-энцефалита коз и висны-маэди овец. Козы, вакцинированные провирусной ДНК или вирионами, дефектными по гену tat (tat-), становились иммунными к патогенному вирусу дикого типа.
Артрит-энцефалит коз (англ. - Caprine arthritis/encephalitis, или CAE) является вирусным заболеванием, распространенным во многих странах мира. Многочисленные опыты подтверждают, что именно международная торговля является основным фактором распространения инфекции между различными регионами. Кроме того, CAE - это медленная инфекция, для которой характерно отсутствие сезонности и периодичности эпизоотии, географической принадлежности. Учитывая эпизоотологические особенности CAE, можно предположить вероятность большей распространенности этой болезни в зарубежных странах, чем это показывают данные МЭБ.
Чаще всего вирус встречается в районах интенсивного козоводства - Европе, Австралии, США. Только у 1-2% инфицированных животных болезнь влияет на ЦНС, в то же время у 30-40% коз определяют поражение суставов. Наибольшей группой риска являются козлята в возрасте 1-5 месяцев. Для нашей страны болезнь является экзотической и неизученной. По клиническим признакам вирус CAE похож на синдром Висна-Мэди у овец. В ранних сообщениях он был описан как Висна-Мэди: по аналогии с аденоматозом овец, артрит-энцефалит коз проявляется атаксией, гиперестезия, иногда лихорадкой, прогрессивными парезами конечностей, в свою очередь перерастают в паралич. Процесс чаще начинается с задних конечностей и распространяется на передние.
Передача вируса в стаде легко происходит путем выпаивания инфицированного молока козлятам - это основной способ распространения инфекции. Даже однократное введение CAEV-загрязненного молока или молозива козленку хватает для возникновения инфекции. У взрослых коз инфекция распространяется путем вдыхания респираторных секретов. Этот путь заражения требует длительного прямого контакта между животными. Аналогично было показано наличие CAEV в сперме инфицированных козлов, но половой путь инфицирования не подтверждался. Широкому распространению инфекции также способствует симптомокомплекс поражения ЦНС, суставов, легких. Картина крови обычно без изменений, иногда может наблюдаться лимфопения. В цереброспинальной жидкости отмечается плеоцитоз, в основном через мононуклеарные клетки и увеличение количества белка. Течение болезни - несколько недель, результат - летальный.

Фото 1. Клинические признаки САЭ у козы (увеличение путового сустава)
Клинические признаки проявляются у примерно 20% коз, инфицированных CAE вирусом (фото 1). Самым распространенным проявлением является артрит, который прежде всего наблюдается у взрослых коз, но может проявиться и у молодняка. У пораженных вирусом коз шерсть может поредеть, на более поздних стадиях заболевания наблюдается потеря веса и хроническое истощение.

Фото 2. Козленок в возрасте 2 месяца инфицированный вирусом (клинические признаки болезни не проявляются)
Патологоанатомические признаки
Патологоанатомические изменения локализуются в центральной нервной системе, суставах и легких. Наиболее выраженные поражения чаще выявляются в шейных и грудных участках спинного мозга. В суставах выявляется гиперплазия синовиальных клеток. В случае прогрессирования болезни нарастают дегенеративные изменения, такие как фиброз, некроз и минерализация синовиальных оболочек. В легких - интерстициальная пневмония, гиперплазия лимфоидной ткани.
Диагностика
Диагноз устанавливают на основании клинико-эпизоотологических данных и результатов патолого-гистологических, вирусологических (культивирование возбудителя на культурах тканей и типизация в РДП, ИФА) и серологических (РИД, ИФА, РН) исследований. На дифференциальной диагностике следует исключить инфекционные болезни: Висна-Мэди, скрепи, листериоз, полиоенцефаломаляцию, токсоплазмоз, болезнь Борна; другие заболевания мышечной и скелетной систем (недостаток витамина Е и меди, септические артриты и травмы).
Профилактика
После заражения у инфицированных животных образуются сывороточные антитела, которые не создают защиты. Средства специфической профилактики не разработаны. Меры борьбы сводятся к проведению в неблагополучном хозяйстве ветеринарно-санитарных мероприятий, выявления и выбраковка больных и серопозитивных животных. Несколько недавних исследований в Польше показали, что распространенность CAE среди поголовья коз колеблется от 4,2 до 80%, но в большинстве стад было около 30-40%. В одном из товарных польских хозяйств вообще все взрослые животные были больными.
Для сравнения - в Норвегии распространенность внутри стад колеблется от 11,5 до 97,3%. Исследование, проведенное в стадах молочных коз в Калифорнии, показало, что носителями вируса являются от 38,3 до 80,1%. Очевидно, распространенность внутри стада увеличивается пропорционально сроку, прошедшее с момента инфицирования. Поскольку вирус передается преимущественно через инфицированное молоко, эффективными мерами оздоровления стада является отлучение козлят сразу после рождения и выращивания их в строгой изоляции, скармливая молозиво здоровых коз или пастеризованное молоко, скармливание молозива только после прогрева в течение 60 мин при температуре +56 ° С. Проводят серологический контроль выращенных таким образом коз на наличие антител к вирусу САЭ в РДП или ИФА с 6-месячным интервалом. Хозяйство считается оздоровленным, если в нем не обнаружено ни одного положительного на вирус животного.
Артрит-энцефалит коз (англ. — Caprine arthritis/encephalitis; лейкоэн-цефаломиелит-артрит коз, АЭК) — медленно прогрессирующая болезнь коз, характеризующаяся развитием демиелинизирующего энцефалита, прогрессирующего артирита, интерстициальной пневмонии и гибелью животных.
Историческая справка, распространение, степень опасности и ущерб.АЭК как лейкоэнце-фалит впервые был описан в 1974 г., в ранних сообщениях болезнь была представлена как мэди, или прогрессирующая пневмония коз, по аналогии с болезнью овец, но в последующие годы возбудитель был охарактеризован подробнее. АЭК обнаружен во многих странах, в частности европейских. На территории России болезнь официально не зарегистрирована. Предполагается, что широта распространения и степень инфицирования высокие.
Возбудитель болезни. Возбудитель АЭК — ДНК-РНК-содержащий медленный вирус (Lentivirus) семейства Retroviridae, диаметром Ю0. 120нм, со свойствами, характерными для ретровирусов, в частности вируса вис-ны-мэди овец (содержит РНК-зависимую ДНК-полимеразу). Структурные белки вируса АЭК также очень похожи на белки вируса висна-мэди овец. Однако установлено, что вирусы АЭК и висна-мэди различаются по критерию гомологичности нуклеотидных последовательностей генома и являются двумя различными представителями семейства ретровирусов.
Возбудитель выращивают в некоторых культурах тканей (в частности, синовиальной ткани) коз и овец. Размножение вируса происходит параллельно с образованием синцитиев, но литического ЦПД не наблюдают. Патогенный спектр ограничивается козами.
Эпизоотология. Сведения об эпизоотологии АЭК неполные. Серологические исследования свидетельствуют о широком распространении инфекции. Болезнь поражает козлят в возрасте 1. 5 мес. Эпизоотологичес-
360кие наблюдения позволяют предположить, что козлята заражаются внутриутробно или сразу же после рождения. Клинически болезнь проявляется только у 20 % всех инфицированных животных, у остальных протекает преимущественно бессимптомно. Естественная передача вируса АЭК происходит с молоком инфицированных матерей. Вероятно, возбудитель может переноситься с другими секретами или трансплацентарно.
Вирус АЭК обнаружен в молоке и молозиве инфицированных коз. В экспериментальных условиях вирусом могут быть инфицированы ягнята, у которых он вызывает артриты и продукцию вирусспецифических антител.
Патогенез.После интрацеребрального, интраартикулярного или интраперитонеального заражения развиваются разного рода изменения. Через 1 нед появляются первые воспалительные повреждения в головном мозге, суставах и легких, которые сохраняются в течение 8. 21 мес независимо от возраста животных. В лейкоцитах периферической крови жизнеспособный вирус обнаруживается начиная со 2-й недели после заражения в течение всей жизни животного.
Течение и клиническое проявление.Заболевание наблюдается у козлят в возрасте 1. 5мес. В целом заболевание характеризуется неврологическими изменениями с лейкоэнцефалитом, интерстициальной пневмонией и артритом.
Клинические симптомы развиваются очень медленно. Заболевание проявляется атаксией, гиперестезией, иногда лихорадкой, прогрессирующими парезами конечностей, перерастающими в параличи. Процесс чаще начинается с задних конечностей и распространяется на передние. Кроме того, отмечают хромоту вследствие развития артрита и одышку. У заболевших животных свалявшаяся шерсть, они отстают в росте. Аппетит не нарушен. Иногда наступает атрофия мускулатуры на парализованной конечности. Присоединяются явления пневмонии. Животные больше не могут стоять и погибают в положении лежа.
У взрослых коз чаще развивается артрит, особенно на карпальных суставах, в то время как у 2. 4-месячных козлят болезнь проявляется прежде всего лейкоэнцефаломиелитами. Течение АЭК — несколько недель, исход летальный.
Картина крови, как правило, без изменений, иногда может наблюдаться лимфопения. В цереброспинальной жидкости отмечают плеоци-тоз, в основном за счет мононуклеарных клеток, и увеличение содержания белка.
Патологоанатомические признаки.Патологоанатомические изменения локализуются в центральной нервной системе, суставах и легких.
Гистологически доминирует демиелинезирующий энцефалит с очаговыми скоплениями лимфоцитов и макрофагов в малом мозге. Вместе с тем наблюдаются очаговые некрозы. Изменения выражены в белом веществе головного и спинного мозга и мозжечка. Наиболее выраженные поражения чаще обнаруживают в шейных и грудных отделах спинного мозга. Микроскопически они характеризуются образованием плотных пери-васкулярных муфт из мононуклеарных клеток, формированием лимфоци-тарных инфильтратов, пролиферацией глии и выраженной первичной демиелинизацией. В тяжелых случаях участки нервных клеток замещаются глиальными рубцами.
Поражения суставов характеризуются артритами с синовиальной гиперплазией. При прогрессировании болезни нарастают дегенеративные
361изменения, такие, как фиброз, некроз и минерализация синовиальных оболочек, появляются периартикулярные коллагенозные структуры.
В легких отмечают диффузную интерстициальную пневмонию, как при мэди.
Диагностика и дифференциальная диагностика.Диагноз устанавливают на основании клинико-эпизоотологических данных и результатов патоло-гогистологических, вирусологических (культивирование возбудителя на культурах тканей и типизация в РДП, ИФА) и серологических (РИД, ИФА, РН) исследований.
При дифференциальной диагностике необходимо исключить инфекционные болезни: висна-мэди, скрепи, листериоз, по-лиоэнцефаломаляцию, токсоплазмоз, болезнь Борна; другие заболевания мышечной и скелетной систем (недостаток витамина Е, септические артриты и травмы, недостаток меди).
Иммунитет, специфическая профилактика.После заражения у инфицированных животных образуются сывороточные антитела, которые, однако, защиты не создают. Средства специфической профилактики АЭК не разработаны.
Профилактика.Проводят комплекс профилактических, ветеринарно-санитарных мероприятий, таких же, как при других медленных инфекциях овец и коз.
Лечение.Неэффективно.
Меры борьбы.Меры борьбы сводятся к проведению в неблагополучном хозяйстве ветеринарно-санитарных мероприятий, выявлению и выбраковке больных и серопозитивных животных.
Применяют метод изолированного выращивания козлят путем разделения матерей и козлят сразу же после окота; скармливание молозива только после прогревания в течение 60 мин при 56 °С или скармливание молока свободных от вируса коз или пастеризованного молока коз или коров.
Проводят серологический контроль выращенных таким образом коз на наличие антител к вирусу АЭК в РДП или РИД с 6-месячным интервалом и удаление всех серопозитивных животных.
При получении двух отрицательных результатов с 6-месячным интервалом животные считаются свободными от АЭК-вируса. Хозяйство считается оздоровленным, если в нем не выявлено ни одного положительно реагирующего животного.
Контрольные вопросы и задания.1. Охарактеризуйте основные клинические признаки симтомокомплекса мэди и аденоматоза у овец. 2. В чем заключаются основные паталого-анатомические различия при мэди и аденоматозе овец? 3. Какой основной метод лабораторной диагностики висна-мэди? 4. Чем заканчиваются заболевания овец медленными вирусными инфекциями?
ЧУМА СВИНЕЙ
Чума свиней (лат. — Pestis suum; англ. — Swine fever, Hog cholera; классическая чума свиней) — высококонтагиозная болезнь, характеризующаяся при остром течении лихорадкой, септицемией и геморрагическим диатезом, а при подостром или хроническом течении — крупозной пневмонией и крупозно-дифтеритическим воспалением слизистой оболочки толстого отдела кишечника (см. цв. вклейку).
Историческая справка, распространение, степень опасности и ущерб.Болезнь впервые описана в Северной Америке в 1833 г. В 60-х годах XIX в. она распространилась в большин-
362стве стран Европы, и до 50-х годов XX в. ее регистрировали во многих странах мира. В Россию вирус чумы занесен в 1893 г. из Западной Европы. Вирусную природу болезни установили в 1903 г. американские исследователи Швейниц и Дорсет. В 1908 г. впервые была предложена противочумная гипериммунная сыворотка, с 1936—1939 гг. началось производство вакцин (США, СССР и другие страны).
В настоящее время болезнь встречается более чем в 60 странах на всех континентах (за исключением США, Канады, Австралии, Скандинавских стран). Более других от этой инфекции страдают страны Европы, Азии, Южной и Центральной Америки, где хорошо развито свиноводство. В России в конце XX в. в результате проведения систематических про-тивоэпизоотических мероприятий с применением вакцин ареал распространения заболевания сократился, болезнь отмечается в виде энзоотических вспышек, число неблагополучных пунктов снизилось до единичных. За последние годы чума свиней интенсивно изучалась, предложены вакцины, разработаны средства и методы диагностики, однако предпринимаемые попытки полностью ликвидировать болезнь успеха пока не имеют.
За рубежом считается аксиомой, что страны, в которых продолжается вакцинация свиней против классической чумы свиней, да еще и живыми вакцинами, нельзя считать полностью свободными от возбудителя этой болезни.
Классическая чума свиней (КЧС) относится к списку А особо опасных инфекций и наносит большой экономический ущерб свиноводству как в развивающихся, так и в развитых странах с хорошо организованным ветеринарно-санитарным надзором.
Возбудитель болезни.Возбудитель чумы свиней — довольно мелкий (40. 60нм) РНК-содержащий вирус из рода Pestivirus , семейства Flaviviridae. По степени вирулентности различают А-, В- и С-варианты вируса. В вариант А входят вирулентные эпизоотические штаммы, вызывающие у свиней всех возрастов остро протекающую болезнь. Вирусы варианта В вирулентны только для поросят и вызывают атипичную или хроническую чуму. К варианту С относится американский слабовирулентный штамм. По антигенной структуре вирус однороден и не имеет ни серологических, ни иммунологических вариантов, но обладает антигенным родством с вирусом диареи крупного рогатого скота. В организме инфицированных или вакцинированных живыми вирус-вакцинами свиней вырабатываются специфические антитела.
Вирус патогенен только для домашних свиней и диких кабанов. Животные других видов, в том числе лабораторные, а также человек нечувствительны к заражению. В организме свиней вирус пантропен — накапливается во всех органах и тканях, но преимущественно в лимфатических узлах, костном мозге, селезенке, печени, слизистой оболочке кишечника и эндотелии кровеносных сосудов. Вирус размножается в гомологичных (свиньи) и гетерологичных (крупный рогатый скот, овцы, козы) первичных культурах клеток без ЦПД.
По устойчивости к химическим дезинфицирующим средствам вирус чумы относится к устойчивым (вторая группа). В свинарниках не теряет вирулентности до 1 года, в замороженном мясе — более 4 лет, в свежеох-лажденном мясе —45. 71 день, в солонине — более бмес, в копченостях — 3 мес. Прогревание мясных продуктов при 44 °С инактивирует вирус через 4 ч. В навозе и трупах возбудитель погибает через 3. 5 дней, в почве —через 1. 2 нед. Вирус неустойчив к высоким температурам, при кипячении погибает моментально, при 60 "С — за 10 мин, быстро инакти-вируется под действием ультрафиолетового облучения. Для дезинфекции наиболее эффективны растворы: гидроксида натрия 4%-ный, формалина 2%-ный, хлорной извести 3%-ный, хлорида йода 5%-ный, пероксида водорода 4%-ный, йодеза 1%-ный, виркона С 1: 350 и др.
Эпизоотология.Важнейшие эпизоотологические данные о чуме представлены на рисунке 5.5.
В благополучные хозяйства возбудитель заносится чаще с необеззара-женными пищевыми и боенскими отходами, с транспортом и с животны-
363 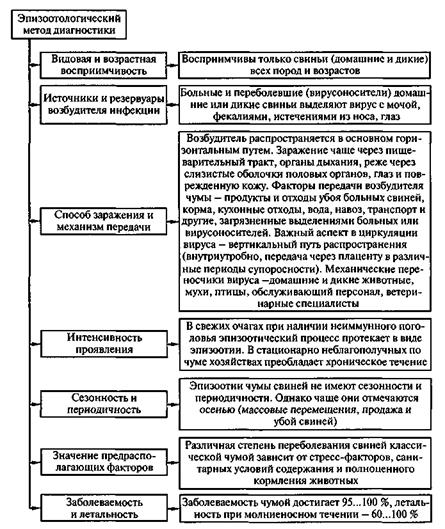
Рис. 5.5. Эпизоотологическая характеристика классической чумы свиней
ми-вирусоносителями. Возможен занос вируса с грубыми и сочными кормами, загрязненными выделениями больных диких свиней, а также комарами.
Природная очаговость болезни связана с территориями обитания инфицированных диких кабанов. Слабовирулентные вирусы варианта В вызывают атипичную форму, отличающуюся по клиническим признакам и сопровождающуюся низкой летальностью.
Патогенез.Вирус, попав в организм свиньи, репродуцируется в лимфоидно-ретикуляр-ной ткани входных ворот (миндалины и носоглотка). Через 16. 24ч он проникает в регионарные лимфатические узлы, репродуцируется и накапливается преимущественно в органах, богатых лимфоидно-ретикулярными клетками (селезенка, лимфатические узлы, костный мозг, печень и эндотелий кровеносных сосудов), вызывая дистрофические и некротические изменения. В результате этого повышается проницаемость стенок сосудов, что приводит к возникновению кровоизлияний, отеков и воспалительных процессов в различ-
364ных тканях и органах, а в селезенке — к инфарктам. Вирусемия сопровождается лихорадкой, нарушением обмена веществ. В результате поражения кроветворных органов развиваются анемия и лейкопения, сильное угнетение опсоно-фагоцитарной реакции и резкое снижение бактерицидности сыворотки крови. Размножаясь в клетках иммунной системы и вызывая их разрушение, вирус заметно снижает иммунные силы организма, что способствует активизации условно-патогенных микроорганизмов, следствием чего становятся пневмония и крупозно-дифтеритический колит. Воспалительные процессы в мозговой ткани обусловливают появление в ней инфильтратов, что клинически проявляется нервными явлениями (депрессия, возбуждение, припадки). При остром течении смерть наступает в результате морфологических поражений всех систем организма, особенно органов кроветворения и кровообращения.
Течение и клиническое проявление.Инкубационный период в зависимости от вирулентности вируса, дозы, метода заражения и резистентности животного длится 3. 9 дней, реже 12. 20 дней.
Болезнь может протекать сверхостро, остро, под остро и хронически.
Сверхострое течение наблюдают в основном в популяции неиммунных свиней и у молодняка. Отмечают повышение температурь: тела (41. 42 °С), угнетенное состояние. У больных отсутствует аппетит, возникают рвота, жажда, учащаются сердцебиение и дыхание, на коже появляются ярко-красные пятна. Животные погибают через 1. 2 дня.
Острое течение чаще регистрируют в начале эпизоотии. Основные признаки: лихорадка постоянного типа до 40,5. 41 °С, угнетение, отказ от корма. Развивается гнойный конъюнктивит, появляются рвота, запор, а затем диарея (фекалии иногда с примесью крови). Мочеиспускание затруднено. Одновременно с этим общее число лейкоцитов снижается с 8,5. 9,0тыс/мкл [(8,5. 9) 10 9 /л] до 2,5. 3,0тыс/мкл [(2,5. 3) 10 9 /л], увеличивается доля эозинофильных и базофильных гранулоцитов, число тромбоцитов уменьшается со 180. 300тыс/мкл (в норме) до ЮОтыс/мкл. Животные передвигаются с трудом, спина сгорблена, отмечаются парезы задних конечностей. Супоросные свиньи абортируют, часто возникает сли-зисто-гнойный ринит, а у отдельных животных — носовое кровотечение. На коже внутренней поверхностей бедер, живота, шеи и основания ушных раковин появляются пустулы, заполненные желтоватым экссудатом, а позже — точечные кровоизлияния, которые в дальнейшем сливаются и образуют темно-багровые пятна, не исчезающие при надавливании. В результате сердечной недостаточности кожа пятачка, ушных раковин, живота и конечностей приобретает синюшную окраску. Перед гибелью температура понижается до 35. 36 °С. Животные погибают в состоянии комы на 7. 10-й день.
Подострое течение длится до 3 нед и проявляется преимущественно поражением органов дыхания (грудная форма) или пищеварения (кишечная форма). Продолжительность болезни увеличивается до 10. 20 дней. У животных наблюдают затрудненное дыхание, кашель, слизисто-гнойное истечение из носа. При поражении желудочно-кишечного тракта запоры сменяются диареей со зловонным запахом и примесью слизи, а иногда крови. Свиньи худеют, ослабевают, передвигаются с трудом, и болезнь заканчивается гибелью, реже переходит в хроническое течение.
Хроническое течение продолжается до 2 мес и более. Клинические признаки могут сильно варьироваться в зависимости от осложнений секун-дарной инфекцией. Наблюдаются периодические диареи, лихорадка непостоянного типа, кашель. Животные имеют изнуренный и истощенный вид, на кожных покровах области живота, шеи и особенно ушных раковин и хвоста появляются экзематозные, иногда кровоточащие струпья грязного цвета, вследствие чего возможны случаи некроза ушей и хвоста.
365Свиньи приобретают вид заморышей, полностью не выздоравливают и остаются вирусоносителями. При подостром и хроническом течении летальность достигает 30. 60 %.
В последнее время под влиянием различных причин болезнь часто протекает атипично (более продолжительный инкубационный период, субклиническое переболевание взрослого свинопоголовья, а у поросят и подсвинков — развитие нервного синдрома без явного геморрагического диатеза).
Атипичная форма обычно проявляется у поросят-сосунов и отъемы-шей, имевших колостральный иммунитет или зараженных слабовирулентным вирусом варианта В. Для нее характерно подострое и хроническое течение продолжительностью 2. 3 нед и более. Болезнь характеризуется анорексией, конъюнктивитом, внутрикожными кровоизлияниями, гипертермией. Одни животные выздоравливают, а у других болезнь осложняется вторичной бактериальной инфекцией, заканчивающейся гибелью либо превращением в заморышей.
Обладая тератогенными свойствами, вирус, попавший в организм свиноматок в период 60. 70 дней супоросности, более чем у 30 % из них вызывает гибель плодов. У свиноматок, инфицированных на 94. 101-й день супоросности, гибели плодов не наблюдается. Аналогичными свойствами обладают и вакцинные вирусы, которые могут проникать в плоды свиноматок 60. 70 дней супоросности, репродуцироваться в них, вследствие чего после рождения поросята становятся толерантными к вирусу, их иммунная система не обеспечивает образование иммунитета после вакцинации. Эти поросята остаются восприимчивыми к полевым вирусам, и в случае его циркуляции возникают новые вспышки чумы.
Общие признаки классической чумы свиней при различных течениях болезни приведены в таблице 5.7.
Читайте также:


