Бактериофаг при ротавирусной инфекции
Предосторожность проста, а раскаяние многосложно.
Тем не менее человека, ни разу не болевшего кишечной инфекцией, просто не существует. Не существует хотя бы потому, что имеется множество способов нейтрализации всех многочисленных защитных сил — глотать, не пережевывая, чтобы слюна не успела до микробов добраться, переедать, нейтрализовать щелочными напитками кислый желудочный сок, убивать собственных микробов антибиотиками и т. д.
Но наиглавнейшей причиной кишечных инфекций было, есть и будет несоблюдение элементарных гигиенических норм — неправильное хранение пищевых продуктов, немытые руки, снующие между обеденным столом и туалетом мухи. В конце концов, какими бы замечательными защитными силами человеческий организм ни обладал, всегда найдется такое количество микробов, нейтрализовать которое просто невозможно.
Возбудителями кишечных инфекций могут быть бактерии (дизентерийная палочка, сальмонелла, стафилококк, палочка брюшного тифа, вибрион холеры) и некоторые вирусы.
Конкретное имя конкретного возбудителя конкретной кишечной инфекции интересует, прежде всего, медицинских работников. Объем, направленность и интенсивность противоэпидемических мероприятий во многом определяется именно видом возбудителя.
Одни бактерии распространяются через воду, другие — через продукты питания, причем продукты эти не какие угодно, а совершенно определенные. В одном случае — овощи, в другом — яйца, в третьем — молочные продукты и т. д.
Одни бактерии очень(!) заразны (например возбудитель холеры), другие — поменьше.
В одном случае заболевание развивается стремительно и представляет собой реальную угрозу человеческой жизни, в другом — симптомы развиваются медленно, а сама болезнь не особенно опасна.
Микробы, возбудители кишечных инфекций, могут (как правило, так оно и происходит) поражать не весь желудочно-кишечный тракт, а определенные его отделы. Воспалительный процесс в каждом таком отделе имеет свое медицинское название: воспаление желудка — ГАСТРИТ, двенадцатиперстной кишки — ДУОДЕНИТ, тонкого кишечника — ЭНТЕРИТ, толстого кишечника — КОЛИТ.
После проникновения в человеческий организм возбудители кишечных инфекций начинают активно размножаться, что приводит, во-первых, к нарушениям процесса пищеварения и, во-вторых, к воспалению клеток слизистой оболочки кишечника. Типичным и наиболее характерным следствием двух указанных процессов является основной симптом любой кишечной инфекции — понос[1]. Другие признаки болезни — тошнота, рвота, боли в животе, повышение температуры тела, отсутствие аппетита, общая слабость — встречаются часто, но обязательными спутниками кишечной инфекции не являются.
Кстати, следует отметить, что на бытовом и на медицинском уровне понятия кишечной инфекции весьма разнятся. Для обычного человека ясно: раз есть понос, значит, и кишечная инфекция есть, а для врача главное не симптомы, а путь заражения. С медицинских позиций, любая болезнь, передающаяся через рот (с пищей, водой, немытыми руками — так называемый фекально-оральный путь инфицирования), является типичной кишечной инфекцией. Наиболее показательный пример — вирусный гепатит А (болезнь Боткина). Заражение вирусом всегда происходит при его попадании в желудочно-кишечный тракт, но поражается печень, а никакого поноса в большинстве случаев нет.
Пути профилактики кишечных инфекций достаточно очевидны и сводятся к соблюдению элементарных гигиенических норм: мытью рук, особенно тщательно после посещения туалета, термической обработке пищи и воды, выполнению правил хранения пищевых продуктов, изоляции больных и, как минимум, обязательному выделению им отдельной посуды.
Всегда следует помнить, что наиболее страшным и опасным последствием любого поноса является потеря организмом жидкости и солей. Без пищи человеческий организм более или менее благополучно может просуществовать пару недель, но без адекватного обеспечения водой и солями калия, натрия, кальция человек жить не может: в этом случае счет идет на часы.
Запасы воды и солей особенно невелики в организме ребенка, и именно для детей кишечные инфекции представляют собой реальную угрозу здоровью и жизни.
Таким образом, истинная тяжесть кишечной инфекции зачастую определяется не частотой стула, не запахом и цветом испражнений, а именно степенью обезвоживания. Определить тяжесть кишечной инфекции может только врач, но вероятность того, что по поводу каждого поноса люди будут обращаться за медицинской помощью, очень невелика. Поэтому подчеркнем, что вне зависимости от того, как называется конкретная кишечная инфекция, существуют совершенно определенные правила поведения больного и его родственников.
- Всегда следует задуматься над тем, что это вы такое съели или чем накормили ребенка. Полбеды, если это ваш личный кулинарный шедевр, но если это пирожное из близлежащего магазина, то следует проявить сознательность и подумать о тех, кто может пойти по вашим следам. Узнать телефон районной санитарной станции совсем не трудно.
- Кишечная инфекция у любого члена семьи — сигнал тревоги для всех остальных. Больному — отдельная посуда, всем остальным — организовать идеальную чистоту, тщательно мыть руки, убрать от греха подальше подозрительные продукты, всю посуду перекипятить, не жалеть дезинфицирующих средств.
- И понос, и рвота являются способами защиты организма. В упрощенном варианте это выглядит так: в желудочно-кишечный тракт попало что-то не то, и организм всеми возможными способами пытается эту гадость удалить. Поэтому в первые часы кишечной инфекции мы вовсе не заинтересованы в том, чтобы понос и рвота прекратились. Наоборот, в обоих направлениях организму следует помогать — пить и рвать (а если не хочется — сознательно вызывать рвоту, промывая тем самым желудок), очистить толстый кишечник с помощью клизмы. Для клизмы используется обычная кипяченая вода, ни в коем случае не теплая (оптимальная температура около 20 °С), обязательно следить за тем, чтобы вышла вся введенная жидкость.
- Главный принцип помощи — восполнение потерь жидкости и солей. Для этой цели идеально подходят лекарственные средства, имеющиеся в любой аптеке и представляющие собой заранее приготовленную смесь различных солей, которую перед употреблением разводят кипяченой водой. Если же аптека далеко, вполне подойдут минеральные воды, отвары изюма, трав, шиповника, компот из сухофруктов, можно чай, лучше зеленый, чем черный. В конце концов, лучше пить то, что есть под рукой, чем не пить ничего.
- Температура напитков ориентировочно должна быть равна температуре тела — при этом всасывание жидкости из желудка в кровь будет максимально быстрым.
- При упорно повторяющейся рвоте помните, чтонадо пить чаще, но малыми порциями, чтобы не растягивался желудок, а использование любых противорвотных препаратов всегда согласовывать с врачом.
- По большому счету, существует лишь два абсолютно безопасных способа самостоятельного лечения кишечных инфекций — голод и обильное питье. Любые лекарственные препараты могут привести к самым неожиданным последствиям, ну разве что кишечные сорбенты[2] целесообразны и показаны практически всегда.
- Интенсивность ваших волнений должна быть теснейшим образом связана с общим состоянием ребенка, а не с тем, сколько раз он запачкал пеленки (попросился на горшок, сбегал в туалет). Следите за цветом мочи: если она светлая — дефицита жидкости нет.
- Обращение к врачу обязательно при поносе у детей первого года жизни и, вне зависимости от возраста, при отсутствии тенденции к улучшению в течение суток.
10. Немедленно обращайтесь за медицинской помощью, если:
- наиболее волнующим симптомом кишечной инфекции является боль в животе;
- из-за упорной рвоты вы не можете ребенка напоить;
- более 6 часов нет мочи;
- сухой язык,запавшие глаза, кожа приобрела сероватый оттенок;
- в кале имеется примесь крови;
- понос прекратился, но при этом усилилась рвота, и (или) резко поднялась температура тела, и (или) появились боли в животе.
11. При улучшении состояния не торопитесь скармливать детенышу все подряд. Чай с нежирным творожком, рисовая и овсяная кашки — пусть потерпит-поголодает сутки-двое, здоровее будет.
Следует отметить: современная терапия кишечных инфекций вовсе не предусматривает глотание всеми любимых фталазола и левомицетина хотя бы потому, что причиной каждого второго поноса являются вирусы[3], на которых упомянутые антибактериальные препараты не действуют вообще. Но даже если это бактерия, отношение к использованию антибактериальных препаратов неоднозначно. Так, при дизентерии антибиотики используются практически всегда, а при сальмонеллезе — значительно реже.
Парадоксальность лечения кишечных инфекций состоит прежде всего в том, что строгая диета, восполнение потерь жидкости и солей да плюс время и терпение — это почти всегда достаточные условия для выздоровления (соблюдение при этом правил гигиены подразумевается).
Тем не менее с грустью приходится признавать, что, несмотря на теоретическую логичность и привлекательность, практическое применение и эубиотиков, и бактериофагов вовсе не приводит к выздоровлению быстрее, нежели все те же диета да питье.
Неудивительно, что в подавляющем большинстве стран мира эти лекарственные средства не применяются (и не выпускаются, и не регистрируются), поскольку доказать их эффективность медицинская наука пока еще не в состоянии[4].
В стационаре основным способом оказания неотложной помощи при кишечных инфекциях является инфузионная терапия, т. е. внутривенное введение жидкости и солей для быстрого возмещения потерь.
При самой опасной кишечной инфекции — холере — инфузионная терапия вообще является наиглавнейшей. Возбудитель холеры вырабатывает экзотоксин (он называется холероген), который находится в просвете кишечника, и его в этой связи не удается нейтрализовать сывороткой. Под действием холерогена клетки слизистой оболочки кишечника как бы сморщиваются и теряют жидкость литрами! Вот и приходится в огромных количествах вводить препараты внутривенно и проводить очень активное лечение до тех пор, пока в организме не появятся антитела к токсину.
[2] Кишечные сорбенты — многочисленная группа лекарственных препаратов, способных связывать (сорбировать) и обезвреживать яды (токсины), находящиеся в просвете кишечника. Самым известным кишечным сорбентом является знаменитый активированный уголь, хотя есть и другие препараты, в десятки и сотни раз более активные.
[3] Самым известным вирусом, вызывающим у детей тяжелейшие кишечные инфекции, является так называемый ротавирус, чаще всего поражающий малышей первых двух лет жизни. Неудивительно в этой связи, что вакцинация от ротавирусной инфекции присутствует в календаре прививок многих стран мира.
Классификация кишечной инфекции у детей
По клинико-этиологическому принципу среди кишечных инфекций, наиболее часто регистрируемых в детской популяции, выделяют шигеллез (дизентерию), сальмонеллез, коли-инфекцию (эшерихиозы), иерсиниоз, кампилобактериоз, криптоспоридиоз, ротавирусную инфекцию, стафилококковую кишечную инфекцию и др.
По тяжести и особенностям симптоматики течение кишечной инфекции у детей может быть типичным (легким, средней тяжести, тяжелым) и атипичным (стертым, гипертоксическим). Выраженность клиники оценивается по степени поражения ЖКТ, обезвоживания и интоксикации.
Характер местных проявлений при кишечной инфекции у детей зависит от поражения того или иного отдела ЖКТ, в связи с чем выделяют гастриты, энтериты, колиты, гастроэнтериты, гастроэнтероколиты, энтероколиты. Кроме локализованных форм, у грудных и ослабленных детей могут развиваться генерализованные формы инфекции с распространением возбудителя за пределы пищеварительного тракта.
В течении кишечной инфекции у детей выделяют острую (до 1,5 месяцев), затяжную (свыше 1,5 месяцев) и хроническую (свыше 5-6 месяцев) фазы.
Симптомы
В большинстве случаев заражение кишечной инфекцией, как правило, выражается рядом универсальных симптомов:
Лечение кишечной инфекции у детей
Комплекс лечения кишечной инфекции у детей включает в себя лечебное питание, этиотропную терапию, патогенетическую и симптоматическую терапию.
При легкой форме сохраняется возрастная диета с ограничениями: уменьшение объема питания - по аппетиту, механическое щажение и другие. При среднетяжелых формах инфекции объем питания уменьшают на 30-50 %, увеличивая при этом кратность кормления до 5-8 раз в сутки. В питании детей старше 4-х месяцев целесообразно включение кисломолочных смесей. При инвазивных энтеритах, гастроэнтеритах, протекающих с выраженным метеоризмом, назначают низколактозные или безлактозные смеси. При острой кишечной инфекции применяют смеси, обогащенные защитными факторами: бифидобактериями, лактобактериями, биологически активными добавками.
Детям старшего возраста в первые дни болезни показана легкоусвояемая, протертая пища. Не рекомендуют употреблять:, цельное молоко, черный хлеб, йогурты, ряженку, сливки, каши на цельном молоке, свеклу, бобовые, цитрусовые, мясные и рыбные бульоны, жирные сорта мяса, рыбы, птицы. При тяжелых формах кишечной инфекции при возникновении дефицита белка у детей раннего возраста его корригируют с 3го дня болезни смесями, обогащенными белком. При нарушении внешнесекреторной функции поджелудочной железы и развития синдрома мальабсорбции показано назначение лечебных смесей.
Этиотропная терапия кишечных инфекций у детей проводится антибиотиками и кишечными антисептиками (полимиксин и др.), энтеросорбентами (смекта). Показан прием специфических бактериофагов и лактоглобулинов (сальмонеллезного, дизентерийного, колипротейного, клебсиеллезного и др.), а также иммуноглобулинов (антиротавирусного и др.). Патогенетическая терапия предполагает назначение ферментов, антигистаминных препаратов; симптоматическое лечение включает прием жаропонижающих, спазмолитиков. В период реконвалесценции необходима коррекция дисбактериоза, прием витаминов и адаптогенов. Этиотропная терапия включает в себя антибиотики, химиопрепараты, специфические бактериофаги, энтеросорбенты, энтеральные иммуноглобулины, лактоглобулины.
Назначаются следующие антибиотики и химиопрепараты: налидиксовая кислота (невиграмон, нергам), фуразолидон, эрцефурил, гентамицин, анамицина сульфат, канамицин.
Специфические бактериофаги показаны как монотерапия при легких и стертых формах кишечной инфекции.
Энтеросорбенты показаны при секреторных диареях (ротавирусная инфекция). Препаратом выбора при легкой и средней тяжести кишечных инфекциях является смекта. Курс лечения энтеросорбентами 5-7 дней.
Патогенетическая терапия включает в себя оральную регидратацию (регидроном, оралитом, гастролитом, цитроглюкосоланом), ферментную терапию (панзинорм форте, абомин-пепсин, панкреатин, панкурмен, дигестал, фестал, мезим форте, креон и другие), антиаллергическую терапию, а также коррекцию дисбактериоза.
Назначаются антидиарейные препараты: имодиум, диарол. При инвазивной и осмотической диареях детям до 2-х лет эти препараты не назначаются. Для купирования болевого синдрома показаны миотропные спазмолитики: дротаверин, папаверин, спазмомен 40 и другие. Витаминотерапия назначается всем детям в период реконвалесценции. Курс лечения 10-14 дней.
При острой кишечной инфекции у детей могут развиваться следующие синдромы: нейротоксикоз, отек мозга, электролитные нарушения, инфекционно-токсический шок, сепсис, гемолитико-уремический синдром, токсико-дистрофические состояние.
Никакая информация, размещенная на этой или любой другой странице нашего сайта, не может служить заменой личного обращения к специалисту. Информация не должна использоваться для самолечения и приведена только для ознакомления.

Ребята, мы вкладываем душу в AdMe.ru. Cпасибо за то,
что открываете эту красоту. Спасибо за вдохновение и мурашки.
Присоединяйтесь к нам в Facebook и ВКонтакте
И кстати, к гриппу ротавирус не имеет ни малейшего отношения.


Основные симптомы ротавируса — это:
- тошнота и рвота
- диарея
- высокая температура
- боль и урчание в животе
Главная опасность заключается в том, что каждый этот симптом по отдельности вызывает обезвоживание. Можно представить, какой удар по организму дает их совокупность.
В отдельных случаях могут появиться кашель и насморк, поэтому так трудно определить, что именно происходит с ребенком. Иногда из-за быстро наступающего обезвоживания у малыша могут наступить судороги и потеря сознания.

Отравился ли ребенок или подхватил вирус, можно понять довольно быстро, однако большой разницы в лечении нет. При отравлении также важно дать малышу сорбенты и следить за тем, чтобы он получал много жидкости.
- есть рвота, но она умеренная
- температуры нет, либо она быстро проходит
- диареи нет, либо она быстро проходит
- боль в животе кратковременная

Так как главная опасность вируса — это обезвоживание организма и потеря жизненно важных минеральных солей, то и лечение должно быть направлено на решение этой проблемы. Конкретного лекарства от ротавирусной инфекции не существует, все лечение симптоматическое.
- обеспечить поступление жидкости. Специальные солевые растворы (электролиты) быстро восстановят баланс в организме, но, конечно, не стоит пренебрегать и обычной водой. При сильной рвоте нужно давать жидкость маленькими порциями постоянно. Сложнее всего в этом случае приходится с младенцами. Если ребенок отказывается от груди и бутылочки, попробуйте понемногу поить малыша из шприца
- контролировать температуру. Если жидкости будет достаточно, организм быстрее справится с вирусом, но при очень высокой температуре стоит применить жаропонижающее средство
- использовать сорбенты (активированный уголь, смекту, энтеросгель)
- не использовать антибиотики. Антибиотики не борются против вирусов, а в случае с ротавирусом не просто бесполезны, а и могут стать опасны. Они негативно воздействуют на кишечник, который и без того сильно ослаблен, и провоцируют еще большую диарею. Антибиотики могут быть показаны только в отдельных случаях (диарея более 14 дней, обнаружение гельминтов, подозрение на холеру) и строго назначены врачом.
Если нет возможности использовать аптечные электролиты, можно быстро сделать смесь, которая восполнит водно-солевой баланс:

Заболеть можно в любом возрасте, но наиболее подвержены вирусам дети до 6 лет. В некоторых ситуациях домашним лечением не обойтись. Врачи говорят и о профилактике ротавирусной инфекции — от нее существуют вакцины.
Особенно опасно промедление для детей до 2 лет.
Стоит срочно обратиться за помощью, если у ребенка критическое обезвоживание. Это проявляется: отсутствием пота, трудностями с дыханием, отсутствием мочеиспускания более 3 часов. У грудных детей появляется плач без слез, заметна сухость языка и слизистых. На этом фоне может очень быстро развиться пневмония.
Не стоит бояться больницы или скорой помощи в этом случае — капельницы очень быстро поставят малыша на ноги.

В первые сутки больному не до еды, а жидкости должно быть как можно больше. Можно давать малышу слабые компоты, морсы и чай, помимо воды. А вот молоко и молочные продукты могут быть опасными, и начнется новый виток болезни, ведь при ротавирусной инфекции развивается временная лактозная недостаточность.
Стоит забыть и о панацее наших бабушек — курином бульоне. Он спровоцирует еще большую диарею.
Что же можно есть? Понемногу вводите нейтральные продукты, расширяя рацион, когда диарея пройдет:
- сухарики
- каши на воде
- галетное печенье и сушки
- пюре на воде и овощные супы
- печеные яблоки
Надеемся, вам не пригодятся эти советы и малыши будут здоровы!
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
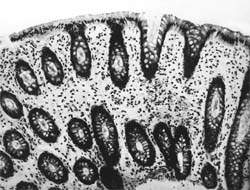 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
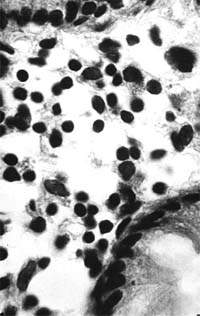 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Читайте также:


