Белковый инфекционный агент прионы
- 13729
- 11,8
- 21
- 4
Путь прионов

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
Биологическая сущность прионов
Рисунок 1. Метафора нейродегенеративного поражения мозга — это губка, в которую превращается нервная ткань в результате массовой гибели нейронов.
И тогда происходит удивительное событие: нормальные молекулы белка, контактируя с патологическими, сами превращаются в них, изменяя свою пространственную структуру (механизм трансформации остаётся загадкой и по сей день) [1]. Таким образом прион, как самый настоящий инфекционный агент, заражает нормальные молекулы, запуская цепную реакцию, разрушительную для клетки.
Некоторые сведения о прионах
Условия возникновения заболеваний
Условия возникновения прионовых болезней уникальны. Они могут формироваться по трём сценариям: как инфекционные, спорадические и наследственные поражения. В последнем варианте главную роль играет генетическая предрасположенность [2].
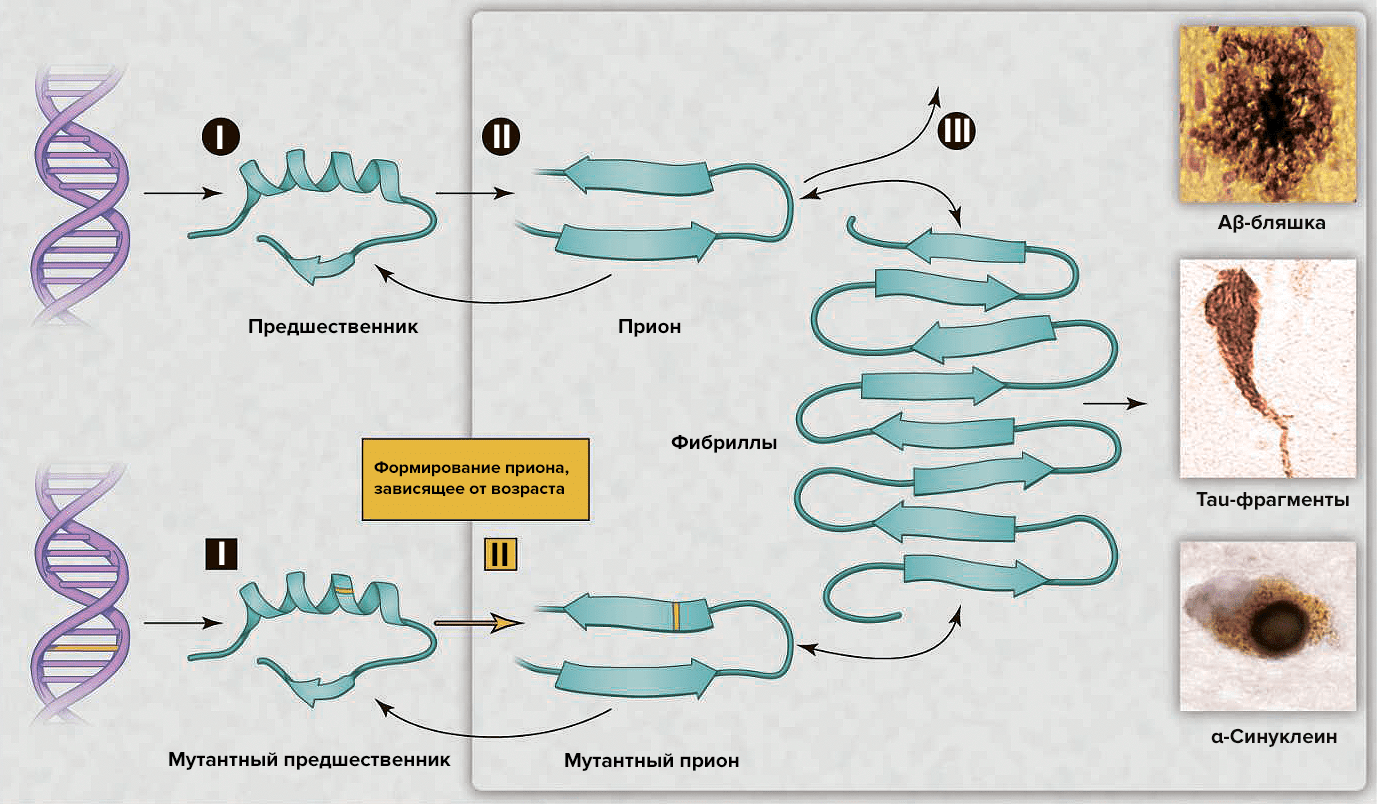
В последнее десятилетие интерес к этой теме возобновился в связи с возможностью развития диагностики и эффективной терапии [5]. Появилось множество различных объяснений для возрастных нейродегенеративных болезней, — например, окислительная модификация ДНК, липидов и/или белков; соматические мутации; измененный врождённый иммунитет; экзогенные токсины; несоответствия ДНК—РНК; нарушение работы шаперонов; отсутствие одного из аллелей гена [5]. Альтернативным комплексным разъяснением служит то, что различные группы белков могут формировать прионы. Несмотря на то, что небольшое количество прионов может быть удалено посредством путей белковой деградации, их чрезмерное накопление с течением времени позволяет прионам самостоятельно распространяться в организме (рис. 2), что приводит к нарушению деятельности центральной нервной системы [5].
Группы риска прионных заболеваний
Вот кого прионные заболевания могут настичь с наибольшей вероятностью:
- работники пищевой промышленности;
- ветеринары;
- патологоанатомы;
- хирурги;
- пациенты трансплантолога;
- каннибалы;
- лица, в семье которых были замечены синдромы Герстманна—Штрейслера—Шейнклера или фатальной инсомнии.
Лабораторная диагностика и лечение
Диагностика базируется на внутримозговом заражении мышат или хомяков, у которых медленно (до 150 дней) развивается соответствующее заболевание, если пациент был болен [2]. Часто проводится гистологическое исследование головного мозга погибших животных [2].
К сожалению, до настоящего времени еще не разработаны эффективные методы лечения прионовых болезней, хотя попытки предотвратить конформационный переход нормального белка в аномальный производятся. Поэтому самым надёжным способом предупреждения развития инфекционных форм является профилактика [2].
Перспективы
По-видимому, интерес к прионам не угаснет до тех пор, пока предположения на их счёт полностью не подтвердятся и не будут найдены эффективные способы лечения прионных заболеваний. В статье [6] говорится о необходимости современного исследования, которое требует тщательного рассмотрения чужеродных прионов в экстраневрональных тканях.
В качестве модельных объектов авторы использовали мышей: две линии, которые трансгенно экспрессировали овечий прионный белок, и одну линию, которая экспрессировала человеческий прионный белок (рис. 3). Задачей было сравнить эффективность межвидовой передачи инфекции посредством тканей мозга и селезёнки. Внутримозговое заражение чужеродным прионным белком выражалось в отсутствии или небольшом количестве инфекционного агента в мозгах этих мышей. Однако инфекционные чужеродные прионы обнаруживались в селезёнке на более ранних этапах заражения в сравнении с моментом, когда были использованы нейротропные прионы, тем самым определяя, что лимфатическая ткань может быть более пермиссивной к распространению чужеродных прионов по сравнению с мозгом.
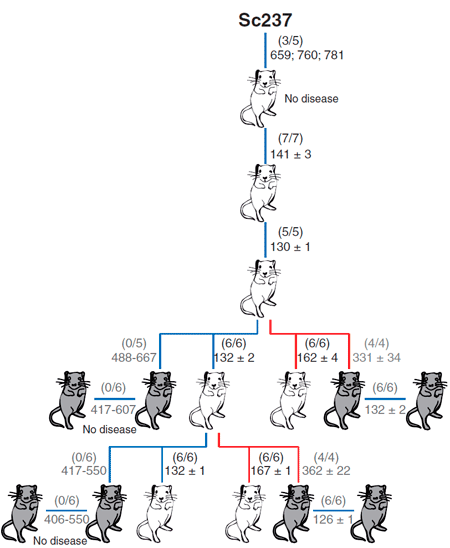
Рисунок 3. Способность приона хомяков Sc237 заражать и передаваться при введении в мозг или селезенку трансгенным мышам, имеющим прионный белок PrP овцы (tg338; белые мыши) или человека (tg7; серые мыши). Число заболевших/инъецированных мышей показано в скобках; ниже приведено среднее время жизни (в днях).
Чем вызвана эта предпочтительная репликация прионов в лимфатических тканях, пока неизвестно. Однако полученные данные показывают, что человек может быть более чувствительным к чужеродным прионам, чем предполагалось ранее на основании присутствия прионов в мозгу, и по этой причине бессимптомный переносчик прионной болезни может быть не распознан. Это ещё раз подтверждает, что такая могущественная биомолекула как прион таит в себе немало загадок, раскрытие которых, возможно, поможет в понимании ряда неразрешимых проблем человечества.
Прион- особая форма инфекционного агента, которая представлена низкомолекулярным белком, имеющим аномальную, по сравнению с белками человека, третичную структуру. Прионы лежат в основе развития медленных инфекций, т.е. инфекций, имеющих длительный период развития и заканчивающихся всегда летально. Главным отличием прионов от других инфекционных агентов является отсутствие у них как такого генетического материала, заключенного в нуклеиновых кислотах (ДНК и РНК). Прионы полностью состоят из белков с низкой молекулярной массой, они не вызывают воспаления и иммунного ответа, а также устойчивы ко многим видам воздействий (высокие температуры, излучение и т.д.). Считается, что прионы могут синтезироваться каждой клеткой организма, но в норме ген, ответственный за воспроизводство прионов репрессирован.
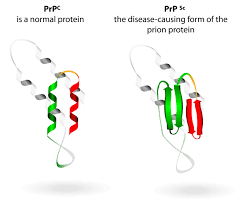
Разница в конформации нормального и патогенного белка
Прионы, соответственно, вызывают прионные заболевания. Прионные заболевания относятся к нейродегенеративным заболеваниям, в процессе развития которых в нервной ткани накапливается аномальной структуры белок. Это происходит вследствие того, что инфекционный прионовый белок PrPsc вызывает мутацию гена, который кодирует нормальный нейрональный прионный белок PrPc, в результате чего клетка начинает синтезировать PrPsc, который отличается от нормального нарушенной третичной структурой. Также PrPsc способен распространяться по типу зомби-вируса из голливудских фильмов, контактируя с нормальным PrPc, он вызывает изменение его конформации и превращение в PrPsc, который способен поражать новые PrPc, в результате чего скорость распространения инфекции по организму растет в геометрической прогрессии. Если клетки инфицируются одиночными инфекционными молекулами, число молекул РrРSс. образующихся в течение суток, достигает 500-1000, в течение года - до полумиллиона. Это неизмеримо меньше по сравнению со скоростью размножения бактерий и вирусов (многие миллионы частиц в течение часов), что объясняет большую длительность инкубационного периода прионовых болезней. Физиологическое значение белка РrРsс прионовых инфекций связывают с реализацией функций синапсов, сохранением клеток Пуркинье, регуляцией внутриклеточного содержания Са2+ в нейронах, поддержанием трофики некоторых их популяций и сохранением резистентности нейронов и астроцитов к повреждающим факторам. Белок PrP — короткоживущий (период полураспада 5-6 ч). В противоположность этому инфекционный прионовый белок PrPSc накапливается в цитоплазменных везикулах, что приводит к последующему нарушению функций синапсов и развитию глубоких неврологических дефектов. Позднее PrP с высвобождается во внеклеточное пространство и откладывается в амилоидных бляшках.
Прионные инфекции имеют три пути возникновения: заражение, по наследству и спонтанное появление. Чаще всего обнаруживается спонтанное появление прионной инфекции. После инфицирования белок попадает в кровь откуда проникает в мозг, где и накапливается, вызывая характерные изменения. Одной из особенностей инфекции является то, что при заражении не происходит каких-либо изменений в периферической крови, в результате чего затруднена диагностика заболевания на ранних этапах его развития. Макроскопически у больного, умершего от прионной инфекции, определяют атрофические процессы в головном мозге. Микроскопически определяется дегенерация и атрофия, а также утрата нервных клеток с заменой их разрастающийся глиальной тканью. Определяются амилоидные бляшки, содержащие прионный белок. Клинически прионные инфекции проявляются по-разному в зависимости от пораженного участка мозга. Приведем в качестве примера некоторые из них.
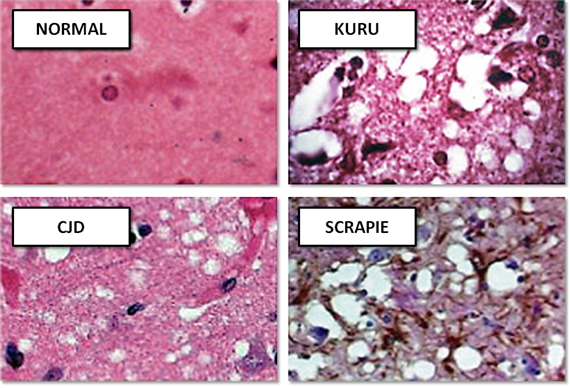
Сравнение гистологических срезов ткани в норме и при различных прионных заболеваниях
Фатальная семейная бессонница. Наследственное заболевание с аутосомно-доминантным типом наследования. При этом заболевании происходит образование амилоидных бляшек в области таламуса. Заболевание развивается медленно и проходит ряд стадий. На первой из них больной жалуется на стойкую бессонницу, при которой не помогают снотворные средства, больной хочет спать, но не может заснуть, позднее возможно присоединение повышенного слюно- и потоотделения, учащение пульса и частоты дыхания, возможно повышение температуры тела. Эта стадия длится около 4х месяцев. Далее к уже имеющийся симптоматике присоединяются панические атаки и галлюцинации. Из-за перенапряжения мозга в связи с отсутствием сна начинаются когнитивные нарушения. Возможно появление непроизвольных движений и подергиваний. Эта стадия длится около 5 месяцев. На следующей стадии сон отсутствует полностью, больной истощен, развивается мышечная слабость, поведение становится неконтролируемым. Это продолжается около 3х месяцев. На заключительной стадии развивается тяжелая деменция, больной перестает ходить, есть. Возможно присоединение вторичной инфекции. Это продолжается около 6 месяцев и неминуемо заканчивается смертью. Заболевание очень редкое, есть данные о наличии этого заболевания у 40 семей итальянского или итало-американского происхождения.

Куру. Ее также называют болезнью каннибалов. Встречается в Новой Гвинеи у аборигенов племени форе. Причинной заболевания является ритуальный каннибализм, во время которого поедается мозг человека, пораженного болезнью. Куру является одной из первых открытых прионных заболеваний. При развитии заболевания постепенно усиливаются головокружение и усталость, затем присоединяются судороги и дрожь. В это время ткани головного мозга постепенно деградируют, превращаясь в губчатую массу (губчатая энцефалопатия). Больные не могут самостоятельно передвигаться, развивается мышечная слабость, на поздних этапах развивается деменция, сходящееся косоглазие и дизартрия. Смерть наступает в течении 2-3 лет. Так как на данный момент ритуальный каннибализм не практикуется, то и болезнь практически исчезла и представляет лишь исторический интерес.

Мальчик больной куру
Болезнь Крейтцфельдта-Якоба- Спорадическое прионное заболевание (т.е. развивающееся без всякой причины), также может возникнуть после употребления зараженного мяса (говядина), возможно заражение при проведении гормональной терапии человеческими гормонами. Ее также называют человеческим вариантом коровьего бешенства, т.к. данный вид прионной болезни вызывает губчатую энцефалопатию у коров. Это заболевание составляет большую часть всех случаев заражений прионными инфекциями (85%). Клинические проявления начинаются с появления раздражительности, рассеянности, головных болей, нарушений сна, изменений поведенческих реакций и т.д. Возможно развитие двигательных нарушений, а в некоторых случаях кратковременной эйфории или депрессии. Позднее развиваются прогрессирующие параличи, эпилептические припадки. Постепенно нарастает деменция, возникают нарушения речи. На поздних стадиях развивается тяжелая деменция, выраженная мышечная атрофия, нарушения глотания, возможно присоединение вторичной инфекции.
К сожалению, в наше время не разработано методов диагностики и лечения прионных инфекций. К счастью, они встречаются очень редко и недостаточно контагиозны, иначе данные инфекции могли бы обернуться настоящей катастрофой с возможным исчезновением всего человеческого рода.
Амилоидозы
Болезни нарушения фолдинга
Некоторые растворимые в воде белки могут при изменениях условий
приобретать конформацию плохо растворимых, способных к агрегации молекул, образующих в клетке фибриллярные отложения, называемые амилоидом. Причинами таких изменений могут быть: увеличение концентрации самих белков, влияющих на конформацию других белков, активация протеолиза нормальных белков с образованием нерастворимых белков, мутации генов данных белков.
В результате отложения амилоида в клетке нарушается ее структура и функции, накапливаются её дегенеративные изменения. Развиваются болезни, называемые амилоидозами. На сегодня известно более 15 видов этого заболевания. Одним из них является болезнь Альцгеймера или β– амилоидоз нервной ткани, поражающий людей преклонного возраста и характеризующийся прогрессирующим расстройством памяти и полной деградацией личности. Причина болезни - накопление в ткани мозга β-амилоида - белка, образующего нерастворимые фибриллы, нарушающие структуру и функции нервных клеток. β-амилоид –продукт изменения конформации нормального белка, у которого в результате частичного протеолиза в процессе фолдинга вторичной структуры вместо α-спиралей образуется β-структура. Изменение конформации меняет свойство белка: он агрегирует с образованием нерастворимых фибрилл и становится устой- чивым к действию протеаз.
Прионовые болезни - это группа заболеваний, характеризующаяся поражением различных отделов нервной системы. Причиной возникновения заболеваний является класс белков, обладающих инфекционным свойством (лат. inficio – вношу вредное, заражаю) и выступающих как инфекционный агент (единственный случай, когда инфекционный агент лишен нуклеиновой кислоты). Называются такие белки – прионы (анг. рroteinacous infection particle – белковая инфекционная частица).
Прионовые белкисуществуют в двухизоформах: нормальный клеточный прионовый (РrР c ) и измененный патологический инфекционный (РrР s r ). (РrР – от анг. рrion protein; с – клеточный; sr – от названия прионовой болезни овец скрепи - scrеpie).
Нормальный клеточный прионовый белок (РrР c ) обнаружен в клетках мозга. Его молекулярная масса равна 33-35 кДа. Конформация вторичной структуры содержит в основном α-спирали. Гeн прионового белка РrNP находится в коротком плече хромосомы 20, имеет протяженность в 16 т.п.н. и содержит 2 интрона. Функция прионового белка – регуляция передачи нервных импульсов, суточных ритмов и метаболизма меди в ЦНС; обладает свойством гидрофильности и чувствителен к действию протеаз: протеаза К полностью разрушает нормальный прионовый белок.
Патологический инфекционный белок - прион (РrР s r ) имеет молекулярную массу 27-30 кДа, кодируется тем же геном РrNP и имеет такую же первичную структуру как и нормальный прионовый белок, но другую конформацию: его вторичная структура характеризуется высоким содержанием β- структур, в результате чего он приобретает другие свойства:
1 - устойчив к действию протеаз (расщепляется частично только до молекулярной массы 27-30кДа);
2 - гидрофобен, образует нерастворимые фибриллы, которые агреги- руют в амилоид;
3 - не вызывает воспалений и высокой температуры (следовательно, длительно не диагносцируется);
4- устойчив к высокой температуре и радиации;
5- накапливается в клетках.
Патологические прионы появляются в клетке разными путями:
1 – являются результатом мутации гена РrNP. Известно около 20 мутаций этого гена: точковые мутации кодирующий части, инсерции и др.; в этом случае прионова болезнь носит наследственный характер;
2 – попадают в организм с пищей (мясо зараженных животных и каннибализм), в результате инъекций инфицированного материала (гемонтрансфузия - переливание крови) или трансплантации органов и тка- ней и др.;
3 – возникают в клетке спонтанно в результате ошибки фолдинга (чрезвычайно редко).
При любом пути появления в клетке прионы способствуют превращению нормального прионового белка (РrР c ) в прион (РrР s r ). Достаточно одной молекулы белка РrР s r , чтобы запустить патогенетический механизм прионовых болезней. Молекулы приона (РrР s r ), взаимодействуя с
клеточной формой нормального прионового белка (РrР c ), изменяют его конформацию, превращая его в прион (РrР s r ). Взаимодействие несет характер цепной реакции, приводящей к накоплению молекул инфекционного белка. Процесс происходит до тех пор, пока весь нормальный прионовый белок не изменится.
Таким образом, прионы играют роль антишаперонов, осуществляя фолдинг наоборот у одного определённого вида белка. Это нарушает нормальный фолдинг данного белка и становится причиной болезни.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Инфекционные агенты можно классифицировать на основании сложности их строения: прионы, вирусы, риккетсии, хламидии, микоплазмы, бактерии, грибы, простейшие, гельминты.
Прионы — это живые белковые молекулы, которые внедряясь в клетки организма способны воспроизводить себе подобных (подробнее прионы рассматриваются в лекции “Вирусные инфекции”).
Простейших и гельминтов часто называют паразитами, хотя этот термин имеет более широкое понятие.
Каждая группа инфекционных агентов может также классифицироваться на различные группы. Например, вирусы делятся на ДНК-содержащие и РНК-содержащие. Бактерии делятся на основании формы на кокки, палочки (бациллы), спирохеты и вибрионы, на основании окраски по Граму на грам-положительные и грам-отрицательные; на основании необходимости кислорода для роста на аэробные и анаэробные. Риккетсии и хламидии — это небольшие бактерии, которые являются облигатными внутриклеточными паразитами.
Способность инфекционных агентов проникать в ткани организма называется инвазивностью, способность его вызывать заболевание называется патогенностью. По степени патогенности они делятся на: высокопатогенные (высоковирулентные) ;низкопатогенные (низковирулентные).
Высоковирулентные микроорганизмы вызывают заболевание в нормальном организме, низковирулентные — только в иммуносупрессированном организме (оппортунистические инфекции).
Бактерии синтезируют их собственные ДНК, РНА и белки, но их благоприятное существование зависит от хозяина. Некоторые микроорганизмы процветают, главным образом, на поверхности тела: нормальные люди несут 1012 бактерий на коже, включая Staphylococcus epidermidis и Propionibacterium угрей, которые ответственны за юные прыщи. Обычно, 1014 бактерий постоянно проживают внутри желудочно-кишечного трактата.
От места размножения возбудителя во многом зависит реакция организма на него. По локализации размножения различают: облигатные и факультативные внутриклеточные и внеклеточные микроорганизмы.
Облигатные внутриклеточные организмы могут расти и размножаться только в клетках организма человека и используют метаболический аппарат клетки для своего роста. В основном поражаются паренхиматозные клетки. Для культивирования данных организмов необходимы живые ткани, например, куриные эмбрионы, тканевые культуры или лабораторные животные.
Факультативные внутриклеточные организмы могут расти и размножаться как внутри, так и вне клеток организма. Внутриклеточное размножение обычно происходит в макрофагах. Степень необходимости клеток хозяина для размножения может сильно варьировать; так Mycobacterium leprae практически всегда размножается в клетках, а Actinomyces israelii — довольно редко.
Внеклеточные организмы — как видно из названия, эти организмы развиваются вне клеток. Практически все они растут на искусственных средах, за исключением Treponema pallidum.
Инфекционный процесс очень сложный и его развитие определяют как особенности возбудителя, так и реактивное состояние макроорганизма.
К особенностям возбудителя инфекционного заболевания относится не только его строение, химическая структура, антигенные свойства, но и характер его взаимодействия с макроорганизмом.
Сосуществование микро - и макроорганизма может быть 3 видов:
симбиоз - сосуществование микроба и макроорганизма в интересах каждого (например, кишечная палочка в кишечнике); комменсализм - (от франц. сommensal - сотрапезник), при котором микроб и макроорганизм не оказывают взаимного влияния друг на друга; паразитизм - жизнь микроба за счет макроорганизма, что сопровождается развитием болезни.
Под влиянием различных экзогенных и эндогенных факторов взаимоотношения между микро - и макроорганизмом могут быть нарушены в пользу микроорганизма, который приобретает патогенные свойства. В этих условиях индифферентный комменсал, или безвредный симбионт, становится паразитом и вызывает заболевание. Такие ситуации возникают при лечении многими препаратами, но прежде всего антибиотиками, которые нарушают установившееся равновесие микробной флоры. Инфекционная болезнь может быть и результатом ослабления фагоцитарной и иммунной систем организма, что встречается, например, при лечении иммунодепрессантами и цитостатическими средствами. Бактериофаги, плазмодии являются носителями активных генетических элементов, которые кодируют бактериальные факторы вирулентности (например, фактор адгезии, токсины или ферменты, которые оказывают сопротивление антибиотикам). Они могут инфицировать бактерии и включать себя в их геном, таким образом, преобразовывая ранее безопасную бактерию в вирулентный или чувствительный к антибиотику микроорганизм - в устойчивый. Обмен этими элементами между бактериальными колониями обеспечивает получателей таких генов преимуществом выживания, или способностью вызвать болезнь.
Большинство возбудителей болезней попадает в организм человека из внешней среды через входные ворота, например, через кишечник с пищей, через легкие с вдыхаемым воздухом, при укусах насекомых, через поврежденную кожу или слизистые оболочки и т. д. В таких случаях говорят об экзогенной инфекции.
Первые и наиболее важные барьеры к инфекции - неповрежденная кожа и слизистые оболочки организма. Например, выделяемые железами слезы содержат лизоцимы (peptidoglycans), которые разрушают бактериальные оболочки и защищают, таким образом, глаза от инфекции. Кислотный желудочный сок смертелен для некоторых кишечных патогенных микроорганизмов; например, добровольцы с нормальной кислотностью желудочного сока не были инфицированы вибрионом холеры, принимая не более 1011 микроорганизмов. Напротив, Shigella и Giardia относительно устойчивы к кислоте, и наличие их в количестве меньше чем по 100 каждой разновидности - вызывает заболевание. Вообще, инфекционные болезни кожи у нормальных людей имеют тенденцию возникать лишь в поврежденных участках, то есть, в рваных ранах или ожогах и могут быть вызваны бактериями с относительно низкой вирулентностью. И, наоборот, для развития заразных болезней дыхательного, желудочно-кишечного или мочеполового тракта требуются вирулентные организмов, способные к повреждению или проникновению через нормальные барьеры слизистой оболочке.
Жители городов вдыхают приблизительно 10000 микроорганизмов в день, включая вирусы, бактерии, и грибы. Большинство из этих микроорганизмов выводятся реснитчатым эпителием верхних дыхательных путей. Только частицы 5 микрон или меньше достигают альвеол, где они поглощаются альвеолярными макрофагами или нейтрофилами, привлеченными к поврежденному участку цитокинами. Эта нормальная система защиты весьма эффективна. Но действию реснитчатого эпителия может вредить курение, повышение вязкости секрета (при муковисцедозе), травма при бронхиальном зондировании, попадание аспирационного кислого содержимого желудка и др. Некоторые вирусы (например, вирусы гриппа) обладают гемагглютининами, которые прочно соединяются с карбогидратам наружной мембраны эпителиальных клеток и, таким образом, подавляют действия реснитчатого эпителия. Ряд патогенных для органов дыхания бактерий (например, Haemophilus и Bordetella) вырабатывают токсины, которые парализуют реснички слизистой оболочки. Микобактерии туберкулеза в нормальных альвеолах очень устойчивы к действию неактивизированных макрофагов.
Однако заражение может быть в результате активации эндогенной флоры организма, тогда речь идет об эндогенной инфекции, или аутоинфекции.
Патологические изменения в инфицированных тканях складываются из трех компонентов: повреждения клеток инфекционным агентом; воспалительного ответа организма; иммунного ответа организма.
Инфекционный агент не всегда приводит к развитию заболевания. При латентном течении процесса инфекционный агент, например, вирус, может в течение длительного времени, иногда годами, не вызывать поражения клеток, а затем под влиянием каких-либо стимулирующих факторов может активироваться.
При всех инфекционных болезнях возникает ряд общих и местных изменений.
Местные изменения представляют собой очаг воспаления и зависят от характера инфекции, ворот инфекции, способа заражения. Например, при дифтерии зева возникает фибринозное воспаление в миндалинах, при гриппе - воспалительные изменения наблюдаются в бронхах, дизентерийная палочка ведет к развитию воспаления в толстой кишке. Но иногда, если инфекция проникает в кровь, то местные изменения бывают слабо выраженными и процесс приобретает генерализованный характер.
Из общих изменений наблюдаемых в инфицированном организме необходимо отметить наличие расстройств кровообращения. Любая инфекция сопровождается интоксикацией, нарушением сердечной деятельности. В органах выражено полнокровие, стаз, мелкие периваскулярные кровоизлияния, периваскулярный и перицеллюлярный отек. Особенно характерен тромбоз сосудов микроциркуляторного русла (гиалиновые тромбы). Особенно важны изменения в головном мозге и его оболочках. Жалобы больных на головную боль при инфекционных заболеваниях обусловлены отеком оболочек мозга, иногда кровоизлияниями. Чем тяжелее инфекционное заболевание, тем сильнее выражены расстройства кровообращения.
В миокарде, почках, печени, надпочечниках, головном мозге могут возникать все виды паренхиматозных дистрофий (зернистая, гиалиново-капельная, вакуольная, жировая), а в тяжелых случаях наблюдается некроз клеток. При некоторых длительно протекающих инфекциях может наблюдаться амилоидоз. Выраженные дистрофические изменения при инфекционных болезнях в клетках центральной нервной системы (нейроцитах) могут в клинике сопровождаться возбуждением или сонливостью, вплоть до полной потери сознания. Дистрофические изменения в миокарде клинически проявляются расширением границ сердца, увеличением числа сердечных сокращений (тахикардия) или их сокращением — брадикардия и т.д. Иногда больные погибают от паралича сердца. Печень у инфекционных больных увеличена, край округлен (из-за полнокровия, отека, дистрофических изменений), капсула напряжена, что сопровождается выраженной болезненностью. В клинике нередко наблюдаются признаки печеночной недостаточности, легкая паренхиматозная желтуха. В почках поражается преимущественно эпителий извитых канальцев, что сопровождается олигоурией, протеинемией.
При инфекционном процессе независимо от характера возбудителя появляются иммунные реакции, направленные на разрушение и элиминацию инфекта. Циркулирующие в крови антитела образуются в ответ на антигенную стимуляцию иммунной системы. Соединения антигена с антителом в присутствии комплемента производят антимикробное и антитоксическое действие, обеспечивающее послеинфекционный гуморальный иммунитет. При всех инфекционных заболеваниях наблюдаются изменения в органах иммуногенеза — тимусе, селезенке, лимфатических узлах, костном мозге, миндалинах, лимфоидном аппарате кишечника. Периферические органы иммуногенеза увеличиваются в размерах, в них наблюдается плазматизация, которая является показателем напряженности иммунитета. В то же время длительное антигенное воздействие при инфекционном заболевании ведет к сенсибилизации организма, появлению реакций гиперчувствительности как немедленного, так и замедленного (аллергические реакции) типа. Защитные реакции организма - это обоюдоострый меч: они необходимы для того, чтобы преодолеть инфекцию, но в то же самое время могут непосредственно наносить ущерб ткани. Из этого следует, что тканевые повреждения при инфекционных заболеваниях могут развиваться не только под воздействием инфекта, но в связи с реакциями гиперчувствительности.
Не нашли то, что искали? Воспользуйтесь поиском:
Прионы — одна из самых больших загадок в биологии и медицине. Возможно, когда-то именно эти неживые вещества, ведущие себя подобно микроорганизмам, привели к исчезновению неандертальцев. Сегодня же они являются объектом огромного интереса со стороны врачей и ученых. MedAboutMe рассказывает о нюансах прионных инфекций и медленных смертельных болезнях, которые они вызывают.
XX век — столетие прионов

Хотя сами прионы были открыты сравнительно недавно, свою историю в медицине прионные инфекции ведут с XVIII века. Первые упоминания об овечьей почесухе (скрепи) в Англии датируются 1732 годом. Явление было столь распространено, что его даже обсуждали в Британском парламенте. В 1899 году ученые доказали инфекционную природу заболевания: то есть тот факт, что необычное поведение овец, которые в результате умирали в судорогах, заразно и передается через повреждения на коже и пищу. Среди характерных признаков скрепи были очень длительный инкубационный период и специфические поражения тканей и органов.
В 1986 году в Великобритании разразилась эпидемия трансмиссивной губчатой энцефалопатии рогатого скота. Источником инфекции стала мясо-костная мука, которой выкармливали телят. Изначально при ее производстве сырье (кости, остатки туш животных) обрабатывалось при температуре до 130°С, но в конце 1970-х годов производители изменили технологию и снизили температуру обработки до 110°С. Это и привело к массовому заражению коровьим бешенством. Попутно оказалось, что многие другие виды млекопитающих, которым перепадала мясо-костная мука или части зараженных коров, также болеют губчатой энцефалопатией.
В марте 1996 года англичане сообщили о первых 10 жертвах прионов среди людей. Через месяц стало известно о пострадавших во Франции, а на данный момент число жертв губчатой энцефалопатии среди людей превысило 200 человек только на территории Европы. Число стран, где были зафиксированы случаи коровьего бешенства у животных, к 2006 году достигло 40.
Прионы — форма белковой псевдожизни

Итак, прионы — это группа белков, имеющих определенную трехмерную конфигурацию, которая считается аномальной. При встрече с аналогичным белком нормальной конфигурации прион запускает процесс его превращения в такую же аномальную структуру. Как и легендарный царь Мидас, превращавший в мертвое золото все, к чему он прикасался, прионы трансформируют нормальный белок в себе подобный, способный разносить инфекцию дальше. То есть, стоит подхватить прионную инфекцию, как в организме запускается цепная реакция, медленно, но верно разрушающая ткани мозга (прионы проходят сквозь гематоэнцефалический барьер).
- нормальную — PrPC,
- прионную — PrPSc.
За производство прионной формы белка отвечает тот же ген, но имеющий одну или несколько из почти 40 мутаций, известных на сегодняшний день. Постепенно трансформируя подходящие белки, прионы образуют амилоиды — агрегаты белковой природы, сходные с амилоидными бляшками, формирующимися при болезни Альцгеймера. И это приводит к аналогичным последствиям — разрушению нервных клеток. Поэтому прионные инфекции относят к нейродегенеративным заболеваниям.
Среди ученых до сих пор не утихают споры на тему, являются ли прионы формой жизни. С одной стороны, они размножаются: был один прион, нашел подходящий белок — стало два приона. С другой стороны, у них нет ДНК (или РНК) — переносчика наследственной информации, как у вирусов, бактерий, грибков и других инфекций.
Для кого опасны прионы?

Прионы опасны для всех форм жизни, у которых есть белок PrP. Прионные болезни уже обнаружены, кроме человека, у овец, коз, коров, норок, оленей, лосей, мулов, кошек (и домашних, и диких), антилоп, страусов и даже у дрожжей. К счастью для всего живого на Земле, прионные инфекции в большинстве своем видоспецифичны. Это значит, что PrP белки разных видов незначительно отличаются друг от друга, поэтому в большинстве случаев у человека нет шансов умереть, скажем, от прионов страуса или дрожжевого грибка.
Но из каждого правила есть исключения. Прионы, губительные для коров, вызывают у человека один из вариантов болезни Крейтцфельдта-Якоба. А подхватить коровий прион можно, съев зараженное мясо. Правда, не каждый человек, употребивший бифштекс коровы, которая скончалась от губчатой энцефалопатии рогатого скота, заболеет. Для заражения необходима комбинация факторов, в число которых входит генетическая предрасположенность к таким инфекциям.
Сегодня выделяют следующие разновидности прионных болезней человека:
Упоминавшаяся выше болезнь гвинейских аборигенов, сегодня практически полностью искорененная в силу отказа племен от каннибализма.
Крайне редкое, наследственное заболевание с инкубационным периодом от 5 до 30 лет.
- Фатальная семейная бессонница (FFI).
Тоже очень редкое и передающееся по наследству заболевание, в результате которого человек погибает от необратимых повреждений мозга на фоне бессонницы.
- Болезнь Крейтцфельдта-Якоба (CJD).
Она же — коровье бешенство или трансмиссивная спонгиоформная энцефалопатия и др. Эта болезнь существует в нескольких модификациях. Выделяют спорадическую (sCJD), наследственную (fCJD) и ятрогенную (iCJD) формы. А с 1955 года, после вспышки коровьего бешества в Великобритании — новый вариант nvCJD.
Статистика, собранная в отношении болезни Крейтцфельдта-Якоба, показывает, что только в 1-5% случаев человек может получить прионную инфекцию путем заражения извне, например, при пересадке органов и тканей. В 10-15% случаев заражение является наследственным заболеванием. И, наконец, в 85% случаев причина внезапного развития болезни остается неизвестной. Чаще всего, она поражает людей в возрасте от 40 до 69 лет.
Уничтожить прионы: миссия невыполнима

Ученые давно бьются над проблемой ранней диагностики прионных заболеваний, но пока их поиски не увенчались особым успехом. В биологических жидкостях, то есть в крови и моче, прионы присутствуют в столь малых концентрациях, что определить их довольно сложно. Самый точный метод их выявления — анализ образцов тканей мозга, но его можно провести только посмертно. О ранней и массовой диагностике, таким образом, пока речи не идет.
Лекарств против прионов не существует. Они настолько просты, что близки к совершенству в плане противостояния любых угроз. Это всего лишь хорошо упакованный белок. Его невозможно уничтожить кислотой, УФ-излучением, ферментами, разрушающими другие белки, и даже ионизирующая радиация бессильна против прионных частиц — настолько они малы.
Можно ли защитить здоровье человека?
Меры профилактики: запрет на мясо и лекарства

Раз пока не получается справиться с прионами, остается одно: строгие меры профилактики. Если страна-поставщик мясной продукции объявляет о том, что на ее территории выявлены случаи коровьего бешенства, в подавляющем большинстве случае другие страны отказываются закупать у нее мясо до решения проблемы со вспышкой прионных инфекций.
Особое внимание уделяется использованию различных органов и тканей крупного рогатого скота для производства лекарств, косметических средств и медицинских изделий. Безопасных частей зараженного животного не существует. Это, кстати, привело к тому, что в Великобритании по итогам эпидемии было запрещено производство и использование большого числа лекарств, производимых из тканей и органов коров. И в России под запрет попали некоторые препараты (кортикотропин, лактин и питуитрин для инъекций и др.). Некоторые лекарственные средства (актовегин, солкосерил) запрещены в одних странах (США) и разрешены в других (Россия).
Справится ли человечество с прионами — покажет время. А пока банальный совет: не покупайте мясо, чистота которого не подтверждена санитарными сертификатами. Прионные инфекции встречаются крайне редко, и жить с ними можно очень долго, но исход у них один.
Читайте также:


