Блрс инфекция что это такое
Обоснованные рекомендации по выявлению БЛРС фенотипическими методами распространяются только на штаммы Klebsiella spp. и E.coli. Однако продукция БЛРС может отмечаться практически у всех видов семейства Enterobacteriaceae и ряда других грамотрицательных микроорганизмов. Учитывая распространенность ферментов этой группы, представляется целесообразным проведение скрининга всех выделенных в лаборатории штаммов Enterobacteriaceae с последующим использованием специальных подтверждающих исследований у любых штаммов, которые по данным предварительного тестирования проявляют пониженную чувствительность хотя бы к одному из цефалоспоринов III поколения (МПК >2 мг/л, либо эквивалентное уменьшение диаметра зоны подавления роста – таблица 3).
Скрининг не предполагает проведения специального исследования, его основу должен составлять анализ данных, получаемых в рутинной практике. В то же время для эффективного скрининга в рутинное микробиологическое исследование необходимо включать несколько цефалоспориновых антибиотиков, даже если использование некоторых из них в качестве терапевтических препаратов не планируется. Наиболее чувствительными к гидролизу БЛРС считаются цефподоксим и цефтазидим. Соответственно, эти препараты целесообразно включать в набор для определения чувствительности Enterobacteriaceae. При отсутствии возможности тестирования цефподоксима, минимальный набор цефалоспоринов III поколения, используемых для определения чувствительности грамотрицательных микроорганизмов, должен включать цефотаксим, цефтриаксон и цефтазидим.
Чем больше цефалоспоринов использовано для тестирования, тем более достоверными будут результаты выявления БЛРС. Некоторые штаммы могут проявлять высокий уровень устойчивости ко всем АБП, у других же обнаруживается лишь незначительное повышение МПК к 1–2 АБП цефалоспоринового ряда. Результаты тестирования Klebsiella spp. и E. coli к цефалоспоринам, указывающие на возможную продукцию БЛРС этими штаммами, приведены в таблице 10.
После выявления штамма, подозрительного на продукцию БЛРС, рекомендуется провести подтверждающий тест.
Тесты, подтверждающие продукцию БЛРС.
Все фенотипические тесты для подтверждения продукции БЛРС являются вариантами стандартных методов определения чувствительности к АБП и основаны на ингибиции БЛРС клавуланатом. При постановке этих тестов проводится сравнение чувствительности исследуемых микроорганизмов к различным цефалоспоринам III поколения и к комбинации этих антибиотиков с клавулановой кислотой.
Диско-диффузионный метод предусматривает использование стандартных дисков с обычным содержанием цефотаксима и цефтазидима (30 мкг) или диска с цефподоксимом (10 мкг), а также диски, содержащие комбинации: цефотаксим + клавуланат или цефтазидим + клавуланат (30/10 мкг) или цефподоксим + клавуланат (10/10 мкг). В исследование целесообразно включать одновременно и диски с цефотаксимом и диски с цефтазидимом и их комбинациями с клавуланатом.
Методика приготовления микробной взвеси и инокуляции чашек с агаром стандартные. На поверхность агара накладывают диски
с цефалоспоринами и их комбинациями с клавулановой кислотой. Чашки инкубируют
в термостате при 35 о С в течение 18-20 часов.
Различие в диаметрах зон подавления роста для дисков с цефподоксимом/клавулановой кислотой и цефподоксимом на 6 мм и более, дли дисков с цефотаксимом/клавулановой кислотой и цефотаксимом, цефтазидимом/клавулановой кислотой и цефтазидимом – на 5 мм и более, свидетельствует о продукции штаммом БЛРС. Необходимо подчеркнуть, что результат считается положительным, если указанные различия получены хотя бы для одной пары дисков.
Для контроля качества исследования необходимо использовать 2 штамма (отрицательный и положительный контроли):
- отрицательный контроль. При тестировании контрольного штамма E. coli , не продуцирующего b-лактамаз, различия в диаметрах зон между дисками с ингибитором и без него не должны превышать 2,0 мм.
- положительный контроль. При тестировании контрольного штамма K.pneumoniae, продуцирующего БЛРС, различия в диаметрах зон между дисками с цефподоксимом/клавулановой кислотой и цефподоксимом >6 мм, с цефотаксимом/клавулановой кислотой и цефотаксимом >3 мм,
с цефтазидимом/клавулановой кислотой и цефтазидимом >5 мм.
Метод серийных разведений в бульонепредполагает использование двойных серийных разведений препаратов в следующих диапазонах концентраций: цефтазидима
от 0,25 мг/л до 128,0 мг/л, цефтазидима/клавуланата от 0,25/4,0 мг/л до 128,0/4,0 мг/л; цефотаксима от 0,25 мг/л до 64,0 мг/л; цефотаксима/клавуланата от 0,25/4,0 мг/л до 64,0/4,0 мг/л. В исследование целесообразно включать оба цефалоспорина и их комбинации с клавулановой кислотой.
Методика выполнения исследования (приготовление разведений антибиотиков в бульоне, микробной взвеси, инокуляция и инкубация) – стандартная.
Снижение МПК цефтазидима или цефотаксима не менее чем в 8 раз (на 3 последовательных двукратных разведения) в присутствии ингибитора, в сравнении со значениями МПК соответствующих цефалоспоринов без ингибиторов, свидетельствует о продукции штаммом БЛРС.
- отрицательный контроль. При тестировании контрольного штамма E. coli, не продуцирующего b-лактамаз, соотношения МПК соответствующих цефалоспоринов III поколения к МПК их комбинации с клавуланатом должны быть 8.
Метод двойных дисков.
Хотя этот метод и не относится к хорошо стандартизованным, чувствительность, специфичность и простота выполнения позволяют рассматривать его приемлемым методом для рутинной практики. Метод предполагает использование доступных коммерческих дисков с цефалоспоринами III поколения и с амоксициллином/ клавуланатом.
Метод "двойных дисков" представляет собой вариант классического ДДМ определения чувствительности, который позволяет выявить продукцию БЛРС по наличию расширенной зоны подавления роста вокруг диска с каким-либо цефалоспорином III поколения напротив диска, содержащего клавулановую кислоту (синергизм отмечается в
участке пересечения зон диффузии двух дисков, расположенных на небольшом расстоянии друг от друга).
Методика приготовления микробной взвеси, инокуляции и инкубации чашек не имеет отличий от стандартного ДДМ. Особенностью метода является то, что через 5–10 мин. после инокуляции на поверхность агара накладывают диски с АБП: в центр – диск, содержащий клавулановую кислоту, обычно в виде комбинации амоксициллин/клавуланат (20/10 мкг), по бокам от него на расстоянии 20 и 30 мм между центрами дисков – диски с цефтазидимом (30 мкг) и цефотаксимом (30 мкг). Использование двух дисков каждого АБП, расположенных на разном расстоянии от диска с клавулановой кислотой, позволяет повысить эффективность обнаружения БЛРС.
Рис. 2. Выявление продукции БЛРС с помощью метода "двойных дисков".
Отрицательные результаты: a) E.coli (БЛРС-)б b) E. cloacae (гиперпродукция AmpC).
Положительные результаты: c), d) K. pneumoniae (БЛРС+)
Обозначения дисков: AMC - амоксициллин/клавулановая кислота (20/10 мкг),
CAZ - цефтазидим (30 мкг), CTX - цефотаксим (30 мкг), CPO - цефпиром (30 мкг)
Параллельно с анализом исследуемых культур тестируют контрольные штаммы.
К сожалению ни один из традиционных микробиологических методов, основанных на оценке фенотипа микроорганизма, не обеспечивает выявление БЛРС в 100% случаев. Ситуация существенно затрудняется при наличии у микроорганизмов нескольких детерминант устойчивости одновременно, что встречается достаточно часто. Например, при продукции БЛРС и гиперпродукции хромосомных бета-лактамаз класса С устойчивость последних к клавуланату маскирует присутствие БЛРС.
6.3. Определение чувствительности P.aeruginosa, Pseudomonas spp., Acinetobacter spp. и других неферментирующих бактерий (НФБ).
При определении чувствительности НФБ следует иметь в виду, что ДДМ достаточно стандартизован лишь для P.aeruginosa и Acinetobacter spp. При исследовании Stenotrophomonas maltophilia, Pseudomonas spp. (кроме P.aeruginosa) и других НФБ, предпочтение следует отдавать методам серийных разведений. Примерный перечень АБП, рекомендуемых для определения чувствительности рассматриваемой группы бактерий приведен в таблице 1211.
Препараты первого ряда.
В первую очередь для оценки антибиотикочувствительности Pseudomonas spp. и Acinetobacter spp. следует использовать препараты, отличающиеся наибольшей природной активностью. К ним относятся:
Цефтазидим. Является одним из основных АБП, используемых для лечения инфекций, вызываемых рассматриваемой группой микроорганизмов.
Цефепим. При сопоставимом с цефтазидимом уровне природной активности, в ряде случаев цефепим сохраняет активность в отношении микроорганизмов, устойчивых к цефтазидиму.
Гентамицин, амикацин. Аминогликозиды для монотерапии инфекций, вызываемых рассматриваемой группой бактерий не применяются, однако во многих случаях являются необходимым компонентом комбинированных схем терапии. Целесообразность включения в перечень препаратов первого ряда амикацина и гентамицина обосновывается высокой частотой устойчивости к последнему антибиотику в ряде учреждений.
Ципрофлоксацин. Среди фторхинолонов ципрофлоксацин является препаратом выбора при лечении рассматриваемой группы инфекций.
Меропенем, имипенем. Меропенем характеризуются наибольшим уровнем активности в отношении рассматриваемой группы микроорганизмов, имипенем ему несколько уступает. Целесообразность включения обоих карбапенемов объясняется отсутствием между ними в некоторых случаях перекрестной резистентности.
Дополнительные препараты по уровню природной активности, как правило, уступают антибиотикам первого ряда, однако во многих случаях, прежде всего, по экономическим соображениям могут быть использованы в терапии. Кроме этого необходимо учитывать, что неферментирующие бактерии существенно различаются по уровню природной чувствительности к АБП.
Азтреонам, цефоперазон. По основным свойствам близки к цефтазидиму.
Цефоперазон/сульбактам, тикарциллин/клавуланат, Доступные ингибиторы не способны подавлять активность большинства бета-лактамаз распространенным среди P. aeruginosa и, в силу этого комбинированные препараты, не обладают существенными преимуществами с сравнении с исходными антибиотиками.
Цефоперазон/сульбактам (а также ампициллин/сульбактам) могут иметь реальное значение в лечении инфекций, вызываемых Acinetobacter spp. благодаря наличию у сульбактама собственной активности в отношении указанного микроорганизма.
При инфекциях вызываемых Stenotrophomonas maltophilia клиническое значение имеет ко-тримоксазол и тикарциллин/клавуланат. Микроорганизм обладает природной устойчивостью ко всем бета-лактамам кроме (тикарциллина/клавуланата)
Карбенициллин. В силу выраженной токсичности и высокой частоты устойчивости применение карбенициллина даже для лечения инфекций, вызываемых P. aeruginosa следует признать нецелесообразным.
Поскольку тяжелые инфекции, вызываемые псевдомонадами, являются показанием для назначения комбинированной терапии, целесообразно при выдаче ответа в клинику указывать на наиболее эффективную с микробиологической точки зрения комбинацию антибиотиков.
Пограничные значения МПК антибиотиков (и соответствующие диаметры зон ингибиции роста) в отношении Pseudomonas spp., Acinetobacter spp. и неферментирующих бактерий, используемые для интерпретации результатов оценки антибиотикочувствительности приведены в таблице 4.
6.4. Определение чувствительности Staphylococcus spp.
При оценке чувствительности Staphylococcus spp. в первую очередь необходимо тестировать препараты, имеющие основное клиническое значение: бета-лактамы, макролиды, фторхинолоны, аминогликозиды и ванкомицин.
Критерии интерпретации результатов определения чувствительности Staphylococcus spp. (пограничные значения диаметров зон подавления роста и МПК АБП) приведены в таблице 5.
Бета-лактамы. Препаратами выбора для лечения стафилококковых инфекций (вызванных как Staphylococcus aureus, так и коагулазонегативными стафилококками) являются бета-лактамные антибиотики, следовательно, в первую очередь необходимо определять чувствительность стафилококков к этим препаратам.
Устойчивость стафилококков к бета-лактамным АБП связана либо с продукцией бета-лактамаз, либо с наличием дополнительного пенициллино-связывающего белка - ПСБ2а. Выявление и дифференцировка этих двух механизмов резистентности позволяет надежно прогнозировать активность всех бета-лактамных антибиотиков без непосредственной оценки чувствительности к каждому из этих препаратов. При этом необходимо учитывать следующие закономерности:
- штаммы Staphylococcus spp., лишенные механизмов резистентности, чувствительны ко всем бета-лактамным АБП;
- бета-лактамазы (пенициллиназы) Staphylococcus spp. способны гидролизовать природные и полусинтетические пенициллины, за исключением оксациллина и метициллина. Чувствительность или резистентность к бензилпенициллину является индикатором активности природных и полусинтетических амино-, карбокси- и уреидопенициллинов. Остальные бета-лактамы с потенциальной антистафилококковой активностью (антистафилококковые пенициллины, цефалоспорины I, II и IV поколений и карбапенемы) сохраняют активность в отношении бета-лактамазпродуцирующих штаммов;
- штаммы Staphylococcus spp, обладающие ПСБ2а, клинически устойчивы ко всем бета-лактамным АБП. Маркером наличия ПСБ2а является устойчивость к оксациллину и метициллину. Такие штаммы исторически получили название метициллинорезистентных стафилококков.
Таким образом, определение чувствительности Staphylococcus spp. к бета-лактамным АБП должно включать выполнение двух тестов:
- определения чувствительности к бензилпенициллину или выявления продукции бета-лактамаз (пенициллиназ);
- определения чувствительности к оксациллину или выявления ПСБ2а или кодирующего его гена mecA.
Последнее изменение этой страницы: 2016-08-12; Нарушение авторского права страницы
В настоящее время четко определены основные серьезные проблемы, связанные с антибиотикорезистентностью бактерий, ответственных за развитие НКИ: MRS A, MRS-КНС, VRE, штаммы грамотрицатсльных палочек, продуцирующих БЛРС (Klebsiella pneumoniae и Е. Coli), мультирезистентные и папрезистентные штаммы энтеробактерий, неферментирующих грамотрицательных палочек А. baumannii и P. aeruginosa, появление штаммов стафилококков и энтерококков, резистентных к ванкомицину и линезолиду (Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Healthcare Settings Recommendations of the Healthcare Infection Control Practices).
Ключевая роль лаборатории клинической микробиологии состоит в своевременном и точном выявлении MDR у микроорганизмов, представляющих возбудителей НКИ. Существуют различные доступные в настоящее время методы диагностики резистентности (стенотипический, молекулярный, микробиологические анализаторы MDR, составляет 19 и 33% соответственно. Назначение хиполонов и антипсевдомонадных пенициллинов служит независимым фактором риска резистентности к карбапенемам у зитеробактерий.
По нашим данным, Е. coli, К. pneumoniae и Е. cloacae — это основные виды грамотрицательных палочек из семейства зитеробактерий, которые вызывают послеоперационные РИ у онкологических больных. Все три вида имеют свои особенности, которые необходимо учитывать при назначении антибактериальных препаратов.
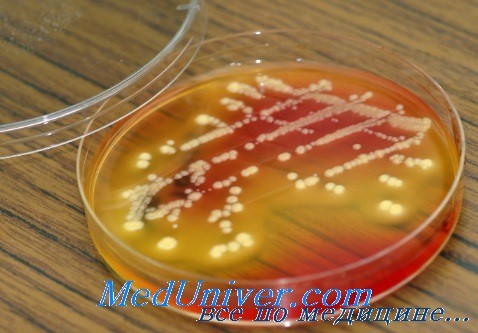
При определении чувствительности грамотрицательных палочек семейства Enterobacteriaceae весьма важен поиск штаммов, способных вырабатывать ферменты, объединенные в группу бета-лактамаз расширенного действия (БЛРС). Инфекции, обусловленные микроорганизмами, продуцирующими такие ферменты, поддаются терапии ограниченным количеством антимикробных препаратов. Обоснованные рекомендации по выявлению БЛРС фенотипическими методами распространяются только на штаммы Klebsiella spp. и Е. coli. Выработка БЛРС может быть выявлена практически у всех видов этого семейства и даже у целого ряда других грамотрицательных палочек.
Продуценты бета-лактамаз расширенного действия (БЛРС) устойчивы ко всем пенициллинам, цефалоспоринам и монобактамам, даже когда in vitro эти препараты эффективны, Существуют различные методы выявления микроорганизмов, вырабатывающих бета-лактамаз расширенного действия (БЛРС), доступные практическим лабораториям. Ориентировочно можно предположить способность грамотрицательных палочек к продукции бета-лактамаз расширенного действия (БЛРС), если in vitro отмечается снижение чувствительности к таким препаратам, как цефподоксим, цефтазидим, цефтриаксон, цефотаксим или азтреонам.
Далее, при выявлении подавления действия b-лактамаз ингибиторами (например, сульбактамом, клавулановой кислотой, тазобактамом) можно утверждать, что данный штамм вырабатывает БЛРС (CLSI, M100-S18, 2003).
При выявлении продуцентов бета-лактамаз расширенного действия (БЛРС) препаратами выбора служат карбапенемы (имипенем, меропенем). Доля продуцентов бета-лактамаз расширенного действия (БЛРС) у пациентов хирургических отделений отечественных стационаров высока и примерно одинакова как для К.pneumoniae (46,2 %), так и для Е. coli (48,2%). По данным мониторинга антибиотикорезистентности в Европе при НКИ за 2005 2008 гг. (SMART), БЛРС — продуценты Е. coli составляют 10,8% (298 из 2764 штаммов), К. pneumoniae - 19,3% (128 из 662), что статистически значимо ниже частоты выделения подобных штам мов в отечственных клиниках.
Следует отметить высокую чувствительность всех штаммов энтеробактерий отечественных клиниках к карбаненемам. При этом к имипенему отмечается более низкая по сравнению с меропенемом чувствительность, особенно в группе Proteus spp., где чувствительность к меропенему достоверно выше по сравнению с имипенемом (97,7% против 54,2% соответственно).
In vitro чувствительность энтеробактерий к препаратам группы аминогликозидов от 30 до 100% и весьма зависит не только от рода, по и от вида энтеробактерий, что подтверждает необходимость организации микробиологических исследований на высоком уровне, который может быть обеспечен в современных условиях.
Такие же выводы можно сделать и в отношении фторх и полонов (ципрофлоксацин, левофлоксацин). В крупных международных исследованиях отмечается высокий процент устойчивых к ципрофлоксацину штаммов E. coli, что наблюдается и в отечественных клиниках: около половины штаммов кишечной палочки устойчивы к ципрофлоксаципу. Многофакторный анализ показал, что профилактика фторхиполопами достоверно связана с увеличением устойчивости микроорганизмов к фторхинолонам и с продукцией БЛРС Е. coli.
Что такое ESBL?
Ключевые моменты
- ESBL - это тип фермента или химического вещества, которое может вызвать бактериальные инфекции.
- Вы можете распространять инфекцию ESBL, просто касаясь кого-то или оставляя бактерии на поверхности, которую кто-то еще касается.
- ИМП, диарея и пневмония - это некоторые условия, которые могут быть вызваны инфекцией ESBL.
Бета-лактамазы расширенного спектра (или короткодействующие ESBL) представляют собой тип фермента или химического вещества, производимого некоторыми бактериями. ESBL ферменты заставляют некоторые антибиотики не работать для лечения бактериальных инфекций. Общие антибиотики, такие как цефалоспорин и пенициллин, часто используются для лечения бактериальных инфекций. При инфекциях ESBL эти антибиотики могут стать бесполезными.
Бактерии используют ESBL, чтобы стать устойчивыми к антибиотикам. Наиболее распространенные типы бактерий, которые производят ESBL, включают:
- Escherichia coli (более известный как E. coli ): Это нормально безвредные бактерии, которые живут в вашей кишке, но также могут вызывать инфекции и пищевое отравление ,
- Klebsiella : Это еще одна безвредная бактерия, которая живет во рту, носе и кишечнике. Но это также может вызывать такие состояния, как инфекции мочевых путей. Это было обнаружено в колониях в больничных условиях и может вызвать распространение инфекций в больницах.
E. coli и инфекции Klebsiella обычно можно лечить обычными антибиотиками, такими как пенициллин и цефалоспорин. Но когда эти бактерии продуцируют ESBL, они могут вызывать инфекции, которые больше нельзя лечить этими антибиотиками. В этих случаях ваш врач найдет другое лечение, чтобы остановить новую инфекцию, которая стала устойчивой к антибиотикам.
Как они распространяются?
Вы можете получить ESBL от касания воды или грязи, содержащей бактерии. Это особенно возможно с водой или почвой, которая была заражена фекалиями человека или животных (корма). Прикосновение к животным, которые несут бактерии, также может распространять бактерии на вас.
Некоторые инфекции, которые также могут вызывать резистентность к антибиотикам, могут увеличить риск заражения бактериальной инфекцией ESBL, например, MRSA (инфекция стафилококка).
Вы можете распространять инфекцию ESBL, просто касаясь кого-то или оставляя бактерии на поверхности, которую кто-то еще касается. Это может включать в себя:
- рукопожатие
- дыхание кого-то
- обращение с объектом, который затем обрабатывается кем-то другим
В некоторых случаях вы можете распространять бактерии с ESBL без заражения сам. Это называется колонизацией. Когда это происходит, ваше тело несет бактерии с ESBL, но не активно заражается. Вам не нужно лечиться, пока вы колонизированы, но вы все равно можете передать инфекцию кому-то еще.Затем их нужно будет лечить.
Бактерии с ESBL особенно распространены в больницах. Они наиболее легко распространяются врачами, медсестрами или другими специалистами здравоохранения, которые касаются людей, предметов или поверхностей в помещениях, где живут бактерии.
Условия, связанные с ESBL
Условия и инфекции, которые могут быть вызваны бактериями, продуцирующими ESBL, включают:
- инфекция мочевых путей (UTI)
- диарея
- кожа инфекции
- пневмония
Симптомы инфекции SBL
Симптомы инфекции ESBL
Симптомы инфекции ESBL зависят от того, какой тип бактериальной инфекции вызвал ESBL.
Если у вас есть ИМП, возможно, вам придется чаще мочиться, чем обычно, и вы можете почувствовать жжение при мочеиспускании. Если у вас есть инфекция кожи с помощью ESBL, вы можете увидеть покрасневшую кожу вокруг участка инфекции и жидкости, выходящей из области.
Если инфекция в кишечнике, вы можете заметить следующие симптомы:
- потеря аппетита
- кровь в вашем стуле
- судороги в желудке
- диарея
- чрезмерный газ или вздутие живота
- лихорадка
Если инфекция ESBL попала в вашу кровь, у вас может быть один или несколько из следующих симптомов:
- чувство дезориентации
- лихорадка
- чувство озноба
- тошнота
- рвота
- проблемы с дыханием
Лечение инфекции ESBL
Лечение инфекции ESBL
Возможные лекарства, используемые для лечения инфекции ESBL, включают:
- карбапенемы, которые полезны против инфекций, вызванных E. coli или Klebsiella pneumoniae бактерии фосфомицин, который эффективен против бактериальных инфекций ESBL
- ингибиторов бета-лактамазы
- антибиотиков небета-лактам
- colistin, который предписывается в редких случаях случаи, когда другие лекарства не смогли остановить инфекцию ESBL
- Средства защиты от образа жизни
Профилактика и перспективы
Профилактика и перспективы
Мытье рук - лучший способ предотвратить распространение бактериальных инфекций ESBL. Мытье рук особенно важно, если вы находитесь в больнице или другом медицинском учреждении. Мойте руки, если вы вступаете в контакт с тем, у кого недавно была инфекция.
Надевайте перчатки, когда вы находитесь рядом с кем-то, у кого есть инфекция или обращение с объектами в больнице или в медицинском учреждении. Перчатки также могут помочь защитить вас от сбора бактерий ESBL. Мойте одежду, постельные принадлежности или другие материалы, которые вы коснулись, носили или спали, пока у вас была инфекция ESBL. Это может привести к распространению бактерий.
Если у вас есть инфекция ESBL, когда вы находитесь в больнице, ваш врач может захотеть сохранить контактную изоляцию.В этом случае вы останетесь в районе больницы, где ваша инфекция может содержаться и не будет распространяться среди других людей, проживающих на объекте. В зависимости от того, насколько серьезна ваша инфекция, вам может потребоваться изолировать от нескольких часов до нескольких дней.
Большинство инфекций ESBL можно успешно лечить, как только ваш врач найдет лекарство, которое может остановить устойчивые бактерии. После того, как ваша инфекция будет лечиться, ваш врач, скорее всего, даст вам хорошие методы гигиены. Они могут помочь вам не развить какие-либо другие инфекции, которые также могут противостоять антибиотикам.
Бета-лактамазы расширенного спектра, или ESBL, представляют собой ферменты, продуцируемые некоторыми типами бактерий. Эти ферменты могут разрушать активные ингредиенты во многих распространенных антибиотиках, что делает их неэффективными.
Существует не менее 200 различных типов ESBL-ферментов. Исследователям еще многое предстоит узнать о них, отчасти потому, что инфекции, связанные с ESBL, были обнаружены только недавно.
Первый зарегистрированный случай инфекции с участием ESBL произошел в Греции в 1960-х годах. Соединенные Штаты сообщили о своем первом случае в 1988 году.
Триггеры

До сих пор ESBL сообщалось только о грамотрицательных бактериальных инфекциях. Грамотрицательные бактерии будут розовыми во время окрашивания при подготовке к микроскопическому исследованию.
Бактерии имеют встроенные инструменты, чтобы обмануть иммунную систему и отключить лекарства. Они также могут развивать лекарственную устойчивость через случайную мутацию и передавать полезные мутации следующему поколению.
Несколько различных видов бактерий способны продуцировать ESBL. Исследователи по-прежнему не уверены в том, что побуждает бактерии вырабатывать резистентные к лекарственным средствам ферменты, но подозревается злоупотребление или злоупотребление антибиотиками.
Важно знать, что в каждой семье и группе бактерий обычно встречаются сотни разных видов, только некоторые из которых могут продуцировать ESBL.
Бактериальные группы, которые, как известно, производят ESBL, включают:
коробка передач

Любой, кто имеет контакт с поверхностью, объектом, животным или другим лицом, инфицированным или подвергшимся воздействию бактерий, продуцирующих ESBL, может распространять инфекцию.
Однако большинство инфекций ESBL развиваются в медицинских учреждениях и связаны с заражением фекальных матерей.
Согласно исследованию 2015 года, большинство людей, инфицированных бактериями, продуцирующими ESBL, были госпитализированы в среднем за 11-64 дня до развития инфекции.
В то время как традиционно ассоциируется с лицами, страдающими иммунитетом, больницами и домами престарелых, инфекция становится все более частым и широко распространенным явлением.
По данным Американских центров по контролю и профилактике заболеваний (CDC), бактерии, продуцирующие EBSL, считаются серьезной угрозой в США.
Важно принимать дополнительные меры предосторожности, включая повышенную мытье рук, всякий раз, когда возникает или возникает подозрение.
Многие бактерии могут жить на поверхности кожи в течение нескольких дней и даже передаваться через дыхание человека. Некоторые люди, которые не развивают инфекции или проявляют симптомы, могут действовать как носители, распространяя инфекционные бактерии, не зная об этом.
Связанные условия и симптомы
Известно, что бактериальные инфекции, связанные с ESBL, вызывают несколько связанных состояний здоровья. Общие осложнения и симптомы, сопровождающие бактериальные инфекции, включают:
Большинство бактерий, продуцирующих ESBL, называются семейством бактерий, которые обычно живут в желудочно-кишечном тракте, не вызывая инфекции.
По этой причине многие связанные с ESBL инфекции раздражают желудочно-кишечную оболочку. Когда у тела есть инфекция, иммунная система также способствует увеличению метаболизма и удалению отходов, вызывая диарею.
Общие симптомы диареи включают:
- с тремя или более свободными стульями за один день
- кровавый стул
- газ и вздутие живота
- лихорадка
- спазмы желудка
- потеря аппетита
Бактериальные инфекции в ранах могут привести к красному и опуханию кожи. Жидкость также может просачиваться из места раны.
Несколько внутренних бактериальных инфекций также могут вызывать дерматологические симптомы, в том числе красные, повышенные удары.
Пневмония возникает, когда бактерии заражают легкие и дыхательные пути. Общие симптомы пневмонии включают:
- кашель, часто с мокротой или толстой слизистой
- затрудненное дыхание
- усталость или необъяснимое истощение
- сбивчивое дыхание
- лихорадка и озноб
- потение и встряхивание
- тошнота и рвота
- понос
- низкая температура тела
Инфекции мочевых путей (ИМП) возникают, когда в мочевом тракте развиваются бактерии. Общие симптомы ИМП включают:
- повышенная потребность в мочеиспускании
- ощущение жжения во время мочеиспускания
- зуд, жжение в половой области
Сепсис возникает, когда инфекция вызывает чрезмерную реакцию иммунной системы, высвобождая химические вещества в кровоток, которые вызывают воспалительный ответ на весь организм. Сепсис опасен для жизни и может привести к выпадению органов и смерти.
Общие симптомы сепсиса включают:
- лихорадка и озноб
- тошнота и рвота
- чувство дезориентированности и смущения
- затрудненное дыхание
Лечение и перспективы
Поскольку бактерии, продуцирующие ESBL, устойчивы к общим антибиотикам, лечение включает использование менее распространенных лекарств, которые иногда могут быть менее эффективными.
Кроме того, у многих бактерий, продуцирующих ESBL, есть дополнительные инструменты для отключения других типов антибиотиков. Если у человека была инфекция в течение длительного времени или при использовании препаратов, бактерии могут развиваться и развивать иммунитет к ним.
Первая линия лечения людей, которые были подтверждены как имеющие инфекцию, обычно представляет собой класс препаратов, называемых карбапенемами. Процесс лечения может включать некоторую степень проб и ошибок.
Для полного устранения инфекции человека может потребоваться несколько курсов лечения и различные лекарства.
Обычно используемые лекарства для лечения инфицированных ESBL включают:
- карбапенемы (имипенем, меропенем и дорипенем)
- цефамицины (цефокситин и цефотетан)
- фосфомицина
- нитрофурантоином
- ингибиторы бета-лактамазы (клавулановая кислота, тазобактам или сульбактам)
- не-бета-лактамаз
- colistin, если все другие лекарства потерпели неудачу
По данным CDC, устойчивые к карбапенем — очень серьезная угроза развития.
Устойчивые к карбапенем инфекции невосприимчивы к почти любой форме доступных антибиотиков и несут ответственность за 9 000 инфекций в год и 600 смертей. Почти половина людей, у которых развилась инфекция в их кровотоке, умерла.
В некоторых ситуациях, особенно если у человека есть ослабленная иммунная система, может потребоваться госпитализация и изоляция. Большинство инфекций занимает несколько недель или месяцев для лечения.
профилактика

Люди с долгосрочными условиями и люди, которые госпитализированы, являются наиболее подверженными риску развития инфицированных ESBL инфекций. Дополнительные меры предосторожности, такие как повышенная мытье рук, всегда должны использоваться в медицинских учреждениях.
Общие рекомендации по предотвращению бактериальных инфекций, связанных с ESBL, включают:
- избегая тесного контакта с людьми или животными с бактериальными инфекциями
- ношение перчаток в медицинских учреждениях или вокруг инфицированных лиц
- избегая касания лица и рта
- носить одежду с длинными рукавами, когда вокруг инфицированных людей
- мытье рук до и после контакта с инфицированными лицами
- стирка всей одежды и постельных принадлежностей, которые могли быть подвергнуты воздействию инфицированных людей в горячей воде
- дезинфицирующие поверхности, особенно в ванных комнатах и кухнях
- дезинфицирующие приспособления, такие как дверные ручки и краны
- принимая антибиотики точно так, как указано
- говоря врачу, если антибиотики не улучшают симптомы инфекции
- беседу с врачом и принятие дополнительных мер предосторожности при гигиене, если в течение короткого промежутка времени необходимо несколько курсов антибиотиков
- если инфекция, участвующая в ESBL, подтверждается, избегая контакта с другими людьми или находясь в общественных местах, особенно в переполненных районах
Читайте также:


