Гнойно воспалительные инфекции микробиология
ЛЕКЦИЯ № 19. Грамотрицательные бактерии – возбудители гнойно-воспалительных заболеваний
1. Гемофильная палочка
Семейство Pasterellaceae, род Haemophilus, вид H. influenza.
Это мелкие или средних размеров прямые палочки, неспоробразующие, неподвижные, грамотрицательные, аэробы. В организме образуют капсулу.
Для культивирования требуются питательные среды, содержащие кровь (кровяной агар) или ее препараты (шоколадный агар).
В окружающей среде микроорганизмы быстро погибают от действия температуры выше 55 °C, солнечных лучей, высушивания, дезинфицирующих растворов.
Биохимическая активность выражена слабо. Расщепляют в основном углеводы до кислоты (без образования газа). По способности образовывать индол, продуцировать уреазу и орнитиндекарбоксилазу гемофилы инфлюэнцы делятся на шесть биоваров.
1) соматический белковый О-антиген;
2) капсульный полисахаридный К-антиген;
По строению капсульного К-антигена вид делится на пять сероваров (обозначаемых a, b, c, d, e). Серовар b – наиболее частый возбудитель менингитов.
2) капсульный полисахарид, обладающий антифагоцитарной активностью.
Экзотоксин не продуцирует.
Гемофильная палочка может входить в состав нормальной микрофлоры слизистой ротоглотки и верхних дыхательных путей, поэтому инфекция может возникать как эндогенная.
При экзогенном инфицировании вызывает инфекции лор-органов и органов дыхания (отиты, пневмонии), менингит. Путь передачи воздушно-капельный. Источником инфекции являются больной или бактерионоситель (антропонозная инфекция).
Чаще всего заболевание развивается как вторичная инфекция при снижении общей резистентности организма, обусловленной основным заболеванием.
Бактериальные менингиты, вызванные гемофильной палочкой, возникают чаще всего у детей от 6 месяцев до 3 лет. Это связано с тем, что у детей в возрасте до 3 месяцев обнаруживаются сывороточные антитела, переданные им от матери, но впоследствии исчезающие, и только к 3–5 годам вновь появляются бактерицидные комплементзависимые антитела к капсульному полисахариду возбудителя.
1) бактериологическое исследование – основной метод; материал – мокрота, спинномозговая жидкость, кровь; среда – кровяной агар. Необходимо дифференцировать от сходных микроорганизмов этого же рода – представителей нормальной микрофлоры носоглотки и ротовой полости;
2) экспресс-метод – иммуноиндикация с помощью реакции иммунофлюоресценции со специфической сывороткой типа b (используют при диагностике менингитов).
Этиотропная терапия проводится антибиотиками с учетом чувствительности возбудителя.
Специфическая профилактика: химическая вакцина.
2. Синегнойная палочка
Относится к семейству Pseudomonadaceae, роду Pseudomonas, виду P. aerugenosa.
Род Pseudomonas, кроме синегнойной палочки, включает в себя еще более 20 видов, многие из которых также могут вызывать заболевание у человека.
Это прямые или слегка изогнутые палочки средних размеров, подвижные (лофотрихи или монотрихи), грамотрицательные, облигатные аэробы. Спор не образуют, имеют тонкую слизистую капсулу.
Синегнойная палочка нетребовательна к питательным средам, хорошо растет на искусственных питательных средах. На мясопептонном бульоне дает рост в виде помутнения с сероватой пленкой на поверхности. На плотных питательных средах формируются крупные полупрозрачные колонии флюоресцирующего зеленоватого цвета. При этом в толщу среды диффундируют синевато-зеленые водорастворимые пигменты – пиоцианин или флюоресцеин. Способность псевдомонад образовывать пигменты – наиболее характерный дифференциально-диагностический признак.
Культура синегнойной палочки при культивировании на питательных средах имеет кисловато-сладкий ароматный запах (специфический запах жасмина).
Устойчива во внешней среде. Обладает естественной устойчивостью к антибиотикам.
1) низкая сахаролитическая активность, расщепляет глюкозу до кислоты;
2) высокая протеолитическая активность, разлагает некоторые аминокислоты;
3) редуцирует нитриты до газообразного азота;
4) разжижает желатин.
Метаболизм только окислительный.
1) соматический О-антиген, группоспецифический, по его строению делится на серогруппы;
2) жгутиковый Н-антиген;
3) М-антиген внеклеточной слизи.
1) в организме может образовывать капсулоподобное вещество, имеющее защитные свойства;
2) выделяет термолабильный экзотоксин А, обладающий цитотоксическим и дермонекротическим действием;
3) выделяет эндотоксин;
4) некоторые штаммы продуцируют гемолизины и лейкоцидин;
5) имеет ферменты агрессии, такие как плазмокоагулаза, протеазы, антиэластазы.
Синегнойная палочка может обитать в кишечнике человека, обнаруживается на коже и слизистых оболочках.
Чаще всего синегнойная инфекция является внутрибольничной. Источник – больной (или бактерионоситель). Может вызывать различные заболевания. Особенно часто выделяется при гнойно-воспалительных осложнениях ожоговых ран.
Иммунитет после перенесенной инфекции обусловлен гуморальными и клеточными механизмами.
Диагностика: бактериологическое исследование; материал определяется клиническими проявлениями заболевания.
1) антибиотики (цефалоспорины, аминогликозиды);
2) синегнойный бактериофаг;
3) синегнойная иммунная плазма;
4) убитая лечебная стафило-протейно-синегнойная вакцина.
Род Klebsiella включает в себя несколько патогенных для человека видов. Наиболее значимы K. pneumoniae, K. ozaenae, K. rhinoscleromatis.
Это грамотрицательные палочки средней величины, не образующие спор. Факультативные анаэробы. В препаратах располагаются поодиночке, попарно или короткими цепочками. Не имеют жгутиков, неподвижны. Спор не образуют.
Это истинно-капсульные бактерии: образуют капсулу в организме и на питательных средах. Капсула имеет полисахаридную структуру.
Нетребовательны к питательным средам. На плотных питательных средах образуют характерные куполообразные мутные слизистые колонии. При росте на мясопептонном бульоне вызывают равномерное помутнение, иногда со слизистой пленкой на поверхности.
Клебсиеллы устойчивы к факторам внешней среды, благодаря капсуле длительно сохраняются в воде, на предметах, в помещениях.
Обладают выраженной сахаролитической активностью, ферментируют углеводы с образованием кислоты и газа. По биохимическим свойствам род делится на шесть видов. Для дифференциации используют следующие тесты:
1) ферментацию глюкозы;
2) ферментацию лактозы;
3) образование уреазы;
4) утилизацию цитрата.
1) соматический О-антиген – группоспецифический;
2) капсульный К-антиген.
К-антигены является общими с антигенами эшерихий и сальмонелл.
1) обладают выраженными адгезивными свойствами;
2) главный фактор – капсула, защищающая микроорганизмы от фагоцитоза;
3) имеют К-антиген, подавляющий фагоцитоз;
4) выделяют эндотоксин.
Клебсиеллы нередко обнаруживаются на коже и слизистых оболочках, в связи с чем возможно развитие эндогенной инфекции. Но экзогенное заражение встречается чаще. Источниками инфекции могут быть больной, бактерионоситель, объекты внешней среды. Пути передачи – воздушно-капельный, контактно-бытовой.
K. pneumoniae может вызывать у человека пневмонию, поражение суставов, мозговых оболочек, мочеполовых органов, гнойные послеоперационные осложнения, сепсис.
K. ozaenae поражает слизистую оболочку верхних дыхательных путей и придаточных пазух носа, вызывая их атрофию.
K. rhinoscleromatis поражает слизистую оболочку носа, трахею, бронхи, глотку, гортань.
Постинфекционный иммунитет нестойкий.
1) бактериологическое исследование; материал – отделяемое пораженных слизистых оболочек;
1) антибиотики, фторхинолоны с учетом чувствительности возбудителя;
2) убитая лечебная вакцина Солко-Уровак (для лечения урогенитальных инфекций);
3) вакцина ВП-4 (для лечения инфекций дыхательных путей).
Специфическая профилактика: вакцина IRS19.
Род Proteus. Возбудителем гнойно-воспалительных заболеваний является вид P. mirabilis.
Это полиморфные грамотрицательные палочки с закругленными концами, факультативные анаэробы. Капсулообразование отсутствует. Имеют перитрихиально расположенные жгутики.
Н-формы этих бактерий отличаются высокой подвижностью, хотя встречаются и неподвижные (О-формы).
Нетребовательны к питательным средам. На мясопептонном агаре Н-форма протея дает характерный ползучий рост в виде нежной вуали голубовато-дымчатого цвета (феномен роения), затягивающий всю поверхность сплошным налетом без образования отдельных колоний. В жидкой питательной среде дает рост в виде диффузного помутнения. При культивировании характерен гнилостный запах.
О-формы образуют крупные с ровными краями колонии. Некоторые штаммы вызывают гемолиз эритроцитов в кровяных средах.
В окружающей среде устойчивы, могут сохранять жизнеспособность в слабых растворах дезинфектантов. Широко распространены в природе. Являются обитателями кишечника человека и животных.
1) ферментируют глюкозу до кислоты;
2) не разлагают маннит и лактозу;
3) продуцируют сероводород;
4) разжижают желатин, расщепляют мочевину с образованием аммиака;
5) обладают протеолитической и пептолитической активностью.
1) соматический О-антиген – группоспецифический;
2) жгутиковый Н-антиген – вариантспецифический.
По Н-антигену протеи делят на 110 сероваров. Внутри вида различают фаговары, бактерициновары, бактериоциногеновары.
1) адгезины – пили;
3) патогенные амины – индол, скатол;
4) ферменты агрессии – протеазы.
Протеи в небольших количествах могут обнаруживаться в кишечнике здорового человека, поэтому протейная инфекции может развиваться как эндогенная.
Основным местом их обитания являются объекты внешней среды, гниющие продукты, сточные воды, почва. Источниками инфекции для человека могут быть больной и бактерионоситель.
Бактерии участвуют в развитии гнойно-воспалительных заболеваний мочевыводящих путей, быстро распространяются по ожоговой поверхности, давая характерный гнилостный запах.
Постинфекционный иммунитет нестойкий.
Диагностика: основной метод – бактериологическое исследование; материал определяется локализацией очага поражения. Посев по методу Шушкевича в каплю конденсированной влаги свежескошенного мясопептонного агара; характерен рост в виде вуали по всей поверхности среды.
1) антибиотики, нитрофураны, фторхинолоны;
2) протейный или колипротейный бактериофаг;
3) убитая лечебная стафило-протейно-синегнойная вакцина.
Раневые и гнойные инфекции часто встречаются в хирургической, акушерско-гинекологической, терапевтической, педиатрической практике, а также других отраслях медицины. Нередко они носят характер внутрибольничной (госпитальной) инфекции. Возбудителями раневой и гнойной инфекции являются бактерии, которые относятся к разным семействам, родам и видам. Среди них известны аэробные и анаэробные, грам-положительные и грамотрицательные бактерии.
БАКТЕРИИ - ВОЗБУДИТЕЛИ РАНЕВОЙ И ГНОЙНОЙ ИНФЕКЦИИ
Chryseobacterium indologenes Chryseobacterium meningosepticum Enterococcus faecalis и другие виды Enterococcus Erysipelothrix rhusiopathiae Staphylococcus aureus Staphylococcus epidermidis Staphylococcus saprophiticus и другие виды Staphylococcus Streptococcus pyogenes Streptococcus agalactiae
Burkholderia cepacia Citrobacter koseri Edwardsiella tarda Eikenella corrodens Enterobacter spp. Escherichia coli Haemophilus influence Klebsiella spp. Listeria monocytogenes Moraxella catarrhalis Proteus vulgaris Proteus mirabilis Pseudomonas aeruginosa Pseudomonas putida Pseudomonas fluorescens Salmonella enterica
подвид enterica биовар typhimurium Serratia spp. Spirillum minus Streptobacillus moniliformis Vibrio vulnificus
Неспорообразующие грамотрицательные анаэробы
и другие виды рода Bacteroides
и другие виды рода Prevotella
Неспорообразующие грамположи-тельные анаэробы
Peptostreptococcus spp. Propionibacterium acnes
Спорообразующие грамположи-тельные анаэробы
Clostridium Clostridium Clostridium Clostridium Clostridium Clostridium Clostridium
Бактерии, перечисленные выше, вызывают гнойно-воспалительные процессы различной локализации, в том числе ангины, фурункулы, циститы и пиелиты, плевриты, перикардиты, сепсис и др. Многие из этих возбудителей встречаются в нормальной микрофлоре человека и проявляют свою патогенность только при нарушении нормальной экологии.
Стафилококки, стрептококки, протей, эшерихии и анаэробные бактерии нередко вызывают смешанную инфекцию как в разнообразных сочетаниях между собой, так и с другими микроорганизмами — вирусами, грибами.
Тема 12.1. АЭРОБНЫЕ БАКТЕРИИ -ВОЗБУДИТЕЛИ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И РАНЕВЫХ ИНФЕКЦИЙ
План
Программа
Биологические свойства возбудителей гнойно-воспалительной и раневой инфекции, их патогенность, экология, особенности инфекции и эпидемиология вызываемых заболеваний.
Диагностические препараты, профилактические и лечебные препараты.
Рост а- и р-гемолитических стрептококков на кровяном агаре.
Рост и образование пигмента P.aeruginosa на агаре.
Диагностические и лечебно-профилактические препараты.
а Задание студентам
Микроскопировать и зарисовать мазки из чистых культур возбудителей гнойных инфекций: S.aureus, S.pyogenes, P.aeruginosa, E.coli, P.vulgaris. Окраска по методу Грама.
Микроскопировать и зарисовать мазки из гноя, содержащие возбудителей: стафилококков, стрептококков. Окраска по методу Грама.
Ознакомиться с питательными средами, применяемыми при микробиологической диагностике гнойных и раневых инфекций. Указать назначение отдельных питательных сред.
Микробиологическое исследование при раневых и гнойных инфекциях:
а) указать материал, подлежащий исследованию;
б) микроскопический метод: микроскопировать мазок из гноя, окраска по методу Грама. Сделать вывод;
в) наметить план дальнейшего исследования.
Задание студентам
1. Микробиологическое исследование гноя:
а) учесть результат посева гноя на кровяной агар в чашке Петри, описать подозрительные колонии, отметить наличие гемолиза, составить план дальнейшего исследования;
б) учесть результаты определения лецитиназы и плазмокоагулазы у выделенной культуры стафилококка.
Сделать вывод;
в) учесть результаты определения чувствительности культуры стафилококка к антибиотикам. Сделать вывод.
Микробиологическое исследование мочи. Определить количество бактерий в 1 мл мочи по результатам метода секторных посевов. Дать заключение.
Серодиагностика ревматизма. Ознакомиться с описанием стрептолизиновой реакции. Внести в протокол результаты определения анти-0-стрептолизина в сыворотке крови больного. Сделать вывод.
Дать краткую характеристику демонстрируемым антимикробным, диагностическим и лечебно-профилактическим препаратам.
Методические указания
Материал для исследования: раневое отделяемое, гной, экссудат, моча, мазки со слизистых оболочек (носоглотки, зева и др.), кровь при подозрении на сепсис.
• Микробиологическая диагностика стафилококковых инфекций
МЕТОДЫ ДИАГНОСТИКИ:
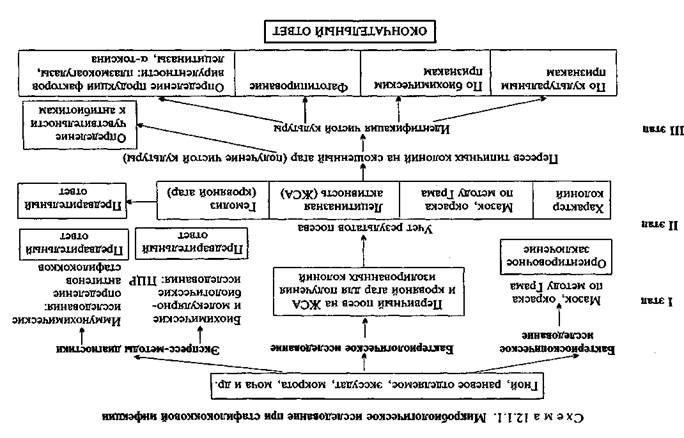
Бактериоскопическое исследование (схема 12.1.1). Из исследуемого материала (за исключением крови) готовят мазки для первичной бактериоскопии, окрашивают по методу Грама и микроскопируют. Наличие в препаратах грамположителькых кокков, располагающихся в виде гроздевидных скоплений (рис. 12.1.1; на вклейке), позволяет поставить предварительный диагноз стафилококковой инфекции. Следует иметь в виду, что в патологическом материале стрептококки редко образуют типичные скопления, чаще располагаются поодиночке или небольшими группами по 2—3 бактерии.
Бактериологическое исследование. Испытуемый материал засевают петлей на чашки с кровяным и желточно-солевым агаром
| Признак Вид S.aureus S.epider- S.sapro-midis phyticus Образование: плазмокоагулазы + — — лецитиназы + — — альфа-токсина + — — Ферментация: глюкозы + + — маннита в анаэробных условиях + — + Чувствительность к новобиоцину S S R |
Определение чувствительности стафилококка к антибиотикам — см. тему 7.2.
Экспресс-методы диагностики: иммунохимические, биохимические и молекулярно-биологические исследования.
Иммунохимические исследования. Основаны на обнаружении антигенов (токсинов и ферментов) возбудителя в материале от больного с помощью чувствительных серологических реакций.
Биохимические и молекулярно-биологические исследования. Исследуемый материал, полученный из очага инфекции, используют для обнаружения ДНК возбудителя с помощью ПЦР. В случае обнаружения соответствующих молекул можно поставить предварительный диагноз.
• Микробиологическая диагностика стрептококковых инфекций (схема 12.1.2)
Бактериоскопическое исследование. Мазки для первичной бактериоскопии готовят из патологического материала (за исключением крови), окрашивают по методу Грама и микроско-пируют. При положительном результате обнаруживают цепочки грамположительных кокков (см. рис. 12.1.1). Следует иметь в виду, что в патологическом материале стрептококки редко образуют типичные скопления, чаще располагаются поодиночке или небольшими группами по 2—3 бактерии.
Бактериологическое исследование. Исследуемый материал засевают на кровяной агар в чашку Петри. После инкубации при 37 "С в течение 24 ч отмечают характер колоний и наличие вокруг них зон гемолиза. Из части материала, взятого из колоний, готовят мазок, окрашивают по методу Грама и микро-скопируют. Для получения чистой культуры 1—3 подозрительные колонии пересевают в пробирки со скошенным кровяным агаром и сахарным бульоном. На кровяном агаре Streptococcus pyogenes образует мелкие, величиной с булавочную головку, мутноватые круглые колонии. В бульоне стрептококк в отличие от стафилококка дает придонно-пристеночный рост в виде хлопьев или зерен, оставляя среду прозрачной.
По характеру гемолиза на кровяном агаре стрептококки делятся на три группы: 1) негемолитические; 2) ссргемолити-ческие, или зеленящие, образующие зеленоватую зону частичного гемолиза; 3) р-гемолитические, образующие вокруг колонии полностью прозрачную зону гемолиза.
Заключительным этапом бактериологического исследования является идентификация выделенной культуры по антигенным свойствам (табл. 12.1.2). Серогруппу стрептококков определяют в реакции преципитации с экстрактом из исследуемой культуры (полисахаридным преципитиногеном С) и группоспецифи-
| Вид Рост при Рост на средах, содержащих желчь (40%) 10 °С 45 "С метиленовый хлорид натрия синий (0,1%) (6,5%) S.pyogenes — — — — — S.pneumoniae — + ± — — S.sanguis — ± — — + S.salivarius — + — — — Вид Рост Термоустойчи- Образование раствори- Антиген- при вость при 60 "С мого гемолизина ная груп- рН в течение 1 па (серо- 9,6 30 мин О S группа) S.pyogenes — — -f + A S.pneumoniae — — + — — S.sanguis ± H(— ) S.salivarius — — — — —(К) |

1:50, 1:250, 1:1000. Диагностический препарат О-стрептолизина также разводят буфером и применяют в количестве 0,3 мл, в котором содержится 1 рабочая доза О-стрептолизина. Рабочая доза — количество О-стрептолизина, которое почти полностью нейтрализуется половиной международной единицы анти-О-стрептолизина стандарта ГИСК. О-стрептолизин в рабочей дозе должен вызывать полный лизис 0,2 мл 5 % взвеси эритроцитов. Разведенную сыворотку и другие ингредиенты разливают по пробиркам так, как указано в табл. 12.1.3, и инкубируют. После инкубации отмечают последнюю пробирку, в которой сыворотка еще нейтрализует рабочую дозу О-стрептолизина (гемолиз отсутствует). Титр сыворотки выражают числом единиц анти-О-стрептолизина в 1 мл (АЕ St-O в 1 мл). В табл. 12.1.3 приведено число АЕ St-O в 1 мл сыворотки при нейтрализации О-стрептолизина различными разведениями сыворотки. Титр анти-О-стрептолизина до 250 АЕ St-O обнаруживается у практически здоровых людей. При ревматизме с первых дней болезни антитела к О-стрептолизину выявляются в высоких титрах — 500 АЕ St-O и выше.
• Микробиологическая диагностика гнойно-воспалительных заболеваний, вызванных грамотрицательными аэробными бактериями
Бактериоскопическое исследование. Из исследуемого материала (гной, раневое отделяемое, участки ожоговой ткани и др.) готовят мазки, окрашивают по методу Грама и микроско-пируют. Обнаружение в мазках грамотрицательных бактерий позволяет сделать предварительное заключение.
Бактериологическое исследование. Для выделения культуры Pseudomonas aeruginosa исследуемый материал засевают в чашки Петри на основные (МПА) или селективные питательные среды (агар, содержащий цитилпиридиний хлорид, который угнетает рост сопутствующей микрофлоры — ЦПХ-агар). Посевы инкубируют при 37 °С в течение суток. P.aeruginosa образуют круглые плоские слизистые колонии, окрашивая среду характерным сине-зеленым пигментом. При бактериоскопии темнопольным методом нативных препаратов, приготовленных из колоний, в "раздавленной" или "висячей" капле обнаруживают подвижные и слегка изогнутые палочки; в мазках, окрашенных по методу Грама, — грамотрицательные палочки. Чистые культуры P. aeruginosa идентифицируют по биохимическим признакам и образованию пигмента.
Для эпидемиологического анализа госпитальных инфекций определяют серовары в реакции агглютинации, пиоциновары и фаговары.
Для выделения энтеробактерий исследуемый материал засевают на одну из дифференциально-диагностических сред, например на среду Эндо (см. тему 3.1). Для выделения бактерий рода Proteus используют метод Шукевича (см. тему 3.1).
Экспресс-методы диагностики: иммунохимические, биохимические и молекулярно-биологические исследования. Иммунохимические исследования. Патогенные штаммы P.aerugi-nosa выделяют различные растворимые белковые (экзотоксины и экзоферменты) и небелковые (экстрацеллюлярная слизь) антигены, которые могут быть обнаружены в материале от пациента (из очага, в крови или моче) с помощью чувствительных серологических реакций (ИФА и др.).
Биохимические и молекулярно-биологические исследования. Исследуемый материал, полученный из очага инфекции, используют для обнаружения ДНК возбудителя с помощью ПЦР. В случае обнаружения соответствующих молекул можно поставить предварительный диагноз.
• Микробиологическая диагностика сепсиса
МАТЕРИАЛ ДЛЯ ИССЛЕДОВАНИЯ: кровь; при септико-пиемиях исследуют также материал из первичных и вторичных местных очагов инфекции. Кровь берут в период подъема температуры до начала антибиотикотерапии из локтевой вены в количестве не менее 10 мл у взрослых и 5 мл у детей, так как микроорганизмы находятся в крови в сравнительно небольших количествах. Посевы делают у постели больного в колбы с 50—100 мл питательной среды. Сравнительно большие объемы питательной среды (в 10 раз превышающие количество крови) необходимы для устранения бактерицидного действия сывороточных белков.
В случае необходимости транспортировки крови к ней добавляют антикоагулянты: цитрат или оксалат натрия, декстран сульфат, гепарин. В качестве добавки к среде для выделения бактерий из крови используют полианетолсульфонат натрия, являющийся антикоагулянтом и одновременно угнетающий бактерицидную активность сыворотки, фагоцитоз, инактиви-рующий комплемент и нейтрализующий лизоцим.
Бактериологическое исследование. Является ведущим при лабораторной диагностике сепсиса. Посевы производят на жидкие среды обогащения: сахарный бульон и др.; при подозрении на анаэробную флору — на тиогликолевую среду, среду Китта—-Тароцци или другие элективные среды для анаэробов (см. тему 3.1) и инкубируют их при 37 °С в течение 10 дней при ежедневном контроле. В случае отсутствия роста микроорганизмов дают отрицательный ответ. При наличии роста делают мазки, которые окрашивают по методу Грама. Выделенную чистую

| Число колоний в секторах Количество 1 1 1 бактерий А I II III в 1 мл мочи 1—6 — — — Менее 10 3 8-20 - - - 3-Ю 3 20-30 - - - 5-Ю 3 30-60 - - - 10 4 70-80 - - - 5-1 0 4 100-150 5-10 - - 10 5 Несосчитываемое 20—30 — — 5-Ю 5 Несосчитываемое 40—60 — — 10 6 ^сосчитываемое 100—140 10—20 — 5-1 0 6 Несосчитываемое Несосчи- 30—40 — 10 7 тываемое Несосчитываемое То же 60—80 Единичные 10 8 колонии |
Иммуноглобулин человеческий противостафилококковый.
Гамма-глобулиновая фракция сыворотки крови, содержащая стафилококковый антитоксин. Готовят из крови животных или людей, иммунизированных стафилококковым адсорбированным анатоксином. Применяют для специфического лечения при стафилококковых заболеваниях.
Стафилококковый бактериофаг (жидкий). Фильтрат фаголи-зата стафилококков. Применяют наружно, внутрикожно, внутримышечно для лечения при стафилококковых заболеваниях.
Диагностические стафилококковые фаги. Набор типоспеци-фических фагов для фаготипирования стафилококков.
О-стрептолизин сухой. Лиофильно высушенный фильтрат бульонной культуры стрептококка — активного продуцента О-стрептолизина. Применяют для серодиагностики — определения антител к О-стрептолизину в сыворотках крови больных стрептококковыми инфекциями (чаще ревматизмом).
Антибиотики. Грамположительные бактерии — р-лак-тамные антибиотики, ванкомицин, тетрациклины, аминогли-козиды, макролиды, линкомицины, сульфаниламиды, фторхи-нолоны и др.
Грамотрицательные бактерии — р-лактамы, спектр действия которых сдвинут в сторону грамотрицательных микроорганизмов, хлорамфеникол, аминогликозиды, тетрациклины, сульфаниламиды, фторхинолоны и др.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.


Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.
Граница между патогенными и непатогенными микроорганизмами четко не обозначена. Помимо микроорганизмов, которые практически всегда при минимальных инфицирующих дозах вызывают у человека инфекционное заболевание, и микроорганизмов, которые даже при больших инфицирующих дозах не вызывают болезни человека, существует множество микроорганизмов, занимающих промежуточное положение. Их нередко высевают при обследовании совершенно здорового человека, не предъявляющего никаких жалоб, и эти же микроорганизмы могут вызывать тяжелейшее заболевание человека нередко со смертельным исходом.
Многими учеными делались попытки провести четкие грани между патогенными, условно-патогенными, или микробами-оппортунистами, и непатогенными микроорганизмами, но эти грани настолько размыты и настолько важную роль играет состояние макроорганизма в возникновении инфекции, что на уровне современных знаний это вряд ли возможно.
Необоснованное назначение гормональных препаратов, антибиотиков может вызывать иммунодепрессивное состояние, не говоря о тех случаях, когда врач вынужден угнетать иммуногенез для предотвращения отторжения трансплантата (например, пересадка почки) или в других случаях. Большое количество иммунокомпромиссных хозяев находится в различных стационарах (хирургические отделения, ожоговые центры, отделения реанимации и интенсивной терапии, отделения недоношенных детей и т.п.). Поэтому оппортунистические инфекции обычно носят характер госпитальных инфекций. Обычно уровень заболеваемости госпитальными инфекциями колеблется от 5 до 500 на 10 000 госпитализированных. Поэтому оппортунистические инфекции представляют собой серьезную проблему современной клинической медицины во всем мире.
Распространению госпитальных инфекций немало способствуют антисанитарные условия пребывания больных в стационарах, погрешности медицинских работников в асептике и антисептике. Часто медицинский инструментарий и аппаратура не подвергаются достаточной дезинфекции и стерилизации, иногда условно-патогенные бактерии можно обнаружить даже на перевязочном и шовном материале, в готовых лекарственных формах. В некоторых случаях условно-патогенные микроорганизмы кон-таминируют (заселяют) больничную аппаратуру, служащую для обследования и лечения больных, или аптечные приборы, используемые для приготовления лекарственных форм.
Например, контаминация псевдомонадами дистиллятора приводит к тому, что дистиллированная вода, которую используют для приготовления многих лекарственных средств для больных, содержит P.aemginosa и вместе с лекарственным средством попадает в организм больного. Диагностика оппортунистических инфекций связана с многими трудностями из-за многообразия локализации воспалительных процессов и, следовательно, симптоматики заболеваний. Кроме того, обнаружение в гное или мокроте стафилококка не является доказательством того, что стафилококк вызвал это заболевание, так как стафилококк (как и большинство других условно-патогенных микроорганизмов) является представителем нормальной микрофлоры человеческого тела.
Для доказательства этиологической значимости выделенных микроорганизмов-оппортунистов необходимы количественные исследования, доказывающие высокую концентрацию данного микроорганизма в исследуемом субстрате. Другим доказательством этиологической значимости выделенной культуры может служить положительная сероконверсия: нарастание титров антител к данному микроорганизму при наблюдении за больным в течение 2-3 нед. Однократное исследование титра антител не может служить доказательством этиологической значимости, так как диагностические титры неизвестны из-за их вариабельности у разных людей.
Обычно титры антител к представителям нормальной микрофлоры человека очень низкие и не служат целям диагностики. Большинство клинических микробиологических лабораторий и лабораторий санитарно-эпидемиологических станций мало используют технику анаэробных посевов, поэтому редко обнаруживают в исследуемом материале облигатных анаэробных возбудителей гнойно-воспалительных заболеваний. Одни из наиболее распространенных нормальных обитателей кишечника человека бактерии рода Bacteroides нередко в сочетании с другими микробами-оппортунистами вызывают локальные абсцессы брюшной полости, полости малого таза, челюстно-лицевой области и др.
Условно-патогенные бактерии могут быть обнаружены не только в патологическом материале, взятом от больного, но и в смывах с предметов окружающей среды: халатов, рук персонала больницы или аптеки, инструментов, посуды, лабораторной аппаратуры, перевязочного и шовного материала, готовых лекарственных форм. Смывы производят стерильным тампоном, смоченным стерильным изотоническим раствором хлорида натрия, с последующим посевом на среды накопления, дифференциально-диагностические и элективные среды. Выделенные чистые культуры идентифицируют до вида. По требованию лечащих врачей-эпидемиологов лаборатория проводит дополнительные исследования по определению чувствительности выделенных бактерий к антибиотикам (антибиотикограмма) или фагам, бактериоцинам и другим маркерам для расшифровки эпидемиологической ситуации в стационаре.
В эту группу входят патогенные и условно-патогенные для человека круглые формы бактерий. Среди них есть строгие анаэробы (пептококки, пептострептококки, вейлонеллы), факультативные анаэробы и аэробы (стафилококки, стрептококки, нейс-серии). Все они могут вызывать у человека гнойно-воспалительные заболевания, различающиеся по локализации и тяжести.
Клеточная стенка содержит большое количество пептидогликана, связанных с ним тейхоевых кислот, протеин А. Стафилококки хорошо растут на простых средах (рН 7,0.7,5); факультативные анаэробы. На плотных средах образуют гладкие круглые выпуклые колонии с различным пигментом. Пигмент не имеет таксономического значения. Могут расти на агаре с высоким содержанием (8-10 %) NaCl. Продуцируют сахаролитические и протеолитические ферменты. Стафилококки вырабатывают гемолизины, фибринолизин, фосфатазу, р-лактамазу, бактериоцинины, энтеротоксины, коагулазу, ДНК-азу, лейкоцидины, лецитовителлазу и др.
Стафилококки очень пластичны: быстро вырабатывают устойчивость к антибактериальным препаратам. Существенную роль в этом играют плазмиды, передающиеся с помощью трансдуцирующих фагов от одной клетки к другой. R-плазмиды детерминируют устойчивость к одному или нескольким антибиотикам, в том числе и за счет экстрацеллюлярной продукции р-лактамазы – фермента, разрушающего пенициллин, разрывающего его р-лактамное кольцо.Антигенная структура стафилококков сложная и вариабельная. Известно около 30 антигенов, представляющих собой белки, полисахариды, тейхоевые кислоты.
Протеин А обладает свойством прочно связываться с Fc-фрагментом любой молекулы IgG. При этом Fab-фрагмент молекулы иммуноглобулина остается свободным и может соединяться со специфическим антигеном. В связи с этим свойством протеин А нашел применение в диагностических методах (коагглютинация). Большинство внеклеточных веществ, продуцируемых стафилококками, также обладает антигенной активностью. Чувствительность к бактериофагам (фаготип) является стабильной генетической характеристикой, базирующейся на поверхностных рецепторах. Многие штаммы стафилококков являются лизогенными. Из а-токсина (экзотоксин) можно приготовить анатоксин.
При микробиологической диагностике отнесение культуры к роду стафилококков основывается на типичной морфологии и окраске клеток, их взаимном расположении и анаэробной ферментации глюкозы. Для видовой идентификации используют в основном 3-4 теста: продукцию плазмокоагулазы, лецитовител-лазы, анаэробную ферментацию маннита и глюкозы. В сомнительных случаях проводят тесты на наличие ДНК-азы, а-токсина.Возбудителем стафилококковых инфекций чаще бывает S. aureus, несколько реже – S. epidermidis, очень редко – S. saprophyticus. Стафилококки являются представителями нормальной микрофлоры человеческого тела, поэтому микробиологическая диагностика стафилококковых инфекций не может ограничиться выделением и идентификацией возбудителей; необходимы количественные методы исследования, т. е. определение числа микроорганизмов в пробе.
Лечение стафилококковых инфекций обычно проводят антибиотиками и сульфаниламидными препаратами. В последние годы от больных часто выделяют стафилококки, резистентные к большинству химиотерапевтических препаратов. В таких случаях для лечения используют антитоксическую противостафилококковую плазму или иммуноглобулин, полученные из крови доноров, иммунизированных стафилококковым анатоксином. Для активной иммунизации (плановых хирургических больных, беременных женщин) может быть использован адсорбированный стафилококковый анатоксин.
Стрептококки . Отдел Firmicutes, семейство Streptococcaceae, род Streptococcus. В род Streptococcus входят более 20 видов, среди которых есть представители нормальной микрофлоры человеческого тела и возбудители тяжелых инфекционных эпидемических заболеваний человека. Стрептококки – мелкие (меньше 1 мкм) шаровидные клетки, располагающиеся цепочками или попарно, грамположительны, спор не образуют, неподвижны. Большинство штаммов стрептококков образуют капсулу, состоящую из гиалуроновой кислоты. Клеточная стенка содержит белки (М-, Т- и R-антигены), углеводы (группоспецифические) и пептидогликаны.
Стрептококки группы А вырабатывают более 20 внеклеточных веществ, обладающих антигенной активностью. Наибольшее значение в патогенезе стрептококковых инфекций имеют:
- А стрептокиназа (фибринолизин) – протеолитический фермент, расщепляющий фибрин и другие белки;
- А ДНК-аза – фермент, деполимеризующий ДНК. Смесь ДНК-азы и фибринолизина способна разжижать экссудаты, лизировать венозные тромбы, поэтому может быть использована для удаления гноя и некротизированных тканей из раны;
- А эритрогенин – токсин, продуцируемый р-гемолитическими стрептококками группы А, способными вызывать скарлатину. Выделяется только лизогенными культурами.
Стандартизованный разведенный эритрогенин используют при постановке внутрикожной пробы (проба Дика) для выявления чувствительности к этому токсину (восприимчивость к скарлатине).
Нейссерии . Отдел Gracilicutes, семейство Niesseriaceae, род Niesseria. Наиболее патогенные для человека виды нейссерий (N. gonorrhoeae и N. meningitidis) описаны в главах, посвященных инфекциям, передающимся контактным (гонорея) и респираторным (менингококковый менингит) путями.
Не нашли то, что искали? Воспользуйтесь поиском:
Читайте также:


