Хирургическое лечение при саркомах мягких тканей

Саркомы мягких тканей представляют большую группу опухолей мезенхимального происхождения, различных по клиническим и морфологическим признакам. На их долю приходится около 2 % в структуре онкопатологии. Статистика последних лет свидетельствует о неуклонном росте заболеваемости и смертности от сарком мягких тканей [2, 4, 9].
Общим для многообразия клинико-морфологических форм сарком мягких тканей является крайне агрессивное течение, характеризующееся многократным рецидивированием, гематогенным метастазированием, определяющим неблагоприятный прогноз заболевания.
Лечение больных саркомами мягких тканей – одна из сложных проблем современной онкологии, над разрешением которой работают и хирурги, и радиологи, и химиотерапевты. Несмотря на разработку различных приемов лучевого воздействия на опухоль, бурное развитие химиотерапии с применением все более современных препаратов, различных их комбинаций и способов введения, хирургический компонент в лечении сарком мягких тканей остается основным.
Строгое следование принципам хирургического радикализма в ходе операций по удалению опухолей мягких тканей приводит к образованию обширных раневых дефектов. Кроме того, при упорно рецидивирующих опухолях предшествующее хирургическое и лучевое воздействие создает неблагоприятный фон для удаления опухоли и пластического закрытия раневого дефекта. Особенностью лечения таких больных заключается в выполнении расширенных, нередко комбинированных вмешательств [5, 7, 8].
Анализ основных тенденций развития онкологии убедительно показывает практическую необходимость в использовании современных технологий пластической хирургии в общей схеме лечения онкологических больных. В частности, хирургический метод развивается по пути реконструктивно-пластического устранения анатомо-функционального дефекта, возникшего при противоопухолевом лечении. Пластическое восполнение послеоперационного дефекта дает возможность более широкого иссечения опухоли, тем самым увеличивая радикальность хирургического вмешательства. Кроме того, адекватное замещение дефектов, образующихся в результате удаления новообразований, исключает значительное натяжение краев раны, которое может повлечь развитие краевого некроза кожи с расхождением краев раны и длительным ее заживлением, отсрочить другие этапы лечения [6, 10].
В настоящее время практически нет разногласий о целесообразности восстановления тканей после удаления злокачественных опухолей мягких тканей и других новообразований наружных локализаций, когда отсутствует возможность закрытия послеоперационной раны без использования дополнительного пластического материала. Гипотеза о повышенной чувствительности кожного трансплантата к поражению опухолевым процессом и о том, что пластическое замещение раневого дефекта после удаления опухоли способствует развитию местных рецидивов, не нашла клинического подтверждения [3].
Более того, отказ от восстановления тканей ведет к сужению границ иссечения опухоли, что является одной из основных причин увеличения частоты локальных рецидивов. Данные авторы убедительно показали, что подобные операции заметно улучшают результаты хирургического лечения больных с далеко зашедшими и рецидивными опухолями. Отмечено, что наиболее рациональна именно одномоментная с удалением опухоли пластика, которая обеспечивает быстрое заживление раны, сокращает длительность послеоперационного периода, предупреждает развитие уродующих рубцов и контрактур. Использование многоэтапных и отсроченных пластических операций малорационально, требует длительного времени и задерживает продолжение специального лечения.
Безусловно, на первом месте должна стоять задача максимально надежного излечения больного от злокачественного новообразования. Это означает, что любые восстановительные операции должны быть спланированы и произведены таким образом, чтобы не нарушать основную лечебную программу. С другой стороны, результат пластики тканевого дефекта должен быть изначально заложен в лечебную тактику.
Исходя из вышеизложенного, концепция единого лечебно-реабилитационного комплекса лечения онкологических больных, предусматривает следующие основные положения:
В данной статье мы хотим привести клинический пример успешного хирургического лечения больной с распространенной дерматофибросаркомой мягких тканей, развившейся на фоне рецидивирующего нейрофиброматоза. Реконструктивно-пластический компонент явился завершающим этапом хирургического вмешательства, поскольку простое ушивание краев раны без использования дополнительного пластического материала не представлялось возможным из-за размеров раневого дефекта, трофических, рубцовых изменений тканей после предшествующих многократных операций.
Дерматофибросаркома выбухающая – злокачественная мезенхимальная опухоль кожи. Встречается в 0,01 % случаев среди всех злокачественных опухолей и 2–6 % среди опухолей мягких тканей. Опухоль встречается редко, поражает лиц мужского и женского пола. Дерматофибросаркома возникает обычно у взрослых, наиболее часто между 30 и 40 годами, чаще у мужчин, но может быть и у детей. Располагаться может на любом участке кожного покрова, но чаще на туловище.
В большинстве случаев обладает медленным ростом, возможно изъязвление, выражена склонность к рецидивированию (до 30–50 %). Практически не метастазирует, только после многих лет существования, в регионарные лимфатические узлы, легкие, мозг, кости.
Для закрытия дефекта мягких тканей после широкого иссечения опухоли у данной больной нами был использован кожно-жировой лоскут на питающей сосудистой ножке. Принимая во внимание расположение питающих сосудов, можно перемещать большие кожно-жировые массивы на ножке и закрывать значительные по величине дефекты. К пластике лоскутом на ножке особенно применим принцип совмещения тщательного планирования операции и учета всех индивидуальных особенностей данной анатомической зоны.
Пластику лоскутом на ножке, образованным поблизости от дефекта, производят в тех случаях, когда по соседству имеется достаточное количество хорошо смещаемой кожи, из которой можно позаимствовать лоскут значительных размеров. Принимая во внимание расположение питающих сосудов, можно перемещать большие кожно-жировые массивы на ножке и закрывать значительные по величине дефекты. К пластике лоскутом на ножке особенно применим принцип совмещения тщательного планирования операции и учета всех индивидуальных особенностей данной анатомической зоны.
При выкраивании лоскутов мы руководствовались типичными разрезами с учетом прохождения сосудистых ветвей, естественных кожных складок, соотношением длины и ширины лоскута 1|:|3 и 1|:|4. Вершину лоскута формировали острой или слегка закругленной, от вершины к основанию лоскут постепенно утолщался, в основание ножки включали достаточное количество мягких тканей с проходящими в них сосудами. Не допускали ротацию лоскутов под большим углом (более 90 °), что вызывает чрезмерное растяжение сосудов питающей ножки и их сдавление.
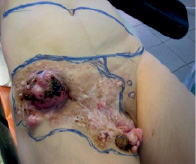
Рис. 1. Вид больной с разметкой
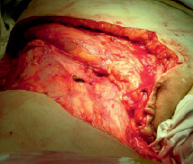
Рис. 2. Вид раневого дефекта после удаления опухоли
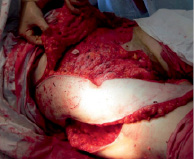
Рис. 3. Этап перемещения лоскута
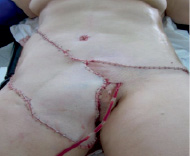
Рис. 4. Окончательный вид послеоперационной раны после ушивания
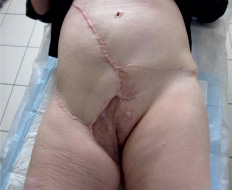
Рис. 5. Общий вид зажившей раны через 6 мес. после оперативного вмешательства
На современном этапе развития хирургической техники и медицины в целом, улучшение результатов хирургического лечения больных опухолями мягких тканей не должно ограничиваться рамками онкологических показателей. Эстетико-функциональные аспекты проблемы могут и должны решаться путем индивидуального подхода к выбору метода кожной пластики, в зависимости от размеров и локализации первичного очага.
Таким образом, дифференцированный подход к способам закрытия обширных мягкотканных дефектов позволил провести радикальное иссечение очага поражения с получением хорошего функционально-эстетического результата. Наиболее надежными способами пластического закрытия ран следует считать перемещение лоскутов на питающей ножке. Индивидуализированный подход к выбору методики для пластического закрытия послеоперационного дефекта в зависимости от локализации опухоли допускает иссечение обширных участков кожи, что повышает радикальность хирургического вмешательства, позволяет избежать осложнений, связанных с натяжением краев раны, улучшая тем самым качество жизни больных и ускоряя медицинскую реабилитацию.
Лечение сарком мягких тканей и остеосарком в EMC проводится междисциплинарной командой специалистов, включающей в себя медицинских онкологов, радиологов, хирургов-ортопедов со специализацией в онкологии, патоморфологов и реабилитологов. План лечения пациента с диагнозом саркома разрабатывается на онкологическом консилиуме. Врачи Института онкологии EMC специализируются на лечении редких видов онкологических заболеваний с использованием современных методов хирургического лечения, лучевой и химиотерапии.
Саркомы представляют собой редкую и разнородную группу злокачественных опухолей: менее 1% всех злокачественных новообразований у взрослых и около 12% случаев рака у детей. Приблизительно 80% сарком образуются из мягких тканей, остальные – из костной ткани.
Наиболее распространенные подтипы сарком мягких тканей у взрослых:
гастроинтестинальные стромальные опухоли (ГИСО, ГИСТ).
недифференцированная плеоморфная саркома
Важно различать виды сарком, как с точки зрения прогноза, так и с точки зрения различий в лечении. Это особенно важно для педиатрических опухолей, которые развиваются у взрослых, таких как рабдомиосаркома (РМС). Как эмбриональные, так и альвеолярные РМС более восприимчивы к химиотерапии и имеют лучший прогноз, чем многие типы сарком мягких тканей у взрослых. Тем не менее, плеоморфные РМС имеют относительно неблагоприятный прогноз, по сравнению с другими подтипами РМС. Такие опухоли преобладают у взрослых, и исходы при данном виде саркомы хуже, чем у детей.
Этиология и патогенез
Почти во всех случаях саркомы возникают первично, а не развиваются из доброкачественных поражений. В большинстве случаев точная этиология неясна, но определено есть несколько сопутствующих или предрасполагающих факторов.
К ним относятся:
генетическая предрасположенность (например, синдром Ли Фраумени, нейрофиброматоз I типа, ретинобластома)
воздействие лучевой терапии или химиотерапии
лимфедема (отек мягких тканей пораженной области)
вирус иммунодефицита человека (ВИЧ) и вирус герпеса 8 типа (при саркоме Капоши)
Симптомы сарком мягких тканей
Наиболее частой жалобой при саркомах мягких тканей является постепенно увеличивающееся в размерах безболезненное объемное образование. Опухоли могут достигать достаточно больших размеров, особенно в области бедра и забрюшинном пространстве. Некоторые пациенты жалуются на боль или симптомы, связанные со сдавлением объемным образованием, включая парестезии или отек конечности. В редких случаях у пациентов наблюдаются общие симптомы: лихорадка или снижение массы тела.
Саркомы мягких тканей могут развиваться в любой части тела, но чаще всего на конечностях.
По данным Американской коллегии хирургов локализация сарком мягких тканей распределяется следующим образом:
Бедро, ягодицы и паховая область – 46%
Верхние конечности – 13%
Забрюшинное пространство – 13%
Голова и шея – 9%
Наличие отдаленных метастазов на момент первичного установления диагноза наблюдается нечасто, но более вероятно при крупных, глубоких саркомах высокой степени злокачественности.
Распространение в регионарные лимфоузлы при саркомах мягких тканей встречается редко.
Наиболее высокий риск метастазирования в лимфоузлы характерен для рабдомиосаркомы, синовиальной саркомы, эпителиоидной саркомы, светлоклеточной саркомы и сосудистых сарком (включая ангиосаркомы).
Рецидив после лечения саркомы мягких тканей может быть как локальным, так и в виде метастазирования. В 70-80 % метастазирование происходит в легкие.
Факторы прогноза при саркоме мягких тканей
Наиболее важными прогностическими факторами являются гистологическая оценка, размер опухоли и стадия на момент постановки диагноза.
В исследовании, проведенном Memorial Sloan Kettering Cancer Center (MSKCC) с использованием классификации злокачественных новообразований TNM, 5-летние показатели безрецидивной выживаемости для I, II и III стадии заболеваний составили 86, 72 и 52% соответственно.
Диагностика сарком мягких тканей
Первоначальная оценка пациента с подозрением на саркому мягких тканей начинается со сбора анамнеза. Устанавливается скорость роста опухоли и наличие симптомов, позволяющих предположить нейроваскулярное нарушение. При физическом обследовании уделяется особое внимание размеру и глубине расположения опухоли, ее связи с окружающими структурами, наличию сопутствующего отека или признаков вовлечения нервов.
Нередко диагноз саркомы мягких тканей устанавливают поздно. Пациенты часто откладывают обращение за медицинской помощью, поскольку опухоль безболезненна.
Частичное иссечение опухоли до направления к специалисту может привести к появлению отдаленных метастазов и необходимости расширенной повторной резекции. Диагностическая биопсия, проведенная несоответствующим образом, может помешать последующему проведению хирургической резекции, косметическому восстановлению, или привести к необходимости более масштабного хирургического вмешательства. Поэтому рекомендовано как можно раньше обратиться в специализированное медицинское учреждение.
Диагностическое обследование опухолей мягких тканей включает в себя:
Магнитно-резонансную топографию (МРТ) при опухолях конечностей, туловища, области головы и шеи или компьютерную топографию (КТ) при опухолях брюшной полости и забрюшинного пространства
Толстоигольную биопсию с последующим морфологическим исследованием, если это технически выполнимо. Если требуется открытая (инцизионная) биопсия, она должна быть тщательно спланирована и выполнена хирургом, который будет проводить тотальную резекцию.
Морфологическое исследование образцов, подозрительных на саркомы мягких тканей, проводится в собственной гистологической лаборатории EMC. При необходимости материалы биопсии могут быть пересмотрены в лабораториях клиник-партнеров EMC в Израиле, Германии или США.
Как только диагноз саркомы мягких тканей подтвержден, проводится исследование органов грудной клетки всем пациентам, чтобы проверить наличие метастазов в легких. У пациентов с высоким риском метастазирования в легкие (опухоли >5 см, глубоко расположенные или имеющие среднюю или высокую степень злокачественности) используется КТ. При круглоклеточных/миксоидных липомах рекомендуется также КТ брюшной полости и таза, поскольку часто встречаются внелегочные метастазы в брюшной полости и забрюшинном пространстве.
Исследование с визуализацией головного мозга предлагается пациентам с ангиосаркомой и альвеолярной саркомой мягких тканей, поскольку эти опухоли характеризуются высокой склонностью к метастазированию в центральную нервную систему.
В повседневной практике позитронно-эмиссионная топография (ПЭТ) или ПЭТ/КТ для первичной оценки стадии при впервые установленном диагнозе саркомы мягких тканей не проводится. ПЭТ или сканирование с галлием может быть значимым у пациентов с нейрофиброматозом в качестве вспомогательного метода дифференциальной диагностики.
Лечение сарком мягких тканей
В большинстве случаев лечение сарком комбинированное. На выбор метода лечения влияет размер и расположение опухоли, степень злокачественности, а также распространенность процесса.
Хирургия как единственный метод лечения может применяться только в том случае, если опухоль высокодифференцированная и возможно ее радикальное удаление.
Хирургическое лечение сарком мягких тканей
Хирургическая резекция первичной опухоли является основным компонентом лечения практически всех пациентов с саркомами мягких тканей конечностей. У большинства пациентов возможна резекция опухоли с адекватными границами резекции, и этот метод позволяет сохранить функцию конечности; небольшой подгруппе пациентов может потребоваться первичная ампутация.
Резекция должна проводиться с захватом тканей, выходящих за пределы псевдокапсулы опухоли, если таковая есть, до достижения визуально здоровой, не вовлеченной в процесс ткани. Повреждение опухоли (т.е. рассечение опухоли или резекция, после которой остается макроскопический или микроскопический остаточный фрагмент опухоли) связано с более высокой частотой местного рецидива, даже если проводится лучевая терапия (ЛТ). Границы резекции служат наиболее важным показателем, который влияет на местный контроль опухоли.
Лучевая терапия сарком мягких тканей
Применение лучевой терапии в сочетании с резекцией снижает необходимость в ампутации и увеличивает вероятность удаления саркомы при сохранении функции конечности. В большинстве случаев сочетание операции с сохранением конечности и лучевой терапии обеспечивает лучший местный контроль.
Послеоперационная лучевая терапия значительно повлияла на частоту сохранения конечностей при саркомах мягких тканей конечностей. В 1970-е годы примерно половине пациентов с СМТ конечностей проводилась ампутация. С развитием лучевой терапии частота ампутаций сократилась почти до 1% без ощутимого снижения общей выживаемости.
Метастазы саркомы. Химиотерапия.
Хирургическая резекция при метастатическом процессе обеспечивает долгосрочную безрецидивную выживаемость и, возможно, излечение у отдельных пациентов, у большинства из которых имеются изолированные метастазы в легких. Однако большинству пациентов с метастатическими саркомами мягких тканей химиотерапия назначается в качестве паллиативного лечения с целью уменьшения общего объема опухоли, уменьшения симптомов, улучшения качества жизни и увеличения выживаемости.
Естественное течение заболевания у пациентов с нерезектабельным метастатическим заболеванием может быть различным и в большей степени зависит от биологических особенностей опухоли, а не от лечения. У некоторых пациентов с бессимптомным нерезектабельным заболеванием низкой степени злокачественности может быть рациональным наблюдение за пациентом без активной химиотерапии. И, наоборот, у пациентов с опухолью высокой степени злокачественности, чувствительной к химиотерапии, такой как синовиальная саркома или липосаркома, может быть предпочтительным раннее начало комбинированной химиотерапии.
Саркомами называют опухоли, которые развиваются из клеток предшественниц соединительной ткани — мезодермы. Как и рак, они представляют собой злокачественные новообразования, но с той разницей, что источником раковой опухоли является эпителий, выстилающий внутренние органы и тело человека. Поэтому эти опухоли имеют привязку к конкретному органу, например, рак предстательной железы, рак молочной железы и др. Саркомы же развиваются из соединительной ткани и могут возникнуть в любом органе, где есть такие клетки, то есть фактически везде.
- Виды сарком мягких тканей
- Стадии развития
- Факторы риска
- Симптомы саркомы мягких тканей
- Диагностика саркомы мягких тканей
- Лечение саркомы мягких тканей
- Прогноз выживаемости при саркоме мягких тканей
Виды сарком мягких тканей
Саркома мягких тканей — это собирательный термин, который объединяет большое количество злокачественных опухолей, среди которых наиболее часто встречаются следующие:
- Лейомиосаркома — опухоль из гладкомышечных клеток.
- Рабдомиосаркома — опухоль из поперечно-полосатой мускулатуры.
- Липосаркома — злокачественная опухоль из жировой ткани.
- Ангиосаркома — злокачественное новообразование, произрастающее из ткани кровеносных сосудов.
- Фибросаркома — опухоль из фиброзной ткани.
Также саркомы мягких тканей принято разделять по степени злокачественности. Низкозлокачественные новообразования редко метастазируют, но склонны к упорному рецидивированию. Высокозлокачественные опухоли склонны давать метастазы гематогенным путем (с током крови), лимфатические узлы поражаются реже.
Стадии развития
Стадия саркомы мягких тканей определяется степенью злокачественности опухоли, ее размером и наличием метастазов.
- К 1 А стадии относят новообразования низкой степени злокачественности, размером менее 5 см, без метастазов в регионарных лимфатических узлы и отдаленных органах.
- 1 В стадия — опухоли низкой степени злокачественности, более 5 см без метастазов.
- 2А стадия — новообразования средней степени злокачественности, менее 5 см без метастазов.
- 2В стадия — новообразования средней степени злокачественности, более 5 см в наибольшем измерении, без метастазов.
- 3А стадия — саркомы высокой степени злокачественности, менее 5 см без поражения лимфатических узлов и внутренних органов.
- 3В стадия — саркомы высокой степени злокачественности, более 5 см без метастазов.
- 4 стадия — саркома любой степени злокачественности, любого размера при наличии поражения лимфатических узлов или метастазов во внутренних органах.

Факторы риска
В большинстве случаев, саркомы мягких тканей развиваются спонтанно, т. е. без видимых причин. Однако есть определенные обстоятельства, которые увеличивают вероятность развития данного заболевания:
- Воздействие химических канцерогенов, в частности гербицидов, хрорфенолов.
- Генетическая предрасположенность — нейрофиброматоз, синдром Ли-Фраумени, синдром Гарднера.
- Воздействие ионизирующего излучения, например, прохождение лучевой терапии.
- Иммунодефицитные состояния — иммуносупрессия после трансплантации органов, прохождение химиотерапии, СПИД.
- Некоторые виды сарком мягких тканей могут развиваться на фоне лимфостаза конечности.
Симптомы саркомы мягких тканей
На начальных этапах, саркома мягких тканей проявляется как безболезненная опухоль, которая медленно увеличивается в размерах. Может иметь капсулу, которая, впрочем, не мешает метастазированию. Также опухоль может иметь инфильтративный рост, в этом случае определить ее края проблематично.
При дальнейшем росте, симптоматика будет зависеть от локализации опухоли. Например, при саркомах матки будут кровотечения, при поверхностной локализации опухоль вызывает отечность и боли, при этом нарушается функция пораженного органа, например, руки или ноги.
Диагностика саркомы мягких тканей
В рамках диагностики саркомы мягких тканей проводится физикальное обследование, используются методы медицинской визуализации с последующим проведением биопсии и морфологического исследования полученного материала.
Обязательно проводится КТ или МРТ пораженной области. Во-первых, исследование помогает обнаружить опухоль, а во-вторых проконтролировать радикальность излечения.
Для постановки диагноза обязательно проводится морфологическое исследование фрагмента опухоли. Чтобы его получить, выполняют трепанбиопсию с помощью специальной толстой иглы под контролем УЗИ, или инцизионную биопсию, которая подразумевает хирургическое иссечение фрагмента новообразования. В ряде случаев, для уточнения типа саркомы необходимо более детальное исследование, тогда проводят иммуногистохимические и молекулярно-генетические анализы.
Для того чтобы установить степень распространения опухоли, проводят КТ грудной клетки, брюшной полости, а также ультразвуковое исследование лимфатических узлов.
Лечение саркомы мягких тканей
Выбор метода лечения саркомы определяется степенью ее злокачественности, местом расположения и наличием метастазов. Для лечения низкозлокачественных опухолей, лечение преимущественно хирургическое, в остальных случаях используются комбинированные методы, включающие облучение и химиотерапию.
При хирургическом лечении сарком используются следующие виды операций:
- Широкая местная резекция. Таким способом удаляются низкозлокачественные небольшие новообразования, располагающиеся в коже и подкожной клетчатке.
- Широкое иссечение. При таком вмешательстве саркома удаляется в пределах анатомической зоны, отступая от края новообразования не менее чем на 4-6 см.
- Радикальная органосохраняющая операция. При таком объеме вмешательства удаляется опухоль совместно с мышечными фасциями и неизмененными мышцами, которые отсекаются в месте их прикрепления. При вовлечении в процесс кровеносных сосудов, нервных стволов и костей, производят их резекцию с одномоментной пластикой кожным или кожно-мышечным лоскутом.
- Ампутации или экзартикуляции — удаление конечности или ее вычленение по линии суставной щели. Такие вмешательства проводятся при обширных местно-распространенных высокозлокачественных процессах с вовлечением магистральных кровеносных и нервных стволов на большом протяжении, а также костных структур и мышц.
Во время операции обязательно проводится интраоперационное срочное гистологическое исследование. При наличии злокачественных клеток в краях отсечения и при потенциальной возможности радикального удаления опухоли, выполняют реоперацию.
Лучевая терапия применяется в рамках комбинированного лечения в предоперационном и/или послеоперационном этапе. В первом случае преследуется цель — уменьшение размера саркомы и создание условий для проведения радикального вмешательства. Во втором — уничтожение оставшихся злокачественных клеток. Чтобы воздействие на опухоль было равномерным, используются многопольные методики облучения.
Предоперационная лучевая терапия
При предоперационной ЛТ, границы полей облучения (ПО) должны выходить за размеры ткани опухоли минимум на 3-4 см. Если опухоль имеет большие размеры, производят облучение в пределах 10 см от ее края до достижения суммарной очаговой дозы 45-50Гр. Затем ПО сокращают до размеров новообразования.
Если опухоль располагается на конечности, есть вероятность развития остеолучевого некроза, мышечных контрактур и отеков. Чтобы этого избежать, рекомендуется облучать не более 2/3 окружности конечности, если это возможно. Минимальная толщина необлучаемых тканей в зоне предплечья составляет 2 см, на бедре 4 см, и на голени — 3 см.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия показана в следующих случаях:
- Высокая степень злокачественности саркомы по данным гистологического исследования.
- Нерадикально проведенная операция — наличие злокачественных клеток в краях отсечения при невозможности проведения реоперации.
- Вскрытие капсулы саркомы во время хирургического вмешательства.
Послеоперационную ЛТ начинают выполнять не позднее, чем через 4 недели после окончания хирургического лечения.
Если предоперацинная ЛТ не выполнялась, поля облучения включают в себя следующие области:
- Ложе опухоли.
- Ткани, которые располагаются на расстоянии 2 см от удаленной опухоли.
- Послеоперационный рубец.
Облучение проводят в суммарной очаговой дозе 60 Гр. Если была проведена нерадикальная операция, дозу увеличивают до 70 Гр. В аналогичном режиме проводят лучевую терапию при невозможности оперативного лечения.
Химиотерапия широко используется для лечения высокозлокачественных сарком мягких тканей. Как и при лучевой терапии, ее могут назначать на дооперационном и/или послеоперационном этапе. Неоадъювантная (предоперационная) ХТ призвана воздействовать на очаг опухоли, уничтожать микрометастазы и создать условия для органосохраняющего хирургического лечения. С этой целью проводят 2-3 курса химиотерапии с перерывом в 3-4 недели.
Послеоперационная ХТ может проводиться для уничтожения микрометастазов или уже визуализируемых метастазов. С этой целью выполняют 3-4 курса лечения. При химиотерапевтическом лечении сарком применяют различные комбинации следующих препаратов:
- Доксорубицин.
- Этопозид.
- Винкристин.
- Ифосфамид.
- Дакарбазин.
- Цисплатин и др.
Схема химиотерапии будет определяться морфологическим вариантом опухоли и ее чувствительностью к ранее проводимому лечению.
Прогноз выживаемости при саркоме мягких тканей
Прогноз выживаемости зависит от многих факторов:
- Степень злокачественности саркомы. Наиболее благоприятное течение у низкозлокачественных сарком без метастазов во внутренних органах и лимфоузлах.
- Размеры опухоли.
- Возможность проведения радикального лечения.
- Возраст больного. Наиболее благоприятные прогнозы у детей. У них полного выздоровления удается достичь в 60% случаев. Наименее благоприятные прогнозы у людей старше 60 лет.
При своевременном лечении начальных стадий низкозлокачественных сарком мягких тканей, удается достичь 5-летней выживаемости у половины больных. При 4 стадии процесса, этот показатель не превышает 10%.
Эффективных методов профилактики саркомы мягких тканей нет. Общие рекомендации являются стандартными — отказ от вредных привычек, ведение здорового образа жизни.
Читайте также:


