Хронические инфекции реактивация это
Т.Н. Лопаткина, Д.Т. Абдурахманов, Е.В. Волчкова
ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздравсоцразвития России
Данные, приведенные в статье, были получены в исследовании оригинального препарата энтекавира (Бараклюд ® ). Применение несертифицированных противовирусных средств может угрожать вашему здоровью, привести к возникновению мутантных штаммов вируса гепатита В и неэффективности дальнейшей терапии.
Заражение вирусом гепатита В (HBV) может быть причиной серьезной реактивации и даже смерти у пациентов с онко-гематологическими заболеваниями, а также у больных после трансплантации костного мозга. Представлены 3 клинических наблюдения реактивации HBV-инфекции у больных В-клеточной лимфомой с развитием печеночно-клеточной недостаточности, которые удалось купировать с помощью нуклеозидных аналогов. Обсуждаются способы профилактики и лечения реактивации HBV-инфекции у больных с лимфомами, получающих химиотерапию.
Ключевые слова: HBV-инфекция, реактивация, В-клеточная лимфома, химиотерапия, иммуносупрессивная терапия, нуклеозидные аналоги, ламивудин, энтекавир.
Для корреспонденции:
Лопаткина Татьяна Николаевна, канд. мед. наук, доц. каф. терапии и профзаболеваний ГБОУ ВПО Первый Московский государственный медицинский университет им. И.М. Сеченова Минздравсоцразвития России
Адрес: 119992, Москва, ул. Россолимо, д. 11
Заражение вирусом гепатита В (HBV) нередко является причиной серьезных осложнений и даже смерти у больных с опухолевыми заболеваниями, особенно с гематологическими опухолями, получающих химиотерапию или перенесших трансплантацию костного мозга. Известно, что частота реактивации HBV-инфекции у больных, получающих химиотерапию, достигает 36,8 %, у 13 % больных может развиться острая печеночная недостаточность, а 5,5 % погибают от заболеваний печени. Особенно высока вероятность реактивации HBV-инфекции при длительной иммуносупрессии и использовании при иммуносупрессии или химиотерапии глюкокортикостероидов и ритуксимаба [1–3].
Признаки реактивации HBV-инфекции
Реактивация HBV-инфекции оценивается по ряду признаков. Это, во-первых, развитие гепатита с повышением уровня HBV ДНК в сыворотке крови более чем на 1 log10 копий/мл от исходного уровня, во-вторых, абсолютное увеличение вирусной нагрузки свыше 6 log10 копий/мл или конверсия HBV ДНК в сыворотке крови из отрицательной в положительную.
На 2-й стадии реактивации происходит восстановление иммунной системы после отмены химиотерапии и наступает разрушение гепатоцитов, инфицированных HBV. Нарастает уровень АЛТ в сыворотке крови, в ткани печени у большинства больных развиваются массивные некрозы, которые сопровождаются выраженной желтухой и признаками декомпенсации заболевания печени. Реактивация HBV-инфекции протекает в виде острого вирусного или даже фульминантного гепатита с классическими признаками, включающими слабость, анорексию, желтуху, асцит и коагулопатию. Могут появиться признаки печеночной энцефалопатии, печеночно-клеточной недостаточности, не исключен летальный исход. У некоторых больных на короткий период времени может снизиться уровень HBV ДНК в сыворотке крови. У отдельных больных клиническая картина реактивации HBV-инфекции проявляется рецидивом активности хронического гепатита В с повышением активности АЛТ не менее чем в 3 раза от исходного уровня, что фиксируется при повторном исследовании с интервалом в 5 дней. У части больных реактивация HBV-инфекции может протекать бессимптомно с повышением уровня HBV ДНК в сыворотке крови, но при отсутствии клиники острого гепатита.
На 3-й стадии реактивации наступает реконвалесценция, отмечается клиническое разрешение гепатита и возврат к исходным маркерам HBV. У больных с тяжелым течением 2-й стадии реактивации HBV-инфекции реконвалесценция может не наступить, у них проявляются клиника хронического гепатита В и нарушение печеночно-клеточной функции [4].
Для верификации реактивации HBV-инфекции необходимо исключить другие причины гепатита, в том числе суперинфекцию другими вирусами (например, острого гепатита А, гепатита дельта, цитомегаловируса, вирусов простого герпеса, опоясывающего герпеса, Эпштейна-Барр или аденовируса), лекарственное поражение печени, синдром обструкции синусоидов, обусловленный применением ряда химиотерапевтических препаратов, реакцию отторжения трансплантата и наличие прямого опухолевого поражения печени. Прерывание противоопухолевой химиотерапии вследствие реактивации HBV-инфекции снижает общую выживаемость больных [4, 5].
Следует отметить, что реактивация HBV-инфекции отмечается у больных хроническим HBeAg-положительным или HBeAg-отрицательным гепатитом В, а также на стадии неактивного носительства HBsAg – самой частой формы хронической HBV-инфекции (обнаруживается у 60–70 % лиц с HBsAg в крови). Для нее характерны:
– стойко нормальный уровень трансаминаз в сыворотке крови;
– отсутствие HBeAg и наличие HBeAb в сыворотке крови;
– низкая репликативная активность вируса с уровнем HBV ДНК в сыворотке крови менее 2000 МЕ/мл (менее 10 000 копий/мл);
– минимальные признаки активности печеночного процесса по данным морфологического исследования (индекс гистологической активности менее 6 баллов по шкале Knodell или Ishak).
Данная категория больных имеет относительно благоприятный прогноз (очень низкий риск прогрессирования заболевания, развития цирроза печени, гепатоцеллюлярной карциномы и печеночной летальности) и не нуждается в противовирусной терапии. Стойко нормальный уровень АЛТ в течение длительного периода и низкая вирусная нагрузка снижают настороженность врача в отношении данных больных, однако под влиянием экзогенной иммуносупрессии, химиотерапии, лечения стероидами и биологическими препаратами, злоупотребления алкоголем возможна реактивация вируса и развитие острого гепатита тяжелого течения с осложнениями.
Вирусологическая и клиническая реактивация латентной HBV-инфекции отмечена при ряде клинических состояний (злокачественные гематологические заболевания, ВИЧ-инфекция, трансплантация костного мозга и органов и др.). Появление новых лекарственных препаратов иммуносупрессивного действия, таких как моноклональные антитела к CD20 (ритуксимаб), CD52 (алемтузумаб), ФНО-альфа (инфликсимаб), широко применяемых при различных заболеваниях, также несет повышенный риск реактивации скрытой HBV-инфекции с развитием острого гепатита [11–13].
Факторы риска реактивации HBV-инфекции
Факторы риска реактивации HBV-инфекции определяются вариантом злокачественного заболевания и, особенно, проводимой иммуносупрессивной терапией. Наиболее высокому риску подвержены больные с лимфомой, однако имеются данные о возрастающем риске реактивации среди больных с солидными опухолями. Так, реактивация HBV-инфекции в период химиотерапии отмечена у 41–56 % больных раком легкого с маркерами HBV [14, 15], а также у 36 % больных с гепатоцеллюлярной карциномой, получающих системную химиотерапию. Противоречивы данные о реактивации инфекции после химиоэмболизации гепатоцеллюлярной карциномы [16, 17]. Ряд факторов, в первую очередь уровень вирусной нагрузки, также определяет серьезный риск реактивации. Среди 137 больных реактивация HBV-инфекции чаще отмечалась среди HBsAg-положительных пациентов с определяемой HBV ДНК в сыворотке крови до трансплантации костного мозга по сравнению с больными с неопределяемой HBV ДНК. Показано также, что вирусная нагрузка с уровнем HBV ДНК более 10 5 копий/мл является важным фактором риска реактивации [18]. Среди других факторов риска выделяют мужской пол, возраст (от 20 до 64 лет), наличие HBeAg в сыворотке крови, использование кортикостероидов и ряда химиотерапевтических препаратов (антрациклины, циклофосфан), моноклональных антител (ритуксимаб, алемтузумаб) в монотерапии или в комбинации с другими иммунодепрессантами. По данным литературы, 39 % наблюдений реактивации HBV-инфекции были отмечены у больных, леченных ритуксимабом, летальность вследствие печеночной недостаточности составила 52 % [19]. Более того, отмечена реактивация латентной HBV-инфекции (HBsAg-отрицательные, HBcAb-положительные больные) при лечении ритуксимабом [20].
Таким образом, отсутствие превентивного противовирусного лечения у больного с неактивным носительством HBsAg при достижении значительной вирусной нагрузки (более 10 9 копий/мл) в результате химиотерапии с использованием кортикостероидов и циклофосфана обусловили развитие тяжелого поражения печени с признаками острого вирусного гепатита и печеночно-клеточной недостаточности. Медленная динамика уровня трансаминаз и виремии при противовирусной терапии явилась показанием к длительной (2 года) терапии нуклеозидными аналогами, которые обеспечили подавление репликации вируса и восстановление синтетической функции печени.
Частота реактивации HBV-инфекции у неактивных носителей HBsAg при проведении химиотерапии составляет, по данным разных исследователей, от 14 до 72 %. Смертность в этой группе больных может достигать 5–52 %. Возможным объяснением широкой вариабельности показателей могут служить различия в популяции больных, вариантах опухолевых заболеваний, режимах химиотерапии и определении статуса реактивации [4].
Более тяжелое течение реактивации HBV-инфекции при иммуносупрессии В-клеточной лимфомы отмечается у больных хроническим гепатитом В с определяемой HBV ДНК в сыворотке крови до химиотерапии.
Таким образом, реактивация HBV-инфекции с нарастанием уровня виремии свыше 10 7 МЕ/мл у молодой больной, получавшей ламивудин только в период химио- и лучевой терапии, развилась через 2,5 мес после лечения. Клиническая картина холестатического варианта хронического гепатита В фульминантного течения с тяжелой печеночно-клеточной недостаточностью и печеночной энцефалопатии появилась позже, через месяц. Противовирусная терапия ламивудином и интенсивная симптоматическая терапия позволили изменить прогноз заболевания и восстановить синтетическую функцию печени, однако, при наличии лечения ламивудином в прошлом и в период реактивации HBV - инфекции, быстро развилась резистентность к проводимой терапии. Препаратом выбора для дальнейшей терапии в данном случае является энтекавир.
Профилактика и лечение реактивации HBV-инфекции
Первым шагом в профилактике реактивации HBV-инфекции является скрининг на маркеры HBV всех больных перед химиотерапией, особенно больных групп повышенного риска: жителей эндемичных по гепатиту В регионов (где HBsAg встречается более чем в 2 % популяции); родившихся в регионах с распространенностью HBsAg ? 8 %; употреблявших в прошлом наркотики; находившихся на гемодиализе; ВИЧ-инфицированных; гомосексуалистов [22]. Так как не всегда удается уточнить группу риска по гепатиту В, необходимо исходить из правила, что все больные, получающие иммуносупрессивное лечение, должны быть обследованы на маркеры HBV. Данное рутинное обследование рекомендовано в США с 2008 г. и касается больных с любыми опухолевыми заболеваниями, которым планируется проведение иммуносупрессивной и химиотерапии, и тех, кто уже получает такое лечение, особенно если оно включает ритуксимаб. Скрининг включает исследование HBsAg и HBcAb. Больные, у которых выявлен HBsAg, должны быть дополнительно обследованы на наличие HBeAg, HBeAb и уровень HBV ДНК. HBsAg-отрицательных больных, у которых в сыворотке крови обнаружат HBcAb, необходимо обязательно обследовать на наличие HBsAb. При отсутствии HBsAb в сыворотке крови следующим шагом является выявление HBV ДНК, так как у этих больных отсутствует иммунитет против HBV и возможно наличие латентной инфекции HBV.
Противовирусные препараты в лечении реактивации HBV
Профилактика реактивации у HBsAg-положительных больных должна начинаться как можно раньше до начала иммуносупрессии опухоли. При высокой (HBV – ДНК сыворотки более 2000 МЕ/мл) вирусной нагрузке и повышении уровня АЛТ терапию необходимо начинать незамедлительно! Среди применяемых в лечении ХГВ нуклеоз(т)идных аналогов (ламивудин, телбивудин, адефовир, энтекавир, тенофовир) ламивудин имеет наибольшую длительность (с 2000 года) и опыт применения. Ламивудин – нуклеозидный аналог (2',3'-дидезокси-3'-тиацитидина), блокирует полимеразу HBV, характеризуется хорошим профилем эффективности, отсутствием нежелательных явлений и имеет хорошие результаты лечения как при гематологических, так и при солидных опухолях. В исследовании G.K. Lau и соавт. [23] 30 больных с лимфомой и HBsAg в сыворотке крови были рандомизированы в 2 группы: в 1-й пациенты получали ламивудин в дозе 100 мг/сутки за 1 нед до начала химиотерапии, во 2-й прием нуклеозидного аналога назначали при наличии серологических признаков развившейся реактивации HBV. В 1-й группе виремия не появилась ни у одного больного, в то время как во 2-й группе реактивация HBV-инфекции наступила у 53 % пациентов (р=0,002). В другом рандомизированном исследовании [24], включавшем 43 больных с неходжкинской лимфомой, положительных по HBsAg, выявлен значительно более низкий риск реактивации HBV у пациентов, принимавших ламивудин профилактически перед или в 1-й день химиотерапии по сравнению с теми, кому препарат назначали при нарастании уровня АЛТ в сыворотке крови (11,5 и 56 % соответственно; р=0,001)). Результаты мета-анализа 14 клинических исследований, который включал 214 больных, принимавших ламивудин, и 399 пациентов группы контроля, показали, что предварительное лечение ламивудином HBsAg-положительных больных, получающих химиотерапию, способно в значительной степени снизить риск реактивации HBV-инфекции и фатального прогноза у ряда больных (см. таблицу). Сделано заключение, что профилактическое назначение ламивудина позволяет предотвратить 1 летальный исход на каждые 15 больных, получающих иммуносупрессивную терапию [25, 26].
Таблица. Частота реактивации HBV-инфекции (в %) на фоне иммуносупрессивной терапии HBsAg-положительных больных, получавших и не получавших ламивудин
Осложнения химиотерапии
Больные, получающие ламивудин (n=214)
Контрольная группа ((n=399)
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Последние десятилетия ознаменовались огромным прогрессом как в диагностике, так и в создании новых препаратов для лечения хронического гепатита В (ХГВ), в частности аналогов нуклеозидов (АН). Однако остается много вопросов по их применению: как долго лечить, каков риск возникновения резистентности при длительной терапии, каковы критерии отмены АН без вероятности реактивации ХГВ, влияет ли терапия на предотвращение цирроза печени и гепатоцеллюлярной карциномы?
В статье представлен клинический случай ХГВ без дельта-агента, фаза 2 (HbeAg+), с высокой биохимической и вирусной нагрузкой, фиброзом 2 стадии. Больная получала в течение 10 лет аналог нуклеозида, активность печеночных ферментов на фоне его приема быстро нормализовалась и была стабильной. После самостоятельной отмены АН произошла реактивация ХГВ. При назначении тенофовира активность АЛТ нормализовалась, вирусная нагрузка уменьшилась на 2 log — до 1,45×10 4 МЕ/мл и держится в этих пределах.
Приведенный клинический случай показывает, что пациенты с ХГВ должны постоянно принимать АН, чтобы остановить прогрессирование и трансформацию заболевания в цирроз печени или гепатоцеллюлярную карциному. Остаются актуальными выявление маркеров, которые позволят определить возможность отмены АН, и разработка новых препаратов, воздействующих на ДНК вируса, чем сейчас и занимаются многие исследователи.
Ключевые слова: хронический гепатит В, лечение, аналоги нуклеозидов, реактивация HBV.
Для цитирования: Макашова В.В., Омарова Х.Г. Реактивация хронического гепатита В после отмены терапии. РМЖ. 2019;10:50-52.
Chronic hepatitis B reactivation after treatment discontinuation
V.V. Makashova 1,2 , Kh.G. Omarova 1
1 Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow
2 Infectious Clinical Hospital No. 2, Moscow
The last decades have witnessed dramatic progress both in the diagnosis and development of novel drugs for chronic hepatitis B, in particular, nucleoside analogues. However, many aspects are still challenging, i.e., treatment duration, the risk of resistance in long-term treatment, criteria for drug discontinuation without any risk of chronic hepatitis B reactivation, the effect on the prevention of liver cirrhosis and hepatocellular carcinoma etc.
The paper addresses case history of chronic hepatitis B without delta agent, phase 2 (HbeAg+), characterized by high biochemical marker levels, high viral load, and liver fibrosis stage 2. This woman has received nucleoside analogue for 10 years. Liver enzyme levels have returned to normal quickly and were stable. However, after discontinuing the treatment, hepatitis B reactivation has occurred. The patient was prescribed with tenofovir. ALT has re turned to normal levels, viral load has reduced by 2 logs (to 1.45×10 4 IU/ml) and was stable.
This case history demonstrates that patients should not discontinue the treatment with nucleoside analogues to prevent disease progression and its transformation to liver cirrhosis and hepatocellular carcinoma. Identification of markers to assess the possibility of nucleoside analogue discontinuation and the development of novel drugs targeting viral DNA are still important.
Keywords: chronic hepatitis B, treatment, nucleoside analogues, hepatitis B reactivation.
For citation: Makashova V.V., Omarova Kh.G. Chronic hepatitis B reactivation after treatment discontinuation. RMJ. 2019;10:50–52.
Статья посвящена проблеме реактивации хронического гепатита В после отмены терапии. Представлен клинический случай хронического гепатита В без дельта-агента, фаза 2, с высокой биохимической и вирусной нагрузкой, фиброзом 2 стадии
Вирусный гепатит В (ВГВ) представляет собой важную проблему здравоохранения во всем мире в связи с широкой распространенностью (350 млн носителей ВГВ) и высоким риском развития цирроза печени (ЦП) и гепатоцеллюлярной карциномы (ГЦК). В мире каждый год ВГВ заболевают около 50 млн человек, а умирают от него около 650 тыс. человек в год [1]. С 1999 по 2013 г. количество летальных исходов, связанных с ЦП и ГЦК в исходе хронического гепатита В (ХГВ), увеличилось на 33% [2]. В России приблизительно 3 млн носителей ВГВ и больных ХГВ [3].
Последние десятилетия ознаменовались огромным прогрессом как в диагностике, так и в создании новых препаратов для лечения ХГВ, в частности аналогов нуклеозидов (АН). Однако остается много вопросов по их применению: как долго лечить, каков риск возникновения резистентности при длительной терапии, каковы критерии отмены АН без вероятности реактивации ХГВ, влияет ли терапия на предотвращение ЦП и ГЦК — все это предстоит выяснить в ближайшее время.
В связи с этим представляется крайне важным рассмотреть клинический случай реактивации ХГВ у молодой женщины.
Пациентка К., 28 лет, обратилась в июле 2008 г. с жалобами на слабость, быструю утомляемость, сонливость в первой половине дня, снижение аппетита, периодическую тошноту, головные боли, нечастое повышение АД до 135/100 мм рт. ст.
Анамнез заболевания. В феврале — марте 2008 г. после сильного стресса стала беспокоить сильная слабость. Обратилась к врачу. Выявлено повышение печеночных ферментов в 2–3 раза, наличие HbsAg. При дополнительном обследовании выявлена ДНК HBV — 6,8×10 8 МЕ/мл.
Эпиданамнез. Удаляла зубы 1,5 года назад. У мужа однократно обнаруживали HbsAg, при повторном обследовании HbsAg не обнаружен.
Перенесенные заболевания. В детстве до 5 лет — корь, краснуха, ветряная оспа. Цистит с 21 года, пиелонефрит, кольпит после вторых родов, аутоиммунный тиреоидит.
Аллергоанамнез: не отягощен.
Наследственность: у бабушки по отцу — рак желудка, у матери — хронический пиелонефрит.
Объективно по результатам осмотра. Кожные покровы и видимые слизистые обычной окраски, чистые. Вторичных печеночных знаков нет. Печень пальпируется на 1,0–1,5 см ниже реберной дуги, селезенка не пальпируется. Рост 162 см, вес 53 кг.
Вредные привычки: не курит, алкоголь не употребляет.
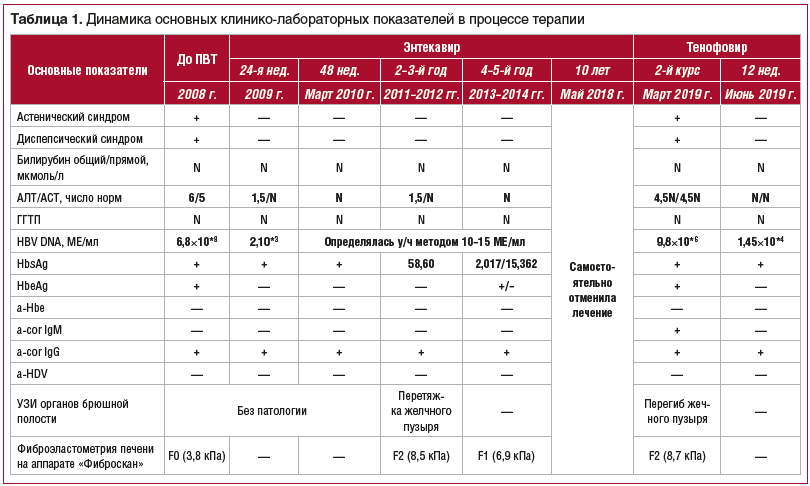
Динамика основных показателей общего и биохимического анализов крови, данные ПЦР-диагностики, УЗИ органов брюшной полости и фиброэластометрии представлены в таблице 1.
Пациентке было проведено обследование на гормоны щитовидной железы: Т4 свободный, ТТГ, АТ ТПО, АТ ТГ — все в пределах нормы. УЗИ щитовидной железы.
Заключение: Диффузные изменения тиреоидной ткани по типу аутоиммунного тиреоидита; фокальные изменения по типу коллоидных в левой доле (в центральной части левой доли визуализируется 2 фокальных образования округлой формы, гипоэхогенные, 2,3×4,5, без повышения кровотока).
Для решения вопроса о назначении противовирусной терапии (ПВТ), в частности интерферонотерапии, было проведено тестирование по госпитальной шкале тревоги и депрессии (HADS). Результат: 24 балла (в норме: до 11 баллов), что свидетельствовало о выраженном психоэмоциональном напряжении.
На основании вышеуказанных данных был поставлен диагноз: Хронический гепатит В (HbeAg позитивный), без дельта-агента, фаза 2 (высокая биохимическая и вирусная нагрузка). Сопутствующие диагнозы: аутоиммунный эутиреоидный тиреоидит; хронический пиелонефрит в стадии ремиссии; психовегетативный синдром.
В связи с последним сопутствующим диагнозом препараты интерферонов противопоказаны. Назначен аналог нуклеозида — энтекавир (0,5 мг/сут) длительно. С пациенткой была проведена подробная беседа о необходимости ежедневного приема препарата (без пропусков), своевременной сдачи анализов крови для контроля активности инфекционного процесса и коррекции терапии. Помимо ПВТ рекомендован прием следующих лекарственных средств: адеметионин в течение 1 мес., урсодезоксихолевая кислота 1 капс. (250 мг) × 2 р./день в течение 3 мес. Получено согласие на лечение и обследование.
Через 24 нед. приема энтекавира исчезли жалобы (см. табл. 1), активность АЛТ значительно снизилась — до 1,5 нормы, активность АСТ нормализовалась, уровень ДНК HBV уменьшился до 2,10* 3 МЕ/мл, HbeAg перестал определяться, но а-Hbe не появились, т. е. сероконверсии не произошло. На фоне ПВТ через 48 нед. (1 год) активность печеночных ферментов полностью нормализовалась, ДНК вируса гепатита В (ВГВ) определялась только ультрачувствительным методом (чувствительность 10–15 МЕ/мл). Однако сероконверсия HbeAg на а-Hbe не зафиксирована. Аналогичная клинико-лабораторная характеристика наблюдалась в течение 5 лет. Необходимо заметить, что периодически отмечалось повышение активности АЛТ до 1,5 нормы, титр HbsAg колебался от 58,960 до 2,017 МЕ/мл и вновь повышался до 15,362 МЕ/мл, фиброз печени, несмотря на противовирусную терапию в течение 2011–2013 гг., фиксировался на стадии F2, но к 5-му году лечения уменьшился до F1 (см. табл. 1).
В последующие 5 лет пациентка не наблюдалась (живет в другом городе). В марте 2019 г. по телефону с большой обеспокоенностью сообщила, что год назад (в мае 2018 г.) самостоятельно прекратила прием энтекавира, т. к. жалоб не было и они с мужем решили завести еще одного ребенка (двое детей у семейной пары уже есть). Дети и муж обследованы: маркеры ВГВ не обнаружены. Анализы не сдавала, а при сдаче в марте 2019 г. вновь обнаружено повышение активности АЛТ и АСТ в 4,5 раза, вирусная нагрузка — 9,8×10* 6 МЕ/мл, вновь появился HbeAg при отсутствии а-Hbe, фиброз печени — F2. Все эти данные свидетельствовали об активности патологического процесса: ХГВ, фаза 2. Назначен тенофовир 300 мг ежедневно постоянно. Повторно проведена беседа о необходимости постоянного приема. Объяснено, что в настоящее время гепатит излечить полностью невозможно, поэтому для подавления размножения ВГВ необходимо принимать противовирусный препарат. Через 12 нед. ПВТ активность ферментов нормализовалась (см. табл. 1), уровень ДНК ВГВ уменьшился на 2 логарифма, HbeAg перестал определяться, но без сероконверсии, a-cor, пробы на IgM стали отрицательными. Это свидетельствует о положительном результате лечения АН. Однако важно подчеркнуть, что эффективность терапии будет целиком зависеть от комплаентности пациентки.
Заключение
Лечение ХГВ остается сложной проблемой в связи с невозможностью полностью подавить вирусную репликацию, т. к. ДНК ВГВ внедрена в геном человека. Терапия интерфероном обладает огромным количеством побочных действий, многим больным она противопоказана, а эффективность ее очень мала (15–30%). Пациенты должны постоянно принимать АН, чтобы остановить прогрессирование и трансформацию заболевания в ЦП или ГЦК.
Поэтому в настоящее время основными целями, стоящими перед медицинским сообществом, являются: 1) выявление маркеров, которые позволят определить возможность отмены АН; 2) разработка и исследование новых препаратов, воздействующих на ДНК ВГВ. Исследования в этой области продолжаются.
Всем привет. Не очень хотела писать пост о том как Я болею этой заразой. Но возможно эта статья поможет людям, которые тоже столкнулись с хронически течением заболевания. Попытаюсь изложить, как нужно Себя вести и что делать. Главное не отчаиваться, набраться терпения, запастись успокоительными, и бороться. Итак немного общей информации. Из годового опыта поняла, что тема о Вирусе Эпштейна Барра очень болезненная для многих. А так же мало изученная и протекающая хоть и с основными симптомами у всех, но все равно имеет индивидуальное течение для каждого человека. Итак. Вирус Эпштейна Барра имеется у 90 процентов населения всей земли. В основном им болеют по типу простого ОРВИ. Вирус имеет два основных вида диагностики IgG и IgM. По утверждению медицинского сообщества при выявлении титров IgG и отсутствия IgM лечение не требуется. При показателях где увеличен титр IgM требуется лечение противовирусными препаратами, такими как ацикловир, валвир, и ганцикловир(при запущенных случаях) При высоких показателях IgM человек болеет Инфекционным Мононуклеозом. Для подтверждения диагноза так же часто направляют на сдачу анализов крови на атипичные момонуклеары. При их обнаружении диагноз подтверждается на 100 %. Это основная и самая известная схема диагностики заболевания. Обычно заболевание проходит достаточно быстро и без особых осложнений при грамотно лечении. Лечение занимаются такие врачи как инфекционист, имунолог, Лор врач. Основные симптомы инфекционного мононуклеоза. Температура от 37.5 до 40 градусов. Воспаленные лимфотические узлы, боль в горле. Не редко увеличение лимфатические узлов в других областях тела, увеличение печени, и селезенки.
Но бывают случаи, когда люди страдают от ВЭБ инфекции при отрицательных титрах ImM при наличии только завышенных показателей IgG. Такое течении называется хроническим, об этом и поговорим. Основные симптомы у хронического течения, воспаление шейных лимфотических узлов, завышенные показатели лимфоцитов в крови, субфебрилитет 37-37.5. Боли в горле, усталость, ломота в мышцах, стоматит. Боли в правом подреберье. В официальных источниках лечение кроме основного курса ацикловира не назначается. К ним добавляются имуномодуляторы, такие как изопринозин. Хронической ВЭБ инфекцией люди болеют годами. Потому как этот вирус коварный, постоянно мутирует. Благодаря чему иммунитет не может самостоятельно с ним справится, и выздоровление в таком случае затягивается на очень продолжительное время.
Помимо болевых ощущений которые доставляют немалый дискомфорт, присутствует нагрузка на нервную систему, это особенность вируса, он угнетает ЦНС и ЦВС. Люди сталкиваются с психологическими трудностями примерно через пол года болезни. Возникают дипрессии, подавленность, усталость как психологическая так и физическая. Страх онко патологии. Так как активно обсуждается, что ВЭБ инвекция является прародителем многих онкологических заболеваний. Но изучив множество информации и консультировавшись с многими специалистами эта информация на данный момент не имеет 100 процентного подтверждения. Так как все зависит от индивидуальных особенностей организма, наследственности и множество других факторов. Проще говоря возможно, но не факт)
Сразу скажу, что люди болеющие хронической ВЭБ сталкиваются с большими трудностями в оказании помощи при лечении, так как повторюсь, официально медицина подтверждает факт того, что ВЭБ очень сильно усложняет жизнь, и люди без при увеличения страдают, но лечения как такового нет. Всё сводится к повышению иммунитета больного, устранения болевых симптомов. Остаётся только ждать когда Ваш собственный иммунитет, обхетрит эту заразу и сможет дать Ей в жбан и отправить на боковую на долгое время. Такой период называется ремиссией. При наступлении ремиссию нужно поддерживать организм минералами и витаминами. Физической активностью, что бы не допустить рецидивов.
Как я уже писала выше, ВЭБ сильно играет на нервах, и это Его основной козырь, потому как тяжёлое психологическое состояние помогает инфекции надолго обосноваться в организме, подавляя тем самым иммунитет, перевезти вещи и паразитировать на качестве вашей жизни. Основным рычагом в запуске дисбаланс в психологическом состоянии является страх онкологии.
Как только Вы поймате себя на мысли, что устали, то должны молниеносно среагировать, это тот период когда Вы должны любыми способами поддерживать Свое стабильно позитивное состояние. Пейте успокоительное, много спите, не волнуйтесь. Как бы это не звучало для некоторых, запишитесь к психологу. Лучше сделать это заранее, поверьте поможет. Многие сталкиваются с непониманием врачей из за сильной озабоченностью своим здоровьем, опираясь только на наличие титров IgG и отсутствии IgM. Они не видят смысла что либо делать. Ссылая все Ваши недуги только на психическое состояние. Соберитесь, вы не одни.
Запишитесь на приём к онкологу. Стабильно наблюдайтесь, убивая тем самым двух зайцев, свой страх онкологии, и в случае чего обнаружении Её на ранних стадиях.
Если Вы уже полностью обследовались и врачи не нашли других причин для вашего самочувствия, то смеритесь с тем, что это оно. Если ещё не сделали этого, обследуйтесь полностью, помимо того, что Вы 100 % будете уверены в том, что критических патологий в других органах у Вас нет, это даст и психологическое спокойствие. Делайте это хотя бы раз в год. Я делаю раз в пол года.
Другая не маловажная проблема это горло и лимфоузлы которые постоянно болят. Повторюсь, большой аспект на выздоровление это психологический покой, делайте узи лимфоузлов раз в месяц. Не мерьте температуру каждые пол часа, запомните ВЭБ является примым источником возникновения тонзилита, который и даёт субфебрилитет. Наблюдайтесь у Лор врача, делайте предписанные указания(промывание, и. т. д) Обычно тонзилит из за ВЭБ определяется методом ПЦР (соскоб из ротоглотки), или анализом из слюнны. Может быть такое, что анализ из ротоглотки не выявит ни чего, не ВЭБ ни стафилокок, ни чего кроме обычных бактерии которые будут находится в пределах нормы. Но горло будет болеть с небольшой переодичностью. Это обусловливается тем, что ВЭБ находится в слюнной жидкости или лимфоузлах(миндалинах) что и вызывает болевой синдром и воспаление. Часто к ВЭБ накладываются и бактериальные неприятности, в таком случае нужна антибиотикотерапия прописанная Вашим врачем. Обычно при ВЭБ не назначают антибиотики пеницелинового ряда. Используют антибиотики разряда тетрациклинов, например Юнитокс Солютаб.
Часто бывает такое, что человек испытывает блуждающие боли. Это означает, что при улучшении при болях в горле начинают болеть лимфоузлы, при нормализации лимфоузлов, начинают болеть мышцы и суставы, или горло. Так сказать чередуется. С чем это связанно Я до сих пор не знаю. Может вирус выходит на прогулку, а может это реакция нервной системы. Некоторые удаляют гланды, на счёт показаний к удалению ни чего не могу сказать все индивидуально, если у Вас повторяющиеся ангины и стафилококк, то скорее всего надо, дабы не получить осложнения на другие органы. Если стафилокока нет, то удаление из за постоянного воспаления тоже показано, но не желательно. Потому как врачи не знают как это скажется на организме, если совсем станет не вмоготу, Я буду удалять на Свой страх и риск.
На данный момент, Я пролежала в больнице в инфекционном отделении из за усуглубления самочувствия. Мне ставили иммуномодуляторы. Очень помог имуноглобулин человеческий, лечили противовоспалительными препаратами в виде капельниц из за воспаленных лимфоузлов. Кстати сильные иммуномодуляторы используются в лечении очень редко, дабы не расслабить собственную иммунную систему, не советую с ними перебарщивать.
Так же залогом улучшения самочувствия является система ЖКТ.
ВЭБ бьёт и по ней, нужно постоянное поддержание правильной работы ЖКТ, так как 60 ‰ иммунитета как ни странно находится в желудке. Не допускать не правильного питания и дисбаланса.
Ну и самое главное Лимфосистема. Чистка лимфы должна быть регулярная. Я чищу Её при помощи трав и физ нагрузок, лимфодренажного массажа.
Стоматит. Не знаю как с Ним бороться, для устранения боли капаю витамин в12. Помогает. Не глотать! Воспаление языка пройдёт само как только это закончится.
Ниже приведу примерную схему лечения без названий. Потому как подбирать лечение нужно с арачем и бла бла бла.
1. В больничке(курс имуномодуляторов, противовоспалительных и антибиотиков)
2.Потом разного рода травы, в пакетах эхинацея, а так же трава для работы ЖКТ, мочевой системы, пью воды не менее двух литров в день.
3. Масла из трав и шишек. Если кому надо спрашивайте напишу.
4. 2 раза в неделю свечи с интерфероном
5. Витаминый комплекс.
6.Белковая пищща, много клетчатки. Исключаем сахар вообще, переходим на мед. Поймёте почему.
7.При болях в мышцах, терпим, мажем мази болеутоляющие. Проверяем я на всякий случай.
8.При стоматите B12. И не знаю почему, но Мне помогает лук, много лука, ешь со всем пока не пройдёт.
9. Повторюсь много воды, потому как бывает такое, что начинает чесаться тело, сыпь, или же руки. Не знаю почему у большинства хроников чешутся именно руки, ладошки. Вода нужна для вывода всякой дряни из организма, при зуде у Вас наверняка повышен катионный белок. Вода просто необходима, а так же антигистаминные типо супрастина.
10. Чистка лимфы, я пью траву из корня солодки, и в баню. С большим количеством употребления воды во время банных процедур. Правильная чистка лимфы в бане и информация о ней есть на ютубе, смотрите)
Сейчас Мне намного лучше, по крайней мере Я уже не Умираю) Есть просвет и с температурой)
Ну вот. Пока так. Надеюсь кому то поможет мой опыт длиною в год. А Я борюсь дальше. Пожелайте Мне удачи, и не отчаивайтесь.
Читайте также:


