Иммуноглобулин от лихорадки эбола
По данным Минздрава Демократической Республики Конго, на начало декабря этого года в стране зарегистрировано 3201 подтвержденных случаев заболевания лихорадкой Эбола, 2209 заболевших умерли.
Сергей Нетёсов, доктор биологических наук, профессор, заведующий лабораторией биотехнологии и вирусологии факультета естественных наук Новосибирского государственного университета, член-корреспондент РАН
Африканский вирус оказался более актуальным, чем российские
Возбудитель лихорадки — вирус Эбола — впервые был обнаружен в 1976 году во время вспышки болезни в районе реки Эбола, протекающей между тогдашним Заиром (ныне Демократическая Республика Конго) и Суданом.
Если рассмотреть хронику создания вакцины против вируса Эбола и современное состояние дел в этой области в мире и в России, то становится понятным, как это поможет всем нам.
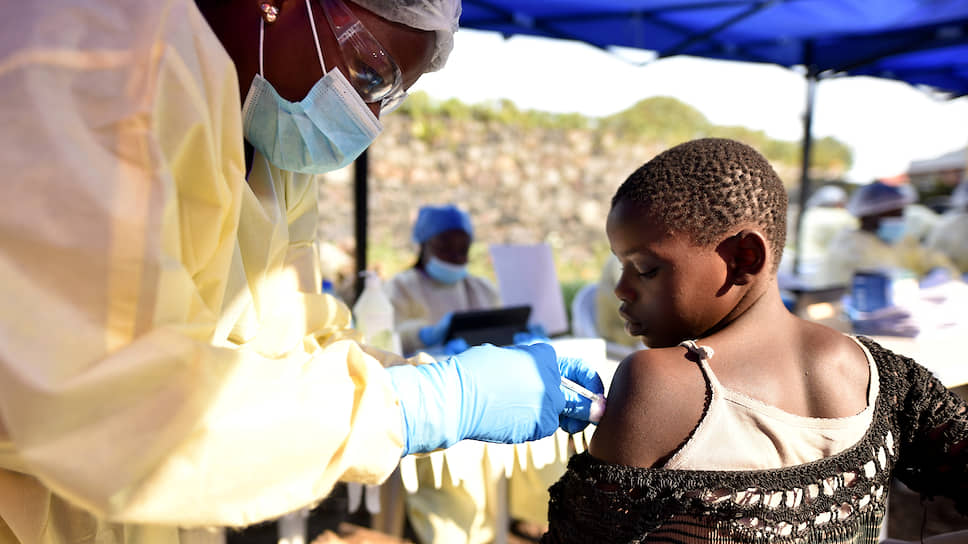
Вирус Эбола был впервые идентифицирован в 1976 году во время крупной вспышки вызванного им заболевания в Судане и тогдашнем Заире (теперь Демократическая Республика Конго; ДРК). Поскольку такие вспышки позднее случались не каждый год и их охват в несколько последующих лет был намного меньше, то ученые ограничились в те времена лишь разработкой иммуноферментных диагностикумов на ее маркеры.
Правда, основные фундаментальные исследования были проведены, в том числе секвенирование генома этого возбудителя, причем российские ученые здесь были одними из первых, включая вашего покорного слугу.
В 1990-е, а особенно в 2000-е годы масштаб и число вспышек заметно увеличились, и некоторые лаборатории в США и Канаде начали разработки и вакцинных препаратов, и средств лечения, а также диагностикумов нового типа на основе полимеразной цепной реакции. Однако для проведения полного цикла доклинических испытаний вакцинных препаратов необходимы весьма значительные средства, а с учетом особой опасности этой инфекции значительную часть таких работ необходимо проводить в лабораториях высшего, четвертого уровня биобезопасности. Ввиду этих причин полного цикла доклинических исследований перспективных, кандидатных, как говорят специалисты, вакцин против Эбола-вирусной инфекции до 2014 года так и не было завершено ни в одной из лабораторий мира.
По самым последним данным, природным резервуаром вируса Эбола вернее всего являются фруктоядные летучие мыши. Три вида таких мышей (Hypsignathus monstrosus, Epomops franqueti и Myonycteris torquata) могут быть носителями вируса без признаков заболевания. Из 24 видов растений и 19 видов позвоночных, экспериментально зараженных вирусом Эбола, удалось заразить только летучих мышей. Причем они не заболели, а просто несли в себе вирус в течение долгого времени. В обследовании в 2002–2003 годах 1030 животных, включая 679 летучих мышей из Габона и Республики Конго, только 13 фруктоядных мышей несли этот вирус. Кроме того, фрагменты вируса Эбола выделяли из тканей некоторых умерших западноафриканских равнинных горилл и центральноафриканских шимпанзе, которые иногда питаются фруктоядными летучими мышами. Что еще более важно, фрагменты РНК вируса Эбола были выявлены у клинически здоровых летучих мышей разных видов. Это означало, что летучие мыши могут быть носителями вируса без признаков заболевания, то есть хроническими носителями. А это и есть главное условие поддержания циркуляции вируса Эбола в природе.
Неожиданная по размаху, месту возникновения и продолжительности вспышка этого заболевания 2014 года в Гвинее, Сьерра-Леоне и Либерии сдвинула ситуацию с места. И уже в конце 2015 года несколько лабораторий и научно-исследовательских институтов в США, Канаде и некоторых других странах объявили о завершении доклинических испытаний нескольких кандидатных, вакцинных препаратов.
О создании прототипной вакцины объявили и у нас в России. Первыми были публикации группы ученых из НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи Министерства здравоохранения России о разработке живой вакцины на основе рекомбинантного аденовируса. Однако к этому времени и сама вспышка закончилась, так что испытывать эти вакцины в полевых условиях реальной эпидемии стало негде.
В том же 2018 году, и опять неожиданно, началась вспышка Эбола-вирусной инфекции в ДРК. Как оказалось, один из вакцинных препаратов, разработанный на основе рекомбинантного живого вируса везикулярного стоматита, прошел к этому времени ограниченные клинические испытания в США.
От человека к человеку вирус передается при попадании вируссодержащих жидкостей от больных людей или инфицированных животных на слизистые оболочки или на микротравмы на коже. У больных и умерших концентрация этого вируса в крови и на слизистых оболочках необычайно велика и достигает 10 млн вирусных частиц на 1 мл. Поэтому близкое общение с больным с большой вероятностью приводит к заражению. Наконец, уже выздоровевший человек может нести в себе вирус (в семени мужчин, в грудном молоке женщин) до одного года после выздоровления.
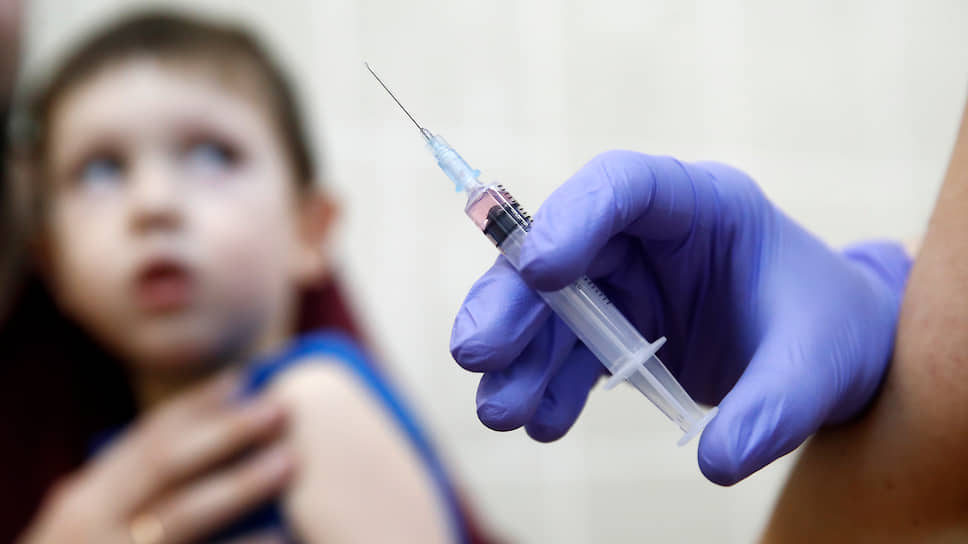
Фото: Артем Геодакян / ТАСС
Производит сейчас этот препарат под названием Ervebo всемирно известный фармгигант MSD (Merck, Sharp and Dohme). Вследствие этого Всемирная организация здравоохранения совместно с правительством ДРК приняли решение о начале клинических испытаний данной вакцины прямо в очаге инфекции.
В настоящее время выявлено пять таксономических видов вируса Эбола, которые отличаются друг от друга процентом летальности. Штаммы вида Заир, которые и циркулируют сейчас в Демократической Республике Конго, самые опасные — со смертностью до 80%.
К настоящему времени, по данным сайта promedmail.org, этой вакциной привито уже более 250 тыс. человек из числа контактных лиц. По имеющимся данным, ни один из вакцинированных не заболел. Однако вспышку пока остановить не удалось, поскольку она развивается в зоне военного межплеменного конфликта, и даже просто находиться там опасно: были случаи убийств местных и иностранных врачей, да и противодействие вакцинации части населения тоже имеет место.
Между тем американская же компания Johnson & Johnson довела до клинических испытаний другую, двухкомпонентную вакцину на основе рекомбинантных аденовируса и вируса осповакцины, производящих при инъекции в организм антигенно значимые белки вируса Эбола. И в середине ноября эта вакцина также была разрешена ВОЗ для проведения полевых испытаний в ДРК, которые в ноябре же и начались.
В России за последнее десятилетие не было ни одного больного эболавирусной инфекцией. В то же время за эти же годы у нас в стране были десятки тысяч больных другими, домашними вирусными инфекциями (ветряная оспа, ротавирус, респираторно-синцитиальный вирус, метапневмовирус, вирусы парагриппа и другие) и сотни умерших от них.
Может, пора вспомнить про эти патогены и начать, наконец, разработки и производство вакцин против них, гораздо более актуальных для России инфекций?
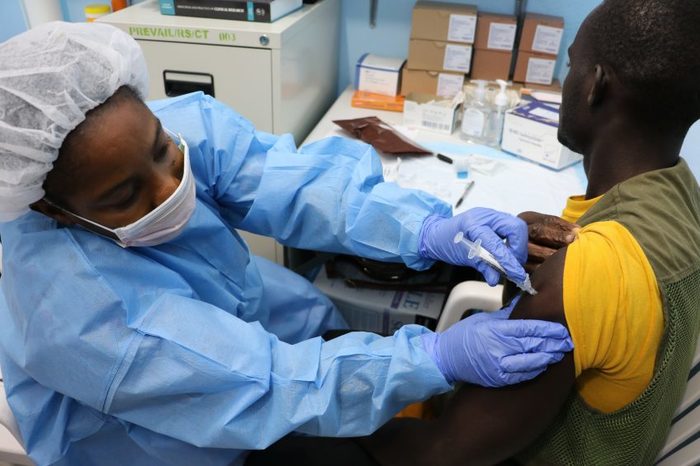
Регуляторные органы в Европе впервые в мире одобрили вакцину против лихорадки Эбола, и представители здравоохранения не тратят время на ее внедрение.
Нынешняя вспышка в ДРК убила почти 2200 человек с августа 2018 года, что привело к почти 3300 случаев заболевания. Вспышка является второй по величине зарегистрированной, опережает ее только вспышка в Западной Африке в 2014 году, которая привела к гибели более 11 000 человек и 28 000 случаев заражения.
Предварительные данные о вакцинах от текущей вспышки ДРК показали, что Ervebo на 97,5% эффективен в предотвращении разрушительного вирусного заболевания. Во время вспышки он защитил более 90 000 человек.
Вакцина защищает от одного из четырех видов лихорадки Эбола, которые, как известно, заражают людей, — от вируса Заира. Заир несет ответственность за текущую вспышку в ДРК, а также за вспышку в Западной Африке в 2014 году и почти все другие вспышки, зарегистрированные с момента обнаружения Эболы в 1976 году.
Первоначально вакцина была разработана исследователями из Агентства общественного здравоохранения Канадской национальной лаборатории микробиологии, которая впоследствии лицензировала ее для NewLink Genetics Corporation. Merck получила лицензию в 2014 году на фоне вспышки в Западной Африке и доработала ее.
Компания отпраздновала одобрение вакцины в понедельник.
Ожидается, что Управление по контролю за продуктами и лекарствами США примет решение об одобрении вакцины в марте 2020 года.
![]()
Предприятие готово к выпуску вакцины в размере 5 тыс. доз для стран Африки.
у нас же вроде разработали уже - и дешевле, и эффективнее
С них красть нечего

Это заговор фармацевтов вместо того чтобы залить напалмом всю Африку и выжечь эболу они свои вакцины впаривают несчастным неграм чтобы те не размножались

"начать новую игру"
"вирус"
"ебобола"
ждем новостей)
Врач Стэнли Плоткин, чья вакцина 1964 года отразила краснуху, работает над тем, чтобы победить новый коронавирус

![]()
В США начались испытания вакцины против COVID-19
В Сиэттле 45 здоровых добровольцев получили первую дозу экспериментальной вакцины от COVID-19. Через четыре недели им введут ещё одну. Препарат содержит матричную РНК коронавируса в липидной оболочке. Первая фаза клинических испытаний вакцины, созданной биотехнологической компанией Moderna совместно с Национальными институтами здравоохранения, призвана определить, безопасен ли этот препарат и вызывает ли нужный иммунный ответ. Предварительные результаты станут известны через три месяца, а окончательные — к июню 2021 года.
![]()
Влияет ли вакцинация против ВПЧ на фертильность?

Способность женщины к рождению здорового ребенка – чудо, достоинство, преимущество, да, как ни назови, - богатство практически любой женщины. Именно поэтому вопрос, может ли прививка от ВПЧ оказывать влияние на фертильность, волнует многих молодых девушек и их матерей в первую очередь. Причем только тех, кто следит за своим здоровьем, регулярно повышая свой уровень медицинской грамотности, остальные или не знают о ее существовании, или не задумываются о вероятности получения ВПЧ-инфекции.
Можно продолжать бесконечно… Так что же делать? Если верить всему, что написано, лично я вижу только один выход: не жить половой жизнью! Это, конечно же, шутка. Я сама мама и чуть позже, думаю, с нетерпением буду ждать от своего ребенка внуков! Поэтому давайте разбираться, будем ли мы с вами делать себе и своим дочерям прививку от ВПЧ?
Так что же, появилось еще больше сомнений?
В целом о вакцинации…
Анализируя сообщения в интернете, могу сказать, что сегодня люди настроены против любой профилактической прививки. Единичные случаи неблагоприятных исходов, не всегда имеющие прямую связь с перенесенной инъекцией, представлены кричащими, пугающими заголовками. Страшно читать об ужасных последствиях проведенных вакцинаций против АКДС, кори, полиомиелита… При этом вакцина от ВПЧ фигурирует в качестве виновника осложнений и неблагоприятных явлений намного реже, чем любая другая, что, возможно, связано с небольшим числом вакцинированных в нашей стране. Так что же теперь, не делать прививки вообще? Это добровольный выбор каждого, но, отмечу, что к родителям непривитых детей при устройстве в детский сад, школу, как правило, возникает намного больше вопросов. Политика государства ясна, прививкам – да! Отмечу, что большинство родителей за программу вакцинации, число непривитых детей в детских учреждениях в разы меньше.
Моя личная позиция
Своего ребенка прививаю согласно календарю профилактических прививок. В 3 месяца после вакцинации против дифтерии, коклюша, столбняка и гепатита В на фоне подъема температуры до 39 градусов, дочка выдала судорожный синдром. Страшно было так, что я и думать забыла о том, что я врач, превратилась в истеричную мамашу и измучила звонками педиатра. Да, понервничала, но я была предупреждена о возможной гипертермии. Инструкции были даны мне дежурным врачом и выполнены безукоризненно. Все обошлось, и далее мы выполняем программу без особых сложностей. У меня не сформировалось предвзятого отношения к вакцинации, во многом благодаря тому, что я была осведомлена о возможности осложнений и о тактике, которую необходимо предпринять в случае их возникновения.
В 70 странах мира прививка от ВПЧ включена в национальные программы вакцинации, что привело к снижению показателей заболеваемости и смертности от рака шейки матки. Как здравомыслящий человек, могу сказать одно, если бы риски вакцинации были велики, уверена, что от профилактики уже давно бы отказались. Остро стоит вопрос о включении вакцин от ВПЧ в национальный календарь прививок в России в связи с увеличением заболеваемости раком шейки матки. Всемирная организация здравоохранения и ведущие регуляторные организации настоятельно рекомендуют включение вакцинации против ВПЧ в национальные календари прививок всех стран мира.
Почему в России сегодня ситуация по раку шейки матки (казалось бы, визуальному, легко диагностируемому заболеванию), несмотря на достижения современной медицины, стала хуже, чем в СССР?
Во – первых, воспитание было иным. Понятно, что и в СССР секс был, но, позвольте, не в таких же количествах и разнообразии, как сегодня! И принять во внимание нужно тот факт, что не обязательно женщина должна быть крайне сексуально активной для высокой вероятности встречи с вирусом, вполне достаточно единственного незащищенного полового контакта с носителем ВПЧ.
В 60-х годах прошлого столетия в стране был организованный массовый скрининг. Существовала сеть цеховых, сельских и участковых врачей, велись активные работы по санитарному просвещению населения. Однако эффективная превентивная система здравоохранения была разрушена в 90-е годы.
Сегодня сократили большую часть фельдшерско-акушерских пунктов, катастрофически не хватает работников первичного звена системы здравоохранения, санитарно-просветительские работы вести некому. Вот и выходит, что осведомленность населения низкая. И несмотря на наличие в нашей стране бесплатного диспансерного наблюдения, далеко не все проходят программу диспансеризации. Уверена, что мои читатели к данной категории лиц не относятся.
Можно ли снизить заболеваемость, не прибегая к вакцинации?
В нашей стране уже реализовано 12 пилотных программ иммунизации с положительными результатами. Тяжелых побочных эффектов вакцинации, к которым и относятся бесплодие или смертельный исход, в Российской Федерации не наблюдалось.
А какие результаты вакцинации освещены в мире?
Подведем итоги вышеизложенному:
1. Прививка от ВПЧ не несет в себе больший риск, чем любая другая прививка, входящая в национальный календарь прививок.
2. Вероятность каких-либо нежелательных реакций – минимальная, но, к сожалению, она есть, как и после проведения любой другой прививки.
3. Вакцинация от ВПЧ в масштабах нашей страны – великое благо, которое однозначно приведет к снижению заболеваемости и смертности. Сейчас дела обстоят так: заболеваемость в РФ составляет 20 женщин на 100000, смертность – 9,6; в Швеции, где введена массовая вакцинация, данные показатели составляют 9,5 и 3,9 на 100000 женщин соответственно.
4. Решение о том, нужно ли делать прививку от ВПЧ, Вы принимаете самостоятельно. Мое дело, как врача, предоставить Вам информацию: польза перевешивает риски в сотни раз, опять – таки, как и при проведении любой другой прививки.
5. То, что Вы вакцинированы, не означает отсутствие необходимости посещения гинеколога: вакцина защищает не от всех типов вируса, и помимо плоскоклеточного рака, существует еще и аденокарцинома. Да и вообще, кроме шейки есть еще вульва, влагалище, матка и ее придатки.
А для тех, кто дочитал до конца и был терпелив, в качестве бонуса приведу свои скромные размышления о времени, когда лучше выполнить вакцинацию, и о том, как быть, если Вы боитесь ее больше, чем перспективы инфицирования.
Благополучным моментом вакцинации считаю время перед началом половой жизни. Единственное, для формирования стойкого иммунитета к вирусу необходим временной интервал в 6 – 12 месяцев. Поэтому данный подход оправдан только в случае, если
- у Вас доверительные отношения с ребенком,
- Вы являетесь для него авторитетом,
- подросток сознателен и терпелив.
Чаще бывает более печальный вариант: мама может не догадываться о том, что половой дебют уже произошел, а сегодня, когда молодые пациентки честно говорят, что половую жизнь начали в 13 лет, я уже и не удивляюсь. Поэтому, если Вы не уверены, что ребенок Вас посвятит в подробности своей личной жизни, то 13 лет, на мой взгляд, оправданный возраст.
Помните о цитологическом скрининге и ВПЧ - тестировании! Начало их должно быть привязано к половому дебюту. И, даже если у Вас один половой партнер, и Вы в нем уверены на все 100%, и чувствуете Вы себя замечательно, не игнорируйте ежегодные посещения гинеколога и цервикальный скрининг.
Конечно, хорошо, чтобы ничего не было найдено. Но, если уж найдено, помните, у ВПЧ есть право находиться в Вашем организме не более 2 лет, далее вероятность неблагоприятных последствий его присутствия возрастает в разы. Поэтому до 2 лет допустимо наблюдение со строгим цитологическим контролем и, возможно, биопсией, а далее – только активная тактика!

Лихорадка Эбола - особо опасная вирусная инфекция, вызываемая вирусом Эбола и протекающая с тяжелым геморрагическим синдромом. Начальные клинические признаки лихорадки Эбола включают высокую температуру и выраженную интоксикацию, катаральные явления; в период разгара присоединяются неукротимая рвота, диарея, боли в животе, геморрагии в виде кожных кровоизлияний, наружных и внутренних кровотечений. Специфическая диагностика лихорадки Эбола осуществляется с помощью вирусологических и серологических методов. Этиотропная терапия лихорадки Эбола не разработана; получен положительный эффект от введения больным плазмы реконвалесцентов. Патогенетические мероприятия направлены на борьбу с инфекционно-токсическим шоком, дегидратацией, геморрагическим синдромом.
Общие сведения
Лихорадка Эбола - высококонтагиозное вирусное заболевание из группы геморрагических лихорадок, характеризующееся крайне тяжелым течением и высокой летальностью. Впервые лихорадка Эбола заявила о себе в 1976 г., когда одновременно были зарегистрированы две вспышки инфекции в Судане и Заире (Конго). Свое название лихорадка получила в честь реки Эбола в Заире, где впервые был выделен вирус.
Последняя вспышка лихорадки Эбола в Западной Африке, начавшаяся в марте 2014 г., является самой массовой и тяжелой со времени обнаружения вируса. В течение этой эпидемии заболело и умерло людей больше, чем во все предыдущие годы. Кроме этого, впервые вирус пересек не только сухопутные, но и водные границы, оказавшись на территории Северной Америки и Европы. Летальность при эпидемических вспышках лихорадки Эбола достигает 90%. В августе 2014 г. ВОЗ признала лихорадку Эбола угрозой всемирного масштаба.

Причины лихорадки Эбола
Вирус Эбола (Ebolavirus) принадлежит к семейству филовирусов и по своим морфологическим признакам схож с вирусом, вызывающим геморрагическую лихорадку Марбург, однако отличается от последнего в антигенном отношении. Всего известно 5 видов вируса Эбола: Zaire ebolavirus (Заир), Sudan ebolavirus (Судан), Tai Forest ebolavirus (Таи форест), Bundibugyo ebolavirus (Бундибуджио), Reston ebolavirus (Рестон). Крупные вспышки лихорадки Эбола в Африке ассоциируются с эболавирусами Заир, Судан и Бундибуджио; эпидемия 2014 года вызвана вирусом вида Заир. Рестонский эболавирус не представляет опасности для человека.
Предполагается, что естественным резервуаром вируса Эбола служат летучие мыши, шимпанзе, гориллы, лесные антилопы, дикобразы и другие животные, обитающие в экваториальных лесах. Первичное заражение человека происходит при контакте с кровью, выделениями или трупами инфицированных животных. Дальнейшее распространение вируса от человека к человеку возможно контактным, инъекционным, половым путем. Чаще всего заражение лихорадкой Эбола происходит при прямом контакте с биологическим материалом больных людей, загрязненными постельными принадлежностями и предметами ухода, с телом умершего при погребальных обрядах, совместном питании с больным, реже – при половых контактах и т. д. Больные лихорадкой Эбола представляют высокую опасность для окружающих примерно в течение 3-х недель от начала заболевания, выделяя вирус со слюной, носоглоточной слизью, кровью, мочой, спермой и др.
Входными воротами инфекции служат микротравмированные кожные покровы и слизистые оболочки, однако местные изменения в очаге внедрения вируса отсутствуют. Первичное размножение вируса происходит в регионарных лимфоузлах и селезенке, после чего возникает интенсивная вирусемия и диссеминация возбудителя в различные органы. Эболавирус способен оказывать как прямое цитопатическое действие, так и вызывать комплекс аутоиммунных реакций. В результате этого уменьшается образование тромбоцитов, происходит поражение эндотелиальных клеток сосудов, развиваются кровоизлияния и очаги некрозов во внутренних органах, что в клинической картине соответствует признакам гепатита, интерстициальной пневмонии, отека легких, панкреатита, орхита, эндартериита мелких артерий и др. При аутопсии обнаруживаются некрозы и кровоизлияния в печени, селезенке, поджелудочной железе, надпочечниках, гипофизе, гонадах.
Повышенному риску заражения лихорадкой Эбола подвержены члены семьи и медицинский персонал, ухаживающий за больными, а также лица, занимающиеся отловом и транспортировкой обезьян. После перенесенной лихорадки Эбола формируется устойчивый постинфекционный иммунитет; случаи повторного заражения редки (не более 5%).
Сиптомы лихорадки Эбола
Примерно с 5-7 суток, в период разгара клинического течения лихорадке Эбола, возникают боли в грудной клетке, мучительный сухой кашель. Усиливаются абдоминальные боли, понос становится профузным и кровавым, развивается острый панкреатит. С 6-7 дня на коже нижней половины туловища, разгибательных поверхностях конечностей появляется кореподобная сыпь. Часто возникают язвенные вульвиты, орхиты. Одновременно развивается геморрагический синдром, характеризующийся кровоизлияниями в местах инъекций, носовыми, маточными, желудочно-кишечными кровотечениями. Массивная кровопотеря, инфекционно-токсический и гиповолемический шок становятся причиной гибели больных лихорадкой Эбола в начале 2-й недели заболевания.
В благоприятных случаях через 2-3 недели наступает клиническое выздоровление, однако период реконвалесценции растягивается на 2-3 месяца. В это время выражен астенический синдром, плохой аппетит, кахексия, боли в животе, выпадение волос, иногда развиваются тугоухость, потеря зрения, психические нарушения.
Диагностика
Лихорадка Эбола может быть заподозрена у лиц с характерными клиническими симптомами, находящихся в эпидемиологически неблагополучных регионах Африки или контактировавших с больными. Специфическая диагностика инфекции проводятся в специальных вирусологических лабораториях с соблюдением требований биологической безопасности повышенного уровня. Эболавирус может быть выделен из слюны, мочи, крови, носоглоточной слизи и других биологических жидкостей с помощью заражения клеточных культур, ОТ-ПЦР, электронной микроскопии биоптатов кожи и внутренних органов. Серологическая диагностика лихорадки Эбола основана на обнаружении антител к вирусу методами ИФА, РНГА, РСК и др.
Неспецифические изменения в общем анализе крови включают анемию, лейкопению (позже – лейкоцитоз), тромбоцитопению; в общем анализе мочи – выраженную протеинурию. Биохимические изменения крови характеризуются азотемией, увеличением активности трансфераз и амилазы; при исследовании коагулограммы выявляются признаки гипокоагуляции; КОС крови - признаки метаболического ацидоза. С целью оценки тяжести течения и прогноза лихорадки Эбола больным может потребоваться проведение рентгенографии органов грудной клетки, ЭКГ, УЗИ органов брюшной полости, ФГДС. Дифференциальная диагностика проводится с малярией, септицемией, тифом, другими геморрагическими лихорадками, прежде всего, с лихорадкой Марбург, Ласса, желтой лихорадкой. Больным могут быть показаны консультации инфекциониста, гастроэнтеролога, невролога, гематолога и других специалистов.
Лечение лихорадки Эбола
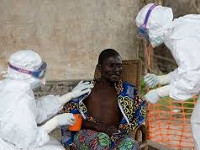
Транспортировка и лечение пациентов с лихорадкой Эбола осуществляется в специальных боксах-изоляторах. Весь ухаживающий персонал должен пройти специальный инструктаж, использовать барьерные средства защиты (специальные костюмы, очки, респираторы перчатки, обувь и т. д.), рекомендуемые при таких особо опасных инфекциях, как чума и натуральная оспа. Пациенту организуется строгий постельный режим и круглосуточное медицинское наблюдение.
На сегодняшний день вакцины от лихорадки Эбола не существует; сразу в нескольких странах мира проходят испытания экспериментальные образцы. Лечение сводится, главным образом, к симптоматическим мероприятиям: дезинтоксикационной терапии, борьбе с обезвоживанием, геморрагическим синдромом, шоком. В некоторых случаях положительный эффект дает введение плазмы выздоровевших людей.
Прогноз и профилактика
Летальность от лихорадки Эбола, вызванной штаммом вируса Заир достигает почти 90%, штаммом Судан – 50%. Критериями выздоровления считаются нормализация общего состояния пациента и трехкратные отрицательные результаты вирусологических исследований. Пресечь распространение лихорадки Эбола позволяет отслеживание контактов больных, соблюдение мер индивидуальной защиты, безопасное захоронение умерших, обеззараживание биологических материалов от больных геморрагическими лихорадками. В аэропортах различных стран усилен санитарно-карантинный контроль пассажиров, прибывающих из Африки. Контактные лица подлежат обсервации в течение 21 дня. При подозрении на заражение вирусом лихорадки Эбола пациенту вводится специфический иммуноглобулин из сыворотки крови лошадей.
Изобретение относится к способу получения гипериммунной сыворотки для производства лечебного иммуноглобулина против лихорадки Эбола и может быть использовано в медицине для экстренной профилактики лихорадки Эбола.
Известен способ получения гетерологических иммуноглобулинов против вирусных инфекций Марбург и Эбола, включающий иммунизацию животных-продуцентов вирусными антигенами, приготовленными из органов инфицированных животных, периодический забор крови у животных-продуцентов с последующим выделением сыворотки, спиртовое осаждение фракции глобулинов из сыворотки крови при отрицательных температурах и последующую очистку глобулинов (патент РФ №2089217, МПК А61К 39/295, опубл. 10.09.1997 г.). В качестве животных-продуцентов используют овец или коз, а забор крови у этих животных осуществляют при достижении активности индекса нейтрализации 2,0 lg и более в реакции биологической нейтрализации на лабораторных животных при инфицировании животных-продуцентов вирусом Марбург и активности индекса нейтрализации 2,75 lg и более при инфицировании животных-продуцентов вирусом Эбола.
Известен способ получения иммуноглобулина из гипериммунной лошадиной сыворотки, содержащей антитела к вирусу Эбола (патент РФ №2130318, МПК А61К 39/42, опубл. 20.05.1999 г.). Забор крови от продуцента осуществляют на 28-42 сутки после 3-ей и последующих иммунизаций (с учетом грунд-иммунизации) лошадей нативным вируссодержащим материалом, когда антитела достигают максимального уровня. Выделение иммуноглобулина Эбола проводят методом спиртового фракционирования на холоду по Кону.
Однако для формирования у животных пула нейтрализующих антител используется живой вирус Эбола в виде культуральной вируссодержащей жидкости или гомогената печени зараженных вирусом Эбола морских свинок. Использование живого вируса Эбола, относящегося к I группе патогенности по классификации Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Санитарно-эпидемиологические правила, СП 1.3.3118-13 БЕЗОПАСНОСТЬ РАБОТЫ С МИКРООРГАНИЗМАМИ I-II ГРУПП ПАТОГЕННОСТИ (ОПАСНОСТИ), требует использования вивария для содержания зараженных животных, оборудованного сложнейшими инженерно-техническими системами. Кроме этого, использование живого вируса Эбола в качестве антигена для иммунизации связано с его получением в препаративных количествах, и также как и содержание иммунизированных животных, требует проведение работ в максимально защищенных лабораториях. Такого рода работы с точки зрения биобезопасности связаны с высоким риском заражения для персонала лаборатории.
Известен способ получения рекомбинантных гуманизированных антител, обладающих нейтрализующей активностью в отношении вируса Эбола (Olinger GG Jr, Pettitt J., Kim D., et al. Delayed treatment of Ebola virus infection with plant derived monoclonal antibodies provides protection in rhesus macaques // Proc. Natl. Acad. Sci. USA, 2012; 109:18030-5; Pettitt J., Zeitlin L., Kim K, et al. Therapeutic intervention of Ebola virus infection in rhesus macaques with the MB-003 monoclonal antibody cocktail // Sci. Transl. Med. 2013; 5:199). Например, американской биотехнологической фирмой Марр Biopharmaceutical Inc. (США) разработан препарат ZMapp, который представляет собой композицию трех гуманизированных моноклональных антител, которые производиться в листьях табака (род Nicotiana). Для получения препарата гены, кодирующие химерные моноклональные антитела, были вставлены в вектора, которыми были заражены растения табака. Препарат ZMapp был использован в составе комплексной терапии для лечения людей во время эпидемии лихорадки Эбола в странах северо-западной Африки в 2014-2016 годах.
Однако недостатком такого способа получения рекомбинантных гуманизированных антител является долгий срок получения препарата (несколько месяцев, пока растет растение: Pollack, Andrew (8 August 2014). "In Ebola outbreak, who should get experimental drug?". The New York Times), необходимость строгого выполнения условий выращивания в условиях оранжереи при определенной температуре и освещенности и низкий выход препарата при наработке (из 18 растений можно получить 1 лечебную дозу для человека).
Наиболее близким аналогом (прототипом) является способ получения иммуноглобулинов против вируса Эбола (патент Китая № CN 104829710, МПК А61К 39/42, опубл. 12.08.2015 г.) путем иммунизации лошадей либо 1) ДНК-препаратом, включающим в свой состав ген, кодирующий GP белок эболавируса Заир, либо 2) ДНК-препаратом, включающим в свой состав ген, кодирующий GP белок эболавируса Судан, либо 3) ДНК-препаратом, включающим в свой состав ген, кодирующий GP белок эболавируса Кот-д’Ивуар, либо 4) смесью перечисленных препаратов в соотношении 1:1:1. Для получения гипериммунной сыворотки против одного из видов эболавируса (эболавируса Заир, эболавируса Судан или эболавируса Кот-д’Ивуар) первую иммунизацию лошадей проводят дозой 1 мг ДНК-препарата, содержащего GP ген любого из указанных эболавирусов; вторую - дозой 1 мг ДНК-препарата, содержащего GP ген любого из указанных эболавирусов; третью - дозой 2 мг ДНК-препарата, содержащего GP ген любого из указанных эболавирусов; и четвертую - дозой 3 мг ДНК-препарата, содержащего GP ген любого из указанных эболавирусов. Для получения гипериммунной сыворотки против 3 видов эболавируса (эболавируса Заир, эболавируса Судан или эболавируса Кот-д’Ивуар) первую иммунизацию лошадей проводят дозой 9 мг смеси ДНК-препаратов, содержащих GP ген каждого из указанных эболавирусов, в пропорции 1:1:1 (по 3 мг каждого ДНК-препарата); вторую - дозой 18 мг смеси ДНК-препаратов, содержащих GP ген каждого из указанных эболавирусов, в пропорции 1:1:1 (по 6 мг каждого ДНК-препарата); третью - дозой 36 мг смеси ДНК-препаратов, содержащих GP ген каждого из указанных эболавирусов, в пропорции 1:1:1 (по 12 мг каждого ДНК-препарата); и четвертую - дозой 72 мг смеси ДНК-препаратов, содержащих GP ген каждого из указанных эболавирусов, в пропорции 1:1:1 (по 24 мг каждого ДНК-препарата). Авторы заявляют также о возможности использования в схемах получения гипериммунных сывороток на лошадях еще 2 препаратов: субъединичной вакцины на основе белка GP эболавирусов Заир, Судан или Кот-д’Ивуар и препаратов на основе вирусоподобных частиц (ВПЧ), сформированных на основе белков GP и VP40 указанных эболавирусов. Гипериммунные сыворотки могут быть получены с использованием как субъединичных вакцин, так и ВПЧ, по схемам, описанным выше для ДНК-препаратов. Кроме этого, авторы заявляют о возможности использования комбинированных схем получения гипериммунных сывороток на лошадях с использованием всех 3 препаратов (ДНК-препараты, субъединичные вакцины и ВПЧ) как против каждого их эболавирусов (эболавирус Заир, Судан или Кот-д’Ивуар) так и против всех 3 видов эболавирусов вместе.
К недостаткам получения гипериммунной сыворотки способом-прототипом можно отнести сложность технологии получения гипериммунной сыворотки, т.к. в схеме вакцинации используется три ДНК-препарата или их смесь, что усложняет схему и увеличивает время иммунизации лошадей. Кроме того, для формирования у животного напряженного иммунного ответа, необходимо получить по 45 мг каждого ДНК-препарата, содержащего кодирующий GP-ген эболавируса, что приводит к увеличению затрат на производство гипериммунной сыворотки и, соответственно, лечебных иммуноглобулинов. По мнению заявителя, это связано с отсутствием коррекции гена GP для получения всех 3-х типов препаратов (ДНК-препарат, субъединичная вакцина и ВПЧ) в способе-прототипе. Известно, что экспрессия GP белка из клетки, в которой находится плазмида, существенно снижена по сравнению с экспрессией этого белка вирус-инфицированной клеткой. На повышение экспрессии GP белка эболавируса влияет замена 2-х аминокислот, находящихся непосредственно рядом с сайтом расщепления, в позициях D637A и Q638V. Особенностью получения ДНК-препарата и ВПЧ-препарата (используемых в предлагаемом заявителем способе иммунизации) является введение мутации D637L в сайте разрезания ТАСЕ-протеазы, что приводит к усилению отщепления GP с поверхности клеток [Escudero-Perez В., Volchkova V.A., Dolnik О. et al. Shed GP of Ebola virus triggers immune activation and increased vascular permeability // PLoS Pathog. 2014, 10(11):e1004509. doi: 10.1371/journal.ppat.l00450].
Техническим результатом предлагаемого изобретения является упрощение технологии получения гипериммунной сыворотки и сокращение затрат на ее получение.
Указанный технический результат достигается тем, что в способе получения гипериммунной сыворотки, содержащей гетерологичные иммуноглобулины против лихорадки Эбола, включающем 4-кратную иммунизацию лошадей вирусными антигенными препаратами, не содержащими живой вирус Эбола, с последующим забором крови у животных- продуцентов и выделением гипериммунной сыворотки, согласно изобретения, в качестве вирусных антигенных препаратов используют ДНК-препарат, содержащий ген гликопротеина вируса Эбола, и ВПЧ-препарат, содержащий вирусоподобные частицы, включающие ген гликопротеина вируса Эбола, 3-кратное введение ДНК-препарата осуществляют внутримышечно по следующей схеме: 1-я иммунизация - введение ДНК-препарата в дозе 4 мг/животное на 0 сут, 2-я иммунизация - введение ДНК-препарата в дозе 4 мг/животное на 21-28 сут после 1-го введения препарата, 3-я иммунизация - введение ДНК-препарата в дозе 4 мг/животное на 21-28 сут после 2-го введения препарата, четвертую иммунизацию осуществляют подкожно введением ВПЧ-препарата в дозе 3×10 9 ВПЧ/животное на 56 сут после 3-го введения ДНК-препарата, позволяющие индуцировать у лощадей образование общих специфических антител в титрах не менее 1:75000 и образование нейтрализующих антител к вирусу Эбола в титрах не менее 1:640, а отбор крови для получения гипериммунной сыворотки, содержащей иммуноглобулины, проводят на 10-13-е сутки после иммунизации ВПЧ-препаратом. Общее время иммунизации (от 1-й иммунизации до забора крови) составляет 122 дня.
ДНК-препарат представляет собой ДНК-конструкцию phCMV-GP/D637L, содержащую ген гликопротеина вируса Эбола под контролем промотора цитомегаловируса, а вирусоподобные частицы ВПЧ-препарата получены из среды упаковочных клеток, трансфицированных репликоновой РНК вируса Кунджин, которая содержит ген гликопротеина вируса Эбола.
Изобретение иллюстрируется следующими графическими материалами. На фиг. 1 приведена физическая и генетическая карта плазмиды phCMV-GP/D637L. На фиг. 2 представлен вектор SP6KUNrep5-GP, используемый для получения репликоновой РНК. На фиг. 3 дана схема получения вирусоподобных частиц. На фиг. 4 приведена схема иммунизации лошадей для получения гипериммунной сыворотки, содержащей иммуноглобулины против вируса Эбола.
Пример 1. Описание состава препаратов, используемых для иммунизации лошадей и получения гипериммунной сыворотки, содержащей гетерологичные иммуноглобулины против лихорадки Эбола
Для первых 3-х иммунизаций используется ДНК-конструкция - phCMV-GP/D637L (Escudero-Perez В et al., PLoS Pathog 2014 10, Reynard O. et al. // J.Infect. Dis. 2011, 204 Suppl 3:s 1060-5), содержащая GP-ген вируса Эбола. Эта ДНК содержит ген гликопротеина вируса Эбола под контролем промотора цитомегаловируса. Введенная мутация (D637L) в сайте разрезания ТАСЕ-протеазы (фиг. 1) приводит к усилению отщепления GP с поверхности клеток, уменьшая присутствие GP на поверхности клеток и тем самым уменьшая цитопатогенный эффект.
Для четвертой иммунизации используется ВПЧ-препарат (Reynard О. et al. // J.Infect. Dis. 2011, 204 Suppl 3:s1060-5; Pyankov O.V. et al. // J.Infect. Dis. 2015, 212 Suppl 2:s368-71) в дозе 3×10 9 ВПЧ/животное. ВПЧ получены из среды упаковочных клеток, трансфицированных репликоновой РНК вируса Куинджи, которая содержит ген гликопротеина (GP/D637L) вируса Эбола. Для получения репликоновой РНК использовали вектор SP6KUNrep5-GP, представленный схематично на фиг. 2 и содержащий следующие элементы: SP6 - промотор РНК полимеразы; 5'UTR, 3'UTR - нетранслируемые области вируса Кунджин; GP/D637L - ген гликопротеина вируса Эбола; Stop - стоп-кодон; IRES - внутренний сайт посадки рибосомы ЕМС вируса; KUN NSPs - неструктурные белки NS1, NS2A, NS2B, NS3, NS4A, NS4B, NS5 вируса Кунджин; С20 - первые 20 аминокислот белка сердцевины вируса Кунджин; Е22 - последние 22 аминокислоты Е белка вируса Кунджин; FMDV2A - 2А-автопротеаза вируса FMDV; HDVr - антигеномный рибозим вируса гепатита дельта; рА - сигнал полиаденилирования вируса SV40. Получение ВПЧ частиц проводили по схеме, представленной на фиг. 3.
Пример 2. Способ иммунизации лошадей для получения гипериммунной сыворотки, содержащей гетерологичные иммуноглобулины против лихорадки Эбола
Гипериммунную сыворотку получают после 3 циклов иммунизации животного ДНК-препаратом, содержащей ген, кодирующий гликопротеин (ГП, GP) вируса Эбола и однократной вакцинацией вирусоподобными частицами (ВПЧ), на основе вируса Кунджин, также содержащими ген, кодирующий гликопротеин вируса Эбола [1]. Схема иммунизации лошадей для получения препарата лечебных иммуноглобулинов приведена на фиг. 4.
Для первых 3-х иммунизаций используется ДНК-конструкция - phCMV-GP/D637L (Escudero-Perez В., Volchkova V.A., Dolnik О. et al. Shed GP of Ebola virus triggers immune activation and increased vascular permeability // PLoS Pathog. 2014, 10(11):e1004509. doi: 10.1371/journal.ppat.l004509), содержащая GP-ген вируса Эбола. Эта ДНК содержит ген гликопротеина вируса Эбола под контролем промотора цитомегаловируса. ДНК-препарат вводится внутримышечно в дозе 4 мг/лошадь. Для стимулирования иммунного ответа препарат вводится по следующей схеме: 1-я иммунизация - на 0 сут, 2-я иммунизация - на 21-28 сут после 1-го введения препарата, 3-я иммунизация - на 21-28 сут после 2-го введения препарата.
Через 56 сут после последнего, 3-го введения ДНК-препарата лошадям подкожно вводится ВПЧ-препарат [Reynard О. et al. // J.Infect. Dis. 2011, 204 Suppl 3:s1060-5; Pyankov O.V., Bodnev S.A., Pyankova O.G. et al. A Kunjin Replicon Virus-like Particle Vaccine Provides Protection Against Ebola Virus Infection in Nonhuman Primates // J. Infect. Dis. 2015, 212 Suppl 2:S368-71.] в дозе 3×10 9 ВПЧ/животное. Отбор крови у лошади в объеме 5-15 л проводится на 10-13-е сутки после введения ВПЧ-препарата (см. схему на фиг. 4). Из крови получают плазму или сыворотку, которая используется для получения лечебных иммуноглобулинов.
Пример 3. Изучение эффективности иммуноглобулинов, полученных заявляемым способом из гипериммунной сыворотки лошадей
Читайте также:


