Инфекционный мононуклеоз у ребенка увеличена печень
Инфекционный мононуклеоз — широко распространенное инфекционное заболевание. Для инфекционного мононуклеоза характерна выраженная полиорганность процесса, растянутый лихорадочный период, вариабельность клинической картины, несоответствие симптомов течени
Инфекционный мононуклеоз — широко распространенное инфекционное заболевание. Особенностью патогенеза инфекционного мононуклеоза (ИМ) является клинический полиморфизм и поражение иммунной системы, при котором стимулируется синтез иммуноглобулинов, что может провоцировать появление злокачественных лимфопролиферативных заболеваний [6; 7; 9; 10; 11].
 |
| Рисунок 1. Функциональное состояние печени определяется с помощью биохимического анализатора ЭББОТ VP (США) |
Как правило, отмечается выраженная полиорганность процесса, при которой поражение ротоглотки встречается довольно часто и, по данным одних авторов, носит вирусный характер, по мнению других — бактериальный [5] или смешанный вирусно-бактериальный [4; 12;].
При лечении антибиотиками (в частности, ампициллином) нередко наблюдаются аллергические осложнения. Еще одной особенностью ИМ является растянутый во времени лихорадочный период, по-видимому обусловленный ангинозным процессом.
Обнаружение характерных принципов поражения органов, в частности печени, крайне важно для выявления типичных биохимических сдвигов и понимания особенностей патогенеза с целью коррекции проводимой терапии. Под нашим наблюдением находилось 26 больных ИМ средней степени тяжести, поступивших в клинику на 10 — 15-й день болезни. У всех больных заболевание характеризовалось подострым постепенным началом —субфебрильной температурой в течение 5—7 суток, умеренными болями в горле при глотании, болями в области шеи за счет увеличения лимфатических узлов, а также постепенным нарастанием признаков интоксикации.
На момент поступления в стационар интоксикация отмечалась у всех больных, лимфоаденопатия — в 95% случаев, причем увеличивались в большей степени лимфатические узлы шейной группы, ангина выявлялась в 85% случаев, гепатомегалия — в 80%, тогда как желтуха наблюдалась только в 25% случаев, а спленомегалия — в 20% случаев.
В 55% случаев после применения ампициллина заболевание осложнялось появлением сыпи токсико-аллергического характера.
Инфекционный мононуклеоз диагностировался на основании клинической картины заболевания (наличия лихорадки и симптомов интоксикации, полилимфаденопатии, ангины, гепатоспленомегалии), эпидемиологического анамнеза, а также по характерным лабораторным данным:
а) в периферической крови наблюдался лимфоцитоз, выявлялись атипичные мононуклеары с широкой светлой базофильной протоплазмой;
б) при серологическом исследовании крови реакция Хофф-Бауэра была положительной в 100% случаев.
Анализ биохимических данных показал (см. таблицу), что у больных рассматриваемой группы изменены основные биохимические параметры, преимущественно связанные с ферментами печени. Во всех случаях отмечается повышение уровня активности АЛТ и ЩФ, реже АСТ и ГГТ. Отмечается повышение тимолового показателя, что свидетельствует о выраженных диспротеинемических сдвигах, вероятно связанных с появлением в крови дополнительных белковых фракций [2].
Превышение активности АСТ над АЛТ в пределах нормальных значений обычно характерно для здоровых людей. Однако повышение АСТ с одновременным ростом отношения АСТ/АЛТ (коэффициент де Ритиса больше 2) свидетельствует о поражении сердца, это же отношение с коэффициентом де Ритиса, меньшим 1, говорит о поражении печени. Высокие уровни ферментемии при всех видах вирусного гепатита характеризуются низким коэффициентом де Ритиса (за исключением дельта-гепатита) и являются прогностически неблагоприятным признаком течения болезни.
При клиническом наблюдении за больными ИМ не отмечалось признаков поражения сердечно-сосудистой системы, однако при электрокардиографическом исследовании у 38% больных выявлялись признаки поражения сердца, заключавшиеся в изменении конечной части желудочкового комплекса.
Нами было установлено, что основную группу составили 18 больных, у которых значения АЛТ доходили до 200 МЕ/л, а то время как повышение АСТ до этого уровня отмечалось у 25 больных. Таким образом, эти данные указывают как на сочетание поражения органов (печень, сердце), так и на скорее диффузное, чем локальное поражение печени.
Встречались отдельные больные с гигантскими значениями ферментемии по АСТ и АЛТ.
Уровень активности ЩФ, в среднем равный 380 МЕ/л (разброс значений от 80 до 780), указывает на несколько возможных источников (костная ткань, кишечник, печень, лимфатическая система) ее происхождения или на высокую активность процесса в одном из них. Уровень активности ГГТ, относящейся к мембранным структурам, как и ЩФ, равный в среднем 75 МЕ/л (от 2 до 380), указывает на заинтересованность мембранных структур различных клеток, однако соотношение ЩФ/ГГТ характеризуется выраженным превалированием первого фермента над вторым (в среднем 18,1).
Повышенное СОЭ указывает на признаки грубого повреждения форменных элементов крови (это подтверждается спленомегалией, появлением билирубина в моче, а также случаями желтухи), что увеличивает функциональную нагрузку на печень, связанную с детоксикацией продуктов разрушения гемоглобина. Все это происходит на фоне диспротеинемии и сопровождается одновременным снижением уровня общего белка в среднем до 63,4 г/л — вероятно, за счет подавления белок-синтетической функции, что подтверждается и снижением уровня мочевины.
Нормальный уровень билирубина указывает на эффективную детоксицирующую функцию печени, несмотря на то, что потемнение мочи свидетельствует об усилении распада эритроцитов. Высокий уровень общей ЛДГ можно считать дополнительным признаком компенсируемого распада эритроцитов, в которых она богато представлена [1; 3].
Высокие значения ЩФ и ГГТ вряд ли могут быть результатом холестаза, поскольку уровень ЩФ слишком высок, а уровень ГГТ не соответствует уровню ЩФ. Все это происходит на фоне функциональной диспротеинемии, подтверждаемой умеренным повышением тимолового показателя до 33 (от 2 до 68 ед.).
Повышенный в среднем до 570 мг% уровень b-ЛП указывает на изменения в обмене липидов при данной инфекции или является результатом гепариновой недостаточности, вызванной тромбогеморрагическими расстройствами, так как гепарин является активатором липолиза в липопротеидах и его потребление значительно возрастает при гемореологических нарушениях. Однако все вышеперечисленные причины вряд ли объясняют столь высокие уровни ЩФ. Нам кажется более вероятным считать ее происхождение из бурно разрастающейся лимфоидной ткани, строма которой богато представлена ЩФ.
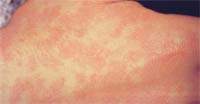 |
| Рисунок 2. Сыпь при инфекционном мононуклеозе |
Анализ биохимических данных выявил во всех рассмотренных случаях поражение печени с гигантскими уровнями АЛТ, которые клинически не всегда сочетались с биохимическими нарушениями. Клинические признаки поражения печени у этих больных проявлялись в гепатомегалии, субиктеричности склер, в ряде случаев анорексии. Динамика показателей и их уровни указывают на явно выраженный цитолитический компонент. Повышение ЩФ и ГГТ, традиционно рассматриваемое как признак холестаза, не сочетается (за единичными исключениями) с повышением билирубина, а значительное превышение ЩФ над ГГТ ставит вопрос о дополнительном источнике ее появления (кости, кишечник, лимфоидная ткань). Аналогичная патология у детей протекает с понижением уровня ЩФ даже при обязательной для их возраста ферментемии, по данным М. А. Гаспарян [4]. Вполне допустимо предположение, что в определенный момент заболевания происходит компенсаторное торможение функционирования костной ткани, что проявляется в обратном (по сравнению со взрослыми) феномене. Низкие по отношению к ЩФ значения ГГТ, возможно, указывают на подавление детоксицирующей системы печени в патогенезе данной инфекции. Так, более детальный анализ показал сохранение нормальных значений ГГТ в 30% общего числа наблюдений, что как раз и указывает не на поражение, а на заинтересованность детоксицирующей системы организма [5], к которой она и относится.
Хотя анализ биохимических данных и выявляет несоответствие между лабораторными и клиническими показателями (компенсированный вариант цитолиза), но значительная вариативность биохимических изменений в общем соответствует клиническому, иммунологическому и гуморально-клеточному полиморфизму ИМ.
Таким образом, анализ биохимических данных у больных инфекционным мононуклеозом выявил следующее: во-первых, характерную для ИМ картину энзимологических сдвигов – преобладание мембранно-холестатической пары над цитолитической за счет преимущественного повышения ЩФ; во-вторых, несоответствие клинического течения болезни выраженности биохимических изменений. И, главное — повышение уровня ЩФ указывает на необходимость выявления источника ее происхождения, а не соответствующий ей уровень ГГТ свидетельствует о заинтересованности детоксицирующей системы организма, к которой она относится.
Литература
1. Баркаган З. С., Тамарин И. В. Оценка степени повреждения эритроцитов при диссеминированном внутрисосудистом свертывании крови. Лабораторное дело, 1988, 4: 35 — 39.
2. Вапцаров Н. и др. Диспротеинемии. София: Медицина и физкультура, 1978.
3. Верхотин М. А., Савельева Л. В. Спектрофотометрии. Оценка влияния следов гемолиза на некоторые показатели сыворотки крови. Лабораторное дело, 1988, 4: 42 — 45.
4. Гаспарян М. А. Инфекционный мононуклеоз у детей. Дис. . д. м. н., 1977.
5. Голиков Ф. Н., Саноцкий И. В., Тиуов Л. А. Общие механизмы токсического действия. М.: Медицина, 1986.
6. Гурцевич В. О. Использование серологических маркеров вируса Эпштейн — Барр для дифференциальной диагностики рака носоглотки. — Опухоли головы и шеи. Кишинев, 1983. С. 52 — 57.
7. Мазуренко И. П. Дальнейшее изучение связи вируса Эпштейн — Барр с лимфогранулематозом и назофаренгиальным раком человека. В кн.: Вирусы рака и лейкоза. Сб. науч. трудов, 1980. С. 57 — 59.
8. Маринеску. Острый инфекционный лимфоцитоз и инфекционный мононуклеоз. Бухарест, 1961. С. 229 — 230.
9. Obekender H. Антитела к вирусу Эпштейн — Барр при раке носоглотки, раке миндалин и в контрольной группе. Actavirolocica 1983, т. 27, вып. 3. С. 277— 281.
10. Рузаев Л. Н. Ассоциация вируса Эпштейн — Барр с некоторыми неопластическими новообразованиями. В кн.: Вопросы ранней диагностики, профилактики и лечения злокачественных опухолей. Тез. докл. Якутск, 1984. С. 129 — 130.
11. Шварцвергс А. М. Маркеры вируса Эпштейн — Барр, их роль в диагностике опухолевых заболеваний верхних дыхательных путей. Профилактика, ранняя диагностика и лечение злокачественных новообразований, Тез. докл., ч. I. Рига, 1985. С. 148 — 149.
12. Руденская И. М. Аллергическая реакция на ампициллин при инфекционном мононуклеозе. Вопросы охраны материнства и детства, 1981, т. 26 № 2, с. 71 — 72.

Пути передачи, диагностика и лечение.
Дело в том, что вирус Эпштейн-Барр очень распространен среди людей – он обнаруживается у 80-90% взрослых. Это означает, что чем старше человек, тем больше вероятность того, что он является носителем этого вируса, а значит – переболел данной инфекцией ранее, в острой или стертой форме. Инфекция, вызванная вирусом Эпштейн-Барр, оставляет после себя достаточно стойкий иммунитет, благодаря чему повторно заболеть инфекционным мононуклеозом невозможно. Однако это не является условием для полного уничтожения вируса в организме у человека – то есть после перенесенной инфекции острых клинических проявлений болезни уже может не быть, однако такой человек может ещё очень долго быть источником вируса для окружающих.

Вирус Эпштейн-Барр передается от больного или вирусоносителя в основном воздушно-капельным путем. Накапливается вирус в клетках эпителия слюнных желез, и в слюне его содержание больше всего. Этот вирус не обладает такой устойчивостью и летучестью – как, например, вирусы-возбудители ОРВИ, и для его передачи необходим не просто контакт с больным человеком, а контакт с его слюной или с предметами, из которых ел, пил или которые облизывал больной (например, это игрушки в детском саду). Этот вирус действительно передается с поцелуями – поэтому если ребенок не переболел данной инфекцией в более раннем возрасте, то он может с большой вероятностью заболеть инфекционным мононуклеозом, став подростком, с появлением первых влюбленностей.
К слову, чем раньше ребенок переболеет инфекционным мононуклеозом, тем будет лучше для него самого – так как у детей дошкольного возраста инфекционный мононуклеоз часто протекает стерто. А чем старше ребенок – тем больше выражена клиника.
А вот после 40 лет им уже мало кто болеет, так как к 40 годам с этим вирусом проконтактировали уже практически все.
Симптомы инфекционного мононуклеоза – это следствие тех изменений, которые вирус последовательно вызывает в теле заболевшего. Вирус Эпштейна-Барр при попадании в полость рта вызывает изменения в слизистой рта, носоглотки, в миндалинах и слюнных железах. Здесь происходит его размножение, и первым симптомом инфекции становится боль в горле.
Затем вирусы попадают в кровь и разносятся по организму. Главная их цель - В-лимфоциты. Достигнув своей цели, вирус вызывает настоящее клонирование (стихийное размножение) В-лимфоцитов, которые заполняют своей массой лимфатические узлы, которые увеличиваются в размерах, становятся плотными и болезненными. И это второй по очередности симптом болезни.

Вместе с увеличением лимфоузлов у заболевшего человека увеличиваются в размерах селезенка и печень. Выраженное увеличение селезенки опасно особенно у детей, так как их физическую активность не всегда удается контролировать – а между тем известны случаи, когда при инфекционном мононуклеозе происходили разрывы селезенки (эти разрывы крайне опасны для жизни, так как при них за секунды возникает опасная для жизни потеря крови).
И как при любой системной инфекции при инфекционном мононуклеозе у больного повышается температура (причем повышенной она может быть очень долго, иногда до нескольких недель), выражена слабость, бывает головная боль. Также встречается и сыпь – особенно если больной во время лечения пользовался антибиотиками (это многолетнее наблюдение врачей).
Таким образом, клиника инфекционного мононуклеоза с одной стороны, может быть принята за банальное ОРЗ или ангину, а с другой стороны – за заболевание печени или других органов пищеварительной системы.
Необходимо отметить, что у детей дошкольного возраста инфекционный мононуклеоз часто протекает стерто, и чем старше ребенок – тем больше выражена клиника, а вот после 40 лет им уже мало кто болеет.
Безусловно, при диагностике инфекционного мононуклеоза используются и рутинные методы – общий и биохимический анализ крови, но полную картину происходящего и точный ответ с подтверждением диагноза дадут:
- иммуноферментный анализ (ИФА) для обнаружения антител к вирусу Эпштейн-Барр. ИФА проводится для обнаружения антител к разным частям вируса. Чаще всего ИФА проводится для обнаружения трех видов антител к вирусу Эпштей-Барр, реже – для обнаружения пяти видов.
- полимеразная цепная реакция (ПЦР) для определения вируса (в мазках из зева, носа, а также в крови).
Оба из перечисленных выше обследований могут быть сделаны либо по направлению врача, наблюдающего пациента – в случае тяжелого течения инфекционного мононуклеоза у ребенка может быть выдано бесплатное направление в поликлинике по месту жительства (с подписью заведующей), либо при желании родителей – на платной основе.
Стоимость трехкомпонентного ИФА для обнаружения антител к вирусу Эпштейн-Барр в Центре лабораторной диагностики, к примеру, составит сравнительно небольшую сумму – 312 рублей, при этом данный метод позволит врачу судить не только о наличии или отсутствии данной инфекции, но также и об её стадии, включая носительство, стоимость же ПЦР составляет 900 рублей.
Чаще всего эту инфекцию лечат дома, при тяжелом течении инфекционного мононуклеоза больной госпитализируется в ГКБ № 40.
Лечение инфекционного мононуклеоза – неспецифическое, включающее:
- соблюдение постельного режима (многие привыкли переносить лихорадку с болями в горле на ногах, но в случае этой инфекции нужно поберечь ещё и печень с селезенкой – им во время острой стадии инфекции тяжелее всего),
- полоскание горла растворами антисептиков, отварами лекарственных трав,
- прием жаропонижающих и обезболивающих препаратов,
- диету с ограничением соленого, жирного, жареного, копченого, сладкого, сдобного – для того, чтобы уменьшить нагрузку на печень.

При выраженных изменениях в печени больным рекомендуется прием гепатопротекторов и биохимический анализ крови в динамике после выписки из стационара. А также диета, которая даст печени возможность восстановиться при инфекции.
Необходимость лечения в стационаре обычно бывает продиктована тяжелым общим состоянием больного, затруднением дыхания (из-за увеличения миндалин и отека верхних дыхательных путей), нарушениями в работе печени, выраженным увеличением селезенки.
Типичный инфекционный мононуклеоз не оставляет выраженных изменений в работе иммунной системы человека. Безусловно, после этой инфекции важно обратить внимание на общее состояние здоровья ребенка, не отказываться от закаливания, прогулок, но приема каких-либо специфических иммуностимуляторов, особенно без назначения врача, лучше избежать. Тем более, что он и не требуется, так как инфекция сама по себе не вызывает изменений в работе клеток, а вызывает только их бурное размножение, которое прекращается с течением заболевания.
Значительно больше внимание стоит уделить печени, поддержать её диетой, проконтролировать уровень билирубина и основных печеночных проб.
Инфекционный мононуклеоз относится к группе заболеваний, по-видимому, вирусной этиологии. Типичными проявлениями инфекционного мононуклеоза принято считать триаду клинических признаков: лихорадку, ангину и аденоспленомегалию в сочетании с гематологическими изменениями (лейкоцитозом с атипичными мононуклеарами и гетерофильными антителами).
В настоящее время инфекционный мононуклеоз имеет множество названий, из которых следует отметить наиболее часто употребляемые (кроме уже названного) - моноцитарная ангина, доброкачественный острый лимфобластоз, болезнь Филатова, болезнь Пфейфера и мн. др. История вопроса наиболее полно представлена в монографии Г. Маринеску.
В 1962 г. в Бухаресте на Международном съезде, посвященном инфекционной патологии, было признано, что более удачным названием болезни следует считать инфекционный мононуклеоз.
Необходимо, однако, подчеркнуть, что почти не существует органа, который при этом заболевании оставался бы интактным.
Этиология . Возбудитель инфекционного мононуклеоза до сих пор, по существу, не идентифицирован. Много раз выдвигаемые теории о возможной бактериальной его этиологии (стафилококк, стрептококк, пневмококк, фузоспириллы, спирохеты Ванцетта и др.), не подтвердились.
Была изучена этиологическая связь инфекционного мононуклеоза с листереллами, риккетсиями и вирусами.
Исследования, проведенные в Европе и Америке, не подтвердили предположения японских авторов об этиологической роли риккетсий в инфекционном мононуклеозе.
Большинство исследователей считают возбудителем этого заболевания вирус. В настоящее время имеется ряд доказательств в пользу этиологической связи вируса Epstein-Barr с инфекционным мононуклеозом. По мнению ряда исследователей, вирус Е-В связан с лимфомой Burkitt.
Kouba и Lasovska сообщают следующие сведения относительно лимфомы: в конце пятидесятых годов текущего столетия начато ее вирусологическое исследование. В основном лимфома поражает детей и характеризуется злокачественным перерождением тканей с преобладанием недифференцированных лимфоретикулярных клеток, локализованных чаще в верхней челюсти или орбите. Epstein и Вагг в большинстве клеток культуры лимфомы Беркитта обнаружили частицы, весьма напоминающие вирус герпеса. По имени этих авторов, вирус и был назван вирусом Эпштейн-Барр (Е-В). В процессе исследования одна из лаборанток заболела инфекционным мононуклеозом, и в ее крови было обнаружено нарастание титра антител к вирусу Е-В (до заболевания антитела отсутствовали). Этот факт послужил основанием к обследованию доноров США. на наличие у них антител к вирусу Е-В. Установлено, что антитела к вирусу появлялись у лиц, перенесших инфекционный мононуклеоз. Аналогичные данные были получены Niederman и др. и в 6 городах Англии большой группой авторов и заключались в следующем. В октябре 1969 г. при обследовании 1457 студентов, поступивших в университеты Англии, наличие антител к вирусу Е-В было выявлено в 57% случаев. При вторичном обследовании у лиц, у которых ранее антитела не отмечались, последние были обнаружены в 12% случаев. Из числа студентов, у которых было выявлено нарастание титра антител, 50% перенесли (за этот период времени) инфекционный мононуклеоз и у них также выявлялась положительная реакция Пауля-Буннеля-Девидсона.
Evans и сотр. установили корреляционную связь между восприимчивостью к инфекционному мононуклеозу и отсутствием антител к вирусу Е-В. Так, среди 268 обследованных доноров с отсутствием антител к вирусу. Е- В было 174, из числа которых инфекционным мононуклеозом заболело 15%, а среди 94 доноров, у которых определялись антитела, ни один человек не заболел.
Весьма важным, с нашей точки зрения, является факт, позволивший установить, что после удаления гидрофильных антител (обнаруживаемых в реакции Пауля-Буннеля) титр их к вирусу Е-В не изменялся, что послужило основанием считать эти гидрофильные антитела и антитела к вирусу Е-В различными.
У детей, проживающих в США, титр антител к вирусу Е-В нарастает с увеличением возраста ребенка; это подтверждает мнение Evans о том, что инфекционный мононуклеоз у детей - весьма частое заболевание, которое, однако, редко диагностируется.
Нельзя не отметить в этой связи и точку зрения Glade и соавт. о том, что нарастание титра антител к вирусу Е - В может быть обусловлено не перенесенным специфическим заболеванием, а является следствием неспецифической лимфопролиферативной реакции организма, вызванной размножением симбиотического вируса герпетического характера. В фазе лимфопролиферации увеличивается количество лимфомоноцитов. Это состояние возникает при ряде инфекционных форм и, в том числе при вирусном гепатите, инфекционном мононуклеозе, лимфоме Беркитта, эпидемическом паротите, опоясывающем лишае, простом герпесе и цитомегалии.
Хота сейчас нельзя однозначно утверждать связь между вирусом Е-В, лимфомой Беркитта и инфекционным мононуклеозом, однако ясно, что этот вирус не является случайной находкой у больных инфекционным мононуклеозом.
Эпидемиология . Инфекционный мононуклеоз в большинстве случаев носит спорадический характер, хотя описаны и возникающие весной и осенью вспышки в родильных домах, детских садах, семьях. Среди наблюдаемых нами больных представляет интерес больная девочка 1 года 6 месяцев, которая заболела инфекционным мононуклеозом, заразившись в семье. Отец, мать и брат этой больной на протяжении месяца, предшествующего заболеванию, перенесли инфекционный мононуклеоз, ведущим проявлением которого была ангина с налетами, подъем температуры и общая интоксикация. Диагноз был установлен нами на основании характера изменений периферической крови у отца, матери и брата.
Источником инфекции служит человек. Входными воротами является носоглотка; вместе с тем, известны случаи заражения и при проведении гемотрансфузии.
Инфекционный мононуклеоз чаще регистрируется среди молодых лиц.
Инкубационный период . Длительность инкубационного периода в среднем составляет 4-5 дней; вместе с тем, он может достигать даже 49 дней, по данным Petrides.
Патогенез . Распространение инфекции происходит по лимфатическим и кровеносным путям и сопровождается поражением периферических и висцеральных лимфатических узлов, селезенки, печени, почек и, вероятно, костного мозга. Вторично развиваются ангина, лимфаденит.
Патологоанатомические изменения . Основные изменения характеризуются лимфоидной гиперплазией лимфатических узлов и активной пролиферацией клеток ретикулоэндотелия. По данным Г. Маринеску, генерализованная гиперплазия лимфатической и ретикулоэндотелиальной тканей, вызванная вирусом, приводит к появлению в крови в большом количестве типичных и атипичных мононуклеаров, создавая таким образом характерную картину, свойственную данному заболеванию. Увеличение печени, селезенки и лимфатических узлов обусловлено гиперплазией ретикулогистиоцитарной системы в целом.
Архитектоника лимфоузлов изменена, но не полностью разрушена, пульпа узлов, синусы, капсула и окружающая клетчатка инфильтрированы лимфоцитами и крупными широкоплазменными моноцитами. Среди лимфоцитов преобладают юные, но встречаются и другие клетки с пораженной цитоплазмой или же с измененными ядрами. В отдельных случаях возникают очаговые некрозы. Характер и степень морфологических изменений зависит от стадии процесса. Так, в начале заболевания возникает ретикулярная гиперплазия, которая в период разгара быстро прогрессирует, а затем, в фазе начальной реконвалесценции, подвергается регрессу.
McMachon и др. при биопсии шейного узла у ребенка 4,5 лет обнаружил атипичные ретикулярные клетки, часть которых была не отличима от клеток Рид-Штернберга. Спустя 13 месяцев наступило полное клиническое выздоровление и нормализация всех лабораторных показателей.
В миндалинах, селезенке, костном мозге, почках, сердечной мышце и других органах возникают изменения, подобные только что описанным М. О. Гаспарян с соавт., на основании цитологического Исследования миндалин у больных инфекционным мононуклеозом приходит к заключению, что в их ткани происходят специфические для данного заболевания изменения. В миндалинах обнаруживается большое количество лимфоидных клеток, атипичные мононуклеары и разнообразная микробная флора.
По данным И. А. Кассирского и Г. А. Алексеева, реактивные изменения, возникающие в лимфоузлах и селезенке, регистрируются раньше изменений, наступающих в периферической крови.
Следует отметить, что как диффузная, так и очаговые ретикулогистиоцитарная и лимфоцитарная инфильтрации обнаруживаются в ряде органов и систем, в том числе в оболочках мозга, нервных стволах и корешках. Обнаружены и изменения ликвора при отсутствии менингеальных симптомов.
В печени изменения сводятся к интерстициальному воспалению с поражением купферовских клеток. Паренхима при этом страдает лишь незначительно. В тех случаях, когда возникают центролобулярные некрозы, наблюдается нарушение пигментного обмена и развивается желтуха.
Sinister, Ognibene наблюдали лимфоцитарную инфильтрацию в портальной зоне и гипертрофию клеток Купфера без развития холестаза и изменения гепатоцитов. Sworn и Urich нашли, что архитектоника печени при этом заболевании не нарушена, паренхиматозные клетки имеют гранулярную цитоплазму. Гепатоциты в основном интактны, и лишь на отдельных участках возникают их некрозы.
По мнению И. А. Кассирского и Г. А. Алексеева, в печени происходит дискомплексация печеночных клеток, напоминающая изменения, возникающие при вирусном гепатите (болезни Боткина), однако, в отличие от последней, наблюдается скопление большого числа крупных моноцитов и лимфоидных клеток в зоне поражения.
Единой классификации инфекционного мононуклеоза нет до настоящего времени, однако принято выделять следующие варианты болезни: лихорадочный, ангинозный, железистый, спленомегалический, поражение слизистых оболочек, псевдогриппозный, астенический.
И. А. Кассирский и Г. А. Алексеев считают, что более целесообразно оценивать заболевание по тяжести и течению. Нам представляется наиболее правильным, указывая ведущее поражение при инфекционном мононуклеозе, характеризовать форму болезни. В целом не вызывает сомнения, что инфекционный мононуклеоз правильнее рассматривать как заболевание, характеризующееся поражением ряда органов и систем, которое может протекать как в легкой, так и в среднетяжелой и тяжелой формах.
Симптомы инфекционного мононуклеоза . Как правило, у взрослых начало болезни острое, но в отдельных случаях наблюдается продром в виде общего недомогания, мышечных болей, головокружения и субфебрильной температуры. Длительность продрома - не более 2-3 дней. Среди наблюдаемых нами 53 больных начало болезни с продрома имело место в 12,5% случаев и в 40% - постепенное с субфебрилитетом. В противоположность наблюдениям Н. М. Чирешкиной, сообщившей об остром начале инфекционного мононуклеоза у детей в 19,7%, мы наблюдали острое начало в 47,5% случаев. Заболевание, как правило, начиналось с лихорадки, в ряде случаев с ознобами (10,9%), головной болью (15,9%), болями в животе (15,9%), реже наблюдались носовые кровотечения (4,0%).
Повышению, температуры у 41 ребенка (77,3%), предшествовали ангины и лимфаденит. Налеты на миндалинах появлялись спустя несколько дней после начала заболевания и исчезали в среднем на 15,0 ± 0,8 день болезни. Читать подробнее о симптомах инфекционного мононуклеоза
Осложнения . К числу осложнений инфекционного мононуклеоза следует отнести спонтанный разрыв селезенки. Впервые разрыв селезенки был описан в 1941 г.
В 1965 г. York представил подробный обзор по этому вопросу, описав 45 известных в мировой литературе случаев. При детальном описании разрыва селезенки у женщины, больной инфекционным мононуклеозом, Rawsthorne и др. отметили в числе первых признаков появление сильных болей в области головки плеча и быстрое их распространение в левую половину брюшной полости. При гистологическом исследовании селезенки было выявлено наличие атипичных лимфоузлов, рассеянных диффузно и скапливающихся в синусоидах, а также инфильтрация и отек капсулы. В печени - перипортальная инфильтрация круглыми клетками, увеличение числа лейкоцитов в синусоидах, вакуолизация и пикноз гепатоцитов.
На 12-й день после операции больная была выписана в удовлетворительном состоянии с нормальными показателями функциональных проб и периферической крови.
Могут иметь место также и гнойные осложнения, возникающие в лимфатических узлах и других тканях организма.
Г. Маринеску к числу осложнений относит тяжелые дыхательные расстройства вследствие поражения периферических нервов (полиневрит, полирадикулоневрит) или же центральной нервной системы (синдром Ландри и бульбарные поражения).
Исход заболевания . В большинстве случаев больной выздоравливает полностью. Длительность заболевания, по данным большинства исследователей, составляет 2-8 недель. По нашим данным, средний срок заболевания составил 27,0 ± 2,0 дня.
Смертельный исход наблюдается крайне редко.
Среди наблюдаемых нами больных к моменту выписки из клиники регистрировалось полное выздоровление. При диспансеризации обострений не выявлено.
По данным Н. М. Чирешкиной, на протяжении многих лет после перенесенного инфекционного мононуклеоза могут сохраняться остаточные явления в виде увеличения печени, селезенки, гиперплазии лимфатических узлов, лейкопении с относительным лимфоцитозом, что расходится е нашими данными.
Небезынтересны данные Г, Маринеску о возможности хронического течения болезни, при котором гетерофильные антитела либо отсутствуют, либо имеются в незначительном титре.
Диагностика . Дифференциальная диагностика инфекционного мононуклеоза встречает большие затруднения, особенно у детей. Наиболее сложной оказывается диагностика заболевания у детей первых лет жизни, так как у них лимфатический аппарат развит сильнее и реагирует на антигенные раздражители выраженной гиперпластической реакцией при многих заболеваниях.
Относительное увеличение числа одноядерных клеток и наличие атипичных мононуклеаров может иметь место не только при инфекционном мононуклеозе, но и при других инфекциях.
Некоторые формы аденовирусной инфекции также сопровождаются увеличением заднешейных лимфатических желез, печени и селезенки. И. Раудсеп считает, что для дифференциальной диагностики инфекционного мононуклеоза основную роль играет гематологическое исследование, проводимое в первые 10 дней заболевания.
Для установления диагноза, в особенности в сомнительных случаях, большую помощь оказывает серологическая диагностика. Чаще всего применяется реакция Пауля-Буннеля и ее модификация (гетерогемагглютинация).
Реакция Пауля-Буннеля основана на увеличении в крови гемагглютининов к эритроцитам барана, морской свинки, кролика.
Оценка этой реакции клиницистами различна. Так, Г. К. Кушнир считает, что в ряде случаев имеются ложноположительные реакции. И. А. Кассирский регистрировал положительную реакцию в 72% случаев, в то время как А. Д. Сидорова положительные реакции наблюдала лишь в 47%.
В настоящее время наиболее широкое распространение получила модификация реакции Пауля-Буннеля, предложенная Девидсоном. По мнению Mount, использование эритроцитов лошади делает эту реакцию более чувствительной.
Реакция Ловрика представляет собой модификацию реакции гемагглютинации на стекле с использованием эритроцитов барана. Модифицированная таким образом реакция становится более специфичной, чем реакция Пауля-Буннеля, и выпадает положительной у больных в 60% случаев при меньшем проценте ложноположительных результатов.
По мнению Г. К. Кушнир, у детей до 3 лет ни одна из серологических реакций не решает диагностических трудностей. Диагностическим титром автор считал положительную реакцию при разведении сыворотки не менее нем 1/120.
Исследования, проведенные нами, позволяют прийти к заключению, что для диагностики инфекционного мононуклеоза необходим комплекс данных, из числа которого ведущим является клиническая симптоматика, затем результаты гематологического исследования.
Наряду с результатами клинического и гематологического исследования, используемых для дифференциальной диагностики инфекционного мононуклеоза от других поражений печени, существенное значение принадлежит исследованию энзимного спектра крови. Так, исследованиями Kurtar было показано, что цитоплазматический энзим гуаниндезаминаза у больных инфекционным мононуклеозом не нарастает, увеличивается в основном щелочная фосфатаза (печеночного происхождения), непостоянно и умеренно нарастает активность ГПТ и ГЩТ.
Лечение . Отсутствие до настоящего времени методов специфической терапии диктует необходимость использования симптоматического лечения.
К числу симптоматических средств следует отнести при лечении тяжелых форм болезни - соблюдение постельного режима, туалета полости рта, витаминотерапию. Если заболевание протекает с резко выраженными ангинами (с налетами), можно рекомендовать антибиотики широкого спектра действия, так как микробная флора бывает различной (стрептококковой, стафилококковой, пневмококковой и др.). Следует иметь в виду, что ни сульфаниламиды, ни антибиотики не оказывают влияния непосредственно на вирус, вызывающий инфекционный мононуклеоз.
Гормонотерапия (преднизолон) должна быть применена для лечения тяжелых форм болезни, так как оказывает бесспорно хороший эффект. По данным Г. Маринеску и наших личных наблюдений, длительность заболевания при назначении кортикостероидов значительно сокращается. При вариантах инфекционного мононуклеоза, сопровождающихся поражением нервной системы, лечение должно проводиться в соответствии с неврологической симптоматикой (дибазол, витамины B12, В1, B6 - внутримышечно).
При разрыве селезенки необходимо хирургическое вмешательство с проведением спленэктомии.
Представленные в данной статье варианты клинического течения инфекционного мононуклеоза свидетельствуют о многообразии его вариантов, встречающихся у детей, о вовлечении печени в патологический процесс и необходимости тем самым проведения дифференциальной диагностики с вирусным гепатитом.
Читайте также:


