Какие анализы на остеоартроз
Остеоартроз – заболевание, характеризующееся дегенеративными изменениями в суставах, которые могут приводить к значительному нарушению их функций.
Сустав – это подвижное соединение костей скелета. В норме движения в суставах осуществляются с минимальным трением суставных поверхностей в определенных направлениях с ограниченной амплитудой.
Суставы покрыты хрящевой тканью, которая имеет идеально гладкую поверхность. Также они окружены особой оболочкой – суставной сумкой. Внутренний слой суставной сумки – синовиальная оболочка продуцирует синовиальную жидкость, которая выполняет ряд важных функций: обеспечивает питание хрящей, смазывание суставных поверхностей для снижения трения при движениях.
Суставы укреплены связками, ограничивающими объем и направление движений.
При остеоартрозе нарушаются свойства суставных хрящей и они постепенно разрушаются. Это вызывает боль, ограничение подвижности, деформацию суставов.
По мнению исследователей, развитию заболевания способствует ряд факторов. Среди них выделяют следующие: возрастные дегенеративные изменения в суставных хрящах, избыточная масса тела, травмы суставов, генетическая предрасположенность, слабость мышечного аппарата, заболевания суставов (например, ревматоидный артрит), и др.
Остеоартроз широко распространен. Чаще характерные симптомы появляются в возрасте 40-50 лет. Рентгенологические признаки заболевания имеются более чем у 50 % людей старше 65 лет.
В большинстве случаев патологический процесс затрагивает крупные суставы, такие как бедренные, коленные, суставы позвоночника.
Лечение может быть консервативным и оперативным. Консервативная терапия направлена на уменьшение выраженности симптомов заболевания, замедление процессов дегенерации хрящевой ткани. Одним из направлений хирургического лечения является протезирование пораженных суставов.
Остеоартрит, деформирующий остеоартроз.
Osteoarthrosis, Osteoarthritis, Degenerative Joint Disease.
- Боль в пораженных суставах (усиливается при нагрузках и уменьшается после отдыха);
- скованность (особенно после длительного отсутствия двигательной активности, например утром после сна);
- ограничение объема движений в суставах;
- деформация пораженных суставов, припухлость;
- хруст, чувство трения при движениях;
- формирование костных выростов (узелков) на суставах кистей.
Общая информация о заболевании
Остеоартроз – дегенеративное заболевание суставов, которое может приводить к значительному нарушению их функций.
Он развивается в результате постепенного разрушения суставных хрящей. В норме хрящ имеет идеально гладкую поверхность и упругую структуру. Выделяемая синовиальной мембраной жидкость смазывает суставные поверхности, благодаря чему при движениях минимизируется трение в суставах. Амортизационные свойства хрящей смягчают толчки и удары, возникающие во время ходьбы, прыжков и других нагрузок.
Такие качества обеспечиваются особым строением хрящевой ткани. Она состоит из клеток – хондроцитов и синтезируемых ими компонентов межклеточного вещества: коллагена, углеводно-белковых компонентов (протеогликанов, гликозаминогликанов), гиалуроновой кислоты.
На начальных стадиях остеоартроза в хрящевой ткани появляются незначительные дефекты, и хондроциты начинают синтезировать повышенное количество протеогликанов для восстановления возникающих повреждений.
Со временем способность к синтезу протеогликанов снижается. Это вызывает уменьшение эластичности хряща и делает его более уязвимым при различных механических воздействиях. Постепенно толщина хряща уменьшается, в первую очередь это происходит в областях максимального давления на хрящевую ткань.
Наряду с процессами дегенерации хрящевой ткани запускаются механизмы восстановления. При этом вместо нормального хряща образуется грануляционная (рубцовая), фиброзно-хрящевая ткань. В подлежащем слое кости размножение клеток приводит к формированию выростов (остеофитов). Таким образом, постепенно хрящевая ткань утрачивает свои свойства, движения в суставах значительно затрудняются, возникает боль, которая усиливается при нагрузках на пораженные суставы.
Механизмы дегенерации хрящевой ткани при остеоартрозе одинаковы, вне зависимости от вызвавших ее причин. Среди факторов, которые способствуют развитию этого заболевания, выделяют следующие.
- Возрастные изменения в хрящевой ткани. С возрастом уменьшается ее эластичность, снижается способность к синтезу компонентов хряща, ухудшается его питание.
- Повышенная нагрузка на суставы. При остеоартрозе чаще поражаются суставы, испытывающие максимальное механическое воздействие. К ним относятся коленные, бедренные суставы, суставы позвоночника. Факторами риска могут быть избыточная масса тела или длительная повышенная нагрузка (например, при занятиях определенными видами спорта).
- Травмы, оперативные вмешательства на суставах.
- Генетическая предрасположенность.
- Врождённые нарушения структуры суставов могут впоследствии приводить к повреждению суставных хрящей.
- Слабость мышц. При ослабленном мышечном аппарате нагрузка на суставы возрастает.
- Различные заболевания, при которых изменяются структура и функции суставных хрящей (например, подагра).
В настоящее время не существует препаратов, которые способны остановить процесс разрушения хрящевой ткани или эффективно восстановить ее. При значительных нарушениях функции суставов применяется протезирование, после которого у большинства пациентов отмечаются хорошие результаты. В зависимости от уровня активности пациента, через 10-15 лет после этого может потребоваться повторное оперативное вмешательство.
Кто в группе риска?
К группе риска относятся:
- лица старшего возраста,
- перенесшие травмы суставов,
- имеющие избыточную массу тела,
- ведущие малоподвижный образ жизни,
- лица, образ жизни которых связан с постоянными нагрузками на определенные суставы (например, на коленные суставы при поднятии тяжестей),
- имеющие врождённые суставные дефекты,
- страдающие некоторыми заболеваниями, например сахарным диабетом, подагрой).
- Общий анализ крови. Позволяет определить основные параметры в крови: количество эритроцитов, гемоглобина, лейкоцитов, тромбоцитов в крови. При остеоартрозе показатели общего анализа крови в норме, в отличие от некоторых болезней суставов, при которых может повышаться уровень лейкоцитов (например, при ревматоидном артрите).
- Скорость оседания эритроцитов (СОЭ). Неспецифический показатель протекания различных патологических процессов в организме, в основном воспалительной природы. При остеоартрозе СОЭ может быть несколько повышена.
- С-реактивный белок, количественно (метод с нормальной чувствительностью). Один из наиболее чувствительных маркеров воспаления и повреждения тканей. Синтезируется в печени. Уровень данного белка повышен и коррелирует с активностью воспалительного процесса при различных заболеваниях суставов (при ревматоидном артрите). При остеоартрозе этот показатель находится в переделах нормы или повышен незначительно.
- Мочевая кислота в сыворотке. Конечный продукт распада пуриновых соединений, которые входят в состав всех клеток организма. В организме пурины появляются в результате естественной гибели клеток, а также часть поступает с пищей (с красным мясом, красным вином). При избыточном накоплении мочевой кислоты (вследствие повышенного ее образования или недостаточного выведения) развивается специфическое воспаление суставов – подагра. Анализ может быть использован для дифференциальной диагностики остеоартроза и подагры.
- Рентгенография. Позволяет выявить характерные изменения в суставах на разных стадиях заболевания (например, сужение суставной щели, формирование костных выростов – остеофитов).
- Магнитно-резонансная томография (МРТ). Принцип метода основан на воздействии на структуры организма сильного магнитного поля, затем полученная информация регистрируется и обрабатывается на компьютере. Послойные изображения суставов дают возможность оценить степень дегенеративных изменений с высокой точностью, что важно для определения дальнейшей тактики лечения.
- Артроцентез – пункция сустава. Производится с помощью специальной иглы со шприцом. На лабораторный анализ берется синовиальная жидкость. Исследование помогает отличить остеоартроз от других заболеваний суставов, которые могут вызывать похожие проявления.
Обратить изменения, которые уже произошли в пораженных суставах при остеоартрозе, нельзя. Целью консервативной терапии является уменьшение выраженности симптомов заболевания, замедление процессов дегенерации и разрушения суставных хрящей.
Применяются следующие основные группы препаратов:
- нестероидные противовоспалительные препараты – способствуют уменьшению воспаления и болей;
- кортикостероиды – препараты гормонов коры надпочечников, которые обладают противовоспалительным действием; при остеоартрозе используются в виде внутрисуставных инъекций;
- препараты, укрепляющие хрящевую ткань – группа лекарств, в состав которых входят компоненты хрящевой ткани (хондроитина сульфат, гиалуроновая кислота, глюкозаминогликаны); способствуют замедлению процессов дегенерации хрящевой ткани.
Из хирургических методов применяется остеотомия (рассечение костей с их последующей фиксацией), способствующая более выгодному положению кости для снижения нагрузки на сустав, протезирование.
Важную роль в лечении играет изменение образа жизни, выполнение комплексов физических упражнений для укрепления мышечно-связочного аппарата суставов.
- Сохранение нормальной массы тела.
- Выполнение физических упражнений, но без чрезмерной нагрузки на отдельные суставы.
- Избегание длительного пребывания в фиксированных позах.
Рекомендуемые анализы
Литература
- Dan L. Longo, Dennis L. Kasper,J. Larry Jameson, Anthony S. Fauci, Harrison's principles of internal medicine (18th ed.). New York: McGraw-Hill Medical Publishing Division, 2011.Chapter 332. Osteoarthritis.
Артроз – заболевание, развивающееся медленно, на первой стадии практически незаметно для пациента. Мало, идущих в медицинское учреждение при обнаружении первичных симптомов заболеваний коленного, тазобедренного, других суставов.
Независимо от стадии артроза, опроса больного с уточнением жалоб, осмотра недостаточно. Чтобы не спутать артроз с иными заболеваниями, симптомы которых могут быть схожими, стоит провести клинические анализы, исследования. Полученные результаты позволяют установить точный диагноз, назначить правильное, эффективное лечение коленного, голеностопного, тазобедренного сустава.
Список исследований
Анализа, который сразу определит присутствие остеоартроза сустава не существует. Есть исследования, позволяющие исключить наличие других патологий. К ним относятся:
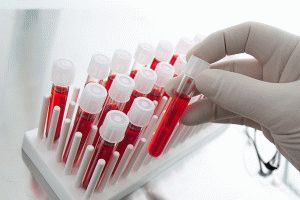
- Клинический, биохимический анализы крови;
- Рентгенографический анализ;
- Магниторезонансная, компьютерная томография;
- УЗИ;
- Артроскопия.
Рентгенографическое исследование позволяет выявить артроз, определить степень заболевания, нарушения, вызванные им. Благодаря снимку выявляются признаки, свидетельствующие о наличии артроза, не иных патологий коленного, тазобедренного, других суставов. К признакам относятся: существенное уменьшение зазоров между суставообразующими костями, уплотнение хрящевой ткани, присутствие остеофитов, наличие костных разрастаний. Рентгеновский анализ считается главным при диагностике суставных заболеваний. Бывают случаи, когда снимок не даёт точных ответов, вызывает сомнения по поводу установки точного диагноза (на ранней стадии артроза сложно выявить разрушение, деформацию суставов). В таких случаях прибегают к МРТ обследованию.
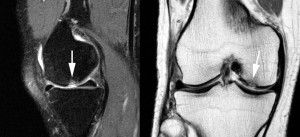
Магниторезонансная томография позволяет получать чёткое изображение, чем при рентгеновском анализе. МРТ отличается стоимостью, которая в разы выше рентгена. Но исследование позволяет подтвердить, опровергнуть наличие остеоартроза – на снимке чётко видны суставные кости, мягкие ткани (капсулы, мениски, хрящи, связки). В обычных поликлиниках не имеется оборудования для проведения таких анализов, при подозрениях наличия артроза лучше обращаться в специализированные клиники, центры.
Компьютерная томография назначается, если пациенту противопоказано проведение МРТ-обследования (при наличии кардиологического стимулятора и др.), нет возможности провести его. КТ позволяет получить изображение всех прослоек сустава. Обследование представляет нечто среднее между рентгеном и МРТ.
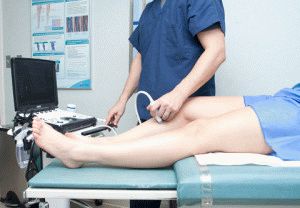
При помощи ультразвукового анализа можно оценить степень изношенности, утончения хрящевой прослойки, проследить количественное изменение жидкости, скапливаемой в суставе. УЗИ редко назначают для диагностирования артроза, анализ позволяет определить сложность ситуации. УЗИ коленного сустава позволяет увидеть степень сохранности менисков, определить наличие, отсутствие кисты Бейкера, кристаллов кислоты мочевой. Объективно описать картину болезни может узкопрофильный врач – УЗИст.
Артроскопия назначается реже, чем УЗИ. Обследование осуществляется путём введения камеры в небольшие надрезы в области суставов. На экране можно увидеть особенности структуры поражённого сустава. Артроскопия уместна при артрозе тазобедренных суставов, применима для коленного, иных суставов.
Для получения полной картины заболевания, оценки ситуации стоит проводить комплексное обследование, в котором внимание уделить анализам крови.
Какие анализы крови сдать при артрозе
Анализы при артрозе назначаются не для его выявления, а для исключения других болезней, сужая круг возможных диагнозов. Кровь при артрозе назначают и сдают в лабораториях медицинских учреждений двух видов: клиническое исследование, биохимия.
Особенность клинического исследования крови заключается, в том, что при наличии артроза он имеет нормальные показания. Часто отслеживается колебание показателей скорости оседания эритроцитов (СОЭ) – красных тел крови.
Если СОЭ повышен, при этом присутствует болевой синдром, то можно говорить о присутствии процессов, носящих ревматический характер. Боли усиливаются утром, ночью, это свидетельствует об артрите, ревматизме, не остеоартрозе. Если СОЭ повышен до уровня 25 мм и больше, то это свидетельствует о присутствии воспаления в суставах. При высоком уровне СОЭ, лейкоцитов в организме происходит воспаление инфекционного характера, отображаются на состоянии суставов нижних конечностей.

При разрушении хрящевой прослойки в суставах ног отклонений в клинических анализах не наблюдается. Все показатели остаются на уровне нормы. В редких случаях артроза, которые сопровождаются скапливанием синовиальной жидкости в суставе (синовит), СОЭ может иметь значительно повышенный уровень. Когда уровень СОЭ в крови повышен, можно говорить о наличии процессов воспаления, характер которых стоит выяснять при помощи дополнительных анализов.
Второй вариант анализа крови при артрите – биохимический. Биохимия крови (берётся кровь с вены) при артрозе осуществляется на голодный желудок (пациент не должен есть минимум 6 часов, в идеале 12). Это позволит получить более чистые показатели. При помощи анализа можно определить, присутствует ли процесс воспаления в организме. Позволяет отличать артрит от артроза.
При артрите наблюдается завышенный показатель C-реактивного белка, серомукоидов, различных видов иммуноглобулинов. Все эти показатели при артрозе остаются в приемлемых рамках нормы. Поэтому сдача БАКа важна при подозрениях на артрит или артроз. Их симптоматика схожа, отличить позволяет анализ крови, показывающий присутствие, отсутствие воспаления в суставах.
Артроз – заболевание не воспалительного характера, отклонения от нормы показателей свидетельствуют о других патологиях. Наличие мочевой кислоты говорит о подагре, высокий уровень глобулинов, иммуноглобулинов – о ревматоидном артрите.
При помощи проведения описанного списка анализов врачи разграничивают, какие могут быть проблемы – заболевания суставов воспалительного характера, артрозы.
Медицинский эксперт статьи

В большинстве случаев у больных с остеоартрозом отсутствуют изменения в анализах крови и мочи, за исключением случаев синовита со значительным выпотом, когда могут возникнуть увеличение СОЭ, гипергаммаглобулинемия, повышение уровня показателей острой фазы - СРБ, фибриногена и др. При исследовании синовиальной жидкости значительных отличий от нормальных показателей не выявляют.
При остеоартрозе патологические изменения происходят главным образом в суставном хряще, а также в субхондральной кости, синовиальной оболочке, других мягких тканях сустава. Поскольку наши возможности непосредственно исследовать эти структуры ограничены, наиболее важными источниками для забора биологических маркеров являются кровь, моча и синовиальная жидкость.
Исследование мочи наиболее предпочтительно, поскольку не сопряжено с какими-либо инвазивными процедурами. На наш взгляд, идеальным материалом для исследования является суточная моча. Анализ утренней порции мочи был бы более целесообразным, однако возможность ее использования основывается лишь на том, что именно такой анализ используют для определения биологических маркеров костного метаболизма при остеопорозе: известно, что биологические маркеры подчиняются циркадным ритмам, а пик концентрации биологических маркеров костного метаболизма приходится на ночные часы. К настоящему времени в литературе отсутствуют сведения о циркадных ритмах биологических маркеров мягких тканей, хряща, поэтому окончательное решение о выборе адекватного анализа мочи будет принято после проведения соответствующих исследований.
Исследование крови относится к рутинным клиническим анализам. Некоторые биологические маркеры в крови определяют уже сегодня, например показатели острой фазы, другие, возможно, в ближайшем будущем войдут в стандартный перечень биохимических тестов. Для каждого биологического маркера необходимо уточнить, в каком компоненте крови его следует определять - в плазме или сыворотке. Результаты исследований свидетельствуют о том, что концентрация биологических маркеров в плазме крови значительно отличается от таковой в сыворотке. Обычно биологические маркеры определяют в сыворотке крови. По данным V. Rayan и соавторов (1998), концентрации биологических маркеров в крови, взятой из вены вблизи пораженного сустава и из более отдаленной вены, различны. Эти данные свидетельствуют о необходимости стандартизации забора крови для исследования биологических маркеров.
Поданным L.J. Attencia и соавторов (1989), хрящ синовиальных суставов взрослого человека составляет всего 10% от общей массы гиалинового хряща организма, включая межпозвоночные диски. Таким образом, определение биологических маркеров в крови и моче скорее отражает системный метаболизм, чем местные изменения в пораженном остеоартрозом суставе. Синовиальная жидкость находится ближе всего к патологическому очагу при остеоартрозе и, вероятно, наиболее точно отражает процессы, происходящие в пораженном суставе. Концентрация биологических маркеров в синовиальной жидкости может быть значительно выше, чем в крови, а значит, ее легче определить. Примерами могут служить эпитоп 846 аггрекана - в синовиальной жидкости его в 40 раз больше, чем в сыворотке крови, хрящевые олигомерные матриксные белки (ХОМБ) - в 10 раз больше, чем в сыворотке крови. Продукты деградации в синовиальной жидкости более точно отражают катаболические процессы в суставном хряще. Дренаж молекул из синовиальной жидкости через местную лимфатическую систему может привести к уменьшению их размеров и даже к их разрушению.
Несмотря на инвазивность методики забора синовиальной жидкости, сопряженной с рядом возможных осложнений, ценность определения биологических маркеров в ней очевидна. Для избежания проблем с так называемым сухим суставом непосредственно перед изъятием жидкости в сустав можно ввести 20 мл изотонического раствора NaCl. Тотчас после инъекции изотонического раствора пациент должен произвести 10 раз сгибание-разгибание конечности в суставе, за этим следует быстрая аспирация разведенной синовиальной жидкости. По мнению E.M.-J.A. Thonar (2000), такое разведение синовии влияет на метаболизм в суставном хряще. Однако результаты исследования F.C. Robion и соавторов (2001) свидетельствуют о том, что повторный лаваж коленных суставов лошадей не вызывает существенных изменений метаболизма хряща. Эти данные, безусловно, требуют подтверждения. Следовательно, для каждого биологического маркера на этапе преклинических исследований у животных необходимо определять влияние лаважа сустава на изменение его концентрации.
Следующим важным моментом является определение для каждого биологического маркера времени полужизни в синовиальной жидкости и в крови. Без таких данных интерпретация результатов анализов будет затруднена. Обычно время полужизни биологически активных веществ в крови меньше, чем в других жидких средах, в связи с эффективным клиренсом печенью и почками. Таким образом, для каждого биологического маркера также необходимо определять путь элиминации. Так, N-пропептид коллагена III типа выделяется печенью путем рецепторопосредованного эндоцитоза, а негликозилированные фрагменты коллагена выводятся главным образом смочойтакже, какостеокальцин. Наэндотелиальных клетках синусов печеночных долек имеются рецепторы к гликозаминогликанам, поэтому гиалуроновая кислота и протеогликаны элиминируются печенью. Время полужизни гиалуроновой кислоты в крови составляет 2-5 мин. Наличие синовита может ускорять клиренс биологических маркеров из суставов, хотя исследование у кроликов не обнаружило существенных различий клиренса протеогликанов при наличии и отсутствии синовита. Таким образом, необходимо исследовать влияние воспаления на изменения концентрации биологических маркеров в жидких средах организма.
Почки селективно фильтруют биологические маркеры. Так, гликозаминогликаны, несущие большой отрицательный заряд, могут не проникать через базальную мембрану почек, тогда как такие гликозаминогликаны, как хондроитин-6-сульфат и хондроитин-4-сульфат, определяются в моче.
Кроме патологии (в частности, остеоартроза) на концентрацию биологических маркеров в жидких средах организма могут влиять ряд факторов:
- Циркадные ритмы исследованы лишь для небольшого количества биологических маркеров. Для маркеров костного метаболизма они изучены. Так, пик концентрации остеокальцина приходится на ночные часы, а поперечных связей коллагена на утренние - на 8 ч. При ревматоидном артрите пик активности ИЛ-6 также приходится на ночные часы (около 2 ч), причем раньше, чем у остеокальцина. Эти данные представляют определенный интерес в отношении участия ИЛ-6 в воспалении и физиологии костной ткани. ФНО-а, напротив, не имеет циркадныхритмов. Однако рецепторы этого цитокина могут подчиняться им.
- Перистальтика. Гиалуроновая кислота синтезируется синовиальными клетками (а также многими другими клетками) и является потенциальным маркером синовита при остеоартрозе и ревматоидном артрите. Однако наиболее высокая концентрация гиалуроната обнаруживается в лимфатической системе кишечника. Не удивительно, что концентрация циркулирующей гиалуроновои кислоты может повышаться после еды. Таким образом, забор крови для определения биологических маркеров следует производить натощак или через 3 ч после еды. А влияние перистальтики на уровень биологических маркеров в крови требует изучения.
- Физическая активность утром после сна приводит к повышению концентрации гиалуроновои кислоты в крови, ММП-3 и эпитопа кератан-сульфата у здоровых лиц. Физическая нагрузка может изменять концентрацию некоторых маркеров как в синовиальной жидкости, так и в сыворотке крови. Такое повышение более выражено у больных с ревматоидным артритом, более того концентрация биологических маркеров коррелирует с клиническим состоянием этих больных.
- Болезни печени и почек. Цирроз печени вызывает значительное повышение уровня гиалуроновои кислоты в сыворотке крови и, вероятно, влияет на элиминацию протеогликанов. Известно, что болезни почек влияют на концентрацию остеокальцина. Данная проблема также требует более глубокого изучения.
- Возраст и пол. В процессе роста организма повышается активность клеток пластинки роста, что сопровождается повышением концентрации скелетных биологических маркеров в сыворотке крови. Примером может служить повышение концентрации фрагментов аггрекана и коллагена II типа в периферической крови и моче у растущих животных. Таким образом, интерпретация анализов биологических маркеров у детей и подростков с заболеваниями опорно-двигательного аппарата затруднена. Для многих биологических маркеров обнаружено повышение концентрации при старении. У мужчин концентрация биологических маркеров значительно превышает таковую у женщин в хрящевой и костной тканях. Кроме того, у женщин в менопаузальный и постменопаузальный периоды можно ожидать изменений концентрации биологических маркеров метаболизма хрящевой ткани подобно тому, что наблюдается в костной ткани.
- Хирургические операции также могут влиять на уровень биологических маркеров, более того, этот эффект может длиться несколько недель.
Основой концепции биологических маркеров остеоартроза является предположение, что они отражают определенные стороны метаболических процессов в тканях суставов. Однако взаимоотношения между концентрациями биологических маркеров в жидких средах организма и метаболизмом хрящевой, синовиальной и других тканей оказались очень сложными.
Так, например, концентрация маркеров деградации ВКМ суставного хряща в синовиальной жидкости может зависеть не только от степени деградации самого матрикса, но и от других факторов, таких, как степень элиминации фрагментов молекул из синовии, о чем уже было сказано выше, а также от количества хрящевой ткани, оставшейся в суставе.
Несмотря на вышеприведенные факты, концентрация биологических маркеров в синовиальной жидкости в общем коррелирует с метаболизмом молекул ВКМ суставного хряща. Так, например, изменения концентрации фрагментов аггрекана, эпитопа 846, ХОМБ и С-пропептида коллагена II в синовиальной жидкости после травмы сустава и при развитии остеоартроза согласуются с изменениями интенсивности метаболизма аггрекана, ХОМБ и коллагена II в экспериментальных моделях остеоартроза у животных/и vivo и в суставном хряще больных с остеоартрозом /и vitro.
Идентификация специфических источников молекулярных фрагментов - сложный процесс. Повышение степени высвобождения фрагментов молекул может происходить как за счет общего усиления процессов деградации, которые не компенсируются синтетическими процессами, так и за счет усиления деградации с одновременным повышением интенсивности синтеза тех же молекул ВКМ; в последнем случае концентрация молекул ВКМ не изменяется. Таким образом, необходим поиск маркеров, специфических для деградации и для синтеза. Примером первых могут быть фрагменты аггрекана, а вторых - С-пропептид коллагена 11.
Даже если биологический маркер связан с определенным аспектом метаболизма, необходимо учитывать специфические особенности этого процесса. Например, идентифицируемые фрагменты могут образовываться в результате деградации синтезированной de novo молекулы, которая еще не успела встроиться в функциональный ВКМ, молекулы, которая была только что встроена в ВКМ и, наконец, постоянной молекулы ВКМ, которая является важной функциональной частью зрелого матрикса. Проблемой также является определение специфической зоны матрикса (перицеллюлярный, территориальный и межтерриториальный матрикс), которая послужила источником биологических маркеров, обнаруженного в синовиальной жидкости, крови или моче. Исследования in vitro свидетельствуют о том, что интенсивность метаболизма в отдельных зонах ВКМ суставного хряща может быть различной. Исследование некоторых эпитопов, связанных с сульфатированием хондроитин сульфатов, могут способствовать идентификации популяции синтезированных de novo молекул аггрекана.
Можно предположить, что появление в суставной жидкости фрагментов молекул, в норме присутствующих в ВКМ хряща, связано с метаболизмом хрящевого матрикса. Однако это не всегда так, поскольку зависит от ряда факторов, в частности от того, насколько концентрация данной молекулы в суставном хряще превышает таковую в других тканях сустава и насколько интенсивность ее метаболизма в хряще превышает таковую в других тканях сустава. Так, общая масса аггрекана в суставном хряще значительно превышает таковую, например в менисках коленного сустава, при этом общая масса ХОМБ в менисках практически не отличается от таковой в суставном хряще. И хондроциты, и синовициты вырабатывают стромелизин-1, однако общее количество клеток в синовиальной оболочке превышает таковое в хряще, поэтому значительная часть обнаруженного в синовиальной жидкости стромелизина-1 скорее всего синовиального происхождения. Таким образом, идентификация специфического источника биологических маркеров чрезвычайно сложна и часто невозможна.
При исследовании биологических маркеров в сыворотке крови и моче появляется проблема определения возможного его внесуставного источника. Кроме того, при моноартикулярном поражении биологическими маркерами, выделяемые пораженным суставом, могут смешиваться с маркерами, выделяемыми интактными суставами, в том числе и контралатеральными. В состав суставного хряща входит менее чем 10% общей массы гиалинового хряща организма. Таким образом, определение биологических маркеров в крови и моче может быть обоснованным скорее при полиартикулярных, или системных, болезнях (применительно к остеоартрозу - при генерализованном остеоартрозе).
Требования к биологическим маркерам зависят оттого, с какой целью их применяют - в качестве диагностического, прогностического или оценочного теста. Например, диагностический тест определяет различия между здоровыми лицами и пациентами с остеоартрозом, что выражается понятием чувствительности и специфичности теста. Прогностический тест выявляет в когорте лиц, у которых наиболее вероятно быстрое прогрессирование болезни. И наконец, оценочный тест базируется на способности маркера мониторировать изменения во времени у отдельного пациента. Кроме того, биологические маркеры можно применять для определения чувствительности пациентов к тому или иному препарату.
Вначале предполагали, что биологические маркеры могут служить диагностическими тестами, которые помогут отличить пораженный остеоартрозом сустав от интактного, а также провести дифференциальную диагностику с другими болезнями суставов. Так, определение концентрации кератан сульфата в сыворотке крови рассматривали как диагностический тест для генерализованного остеоартроза. Однако последующие исследования показали, что данный биологический маркер может лишь отражать деградацию протеогликанов хряща в некоторых ситуациях. Оказалось, что концентрации биологических маркеров в сыворотке крови зависят от возраста и пола обследуемого лица.
Предполагаемые биологические маркеры метаболизма тканей суставов в синовиальной жидкости и сыворотке крови больных с остеоартрозом
Читайте также:


