Кальцификация плода что это
Первое описание пренатальной диагностики инфантильной артериальной кальцификации в 1990 г. принадлежит R. Spear и соавт. В опубликованном ими наблюдении была обнаружена не только кальцификация аорты, но и самого сердца. В последующие годы было опубликовано еще несколько случаев пренатальной ультразвуковой диагностики ИАК, но во всех наблюдениях диагноз был установлен только во второй половине беременности.
В опубликованном нами наблюдении ИАК была заподозрена уже в 13 нед. При оценке сердца плода была обнаружена гиперэхогенная во всех отделах межжелудочковая перегородка. Ее эхогенность была настолько высокой, что она была сравнима с эхогенностью костей плода. При этом размеры желудочков и предсердий были практически одинаковыми, так же как и диаметры главных артерии. Нарушений кровотока через атриовентрикулярные клапаны и клапаны главных артерий не было зарегистрировано не было. Сочетанных пороков не обнаружено. Полученные данные не укладывались ни в одну из описанных нозологических форм, диагностированных в ранние сроки беременности.
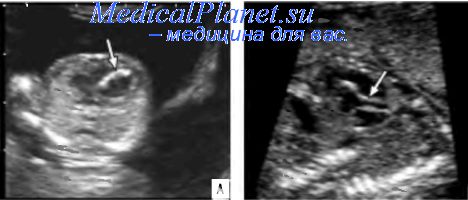
Наиболее вероятный предположительный диагноз, высказанный консультативно, сводился к ИАК, но она обычно сопровождается изменением аорты, а в представленных цифровых материалах аорта была не изменена. На основании полученных данных и их обсуждения было решено провести контрольное обследование в динамике. В 16 нед беременности отмечено выраженное превалирование диаметра легочной артерии над аортой, что свидетельствовало о формировании ее гипоплазии. В 20 нед беременности на фоне сохраняющейся гиперэхогенной межжелудочковои перегородки зарегистрировано выраженное повышение эхогенности стенок аорты, диаметр которой был даже меньше диаметра верхней полой вены. Соответственно было обнаружено превалирование размеров правого желудочка над левым. Таким образом, в 20 нед беременности были зарегистрированы характерные изменения аорты, что дало основание установить диагноз ИАК.
Учитывая неблагоприятый прогноз, беременность прервана в 23 нед по медицинским показаниям. При микроскопическом исследовании было обнаружено, что эндокард в области перегородки и левых отделов сердца резко утолщен (в 10-15 раз) за счет разрастания эластических волокон и в меньшей степени коллагеновых, располагающихся параллельными слоями. Внутренняя оболочка аорты утолщена за счет разрастания эластических волокон и очагов петрификации.
Аномалия Уля - редкая врожденная патология, проявляющаяся выраженной гипоплазией или почти полным отсутствием миокарда одного из желудочков сердца. В основном при данной аномалии поражается миокард правого желудочка. Чаще всего гипоплазия бывает диффузной, хотя возможна очаговая форма. Трикуспидальный клапан может быть нормальным или дисплазированным. В некоторых случаях отмечаетя стеноз или атрезия легочного клапана. Аномалия Уля обычно диагностируется на секции и составляет 0,1% от числа всех ВПС.
В ходе пренатального ультразвукового исследования, в первую очередь обращает на себя внимание выраженная кардиомегалия за счет дилатации пораженного желудочка. Миокард желудочка едва различим, а сократительная способность минимальна. Нередко поэтому при аномалии Уля регистрируются признаки застойной сердечной недостаточности (перикардиальный, плевральный выпоты, асцит).
Впервые о пренатальной ультразвуковой диагностике аномалии Уля в 24 нед беременности сообщили G. Wager и соавт. Е.П. Затикян и соавт. удалось диагностировать этот порок сердца пренатально в 23-24 нед беременности. В представленном ими наблюдении при ультразвуковом исследовании плода наряду с выраженной дилатацией полости левого желудочка отмечалось выраженное истончение миокарда его задней стенки (1 мм). При этом также констатировано практически полное отсутствие сокращения миокарда левого желудочка в различные фазы сердечного цикла. В плевральной полости определялось небольшое количество свободной жидкости. Отмечена также умеренно выраженная брадикардия - 110 уд/мин. Показатель ударного объема сердца оказался сниженным и составил 70% от средних нормативных величин.
С. Benson и соавт. сообщают о случае, в котором аномалия Уля, обнаруженная в 18-19 нед беременности, была расценена как аномалия Эбштейна и только при патологоанатомическом исследовании был установлен правильный диагноз. Авторы указывают на существенные трудности, возникающие при дифференциальной диагностике аномалии Уля с аномалией Эбштейна в начале II триместра беременности, так как оба этих порока сопровождаются выраженной кардиомегалией за счет правых отделов сердца. По мнению R. Oberhoffer и соавт., ключом к правильной пренатальной диагностике аномалии Уля является визуализация нормального (несмещенного) трикуспидального клапана на фоне дилатированного правого предсердия и истонченного миокарда правого желудочка.

- Что это такое?
- Причины развития
- В чем кроется опасность?
- Клинические варианты
- Как проявляется?
Нормальная структура плаценты обеспечивает физиологичное внутриутробное развитие плода. Наличие структурных дефектов и различных аномалий плацентарной ткани значительно затрудняет течение здоровой беременности.
Эта статья расскажет о том, что означает кальциноз плаценты, а также в каких формах он бывает.

Что это такое?
Определить структуру плацентарной ткани можно посредством проведения ультразвукового обследования. Во время проведения УЗИ доктор оценивает плотность, толщину и другие параметры плаценты. В норме плацентарная ткань до 30-32 недели беременности имеет довольно гладкую наружную поверхность. При этом сама плацентарная ткань имеет довольно однородную (гомогенную) структуру, в которой нет никаких дополнительных включений или определяемых образований.
Если же плацента имеет негомогенную структуру, то в таком случае довольно часто в ней обнаруживаются различные кальцинаты — уплотненные участки. Обычно кальцинирование плаценты происходит в третьем, завершающем, триместре беременности. Чем ближе к родам, тем, как правило, большсроке вероятность обнаружения различных кальцинатов в плацентарной ткани.
Если во время обследования плаценты на более ранних сроках беременности были обнаружены плотные участки (кальцинаты), то такое состояние врачи называют кальцинозом. Оно регистрируется в акушерской практике нередко. При кальцинозе кальцинаты обычно обнаруживаются на 26-30 неделе беременности, реже — на более ранних сроках.

Причины развития
Появление кальцинатов в плаценте на 34-36 неделе беременности не должно стать поводом для беспокойства для будущей мамы. На этом сроке даже в здоровой плаценте начинают происходить определенные структурные изменения. Это является своеобразной подготовкой организма к предстоящим родам.
Если же кальцинаты в плацентарной ткани были выявлены гораздо раньше, то в такой ситуации врачи стараются выявить возможную причину развития этого состояния. За будущей мамой, у которой было выявлено такое состояние, в таком случае проводят тщательное врачебное наблюдение.

Врачи выделяют несколько состояний, при которых прогноз развития кальциноза плаценты увеличивается:
- наличие вредных привычек у беременной женщины (курение, злоупотребление алкоголем);
- инфекции мочеполовой системы, передающиеся половым путем;
- некоторые бактериальные, вирусные и грибковые заболевания;
- наличие сопутствующих патологий внутренних органов;
- тяжело протекающий гестоз;
- тяжелая степень анемии;
- хронические заболевания репродуктивных органов (эндометриоз, миома, аномалии развития матки и многие другие).



Считается, что развитие данного состояния является следствием какого-либо патологического процесса, при котором нарушается кровоснабжение плацентарной ткани. Сильное сужение кровеносных капилляров может привести к нарушению поступления питательных веществ и кислорода к определенным участкам плаценты. Существенное уменьшение кровотока приведет к развитию функциональных нарушений, что в конечном итоге будет способствовать образованию уплотненных участков измененной ткани — кальцинатов.
В кальцинированном участке плацентарной ткани откладывается довольно много кальция. Именно из-за этого кальцинат имеет характерный вид и плотность. Кальцинированные участки плаценты гораздо тверже остальной ткани, которая в норме довольно рыхлая и мягкая.

В чем кроется опасность?
Наличие множественных кальцинатов в плаценте опасно тем, что нарушается ее функционирование. В таком случае плод не получает достаточное количество питательных компонентов и кислорода. Это в целом отрицательно влияет на весь процесс внутриутробного развития.
Сильное нарушение обеспечения организма развивающего в материнской утробе малыша может быть опасно развитием фетоплацентарной недостаточности — крайне опасного состояния. Если патологическое состояние будет продолжать прогрессировать, то это даже может способствовать преждевременным родам.


Клинические варианты

Как проявляется?
Течение кальциноза может быть как бессимптомным, так и приводить к появлению различных клинических признаков. Во многом это зависит от того, какие размеры имеют кальцинаты, а также от их количества.
Так, если уплотненные участки множественные, то в таком случае прогноз течения беременности обычно ухудшается. Чем больше поврежденной ткани, тем меньше плацента выполняет свои функции, предназначенные ей природой.
Единичные мелкие кальцинаты обычно никак не влияют на течение развивающейся беременности. Они выявляются, как правило, случайно – во время проведения планового УЗИ. В этом случае повседневная жизнь беременной женщины практически никак не изменяется. У нее отсутствуют неблагоприятные симптомы, характерные для тяжелого течения кальциноза плаценты. Общее состояние плода при этом также не нарушается.

Неблагоприятным признаком является и изменение частоты сердечных сокращений у плода. Этот показатель работы сердца позволяет врачам оценивать общее состояние плода, находящегося в материнской утробе. У ребенка может развиться тахикардия или брадикардия. В этой ситуации требуется обязательное вмешательство врачей для компенсации общего состояния малыша.

Если кальциноз плаценты обнаружен, а до родов еще далеко, то будущей маме назначается терапия. Она включает в себя не только применение лекарственных препаратов, но и подразумевает соблюдение строгих рекомендаций о ведении режима дня и отдыха.
Так, для коррекции возникших нарушений гемодинамики врачи могут прибегнуть к назначению лекарственных средств, которые улучшают кровоток. Оценить динамику при этом можно посредством проведения КТГ. Нормализация скорости сердечного ритма плода и его двигательной активности свидетельствуют об улучшении его общего самочувствия на фоне назначенной терапии.
Добиться полного исчезновения кальцинатов из плацентарной ткани на фоне лечения нельзя, да и не требуется. Целью терапии при кальцинозе является нормализация нарушенных функций, которые выполняет плацента. Также назначение лекарственных препаратов помогает снизить риск развития опасных осложнений течения беременности.

О структуре и функциях плаценты смотрите в следующем видео.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Код по МКБ-10
- Причины
- Факторы риска
- Симптомы
- Формы
- Осложнения и последствия
- Диагностика
- Дифференциальная диагностика
- Лечение
- Профилактика
- Прогноз
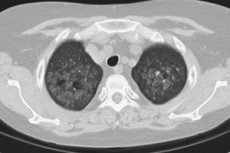
Что значит кальциноз? Это образование скоплений нерастворимых кальциевых солей там, где их наличие не предусмотрено ни с анатомической точки зрения, ни с физиологической, то есть вне костей.
Среди всех биогенных макроэлементов человеческого организма доля кальция – в форме кристаллов гидроксилапатита костной ткани – самая значительная, хотя кровь, клеточные мембраны и внеклеточная жидкость тоже содержат кальций.
И если уровень данного химического элемента значительно повышен, то развивается кальциноз – нарушение минерального обмена (код Е83 по МКБ-10).

[1], [2], [3], [4], [5], [6], [7], [8]
Код по МКБ-10
Причины кальциноза
Метаболизм кальция – многоступенчатый биохимический процесс, и на сегодняшний день ключевые причины кальциноза, как одной из разновидностей нарушения минерального обмена, определены и систематизированы. Но, с учетом тесной взаимосвязи всех протекающих в организме обменных процессов, в клинической эндокринологии принято одновременно рассматривать и патогенез отложения кальцинатов (или кальцификатов).
Первостепенной причиной известковой дистрофии признана перенасыщенность крови кальцием – гиперкальциемия, этиологию которой связывают с повышенным остеолизом (разрушением костной ткани) и высвобождением кальция из костного матрикса.
Из-за гиперкальциемии, а также гипертиреоза или патологий паращитовидных желез сокращается выработка щитовидной железой кальцитонина, который регулирует содержание кальция, угнетая его выведение из костей. Предполагается, что именно наличие скрытых проблем со щитовидной железой у женщин в период постменопаузы – в совокупности со снижением уровня эстрогенов, удерживающих кальций в костях – появляются внекостные кальциевые отложения, то есть развивается кальциноз при остеопорозе.
Есть и другие патологические состояния, которые заставляют кальциевые соли концентрироваться в неположенных местах. Так, у пациентов с первичным гиперпаратиреозом, гиперплазией паращитовидных желез или их гормонально активной опухолью синтез паратиреоидного гормона (паратгормона или ПТГ) возрастает, в результате чего подавляется действие кальцитонина, а уровень кальция в плазме крови, как и деминерализация костей, повышается.
Механизм повышенного остеолиза с выходом фосфата и карбоната кальция из костных депо при наличии раковых опухолей любой локализации объясняют так называемым паранеопластическим синдромом: рост злокачественных неоплазий сопровождается гиперкальциемией, так как мутировавшие клетки способны продуцировать полипептид, по действию подобный паратгормону.
Общеизвестно, что патогенез образования кальциевых солей может быть обусловлен избытком витамина D, с которым в эндокринологии связывают увеличение синтеза 1,25-дигидрокси-витамина D3 – кальцитриола, активно участвующего процессе метаболизма кальция и фосфора. Причастны к развитию известковой дистрофии гипервитаминоз витамина А, приводящий к остеопорозу, а также дефицит поступающего с пищей витамина K1 и эндогенного витамина K2.
При отсутствии эндокринных патологий содержание в плазме крови общего кальция не выходит за пределы физиологической нормы, и тогда причины кальциноза иные, обусловленные местными факторами. В их числе осаждение фосфата кальция на мембранах органоидов поврежденных, атрофированных, ишемизированных или погибших клеток, а также повышение уровня рН жидкости межклеточного пространства из-за активизации щелочных гидролитических ферментов.
Далеко не последнее место в этиологии нарушения кальциевого обмена отводится сдвигу водородного показателя кислотности крови (pH) в щелочную сторону при частичной дисфункции физико-химической буферной системы крови (бикарбонатной и фосфатной), поддерживающей кислотно-щелочное равновесие. Одной из причин его нарушения, приводящего к алкалозу, признан синдром Бернетта, который развивается у тех, кто употребляет много содержащих кальций продуктов, принимая от изжоги или гастрита пищевую соду или нейтрализующие кислоту желудочного сока антациды, адсорбирующиеся в ЖКТ.
Считается, что любое из названных выше эндокринных нарушений усугубляет чрезмерное поступление кальция с пищевыми продуктами. Однако, как утверждают исследователи Harvard University, до сих пор нет веских подтверждений того, что кальций пищи повышает вероятность кальцификации тканей, поскольку не вызывает стойкого повышения уровня Са в крови.

[9], [10], [11], [12], [13], [14], [15], [16]

Кальциноз плаценты — это образование отложений солей кальция в мягких тканях или органах, в которых соли в нерастворённом состоянии содержаться не должны. Какие причины и последствия имеет патологическое изменение в организме, происходящее до 37 недели беременности? Учёные смогли это выяснить.
Особенности и методы исследования
Перед сообществом учёных встала цель, которая подразумевала оценку роли преждевременной кальцификации плаценты в развитии неблагоприятных последствий для беременности. Также исследователям необходимо было определить ассоциированные потенциальные факторы риска, как для женщины, так и для плода.
Учёные включили в исследование 293 женщины, которые наблюдались в трех медицинских центрах.
Чтобы оценить риск опасности от кальцификации и степень зрелости плаценты, исследователи пациенткам проводили трансабдоминальное УЗИ на сроках 28−36 недель беременности. Учачтницы поделились на две группы:
- Женщины, у которых плацента достигла степени зрелости 3 (n = 69);
- Женщины, у которых плацента не достигла степени зрелости 3 (n = 224).
Пассивное курение было единственным предиктором ранней кальцификации плаценты. У женщин, у которых был диагностирован кальциноз плаценты, чаще наблюдались аномальные показания допплеровского исследования и низкий вес ребенка при рождении, а также чаще проводилось оперативное родоразрешение. Не было выявлено никакой связи между гипертензией матери, диабетом, а также другими заболеваниями и формированием кальциноза плаценты.
В заключение стоит отметить, что индекс резистентности в артерии пуповины и отсутствие или изменение (реверсивное) обратной диастолической скорости кровотока чаще регистрировались у пациенток с кальцификацией плаценты до 37 недели гестации. Для таких женщин рекомендуется особо тщательное наблюдение до родов.
Заключение
Кальциноз плаценты — физиологическое явление, однако, в норме плацента не должна достигать степени зрелости 3 до 36−37 недель гестации (так называемая преждевременная кальцификация плаценты, ПКП). В настоящий момент имеется недостаточно данных о клиническом значении преждевременной кальцификации плаценты и исходов беременности. Это исследование было разработано с целью оценить роль преждевременной кальцификации плаценты в развитии неблагоприятных исходов беременности.
Несмотря на тот факт, что в данном исследовании не было курящих пациенток, учёные обнаружили, что пассивное курение было единственным предиктором формирования преждевременной кальцификации плаценты. Аномальное изменение формы доплеровского сигнала артерии пуповины и отсутствие обратной диастолической скорости кровотока чаще наблюдались у женщин с преждевременной кальцификацией плаценты .
Учёные отмечали, что преждевременная кальцификация плаценты может служить признаком беременности высокой группы риска, а также тревожным признаком дисфункции плаценты. Таким образом, для всех пациенток с кальцинозом рекомендуется тщательное наблюдение до родов. Необходимо регулярно проводить исследование состояния плода, чтобы предотвратить осложнения беременности.
Очевидно, что более масштабные исследования могут предоставить больше значимых результатов.



- На заглавную
Поиск
Генерализованная инфантильная артериальная кальцификация у новорожденных: клинический случай
И.Е. ИВАНОВА 1 , Л.Г. НОГТЕВА 2 , В.А. РОДИОНОВ 3 , Е.Н. САВАСЬКИНА 2 , А.В. АБРУКОВА 2 , Е.Н. ИГНАТЬЕВА 4
1 Институт усовершенствования врачей Минздрава Чувашии, 428032, г. Чебоксары, Красная пл., д. 3
2 Президентский перинатальный центр Минздрава Чувашии, 428018, г. Чебоксары, Московский пр., д. 9
3 Чувашский государственный университет им. И.Н. Ульянова, 428015, г. Чебоксары, Московский пр., д. 15
4 Республиканское патологоанатомическое бюро Минздрава Чувашии, 428017, г. Чебоксары, ул. Пирогова, д. 24
Иванова Ирина Евгеньевна ― доктор медицинских наук, заведующая кафедрой педиатрии, тел. (8352) 56-00-10, e-mail: [email protected]
Родионов Владимир Анатольевич ― доктор медицинских наук, профессор, заведующий кафедрой педиатрии и детской хирургии, тел. (8352) 56-31-72, e-mail: [email protected]
Ногтева Лариса Германовна ― заместитель главного врача, тел. (8352) 58-61-62, e-mail: [email protected]
Екатерина Николаевна Саваськина ― заведующая медико-генетической консультацией, тел. (8352) 58-05-85, e-mail: [email protected]
Абрукова Анна Викторовна ― кандидат медицинских наук, врач-генетик, тел. (8352) 58-05-85, e-mail: [email protected] yandex.ru
Игнатьева Евгения Николаевна ― кандидат медицинских наук, заведующая патологоанатомическим отделением №2, тел. (8352) 23-54-57
В статье представлен клинический случай генерализованной инфантильной кальцификации (ИАК) у новорожденного ребенка. Дана характеристика заболевания, анамнестических, клинических, лабораторных данных у пациента. Рассмотрены частота ИАК, клинические и морфологические проявления, прогноз, возможности пренатальной, прижизненной и генетической диагностики. Показан спектр мутаций при ИАК, генетиченский прогноз для рождения последующих детей в семье.
Ключевые слова: генерализованная инфантильная кальцификация, новорожденные, пренатальная диагностика, клиника, прогноз.
I.E. IVANOVA 1 , L.G. NOGTEVA 2 , V.A. RODIONOV 3 , E.N. SAVASKINA 2 , A.V. ABRUKOVA 2 , E.N. IGNATYEVA 4
1 Institute for Advanced Medical Studies of the Ministry of Healthcare of Chuvash Republic, 3 Krasnaya Square, Cheboksary, Russian Federation, 428032
2 Presidential Prenatal Center of the Ministry of Healthcare of Chuvash Republic, 9 Moskovskiy Pr., Cheboksary, Russian Federation, 428018
3 Chuvash State University named after I.N. Ulyanov, 15 Moskovskiy Pr., Cheboksary Russian Federation, 428015
4 Republic Morbid Anatomy Bureau of the Ministry of Healthcare of Chuvash Republic, 24 Pirogov Str., Cheboksary, Russian Federation, 428017
Ivanova I.E. ― D. Med. Sc., Head of the Pediatrics Department, tel. (8352) 56-00-10, e-mail: [email protected]
Rodionov V.A. ― D. Med. Sc., Professor, Head of the Pediatrics and Pediatric Surgery Department, tel. (8352) 56-31-72, e-mail: [email protected]
Nogteva L.G. ― Deputy Chief Doctor, tel. (8352) 58-61-62, e-mail: [email protected]
Savaskina E.N. ― Head of the Medical-Genetic Counseling, тел. (8352) 58-05-85, e-mail: [email protected]
Abrukova A.V. ― Cand. Med. Sc., geneticist, tel. (8352) 58-05-85, e-mail: [email protected]
Ignatyeva E.N. ― Cand. Med. Sc., Head of Morbid Anatomy Department №2, tel. (8352) 23-54-57
The article presents a clinical case of generalized infantile calcification (GIC) in a newborn. The disease, the medical history, clinical and laboratory data of the patient are characterized. The following features were considered: GIC frequency, clinical and morphological manifestations, prognosis, possible prenatal, lifetime and genetic diagnostics. The article shows the spectrum of mutations in case of GIC, genetic prognosis for the birth of subsequent children in the family.
Key words: generalized infantile calcification, the newborn, prenatal diagnosis, clinical picture, prognosis.
Генерализованная ИАК ― заболевание, характеризующееся кальцификацией внутренней эластической оболочки мышечных артерий и их стенозом из-за миоинтимной пролиферации [3]. В первые месяцы жизни развиваются тяжелая сердечная недостаточность и артериальная гипертензия, обусловленные окклюзивным поражением сосудов, в том числе коронарных артерий. Часто в патологический процесс вовлекаются мозговые сосуды с развитием церебральных инсультов. Смерть наступает в первом полугодии жизни из-за ишемии миокарда в результате рефрактерной сердечной недостаточности [4, 5].
Наиболее полное описание заболевания представлено в обзоре Chong и Hutchins [6], в котором была проанализирована клиническая картина у 161 больного с ИАК: 48% пациентов имели раннее начало (внутриутробно или в течение первой недели жизни), 52% ― поздний дебют (средний возраст заболевания ― три месяца). При раннем начале ИАК наиболее распространенными симптомами были дистресс плода (46%), сердечная недостаточность (44%), многоводие (38%), артериальная гипертензия (33%), респираторный дистресс-синдром новорожденного (30%), водянка плода (28%), отеки (24%), транссудаты во внутренних органах (20%), цианоз (22%), кардиомегалия (17%), асцит (13%). При позднем дебюте наблюдались респираторный дистресс-синдром (66%), цианоз (43%), отказ от питания (34%), сердечная недостаточность (29%), рвота (24%), раздражительность (21%), лихорадка (16%), артериальная гипертензия (12%), отеки (7%). Авторами не выявлены гендерные различия в распространенности заболевания.
В отечественной литературе в зависимости от продолжительности болезни выделяют два клинико-анатомических варианта ИАК, различающихся по степени и распространенности поражения артерий, а также по характеру изменений в сердце. Первый вариант сопровождается внезапной смертью ребенка вследствие острой коронарной недостаточности или инфаркта миокарда. При втором варианте развивается сердечная недостаточность в результате кардиомегалии с кардиосклерозом и фиброэластозом эндокарда, распространением кальциноза на большинство артерий других органов. У всех больных клиническая картина характеризуется кардиореспираторным синдромом, сопровождающимся тахикардией, тахипноэ и цианозом. Известны случаи, когда ИАК сопровождалась персистирующей легочной гипертензией, стенозами почечных артерий [7].
Обычно больные погибали от инфаркта миокарда в первые 6 месяцев жизни. На аутопсии во многих случаях было увеличение массы сердца, иногда в 2-4 раза, с расширением его полостей, утолщением стенки левого желудочка, эндокарда левой половины сердца [3]. В ряде случаев отмечались аномалии развития сердца и сосудов. Иногда определялись извитость, уплотнение, обызвествление коронарных артерий с резким сужением их просвета. Во многих случаях выявлены инфаркты миокарда, особенно в папиллярных мышцах, постинфарктные рубцы, участки кальциноза. У детей раннего возраста на аутопсии, кроме ИАК, диагностировались стафилококковый перитонит, пупочный сепсис, родовая травма, цитомегалия. При микроскопическом исследовании при ИАК обнаруживался кальциноз внутренней эластической мембраны и мышечной оболочки артерий крупного и среднего калибра. При этом всегда поражались коронарные артерии. С меньшим постоянством встречался кальциноз почечных, селезеночных, панкреатических, брыжеечных и легочных артерий [8].
В литературе имеется небольшое количество работ, посвященных катамнезу выживших детей. Так, в сообщении Rutsch и др. [9], у восьми из 19 детей с ИАК, которые пережили неонатальный период, наблюдались гипофосфатемия и повышенная потеря фосфора с мочой, у пяти развились признаки рахита, оссалгия, варусная деформация ног и низкорослость в возрасте от восьми месяцев до 11 лет. В других работах описаны множественные проблемы с сердечно-сосудистой системой, органами желудочно-кишечного тракта, патология почек, центральной нервной системы, задержка физического и нервно-психического развития [10].
В настоящее время возможна пренатальная и прижизненная ультразвуковая диагностика ИАК, а также для уточнения диагноза и прогноза рождения больных детей широко применяются генетические методы исследования [3].
Прогноз при ИАК неблагоприятный. По данным Rutsch и соавт. [9], из 55 детей с ИАК, 6 были мертворожденными и 30 родились преждевременно. До шести месяцев, несмотря на интенсивную терапию, умерли 30 детей из 55 (55%), и только один пациент умер после 12 месяцев жизни. Причинами смерти были инфаркт миокарда, застойная сердечная недостаточность, стойкая артериальная гипертензия или полиорганная недостаточность. В литературе имеются единичные сообщения о смерти в более позднем возрасте [11].
Приводим собственное наблюдение ИАГ. В 2016 г. в Президентском перинатальном центре был диагностирован случай заболевания новорожденного ребенка генерализованой ИАК.
Мальчик К., родился от 1 беременности у женщины 24 лет. Беременность наступила через 1,5 года после лечения бесплодия, протекала на фоне эрозии шейки матки, хронического пиелонефрита. В первой половине беременности мать перенесла Herpes labialis, во второй половине ― ОРВИ в легкой форме. С 33 недель получала лечение по поводу угрозы невынашивания, анемии. При ультразвуковом скрининге в 20-21 неделю и 32 недели диагностированы ИАК, расширение ствола легочной артерии и левого желудочка. От прерывания беременности родители отказались. Роды преждевременные (35 недель), самопроизвольные. Масса ― 2770 г, длина ― 49 см, оценка по Апгар ― 5-6 баллов. Состояние ребенка после рождения тяжелое, обусловлено синдромом дыхательных расстройств 2 степени, гемодинамическими нарушениями, общим отечным синдромом. Сразу после рождения мальчик переведен в отделение реанимации и интенсивной терапии, где находился в течение 3 суток. После стабилизации состояния находился в отделении патологии новорожденных. В течение всего времени наблюдения состояние ребенка было тяжелым, отмечались тахикардия, цианоз, тахипноэ, плотные отеки бедер и голеней. Питание усваивал плохо, кормился через зонд. При малейшей физической нагрузке отмечалось снижение сатурации кислорода до 87-86%. Несмотря на проводимую интенсивную терапию, направленную на поддержание и стабилизацию жизненных функций, ребенок умер в возрасте 26 суток при явлениях тяжелой сердечной и дыхательной недостаточности. В лабораторных данных отмечались анемия легкой степени, гипербилирубинемия (общий билирубин 276 мкмоль/л, непрямой ― 256 мкмоль/л), повышение уровня креатиниа до 60 мкмоль/л к 15 суткам жизни. На Эхо-КГ диагностированы стеноз аорты и легочной артерии, аневризма межпредсердной перегородки R-типа, открытое овальное окно 3,3 мм с умеренным сбросом вправо, дилатация всех камер сердца, высокая легочная гипертензия, снижение систолической функции миокарда. На УЗИ сосудов ― генерализованное уплотнение и утолщение стенок артерий верхних конечностей с сужением их просвета, уплотнение стенок артерий печени и селезенки. На нейросонографии ― признаки диффузного поражения структур головного мозга, уплотнение стенок церебральных сосудов, асимметричное расширение желудочков мозга. На ЭКГ ― синусовый ритм со склонностью к тахикардии, преобладание потенциалов правого желудочка, нарушение процессов реполяризации в миокарде. Диагноз был подтвержден при жизни на молекулярно-генетическом уровне методом прямого автоматического секвенирования с исследованием всех кодирующих экзонов (1-25) гена ENPP1 с прилегающими интронными областями. В экзоне 13 выявлена мутация с.1298А>Т в гомозиготном состоянии, приводящая к аминокислотной замене p.Lys433lle. Мутация ранее не описана, по данным компьютерного анализа (Alamut Visual) является патогенной. Риск повторного случая в данной семье составляет 25% (аутосомно-рецессивное наследование).
При аутопсии также верифицирована ИАГ аорты и легочного ствола; обызвествление внутренней эластической мембраны и мышечного слоя в стенке артериальных сосудов сердца, почек, легких, селезенки, надпочечников, поджелудочной железы, кишечника, брыжейки, тимуса, позвоночного столба и конечностей; фиброэластоз левого желудочка сердца, кальциноз и склероз митрального, трикуспидального и аортального клапанов, кардиомегалия, диффузный мелкоочаговый кардиосклероз, крупноочаговый кардиосклероз в АВ-узле, вторичный атриальный и атриовентрикулярный гипоганглиоз в вегетативных ганглиях сердца.
Несмотря на 25% вероятность заболевания детей в семье, при повторной беременности у женщины вновь на сроке 20 недель была диагностирована ИАГ плода, в связи с чем по рекомендации перинатального консилиума и решению родителей беременность была прервана.
Представленный случай является примером современных возможностей ранней верификации редкой врожденной патологии с использованием пре- и постнатальных методов диагностики, включая генетическое исследование, и предупреждения рождения детей с тяжелым заболеванием и неблагоприятным прогнозом.
Читайте также:


