Лечение рака костей операция
Хирургическая операция является основным методом лечения большинства злокачественных костных опухолей. Кроме того, для получения образца опухолевых тканей также используется операция. Биопсия и хирургическое лечение - это две отдельные операции. Однако планировать их одновременно очень важно. Лучше всего, если данные процедуры будут проводиться одним и тем же хирургом. Неправильно проведенная биопсия в некоторых случаях делает невозможным удаление опухоли без ампутации пораженной конечности.
Основная цель хирургической операции заключается в иссечении всей опухоли. Если останется всего несколько злокачественных клеток, они могут дать начало новой опухоли. Чтобы предотвратить подобное, хирург удаляет не только новообразование, но и некоторый объем окружающих его здоровых тканей. Такая процедура называется широкое иссечение патологического образования с окружающими тканями. Удаление внешне здоровых тканей увеличивает вероятность того, что опухоль удалена полностью. После операции полученные ткани изучаются патоморфологом под микроскопом. Он осматривает наружные края образца на предмет наличия опухолевых клеток. Если опухолевые клетки присутствуют на краях иссеченных тканей, это означает, что опухоль могла быть удалена не полностью. Широкое иссечение тканей при наличии "чистых" краев операционной зоны сводит риск рецидива опухоли к минимуму.
Опухоли костей верхних и нижних конечностей
В некоторых случаях для обеспечения полноценного широкого иссечения приходится удалять всю конечность. Такая операция носит название ампутация. Обычно злокачественная опухоль удаляется хирургом без ампутации. Такая операция называется органосохраняющей или органосберегающей. Крайне важно осознавать все преимущества и недостатки каждого вида хирургического вмешательства. Органосохраняющая операция намного сложнее и вызывает массу осложнений. Выживаемость при обоих видах операций одинакова, если вмешательство выполняет опытный хирург. Исследования по изучению качества жизни показали, что существенно не различаются реакции пациентов на конечный результат проведения различных операций. Больше всего по поводу исхода операции волнуются подростки. Их тревожат социальные последствия лечения.
Реабилитация потребуется независимо от вида операции. Она может стать самым тяжелым этапом лечения. Пациенту следует встретиться с врачом-реабилитологом до проведения операции. Это позволит лучше понять предстоящие сложности.
Ампутация
Ампутация - это частичное или полное удаление конечности. При ампутации удаляются все пораженные опухолью ткани, часть здоровых тканей над данным участком и полностью ткани под ним. В настоящее время ампутация проводится только при невозможности органосохраняющего лечения. Ампутация может потребоваться в случае, если при удалении опухоли затрагиваются важнейшие нервы, артерии или мышцы, что существенно нарушает работу конечности.
Чтобы определить объем тканей, которые нужно удалить, операцию необходимо сопровождать проведением МРТ и гистологическим исследованием тканей. При проведении операции вокруг ампутированной кости формируется манжета из мышц и кожи. Сформированная манжета должна соответствовать форме искусственной конечности. Пациенту необходимо научиться пользованию протезом в ходе послеоперационной реабилитации. После ампутации нижней конечности пациент снова сможет ходить через 3-6 месяцев.
Органосохраняющая операция
При органосохраняющей операции удаляется вся злокачественная опухоль и сохраняется функциональность конечности. Такая операция может быть проведена в 90% случаев злокачественной опухоли верхней или нижней конечности. Перед хирургом стоит непростая задача: удалить опухоль целиком, не затронув расположенные рядом нервы, сосуды и связки. Если опухоль проросла в рядом расположенные структуры их приходится удалять вместе с опухолью. Иногда это может привести к появлению болей или невозможностью пользоваться конечностью. В таких случаях ампутация является наилучшим вариантом лечения.
При органосберегающей операции используется широкое иссечение тканей для удаления опухоли. Для замены удаленной кости используется костный трансплантат или эндопротез. Эндопротезы могут быть очень сложными конструкциями и изготавливаются из металлов и других материалов. Эндопротезирование часто применяется у растущих детей. В таких случаях по мере роста и развития ребенка эндопротез самостоятельно удлиняется без дополнительной операции.
Некоторым пациентам после органосохраняющей операции в последующие 5 лет может потребоваться новое хирургическое вмешательство, а некоторым из них - и ампутация.
Органосберегающие операции требуют более интенсивной реабилитации. Пациенту после вмешательства на нижней конечности, требуется в среднем около года, чтобы снова начать ходить.
Реконструктивные операции
При необходимости ампутации до середины бедра, хирург может развернуть оставшуюся голень и стопу на 180о и объединить ее с бедренной костью. При этом голеностопный сустав становится новым коленным суставом. Подобная операция называется ротационная пластика. Для восстановления длины используется протез.
При поражении злокачественноой опухолью верхней конечности, возможно ее удаление с последующим присоединением нижних отделов руки. При этом у пациента сохраняется функционирующая рука, которая просто намного короче.
Опухоли других локализаций
Как можно более широкое иссечение пораженных и здоровых тканей проводится при злокачественных опухолях тазовых костей. Для восстановления кости можно использовать костные трансплантаты.
При расположении опухоли в нижней челюсти проводится полное удаление нижнечелюстной кости с последующим ее восстановлением из других костей.
При расположении опухоли в области позвоночника или черепа не всегда возможно широкое иссечение. Злокачественные новообразования в таких случаях требуют комбинированного лечения, например, кюретаж, криохирургию и радиотерапию.
Кюретаж
При данной процедуре из кости проводится выскабливание опухоли без удаления костной ткани. При этом в кости образуется отверстие. После удаления большей части опухоли хирург проводит обработку прилежащей костной ткани для уничтожения всех оставшихся опухолевых клеток. Криохирургия является одним из способов обработки.
Криохирургия
При данном методе через отверстие, которое образовалось после удаление опухоли, в кость вводится жидкий азот. Это уничтожает раковые клетки, замораживая их. После лечения отверстие в кости может быть заделано с помощью костного трансплантата или костного цемента.
Костный цемент
Костный цемент состоит из полиметилметакрилата (ПММК). Он представляет из себя жидкость, затвердевающую со временем. Костный цемент закладывается в костное отверстие в жидкой форме. При затвердевании ПММК выделяет много тепла. Тепло уничтожает оставшиеся клетки злокачественной опухоли. Это качество позволяет использовать ПММК при некоторых костных опухолях без применения криохирургии.
Хирургическое лечение метастазов
Для излечения злокачественной опухоли кости, она должны быть полностью удалена, включая все существующие метастазы. Легкие являются самым типичным местом появления метастазов. Операция должна быть спланирована очень тщательно. Перед операцией хирург оценивает количество опухолей, их расположение, размер и общее состояние здоровья пациента.
Единственный шанс на излечение дает пациенту удаление всех метастазов в легких. Но не все легочные метастазы можно удалить. Некоторые опухоли слишком близко расположены к важным структурам грудной клетки. Метастазы бывают слишком крупными, для их безопасного удаления.
+7 (495) 50 254 50 - ГДЕ ЛУЧШЕ ЛЕЧИТЬ РАК КОСТИ
Выбор тактики лечения и прогноз определяются типом рака кости, который диагностирован у пациента, и некоторыми другими факторами.
Разновидности рака костей
Остеосаркома — наиболее распространенная разновидность первичного рака костей. Чаще всего встречается в возрасте 10–30 лет, как правило, возникает в костях рук и ног, таза. Мужчины болеют чаще по сравнению с женщинами. Менее 10% случаев остеосаркомы приходится на людей старше 60 лет.
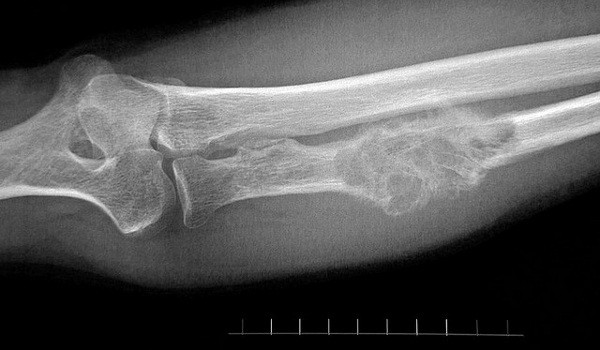
Хондросаркомы происходят из хрящевой ткани, это второй по распространенности тип первичного рака костей. Молодые люди до 20 лет болеют очень редко. С 20 до 75 лет риск возникновения хондросаркомы постепенно нарастает, мужчины и женщины болеют примерно одинаково часто. Хондросаркомы могут возникать в костях рук и ног, таза, черепа, в лопатке. Они могут начать расти и во внутренних органах, в которых присутствует хрящевая ткань, например, в гортани, трахее.
Саркома Юинга — третий по распространенности тип рака костей. Поражает детей, подростков, молодых людей. После 30 лет заболевание встречается крайне редко. Чаще всего опухоль локализуется в костях таза, нижних и верхних конечностях, лопатках, ребрах.
Злокачественная фиброзная гистиоцитома обычно локализуется в мягких тканях, в редких случаях — в костях. Заболевание преимущественно встречается в среднем и пожилом возрасте. При костной локализации чаще всего поражаются кости ног в области колена. Злокачественная фиброзная гистиоцитома склонна к локальному росту, но иногда может давать метастазы, например, в легких.
Фибросаркома также чаще встречается в мягких тканях. У людей среднего и пожилого возраста может поражать кости рук, ног.
Хордома — опухоль, которая чаще всего находится в основании черепа или позвоночном столбе. Обычно диагностируется после 30 лет, у мужчин примерно вдвое чаще, чем у женщин. Хондромы склонны к медленному локальному росту, в редких случаях дают метастазы в лимфатические узлы, печень.
Лечение рака костей
Лечением пациента со злокачественной опухолью костной ткани занимается команда врачей, в которую могут входить: онколог, хирург, специализирующийся в сфере ортопедии, химиотерапевт, врач лучевой терапии, ортопед, реабилитолог, психоонколог.
Хирургическое лечение рака костной ткани
Хирургия — основной радикальный метод лечения рака костей. В прошлом у большинства пациентов прибегали к ампутации — удалению всей конечности или ее части, пораженной опухолью. В настоящее время хирурги стараются отдавать предпочтение органосохраняющим вмешательствам. Удаленную часть кости заменяют костным трансплантатом или эндопротезом из металла, других материалов. Если приходится удалять фрагмент бедренной или плечевой кости, нижележащую часть конечности можно сохранить. При этом рука или нога станет короче, но сможет ограниченно выполнять свои функции.
Иногда в качестве альтернативы хирургическому вмешательству применяют криодеструкцию (разрушение опухолевой ткани низкой температурой), кюретаж (выскабливание специальным инструментом), введение в отверстие в кости цемента из полиметилметакрилата (при затвердевании он нагревается и разрушает опухолевые клетки).
Лучевая терапия при раке костей
Для того чтобы уничтожить опухолевые клетки в кости, требуются высокие дозы излучения, которые приводят к серьезным побочным эффектам. Поэтому лучевая терапия при раке костей находит ограниченное применение:
- Если опухоль невозможно полностью удалить хирургически.
- При положительном крае резекции по данным биопсии после операции.
- В качестве паллиативного метода лечения при рецидиве, чтобы уменьшить боль и отек.
Наиболее широкое применение лучевая терапия находит при саркомах Юинга.

Химиотерапия при раке костей
Химиотерапию чаще всего применяют для лечения остеосарком и сарком Юинга. Другие виды рака костей реагируют на нее плохо. Применяют различные химиопрепараты: цисплатин, доксорубицин, ифосфамид, этопозид, метотрексат, циклофосфамид, винкристин.
Иногда применяют таргетные препараты — лекарственные вещества, которые блокируют молекулы, необходимые для роста и выживания злокачественных опухолей.
Лечение при метастазах рака в костях
При лечении метастазов в костной ткани используют химиопрепараты, которые эффективны против первичной опухоли. Применяют лучевую терапию. Если метастатические очаги приводят к значительному разрушению костной ткани, назначают бисфосфонаты. Эти препараты вводят внутривенно каждые 3–4 недели, они помогают предотвратить патологические переломы, уменьшить боль, снизить уровень кальция в крови.

Хирургическое лечение носит паллиативный характер. При патологических переломах кости укрепляют с помощью винтов, стержней и других металлических конструкций. Иногда прибегают к радиочастотной аблации: в опухоль вводят иглу и подают на нее ток высокой частоты, который разрушает опухолевые клетки.
Реабилитация после лечения рака костей
После ампутации конечности показано протезирование. При правильно спланированных реабилитационных мероприятиях пациенты, перенесшие ампутацию нижней конечности, обычно могут снова ходить спустя 3–6 месяцев.
После органосохраняющих операций реабилитационный период продолжается дольше. Способность ходить восстанавливается примерно через год. Если не проводить реабилитационное лечение, возникает стойкая утрата функции конечности. При инфицировании, смещении или разрушении эндопротеза требуется повторное хирургическое вмешательство. Некоторым пациентам в последующем приходится выполнять ампутацию.
После наступления ремиссии и завершения лечения пациент должен находиться под наблюдением врача. При возникновении любых симптомов нужно посетить клинику и пройти обследование. Это помогает вовремя диагностировать рецидив рака в кости, метастазов в других органах.
Прогноз выживаемости
На прогноз влияют такие факторы, как тип и стадия рака кости, локализация и размер опухоли, возраст пациента. В среднем пятилетняя выживаемость (процент пациентов, которые остаются живы в течение 5 лет с момента диагностики заболевания) при всех типах злокачественных опухолей костей составляет 70%.
Стадии рака костей
Выделяют 4 стадии развития опухолей кости:
- 1 стадия: опухоль ограничена костью, не прорастает в соседние ткани, не распространяется в лимфатические узлы, отдаленные метастазы отсутствуют. Опухоль является высокодифференцированной и отличается низкой степенью агрессивности.
- 2 стадия: опухоль также ограничена костью, не прорастает в соседние ткани, но является низкодифференцированной (опухолевая ткань практически утратила черты нормальной ткани) и более агрессивной.
- 3 стадия: в кости имеется 2–3 очага, они могут быть высоко- или низкодифференцированными.
- 4 стадия: опухоль, которая распространилась за пределы кости в другие органы и ткани.

Причины и факторы риска рака костей
Точные причины возникновения злокачественных опухолей костей неизвестны. Некоторые факторы риска повышают вероятность развития заболевания:
- Остеосаркомы чаще диагностируют у людей, которые перенесли курс лучевой терапии и/или химиотерапии по поводу других типов рака.
- Риски остеосаркомы повышает применение металлических фиксирующих устройств (скоб, спиц, пластин, винтов) при переломах костей.
- Играют роль некоторые наследственные заболевания: наследственная ретинобластома (редкая злокачественная опухоль глаза), синдром Ли-Фраумени.
- У пожилых людей возникновению рака костей может предшествовать Болезнь Педжета — заболевание, при котором нарушается процесс естественного обновления костной ткани, и кости становятся хрупкими.
Симптомы злокачественных опухолей костей
Зачастую первым проявлением рака костей становится боль. Поначалу она возникает лишь во время сна и физических нагрузок, затем становится постоянной, мучительной. Если пораженный участок кости не прикрыт массивными мышцами и находится близко к коже, опухоль можно увидеть при визуальном осмотре, прощупать. Возникает отек.
Рак разрушает нормальную костную ткань, ослабляет кости, в итоге происходят патологические переломы от небольшого усилия. Во время перелома в кости возникает сильная острая боль. Если опухоль сдавливает нерв, в пораженной части тела появляется онемение, покалывание, слабость мышц (парезы, вплоть до паралича).
Похожие симптомы могут возникать и при других заболеваниях, например, при артритах, остеомиелите, после перенесенных травм. Рак костей встречается редко, но при возникновении болей в костях без видимой причины лучше сразу посетить врача и провериться.
Методы диагностики
Компьютерная томография помогает уточнить размеры, расположение, количество опухолевых очагов, степень прорастания в окружающие ткани, обнаружить метастазы в лимфатических узлах и внутренних органах. По показаниям назначают МРТ: она помогает лучше визуализировать опухоль, оценить состояние мягких тканей, головного и спинного мозга.
В поиске мелких метастазов помогает позитронно-эмиссионная томография. Во время исследования в организм вводят молекулы сахара с радиоактивной меткой. Опухолевые клетки поглощают радиофармпрепарат и становятся видимыми на снимках, выполненных специальным аппаратом.
Наиболее точный метод диагностики онкологических заболеваний — биопсия. Во время исследования получают фрагмент предположительно опухолевой ткани и отправляют в лабораторию для изучения внешнего вида клеток, строения ткани, молекулярно-генетических характеристик. Биопсию можно провести разными способами:
- При тонкоигольной биопсии используют шприц с иглой. Если кость находится глубоко, скрыта мышцами, процедуру проводят под контролем компьютерной томографии.
- При трепан-биопсии используют толстую иглу диаметром примерно полтора миллиметра. Считается, что этот метод лучше, чем тонкоигольная биопсия, он позволяет установить более точный диагноз.
- Иногда для исследования нужен большой фрагмент кости. В таких случаях проводят эксцизионную или инцизионную биопсию: выполняют хирургическое вмешательство, удаляют всю опухоль или ее часть.
Рак костей — это опухоли, которые первично появляются в костях. Довольно редко они являются именно раком, то есть, новообразованием их эпителиальной ткани. Чаще в костях обнаруживаются другие злокачественные опухоли: саркомы, которые отличаются тем, что растут из костной или хрящевой ткани.

Операции при раке костей конечностей
Если злокачественная опухоль растет из костей рук или ног, то у врача есть два варианта хирургического лечения:
- ампутация конечности;
- удаление опухоли с сохранением конечности.
Каждый подход имеет свои преимущества и недостатки. В итоге решение принимается совместно с пациентом с учетом всех плюсов и минусов. Большинство людей стремятся сохранить конечность. При этом стоит понимать, что подобные операции более сложные, имеют повышенный риск осложнений.
Ампутация снижает трудоспособность и влияет на качество жизни. Но такое лечение рака костей более простое, надежное, реже дает осложнения и рецидивы.
Если конечность сохранена, часто приходится удалять не только кость, но также мышцы, нервы, сосуды. Всё это требует последующего эндопротезирования и длительной реабилитации. Вместо собственной кости устанавливают искусственную (из металла или других материалов). Иногда приходится ставить также искусственный сустав. Это влечет за собой риск осложнений, с которыми пациент должен быть ознакомлен. Иногда встречается инфицирование эндопротеза или его асептическое расшатывание. Кроме того, в будущем могут потребоваться операции по замене искусственной кости или сустава.
Опухоли других локализаций
Нередко рак костей располагается в других частях тела. Опухоль может расти из костей черепа, челюсти, таза. После удаления требуются реконструктивные операции. Костные дефекты замещают либо собственной костной тканью из донорских участков, либо синтетическими материалами.
Лечение рака костной ткани в случае расположения опухоли вблизи важных органов и невозможности полноценного удаления с достаточным отступом проводится и другими методами:
- Экскохлеация (выскабливание, кюретаж) — позволяет удалить большую часть образования с сохранением основной массы кости.
- Криодеструкция — разрушение опухолевых очагов с использованием критически низких температур (ткани замораживаются, а при оттаивании отмирают).
После выскабливания часто остается костный дефект. Он может быть замещен костным цементом (полиметилакрилатом), который также убивает оставшиеся раковые клетки за счет высокой температуры (ПММА помещается внутрь кости в жидком виде).

Нехирургические методы лечения рака костей
Используется в дополнение к хирургии при положительных краях резекции. Может применяться вместо операции при неоперабельном раке или рецидиве опухоли. При раке костей также используется особый вид лучевой терапии: экстракорпоральное облучение. Оно выполняется в рамках операций, при которых врач стремится сохранить пораженную онкологическим процессом конечность. Кость удаляют, облучают, а затем устанавливают на место.
Метод связан с рядом проблем:
- длительное заживление раны после операции;
- потеря подвижности сустава;
- изменение длины конечности, требующее последующей реконструктивной операции;
- частые переломы в обработанном радиацией участке кости.
Химиотерапия – системный метод лечения в онкологии. Используется редко, так как большинство видов рака костей не чувствительны к химиопрепаратам. Другие методы. При поздних стадиях некоторых видов рака костей используют моноклональные антитела, интерферонотерапию.
Прогноз при онкологии костей
Результаты лечения онкологии костей зависит от множества факторов:
- Гистологический тип опухоли. Некоторые виды рака более агрессивны, другие успешно поддаются излечению у большинства пациентов даже с использованием менее радикальных операций.
- Объем удаленных тканей. При удалении опухоли врач также захватывает некоторое количество неизмененной ткани. Чем больший объем будет удален, тем меньше риск рецидива. В то же время удаление большого количества нормальных тканей делает операцию более радикальной, что влияет на трудоспособность пациента и эстетический результат.
- Положительный или отрицательный хирургический край. После удаления опухоли край резекции исследуется на наличие опухолевых клеток. Если их нет, это благоприятный прогностический признак. С высокой вероятностью рецидива рака не будет. Если же раковые клетки обнаружены в хирургическом крае, он считается положительным. Это фактор риска рецидива рака.
- Расположение. Если опухоль располагается в дистальной части конечности, прогноз значительно лучше по сравнению с расположением аналогичного новообразования в костях черепа. В этом случае часто невозможно выполнить полноценное удаление новообразования, так как врачу приходится больше беспокоиться о сохранности окружающих тканей.
В целом, при большинстве опухолей костей прогноз благоприятный. Если лечение проводится на местнораспространенной стадии, пятилетняя выживаемость составляет 70-75%, на локалнораспространенной — 80-90%.
Онкологическое эндопротезирование единственная возможность сохранить хорошее качество жизни после удаления злокачественной опухоли костей. Остеосаркомой, саркомой Юинга, хондросаркомой болеют преимущественно подростки и лица молодого возраста. Имплантация эндопротеза позволяет им вести нормальную жизнь после выздоровления.
Установка импланта никак не влияет на эффективность противоопухолевого лечения.
Органосохраняющие операции как золотой стандарт
Хирургические вмешательства в онкоортопедии начали применять еще в 80-90х годах. Тогда врачи сохраняли нижнюю конечность по строгим показаниям. Эффективность противоопухолевого лечения довольно высока (пятилетняя выживаемость составляет 75-85%).
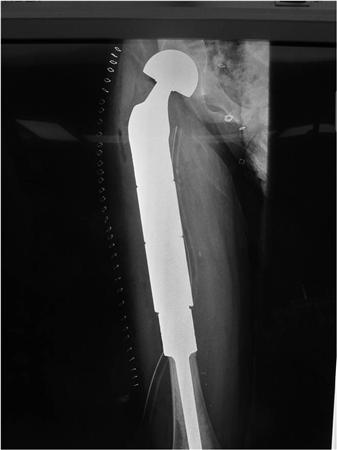
Онкологический имплант бедренной кости.
Эндопротезы устанавливают после удаления опухоли любого крупного сустава (коленного, тазобедренного, голеностопного, плечевого, локтевого). Пациентам со злокачественными новообразованиями плечевых, бедренных, большеберцовых костей выполняют их тотальное или диафизарное эндопротезирование — заменяя не сустав, а часть трубчатой кости.
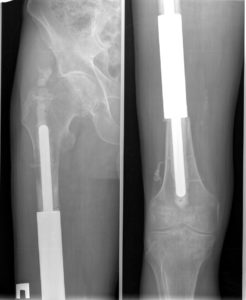
Суть онкологического эндопротезирования заключается в замене удаленных частей сустава искусственными имплантами. Это восстанавливает функции нижней конечности. Операция спасает в 85-90% случаев.
Противопоказания к хирургии
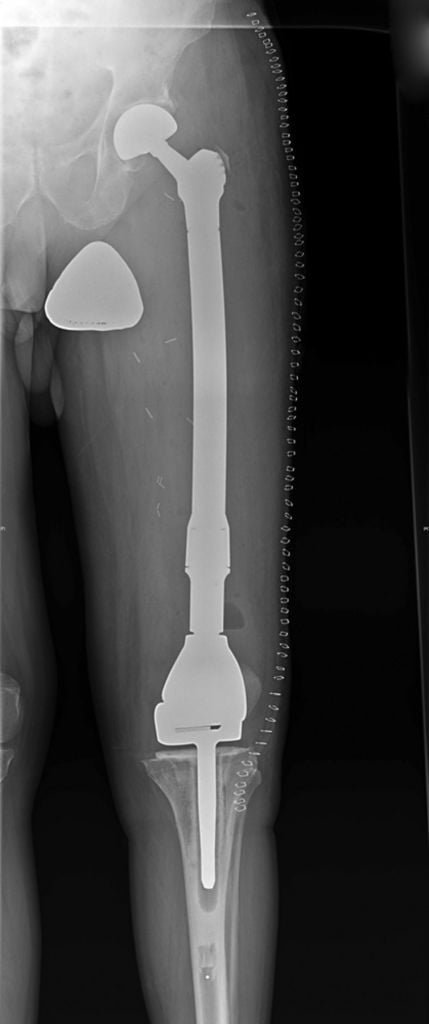
Операция по полной замене бедренной кости с имплантом коленного сустава.
Существует ряд ситуаций, когда ампутация ноги необходима. Иногда отказ от органосохраняющей операции спасает жизнь человека, а попытка сохранить нижнюю конечность приводит к его скорой гибели.
Абсолютные показания к ампутации:
- распад злокачественного новообразования;
- диссеминация (распространение) опухолевых клеток вследствие некачественно выполненной биопсии;
- поражения магистральных сосудов или нервов конечности.
Зачастую врачи рекомендуют ампутацию больным с патологическими переломами, осложнениями химиотерапии и тяжелыми поражениями жизненно важных органов, сопровождающимися декомпенсацией их функций. В этих случаях удаление нижней конечности дает человеку намного больше шансов.
Противопоказанием является невозможность сформировать мышечный футляр для импланта. Это ставит под угрозу приживление протеза и дает риск развития инфекционных осложнений.
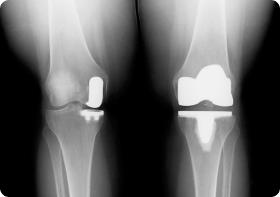
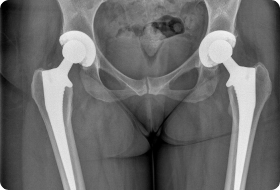
Особенности онкологического эндопротезирования
Если при обычной замене сустава врачи выполняют стандартную резекцию, то при злокачественных опухолях объем удаления костной ткани увеличивается. Врачам нужно подбирать особый имплант каждому больному. Онкологические эндопротезы имеют гораздо больший размер, чем ортопедические.
Таблица 1. Основные различия между онкологическим и обычным эндопротезированием.
| Традиционное | Онкологическое | |
| Предоперационная подготовка | Общеклинические и визуализирующие методы исследования. | Объемное обследование, включающее биопсию, ангиографию, сцинтиграфию, КТ, МРТ и другие нужные методы. |
| Особенности устанавливаемых эндопротезов | Стандартные моноблочные или модульные протезы с цементной или бесцементной фиксацией. | Модульные эндопротезы, форму и размер которых можно отрегулировать в ходе операции. Подобные мегапротезы могут полностью заместить удаленную фрагменты костей. |
| Ход операции | Больному удаляют деструктивно измененные части сустава, а на их место устанавливают эндопротез. | После полноценного обследования пациенту удаляют опухоль вместе с прилегающими тканями. Кости и сустав замещают протезом. Выполняют пластику мягких тканей нижней конечности. |
| Ожидаемые результаты | Полное восстановление функции сустава. Возможны осложнения, устранить которые можно консервативным или хирургическим путем. | Пятилетняя выживаемость после органосохраняющей операции составляет 80%. Онкологическое эндопротезирование позволяет восстановить функции сустава. Риск осложнений в этом случае выше, чем при выполнении обычной ортопедической операции. |
Обследование перед операцией
Перед началом лечения пациента тщательно обследуют. Это помогает выявить злокачественное новообразование, установить его локализацию и размеры.
- Рентгенография. Позволяет подтвердить наличие опухоли и ориентировочно оценить ее размеры. Не дает представления о состоянии магистральных сосудов, нервов, мягких тканей конечности.
- Сцинтиграфия костей скелета. Необходима для выявления метастазов злокачественного новообразования. Обнаруживает опухоли костей любой локализации.
- Биопсия. Наиболее точные результаты дает трепанационная и открытая биопсия. Пункционная и аспирационная менее информативны, поскольку в полученном в их ходе материале не всегда содержатся опухолевые клетки.
- КТ/МРТ. Детальный анализ структуры кости, оценить степень ее разрушения и состояние мягких тканей нижней конечности. Это помогает наиболее точно определить объем резекции и спрогнозировать результаты операции.
- Ангиография. Выявляет дефекты и опухолевые повреждения магистральных сосудов.
- Общеклинические исследования (общий анализ крови и мочи, биохимический анализ крови, ЭКТ, флюорография, УЗИ органов брюшной полости). Необходимы для оценки общего состояния пациента и выявления тяжелых сопутствующих заболеваний.
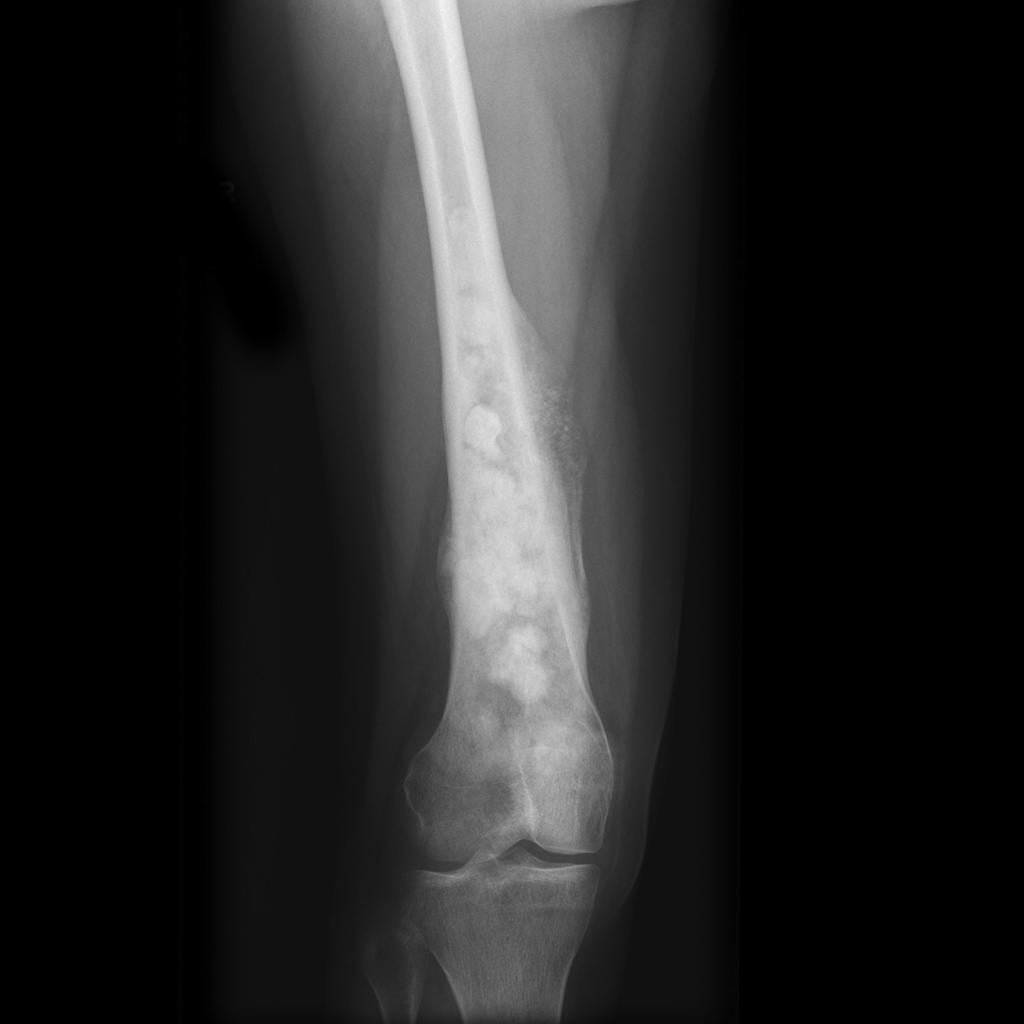
Остеосаркома на рентгене.
Комбинированное лечение опухоли
Для борьбы с опухолями костей используют химиотерапию, лучевую терапию и хирургическое лечение. Их умелое сочетание позволяет проводить органосохраняющие операции даже в тех ситуациях, в которых ранее ампутировали конечность. Химиотерапия позволяет нивелировать последствия перелома или неудачной биопсии.
Онкологические эндопротезы
Импланты, которые используются в онкоортопедии, обычно имеют гораздо больший размер. Это необходимо для замещения удаленных костных тканей. Логично, что мегапротезы нарушают биомеханику сустава, что приводит к нестабильности импланта. При опухолях нижней конечности пациентам могут замещать не только суставы, но и кости. Вид импланта зависит от локализации и размера злокачественного новообразования.
Виды онкологических протезов нижней конечности:
- заменяющие ТБС и часть бедренной кости;
- заменяющие коленный сустав и часть бедренной или большеберцовой кости;
- полностью замещающие бедренную кость;
- спейсеры – замкнутые эндопротезы коленного сустава;
- частично заменяющие и удлиняющие бедренную кость.

Основное отличие онкологических имплантов заключается в их массивности и сложности конструкции.
Производством онкологических протезов занимается несколько компаний: Stryker, ImplantCast, Biomet. Фирмы выпускают модульные эндопротезы, которые можно фиксировать цементным или бесцементным способом.
Особенностью модульных протезов является возможность собрать их во время операции. Это позволяет реконструировать дефекты костей любого размера. Применение модульных эндопротезов дает возможность избежать изготовления индивидуального импланта.
Неожиданные интраоперационные находки в онкологии нередки. Они вынуждают врачей удалять больше костной ткани, чем планировалось. Применение модульных протезов позволяет справиться с этой проблемой с минимальным ущербом для пациента. Чтобы заместить дефект, достаточно всего лишь раздвинуть эндопротез до нужного размера.
Любопытно! В онкоортопедии становятся все популярней эндопротезы с серебряным покрытием. Содержащиеся в нем ионы серебра оказывают антибактериальное действие и снижают риск развития инфекции.
Выполнение операции
Удаление костной ткани и установка протеза при злокачественных новообразованиях происходит совсем не так, как при обычном эндопротезировании. Во время хирургического вмешательства врачи придерживаются целого ряда правил.
Основные правила онкологического эндопротезирования:
- Соблюдение принципа футлярности. Злокачественную опухоль удаляют вместе с окружающими ее фрагментами здоровой костной ткани. Резекцию кости выполняют на расстоянии 5-6 см от новообразования. Вместе с опухолью удаляют зону предшествующей биопсии и все очаги возможной диссеминации.
- Соблюдение правил абластики и асептики. Во время хирургического вмешательства врачи тщательно следят за тем, чтобы опухолевые клетки не проникли в здоровые ткани. Чтобы избежать диссеминации, вначале перевязывают артерии и вены, а лишь затем иссекают опухоль. Параллельно с этим медработники проводят тщательную профилактику инфицирования операционной раны.
- Восстановление двигательной функции конечности. После установки протез прикрывают мышечными лоскутами и делают необходимую пластику. Это позволяет избежать развития инфекционных осложнений и некроза тканей в будущем.
- Адекватное послеоперационное ведение больных. Качественная реабилитация и правильное поведение пациента в послеоперационном периоде помогает восстановить функцию сустава и снизить риск возникновения непредвиденных осложнений.
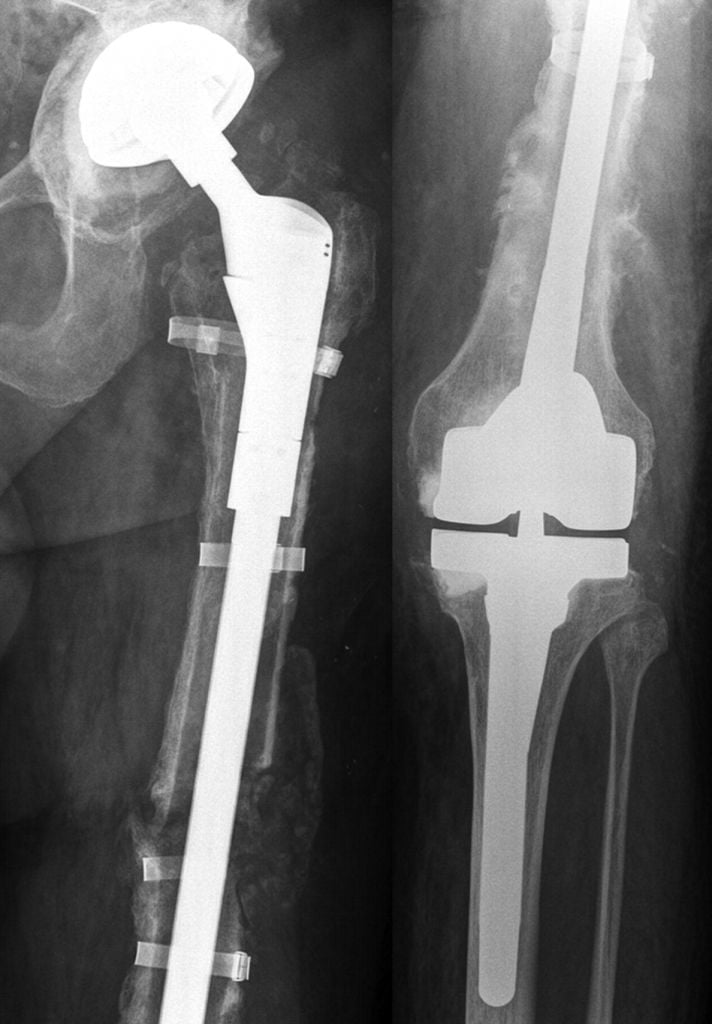
Массивный онкологический эндопротез ТБС.
Факт! Результаты органосохраняющей операции зависят от размера опухоли, степени ее злокачественности, поражения мягких тканей, сосудов и нервов конечности. Немалую роль в успехе лечения играет и внимательность, добросовестность и опытность врачей.
Читайте также:






