Локальная инъекционная терапия при дегенеративных заболеваниях суставов
Локальная инъекционная терапия считается одним из важных компонентов лечения воспалительных и дегенеративных заболеваний суставов, позвоночника и мягких тканей. В статье представлены основные группы лекарственных средств, применяемых для внутрисуставного введения у пациентов с данной патологией, включая глюкокортикостероиды, препараты гиалуроновой кислоты и комплексный биоактивный препарат Алфлутоп. Представлены результаты многочисленных исследований, свидетельствующие о том, что препарат Алфлутоп обладает хондропротективным, противовоспалительным, трофическим действием. Данный препарат характеризуется быстро развивающимся клиническим эффектом, продолжительным периодом последействия (четыре – шесть месяцев), высоким профилем безопасности. Может быть рекомендован для широкого применения в ревматологической, неврологической, терапевтической, травматологической и ортопедической практике.
Локальная инъекционная терапия считается одним из важных компонентов лечения воспалительных и дегенеративных заболеваний суставов, позвоночника и мягких тканей. В статье представлены основные группы лекарственных средств, применяемых для внутрисуставного введения у пациентов с данной патологией, включая глюкокортикостероиды, препараты гиалуроновой кислоты и комплексный биоактивный препарат Алфлутоп. Представлены результаты многочисленных исследований, свидетельствующие о том, что препарат Алфлутоп обладает хондропротективным, противовоспалительным, трофическим действием. Данный препарат характеризуется быстро развивающимся клиническим эффектом, продолжительным периодом последействия (четыре – шесть месяцев), высоким профилем безопасности. Может быть рекомендован для широкого применения в ревматологической, неврологической, терапевтической, травматологической и ортопедической практике.
Cамая частая причина жалоб на боль и нарушение функций опорно-двигательного аппарата – воспаление и дегенеративные изменения структур суставов (гиалиновый хрящ, субхондральная кость). Однако патологический процесс затрагивает не только сустав, но и околосуставные ткани (энтезисы, сухожилия, суставные сумки).
Целями лечения заболеваний опорно-двигательного аппарата являются снижение выраженности симптомов и замедление прогрессирования патологии, что может способствовать улучшению мобильности и качества жизни пациентов.
Один из важных компонентов лечения воспалительных и дегенеративных заболеваний суставов, позвоночника и мягких тканей – локальная инъекционная терапия [1].
В настоящее время эффективность глюкокортикостероидов (ГКС) и препаратов из компонентов матрикса хрящевой ткани для внутрисуставного введения доказана в десятках рандомизированных контролируемых многоцентровых исследований. Поэтому они рекомендованы Европейской антиревматической лигой и Американской ассоциацией ревматологов.
Инъекционная терапия ГКС, применяемая в ревматологии уже более 50 лет, считается хорошей альтернативой терапии как пероральными, так и парентеральными нестероидными противовоспалительными препаратами, а также другим способам локального и системного медикаментозного воздействия на воспалительный процесс в суставах. В результате введения суспензии медленно растворимых кристаллов ГКС эффективно подавляется воспаление в синовиальной оболочке, суставной сумке, сухожильных влагалищах и энтезисах [2].
Показанием к локальному введению ГКС служат [2]:
- воспалительные явления в нескольких суставах, суставных сумках, сухожильных влагалищах, энтезиты при исключении их инфекционного генеза;
- артриты отдельных (наиболее болезненных/функционально значимых) суставов у пациентов с полиартритом в ожидании эффекта от системной терапии;
- артриты одного-двух суставов у больных в целом с хорошо контролируемым полиартритом;
- облегчение программ реабилитации (улучшение возможности больного выполнять упражнения лечебной гимнастики);
- противопоказания к другим видам лечения (активная язва желудка, аллергия ко многим препаратам) или их неэффективность.
- наличие инфекции в суставе или окружающих тканях; геморрагический синдром;
- тяжелое общее состояние;
- нестабильность сустава;
- асептический некроз в прилежащих эпифизах;
- анатомическая недоступность сустава (резкое сужение щели сустава, его анкилоз);
- механический ритм боли в суставе;
- отсутствие воспалительного процесса;
- отсутствие эффекта (или его кратковременность) от предшествующих двух инъекций.
Характеристика ГКС, применяемых для локальной инъекционной терапии, представлена в табл. 1.
Гиалуроновая кислота ответственна за вязко-эластические свойства синовиальной жидкости, которая выполняет функции лубриканта в суставе. Внутрисуставное введение гиалуроната способствует увеличению синтеза внеклеточных матриксных белков, включая хондроитинсульфат и кератансульфат, а также нормализации состава синовиальной жидкости, ингибированию продукции провоспалительных цитокинов и простагландинов, замедлению катаболических процессов в матриксе хряща. При использовании препаратов гиалуроновой кислоты уменьшается выраженность болевого синдрома и улучшается подвижность сустава, что положительно влияет на качество жизни пациентов [2].
Показаниями для введения гиалуронатов являются:
- остеоартрит;
- механический ритм боли;
- отсутствие признаков синовита;
- рентгенологические первая – третья стадии.
Основные препараты из группы гиалуроновой кислоты представлены в табл. 2.
В лечении остеоартрита более четверти века широко используется комплексный биоактивный препарат Алфлутоп (компания Biotehnos S.A., Румыния) [3]. В его состав входят сульфатированные глюкозаминогликаны, аналогичные матриксу гиалинового хряща: хондроитин-4-сульфат, хондроитин-6-сульфат, дерматансульфат, кератансульфат, низкомолекулярные полипептиды (≤ 50 кДа), свободные аминокислоты и микроэлементы (Na, K, Ca, Mg, Fe, Cu, Zn), имеющие большое значение для обменных процессов и метаболизма соединительной ткани в целом.
Алфлутоп воздействует на внешние рецепторы клеток, такие как СD44, ICAM1, TL-4. Доказано, что препарат способен препятствовать фрагментации внеклеточного матрикса, защищая рецепторы, вовлекаемые в воспалительную реакцию, и блокировать сигнальные пути, активируемые фрагментами матрикса. Как следствие, уменьшается транслокация ядерных провоспалительных факторов.
Именно через рецепторное воздействие Алфлутоп контролирует три компонента синовиального воспаления: клеточную инфильтрацию, высвобождение воспалительных медиаторов и ангиогенез.
Приведенные данные служат обоснованием не только парентерального способа введения Алфлутопа, но и целесообразности локальной доставки препарата в поврежденную область.
При внутрисуставном, периартикулярном или околосухожильном введении Алфлутоп также обладает антигиалуронидазной активностью, что позволяет нормализовать физико-химические свойства синовиальной жидкости в полости сустава, то есть препарат осуществляет функцию своеобразного синовиального протектора [4, 5].
На восьмой Европейской выставке инноваций и изобретений (май 2016 г.) исследователей наградили золотой медалью и дипломом за изучение влияния препарата Алфлутоп на хондроциты на гететическом, клеточном и молекулярном уровнях. В ходе исследования было показано, что под действием препарата Алфлутоп in vitro происходит стимуляция пролиферации и обновления хондроцитов, поддерживается взаимосвязь между клетками и внеклеточным матриксом вследствие модуляции внеклеточного трансформирующего ростового фактора бета в человеческих хондроцитах (CHON-001) – основы для внеклеточных сигналов синтеза структурных протеинов. Эти результаты вместе с результатами о вызванной Алфлутопом in vitro модуляции важных медиаторов воспаления (интерлейкинов 6 и 8, факторов роста эндотелия) служат подтверждением хондровосстановительного эффекта препарата при заболеваниях опорно-двигательного аппарата [6, 7].
Алфлутоп можно вводить внутримышечно, внутрисуставно, паравертебрально, периартикулярно, в болевые точки при фибромиалгии [8].
В зависимости от клинической ситуации схемы введения могут быть следующие:
- в случае вовлечения множества суставов – глубоко внутримышечно по 1 мл ежедневно на протяжении 20 дней;
- в случае вовлечения в процесс крупных суставов – внутрисуставно по 2 мл в каждый пораженный сустав один раз в три дня (шесть введений) с последующим внутримышечным введением по 1 мл ежедневно на протяжении 20 дней;
- при поражении позвоночника – паравертебрально по 0,25 мл в четыре точки (суммарно 1 мл) на уровне двух смежных сегментов дважды в неделю (пять введений) с последующим внутримышечным введением по 1 мл ежедневно в течение 20 дней. Повторение курса лечения целесообразно проводить через три – шесть месяцев [8];
- при полиостеоартрозе и остеохондрозе – глубоко внутримышечно по 1 мл в день (всего 20 инъекций);
- возможно сочетание внутрисуставного и внутримышечного введения. Курс лечения целесообразно повторить через шесть месяцев.
В разных научно-медицинских центрах накоплен значительный положительный опыт применения препарата Алфлутоп при дегенеративных заболеваниях суставов и позвоночника [9–11].
С точки зрения доказательной медицины наиболее интересными являются результаты российского двухлетнего многоцентрового слепого рандомизированного плацебоконтролируемого исследования симптом- и структурно-модифицирующего действия Алфлутопа, проведенного Л.И. Алексеевой и соавт. (2014 г.) [12]. В исследование были включены 90 больных остеоартритом коленного сустава второй и третьей стадий по классификации Kellgren – Lawrence. Пациентов рандомизировали на две группы по 45 человек в каждой: первая получала внутримышечные инъекции Алфлутопа по 1 мл курсами по 20 дней с интервалом шесть месяцев в течение двух лет (всего четыре курса), вторая – инъекции плацебо (изотонический раствор натрия хлорида) по аналогичной схеме. В качестве сопутствующей терапии назначался ибупрофен в дозе 600–1200 мг/сут.
Период наблюдения – два года.
Различия в абсолютной величине снижения интенсивности боли по индексу выраженности остеоартрита университетов Западного Онтарио и МакМастера (Western Ontario McMaster Universities OA Index – WOMAC) между группами оказались достоверными (рис. 1).
Достоверное снижение скованности в группе Алфлутопа наблюдалось к третьему визиту, в группе плацебо значимого снижения не зафиксировано (p
Аннотация научной статьи по клинической медицине, автор научной работы — Кундер Е.В.
Похожие темы научных работ по клинической медицине , автор научной работы — Кундер Е.В.
Analgetic treatment of inflammatory and degenerative joint diseases
ЕЯ ВОПРОСЫ АТТЕСТАЦИИ И ПОВЫШЕНИЯ КВАЛИФИКАЦИИ
Анальгетическая терапия воспалительных и дегенеративных заболеваний суставов
Белорусская медицинская академия последипломного образования, Минск
Belarusian Medical Academy of Post-Graduate Education, Minsk
Analgetic treatment of inflammatory and degenerative joint diseases
Ключевые слова: боль, воспаление, нестероидные противовоспалительные препараты, крем, заболевания суставов.
Большинство воспалительных и дегенеративных заболеваний опорно-двигательного аппарата сопровождается хроническим болевым синдромом. Боль - ведущий клинический симптом, она определяет качество жизни пациентов и их функциональную активность. Основными причинами боли являются воспалительные заболевания суставов (артриты), энтезов (энтезиты), периартикулярных тканей (дактилиты, теносиновиты), мышц (миозиты), а также дегенеративные процессы (остеоартроз, остеохондроз, спондило-артроз, спондилез). Болевой синдром в ревматологии требует непрерывной многолетней терапии, которая зачастую сопровождается нежелательными побочными эффектами.
Основной метод лечения воспаления и боли при заболеваниях суставов - использование нестероидных противовоспалительных препаратов (НПВП), обладающих выраженным противовоспалительным, обезболивающим, жаропонижающим эффектом благодаря способности подавлять синтез изоформ циклооксигеназы (ЦОГ) в каскаде превращения арахидоновой кислоты. Однако наряду с несомненными положительными эффектами большинство НПВП оказывают нежелательное воздействие на желудочно-кишечный тракт,
печень, почки, сердечно-сосудистую систему, агрегацию тромбоцитов и т.д. Установлено, что при наличии патологии костно-мышечной системы увеличивается частота развития побочных реакций со стороны желудочно-кишечного тракта [4].
Один из основных неблагоприятных эффектов НПВП - гастро- и энтеротоксич-ность, способность индуцировать эрозивные и язвенные повреждения слизистой желудочно-кишечного тракта, вызывать язвенные кровотечения. При блокировании ЦОГ-1 происходит подавление синтеза про-станоидов, угнетаются защитные свойства слизистой оболочки желудка, повышается чувствительность к воздействию кислоты и пепсина. Патология желудка и двенадцатиперстной кишки, связанная с приемом НПВП, сопровождающаяся повреждением слизистой оболочки с развитием эрозий, язв и их осложнений, называется НПВП-индуцированной гастропатией. Парентеральный и ректальный пути введения уменьшают симптомы поражения слизистой ЖКТ но не снижают риск развития этих поражений. Пациентам с факторами риска НПВП-гастропатии необходимо назначать, прежде всего, селективные НПВП, а также с целью профилактики гастроин-тестинальных осложнений - блокаторы протонной помпы.
Факторы риска НПВП-индуцированной гастропатии: пожилой возраст (старше 65 лет); поражение ЖКТ в анамнезе (язвы, кровотечения); прием высоких доз НПВП; сочетанный прием нескольких НПВП, включая низкие дозы аспирина; коморбид-ные состояния (сопутствующая патология, в том числе сердечно-сосудистая); прием глюкокортикоидов и антикоагулянтов; инфекция Helicobacter pylori.
Пристального внимания из побочных эффектов НПВП заслуживают и кардио-васкулярные проблемы. Актуальность последних объясняется значительным числом пожилых лиц среди пациентов, особенно страдающих остеоартритом. НПВП могут вызывать повышение артериального давления в результате задержки жидкости в организме. Со-четанное применение НПВП снижает антигипертензивную эффективность ингибиторов АПФ, бета-адреноблокато-ров, диуретиков. Препараты из группы селективных ингибиторов ЦОГ-2 могут способствовать тромбообразованию у больных с атеросклерозом и ИБС. Чтобы этого не происходило, их применяют вместе с малыми дозами аспирина. В то же время, например, ибупрофен и индомета-цин подавляют антиагрегантное действие аспирина. Следует помнить, что все НПВП
уменьшают выживаемость больных с хронической сердечной недостаточностью.
Факторы риска сердечно-сосудистых катастроф при приеме НПВП: артериальная гипертензия; гипертрофия левого желудочка; ИБС и другие проявления атеросклероза; атерогенные дислипопро-теинемии; сахарный диабет; хроническая сердечная недостаточность; курение; сердечно-сосудистые катастрофы у лиц репродуктивного возраста в семейном анамнезе.
Таким образом, в ревматологической практике актуальна проблема выбора НПВП, обладающего минимальным риском побочных реакций при высокой противовоспалительной и анальгетической эффективности.
Локальная терапия при заболеваниях опорно-двигательной системы включает внутрисуставное или периартикулярное введение лекарственных средств (глю-кокортикоидов) и применение НПВП местно в виде гелей, кремов и мазей. Преимущество локальной терапии состоит во введении глюкокортикоидов непосредственно в очаг воспаления. Терапия обладает выраженным противовоспалительным действием не только в непосредственном очаге воспаления, но и производит небольшой системный эффект. Однако положительное влияние локальной терапии на прогрессирование деструкции суставов не доказано.
Показания для локальной терапии глюкокортикоидами: выраженные артриты (синовиты) крупных суставов при ревматоидном артрите, псориатическом артрите, реактивном артрите, анкилозирующем спондилите, подагре, дегенеративных заболеваниях (остеоартрите). Локальная терапия показана при необходимости быстро подавить активный воспалительный процесс в суставах в дебюте заболевания или при выраженном обострении.
Наиболее часто для локальной терапии используются следующие препараты: три-амсинолона гексацетонид; триамсинолона ацетонид (кеналог); метилпреднизолона ацетат (метипред); бетаметазона дипропи-онат (входит в состав дипроспана); бета-метазона ацетат; гидрокортизона ацетат. Доза вводимого препарата определяется размером пораженного сустава и составляет, например, при использовании кена-лога 40 мг для коленного сустава, 20 мг для плечевого, локтевого, голеностопного или лучезапястного сустава. В настоящее время предпочтение отдается дипроспану, представляющему собой комбинацию двух солей - бетаметазона натрия фосфата и дипропионата, одна из которых обладает
быстрым анальгетическим эффектом, вторая - длительным действием (30 дней и более). Дипроспан в зависимости от размера сустава вводится в дозе от 0,25 до 2 мл. Максимальный эффект после локального введения глюкокортикоидов наступает на 2-3-й день, сохраняется в течение 2-4 недель.
Основные принципы локальной терапии глюкокортикоидами при ревматоидном артрите: введение в сустав должно осуществляться по строгим показаниям и только при активном артрите; при подозрении на наличие сопутствующей инфекции локальная терапия противопоказана; введение глюкокортикоидов в сустав должно осуществляться в асептических условиях; перед введением препарата производится эвакуация избыточного количества синовиальной жидкости, сустав промывается физиологическим раствором; повторные введения в один и тот же сустав проводятся не чаще чем 3 раза в год; введение в протезированный сустав противопоказано; в течение 24 часов после введения необходимо исключить физическую нагрузку на данный сустав; от введения глюкокортикоидов в тазобедренный сустав целесообразно воздерживаться в связи со сложностью техники артроцентеза и высоким риском развития осложнений, прежде всего остеонекроза головки бедренной кости; частая потребность в локальной терапии должна стать поводом для коррекции проводимого системного (прежде всего базисного) лечения ревматоидного артрита.
Необходимо помнить, что локальная терапия ни в коем случае не является эквивалентом базисного лечения, а назначается и проводится ревматологом в качестве дополнения к системной базисной и противовоспалительной терапии по строгим показаниям.
При остеоартрите глюкокортикоиды для локальной терапии уменьшают боли в суставах и улучшают их функциональное состояние. Эффект сохраняется в течение 2-3 недель. Как правило, этого периода достаточно, чтобы развился эффект от хондропротективных препаратов, назначенных одновременно с локальной терапией, и необходимости в повторных внутрисуставных введениях глюкокор-тикоидов не возникает. К этому методу лечения прибегают при наличии синовиального выпота в суставе, а также при неэффективности неинвазивной терапии. Предпочтение отдается триамцинолону (кеналогу) и метилпреднизолону.
В один и тот же сустав вводить препарат более 3 раз в год противопоказано.
Локальная терапия гелями, кремами и мазями, содержащими НПВП, - перспективный метод лечения воспаления и боли при минимальном риске побочных эффектов. Преимущества локальной терапии НПВП: безопасность и простота применения, возможность использования как местного, так и резорбтивного действия, слабо выраженное системное действие, минимизация побочных эффектов, обеспечение высокой концентрации препарата в очаге воспаления, возможность сочетания в одном препарате нескольких веществ, различных по механизму и направленности лечебного воздействия, возможность пролонгированного действия. Локальная терапия гелями, кремами или мазями при заболеваниях суставов, с одной стороны, является эффективным методом купирования воспаления и болевого синдрома, с другой стороны, практически не имеет противопоказаний и может применяться в любом возрасте и при наличии коморбид-ных состояний.
Основные показания для локальной терапии НПВП: воспалительные заболевания суставов и периартикулярных тканей, миозиты, флебиты. Для локальной терапии болевых синдромов и воспаления, связанных с механическим повреждением нервных корешков и периферических нервов, наряду с НПВП используются препараты, обладающие раздражающими и отвлекающими свойствами.
Эффективность лекарственного средства для локальной терапии определяется рядом факторов. Наибольшее значение имеют наименование и концентрация действующего вещества, лекарственная форма и ее состав, физико-химические свойства препарата, размер его молекулы, рН лекарственной формы.
Состав лекарственного средства должен включать НПВП, обладающий доказанной высокой эффективностью в отношении воспаления и болевого синдрома. Действующее вещество должно содержаться в лекарственной форме в достаточной концентрации для реализации эффекта. Большинство гелей, кремов и мазей имеют 1-2% концентрацию.
Лекарственная форма (гель, крем, мазь) также влияет на эффективность средства для локальной терапии.
При создании лекарственной формы учитывается анатомия и физиология кожи, поскольку эффективность локальной терапии определяется транспортом препарата через кожные барьеры (роговой слой, эпидермис, базальную мембрану, дерму). Следовательно, препарат должен быть ди-фильным [5]. Для лучшего проникновения через базальную мембрану оптимальная атомная единица массы препарата должна составлять не более 500 Да [3].
Уровень pH лекарственного средства для локального применения должен быть приближен к pH кожи. Сухой коже свойствен pH в диапазоне 3-5,5, у жирной кожи он достигает 6. Наиболее кислую реакцию можно зафиксировать на поверхности головы, где pH=5,5. На ладонях и подошвах значение этого показателя может достигать 6,5. Щелочная реакция наблюдается на коже паховых складок, а также подмышечных впадин.
Правильное использование лекарственной формы имеет большое значение для повышения эффективности локальной терапии. Наиболее правильным считается четырехкратное нанесение препарата на область воспаления. При выраженном болевом синдроме и высокой активности воспаления рекомендуется увеличить кратность нанесения до 5-6 раз в сутки. На область крупных суставов наносится полоска крема/геля/мази длиной 5-10 см, на область средних по размеру суставов -3-5 см, на область суставов кистей и стоп - 1-2 см [2].
У пожилых людей снижена способность проникновения мазевых форм через кожу [1], что обусловливает необходимость увеличения дозы наносимого препарата или кратности его использования.
На глубину проникновения вещества в ткани влияют следующие вещества: йод, эфирные масла, альфа-гидроксикислоты, мочевина, проводники (диметилсульфок-сид), ПАВы, чрескожные пенетраторы. В частности, повысить проведение действующего вещества в ткани можно, добавив в лекарственную форму диметилсуль-фоксид (ДМСО), смешав с лекарственным препаратом в соотношении 1:10 или перед использованием крема/геля/мази нанести на кожу аппликацию димексида с лидока-ином в разведении 1:10 - 1:5.
Глубину проникновения локальных форм НПВП можно повысить путем использования их в процедуре фонофореза.
При использовании локальных форм НПВП максимальная концентрация дей-
ствующего вещества создается в жировой ткани (4,7 мкг/г), а в синовиальной жидкости она меньше и составляет лишь 1,31 мкг/г. В крови при этом концентрация составляет 0,0018 мкг/г, исключая системный эффект препарата и, соответственно, развитие нежелательных побочных эффектов.
Эффективность местного использования лекарственных форм, содержащих НПВП, оценивают по выраженности обезболивания, уменьшению припухлости и улучшению функции суставов.
Действующее вещество крема -ацеклофенак, концентрация активного ингредиента составляет 1,5%. Крем содержит такие вспомогательные вещества, как пропилпарагидроксибензоат, метил-парагидроксибензоат, парафин жидкий, эмульсионный воск, вода очищенная.
Эмульсионный воск представляет собой смесь солей эфиров фосфорной кислоты с высшими жирными спиртами. Это один из самых удобных и простых в применении эмульгаторов. Отлично взаимодействует с другими эмульгаторами и активами. Усиливает стабильность и улучшает консистенцию продукта. Помимо эмульгирующих свойств, хорошо увлажняет и смягчает кожу. Предотвращает потерю воды, не оставляет ощущения жирности на коже. Наличие фосфорных групп делает его близким к лецитину и кефалину, входящим в состав кожного жира, поэтому достаточно комфортно воспринимается кожей в составе различных косметических средств. Воск не вызывает аллергии, может использоваться в детской косметике.
Жидкий парафин является синтетическим препаратом, представляет собой очищенную фракцию нефти, получаемую после отгонки керосина. При наружном применении не раздражает кожу, не вызывает аллергии, не всасывается, стойкий, не разлагается, создает окклюзионную пленку.
Несомненное достоинство крема Аэртал - его микронизированная форма, в состав препарата входят >60% частиц размером 90% размером Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Л И Т Е Р А Т У Р А
1. Цветкова Е.С, Алекберова З.С., Балабанова Р.М. и др. // Терапевт. архив. - 1994. - №5. - С.69-72.
3. Brown M.B., Martin G.P., Jones SA, Akomeah FK. // Drug Deliv. - 2006. - Vol.13(3). - P.175-187.
4. Janssen M, Dijkmans M, van derSluijs FA. // Br. J. Rheum. - 1992. - Vol.31. - P.747-752.
5. Singh P., Roberts M.S. // J. Pharm. Sci. - 1994. -Vol.83, N6. - P.774-779.
Поступила 19.12.2014 г.
immrnmrnrn втммт на ШШцШШШМ РЫНКЕ БЕЛАРУСИ
Информация из инструкции по применению*
Держатель разрешения на маркетинг: Les Laboratoires Servier, Ле Лаборатуар Сервье 50, rue Carnot, 92284 Suresnes cedex, France.
*Полную информацию, включающую особые указания и предосторожности при приеме, Вы можете найти в сводных характеристиках препарата.
Уколы для суставов — неотъемлемая часть лечения многих заболеваний опорно-двигательной системы. Чаще всего их назначают при деформирующем остеоартрозе (ОА), травмах и хронических воспалительных болезнях суставов. Для выполнения инъекций используют несколько групп препаратов. Выбор лекарства, способа его введения и схемы терапии осуществляет лечащий врач.
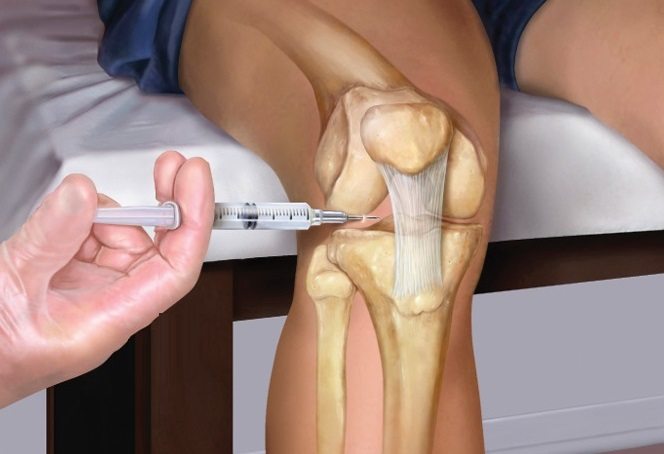
Разберемся, какие уколы от заболеваний суставов вам может назначить специалист в разных ситуациях. Выясним, как действует то или иное лекарство, в чем заключаются преимущества каждого способа введения.
Кому и зачем нужны инъекции для суставов
Важно знать! Врачи в шоке: "Эффективное и доступное средство от боли в суставах существует. " Читать далее.
Лекарственные блокады обычно используются для быстрого купирования болевого синдрома, причиной которого могут быть ушибы, травмы, вывихи, растяжения связок, разрывы менисков, острые воспалительные процессы в области колена. Такие уколы делают при посттравматических болях в коленном суставе. Введение местных анестетиков позволяет облегчить страдания пациента, но не оказывает лечебного эффекта. После инъекции больного обследуют и назначают курс лечения.
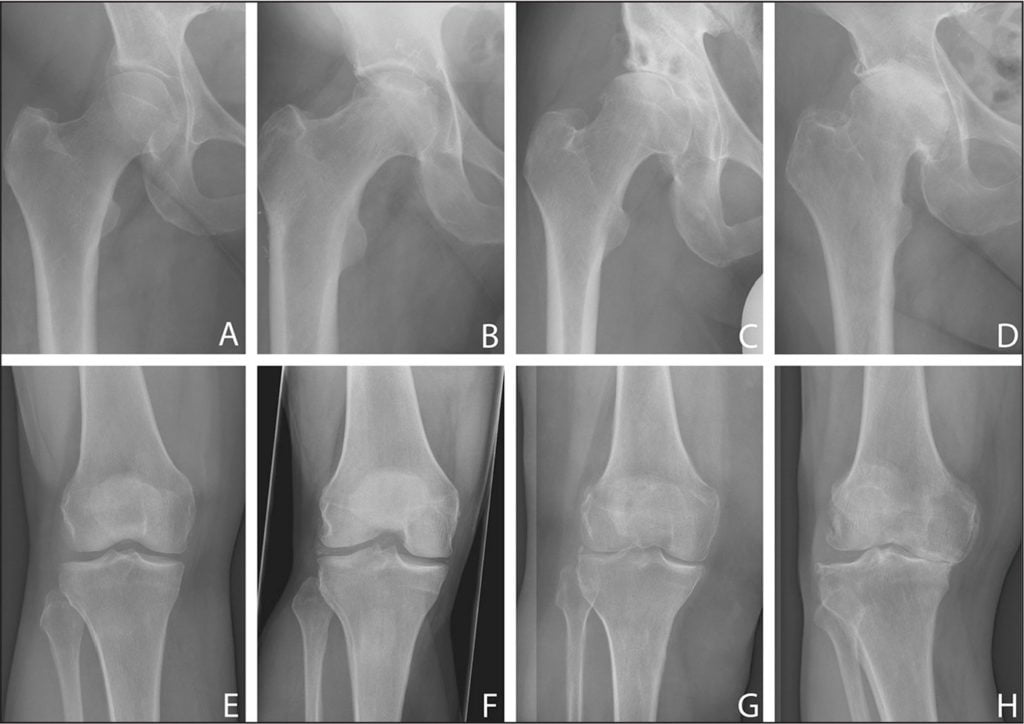
Названия широко используемых уколов от острой боли в суставах: Новокаин, Тримекаин, Лидокаин.
Плановую локальную инъекционную терапию (ЛИТ) назначают только после обследования пациента. Лекарственные препараты и схему лечения врачи подбирают, согласовывая с больным. Процедуры выполняют амбулаторно, реже – в условиях стационара.
Болезни, при которых требуется ЛИТ:
- остеоартроз;
- периартрит;
- ревматоидный артрит;
- бурсит;
- тендинит;
- синовит;
- подагра;
- посттравматические дегенеративные изменения суставов.
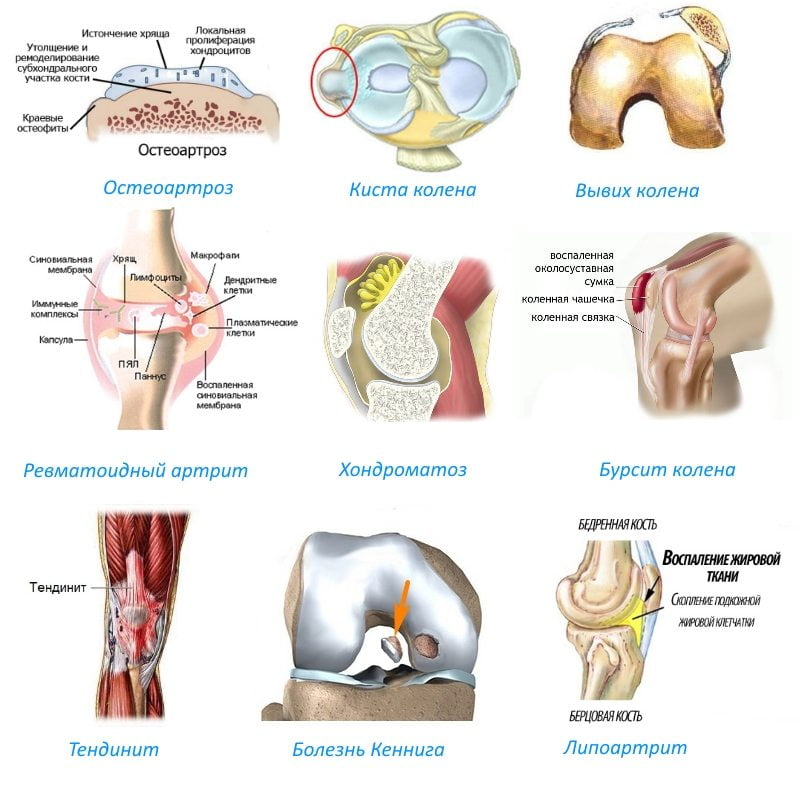
Помимо лекарственных препаратов, в суставные полости также могут вводить углекислый газ (CO2), обогащенную тромбоцитами плазму (ОТП), продукты клеточной или тканевой инженерии. Эти средства применяют при хронических болезнях суставов, которые сопровождаются разрушением хрящей.
При гнойных синовитах, бурситах и артритах пациентам удаляют избыточную синовиальную жидкость, промывают суставную полость и вводят туда антибиотики. Названия популярных антибактериальных уколов для суставов: Цепорин, Ампициллин, Гентамицин.
Виды инъекций
В ортопедии и травматологии используют несколько способов введения лекарственных препаратов. Каждому из них врачи отдают предпочтение в той или иной ситуации. При растяжении или воспалении связок чаще назначают околосуставные инъекции кортикостероидов с местными анестетиками, при тяжелом деформирующем остеоартрозе – внутрисуставное введение гиалуроновой кислоты.
Способы инъекционного введения препаратов в ортопедии и травматологии:
- внутримышечный. Используется, когда необходимо купировать ярко выраженный болевой синдром. Внутримышечно пациентам вводят нестероидные противовоспалительные средства (Артрозан, Мовалис, Династат, Амелотекс). При хроническом остеоартрозе в мышцы больным могут колоть хондропротекторы. Гиалуроновую кислоту и кортикостероиды этим способом не вводят;
- периартикулярный. Лекарства колют в околосуставные ткани. Периартикулярная блокада нужна при сильных болях в суставе, вызванных травмой или воспалением. Введение кортикостероидов и местных анестетиков эффективно, когда поражены только околосуставные ткани, но не сам сустав;
- внутрисуставной. Применяют при тяжелых заболеваниях суставов. В синовиальную полость вводят лекарства, которые оказывают противовоспалительное, регенерирующее или восстанавливающее действие. Для инъекций обычно используют кортикостероиды, хондропротекторы или гиалуроновую кислоту. Иногда для лечения применяют несколько препаратов.
При деформирующем остеоартрозе наиболее эффективно внутрисуставное введение препаратов. Оно позволяет создать максимальную концентрацию лекарства в очагах патологии. Эффект от такой терапии выше, чем от приема таблеток и внутримышечных инъекций.
Группы препаратов для инъекционного введения
Для лечения суставов различной локализации используют одни и те же лекарственные препараты. По направленности действия их можно разделить на противовоспалительные, обезболивающие, антибактериальные и регенерирующие средства. Давайте выясним, как действуют разные группы лекарственных препаратов.
Многих людей интересуют названия уколов для коленного сустава. При травмах и болезнях колена пациентам колют те же препараты, что и при поражении суставов любой другой локализации.
Таблица 1. Инъекционные средства, которые используют в ортопедии и травматологии
Читайте также:


