Микробиологическое исследование воздушно-капельных инфекций
13.1. Коринебактерии.
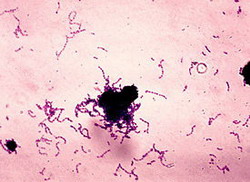
Коринебактерии относятся к семейству Corynebacteriaceae, родуCorynebacterium, видуC.Diphtheriae. Это тонкие палочки, прямые или слегка изогнутые, грамположительные. Для них характерен полиморфизм. На концах булавовидные утолщения – зерна волютина. Эти включения располагаются по одному на каждом конце и могут быть выявлены при окраске по методу Нейссера. В мазках бактерии располагаются под углом, напоминая латинские буквы. Спор и капсул не образуют, неподвижны, имеют фимбрии, являются факультативными анаэробами или аэробами.
Коринебактерии требовательны к питательным средам. Для их культивирования применяются сывороточные среды или среды с добавлением крови. Для выделения используются элективные питательные среды с добавлением теллурита калия в такой концентрации, в которой он не подавляет рост коринебактерий, но ингибирует рост сопутствующей микрофлоры. На кровяно-теллуритовом агаре рост бактерий наблюдается через 24-48 часов в виде черных или черно-серых колоний.
Биохимические свойства: ферментирует глюкозу и мальтозу с образованием кислоты, не разлагает сахарозу, лактозу и манит, не продуцирует уреазу, не образует индол. Продуцирует фермент цистиназу, расщепляет цистин до Н2S, образует каталазу.
По биохимическим свойствам Коринебактерии подразделяются на четыре биовара: gravis,mitis,intermedius,belfanti.
C.Diphtheriaeделятся на токсигенные и нетоксигенные штаммы. Заболевание вызывают только токсигенные. Определение токсина проводят с помощью реакции преципитации в геле.
Антигенная структура: 1) групповой полисахаридный антиген, 2) видовой О-антиген, 3) вариантспецифический К-антиген.
Факторы патогенности: 1) ворсинки, фимбрии или пили; 2) колонизация и инвазия (за счет ферментов нейраминидазы, гиалуронидазы, протеазы); 3) корд-фактор (нарушает фосфорилирование процессов дыхания клеток макроорганизма); 4) экзотоксин – дифтерийный гистотоксин оказывает блокирующее воздействие на синтез белка в органах, наиболее интенсивно снабженных кровью.
Источник инфекции – больные и носители. Пути передачи – воздушно-капельный, контактно-бытовой. Возбудитель проникает через слизистые оболочки ротоглотки, реже – глаз, половых органов, кожу, раневую поверхность. В месте входных ворот возбудитель прикрепляется к соответствующим рецепторам эпителиальных клеток, вызывая воспалительный процесс. Затем происходит кологизация и выделение экзотоксина. Токсин блокирует ферменты синтеза белка в клетках хозяина, что приводит к их гибели. Это обуславливает некроз и летальный исход.
Фибринозная пленка – характерный признак дифтерии. Фибринозное воспаление может быть крупозным или дифтерическим. Дифтерическое воспаление возникает на слизистых оболочках (ротоглотка, надгортанник, голосовые связки). Фибринозная пленка плотно связана с подлежащей тканью и не снимается тампоном при осмотре. При попытке сделать это слизистая оболочка кровоточит. Крупозное воспаление возникает при локализации патологического процесса в дыхательных путях (гортань, трахеяь и бронхи). Здесь фибринозная пленка располагается поверхностно и легко отделяется от подлежащих тканей. Крупозное воспаление ведет к развитию асфиксии.
После перенесенного заболевания формируется нестойкий и непродолжительный антибактериальный антибактериальный иммунитет и стойкий антитоксический.
Лабораторная диагностика. 1) Основной метод – бактериологический. Материалом для исследования является слизь и пленка из очагов поражения. Бактериологическому обследованию в обязательном порядке подлежат все больные с ангинами и подозрением на дифтерию. Сбор материала необходимо проводить в течение 3-4 часов с момента обращения больного. Для взятия материала используют сухие стерильные ватные тампоны. Различают три вида показаний к проведению бактериологических исследований на дифтерию: диагностическое обследование, по эпидемиологическим показаниям (контактные), с профилактической целью; 2) серологический метод (РПГА) – исследуется сыворотка крови больного на выявление антител. С диагностической целью сыворотка исследуется в динамике для определения нарастания титра антител. С целью изучения напряженности иммунитета к дифтерии, сыворотка исследуется однократно. Защитный титр антител – 1:40.
Лечение: 1) специфическая противодифтерийная лошадиная очищенная концентрированная жидкая сыворотка, вводится по Безредке дробно (анафилактический шок); 2) иммуноглобулин человека противодифтерийный для в/в введения; 3) антибиотики – пенициллин, эритромицин, бета-лактамы, макролиды.
Специфическая профилактика. Активная – используются вакцины АКДС, АДС-анатоксин, АДС-М-анатоксин, АД-М-анатоксин, тетракок (коклюш, дифтерия, столбняк, полиомиелит). Иммунизацию проводят, начиная с 3-месячного возраста, троекратно, с интервалами в 4-6 недель. Пассивная – проводится в очагах заболевания антитоксической сывороткой.
[youtube.player]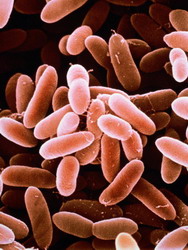
Streptococcus mutans — грамм-положительная, факультативно анаэробная бактерия, обычно обнаруживаемая в ротовой полости.
Возбудителем ВИЧ-инфекции является вирус иммунодефицита человека: ВИЧ — может быть двух типов (1 и 2) (по-английски HI.
Почва — это смесь частиц органических и неорганических веществ, воды и воздуха. Неорганические частицы почвы — это .
Краснуха (устар. — германская корь, коревая краснуха) — острозаразное вирусное заболевание, характеризующееся слабо вы.
Воздушно-капельные инфекции. Род Mycobacterium
В состав рода включены тонкие, ветвящиеся палочки; спирто-кислото-щелочеустойчивые, аэробные, грам+ бактерии. В род микобактерий входят возбудители туберкулеза и лепры, а также сапрофитов, распространенных в окружающей среде. Из патогенных микобактерий выделено 5 групп: М. tuberculosis, M. bovis, M. microti, M. leprae, М. lepraemirium.
M. tuberculosis — Микобактерий туберкулеза человека были открыты Р. Кохом в 1882 г. В честь этого открытия возбудитель туберкулеза до сих пор называют палочкой Коха. Это заболевание известно людям с древних времен. Легочная форма была описана древнегреческим врачом Гиппократом. Тогда эта болезнь не считалась инфекционной, а врач арабского Востока Авиценна считал ее наследственной. Первым связь легочных бугорков с чахоткой увидел Сильвий.
В XVIII—XIX вв. туберкулез унес многие жизни, в том числе и выдающихся деятелей того времени — А.П. Чехова, Н.А. Некрасова, Моцарта, Шопена. Инфекционная природа туберкулеза впервые была доказана Вильмёном (1865 г.), а Р. Кохом был выделен возбудитель в чистом виде.
Морфологические и культуральные свойства. Микобак-терии туберкулеза характеризуются полиморфизмом. Это тонкие, длинные, слегка изогнутые палочки. Иногда имеют небольшие вздутия на концах. В молодых культурах палочки более длинные, а в старых склонны к простому ветвлению. Иногда образуются короткие, толстые палочки. Неподвижны, грамположительны, не образуют спор и капсул. Ми-кобактерии в связи с высоким содержанием миколовой кислоты и липидов в клеточной стенке плохо окрашиваются обычными методами, поэтому для их выявления применяют окраску по Цилю—Нильсену: палочки окрашиваются в ярко-красный цвет на голубом фоне.
На поверхности клеток имеются микрокапсулы. Электронной микроскопией на концах клеток выявлено наличие гранул и вакуолей. Цитоплазма молодых культур гомогенная, старых — зернистая. Кислотоустойчивость объясняется наличием у туберкулезных микобактерий большого количества миколовой кислоты и липидов.
Туберкулезная палочка — это очень медленнорастущий микроорганизм; требовательна к питательным средам, гли-церинзависима. Аэробы, но способны расти и в факультативно анаэробных условиях. Крайние температурные пределы 25—40°С, opt — 37°С. Реакция среды почти нейтральная (рН 6,4—7,0), но может расти в пределах рН 4,5—8,0. Для лучшего роста микобактерий в среды добавляют витамины (биотин, никотиновая кислота, рибофлавин), а также ионты (Mg2+, K+, Na+, Fe2+). Для выращивания часто используют плотные яичные среды, глицериново-картофельный агар, а также синтетические и полусинтетические жидкие среды (например, жидкая среда Сотона). На жидких средах туберкулезная палочка образует через 5—7 суток сухую морщинистую пленку, поднимающуюся на края пробирки. Среда при этом остается прозрачной. На плотных средах туберкулезная палочка образует колонии кремового цвета, напоминающие цветную капусту, крошковатые, плохо снимаются бактериологической петлей. Этот рост наблюдают на 14—40-е сутки.
Антигенная структура. Реакциями агглютинации и связывания комплемента установлено несколько видов микобактерий: млекопитающих, птиц, холоднокровных, сапро-фитов.
Человеческий вид серологически не отличается от бычьего и птичьего видов. Антиген микобактерий туберкулеза содержит протеины, липиды, фосфатиды и полисахариды. Туберкулин считают антигеном, который при действии на инфицированный туберкулезом организм вызывает местную, очаговую аллергическую реакцию (проба Манту).
Резистентность. По сравнению с другими неспорообра-зующими палочками микобактерий туберкулеза очень устойчивы во внешней среде. В проточной воде они могут сохранять жизнеспособность до 1 года, в почве и навозе — 6 мес., на различных предметах — до 3 мес., в библиотечной пыли — 18 мес., в высушенном гное и мокроте— до 10мес. При кипячении палочка Коха погибает через 5 мин, в желудочном соке— через 6ч, при пастеризации— через 30мин. Микобактерий чувствительны к солнечному свету и активированным растворам хлорамина и хлорной извести.
Эпидемиология. Заболевание туберкулезом носит пандемический характер и распространено повсеместно. Источником инфекции М. tuberculosis является больной человек, основной путь заражения — аэрогенный. Человек очень восприимчив к этому заболеванию. Подавляющее большинство населения рано или поздно заражается туберкулезом, но в большинстве случаев заражение вызывает небольшие изменения без наклонности к прогрессирующему развитию болезни. Они даже ведут к повышению устойчивости организма—к специфическому иммунитету. Несмотря на это, во всем мире растет заболеваемость туберкулезом. Ежегодно в мире заболевают туберкулезом более 8 млн человек, 95% из них — жители развивающихся стран. В 1991 г. Генеральная Ассамблея Всемирной организации здравоохранения (ВОЗ) была вынуждена констатировать, что туберкулез является международной и национальной проблемой здравоохранения не только в развивающихся, но и в экономически развитых странах. Ежегодно от туберкулеза умирают 3 млн человек, в ближайшие 10 лет могут умереть 30 млн больных. Поэтому сложившаяся ситуация была охарактеризована ВОЗ как кризис глобальной политики в области туберкулеза.
Патогенез поражений. Туберкулез у человека вызывается двумя основными видами микобактерий — человеческим (М. tuberculosis) и бычьим (М. bo vis), реже микобактериями птичьего типа (М. avium). Заражение происходит воздушно-капельным и воздушно-пылевым путем, иногда через рот, при употреблении пищевых продуктов, инфицированных туберкулезными микобактериями, через кожу и слизистые.
Возможно внутриутробное инфицирование плода через плаценту.
При аэрогенном заражении первичный инфекционный очаг развивается в легких, а при алиментарном — в мезентеральных лимфатических узлах. В развитии болезни выделяют первичный, диссеминированный и вторичный туберкулез, который является эндогенной реактивацией старых очагов, При низкой сопротивляемости организма и неблагоприятных социальных условиях из места первичной локализации возбудитель может распространиться по всему организму и вызвать генерализованную инфекцию.
Образование первичного комплекса характеризуется развитием гранулем в виде бугорков (бугорчатка или туберкулез). Образование гранулем не имеет характерных особенностей и представляет собой клеточную реакцию. Микобактерий окружают лейкоциты и все это скопление окружено эпителиоидными и гигантскими (многоядерными) клетками. Наиболее часто первичный очаг наблюдают в легких (очаг Гона). При хорошей сопротивляемости организма, микобактерий могут находиться в бугорке несколько лет или всю жизнь. В большинстве случаев первичные очаги заживают с полной деградацией содержимого, его кальцификацией и фиброзом паренхимы. При снижении иммунитета первичные очаги активизируются и прогрессируют с развитием вторичного процесса. Такая реактивация обычно происходит через 20—25 лет после первичного инфицирования; обычно ее провоцируют стрессы, нарушение питания и общее ослабление организма. По статистике, 80% людей заболевают леточной формой туберкулеза, остальные 20% — туберкулезом других органов и тканей (диссеминированный туберкулез). Встречаются поражения туберкулезом гениталий, костей и суставов, кожи и др.
Клинические проявления. Инкубационный период при туберкулезе сравнительно продолжительный — от нескольких недель до 5 лет. Заболевание может развиваться остро: резкая одышка, боли в грудной области. Реактивный туберкулез проявляется кашлем, иногда с кровохарканьем; снижением массы тела; ночным потоотделением; субфебриль-ной температурой тела. Симптомов, специфичных только для туберкулеза, нет, так как туберкулез характеризуется многообразием клинических форм, анатомических изменений.
Иммунитет. Иммунитет при туберкулезе нестерильный, обусловлен наличием в организме Z-форм микобактерий. Приобретенный иммунитет является следствием активации Т-клеток с помощью антигенов микобактерий туберкулеза. Поэтому исход болезни определяется активностью клеточных факторов иммунитета.
Одним из факторов защиты являются бактериофаги, оказывающие действие как на вирулентные, так и на авирулен-тные штаммы туберкулезных палочек.
Методы диагностики туберкулеза:
1. Микроскопирование. Этот метод прост, доступен, позволяет быстро дать ответ. В мазках, окрашенных по Цилю— Нильсену, можно выявить красные палочки на голубом фоне. Недостатком этого метода является его небольшая чувствительность (ввиду очень медленного роста микобактерий могут не попасть в мазок, их можно выявить при содержании 100 000—500 000 микобактерий в 1 мл материала).
2. При отрицательном микроскопировании применяют микробиологический метод: высев исследуемого материала на питательные среды (обычно Левенштайна—Йенсена).
Для простоты выделения в среды добавляют антибиотики, подавляющие рост сопутствующих микроорганизмов. Достоинство этого метода заключается в возможности получения чистой культуры, что позволяет ее идентифицировать и определить чувствительность к лекарственным препаратам. Недостаток — медленный рост палочки Коха (от 4 до 14 недель).
4. Для раннего выявления больных туберкулезом используется рентгенологический (флюорографический с 15 лет) метод диагностики. По действующим директивным документам периодичность его проведения определяется эпидситуацией по туберкулезу и группами населения, подлежащего осмотрам.
Профилактика туберкулеза обеспечивается путем ранней диагностики, своевременного выявления больных и их диспансеризации, обезвреживания молока и мяса больных животных. Профилактика заключается в проведении социальных мероприятий (улучшение условий труда и быта населения, повышение его материального и культурного уровня).
Для иммунопрофилактики используется вакцина БЦЖ — аттенуированные микобактерии бычьего типа. В России вакцинацию проводят всем новорожденным. В США — только в группах повышенного риска. Иммунизация, как средство профилактики туберкулеза, не оптимальна, и чем более серьезнее складывается эпидситуация по туберкулезу, тем она менее эффективна. Введение последующих ревакцинаций БЦЖ в более старшем возрасте не оказывает влияния на заболеваемость. Поэтому самое главное в специфической иммунизации — это защитить детей. После вакцинации на некоторое время отказываются от постановки кожных проб для предупреждения гиперреактивных осложнений (некротические реакции и т. д.).
М. bovis — вызывает туберкулез у крупного рогатого скота и в 5% случаях у человека. Крупный рогатый скот заражается туберкулезом аспирационно, при вдыхании инфицированной пыли, а также алиментарно — через зараженные корм и воду. Бацилловыделение с молоком часто происходит даже у животных, у которых нет клинически выраженных изменений. В связи с этим большое значение имеет инфицирование человека молоком или молочными продуктами, полученных от больных животных.
Особую опасность туберкулез крупного рогатого скота и птиц представляет для работников животноводства и птицеводства, мясокомбинатов, убойных пунктов, среди которых туберкулез носит выраженный профессиональный характер.
Поражения у людей отличает склонность к осложнениям, генерализации, экссудативным реакциям и бронхогенному метастазированию. Морфологически не отличается от М. tuberculosis. Методы выделения возбудителя также аналогичны микобактериям человеческого типа. М. bovis выделяют у 60 видов млекопитающих, но эпидемиологическую опасность представляют крупный рогатый скот, верблюды, козы, овцы, свиньи, собаки и кошки.
Схема выделения мнкобактернй туберкулеза
Люми-л 'несцентная4 микроскопия
M. leprae — возбудитель проказы (лепры или болезни Хансена).
Морфологические и культу рал ьные свойства. Палочки лепры прямые или изогнутые, концы могут быть заостренными или утолщенными, неподвижные, спор и капсул не образуют, спирте-, кислотоустойчивые, грамполо-жительные.
M. leprae трудно выращивать на питательных средах. Культуры развиваются очень медленно (6—8 недель), образуют колонии в виде сухого морщинистого налета.
Эпидемиология проказы до конца не изучена. Избирательность заражения не поддается логике. В медицинской литературе описывают случай, когда за больным проказой отцом ухаживала старшая дочь, а заболели средняя и младшая, которые меньше всех контактировали с больным. Поэтому в каждом конкретном случае невозможно выявить путь заражения.
Резервуар инфекции — больной человек. Предположительно заражение происходит контактным путем или воздушно-капельным. Основным способом борьбы с проказой остается изоляция больных. Ведущая роль в распространении инфекции принадлежит социально-экономическим факторам, о чем свидетельствует высокая заболеваемость в странах третьего мира. В России уровень заболеваемости невысокий. В Липецкой, Иркутской, Ленинградской областях — по 1 больному, в Ростовской области — 70 человек (Дон является эндемичной по проказе территорией — еще с тех времен, когда казаки отправлялись в дальние походы).
Патогенез поражений. Проказой болеют только люди, поэтому источник болезни — больной человек. Патогенез обусловлен образованием бугорков (по типу туберкулезных) в различных органах и тканях, куда возбудитель попадает с током крови и лимфы. При хорошей сопротивляемости организма болезнь протекает латентно и может не проявляться в течение жизни. Вероятность заболевания зависит от иммунного статуса организма человека. Тяжелой формой заболевания считается лепро-матозная.
Клинические проявления. Инкубационный период — от 3 до 5 лет, иногда затягивается до 20 лет. В начале заболевания общие симптомы интоксикации: лихорадка, слабость, боли в костях и др. Появляются поражения кожи в виде высыпаний, которые представляют четко ограниченные пятна (леприды) разной окраски и размеров. Потом возникают другие симптомы: отсутствие чувствительности к высокой или низкой температуре, к боли.
Лабораторная диагностика. Материал от больного получают энергичным соскобом слизистой носа, пункции увеличенных лимфатических узлов. Диагностика осуществляется микроскопированием. Мазки окрашивают по Цилю—Нильсену. Также для диагностики применяют ложную пробу с аллергеном М. leprae (лепроминовая проба), которая всегда отрицательна при поражениях лица. Это связано с отсутствием клеточных иммунных реакций.
Схема выделения возбудителя лепры ЛЕПРА
'Соскоб со слизи-4* ^стой оболочки носа,1 пунктах или гистологический срез лепрозных узлов, k отделяемое язв, и др.
Окр. по Цилю—л Нильсену
Метод выявления гиперчувствительности
Проба с лепромином
Лечение. В медицинских кругах бытуют легенды об ученых, прививавших себе лепру, чтобы опробовать испытываемые средства спасения. Однако эксперименты не увенчались успехом: препарата, победившего проказу, нет до сих пор. Часто интенсивная химиотерапия проводится на протяжении всей жизни больного проказой. Основные препараты — сульфоны, рифампицин, клофазилин.
[youtube.player]ЛЕКЦИЯ № 24. Возбудители вирусных воздушно-капельных инфекций
1. Вирусы кори и паротита
Вирус эпидемического паротита и вирус кори относятся к семейству Paramixoviridae.
Вирионы имеют сферическую форму диаметром 150–200 нм. В центре вириона расположен нуклеокапсид со спиральным типом симметрии, окруженный внешней оболочкой с шиповидными отростками. Вирусная РНК представлена односпиральной минус-нитью. Нуклеокапсид покрыт матриксным белком, который состоит из двух липидных слоев и трех вирусных специфических белков.
Вирус эпидемического паротита относится к роду Paramyxovirus. Вирусная инфекция характеризуется преимущественным поражением околоушных слюнных желез и способностью вызывать эпидемические вспышки.
1) внутренний NP-протеин;
2) поверхностные NH– и F-гликопротеины.
Первоначально возбудитель репродуцируется в эпителии носоглотки, затем проникает в кровоток и в период вирусемии проникает в различные органы: околоушные железы, яички, яичники, поджелудочную, щитовидную железы, головной и другие органы. Также возможна первичная репродукция в эпителии околоушных желез.
Основной путь передачи – воздушно-капельный.
Лабораторная диагностика: выделение вируса из спинномозговой жидкости, слюны и пунктатов желез и культивирование на куриных эмбрионах и культурах клеток фибробластов кур.
Средства специфической лекарственной терапии отсутствуют.
1) живая и убитая вакцина;
2) специфический иммуноглобулин.
Вирус кори относится к роду Morbillivirus.
1) гемагглютинин (Н);
3) нуклеокапсидный белок (NP).
Основные пути передачи – воздушно-капельный, реже контактный.
Первоначально вирус размножается в эпителии верхних отделов дыхательных путей и регионарных лимфатических узлах, а затем проникает в кровоток. Вирусемия носит кратковременный характер. Возбудитель гематогенно разносится по всему организму, фиксируясь в ретикулоэндотелиальной системе. Активность иммунных механизмов, направленных на уничтожение инфицированных клеток, приводит к высвобождению вируса и развитию второй волны вирусемии. Тропность возбудителя к эпителиальным клеткам приводит к вторичному инфицированию конъюнктивы, слизистых оболочек дыхательных путей и полости рта. Циркуляция в кровотоке и формирующиеся защитные реакции обуславливают повреждение стенок сосудов, отек тканей и некротические изменения в них.
1) обнаружение многоядерных клеток и антигенов возбудителя (в реакции иммунофлюоресценции) в отделяемом носоглотки;
2) выделение вируса на первично-трипсинизированных культурах клеток почек обезьян или эмбриона человека;
3) выявление нарастания титров антигенов в период реконвалесценции.
Лечение: средства специфической терапии отсутствуют.
1) противокоревой иммуноглобулин человека;
2) живая аттенуированная вакцина.
2. Вирус герпеса
Семейство Herpesviridae включает в себя подсемейства:
1) a-herpesviruses (I и II типов, герпес-зостер);
Относятся к ДНК-овым вирусам. ДНК двухнитевая, линейная. Геном состоит из двух фрагментов: длинного и короткого. Нить ДНК намотана на центральную белковую культуру. Капсидная оболочка построена из простых белков, имеет кубический тип симметрии. Имеется суперкапсидная оболочка (липидная мембрана со слоем гликопротеидов), неоднородная по строению, образует шиповидные отростки.
Герпес-вирусы относительно нестабильны при комнатной температуре, термолабильны и быстро инактивируются растворителями и детергентами.
a-герпес типа I вызывает афтозный стоматит в раннем детском возрасте, лабиальный герпес, реже – герпетический кератит и энцефалит.
a-герпес типа II вызывает генитальный герпес, герпес новорожденных, является предрасполагающим фактором к развитию рака шейки матки.
Герпес-зостер является возбудителем опоясывающего лишая и ветряной оспы. Это типичная герпес-вирусная инфекция. Клинически проявляется появлением пузырьков на коже по ходу ветвей соответствующих нервов. Заболевание протекает тяжело, но быстро наступает выздоровление.
После перенесенной инфекции остается пожизненный иммунитет. Однако возможны рецидивы болезни, связанные с персистенцией вируса в нервных ганглиях.
После перенесенного герпес-вирусного заболевания вирус пожизненно персистирует в нервных ганглиях (чаще тройничного нерва). При снижении защитных сил организма происходит развитие вирусной инфекции.
b-герпес (цитомегаловирус) при размножении в клетках культуры вызывает цитопатические изменения. Имеет сродство с клетками слюнных желез и почек, вызывая в них образование крупных многоядерных включений. При развитии заболевания имеют место вирусемия, поражение внутренних органов, костного мозга, ЦНС, развитие иммунопатологических заболеваний.
g-герпес-вирус (вирус Эпштейна-Бара) вызывает инфекционный мононуклеоз. Может являться предрасполагающим фактором в развитии опухолей.
1) выявление характерных многоядерных гигантских клеток с тельцами включений в соскобах из области поражений;
2) культивирование в куриных эмбрионах;
3) биологическая проба;
4) серологические исследования (РСК, ИФА);
5) метод прямой иммунофлюоресценции с моноклональными антигенами.
1) обнаружение крупных цитомегаловирусных клеток в моче и слюне;
2) культивирование в культуре фибробластов эмбриона человека;
3) серологическое исследование (РСК);
1) выделение вируса в культуре фибробластов;
2) микроскопия мазков осадка мочи, слюны для выявления типичных гигантских клеток;
3) серологические методы (РСК, РПГА и РН).
1) противовирусные препараты (ацикловир);
3. Вирус краснухи
Относится к семейству Togaviridae, роду Rubivirus.
Это сферические оболочечные вирусы с икосаэдральным нуклеокапсидом, заключенным в липидную оболочку. Средняя величина рубивирусов – 60 нм. Поверхность вирусов покрыта гликопротеиновыми спикулами, содержащими гемагглютинины.
Вирус краснухи имеет два антигена:
1) нуклеопротеид, связанный с капсидом;
2) белок суперкапсидной оболочки.
Вирус представлен одним серотипом, обладающим гемагглютинирующей, гемолитической и слабовыраженной нейраминидазной активностью.
У человека вирус вызывает краснуху – острое инфекционное заболевание, обычно наблюдаемое у детей.
Краснуха – высококонтагиозная, широко распространенная инфекция; источник – больной человек; основной путь передачи возбудителя – воздушно-капельный. При выздоровлении формируется пожизненная невосприимчивость.
Патогенез типичной формы включает в себя развитие острых воспалительных реакций в верхних отделах дыхательных путей и циркуляцию возбудителя в кровотоке с последующим поражением различных органов, включая плаценту при беременности.
Характерный признак заболевания – пятнисто-папулезная сыпь бледно-розового цвета, наиболее обильная на разгибательных поверхностях конечностей, спине и ягодицах. Через 2–3 дня кожные элементы исчезают, не оставляя пигментации и шелушения. Взрослые переносят краснуху тяжелее: температура может достигать 39 °C, возможны сильные головные боли и миалгии, выраженные катары слизистой оболочки носа и конъюнктивы.
Наибольшую опасность представляет инфицирование плода во время беременности – при этом наблюдают формирование множественных пороков (катаракты, пороков сердца, микроцефалии и глухоты).
Вирус малоустойчив во внешней среде, погибает при воздействии физических и химических факторов.
1) выделение возбудителя в культурах клеток человеческого эмбриона;
2) серологическая диагностика (РСК, РТГА) методами ИФА и РИА, РН.
1) средства этиотропной терапии отсутствуют;
2) беременным, контактировавшим с больным, профилактически вводят специфический иммуноглобулин.
Специфическая профилактика: живая аттенуироваиная вакцина; иммунизацию женщин детородного возраста следует проводить лишь при отсутствии беременности.
[youtube.player]| Название | Честнова т. В., Смольянинова о. Л. Медицинская микробиология, вирусология и иммунология |
| Анкор | Методическое пособие по микробиологии.doc |
| Дата | 27.09.2017 |
| Размер | 1.77 Mb. |
| Формат файла |  |
| Имя файла | Методическое пособие по микробиологии.doc |
| Тип | Учебно-практическое пособие #20474 |
| страница | 14 из 21 |
| Каталог |
|
Тема 13. Возбудители бактериальных воздушно-капельных инфекций. Коринебактерии относятся к семейству Corynebacteriaceae, роду Corynebacterium, виду C. Diphtheriae. Это тонкие палочки, прямые или слегка изогнутые, грамположительные. Для них характерен полиморфизм. На концах булавовидные утолщения – зерна волютина. Эти включения располагаются по одному на каждом конце и могут быть выявлены при окраске по методу Нейссера. В мазках бактерии располагаются под углом, напоминая латинские буквы. Спор и капсул не образуют, неподвижны, имеют фимбрии, являются факультативными анаэробами или аэробами. Коринебактерии требовательны к питательным средам. Для их культивирования применяются сывороточные среды или среды с добавлением крови. Для выделения используются элективные питательные среды с добавлением теллурита калия в такой концентрации, в которой он не подавляет рост коринебактерий, но ингибирует рост сопутствующей микрофлоры. На кровяно-теллуритовом агаре рост бактерий наблюдается через 24-48 часов в виде черных или черно-серых колоний. Биохимические свойства: ферментирует глюкозу и мальтозу с образованием кислоты, не разлагает сахарозу, лактозу и манит, не продуцирует уреазу, не образует индол. Продуцирует фермент цистиназу, расщепляет цистин до Н2S, образует каталазу. По биохимическим свойствам Коринебактерии подразделяются на четыре биовара: gravis, mitis, intermedius, belfanti. C. Diphtheriae делятся на токсигенные и нетоксигенные штаммы. Заболевание вызывают только токсигенные. Определение токсина проводят с помощью реакции преципитации в геле. Антигенная структура: 1) групповой полисахаридный антиген, 2) видовой О-антиген, 3) вариантспецифический К-антиген. Факторы патогенности: 1) ворсинки, фимбрии или пили; 2) колонизация и инвазия (за счет ферментов нейраминидазы, гиалуронидазы, протеазы); 3) корд-фактор (нарушает фосфорилирование процессов дыхания клеток макроорганизма); 4) экзотоксин – дифтерийный гистотоксин оказывает блокирующее воздействие на синтез белка в органах, наиболее интенсивно снабженных кровью. Источник инфекции – больные и носители. Пути передачи – воздушно-капельный, контактно-бытовой. Возбудитель проникает через слизистые оболочки ротоглотки, реже – глаз, половых органов, кожу, раневую поверхность. В месте входных ворот возбудитель прикрепляется к соответствующим рецепторам эпителиальных клеток, вызывая воспалительный процесс. Затем происходит кологизация и выделение экзотоксина. Токсин блокирует ферменты синтеза белка в клетках хозяина, что приводит к их гибели. Это обуславливает некроз и летальный исход. Фибринозная пленка – характерный признак дифтерии. Фибринозное воспаление может быть крупозным или дифтерическим. Дифтерическое воспаление возникает на слизистых оболочках (ротоглотка, надгортанник, голосовые связки). Фибринозная пленка плотно связана с подлежащей тканью и не снимается тампоном при осмотре. При попытке сделать это слизистая оболочка кровоточит. Крупозное воспаление возникает при локализации патологического процесса в дыхательных путях (гортань, трахеяь и бронхи). Здесь фибринозная пленка располагается поверхностно и легко отделяется от подлежащих тканей. Крупозное воспаление ведет к развитию асфиксии. После перенесенного заболевания формируется нестойкий и непродолжительный антибактериальный антибактериальный иммунитет и стойкий антитоксический. Лабораторная диагностика. 1) Основной метод – бактериологический. Материалом для исследования является слизь и пленка из очагов поражения. Бактериологическому обследованию в обязательном порядке подлежат все больные с ангинами и подозрением на дифтерию. Сбор материала необходимо проводить в течение 3-4 часов с момента обращения больного. Для взятия материала используют сухие стерильные ватные тампоны. Различают три вида показаний к проведению бактериологических исследований на дифтерию: диагностическое обследование, по эпидемиологическим показаниям (контактные), с профилактической целью; 2) серологический метод (РПГА) – исследуется сыворотка крови больного на выявление антител. С диагностической целью сыворотка исследуется в динамике для определения нарастания титра антител. С целью изучения напряженности иммунитета к дифтерии, сыворотка исследуется однократно. Защитный титр антител – 1:40. Лечение: 1) специфическая противодифтерийная лошадиная очищенная концентрированная жидкая сыворотка, вводится по Безредке дробно (анафилактический шок); 2) иммуноглобулин человека противодифтерийный для в/в введения; 3) антибиотики – пенициллин, эритромицин, бета-лактамы, макролиды. Специфическая профилактика. Активная – используются вакцины АКДС, АДС-анатоксин, АДС-М-анатоксин, АД-М-анатоксин, тетракок (коклюш, дифтерия, столбняк, полиомиелит). Иммунизацию проводят, начиная с 3-месячного возраста, троекратно, с интервалами в 4-6 недель. Пассивная – проводится в очагах заболевания антитоксической сывороткой. Возбудителями коклюша и паракоклюша являются B. Pertussis и B parapertussis соответственно. Это мелкие кокковидные грамотрицательные палочки с закругленными концами биполярно окрашенные. Неподвижны. Образуют микрокапсулу, облигатные аэробы. Для выделения бордетелл используют сложные питательные среды с добавлением сорбентов или веществ с высокой сорбционной способностью (активированный уголь, кровь, альбумин): среда КУА- казеиново-угольный агар, среда Борде-Жангу – картофельно-глицериновый агар. Через 24-48 часов на средах бордетеллы образуют мелкие сероватые блестящие колонии, напоминающие капли ртути или жемчужины. Биохимическая активность низкая. Бордетеллы расщепляют глюкозу и лактозу до кислоты без газа. Факторы патогенности: 1) адгезия, 2) токсины: пертуссис-токсин, внеклеточная аденилатциклаза, трахеальный цитотоксин, дерматонекротический токсин, термостабильный эндотоксин. Эпидемиология. Источником инфекции является больной человек. Возбудитель проникает в организм через дыхательные пути при разговоре, кашле, чихании. Путь передачи инфекции воздушно-капельный. Контагиозность коклюша очень высока, т.е. после контакта с коклюшным больным вероятность развития заболевания у неиммунизированного человека составляет 75-90%. Иммунитет после перенесенного заболевания прочный, но видоспецифический. Микробиологичесая диагностика. Материалом для исследования являются:
3) сыворотка крови. Лабораторная диагностика: основной серологический метод - постановка реакции аггютинации в пробирках с антигенным коклюшным и паракоклюшным диагностикумом на обнаружение в сыворотке крови больного антител. Антитела появляются на 10-14 день заболевания. Бактериологический метод- посев исследуемого материала на питательные среды с выделением возбудителя. Лечение. Бордетеллы чувствительны ко многим антимикробным препаратам (кроме пенициллина). Однако антимикробную терапию (эритромицин, ампициллин) назначают лишь в тяжелых случаях. В качестве поддерживающей терапии назначают кислородные ингаляции и антигистаминные или седативные препараты. Профилактика. В течение 1 года жизни каждому ребенку необходима трехкратная вакцинация убитой коклюшной вакциной в составе АКДС. Иммунизацию проводят, начиная с 3-месячного возраста, троекратно, с интервалами в 4-6 недель. В настоящее время разработаны и применяются бесклеточные (ацеллюлярные, субкорпускулярные вакцины), содержащие очищенные антигены возбудителя коклюша. Для экстренной профилактики коклюша у контактировавших неиммунизированных лиц назначают нормальный человеческий иммуноглобулин или эритромицин в первые 5 дней после контакта с заболевшим. Менингококки относится к семейству Neisseriaceae, роду Neisseria, виду Neisseria meningitidis. Экологической нишей является слизистая оболочка носоглотки человека. Neisseria meningitidis является возбудителем менингококковой инфекции. Это диплококки бобовидной формы. Спор не образуют, неподвижны, в организме образуют капсулу, грамотрицательные, строгие аэробы. Менингококки требовательны к питательным средам – растут только на средах, содержащих человеческий белок (сывороточный агар) при температуре 37 0 С. На сывороточном агаре образуют нежные прозрачные колонии средней величины. Биохимически малоактивны, ферментируют только глюкозу и мальтозу, образуя кислоту, но не образуя газ. Антигенная структура: Менингококк имеет 7 антигенных типов, которые обозначаются буквами латинского алфавита: А, В, С, D, X, Y, Z. Тип А вызывает заболевания при эпидемических вспышках; тип В — вызывает заболевания в межэпидемический период; тип С — вызывает заболевания среди военных контингентов. Остальные типы вызывают спорадические заболевания. Факторы патогенности: 1) капсула; 2) эндотоксин; 3) адгезия; 4) ферменты (гиалуронидаза, нейраминидаза). Менингококковая инфекция – антропонозная инфекция, источником является больной или бактерионоситель. Различают три группы источников инфекции: больные генерализованной формой, больные назофарингитом, здоровое носительство. Основной путь передачи – воздушно-капельный. Сезонный характер – осенне-зимний. Болеют в основном дети до 15 лет. Менингококковая инфекция клинически протекает в локализованной форме: менингококконосительство, острый назофарингит и генерализованной форме: менингококкцемия, менингит, менингоэнцефалит, эндокардит, артрит, полиартрит, пневмония. Постинфекционный иммунитет стойкий, повторные случаи почти не наблюдаются. Иммунитет носит гуморальный и группоспецифический характер. Лабораторная диагностика. Поскольку менингококки очень неустойчивы вне организма человека, клинический материал транспортируют в утепленных контейнерах (30-35 0 С). Материалом для исследования являются: носоглоточная слизь от больных и носителей; 2) ликвор; 3) кровь; 4) соскоб из элементов геморрагичнской сыпи на коже; 5) труп- гной с мозговой оболочки. Методы лабораторной диагностики: 1) бактериоскопический (ликвор); 2) бактериологический; 3) экспресс-диагностика – реакция латекс-агглютинации, реакция иммунофлюоресценции; 4) серодиагностика (РПГА). Лечение. Этиотропная терапия: сульфаниламиды, пенициллины, хлорамфеникол. Специфическая профилактика: 1) химическая менингококковая вакцина, содержащая полисахаридные антигены серогрупп А и С (активный антимикробный иммунитет); 2) человеческий иммуноглобулин (пассивный антимикробный иммунитет). Возбудитель туберкулеза относится к семейству Mycobacteriaceae, роду Mycobacterium, виду M. Tuberculosis. Это тонкие, слегка изогнутые палочки, спор и капсул не образуют. Туберкулезная палочка тяжело воспринимает обычные красители из-за большого содержания липидов в клеточной стенке, содержащих миколовую кислоту. По Грамму - грамположительная и окрашивается 24-30ч. Для выявления микобактерий применяют окраску кислото-спирто и щелочеустойчивых бактерий по Цилю-Нильсену. M. Tuberculosis – аэроб, медленно растет (до 30 дней), требователен к питательным средам. Факторы роста – глицерин, аминокислоты. Стимулятор роста – лицетин. Основная питательная среда – яичная среда Левенштейна-Йенсена. На плотных питательных средах образуются морщинистые, сухие, с неровными краями колонии, не сливаются друг с другом. В жидких средах растут в виде пленки. Пленка сначала нежная, сухая, со временем утолщается, становится бугристо-морщинистой с желтоватым оттенком. Среда при этом непрозрачная. Биохимические свойства: туберкулезная палочка образует никотиновую кислоту (ниацин), которая накапливается в жидкой питательной среде и дает с раствором цианида калия и хлорамином Б ярко-желтое окрашивание (ниациновая проба Конно). Факторы патогенности: 1) миколовые кислоты, 2) корд-фактор; 3) сульфатиды; 4) микозиды; 5) липоарабиноманан. Возбудитель туберкулеза проникает в организм в составе мелкодисперсных аэрозолей. Возбудитель должен попасть в альвеолы, где они поглащаются резидентными макрофагами, взаимоотношение с которыми и определяет дальнейшее развитие инфекции. Туберкулез относится к классическим внутримакрофагальным инфекциям. Внутри макрофагов туберкулезные бактерии оказываются устойчивыми к бактерицидным факторам фагоцитов благодаря мощной липидной оболочке. В результате взаимодействия микобактерий и макрофагов под влиянием факторов вирулентности развивается воспаление гранулематозного типа. Гранулема развивается сразу после инфицирования, но в дальнейшем она получает мощный импульс к развитию, когда в организме появляются Т-лимфоциты, сенсибилизированные к возбудителю. Доиммунная гранулема через 2-3 недели под влиянием Т-лимфоцитов превращается в специфическую (постиммунную), которая называется туберкуломой. Из легких туберкулезная палочка попадает в регионарные лимфатические узлы, далее – в кровоток. Дальнейшие события связаны со специфическим воспалением, в основе которого лежит аллергическая реакция на бактериальные антигены. Источником инфекции является больной человек, который в острый период выделяет с мокротой туберкулезные палочки. Путь заражения – воздушно-капельный. Наиболее часто встречается туберкулез легких, но могут поражаться и кишечник, и опорно-двигательный аппарат, и мочеполовая система. Выделяют два патогенетических варианта туберкулеза:
Наиболее часто он самоизлечивается, подвергается фиброзу и кальцификации (очаг Гона). В этом очаге бактерии персистируют, но во внешнюю среду не выделяются. В других случаях развивается острый туберкулез.
Особенности иммунитета при туберкулезе: 1) нестерильный, поддерживается теми бактериями, которые персистируют в организме; 2) неустойчивый, т.е. не предохраняет от реактивации эндогенной инфекции и реинфекции извне; 3) антитела образуются, но они не имеют защитного значения; 4) основной механизм иммунитета – клеточный; основное значение имеет инфекционная аллергия. Лабораторная диагностика. Материалом для исследования являются: мокрота, промывные воды бронхов, желудка, плевральная и цереброспинальная жидкости, моча, кусочки тканей и органов, взятые во время операции или биопсии. Методы диагностики: 1) микроскопический – из мокроты делают два мазка. Один окрашивают по Цилю-Нильсену, другой исследуют с помощью флюоресцентной микроскопии; 2) бактериологический; 3) ускоренный метод Прайса- позволяет увидеть наличие корд-фактора-бактерии складываются в косы, цепочки, жгуты; 4) ПЦР; 5) серодиагностика – ИФА; 6) туберкулинодиагностика – кожная проба Манту, учитывают через 48-72 часа, свидетельствует об инфицированности, а не о заболевании; 7) микрокультивирование на стеклах в среде Школьникова. Лечение. Большинство антибиотиков на микобактерии туберкулеза не действуют, поэтому применяют туберкулостатические препараты: 1) препараты первого ряда – изониазид, пиразинамид, стрептомицин, рифампицин, этамбутол, фтивазид; препараты второго ряда – амикацин, каномицин, аминосалицилат натрия (ПАСК), дапсон, циклосерин и др. Особенности терапии при туберкулезе: 1) лечение должно быть начато как можно раньше, сразу после выявления заболевания; 2) терапия всегда комбинированная – используется не менее двух препаратов; 3) проводится длительно (4-6 месяцев), что связано с большой продолжительностью жизненного цикла микобактерий; 4) должна быть непрерывной, т.к. перерывы ведут к формированию устойчивости возбудителя и хронизации процесса. Специфическая профилактика. Живая вакцина БЦЖ – вакцинация осуществляется в роддоме на 4-7-й дни жизни внутрикожным методом. Ревакцинацию проводят лицам с отрицательной туберкулиновой пробой с интервалом в 5-7 лет до 30-летнего возраста. Таким образом создают инфекционный иммунитет, при котором возникает реакция гиперчувствительности замедленного типа. Legionella pneumophila является возбудителем болезни легионеров (питтсбургской пневмонии, лихорадки Понтиак), относится к семейству Legionellaceae, роду Legionella и вызывает поражения респираторного тракта, развитие тяжелых пневмоний. Legionella pneumophila – это грамотрицательные палочки, подвижны, спор не образуют, аэробы, факультативные внутриклеточные паразиты. Легионеллы распространены в естественных и искусственных водоемах, часто паразитируют на амебах. Требовательны к питательным средам. В состав среды входят пирофосфат железа и активированный уголь. Через 72 часа вырастают колонии темно-синего цвета, в стереоскопическом микроскопе – колонии изумрудного цвета. Факторы патогенности: эндотоксин, гемолитическая активность. Источником инфекции являются системы водоснабжения и кондиционирования воздуха. Поступление возбудителя в организм происходит при вдыхании водных аэрозолей, образующихся в душевых, в кондиционерах, в ваннах. Входные ворота инфекции – дыхательные пути. Лабораторная диагностика. Материалом для исследования являются: бронхосмыв, мокрота, кровь, секционный материал. Методы диагностики: 1) бактериологический; 2) серологический (РНГА, ИФА) на выявление антител и антигенов; 3) ПЦР-диагностика. Профилактика. Периодическая очистка кондиционеров, душевых установок. Выявление водного резервуара возбудителя и его оздоровление. Читайте также:
|



