Миозит специфические антитела блот анализ что это
Комплексный анализ крови на аутоантитела, являющиеся клинико-диагностическими маркерами полимиозита, используемый для дифференциальной диагностики идиопатических воспалительных миопатий.
Серологическая диагностика полимиозита; аутоантитела при полимиозите.
Myositis-specific (MSA) and myositis-associated antibodies (MAA); Serology, PM.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Полимиозит – системное воспалительное заболевание с преимущественным поражением мышечной ткани. Оно относится к группе идиопатических воспалительных миопатий, в которую также входят дерматомиозит, ювенильный дерматомиозит, миозит с включениями и другие. Часто на основании общности клинических и лабораторных признаков полимиозит и дерматомиозит объединяют вместе и рассматривают как одну нозологию – полимиозит/дерматомиозит, или просто – миозит. Хотя этиология воспалительных миопатий не до конца ясна, считается, что определенную роль играют иммунные нарушения. В 50-80 % случаев в крови пациентов с идиопатическими воспалительными миопатиями могут быть обнаружены аутоантитела. При разных миопатиях могут быть выявлены разные антитела, что используют при дифференциальной диагностике заболеваний этой группы. Антитела, обнаруживаемые при миозите, могут быть разделены на две группы.
1. Антитела, специфические для миозита: антисинтетазные антитела (АСА), антитела к антигену Mi-2 (анти-Mi-2) и другие.
АСА – группа аутоантител, направленных против аминоацил-тРНК синтетаз – ферментов, катализирующих связывание аминокислот с соответствующими им транспортными РНК. На сегодняшний день выявлено семь наиболее часто встречаемых при миозите АСА, в том числе анти-Jo-1 (аминокилота: гистидин), анти-PL-7 (треонин) и анти-PL-12 (аланин). Анти-Jo-1 обнаруживаются в 25-35 % случаев миозита, другие АСА – в 1-5 %. Как правило, у одного и того же пациента имеется только один из вариантов АСА.
Анти-Mi-2. Антиген Mi-2 включает два протеина Mi-2a (240 кДа) и Mi-2ß (218 кДа), обладающих структурой, подобной ДНК геликазе, и, вероятно, выполняет схожую с этим ферментом функцию. Анти-Mi-2 обнаруживаются у 8 % пациентов с воспалительными миопатиями, чаще при дерматомиозите, чем при полимиозите.
2. Антитела, ассоциированные с миозитом. В эту группу входят аутоантитела, которые наблюдаются при так называемых overlap-синдромах (состояниях, объединяющих клинические признаки двух и более синдромов), чаще всего при сочетании миозита и системной склеродермии. Антитела к антигену Ku были впервые обнаружены у пациента из Японии с полимиозитом/системной склеродермией и некоторое время считались маркером этого overlap-синдрома. Впоследствии стало ясно, что они также могут быть обнаружены при системной красной волчанке (СКВ), артралгии и феномене Рейно.
Антитела к антигену Pm-Scl также ассоциированы с синдромом полимиозит / системная склеродермия, хотя могут быть выявлены и при других системных заболеваниях соединительной ткани. Примерно у 50 % пациентов с overlap-синдромом полимиозит / системная склеродермия обнаруживаются анти-Pm-Scl (по сравнению с 2 % при изолированной системной склеродермии). Более чем у 80 % пациентов с анти-Pm-Scl наблюдается overlap-синдром полимиозит / системная склеродермия.
Исследование антител при миозите проводят в комплексе с другими анализами, в первую очередь – гистологическим исследованием мышечной ткани. Результат анализа оценивают вместе со всеми значимыми клиническими, лабораторными и инструментальными данными.
Для чего используется исследование?
- Для диагностики полимиозита;
- для дифференциальной диагностики идиопатических воспалительных миопатий.
Когда назначается исследование?
- При наличии симптомов полимиозита: мышечной слабости с преимущественным поражением проксимальных групп мышц (мышцы плечевого и/или тазового пояса) и повышения уровня креатинкиназы.
Что означают результаты?
Компонент
Референсные
значения

ИММУНОБЛОТ миозит-специфических антител
Референсные значения: антител не обнаружено.
Стоимость исследования можно посмотреть в прайс-листе.
Данный полуколичественный метод определения специфических аутоантител в образцах сывороток пациентов позволяет различать отрицательный, пограничный, слабо положительный, положительный и строго положительный результаты. Образцы с пограничными результатами должны быть протестированы еще раз этим или альтернативным методом.
НАЗНАЧЕНИЕ
Myositis plus - набор, основанный на методе иммуноблота на мембране, для полуколичественного определения:
- митохондриальных антител M2 подтипа (AMA-M2),
- IgG аутоантител к ядерному и цитоплазматическому антигену Jo-1 (гистидил-тРНК синтаза),
- PM-ScI-100,
- PL 7 (треонил-тРНК синтаза),
- PL 12 (аланил-тРНК синтаза),
- Mi-2,
- Ku (p70/80)
- SRP (частица распознавания сигнала)
- IgG аутоантител к Rib-P (рибосомальным фосфопротеинам).
В методе Myositis plus использованы типичные и наиболее распространенные антигены для выявления MSA и MAA. Благодаря сочетанию выбранных антигенов данный тест, основанный на иммуноблоте, позволяет быстро и просто выполнять диагностику и дифференциальную диагностику идиопатического воспалительного миозита и сзаболеваний со схожими или аналогичными симптомами. Сочетание используемых антигенов в тесте Myositis plus также позволяет дифференцировать аутоантитела к рибосомам и митохондриям, которые демонстрируют цитоплазматический характер окрашивания методом иммунофлуоресценции.
Антимитохондриальные антитела (AMA) это гетерогенная группа аутоантител, направленных к различным белкам внутренней и внешней сторон митохондриальной мембраны. AMA подтипа M2 направлены к эпитопам комплекса пируватдегидрогеназы. Высокая чувствительность и специфичность аутоантител M2 делает их прекрасным инструментом для выявления первичного билиарного цирроза (PBC).
Антитела к антигену Jo-1, гистидил-тРНК синтазе, являются наиболее частыми миозит-специфическими аутоантителами (MSA). У примерно 90% пациентов, у которых были выявлены анти-Jo-1, в ходе заболевания развивается миозит. Jo-1 – это цитоплазматический фермент, катализирующий связывание гистидина со специфической тРНК в процессе биосинтеза белка.
Как миозит-ассоциированные антитела, аутоантитела к PM-Scl-100 являются важным индикатором при синдроме перекрывания миозит/склеродермия. Они могут обнаруживаться у примерно ¼ пациентов с перекрыванием миозит/склеродермия, но в случаях склеродермии или миозита отдельно они выявляются редко, в 2 и 6 %, соответственно. Анти-PM-Scl-100 направлены к эпитопам экзосом мультиферментного комплекса, состоящего из нескольких РНК-связывающих белков и ферментов с экзорибонуклеазной функцией и играющего важную роль в процессинге РНК.
Аутоантитела PL-7 направлены против треонил-тРНК синтазы цитоплазмы. Анти-PL-7 это миозит-специфические антитела, но они очень редки, встречаются менее чем в 3% случаев.
Анти-Pl-12 это еще одни миозит-специфические антитела к аланил-тРНК синтазе цитоплазмы. Они встречаются менее чем в 3% случаев.
Миозит-специфические антитела к белку Mi-2 являются диагностическим маркером идиопатического миозита. Среди больных с положительными результатами анти-Mi-2 примерно 95% страдают дерматомиозитом и 3% - полимоизитом. Антиген-мишень этих антител это центральный компонент мультибелкового комплекса (NuRD), катализирующего модификацию хроматиновой структуры и, таким образом, действующего как активатор или репрессор транскрипции.
Антиген-мишень этих миозит-ассоциированных антител это Ku-антиген, АТФ-зависимая ДНК хеликаза. Антитела к Ku выявляются у примерно 7% больных с миозитами.
Они также определяются при других аутоиммунных заболеваниях, такие как SLE или синдром Шегрена.
Миозит-специфические анти-SRP антитела могут выявляться в случаях тяжелого миозита. Их встречаемость при миозитах составляет около 4%; у около ¼ SRP-положительных пациентов обнаруживают клинические признаки дерматомиозита. Антиген-мишень этих антител это частица распознавания сигнала (SRP), цитоплазматический рибонуклеопротеиновый комплекс, ответственный за транслокацию вновь синтезированных протеинов из рибосом в эндоплазматический ретикулум.
Rib-P антитела являются диагностическим маркером системной красной волчанки (SLE). Они выявляются у 10 - 20% больных SLE, в первую очередь в активной фазе заболевания; их редко обнаруживают у пациентов с другими аутоиммунным заболеваниями. У пациентов, страдающих склеродермией, присутствие Rib-P антител может указывать на перекрывание склеродермия/SLE. Антиген-мишень этих аутоантител это специфические регионы фосфопротеинов P0 (38 кДа), P1 (19 кДа) и P2 (17 кДа) субъединицы 60S рибосомального комплекса.
Стоимость исследования можно посмотреть в прайс-листе.
Двухстороннее симметричное поражение чаще мелких суставов кистей и лучезапястных, реже — локтевых и коленных.
Напоминает поражение при ревматоидном артрите. Обычно имеет преходящий характер, быстро купируется при назначении глюкокортикоидов, иногда предшествует развитию мышечной слабости.
Описано развитие хронического дегрормирующего артрита с подвывихами суставов кистей, но без эрозивных изменений по
рентгенологическим данным
Развивается на поздних стадиях ПМ/ДМ, чаще при ювенильном ДМ.
Кальцификаты локализованы:
■ подкожно или в соединительной ткани, вокруг мышечных волокон
■ в зонах микротравматизации над локтевыми и коленными суставами
■ на сгибательных поверхностях пальцев и ягодицах
Наблюдается редко. Возможно развитие протеинурии и нефротического синдрома. Выраженная миоглобинурия может приводить к ОПН.
Диагноз и рекомендуемые клинические исследования
Увеличение концентрации креатинфосфокиназы (КФК), MB фракции КФК, альдолазы, глютаминщавелевоуксусной (ГЩТ) и глютиминпировиноградной (ГПТ) трансаминаз, лактатдегидрогеназы (ЛДГ).
Уровень КФК отличается более высокой чувствительностью и специфичностью по сравнению с другими лабораторными по-
Выявление "миозит-специфических" антител — антител к аминоацилсинтетааам транспортной РНК (антисинтетазные антитела): к гистидин (Jo-1), треонил (PL-7), глицин (EJ), лиэин, изолейцин (OJ), аланин (PL-12) тРНК-си нтетазам и некоторые другие.
Антитела Jo-1 выявляются у половины больных ПМ/ДМ, другие антисинтетазные антитела — в 5% случаев.
Продукция антисинтетазных антител сочетается с развитием "антисинтетазного" синдрома.
Более чем у 90% пациентов ПМ/ДМ при исследовании проксимальных и параспинальных мышц выявляются:
■ признаки патологической спонтанной активности миофибрил (потенциалы фибрилляции, сложные повторяющиеся разряды и др.) при раздражении и в покое
■ короткие низкоамплитудные полифазные потенциалы при сокращении
ЭМГ — чувствительный, но не специфичный, метод диагностики. Полезен для мониторинга эффективности лечения, особенно при сомнительных результатах лабораторных и клинических исследований. Нормальная электрическая активность при ЭМГ в большинстве случаев позволяет исключить диагноз ПМ/ДМ. Однако данные ЭМГ плохо коррелируют с клиническими проявлениями мышечной слабости.
При ПМ:
■ инфильтрация мононуклеарными клетками (в основном, имфоцитами), локализующимися в эндрмизии
■ некроз и фагоцитоз мышечных фибрилл
■ регенерация мышечных волокон При ДМ:
■ мононуклеарная инфильтрация локализуется в основном вокруг фасций и кровеносных сосудов
■ выявляются признаки васкулопатии, проявляющиеся поражением эндотели альных клеток (некроз, капиллярный тромбоз), с отеком, гиперплазией, вакуолизацией и дегенерацией
При ПМ и ДМ:
■ на поздних стадиях заболевания обнаруживается атрофия мышечных фибрил, фиброз, замещение жировой тканью
Мышечную биопсию используют для подтверждения диагноза ИВМ даже при наличии характерных клинических, лабораторных и инструментальных признаков заболевания. Наиболее информативна биопсия мышцы, вовлеченной в патологический процесс, но без выраженной атрофии.
Часто выявляются признаки базального пневмосклероза и интерстициального легочного фиброза.
Более чувствительным методом является рентгеновская компьютерная томография с высоким разрешением.
Выявление прогностически неблагоприятных нарушений ритма и проводимости.
Для диагностики ПМ/ДМ следует использовать следующие диагностические критерии
1. Поражение кожи:
■ гелиотропная сыпь (пурпурно-красные эритематозные высыпания на веках)
■ признак Готрона (пурпурно-красная шелушащаяся, атрофическая эритема или пятна на разгибательной поверхности кистей над суставами)
■ эритема на разгибательной поверхности конечностей над локтевыми и коленными суставами
2. Проксимальная мышечная слабость (верхние и нижние конечности и туловище)
3. Повышение уровня КФК и/или альдолазы в сыворотке
4. Боли в мышцах при пальпации или миалгии
5. Миогенные изменения при ЭМГ (короткие полифазные потенциалы моторных единиц со спонтанными потенциалами фибриляции)
6. Обнаружение антител Jo-1 (антитела гистидил тРНК-синтетазе)
7. Недеструктивный артрит или артралгии
8. Признаки системного воспаления (лихорадка более 37°С, увеличение концентрации С-реактивного белка или увеличение СОЭ более 20 мм/час)
Морфологические изменения, соответствующие воспалительному миозиту (воспалительные инфильтраты в скелетных мышцах с дегенерацией или некрозом мышечных фибрилл, активный фагоцитоз или признаки активной регенерации)
Диагноз ДМ (чувствительность 94,1%, специфичность 90,3%) устанавливают при наличии, по крайней мере, одного типа понесения кожи и не менее четырех других признаков (пункты 2—9). Диагноз ПМ (чувствительность 98,9%, специфичность 95,2%) устанавливают при наличии не менее четырех признаков (пункты 2—9).
Частота миозита с "включениями" в общей популяции больных ИВМ колеблется от 15% до 28%. Он развивается у пациентов пожилого возраста (примерно в 61 год), чаще у мужчин, чем у женщин (соотношение 2:1).
Клинические особенности заболевания:
■ очень медленное развитие слабости и атрофии не только в проксимальных, но и в дистальных группах мышц;
■ асимметричность поражения;
■ нормальное КФК или умеренное его увеличение;
■ редкое сочетание с СЗСТ и злокачественными новообразованиями;
■ отсутствие миозит-специфических и других аутоантител;
■ резистентность к глюкокортикоидам
Морфологические особенности:
■ амилоидогенные "очерченные" вакуоли (при световой микроскопии);
■ крупные внутриядерные и внутрицитоплазматические включения (при световой микроскопии);
■ микротубулярные элементы (при электронной микроскопии). Определенное диагностическое значение имеет ЭМГ, при которой обнаруживаются смешанные миопатические и нейропатические изменения.
Частым клиническим проявлением системных заболеваний соединительной ткани (СЗСТ) является проксимальная мышечная слабость, а признаки СЗСТ присутствуют примерно у 20% пациентов ИВМ. Симптомы миопатии могут превалировать в клинической картине ССД, СКВ, РА, синдрома Шегрена, системных васкулитов.
Для перекрестных синдромов характерны:
■ высокая частота феномена Рейно и полиартрита;
■ очень высокие титры АНФ (при отсутствии "миозит-специфических" аутоантител);
■ хороший ответ на ГК;
■ увеличение КФК (в той же степени, что и при идиопатическом ПМ/ДМ);
■ такие же гистологические изменения в мышцах, как и при идиопатических формах заболевания.
При ПМ/ССД в сыворотках выявляются антитела PM/Scl.
Миозит, ассоциирующийся с опухолями, составляет примерно 20% от всех случаев ИВМ. На фоне злокачественных новообразований преимущественно возникает ДМ, а не ПМ. Частота заболевания одинакова у мужчин и женщин (1:1).
Опухоли могут развиваться до появления признаков ИВМ одновременно с ними или после их появления. Частота злокачественных новообразований при ПМ/ДМ в 12 раз выше чем в популяции.
Риск злокачественных новообразований выше при наличии:
■ васкулита
■ некроза кожи
■ амиотрофического дерматомиозита
Риск злокачественных новообразований ниже при наличии:
■ легочного фиброза
■ "миозит-специфических" аутоантител
■ других системных проявлениях СЗСТ.
Локализация и тип опухолей, сочетающихся с миозитом, совпадает с их распределением по частоте в соответствующей возрастной группе. Наиболее вероятными новообразованиями являются рак яичника и носоглоточный рак.
При подозрении на развитие опухолевого миозита рекомендуется проводить дополнительные обследования:
■ определение простат-специфического антигена;
■ СА-125;
■ сканирование легких.
Что такое аутоиммунный миозит?
Аутоиммунный миозит — это группа аутоиммунных ревматических заболеваний, которые вызывают воспаление и слабость мышц (полимиозит) или кожи и мышц (дерматомиозит).
Эти заболевания приводят к воспалению мышц (миозит), мышечной слабости, обусловливающей потерю трудоспособности, и иногда болезненности. Слабость обычно наблюдается в плечах и бедрах, но также может поражать симметричные мышцы тела.
Причины аутоиммунного миозита
Аутоиммунный миозит обычно развивается у взрослых в возрасте от 40 до 60 лет, либо у детей в возрасте от 5 до 15 лет.
Вероятность его развития у женщин в два раза выше, чем у мужчин. У взрослых заболевание может возникать независимо либо в комплексе болезней соединительной ткани, например, при смешанном заболевании соединительной ткани, системной красной волчанке или системном склерозе.
Причина аутоиммунного миозита не установлена. В развитии заболевания могут принимать участие вирусы или аутоиммунные реакции. Онкологические заболевания также могут вызывать это расстройство. Не исключено, что иммунный ответ, направленный против злокачественной опухоли, может также быть направлен на компоненты мышечной ткани. Эта болезнь может быть наследственной.
Различают четыре типа аутоиммунного миозита:
- Полимиозит.
- Дерматомиозит.
- Некротизирующие иммуноопосредованные миопатии.
- Миозит с включениями.
Дерматомиозит обычно вызывает изменения кожи, которых не бывает при полимиозите, что помогает в дифференциальной диагностике обоих заболеваний. Образцы ткани мышц, полученные при биопсии, также выглядят по-разному под микроскопом.
Некротизирующие иммуноопосредованные миопатии — это заболевания, при которых происходит гибель мышечных клеток (миоцитов), но не поражаются другие ткани, кроме мышечной.
Миозит с включениями представляет собой отдельное заболевание, симптомы которого похожи на симптомы хронического полимиозита неизвестной этиологии. Однако это заболевание развивается у пожилых лиц, часто поражает другие мышцы (например, мышцы кистей и стоп), имеет более длительное течение, плохо отвечает на лечение, а мышцы имеют другой вид под микроскопом.
Симптомы и признаки
Симптомы аутоиммунного миозита аналогичны у людей всех возрастов, однако оказалось, что воспаление мышц у детей часто развивается более внезапно, чем у взрослых. Симптомы, которые могут начаться во время инфекции или непосредственно после нее, включают:
- симметричную мышечную слабость (особенно в верхней части рук, бедер и голеней);
- боль в суставах (хотя чаще наблюдается незначительная мышечная боль);
- затруднения при глотании;
- жар;
- утомляемость и снижение массы тела.
Также может возникать феномен Рейно, для которого характерно внезапное побледнение пальцев и ощущение покалывания в них, либо онемение в ответ на воздействие холода или эмоциональное расстройство.
Мышечная слабость может развиваться медленно или внезапно, с постепенным усугублением в течение недель или месяцев. В связи с тем, что поражение в первую очередь затрагивает мышцы вблизи центра тела, возможны серьезные трудности с такими движениями, как поднятие руки выше уровня плеч, движение вверх по ступенькам и подъем с кресла или сиденья унитаза. При поражении мышц шеи может стать невозможным даже подъем головы с подушки. Лицам со слабостью плечевых или бедренных мышц может потребоваться использование инвалидного кресла или постоянный постельный режим. Повреждение мышц верхней части пищевода может приводить к трудностям с глотанием и регургитации пищи. При этом поражения мышц кистей, стоп и лица обычно не происходит.
Боль и воспаление в суставах присутствует приблизительно у 30 % больных. Боль и отек преимущественно незначительны.
Внутренние органы обычно не затрагиваются, кроме горла и пищевода. Однако не исключено поражение легких и сердца, приводящее к нарушениям сердечного ритма (аритмии), одышке и кашлю. Симптомы повреждения желудочно-кишечного тракта, которые могут наблюдаться у детей, но обычно отсутствуют у взрослых, вызваны воспалением кровеносных сосудов (васкулитом). Такие симптомы могут включать кровавую рвоту, черный, дегтеобразный стул и сильную боль в животе, в ряде случаев с образованием отверстия (перфорации) во внутренней оболочке кишечника.
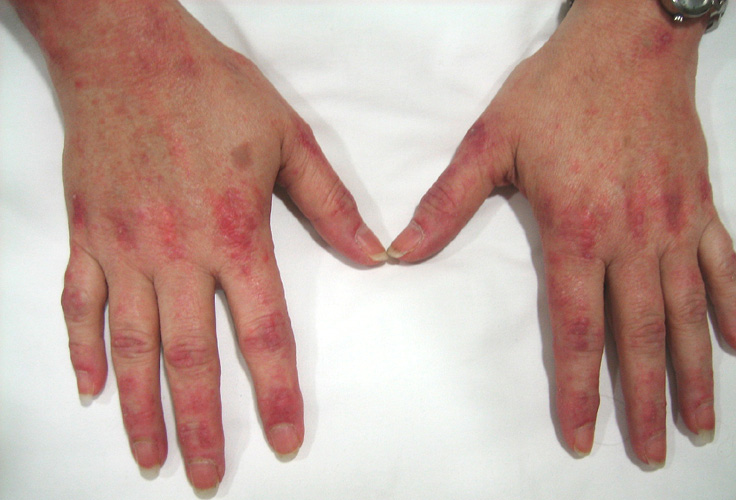
Когда сыпь сходит, на коже может возникать буроватая пигментация, рубцевание, сморщивание или депигментированные бледные пятна. Сыпь на коже волосистой части головы может напоминать псориаз и сильно зудеть. Также наблюдается чувствительность к солнечному свету и язвы на коже. Под кожей или в мышечной ткани, особенно у детей, могут возникать бугорки вследствие отложения кальция. Приподнятые красноватые бугорки могут появляться в области пястно-фаланговых суставов (так называемые папулы Готтрона), а иногда и в области межфаланговых суставов.
Иногда эти характерные кожные изменения наблюдаются при отсутствии мышечной слабости и воспаления. В этом случае заболевание называется амиопатическим дерматомиозитом.
Диагностика
Для диагностики аутоиммунного миозита используются следующие критерии:
- мышечная слабость в плечах или бедрах и голенях;
- иногда характерная сыпь;
- повышенные уровни в крови определенных ферментов мышечной ткани (особенно креатинкиназы), что указывает на повреждение мышц;
- патологические изменения электрической активности мышц по результатам электромиографии или изменения во внешнем виде мышц на снимках, полученных с помощью магнитно-резонансной томографии (МРТ);
- характерные изменения в мышечной ткани, обнаруженные при биопсии и наблюдаемые под микроскопом (наиболее достоверное подтверждение).
Биопсия мышц назначается часто и является самым надежным способом диагностики аутоиммунного миозита, особенно в сомнительных случаях. Другие лабораторные обследования не могут однозначно идентифицировать аутоиммунный миозит, но могут помочь исключить другие нарушения, обнаружить риск осложнений и определить степень тяжести заболевания.
Анализы крови проводятся для измерения уровней антинуклеарных антител (АНА) и других антител, которые присутствуют у большинства лиц с аутоиммунным миозитом. Хотя результаты анализов крови могут помочь диагностировать аутоиммунный миозит, сами по себе они не могут служить подтверждением диагноза аутоиммунного миозита, поскольку обнаруженные с их помощью аномалии иногда присутствуют у здоровых людей или у лиц с другими заболеваниями. Диагноз аутоиммунного миозита устанавливается на основании всей собранной врачом информации, включая симптомы, результаты физикального обследования и результаты всех обследований.
МРТ также может помочь выбрать участок для биопсии. Чтобы исключить другие заболевания мышц, отбирают образцы мышечной ткани для выполнения специфических исследований.
Врачи часто назначают скрининг на онкологические заболевания среди людей в возрасте 40 лет и старше, страдающих дерматомиозитом, или среди людей в возрасте 60 лет и старше, страдающих полимиозитом, поскольку у таких больных возможно наличие скрытых злокачественных опухолей.
Лечение аутоиммунного миозита

Часто на состоянии больных благоприятно сказывается умеренное ограничение физической деятельности в периоды наиболее сильных проявлений воспаления мышц.
Как правило, назначается преднизон (кортикостероидный препарат) для приема внутрь в высоких дозах. Этот препарат приводит к медленному повышению силы мышц, снимает боль и отек, обеспечивая контроль заболевания. Лицам с тяжелым заболеванием с затруднениями при глотании или слабостью дыхательных мышц назначают внутривенные кортикостероиды, такие как метилпреднизолон. Многие взрослые больные вынуждены продолжать прием преднизона в низких дозах либо альтернативного лекарственного препарата в течение многих лет или даже неопределенного срока, для профилактики рецидива.
С целью контроля ответа заболевания на лечение кортикостероидами врачи периодически назначают анализ крови для определения уровней мышечных ферментов. Уровни обычно снижаются до нормальных или почти нормальных, а мышечная сила возвращается через 6-12 недель. МРТ также может выявить участки воспаления, что дает врачу возможность определить ответ заболевания на назначенное лечение. Как только уровни ферментов вернутся к норме, дозу преднизона можно постепенно снижать. При повышении уровней мышечных ферментов доза увеличивается.
Хотя при лечении больных с аутоиммунным миозитом кортикостероиды обычно назначаются в первую очередь, эти препараты вызывают побочные эффекты (например, высокий уровень сахара в крови, перепады настроения, катаракта, риск переломов и глаукомы), особенно при назначении в высоких дозах и на длительный срок. Поэтому для уменьшения срока использования кортикостероидов и минимизации побочных эффектов в дополнение к преднизону можно назначать иммунодепрессанты (такие как метотрексат, такролимус, азатиоприн, микофенолата мофетил, ритуксимаб или циклоспорин). В качестве еще одного метода лечения может назначаться иммуноглобулин (вещество, содержащее различные антитела в больших количествах) для введения в вену (внутривенно). Некоторые больные получают комбинацию кортикостероидов, иммунодепрессантов и иммуноглобулина.
Если мышечная слабость обусловлена злокачественной опухолью, ответ на лечение преднизоном, как правило, незначителен. Однако тяжесть такого состояния обычно облегчается, если есть возможность эффективного лечения злокачественной опухоли.
У больных, получающих кортикостероиды, возрастает опасность переломов вследствие остеопороза. Для предотвращения остеопороза таким больным назначают препараты, используемые для лечения остеопороза, например, бисфосфонаты, пищевые добавки витамина D и кальция. Больным, получающим иммунодепрессанты, также назначают препараты для профилактики инфекций, вызванных такими грибами, как Pneumocystis jirovecii.
Больные аутоиммунным миозитом входят в группу повышенного риска развития атеросклероза и находятся под тщательным наблюдением врача.
Прогноз
До 50% больных (особенно детей), получивших лечение в течение 5 лет после установления диагноза, часто достигают длительного периода бессимптомного течения (ремиссия), а некоторые могут даже полностью выздороветь. Однако в любое время возможен возврат (рецидив) заболевания. После постановки диагноза продолжительность жизни приблизительно 75 % пациентов составляет минимум 5 лет. Этот показатель еще выше среди больных детского возраста.
У взрослых больных повышается риск смерти вследствие тяжелой и прогрессирующей мышечной слабости, затруднений при глотании, недостаточного питания, вдыхания пищи с последующим развитием пневмонии (аспирационная пневмония) или дыхательной недостаточности, которая часто развивается одновременно с пневмонией.
У детей, имеющих ювенильную форму дерматомиозита, может развиться тяжелое воспаление кровеносных сосудов (васкулит), кровоснабжающих кишечник, которое при отсутствии лечения в конечном итоге может привести к перфорации кишечника.
Течение полимиозита характеризуется большей тяжестью и резистентностью к лечению среди больных с поражениями сердца и легких. Полимиозит и, особенно, дерматомиозит, связаны с повышением риска развития онкологических заболеваний. У больных злокачественными заболеваниями основной причиной смертности является опухоль, а не аутоиммунный миозит.
- Все
- А
- Б
- В
- Г
- Д
- И
- К
- Л
- М
- Н
- О
- П
- Р
- С
- Т
- Ф
- Х
- Ц
- Э
Причины
Миозит вызывается различными состояниями, которые приводят к воспалению в мышцах. Причины миозита могут быть разделены на несколько главных групп:
Заболевания, вызывающие воспалительные процессы по всему организму, могут оказать влияние на мышцы, вызывая миозит. Многие из этих состояний - аутоиммунные заболевания, при которых антитела оказывают повреждающее действие на собственные ткани организма. К воспалительным заболеваниям вызывающим потенциально тяжелый миозит относятся:
- Дерматомиозит
- Полимиозит
- Оссифицирующий миозит (болезнь Мюнхмейера)
Другие воспалительные заболевания могут вызывать более умеренные формы миозита:
- Системная красная волчанка
- Склеродермия
- Ревматоидный артрит
Воспалительные заболевания наиболее серьезные причины миозита, требующие длительного лечения.
Вирусные инфекции – являются наиболее распространенной инфекцией, вызывающей миозит. Гораздо реже миозит может быть вызван бактериями грибками или другими микроорганизмами. Вирусы или бактерии могут сами непосредственно воздействовать на мышцы или с помощью выделяемых токсинов. Вирусы ОРЗ гриппа также как и вирус иммунодефицита тоже могут быть причиной миозита.
Существует достаточно много медикаментов, которые могут вызвать нестойкие повреждения мышц. Поскольку не удается в таких случаях подтвердить воспалительный процесс, то эти состояния иногда называют миопатией, а не миозитом. Медикаменты, вызывающие миозит и/или миопатию, включают:
- Статины
- Колхицин
- Плаквенил
- Альфа-интерферон
- Кокаин
- Алкоголь
Миопатия может появиться сразу после начала приема медикаментов или же через некоторое время (несколько месяцев) особенно когда речь идет о наркотиках. Как правило, медикаментозный миозит редко бывает тяжелым.
Миозит после травмы. Интенсивные нагрузки особенно при нетренированных мышцах могут привести к болям в мышцах отечности и слабости в течение часов или дней после нагрузки. Воспаление в мышцах связано с микронадрывами в мышечной ткани и, как правило, симптомы такого миозита быстро исчезают после достаточного отдыха. Иногда при сильном повреждении мышц возможен некроз мышечной ткани. Такое состояние называется рабдомиолиз .Он возникает при повреждении большой группы мышц и сопровождается общей реакцией организма на некротическую мышечную ткань. Молекулы миоглобина могут изменить цвет мочи от коричневого до красного.
Симптомы миозита
Главный симптом миозита – слабость мышце. Слабость может быть очевидной или обнаруживаться только при тестировании. Боли в мышцах (миалгии) могут быть или отсутствовать.
Дерматомиозит, полимиозит и другие воспалительные заболевания сопровождающиеся миозитом проявляются мышечной слабостью с тенденцией к постепенному нарастанию в течение недель или месяцев. Мышечная слабость может захватывать многочисленные группы мышц, включая шею, плечи, бедра, мышцы спины. Как правило, бывает двухсторонняя мышечная слабость.
Мышечная слабость при миозите может приводить к падениям, и даже сложности при выполнении простых двигательных функций, таких как вставание, со стула или с кровати Другие симптомы миозита, которые могут присутствовать при воспалительных заболеваниями, включают:
- Высыпание
- Усталость
- Утолщения кожи на руках
- Трудности при глотании
- Нарушение дыхания
У пациентов с миозитом, вызванным вирусом обычно, есть симптомы вирусной инфекции, такие как насморк, ангина фебрилитет, кашель тошнота и диарея. Однако симптомы вирусной инфекции могут исчезнуть за несколько дней или недель до появления симптомов миозита.
У некоторых пациентов с миозитом бывают боли в мышцах, но нередко боли отсутствуют. У половины пациентов с миозитом вследствие воспалительного заболевания не бывает интенсивной боли в мышцах.
Большинство болей в мышцах связано не с миозитом, а перенапряжением мышц или реактивной реакцией при острых респираторных заболеваниях (ОРЗ или грипп). Эти и другие обычные боли в мышцах называют миалгиями.
Диагностика
Врач может заподозрить миозит, на основе таких симптомов как слабость в мышцах болей и других симптомов, характерных для миозита. В диагностике миозита используются:
Анализы крови. Повышенные уровни ферментов тканей мышцы (например, креатинкиназа), могут быть свидетельством повреждения мышечной ткани. Анализы на наличие аутоантител могут идентифицировать аутоиммунное заболевание.
Магнитно-резонансная томография (МРТ). Сканирование с использованием мощного магнита и компьютера позволяет получить изображение мышц. Анализ МРТ помогает идентифицировать зоны повреждения мышц в текущий момент и в динамике.
Электромиография (ЭМГ). С помощью введения игольчатых электродов в мышцы, врач может проверить реакцию мышц на электрические стимуляторы и нервные импульсы. ЭМГ позволяет идентифицировать слабые или поврежденные миозитом мышцы.
Биопсия мышцы. Это - самый точный анализ при диагностике миозита. Доктор определяет слабую мышцу, делает маленький разрез, и удаляет небольшой кусочек ткани мышцы для того, чтобы исследовать ткань под микроскопом. Биопсия мышцы дает достоверный диагноз миозита.
Существует достаточно много причин мышечной слабости и болей в мышцах более распространенных чем миозит. И поэтому диагноз миозит может быть поставлен не сразу, а через некоторое время.
Лечение
Лечение миозита зависит от причины болезни.
Воспалительные (аутоиммунные) заболевания, вызывающие миозит, нередко требуют лечения препаратами, которые подавляют иммунную систему, включая:
- Преднизон
- Имуран
- Метотрексат
Миозит, вызванный инфекцией, как правило, вирусной не требует лечения. Миозит, вызванный бактериями встречается не часто и требуется лечение антибиотиками (вплоть до внутривенного введения для того чтобы избежать опасного состояния для организма такого как сепсис).
Хотя острый некроз скелетных мышц редко бывает при миозите но при наличии рабдомиолиза необходимо госпитализировать пациента так как нужно проводить большие инфузии жидкости для того чтобы предотвратить повреждение почек.
Миозит, связанный с приемом лекарственным средств, лечится прекращением приема этих препаратов. В случаях миозита, вызванного статиновыми препаратами, воспаление мышцы уменьшается в течение нескольких недель после прекращения приема препарата.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Читайте также:


