Москитная лихорадка в крыму
Флеботомная лихорадка (phlebotomus febris; син.: москитная лихорадка, лихорадка паппатачи, летняя лихорадка, трехдневная лихорадка, солдатская болезнь) — вирусная болезнь, передающаяся через укусы москитов рода Phlebotomus, характеризующаяся доброкачественным течением с кратковременной лихорадкой, сильной головной болью, болями в глазных яблоках, икроножных мышцах и пояснице, инъекцией сосудов склеры, гиперемией конъюнктивы и др.
Содержание
История
Географическое распространение
Флеботомная лихорадка распространена в Испании, Португалии, Франции, Италии, Греции, Сирии, Египте, Судане, Израиле, Иране, Ираке, в северо-западных штатах Индии, Южном Китае и др. Ареал Ф. л. совпадает с ареалом москитов рода Phlebotomus, т. е. расположен в зоне приблизительно между 20° и 45° сев. широты. В СССР Ф. л. регистрировалась в Крыму, Закавказье, Молдавии, Узбекистане, Таджикистане, Киргизии; в 40-х гг. 20 в. очаги Ф. л. на территории СССР были ликвидированы.
Этиология
Вирусная этиология Флеботомной лихорадки установлена в начале 20 в., когда Р. Дерр и сотр. (1909) воспроизвели передачу возбудителей путем введения волонтерам фильтратов крови больных Ф. л. Возбудители Ф. л. — арбовирусы сицилийской Ф. л. и неаполитанской Ф. л. были выделены Сейбином (А. В. Sabin) из крови больных, собранной в период эпидемии среди амер. солдат в 1943—1944 гг. в Италии. Вирусы распространены в странах Азии, Европы и Африки в ареале переносчика Phlebotomus papatasii. Москиты являются, видимо, не только переносчиком, но и резервуаром вирусов в природе, поскольку доказана трансовариальная передача возбудителя потомству москитов обоего пола. Оба вируса принадлежат к роду Phlebovirus сем. Bunyaviridae. Они различаются по антигенным свойствам, но сходны по морфологии и биол. свойствам. Форма вирионов сферическая, диам. 90— 110 нм, тип симметрии спиральный; они имеют липопротеиновую оболочку с ворсинками. Вирионы стабильны при pH 7,0—9,0. Быстро инактивируются при t° 56°, при воздействии УФ-лучами, детергентами и про-теолитическими ферментами. Вирусы культивируют на 1—2-дневных новорожденных белых мышах при заражении в ткань мозга. В культурах клеток Hela, ВНК-21, VERO образуют бляшки, цитопатические свойства выражены слабо (см. Вирусологические исследования, Культуры клеток и тканей).
Эпидемиология
Источником инфекции является больной человек в течение последних 1—2 дней инкубации и первых двух дней болезни. Предполагается существование природных очагов Флеботомной лихорадки, хотя источники инфекции среди животных в природе пока неизвестны. Переносчиком и резервуаром вируса являются москиты рода Phlebotomus — Ph. papatasii, Ph. sergenti, Ph. perniciosus, Ph. caucasicus и др. (см. Москиты). Однако Сейбин (1952) утверждал, что экспериментальных доказательств причастности других видов москитов, кроме Ph. papatasii, к передаче вируса Ф. л. не существует.
На человека нападает только самка москита (обычно ночью или рано утром), к-рая после питания кровью больного Ф. л. через б—8 дней становится способной передавать вирус со слюной и сохранять его пожизненно (до 1—3 мес.). Оптимальной температурой окружающей среды для развития вируса в теле москита является 27—31°. При температуре ниже 18° вирус не развивается. Самки москитов способны передавать вирус трансовариально; из зараженных яиц развиваются личинки москитов, также содержащие вирус. Вирус в них сохраняется в холодное время года, а весной из личинок вылетают зараженные самки, способные при первом кровососании передавать возбудителя. Т. о., москиты являются не только переносчиками, но и резервуарами вируса Ф. л.
Заболеваемость Ф. л. носит сезонный характер, совпадая со временем активности москитов, и продолжается с мая по сентябрь—октябрь. В Субтропиках заболеваемость имеет два подъема — первый в конце мая— начале июня, второй — во второй половине июля — начале августа.
К Ф. л. восприимчивы все люди. В местах распространения Ф. л. болеют преимущественно вновь прибывающие, а из местных жителей — преимущественно дети.
Патогенез
Заражение человека вирусом Флеботомной лихорадки происходит через кожу при укусе инфицированного москита. На месте укуса обычно появляется точечное красноватое пятнышко, как при уколе булавкой. После 3—9-дневного размножения вируса в лимфоидных клетках развивается вирусемия, обусловливающая общетоксические проявления, поражение ц. н. с., костного мозга. Типична воспалительная реакция в месте укуса флеботомусов. Экспериментально удалось вызвать болезнь у обезьян макак-резус путем введения им крови больных Ф. л., в период лихорадочной реакции, а также успешно пассировать вирус от обезьяны к обезьяне. При заражении волонтеров Сейбин (1952) получил типичную 3-дневную лихорадку, протекающую с относительной брадикардией и соответствующими изменениями в крови.
Патологическая анатомия не изучена.
Иммунитет
Стойкий иммунитет вырабатывается примерно у 80% лиц, переболевших Ф. л. однократно. Вместе с тем ряд лиц заболевает 2—3 раза, после чего иммунитет также становится стойким. Повторные заболевания объясняются, вероятно, последовательными заражениями неаполитанским и сицилийским вирусами.
Клиническая картина
Инкубационный период при Флеботомной лихорадке колеблется в пределах 3—9 дней, чаще 4—5 дней. Продромальные явления почти всегда отсутствуют. Обычно болезнь начинается внезапно с озноба, после чего в течение 3—5 час. повышается температура до 39—40°. Больных беспокоит сильная головная боль, особенно в лобной и височной областях, разбитость, выраженная боль в мышцах, особенно конечностей и спины, в суставах, боль при движении глазных яблок, к-рая усиливается при попытке поднять веки, а также при давлении на глазные яблоки (симптом Тауссига), светобоязнь (см.).
Могут быть боли в животе, тошнота и рвота, потеря аппетита. Лицо больных гиперемировано, выражена гиперемия конъюнктив, инъекция сосудов склер, более интенсивная у наружных углов глаз, где она имеет вид треугольника, обращенного основанием к наружным углам глаз, а вершиной — к роговице; эти изменения получили название симптома Пика, к-рый считается патогномоничным для Ф. л. Гиперемирована также слизистая оболочка зева и язычка, нередко выявляются кровоизлияния у его основания. Язык покрыт беловатым налетом, сухой. На губах бывают герпетические высыпания. На месте укуса москита часто появляются зудящие папулы диам. 2—3 мм розового или красного цвета, иногда превращающиеся в везикулы; через 4—5 дней папулы исчезают. Пульс соответствует температуре в 1-й день болезни, затем чаще отмечается брадикардия; АД снижено. Наблюдаются головокружения (см.), бессонница (см.), могут быть бред (см.), потеря сознания (см.), иногда возбуждение и судороги (см.).
Лихорадочный период в большинстве случаев длится 2—4 дня. Период реконвалесценции, продолжающийся до 10 сут., сопровождается астенизацией, иногда депрессией, на 5 — 7-е сутки у больных могут появляться кратковременные (1 — 2 дня) рецидивы болезни.
Осложнения чаще отсутствуют, однако возможно появление отита (см.), паротита (см.), полиневрита (см.), пневмонии (см.).
Диагноз
Диагноз основывается на данных клинической картины. В крови обычно лейкопения с относительным лимфоцитозом, к-рый к концу лихорадочного периода может смениться тенденцией к нейтрофилезу.
Диагноз подтверждается данными вирусологических и серологических исследований (см. Вирусологические исследования, Серологические исследования). Для выделения вируса заражают новорожденных белых мышей путем введения им в мозг крови больных. Вирус обычно удается выделить и идентифицировать при последовательном заражении нескольких животных (см. Идентификация вирусов). Хорошие результаты дает выделение вируса методом бляшек на клетках VERO. Из серол. реакций наиболее достоверные результаты дает реакция нейтрализации методом редукции бляшек на клетках VERO и реакция связывания комплемента (см.).
Дифференцируют Ф. л. с гриппом (см.), малярией (см.), сыпным тифом (см. Сыпной тиф эпидемический), лептоспирозом (см.), денге (см.), клещевым возвратным тифом (см.).
При гриппе выражены катаральные явления со стороны верхних дыхательных путей, отсутствует симптом Пика и зудящие папулезные высыпания.
Лечение
Больных госпитализируют. Назначают постельный режим, полноценное питание и средства дезинтоксикационной и симптоматической терапии: вливание полиионных р-ров. анальгетики (амидопирин, анальгин), седативные препараты, сердечно-сосудистые средства (эфедрин, кофеин, по показаниям — сердечные гликозиды), кортикостероидные гормоны (коротким курсом в 4—5 дней), витамины. Антибиотики не эффективны. Выписывают больных из стационара на 7 — 10-й день нормальной температуры.
Прогноз благоприятный, летальные исходы не зарегистрированы.
Профилактика
Профилактика сводится к уничтожению москитов с помощью инсектицидов (см.), к защите людей от нападения москитов. Для этого двери и окна в домах завешивают мелкоячеистыми (ячейки не более 0,7 мм) или марлевыми пологами (см. Защитные сетки), лучше импрегнированными репеллентами (см.), в частности диэтилтолуамидом (ДЭТА), импрегнацию повторяют через 2—3 нед.
К. М. Лобан; С. Я. Гайдамович (этиол., мет. иссл.).

СИМФЕРОПОЛЬ, 23 авг — РИА Новости Крым. В Белогорском районе зафиксирован случай заболевания лихорадкой Западного Нила (ЛЗН). Об этом РИА Новости Крым сообщила главный государственный санитарный врач по Республике Крым и городу федерального значения Севастополю Наталья Пеньковская.
Готовность номер один
"На прошлой неделе в Белогорском районе зафиксирован случай лихорадки Западного Нила. Дополнительно проведены все организационные мероприятия по выявлению вновь появившихся (переносчиков инфекции — ред.) в водоемах, которые требуют проведения обработок. Такие обработки проводятся", — рассказала она.

"Мероприятия по профилактике таких заболеваний не возникают при появлении чрезвычайных ситуаций в том или ином субъекте: это плановая работа, осуществляемая с момента, когда начинается активность комаров (переносчиков инфекции — ред.), проводятся энтомологические обследования территорий и ларвицидные обработки тех водоемов, на которых возможен выплод комаров (переносчиков соответствующих инфекций — ред.). Все мероприятия, которые необходимы, на территории Крыма проводятся, медицинская служба готова к выявлению таких больных, лабораторная служба готова к их диагностики", — уточнила главный санитарный врач по Крыму и Севастополю.
В начале августа Управление Роспотребнадзора по Краснодарскому краю сообщило о фиксировании на территории края семи случаев заболевания лихорадкой Западного Нила, том числе двух "завозных из других субъектов РФ". В ведомстве уточнили, что подобные случаи фиксируют ежегодно.
В то же время Управление Роспотребнадзора по Ростовской области проинформировало об 11 лабораторно подтвержденных случаев заболевания ЛЗН, в том числе 8 — в Ростове-на-Дону, 2 — в Сальске и один — в Мясниковском районе.
Ареал вируса Западного Нила (ВЗН), являющегося возбудителем инфекции, в России охватывает ландшафтные пояса пустынь, полупустынь, степи, лесостепи на территории юга европейской части, южные районы Сибири и Дальнего Востока. Тенденция потепления климата ведет к изменению условий обитания переносчиков арбовирусов, что способствует расширению ареала вируса.
Смертельная "комарилья"
Основным источником и резервуаром ВЗН в природной среде являются дикие птицы водного и околоводного комплексов, синантропные птицы, а переносчиками — более 60 видов комаров. Как сообщают "Известия", ученые Института медицинской паразитологии, тропических и трансмиссивных заболеваний им. Е.И. Марциновского Первого Московского государственного медицинского университета им. И.М. Сеченова вместе со специалистами Института общей генетики им. Н. И. Вавилова и МГУ им. М. В. Ломоносова выявили распространение на черноморском побережье Краснодарского края популяции двух видов комаров — переносчиков опасных тропических лихорадок: Aedes aegypti и Aedes albopictus.
"Получившие широкое распространение в Крыму и по всему черноморскому побережью Краснодарского края насекомые вызывают эпидемические вспышки лихорадок Денге, Чикунгунья, Зика и др. Вид Aedes aegypti является также основным переносчиком вируса желтой лихорадки, при которой развивается тяжелое состояние, сопровождающееся желтухой. Все эти болезни смертельны (большинство пациентов погибает в течение недели) и имеют тенденцию к быстрому распространению", — отмечает издание.
Как пояснил ведущий научный сотрудник лаборатории молекулярной биологии и биохимии Института Марциновского Александр Лукашев, найденные виды переместились в Россию из Египта и Юго-Восточной Азии из-за глобального потепления. "Если комар-переносчик любой из этих лихорадок укусит лишь одного туриста, этого будет достаточно, чтобы весь регион охватила эпидемия", — предупредил микробиолог.

По словам Лукашева, миграция переносчиков тропических болезней, которые в принципе не должны появляться на севере, в области с подходящими им температурными условиями является общемировой проблемой. "Похожая картина наблюдается и в Европе. По прогнозам ученых, к 2050 году эти комары распространятся даже в Швеции. У нас они размножились на юге, а теперь продвигаются в Центральную Россию", — констатировал ученый.
К возбудителям москитной лихорадки относятся близкие в антигенном отношении вирусы москитной лихорадки Сицилия(входят в комплекс вирусов москитной лихорадки Сицилия), вирусы москитной лихорадки Неапольи Тоскана(входят в комплекс москитной лихорадки Неаполь) и другие вирусы данных серологических групп, а также вирусы серогруппы Кандируи негруппированные вирусы,относящиеся к роду Phlebovirus(более 20 вирусов).
Вирусная этиологияя москитной лихорадки в опытах на волонтерах была установлена Р. Дерр (R. Doerr) совместно с К. Францем и С. Тауссигом (К. Franz, S. Taussig) в 1909 г. Возбудители сицилийской москитной лихорадки и неаполитанской москитной лихорадки были выделены А. Сэйбином (A. Sabin) в 1944 г. из крови больных в период эпидемии среди американских солдат в Италии.
период — 3—7 дней. На месте укуса появляется папула. Болезнь начинается остро с озноба, головной боли, боли в глазных яблоках. Характерен симптом Пика— ограниченная инъекция сосудов наружного угла склер в виде треугольника, обращенного вершиной к зрачку, и синдром Тауссига— резкая болезненность при надавливании на глазные яблоки, а также при их движении или при попытке приподнять веки. Лихорадка Тоскана характеризуется развитием асептического менингита.Это самокупирующееся заболевание. Прогноз благоприятный, летальных исходов нет. Перенесенное заболевание оставляет после себя напряженный типоспе-цифический иммунитет к штамму, циркулирующему в данном эндемическом очаге, который формируется в результате многократного инфицирования. Но поскольку он развивается очень медленно, то возможны повторные случаи заболевания, по 2—3 раза в одном и том же сезоне. Микробиологическая диагностика основана на выделении вируса и обнаружении антител в парных сыворотках с помощью РСК, РТГА, РНГА, РНИФ, ИФА. Обнаружение антигена в крови проводят с помощью РСК, дающей положительные результаты в первые часы заболевания. Специфическое лечение и профилактика не разработаны. В отдельных случаях показана специфическая иммунизация населения с помощью инактивированной формолвакци-ны, которая не нашла широкого применения в связи с самокупирующимся инфекционным заболеванием.
17.1.3.2. Вирус лихорадки Рифт-валли
Вирус лихорадки Рифт-валли назван по долине Рифт в Кении, где он был выделен в1930 г. от больного ягненка во время вспышки заболевания у скота. Вирус Рифт-валли относится к роду Phlebovirus и входит в состав антигенной группы лихорадки долины Рифт. Это один из наиболее патогенных для человека вирусов семейства Bunyaviridae. Он может длительно (в течение нескольких месяцев) сохранять свою жизнеспособность при 4 "С в среде с добавление сыворотки крови и в течение трех часов выдерживает нагревание до 56 "С. Он также хорошо сохраняется в высушенном виде и в состоянии аэрозоля.Вирус инактивируется в течение 3 суток под воздействием 0,1% бетапропиолак-тона при рН 9,0 или 0,25% раствора формалина при 4 'С. Быстрая его инактивация наступает под воздействием кислой среды при рН ниже 6,8. Штаммы вирусов Рифт-валли, выделенные в ЮАР и Родезии(1975 и 1978 год), Египте
(1977-1978 гг.), Мавритании (1978 г.) отличаются от других африканских штаммов по своим биологическим и антигенным свойствам, а также повышенной вирулентностью для людей и лабораторных животных. Вирусы хорошо размножаются в большинстве культур клеток, вызывая развитие ЦПД, а также вызывают гибель белых мышей при внутрибрюшинном введении. Он считается одним из немногих вирусных агентов, вызывающих гибель мышей при периферическом заражении.
Резервуаром и источником вируса в природе являются кровососущие насекомые, прежде всего комары рода Culex и Aedes и др., главным образом С. pipiens и С. antennatus, а также про-кормители кровососущих членистоногих насекомых — крупный и мелкий рогатый скот, верблюды, лошади, антилопы, обезьяны, летучие мыши. Комары включаются в биологический цикл вируса благодаря достаточно длительной и высокой вирусемии у больных животных. В результате трансовариальной передачи вирус может длительное время (на протяжении нескольких засушливых лет) сохраняться в яйцах комаров. В период вирусемии человек также может быть источником заражения для комаров, что свидетельствует о потенциальной способности к эпидемическому распространению заболевания. Обычно эпидемии данной лихорадки развиваются вслед за эпизоотиями среди домашних копытных животных (овцы, козы, крупный рогатый скот, верблюды), которые являются источником возбудителя. Основной механизм заражения трансмиссивный.Возможен также контактный механизм зараженияпри убое и разделке туши больного животного, контакте с инфицированным мясом и внутренними органами животного, когда вирус проникает через поврежденные кожные покровы, а также аэрогенный механизм заражения,например, внутрилабораторное заражение воздушно-пылевым путем при проведении вирусологических исследований. Кровь и ткани внутренних органов больных животных содержат значительные количества вируса; иногда вирус может содержаться в их экскрементах. Во время эпизоотии отмечены многочисленные случаи заражения людей алиментарным путемв результате употребления мяса больных или погибших животных, а также молока больных животных.
В период лактации вирус выделяется с молоком, которое в эндемичных районах должно подвергаться пастеризации.
Помимо Африканского континента, заболевание выявлено в Афганистане и в странах Латинской Америки.
Патогенез заболевания.Характеризуется размножением вируса в месте входных ворот инфекции в регионарных лимфатических узлах и проникновением его в кровь, в результате чего вирус разносится по паренхиматозным органам, где размножается, и снова поступает в кровяное русло, обуславливая развитие выраженной вторичной вирусемиии вызывая повреждение внутренних органов. Вирус пантро-пен. Штаммы, вызывающие геморрагическую форму заболевания, размножаются в основном в эндотелии сосудов (васкулит) и паренхиматозных органах. Инкубационный периоддлится от 3 до 7 дней. Выделяют четыре формы заболевания:неосложненная, менингоэнцефали-тическая, геморрагическая и заболевание с поражением органов зрения (ретинит).
Неосложненная формазаболевания начинается остро и характеризуется лихорадкой, головной болью, миалгией, болями в суставах, светобоязнью, рвотой, диареей, явлениями гепатита; длится 2—7 дней. Полное выздоровление наступает через 20—80 суток от начала заболевания.
Наиболее тяжело протекает геморрагическая форма заболевания,которая характеризуется
наличием желтухи и геморрагического синдрома. Большинство больных погибают от острой печеночной недостаточности. Летальность при менингоэнцефалитической форме заболевания,которая также протекает тяжело, составляет от 5 до 30 %. Восстановление зрения при ретинитахотмечается через 50—70 суток.
Естественная восприимчивость людей высокая. Постинфекционный иммунитет типос-пецифический, нестойкий. Около 20 % переболевших заболевают повторно (2—3 раза).
Микробиологическая диагностикаоснована на выделении вирусаиз крови, фекалий и глоточных смывов путем заражения новорожденных белых мышей и культур клеток в первые 2—3 дня заболевания, а также на обнаружении антителк вирусу в парных сыворотках с помощью РСК, РТГА, РИГА, РНИФ и ИФА. С целью обнаружения вируса и его антигеновв исследуемом материале применяют РИФ.
Специфическое лечениене разработано. Для лечения рекомендуется использовать индукторы интерферона, рибавирин, иммунную сыворотку. Выраженным защитным действием обладает гомологичный иммуноглобулин. В опытах на животных показана эффективность гетерогенных иммуноглобулинов. В целом лечение эффективно. Так как заболевание имеет не только медицинское, но и ветеринарное значение, мерами его предупреждения являются проведение карантинных мероприятий и поголовная вакцинация скота убитой и живой вакцинами. Для профилактики заболевания у людей(ветеринаров, животноводов, сотрудников лабораторий, работников скотобоен и солдат, направленных в эндемичные районы по лихорадке Рифт-валли), применяют только убитую культуральную формолвакцину,созданную в США. Разрабатываются генно-инженерные методы получения безопасных и более эффективных вакцин.
При проведении лабораторных исследований с вирусом следует избегать манипуляций, которые могут привести к образованию аэрозоля и случайному попаданию вируса в окружающую среду.
Молоко в эндемичных регионах должно обязательно подвергаться пастеризации.
17.1.3.3. Вирус геморрагической лихорадки Крым-Конго
Эпидемиология, патогенез и клинические проявления заболевания.Заболевания впервые были выявлены в Крыму в 1944 г. военными врачами среди солдат и переселенцев, занятых уборкой сена. В 1945 г. М. П. Чумаков и его ученики из крови больных в острой стадии болезни и от переносчиков инфекции — иксодовых клещей выделили вирус геморрагической лихорадки Крым-Конго. В 1956 г. в Африке при сходном заболевании был выделен вирус Конго, который по биологическим свойствам оказался идентичен вирусу крымской геморрагической лихорадки, поэтому возбудителя болезни называют вирусом геморрагической лихорадки Крым-Конго. Болезнь, вызванная вирусом в Конго, протекает без геморрагического компонента, относительно редко наблюдается у людей, но вирус часто обнаруживают у животных.
Вирус геморрагической лихорадки Крым-Конго относится к арбовирусным природ-но-очаговым заболеваниям. В России это заболевание встречается на территории Краснодарского и Ставропольского краев, Астраханской, Волгоградской и Ростовской областей, республик Дагестан, Калмыкия и Карачаево-Черкесии. Основным резервуаром вируса в природе и источником инфекции являются многие виды пастбищных клещей, передающих вирус своему потомству трансо-вариально и по ходу метаморфоза. Основное значение имеют гиаломовые клещи, способные сохранять вирус до 250 суток и после кормления практически в 100 % случаев инфицировать теплокровных животных. Животные, на которых паразитируют эти клещи (ежи, зайцы, коровы, овцы и козы), служат вре-
Проникая в организм человека, вирус в течение инкубационного периода (от 1 до 14 дней) размножается в макрофагах, а затем поступает в кровь. Он обладает вазотропнос-тью, что ведет к развитию генерализованного капилляротоксикоза. Вирус поражает также область гипоталамуса и кору надпочечников, избирательно — слизистую оболочку желудка. Убедительных объяснений такой избирательности не существует. В течение заболевания выделяют несколько периодов: начальныйили предгеморрагическийпериод, период разгараили геморрагических проявлений и период реконвалесценции.В типичном случае заболевание характеризуется острым началом: лихорадкой, выраженной интоксикацией, тяжелыми геморрагическими проявлениями, которые более выражены, чем при омской геморрагической лихорадке. Летальность может достигать 40 %. Смерть наступает от инфек-ционно-токсического шока, массивных кровотечений, печеночно-почечной недостаточ-
ности. Так как у части больных(7-9 %) геморрагические проявления могут отсутствовать, выделяют две клинические формы болезни: с геморрагическими проявлениями и без геморрагических проявлений. Последняя форма протекает, как правило, гораздо легче, чем первая. Период реконвалесценции длительный. Трудоспособность восстанавливается не ранее чем через 1—2 месяца. Различные нарушения в организме после выписки больного из стационара могут сохраняться в течение 1—2 лет и более. Иммунитет напряженный. Комплементсвязывающие и преципитирую-щие антитела у переболевших сохраняются свыше 5 лет. В то же время для геморрагической лихорадки Крым-Конго характерен низкий уровень коллективного иммунитета к данному вирусу. Это обусловлено низкой степенью вовлечения населения в эпидемиологический процесс, низким уровнем циркуляции вируса в природе и сравнительно редким нападением его переносчиков на человека.
Микробиологическая диагностика.Диагностика геморрагической лихорадки Крым-Конго основана на выделении вируса из крови больных и внутренних органов погибших путем заражения новорожденных белых мышей и культур клеток с идентификацией в РИФ, а также на обнаружении антител в парных сыворотках с помощью РНИФ, РСК, РДПА, РИГА, РИА и ИФА, постановки ПЦР Экспресс-диагностика вируса в крови, аутопсийном материале и переносчиках осуществляется с помощью РИГА или РИФ с флюоресцирующей моноклональ-ной мышиной сывороткой к вирусу.
Лечение и профилактика.Для лечения геморрагической лихорадки Крым-Конго применяют реаферон, рибавирин. В первые 3 дня вводят гетерогенный специфический лошадиный иммуноглобулин, а также иммунную сыворотку, плазму или специфический иммуноглобулин, полученные из сыворотки крови реконвалесцентов или привитых лиц. Специфический иммуноглобулин используется для экстренной профилактики у лиц, соприкасающихся с кровью больного. Для создания активного иммунитета у сотрудников лабораторий в целях профилактики используют формолвакцину из мозга зараженных сосунков белых мышей или белых крыс. Для
тех, кто выезжает в Южные регионы России (командировка, отпуск и т.д.), рекомендуют вакцинацию против вируса геморрагической лихорадки Крым-Конго вакциной, производимой в Болгарии. В стационарах должна быть обеспечена профилактика внутриболь-ничного распространения вируса, прежде всего парентерально, поскольку вирус находится в высоких концентрациях в крови человека. Поэтому госпитализация больных проводится обязательно в отдельные боксы. Обслуживание больных должно проводиться специально обученным персоналом.
17.1.3.4. Вирусы ГЛПС и синдрома хантавирусной пневмонии
Таксономическое положение и биологические свойства возбудителей.Возбудители ГЛПС и синдрома хантавирусной пневмонии относятся к вирусам семейства Bunyaviridae рода Hantavirus антигенного комплекса Hantaan. Типовой представитель данного рода — вирус Хантаан (HTVN), выделенный из легочной ткани, а также экскрементов Apodemus agrarius corea корейскими учеными в 1978 г. (Н. W. Lee и соавт.) и названный по р. Хантаан, протекающей по Корейскому полуострову. В отличие от типичных буньявирусов, его частицы характеризуются большей гетерогенностью размеров (90—125 нм), а также наличием во внутренней полости неупорядоченно расположенных гранулярно-филаментозных структур. Вирус хорошо размножается в культурах клеток Vero Е-6, А-549, RLC, 2Вс без выраженного ЦПД. Его удается пассировать на полевых мышах, степных пеструшках, джун-гарских и золотистых хомяках, крысах линии Вистар и Фишер. Животные могут быть заражены различными способами, но самый лучший из них — внутрилегочный способ заражения. Все эти животные являются бессимптомными носителями вируса. У них вирусы обнаружены в легких, буром жире, селезенке, прямой кишке и других органах с помощью ЭМ и РНИФ в виде гранул в цитоплазме клеток. Максимальная концентрация вирусов отмечается на 20-30-й день после заражения. Антитела у животных появляются с 10-го дня после заражения и сохраняются в течение года. Хантавирусы неоднородны в антигенном
отношении. Возбудителями ГЛПС являются 4 из 23 известных в настоящее время серотипов вируса: Хантаан, Пуумала, Сеул и Доброва/ Белград.У других хантавирусов связь с заболеванием человека не установлена, антитела к ним не обнаружены. Название ГЛПС было предложено в 1954 г. М. П. Чумаковым и рекомендовано ВОЗ в 1982 г. для единого обозначения этой нозологической формы, которая была описана под разными названиями (корейская геморрагическая лихорадка, геморрагический нефрозо-нефрит, эпидемическая нефрозопатия, эпидемическая геморрагическая лихорадка или болезнь Сонго).
Эпидемиология, патогенез и клиника хан-тавирусных инфекций.Хантавирусы широко распространены в природе. По уровню заболеваемости ГЛПС в России занимает ведущее место среди природно-очаговых болезней человека и регистрируется на 61 из 89 административных территорий.При этом 97 % от общего числа случаев ГЛПС ежегодно регистрируется в европейских и только 3 % — в азиатских регионах России, главным образом на Дальнем Востоке. Наиболее высокие показатели ежегодной заболеваемости ГЛПС отмечаются на территориях Уральского, Поволжского и Волго-Вятского регионов.
Данные вирусы относятся к экологической группе нетрансмиссивных геморрагических лихорадок или робовирусам (от англ. rodent-borne viruses — вирусы, рожденные грызунами). В качестве резервуара и источника инфекции при ГЛПС следует рассматривать мышевид-

Лихорадка паппатачи – острая природно-очаговая инфекция, вызываемая фильтрующимся арбовирусом и протекающая с кратковременным лихорадочным синдромом. Лихорадка паппатачи сопровождается фебрильной температурой, головными и мышечными болями, глазными реакциями (симптомами Пика и Тауссига), гиперемией лица и шеи, геморрагиями, менингеальными явлениями, длительным астеническим синдромом. Распознавание лихорадки паппатачи проводится на основе эпидемиологического анамнеза, клинической картины, серологического и вирусологического исследований. Лечение лихорадки паппатачи симптоматическое; включает дезинтоксикационную терапию, прием жаропонижающих, сердечно-сосудистых средств, витаминов.
Общие сведения
Лихорадка паппатачи (москитная, трехдневная, флеботомная лихорадка) - трансмиссивное вирусное заболевание с характерной кратковременной лихорадкой, выраженной миалгией, патогномоничными реакциями со стороны глаз, неврологической симптоматикой. Территория распространения лихорадки паппатачи совпадает с ареалом обитания москитов-переносчиков и охватывает тропические и субтропические регионы (Средиземноморье, Балканы, Ближний Восток, Восточную и Западную Африку, Южную и Юго-Восточную Азию, Северный Кавказ и Закавказье, Среднюю Азию). Заболеваемость лихорадкой паппатачи характеризуется строгой весенне-летней сезонностью с двумя пиками (май-июнь, июль-август), обусловленными выплодом москитов. Лихорадка паппатачи чаще развивается у неиммунных лиц, впервые приезжающих в эндемичные районы; у коренных жителей имеется иммунитет вследствие заболевания, перенесенного в раннем детстве.

Причины лихорадки паппатачи
Лихорадку паппатачи вызывают 5 серотипов фильтрующегося РНК-геномного вируса из семейства буньяновирусов. Вирусные частицы чувствительны к нагреванию, воздействию дезинфицирующих средств, однако устойчивы к низким температурам; в высушенном состоянии сохраняются до 3-7 месяцев. Существуют природные и антропургические очаги лихорадки паппатачи.
Источником вируса служат инфицированные дикие и синантропные грызуны или больной человек в стадии вирусемии. Специфическими переносчиками вируса лихорадки паппатачи выступают летающие кровососущие насекомые – самки москитов Phlebotomus papatasii. При питании кровью больных животных и человека, находящегося в начальном периоде заболевания, вирус лихорадки паппатачи попадает в организм москита, размножается и остается в нем пожизненно, передаваясь следующим поколениям трансовариально. Человеку лихорадка паппатачи передается чаще всего трансмиссивным путем при укусах зараженных москитов; не исключается возможность парентерального заражения через недостаточно обработанные медицинские инструменты.
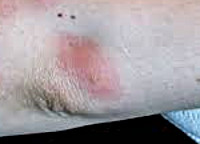
Укусы москитов сопровождаются покраснением кожных покровов, отеком, образованием зудящего узелка, расчесами. В организме человека вирус лихорадки паппатачи поражает клетки моноцитарно-макрофагальной системы, где быстро репродуцируется в течение инкубационного периода и уже в первые 2-3 дня заболевания попадает в кровяное русло с развитием генерализованной вирусемии. Ввиду определенной нейротропности, вирус лихорадки паппатачи оседает в клетках ЦНС, вызывая нарушение ее функций, приводя к церебральной гипертензии. Изменения также затрагивают мелкие сосуды и мышцы.
Симптомы лихорадки паппатачи
Продолжительность инкубационного периода лихорадки паппатачи составляет от 3 до 9 дней. Заболевание имеет острое, внезапное начало с выраженным ознобом и резким скачком температуры до 38-41˚C. Лихорадка паппатачи сопровождается сильной головной болью в височной и лобной зонах; резкой миалгией, особенно в икроножных мышцах, спине и пояснице; болью по ходу нервных стволов. Отмечаются патогномоничные глазные реакции: ограниченная инъекция склер у наружных углов глаз в виде треугольника с вершиной, направленной к роговице (симптом Пика), сильная боль при движении глаз, надавливании на глазное яблоко и попытке поднять пальцами верхнее веко (симптом Тауссига), фотофобия, конъюнктивит.
Заметна одутловатость лица и шеи, гиперемия слизистой оболочки зева с точечными геморрагиями, отеком небных дужек и язычка. На губах возможно появление герпетических высыпаний, на коже – макулезной или уртикарной сыпи и мелкоточечных кровоизлияний. Могут наблюдаться носовые и желудочно-кишечные кровотечения. При тяжелых формах лихорадки паппатачи появляются неврологические симптомы: головокружения, гиперестезия, менингеальные явления, беспокойство, возбуждение, бред, потеря сознания. Нередко возникает вздутие живота, тошнота, рвота, учащенный до 5-6 раз в сутки жидкий стул с примесью слизи.
Длительность лихорадочного периода определяется тяжестью клинического течения лихорадки паппатачи: при легкой форме фаза лихорадки продолжается 1-2 дня, при среднетяжелой – 3-4 дня, при тяжелой – до 8 дней. Температура снижается критически до нормальных или субфебрильных показателей, что сопровождается резкой слабостью и проливным потом, брадикардией. Период реконвалесценции длительный; продолжается несколько недель и протекает с выраженной астенией, невралгиями, депрессией и снижением работоспособности. Иногда имеют место трофические расстройства, проявляющиеся выпадением волос, ломкостью ногтей. Осложнения лихорадки паппатачи отмечаются редко в виде пневмонии, инфекционного психоза.
Диагностика лихорадки паппатачи
Основу диагностики лихорадки паппатачи составляют данные эпидемиологического анамнеза (эндемичный район, сезонность, массовость заболевания), характерной клинической картины (острое начало, кратковременность лихорадки, выраженная миалгия, симптомы Пика и Тауссига), лабораторных исследований (общего анализа крови, серологических реакций, вирусологического метода).
В крови больного лихорадкой паппатачи отмечается нарастающая лейкопения со сдвигом влево, лимфопения, анэозинофилия, моноцитоз. Люмбальная пункция и анализ цереброспинальной жидкости выявляют признаки повышенного ликворного давления, умеренный цитоз и высокое содержание белка. Диагноз лихорадки паппатачи подтверждает выделение вируса из крови и спинномозговой жидкости в лихорадочный период методом интрацеребрального заражения новорожденных мышей. Серологические исследования (РН, РСК, РТГА с парными сыворотками), проведенные на 2-3 день заболевания и через 2-3 недели после этого, показывают нарастание титра специфических антител. Дифференциальная диагностика лихорадки паппатачи проводится с гриппом, малярией, сыпным и клещевым возвратным тифами, лихорадкой денге, безжелтушной формой лептоспироза, энтеровирусной лихорадкой и др.
Лечение и профилактика лихорадки паппатачи
Больные лихорадкой паппатачи подлежат госпитализации в инфекционный стационар. Специфического лечения москитной лихорадки не существует; в острый период больным показан постельный режим, достаточная питьевая нагрузка, прием витаминов. Медикаментозная поддержка включает дезинтоксикационную и симптоматическую терапию (назначение жаропонижающих и сердечно-сосудистых средств; при внутричерепной гипертензии – диуретиков). Выписка пациентов, перенесших лихорадку паппатачи, осуществляется спустя 2-3 недели от начала заболевания (на 7-10 день апирексии).
Исход лихорадки паппатачи благоприятный: осложнения достаточно редки, в некоторых случаях возможны рецидивы. Предупреждение распространения лихорадки паппатачи предполагает уничтожении взрослых москитов и очагов их выплода (нор грызунов, щелей и трещин в стенах и полу построек, мусорных свалок), инсектицидную обработку хозяйственных строений и жилища, защиту людей от укусов москитов (оборудование тамбуров, использование сеток на окнах и пологов над кроватью, ношение защитной спецодежды и сеток, пропитанных репеллентами). Специфическая профилактика лихорадки паппатачи проводится эмбриональной формалинизированной вакциной за 2 месяца до начала эпидемического сезона.
Читайте также:


