Отек мозга у детей при инфекционных
а) Определение и клинические проявления. Отек мозга определяется как повышение объема головного мозга вследствие увеличения содержания в нем воды. Отек является важной причиной повышения ВЧД. Тем не менее, локализованный отек не обязательно вызывает внутричерепную гипертензию, однако может привести к очаговой дисфункции.
Диагностика отека мозга может быть сложна. Клинические проявления включают признаки повышенного ВЧД, а дифференциация отека мозга от застойного полнокровия мозга, т. е. увеличения объема крови в головном мозге, может быть трудной. Повышение объема крови может быть вызвано эпилептической активностью, параличом сосудов вследствие асфиксии, травмой головы, повышением содержания СO2 в крови вследствие заболеваний легких или сердца, венозной обструкцией и эффектами препаратов, таких как нитраты, хлорпромазин и галотан.
Отек мозга может быть выявлен при визуализации. КТ может демонстрировать диффузное или локализованное небольшое ослабление сигнала в результате высокого содержания воды. На МРТ отек часто проявляется интенсивным сигналом на Т2-взвешенных спин-эхо последовательностях (Barnes et al., 1987).
Диффузионно-взвешенная МРТ и диффузионно-тензорная МРТ, позволяющие точнее изучить содержание воды и подвижность, могут дать информацию о локализации отека относительно различных клеточных компартментов и могут быть полезны при определении тактики лечения (Lu et al., 2004; Sinha et al., 2004). Отек может быть изолированной находкой, например, у пациентов с диабетическим кетоацидозом (Rosenbloom et al., 1980) или после унилатерального или фокального эпилептического статуса. Отеком часто сопровождаются другие патологические процессы, такие как опухоли и абсцессы мозга.
Клинические проявления отека мозга часто трудно отделить от проявлений причинного заболевания. Основным последствием отека мозга является уменьшение микроперфузии мозга и ишемия. По этой причине наличие отека мозга, вместе с другими нарушениями или изолированно, играет важную роль в ведении пациентов и в понимании клинической картины.
б) Типы и причины отека мозга. Отек мозга можно разделить на несколько типов в зависимости от локализации и патогенеза, причем каждый тип отека преимущественно ассоциирован с определенными причинами.
Вазогенный отек возникает вследствие повышенной проницаемости эндотелия капилляров гематоэнцефалического барьера, что приводит к экссудации богатого белками фильтрата плазмы во внеклеточную жидкость. Это тип отека вовлекает в наибольшей степени белое вещество мозга, с локальным или диффузным распространением. Вазогенный отек вызывают воспалительные процессы, такие как менингит или абсцессы; опухоли мозга; очаговые поражения, вызывающие воспалительную реакцию с помощью различных механизмов, такие как внутричерепные кровоизлияния или инфаркты; и расстройства, при которых преимущественно поражаются сосуды, такие как свинцовая энцефалопатия или гипертензивная энцефалопатия.
Отек, появляющийся через несколько часов после травмы головы, вероятно, относится к этому типу, так же как и очаговый отек после сложного парциального эпилептического статуса, хотя, в обоих случаях, причин и механизмов может быть несколько. Лечение кортикостероидами эффективно только при этом типе отека.
Цитотоксический отек может сосуществовать с вазогенным отеком. При этом типе клеточные компоненты мозга, особенно астроциты, но также нейроны и эндотелиальные клетки, подвергаются быстрому отеку в результате дисфункции мембран и ионных насосов. Последний обычно возникает вследствие дефицита энергии и может привести к смерти клеток, при которой отек становится необратимым. Самой частой причиной является гипоксия вследствие остановки сердца или вследствие любой причины гипоксически-ишемической энцефалопатии, хотя возможными причинами являются различные токсины и тяжелые инфекционные процессы, а также повышение ВЧД со снижением мозгового кровотока.
Другие механизмы включают гибель нейронов после эпилептического статуса и артериального инфаркта.
Гипоосмолярный отек развивается из-за разницы осмотического давления между низкой осмолярностью плазмы и более высокой осмолярностью глиальных клеток. Внутри астроцитов накапливается вода. Этот тип отека возникает при гипонатриемии, либо ятрогенной, либо вследствие неадекватной секреции АДГ у пациентов с сахарным диабетом при лечении кетоацидоза, и при синдроме нарушенного равновесия у пациентов, находящихся на диализе по поводу почечной недостаточности или по другим причинам.
Интерстициальный отек вызывается трансэпендимальной резорбцией СМЖ из желудочков во внеклеточное пространство у пациентов с гидроцефалией. Этот тип отека хорошо виден при КТ или МРТ, которые демонстрируют снижение аттенуации в перивентрикулярных областях, особенно вокруг передних и задних рогов.
Гидростатический отек возникает, когда повышение внутрисосудистого давления передается на капиллярное ложе вследствие недостаточного повышения сосудистого сопротивления, что приводит к выходу жидкости во внеклеточное пространство. Это происходит при нарушении сложных механизмов ауторегуляции сосудов мозга.

в) Лечение повышенного внутричерепного давления. Повышение ВЧД является одной из основных проблем при опухолях мозга и других объемных образованиях, а также при некоторых острых патологиях, таких как травма, инфекции ЦНС и ишемия. Повышенное ВЧД вызывает многие осложнения, включая смещение структур мозга и грыжу, поэтому требует раннего распознавания и лечения. В таблице ниже перечислены симптомы и признаки угрожающих жизни осложнений.
Эти проявления обычно относятся к грыже, хотя они могут быть вызваны высоким ВЧД со сниженным мозговым кровотоком, поэтому при снижении давления часто достигается регрессия симптомов.
В хронических случаях, например, при опухолях мозга, достаточным обычно является лечение причины (удаление образования). В острых ситуациях, однако, лечение причины столь же необходимо, но может быть недостаточным. Наиболее частые причины острого повышения ВЧД перечислены в таблице ниже. В таких случаях часто необходимо быстрое снижение ВЧД, что может значительно улучшить исход (см. Minns, 1991).
Целью лечения является снижение ВЧД для поддержания мозгового перфузионного давления выше 50 мм рт. ст., что гарантирует нормальную оксигенацию мозга. Мозговое перфузионное давление равно разнице между средним системным давлением и ВЧД. Следовательно, жизненно важным является поддержание системной циркуляции. ВЧД можно определить различными способами, но одиночное измерение имеет малую ценность для правильного ведения пациента. По этой причине все большее применение находит постоянный мониторинг ВЧД. Тем не менее, следует подчеркнуть, что гораздо более важным является неотложное лечение причины, например, менингита, чем постановка монитора ВЧД (Kirkham, 1991).
Когда перфузия мозга приближается к нулю, при допплеровском исследовании обычно наблюдается обратный кровоток в течение диастолы, а на ЭЭГ выявляется замедление и низкая амплитуда коррелирующие с недостатком перфузии мозга.
Лечение повышенного ВЧД, независимо от причины, включает обязательное исключение всех факторов, таких как болезненные стимулы, которые могут транзиторно повысить ВЧД. Следует ограничить кристаллоидные растворы до 60-70% от возрастной нормы и избегать гипоосмотических жидкостей. Следует быстро восстановить адекватную циркуляцию, при необходимости с помощью объемозамещающих растворов и вазопрессорных препаратов, таких как допамин (10-20 мкг/кг/мин); затем следует поддерживать кровообращение с помощью более низких доз (2 мкг/кг/мин). Следует проводить интенсивное лечение судорог, которые приводят к вторичному ухудшению.
Вероятно, целесообразно назначение маннитола (0,25-2 мг/кг в 20% растворе) болюсно в течение 10-15 минут на раннем этапе лечения. Этот препарат имеет высокую эффективность в снижении ВЧД; максимальное действие наступает в течение 30 минут, эффект длится от двух до шести часов. Длительное применение может сопровождаться рикошетной внутричерепной гипертензией и усилением вазогенного отека (Kaufmann и Cardoso, 1992), поэтому вместо регулярных доз без мониторинга, предпочительнее нерегулярное использование небольших доз (0,25 мг/кг) в ответ на острые повышения ВЧД. Некоторые авторы рекомендуют более высокие дозы (Cruz et al., 2004).

Гипервентиляция вызывает церебральную вазоконстрикцию и уменьшает объем крови в мозге, по крайней мере, в начальной стадии. Влияние длительной гипервентиляции является спорным, так как вазоконстриктивный эффект может исчезать, а гемодинамика у бессознательного пациента часто нарушена так, что уменьшение СО2 может сопровождаться повышением мозгового кровотока (Kirkham, 1991). Гипервентиляция со снижением рСО2
Редактор: Искандер Милевски. Дата публикации: 31.12.2018
Отек головного мозга, причины и последствия появления которого мы будем рассматривать в данной статье, – это реакция организма на чрезмерные нагрузки, травмы и инфекции. Как правило, этот процесс происходит довольно быстро. При этом сами клетки и пространство между ними заполняется избыточным количеством жидкости, а мозг в результате увеличивается в объеме, что, в свою очередь, вызывает повышение внутричерепного давления, ухудшение мозгового кровообращения и влечет за собой отмирание клеток.
Такое состояние, как вы понимаете, требует обязательной и неотложной медицинской помощи, чтобы избежать тяжелых последствий и летального исхода.
Причины возникновения отека
Вызвавшие отек мозга причины могут оказаться разными и крыться, например, в нарушении мозгового кровообращения, выраженного ишемическим или геморрагическим инсультом, в черепно-мозговой травме, в наличии внутричерепной раковой опухоли или метастаз от опухолей любой локализации.
Воспалительные процессы в мозге или его оболочке (менингит или энцефалит), переломы свода черепа с повреждением мозгового вещества, а также общие заболевания в виде тяжелых инфекций, сердечно-сосудистых патологий или обширных ожогов также могут вызывать отеки мозга.
Кроме того, спровоцировать развитие данной патологии может даже сильная аллергическая реакция в стадии анафилактического шока или наркотическая и алкогольная интоксикация.
В чем основная опасность отека
Отек любых тканей в человеческом организме – это довольно частое и вполне закономерное явление, которое, как правило, проходит без особых последствий. Но мозг находится в ограниченном пространстве, в плотной черепной коробке, которая не может увеличить свой объем под давлением его тканей.
Каковы бы ни были вызывающие отек мозга причины, они в итоге приводят к тому, что возникает сдавливание его вещества в узком пространстве. А это обстоятельство влечет за собой самую большую опасность: ишемия нейронов усугубляется, усиливается прогрессирование отека, и в какой-то момент утрачиваются функции мозга.

Отек головного мозга при инсульте: чем он вызывается
Одной из распространенных причин возникновения упомянутого отека у больного является перенесенный им геморрагический или ишемический инсульт. К сожалению, эти виды нарушения кровообращения практически всегда сопровождаются описываемой проблемой, выраженной в той или иной степени и являющейся своеобразным индикатором тяжести патологического процесса.
Ишемический инсульт вызывается затруднением поступления крови к отдельным участкам мозга в результате закупорки сосудов по той или по иной причине, что провоцирует кислородное голодание, гибель клеток и, как следствие, отек мозга.
А при геморрагическом инсульте происходит кровоизлияние под оболочку мозга, которое становится толчком для стремительного повышения внутричерепного давления и, соответственно, вызывает отек головного мозга. Причины данного вида инсульта, как правило, одинаковы – высокое артериальное давление, стресс, физическое усилие, вызывающие разрыв кровеносных сосудов в мозге или просачивание крови сквозь их стенки.
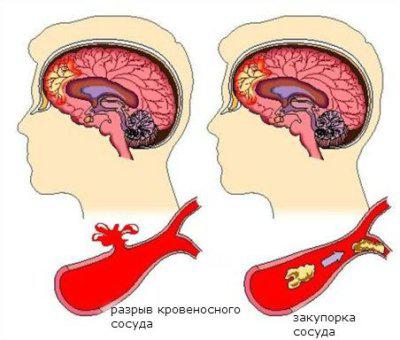
Как происходит развитие отека при инсульте
Вначале отек вызывается нарушением обмена веществ (метаболизма) в пораженном участке. В медицине подобное явление называют цитотоксическим отеком мозга, и он локализуется в основном в сером веществе. Спустя шесть часов к упомянутой патологии присоединяется вазогенный отек, локализующийся уже в белом веществе мозга. Его вызывает процесс так называемого пропотевания жидкости и белков из мелких сосудов во внеклеточное пространство, вызванный замедлением кровотока или его стазом (остановкой).
Одновременно с названными отеками мозга развивается и некроз, который приводит к накапливанию в межклеточном пространстве осмотически активных веществ, которые вызывают еще больший выход жидкости из капилляров.
Отек головного мозга при инсульте развивается очень быстро и спонтанно, при этом он может располагаться в очаге поражения (локальный отек), в одном полушарии (диффузный отек) и в обоих полушариях (генерализованный отек). Очень важно заметить его признаки и вовремя принять меры, хотя, конечно, при инсульте определить развитие отека довольно трудно, так как больной, как правило, находится в состоянии замутненного сознания или в коме.
Признаки отека мозга
Независимо от того, как классифицируются вызвавшие отек мозга причины, его признаки нельзя назвать специфическими и, следовательно, определить наличие опасной патологии у пациента, ориентируясь только на них, довольно трудно.
В медицине их делят на три основных группы:
- признаки, связанные с повышением внутричерепного давления;
- признаки очаговых нарушений;
- признаки стволовой патологии.
Как правило, отек мозга (причины, последствия которого мы рассматриваем) сопровождается сильной головной болью, тошнотой и позывами на рвоту – эти симптомы можно отнести к признакам внутричерепной гипертензии.
Нарушения речи, зрения, слуха и осязания, проблемы с ориентацией в пространстве, а также парезы и параличи – это признаки очаговых нарушений.
При отеках мозга больные часто жалуются на одышку, у них нарушается дыхание, развивается ощущение сонливости, тревожности, повышается артериальное давление, развивается помутнение сознания, иногда сопровождаемое судорогами, – все это признаки стволового отека, требующие срочных реанимационных мероприятий.

Причины отека мозга у новорожденных
Отдельно стоит рассмотреть данную патологию у только что появившихся на свет детей. Вызывающие у них отек мозга причины чаще всего кроются в тяжелом течении родов у матери и родовой травме малыша. Но его могут спровоцировать и врожденные пороки развития или приобретенные заболевания. Абсцессы, опухоли, менингит, энцефалит, внутриутробная гипоксия – все это может вызвать отек мозга у грудничка.
Кстати, течение описываемой патологии у малышей выглядит несколько иначе, чем у взрослых, так как у их организма еще очень ограничены возможности поддержания тонуса сосудов, регуляции внутричерепного давления и ликвородинамики. Единственное спасение ребенка в такой ситуации состоит в особенностях соединения костей черепа, между которыми у него находится или мягкая хрящевая ткань, или зазор (роднички). Между прочим, эта анатомическая особенность оберегает малыша от сдавления и отека мозга, которым мог бы заканчиваться любой крик крохи.
Особенности симптомов отека мозга у грудничков
Отек головного мозга у новорожденных отличается молниеносным течением. В начале развития патологии малыш, как правило, становится вялым, сонным, у него могут появиться судороги, отключиться сознание. У некоторых детей, напротив, отек вызывает возбужденное состояние, выражающееся постоянным безостановочным плачем.
Родничок при этом набухает даже в спокойном состоянии, увеличивается объем головы, у малыша появляется рвота, поднимается температура.
У новорожденных с отеком мозга характерным признаком этой патологии является очень быстрое ухудшение общего состояния и, к сожалению, во многих случаях оно заканчивается летальным исходом.
Отек головного мозга: последствия
Чем раньше больному с данным диагнозом будет оказана квалифицированная медицинская помощь в полном объеме, тем выше его шансы на выздоровление. Но довольно часто восстановление оказывается лишь частичным - все зависит от тяжести патологического процесса.
Последствием иногда оказывается, например, развитие эпилепсии, вызванное нарушением кровоснабжения отдельных участков мозга. У пациента может повыситься внутричерепное давление, приводящее, в свою очередь, к постоянным головным болям, головокружениям, расстройствам сознания и даже к снижению навыков социальной коммуникации.
Если же отек был продолжительным, то следствием его может оказаться нарушение функций мозга и снижение умственных способностей человека.

Как проявляются последствия отека мозга у детей
Последствия рассматриваемого недуга у детей также могут оказаться серьезными и зависят от тяжести протекания заболевания.
К ним относят развитие ДЦП и гидроцефалии, эпилепсии, а также нарушения формирования внутренних органов.
Отек мозга у некоторых детей может спровоцировать проблемы с речью, а также с координацией движения. Перенесенная патология, к сожалению, вызывает у части пациентов нервно-психическую неустойчивость и задержку умственного развития.
Из сказанного выше ясно, что отек мозга у детей – это весьма серьезная патология, которая требует постоянного наблюдения ребенка невропатологом и педиатром, причем длительность его зависит от выраженности последствий перенесенного заболевания.
Отек головного мозга - это неспецифическая реакция на воздействие различных повреждающих факторов (травма, гипоксия, интоксикация и др.), выражающаяся в избыточном накоплении жидкости в тканях головного мозга и повышением внутричерепного давления. Являясь по существу защитной реакцией, отек головного мозга, при несвоевременной диагностике и лечении может стать основной причиной, определяющей тяжесть состояния больного и даже летального исхода.
Из этой статьи вы узнаете основные причины и симптомы отека головного мозга у детей, о том как проводится лечение отека головного мозга у детей и какие меры профилактики вы можете проводить чтобы оградить своего ребенка от этого заболевания.
Лечение отека головного мозга у детей
Лечебные мероприятия при поступлении пострадавшего в стационар, заключаются в максимально полном и быстром восстановлении основных жизненно важных функций. Это, прежде всего нормализация артериального давления (АД) и объема циркулирующей крови (ОЦК), показателей внешнего дыхания и газообмена, так как артериальная гипотония, гипоксия, гиперкапния относятся к вторичным повреждающим факторам усугубляющим первичное повреждение головного мозга.
Общие принципы интенсивной терапии больных с отеком головного мозга:
ИВЛ. Считается целесообразным поддерживать РаО2 на уровне 100-120 мм рт.ст. с умеренной гипокапнией (РаСО2 - 25-30 мм рт.ст.), т.е. проводить ИВЛ в режиме умеренной гипервентиляции. Гипервентиляция предотвращает развитие ацидоза, снижает ВЧД и способствует уменьшению внутричерепного объема крови. При необходимости применяют небольшие дозы миорелаксантов, не вызывающих полную релаксацию, чтобы иметь возможность заметить восстановление сознания, появления судорог или очаговые неврологические симптомы.
Осмодиуретики используются с целью стимуляции диуреза за счет повышения осмолярности плазмы, в результате чего жидкость из внутриклеточного и интерстициального пространства переходит в сосудистое русло. С этой целью применяют маннит, сорбит и глицерол. В настоящее время маннит относится к наиболее эффективным и распространенным препаратам в лечении отека мозга. Растворы маннита (10, 15 и 20%) обладают выраженным диуретическим эффектом, нетоксичны, не вступают в метаболические процессы, практически не проникают через ГЭБ и другие клеточные мембраны. Противопоказаниями к назначению маннита являются острый тубулярный некроз, дефицит ОЦК, тяжелая сердечная декомпенсация. Маннит высокоэффективен для кратковременного снижения ВЧД. При избыточном введении могут наблюдаться рецидивирующий отек головного мозга, нарушение водно-электролитного баланса и развитие гиперосмолярного состояния, поэтому требуется постоянный контроль осмотических показателей плазмы крови. Применение маннита требует одновременного контроля и восполнения ОЦК до уровня нормоволемии. При лечении маннитом необходимо придерживаться следующих рекомендаций:
- использовать наименьшие эффективные дозы;
- вводить препарат не чаще чем каждые 6-8 часов;
- поддерживать осмолярность сыворотки ниже 320 м Осм/л.
Суточная доза маннита для детей грудного возраста - 5-15 г, младшего возраста - 15-30 г, старшего возраста - 30-75 г. Диуретический эффект выражен очень хорошо, но зависит от скорости инфузии, поэтому расчетная доза препарата должна быть введена за 10-20 мин. Суточную дозу (0,5-1,5 г сухого вещества/кг) необходимо разделить на 2-3 введения.
Сорбит (40% раствор) обладает относительно непродолжительным действием, диуретический эффект выражен не так сильно, как у маннита. В отличие от маннита сорбит метаболизируется в организме с продукцией энергии эквивалентно глюкозе. Дозы такие же, как у маннита.
Глицерол - трехатомный спирт - повышает осмолярность плазмы и благодаря этому обеспечивает дегидратирующий эффект. Глицерол нетоксичен, не проникает через ГЭБ и в связи с этим не вызывает феномена отдачи. Используется внутривенное введение 10% глицерола в изотоническом растворе натрия хлорида или пероральное (при отсутствии патологии желудочно-кишечного тракта). Начальная доза 0,25 г/кг; остальные рекомендации такие же как у маннита.
После прекращения введения осмодиуретиков часто наблюдается феномен "отдачи" (из-за способности осмодиуретиков проникать в межклеточное пространство мозга и притягивать воду) с повышением ликворного давления выше исходного уровня. В определенной степени предотвратить развитие этого осложнения можно с помощью инфузии альбумина (10-20%) в дозе 5-10 мл/кг/сут.
Салуретики оказывают дегидратирующее действие путем торможения реабсорбции натрия и хлора в канальцах почек. Их преимущество заключается в быстром наступлении действия, а побочными эффектами являются гемоконцентрация, гипокалиемия и гипонатриемия. Используют фуросемид в дозах 1-3 (в тяжелых случаях до 10) мг/кг несколько раз в день для дополнения эффекта маннита. В настоящее время имеются убедительные данные в пользу выраженного синергизма фуросемида и маннита.
Кортикостероиды. Механизм действия до конца не изучен, возможно развитие отека тормозится благодаря мембраностабилизирующему эффекту, а также восстановлению регионарного кровотока в области отека. Лечение следует начинать как можно раньше и продолжать не менее недели. Под влиянием кортикостероидов нормализуется повышенная проницаемость сосудов головного мозга.
Дексаметазон назначается по следующей схеме: начальная доза 2 мг/кг, через 2 часа -1 мг/кг, затем каждые 6 часов в течение суток - 2 мг/кг; далее 1 мг/кг/сут в течение недели. Наиболее эффективен при вазогенном отеке мозга и неэффективен - при цитотоксическом.
Барбитураты уменьшают выраженность отека мозга, подавляют судорожную активность и тем самым повышают шансы на выживание. Нельзя применять их при артериальной гипотензии и не восполненном ОЦК. Побочными эффектами являются гипотермия и артериальная гипотензия вследствие уменьшения общего периферического сопротивления сосудов, предупредить которое можно введением допамина. Уменьшение ВЧД в результате замедления скорости метаболических процессов в мозге находится в прямой зависимости от дозы препарата. Прогрессивное снижение метаболизма отражается на ЭГГ в виде уменьшения амплитуды и частоты биопотенциалов. Таким образом, подбор дозы барбитуратов облегчается в условиях постоянного ЭЭГ - мониторинга. Рекомендуемые начальные дозы - 20-30 мг/кг; поддерживающая терапия - 5-10 мг/кг/сут. Во время внутривенного введения больших доз барбитуратов больные должны находиться под постоянным и тщательным наблюдением. В дальнейшем у ребенка могут наблюдаться симптомы медикаментозной зависимости (синдром "отмены"), выражающиеся перевозбуждением и галлюцинациями. Обычно они сохраняются не более 2-3 дней. Для уменьшения этой симптоматики можно назначить небольшие дозы седативных препаратов (диазепам - 0,2 мг/кг, фенобарбитал - 10 мг/кг).
Гипотермия снижает скорость обменных процессов в мозговой ткани, оказывает защитное действие при ишемии мозга и стабилизирующее действие на ферментные системы и мембраны. Гипотермия не улучшает кровотока и даже может снижать его за счет увеличения вязкости крови. Кроме того, она способствует повышению восприимчивости к бактериальной инфекции.
Для безопасного применения гипотермии необходимо блокировать защитные реакции организма на охлаждение. Поэтому охлаждение необходимо проводить в условиях полной релаксации с применением медикаментозных средств, предупреждающих появление дрожи, развитие гиперметаболизма, сужение сосудов и нарушение сердечного ритма. Этого можно достичь с помощью медленного внутривенного введения нейролептиков, например аминазина в дозе 0,5-1,0 мг/кг.
Для создания гипотермии голову (краниоцеребральная) или тело (общая гипотермия) обкладывают пузырями со льдом, обертывают влажными простынями. Еще более эффективно охлаждение вентиляторами или с помощью специальных аппаратов.
Кроме вышеперечисленной специфической терапии должны проводиться мероприятия, направленные на поддержание адекватной перфузии головного мозга, системной гемодинамики, КОС и водно-электролитного равновесия. Желательно поддерживать рН на уровне 7,3-7,6, а РаО2 на уровне 100-120 мм рт.ст.
В некоторых случаях в комплексной терапии используются препараты, нормализующие тонус сосудов и улучшающие реологические свойства крови (кавинтон, трентал), ингибиторы протеолитических ферментов (контрикал, гордокс), препараты, стабилизирующие клеточные мембраны и ангиопротекторы (дицинон, троксевазин, аскорутин).
Средства лечения отека головного мозга у детей
С целью нормализации метаболических процессов в нейронах головного мозга используются ноотропы - ноотропил, пирацетам, аминалон, церебролизин, пантогам.
Течение и исход во многом зависит от адекватности проводимой инфузионной терапии. Развитие отека головного мозга всегда опасно для жизни больного. Отек или сдавление жизненно важных центров ствола является наиболее частой причиной смертельного исхода. Сдавление ствола мозга чаще встречается у детей старше 2 лет, т.к. в более раннем возрасте есть условия для естественной декомпрессии за счет увеличения емкости субарахноидального пространства, податливости швов и родничков. Одним из возможных исходов отека является развитие постгипоксической энцефалопатии с декортикационным или децеребрационным синдромом. К неблагоприятному прогнозу относится исчезновение спонтанной активности на ЭЭГ. В клинике - тонические судороги типа децеребрационной ригидности, рефлекс орального автоматизма с расширением рефлексогенной зоны, появление угасших по возрасту рефлексов новорожденных.
Большую угрозу представляют специфические инфекционные осложнения - менингит, энцефалит, менинго-энцефалит, которые резко отягощают прогноз.
Симптомы отека головного мозга у детей
Можно выделить несколько групп детей с высокой степенью риска развития ОГМ. Это, прежде всего, дети раннего возраста от 6 месяцев до 2 лет, особенно с неврологической патологией. Эцефалитические реакции и отек мозга также чаще отмечены у детей с аллергической предрасположенностью.
В большинстве случаев бывает крайне сложно дифференцировать клинические признаки отека головного мозга и симптомы основного патологического процесса. Начинающийся отек мозга можно предположить, если есть уверенность, что первичный очаг не прогрессирует, а у больного появляется и нарастает отрицательная неврологическая симптоматика (появление судорожного статуса и на этом фоне угнетение сознания вплоть до коматозного).
Все симптомы отека головного мозга можно разделить на 3 группы:
- симптомы, характерные для повышения внутричерепного давления (ВЧД);
- диффузное нарастание неврологической симптоматики;
- дислокация мозговых структур.
Клиническая картина, обусловленная повышением ВЧД, имеет различные проявления в зависимости от скорости нарастания. Увеличение ВЧД обычно сопровождается следующими симптомами: головная боль, тошнота и/или рвота, сонливость, позже появляются судороги. Обычно впервые появившиеся судороги имеют клонический или тонико-клонический характер; для них характерны сравнительная кратковременность и вполне благоприятный исход. При длительном течении судорог или их частом повторении нарастает тонический компонент и усугубляется бессознательное состояние. Ранним объективным симптомом повышения ВЧД является полнокровие вен и отек дисков зрительного нерва. Одновременно или несколько позже появляются рентгенологические признаки внутричерепной гипертензии: усиление рисунка пальцевых вдавлений, истончение костей свода.
При быстром увеличении ВЧД головная боль носит характер распирающей, рвота не приносит облегчения. Появляются менингеальные симптомы, повышаются сухожильные рефлексы, возникают глазодвигательные расстройства, увеличение окружности головы (до второго года жизни), подвижность костей при пальпации черепа из-за расхождения его швов, у грудных детей - открытие закрывшегося ранее большого родничка, судороги.
Синдром диффузного нарастания неврологической симптоматики отражает постепенное вовлечение в патологический процесс вначале корковых, затем подкорковых и в конечном итоге стволовых структур мозга. При отеке полушарий мозга нарушается сознание, и появляются генерализованные, клонические судороги. Вовлечение подкорковых и глубинных структур сопровождается психомоторным возбуждением, гиперкинезами, появлением хватательных и защитных рефлексов, нарастанием тонической фазы эпилептических пароксизмов.
Дислокация мозговых структур сопровождается развитием признаков вклинения: верхнего - среднего мозга в вырезку мозжечкового намета и нижнего - с ущемлением в большом затылочном отверстии (бульбарный синдром). Основные симптомы поражения среднего мозга: потеря сознания, одностороннее изменение зрачка, мидриаз, страбизм, спастический гемипарез, часто односторонние судороги мышц разгибателей. Острый бульбарный синдром свидетельствует о претерминальном повышении внутричерепного давления, сопровождающемся падением артериального давления, урежением сердечного ритма и снижением температуры тела, гипотонией мышц, арефлексией, двусторонним расширением зрачков без реакции на свет, прерывистым клокочущим дыханием и затем его полной остановкой.
Причины отека головного мозга у детей
Отек мозга встречается при черепно-мозговых травмах (ЧМТ), внутричерепных кровоизлияниях, эмболии мозговых сосудов, опухолях мозга. Кроме того, различные заболевания и патологические состояния, приводящие к церебральной гипоксии, ацидозу, нарушениям мозгового кровотока и ликвородинамики, изменениям коллоидно-осмотического и гидростатического давления и кислотно-основного состояния также могут привести к развитию ОГМ.
Возникновение отека головного мозга
В патогенезе отека головного мозга выделяют 4 основных механизма:
Является следствием воздействия токсинов на клетки мозга, в результате чего наступает расстройство клеточного метаболизма и нарушение транспорта ионов через клеточные мембраны. Процесс выражается в потере клеткой главным образом калия, и замене его натрием из внеклеточного пространства. При гипоксических состояниях пировиноградная кислота восстанавливается до молочной, что вызывает нарушение ферментных систем, ответственных за выведение натрия из клетки - развивается блокада натриевых насосов. Мозговая клетка, содержащая повышенное количество натрия, начинает усиленно накапливать воду. Содержание лактата выше 6-8 ммоль/л в оттекающей от мозга крови свидетельствует об его отеке. Цитотоксическая форма отека всегда генерализована, распространяется на все отделы, включая стволовые, поэтому достаточно быстро (в течение нескольких часов) возможно развитие признаков вклинения. Встречается при отравлениях, интоксикациях, ишемии.
Развивается в результате повреждения тканей головного мозга с нарушением гематоэнцефалического (ГЭБ) барьера. В основе данного механизма развития отёка мозга лежат следующие патофизиологические механизмы: повышение проницаемости капилляров; повышение гидростатического давления в капиллярах; накопление жидкости в интерстициальном пространстве. Изменение проницаемости капилляров головного мозга происходит в результате повреждения клеточных мембран эндотелия. Нарушение целостности эндотелия является первичным, из-за непосредственной травмы, или вторичным, вследствие действия биологически активных веществ, таких как брадикинин, гистамин, производные арахидоновой кислоты, гидроксильные радикалы, содержащие свободный кислород. При повреждении стенки сосуда плазма крови вместе с содержащимися в ней электролитами и белками переходит из сосудистого русла в периваскулярные зоны мозга. Плазморрагия, повышая онкотическое давление вне сосуда, способствует повышению гидрофильности мозга. Наиболее часто наблюдается при ЧМТ, внутричерепных кровоизлияниях и т.д.
Проявляется при изменении объема мозговой ткани и нарушения соотношения притока и оттока крови. Вследствие затруднения венозного оттока повышается гидростатическое давление на уровне венозного колена сосудистой системы. В большинстве случаев причиной является сдавление крупных венозных стволов развивающейся опухолью.
Образуется при нарушении существующего в норме небольшого осмотического градиента между осмолярностью ткани мозга (она выше) и осмолярностью крови. Развивается вследствие водной интоксикации ЦНС за счет гиперосмолярности мозговой ткани. Встречается при метаболических энцефалопатиях (почечная и печеночная недостаточность, гипергликемия и др.).
Диагностика отека головного мозга у детей
По степени точности методы диагностики отека головного мозга можно разделить на достоверные и вспомогательные. К достоверным методам относятся: компьютерная томография (КТ), ядерно-магнитно-резонансная (ЯМР) томография и нейросонография у новорожденных и детей до 1 года.
Компьютерная томография отека головного мозга
Наиболее важным методом диагностики является КТ, которая помимо выявления внутричерепных гематом и очагов ушибов позволяет визуализировать локализацию, распространенность и выраженность отека мозга, его дислокацию, а также оценивать эффект лечебных мероприятий при повторных исследованиях. ЯМР-томография дополняет КТ, в частности, в визуализации мелких структурных изменений при диффузном повреждении. ЯМР-томография также позволяет дифференцировать различные виды отека мозга, а, следовательно, правильно строить лечебную тактику.
Вспомогательные методы включают: электроэнцефалографию (ЭЭГ), эхоэнцефалографию (Эхо-ЭГ), нейроофтальмоскопию, церебральную ангиографию, сканирование мозга с помощью радиоактивных изотопов, пневмоэнцефалографию и рентгенологическое исследование.
У больного с подозрением на отек головного мозга должно быть проведено неврологическое обследование, основанное на оценке поведенческих реакций, вербально-акустических, болевых и некоторых других специфических ответов, в том числе глазных и зрачковых рефлексов. Дополнительно могут быть проведены более тонкие пробы, например, вестибулярные.
При офтальмологическом исследовании отмечается отек конъюнктивы, повышение внутриглазного давления, отек диска зрительного нерва. Проводится УЗИ черепа, рентгеновские снимки в двух проекциях; топическая диагностика при подозрении на объемный внутричерепной процесс, ЭЭГ и компьютерная томография головы. ЭЭГ целесообразна при выявлении судорог у больных с отеком мозга, у которых судорожная активность проявляется на субклиническом уровне или подавлена действием миорелаксантов.
Дифференциальная диагностика отека головного мозга
Дифференциальную диагностику отека головного мозга проводят с патологическими состояниями, сопровождающимися судорожным синдромом и комой. К ним относятся: травматическое повреждение мозга, тромбоэмболии мозговых сосудов, метаболические расстройства, инфекция и эпилептический статус.
Читайте также:


