Паранеопластический энцефалит что это
Рассмотрены этиопатогенез паранеопластических синдромов (ПНС), способы диагностики, клинические варианты ПНС, подходы к лечению больных. Важную роль в лечении ПНС играет детский невролог, вначале инициируя поиск опухоли, а по окончанию ее терапии корректи
Aetiopathogenesis of paraneoplastic syndromes (PNS) was considered, as well as ways of diagnostics, clinical variations of PNS, approaches to the patients treatment. A children's neurologist plays an important role in PNS treatment, at first initiating the tumor search, and correcting neurological consequences after finishing its therapy.
M. Пранцателли. Паранеопластические синдромы: нераскрытое убийство [5]
Паранеопластические синдромы (ПНС) — это страдание органов, удаленных от места новообразования и его метастазов, не связанное с инфекцией, ишемией или метаболическими нарушениями [1]. Кахексия, гиперкальциемия, синдром Кушинга, синдром Труссо возникают потому, что опухоль секретирует вещества, похожие на гормоны, или вызывает перекрестные аутоиммунные реакции между опухолевой и нормальной тканью. ПНС поражают эндокринные железы, нервную систему, кожу, кровь (табл. 1), изолированно или сочетанно [2].
Наиболее драматичным течением обладают ПНС, поражающие центральную и периферическую нервную систему, нервно-мышечные синапсы и мышцы. Может страдать один отдел (как при лимбическом энцефалите) или один тип клеток (клетки Пуркинье в мозжечке), а может возникать многоуровневое поражение (энцефаломиелополиневропатия). ПНС сопровождают примерно 200 видов опухолей, имеющих разное происхождение и удаленность от неврологического очага, чаще локализующихся в грудной или брюшной полости.
Симптомы ПНС иногда развиваются настолько быстро, что ошибочно трактуются как инсульт. У 50% пациентов ПНС раньше дает о себе знать, чем опухоль. Течение процесса может быть монофазным (симптомы достигают плато, а затем наступает улучшение или стабилизация) или неуклонно прогрессирующим. Описаны случаи, когда опухоль обнаруживают спустя несколько лет после развития неврологических симптомов. Часто именно ПНС заставляют пациента обратиться к врачу. Диагностика осложняется тем, что ПНС не патогномоничны только для опухолей [1].
Клетки опухоли (тимома, мелкоклеточный рак легкого, рак молочной железы и яичников; у детей — нейробластома) экспрессируют онконевральные антигены, которые в норме встречаются в иммунологически привелигированных областях — нервной системе и яичках. Открытие онконевральных антител в 1965 г. привело к широко распространенной в настоящее время гипотезе, что ПНС — иммунологическое расстройство. Предположительно, сходство антигенов опухоли и нервной ткани приводит к потере толерантности и индукции иммунного ответа как против опухоли, так и против нормальных нейронов. Антитела к антигенам опухоли начинают атаковать ядра нейронов, структурные элементы, поверхностные рецепторы, синапсы и ионные каналы [3].
Лучший способ диагностики ПНС — выявление известных антионконевральных белков в сыворотке пациента. Эти антитела специфичны (> 90%) для опухолей, поэтому возможна диагностика рака на доклинической стадии. Например, антитела Tr выявляются только при лимфоме и мозжечковой дегенерации. VGCC-антитела (к мембранным каналам) вырабатываются при миастеническом синдроме Ламберта–Итона [4]. Однако у 30% пациентов антитела не выявляются, а у 5–10% антитела атипичные или обнаруживаются при разных ПНС. Отсутствие антител не исключает ПНС [1].
Являются ли онконевральные антитела причиной лизиса клеток? На животных моделях не удалось воспроизвести неврологические нарушения путем активной иммунизации или пассивной передачи, даже интратекально. В ответ на иммунизацию у животных вырабатываются сывороточные антитела, но неврологические симптомы не появляются. Таким образом, онконевральные антитела, возможно, только указывают на аутоиммунный процесс, но не вызывают его. Существует гипотеза, что важную роль в патогенезе ПНС играют клеточные иммунные механизмы, но ее тоже не удалось воспроизвести на животной модели. Таким образом, аутоиммунную гипотезу ПНС еще предстоит доказать [5].
Паранеопластический энцефаломиелит
Паранеопластический энцефаломиелит характеризуется одновременным поражением различных областей центральной нервной системы (гиппокамп, ствол мозга, спинной мозг, спинно-мозговые ганглии). Клиническая картина соответственно очагам включает: лимбический энцефалит, альтернирующие синдромы, вегетативные нарушения, миелит, мозжечковую дегенерацию, сенсорную невропатию. Реже встречаются паркинсонизм, хорея, оромандибулярная дистония, нейрогенная гиповентиляция. Вегетативные синдромы (ортостатическая гипотензия, сухость во рту, задержка мочи, зрачковые нарушения, импотенция) встречаются в 30% случаев [1–3].
Лимбический энцефалит
Лимбический энцефалит характеризуется подострым началом в виде спутанного сознания с грубым снижением кратковременной памяти. Нередки судороги, которые могут опережать развитие когнитивного дефицита на несколько месяцев. У части пациентов дебютным проявлением служит не эпилепсия с деменцией, а депрессия с тревогой и галлюцинозом. Типичны синдромы поражения гипоталамуса (сонливость, гипертермия, эндокринопатии) и среднего мозга. Лимбический энцефалит вызывают мелкоклеточный рак легкого (50%), опухоли яичка (20%), рак молочной железы (8%). Антитела можно выявить у 50% пациентов. В спинномозговой жидкости выявляется плеоцитоз и повышение содержание белка. Данные магнитно-резонансной томографии (МРТ), как правило, соответствуют норме, но иногда наблюдается изменение сигнала в одной или обеих височных долях медиально. Морфологические изменения в лимбической системе и базальных ганглиях включают: апоптоз нейронов, реактивность микроглии, периваскулярную лимфоцитарную инфильтрацию. Дифференциальный диагноз следует проводить с протекающим более остро герпетическим энцефалитом, в том числе после трансплантации костного мозга, успешно лечащимся в первые часы заболевания [6].
Паранеопластическая мозжечковая дегенерация
Паранеопластическая мозжечковая дегенерация характеризуется быстрым развитием тяжелой атаксии из-за гибели большого числа клеток Пуркинье при относительной сохранности других нейронов мозжечка. Данные компьютерной томографии (КТ) и МРТ-исследования сначала соответствуют норме, а позже выявляют грубую атрофию мозжечка. Дегенерация встречается при разных видах опухолей (рак молочной железы, яичника, лимфома), и при этом могут обнаруживаться различные антитела. Обычно заболевание дебютирует шаткой походкой и дизартрией, затем быстро прогрессирующая мозжечковая атаксия приковывает больного к постели. Смерть наступает от бульбарных нарушений. Патогномоничен нистагм, бьющий вниз. Большинство пациентов жалуются на головокружение, двоение в глазах, дисфагию. Симптоматика, как правило, симметрична. Анализ цереброспинальной жидкости обычно в норме, но его необходимо проводить для исключения метастазов в оболочки мозга, при которых также отмечается шаткость при ходьбе, стабилизирующаяся через несколько месяцев. Лечение неэффективно, даже если резецирована материнская опухоль [7].
Паранеопластический опсоклонус-миоклонус
Паранеопластический опсоклонус-миоклонус наблюдается в трех случаях: 1) у детей с нейробластомой, 2) у взрослых женщин с Ri-антителами и раком молочной железы, 3) у взрослых пациентов без паранеопластических антител с мелкоклеточным раком легких. Симптомы включают опсоклонус (непроизвольные движения глаз), генерализованный миоклонус, мозжечковую атаксию, поведенческие нарушения — раздражительность, нарушения сна. Описано несколько специфических аутоантител, в частности, анти-Ri-антитела (при раке молочной железы, мелкоклеточном раке легкого), антитела к нейрофиламентам у детей с нейробластомой.
Нейробластома — самая частая солидная опухоль у детей. 50% случаев заболевания подвергаются самостоятельному регрессу. Метастазы редки. Морфологические изменения включают апоптоз клеток Пуркинье, атрофию нижних олив, нижних отделов ствола или верхних шейных сегментов мозга. Иногда морфологических изменений не находят. Специфическим паранеопластическим процессом у детей с нейробластомой является опсоклонус-миоклонус. Он остро дебютирует в возрасте до 4 лет — походка становится шаткой, ребенок начинает часто падать, иногда из-за тяжести атаксии даже перестает ходить. Также возникают слюнотечение, опсоклонус, раздражительность, диссомния. Лечение опсоклонуса-миоклонуса — резекция опухоли и иммунотерапия. Если опухоль продолжает расти, неврологические симптомы прогрессируют, несмотря на иммунотерапию. Но даже при успешном лечении нейробластомы большинство детей инвалидизируются из-за нарушений поведения и задержки психоречевого развития. У них сохраняются также диссомния и вспышки агрессии. Существует гипотеза, что развитие опсоклонус-миоклонуса у детей помогает иммунной системе. У многих пациентов выявляют антитела, которые реагируют с поверхностными антигенами нейронов. Известные в настоящее время методы лечения являются неспецифическими и включают нецитостатические и цитотоксические препараты, внутривенные иммуноглобулины, плазмаферез и адсорбцию антител. Также применяют резекцию опухоли и тимэктомию. Сочетание этих методов позволяют снизить дозировку кортикостероидов. Остается проблема оптимизации схемы иммунотерапии [7, 8].
Ниже приведен клинический пример, иллюстрирующий течение заболевания, динамику параклинических исследований и терапию.
Проведенное обследование и лечение приведены в табл. 2 и 3.
В статусе (возраст 4 года 4 месяца): Вес 21,7 кг. Медикаментозный синдром Иценко–Кушинга. Легкое сходящее косоглазие. Мышечный тонус изменен по пластическому типу: в руках D > S, в ногах S > D. Ходит самостоятельно. Походка не нарушена. Сухожильные рефлексы средние S ≥ D. Умеренно выраженный интенционный тремор в левой руке при захвате предметов. Выполняет команды и инструкции, понимает обращенную речь, речь фразовая, отвечает на вопросы в плане заданного, знает основные цвета. (По шкале оценки двигательной функции при опсоклонус-миоклонус синдроме (M. R. Pranzatelli, 2002) — 2 балла, 1-я степень тяжести.)
Миелит и острая некротизирующая миелопатия
Миелит и острая некротизирующая миелопатия быстро прогрессирует. Морфологически выявляют обширный некроз белого и серого вещества, особенно в грудных сегментах [3].
Паранеопластическая ретинопатия при мелкоклеточном раке легкого
Симптомы обычно возникают с двух сторон и отражают одновременное повреждение колбочек и палочек. У пациентов отмечается фотосенситивность, снижение остроты зрения, нарушение цветового восприятия, кольцевые скотомы, никталопия (куриная слепота) и удлинение адаптации к темноте. Офтальмоскопия выявляет сужение артериол и пигментный ретинит, электроретинограмма — ослабление ответа на свет [1, 3].
Паранеопластическая ретинопатия при меланоме
Паранеопластическая ретинопатия при меланоме характеризуется другими симптомами. Острота зрения и цветовое зрение не нарушено, но развиваются внезапные мерцающие фотопсии, куриная слепота и легкое периферическое сужение полей зрения. Симптомы объясняются дисфункцией зрительных нервов, периферическая нервная система не страдает. Типичны антитела к биполярным клеткам сетчатки. Иногда отмечаются увеит, оптическая нейропатия или ретинопатия.
Синдром жесткого человека
Это редкий неврологический синдром, характеризующийся ригидностью мышц, чаще мышц туловища и проксимальных отделов нижних конечностей, которая возникает при совместном сокращении мышц-агонистов и антагонистов. Чувствительные раздражители вызывают болезненные крампи. Болезнь начинается с рук. Электромиография выявляет непрерывную активность двигательных единиц в пораженных мышцах в состоянии покоя. Это заболевание чаще имеет аутоиммунную природу (анти-GAD антитела у 70% больных). Паранеопластический вариант развивается при раке молочной железы, кишечника, легких, болезни Ходжкина, тимоме [1].
Синдромы двигательных нейронов
Сочетание бокового амиотрофического склероза и рака отмечается нередко [4]. Но является ли эта болезнь двигательного нейрона паранеопластическим процессом? На этот вопрос пока нет ответа. Периферическая нервная система часто страдает у онкологических больных, что проявляется моторными, сенсорными, вегетативными и смешанными невропатиями. Этиология полиневропатий при раке не обязательно паранеопластическая, чаще это метаболические, трофические, ятрогенные и токсические факторы. Паранеопластический вариант отличается быстрым нарастанием симптомов и плохим ответом на лечение.
Сенсорная невропатия
Хронические воспалительные демиелинизирующие полиневропатии
Хронические воспалительные демиелинизирующие полиневропатии имеют атипичное течение, резистентны терапии, быстро и драматично прогрессируют.
Паранеопластическая вегетативная невропатия
Данный вид невропатии проявляется панвегетативным синдромом (ортостатическая гипотензия, ангидроз, атония мочевого пузыря, патология зрачков, рвота и тошнота, нарушение саливации и слезоотделения) или псевдообструкцией кишечника.
Хроническая псевдообструкция кишечника
Хроническая псевдообструкция кишечника отмечается у пациентов с тимомой и мелкоклеточным раком легкого. Характерно снижение веса, хронические запоры и метеоризм в результате повреждения нейронов кишечного сплетения. Нарушение моторики пищевода приводит к дисфагии, тошноте и рвоте. Радиологические исследования показывают парез желудка, тонкой или толстой кишки. Манометрия пищевода выявляет спазмы или ахалазию. У некоторых пациентов выявляют антитела к нейронам вегетативных ганглиев, например к рецепторам ацетилхолина [1].
Миастенический синдром Ламберта–Итона
Миастенический синдром Ламберта–Итона является аутоиммунным заболеванием нервно-мышечного синапса, характеризуется слабостью мышц и трофическими нарушениями, преимущественно в нижних конечностях. 60% случаев являются паранеопластическими. В среднем в течение двух лет после установления диагноза выявляют мелкоклеточный рак легкого. На электромиограмме (ЭМГ) отмечается снижение потенциала нервно-мышечного синапса после стимуляции нерва с декрементом при низкой частоте стимуляции (3 Гц) более чем на 10%, прирост после стимуляции высокими частотами (более 20 Гц) более чем на 100%. Серологических маркеров не существует. Антитела присутствуют почти у всех пациентов, как при паранеопластической, так и при непаранеопластический форме. Может сочетаться с мозжечковой дегенерацией [4].
Myasthenia gravis
Myasthenia gravis является самым изученным аутоиммунным заболеванием, протекающим с повреждением постсинаптических рецепторов ацетилхолина в нервно-мышечном синапсе. Примерно в 10–15% случаев миастении выявляется тимома, и наоборот — примерно 30% пациентов с тимомой имеют миастению. Следовательно, миастению можно считать паранеопластическим процессом [5].
Нейромиотония
Нейромиотония — это мышечные спазмы, крампи, ригидность, миокимия. Дифференциальный диагноз проводят с синдромом Шегрена и интоксикацией цисплатином. Морфологически обнаруживают инфильтрацию вокруг нейронов спинномозговых ганглиев. ЭМГ-изменения характерны для миотонии. Заболевание связано с выработкой антител к калиевым каналам [4]. Мышцы при ПНС могут страдать с формированием симптомов полимиозита/дерматомиозита, острой некротизирующей миопатии.
Анализы крови и цереброспинальной жидкости, МРТ, ЭЭГ, ЭМГ редко подтверждают диагноз ПНС. Дифференциальный диагноз проводят с различными структурными повреждениями головного мозга, метастазами оболочек, аутоиммунными заболеваниями, синдромом Шегрена–Ларссона, а также с нейроинфекциями, васкулитами или гранулематозами ЦНС [1, 3].
В цереброспинальной жидкости находят умеренный плеоцитоз, небольшое повышение уровней белка и IgG. Наиболее важный диагностический критерий — специфические антитела в плазме крови и цереброспинальной жидкости, их выявление значительно облегчает поиск опухоли. К сожалению, почти у 50% больных с ПНС нет известных антител, а размеры опухоли могут быть меньше, чем пределы разрешения КТ. Оптимальным методом выявления опухоли в настоящее время является позитронная эмиссионная томография всего тела с фтордезоксиглюкозой.
Отсутствие антител и опухоли не исключает диагноз. Исследования необходимо повторять каждые 6 месяцев до установления диагноза, обычно в течение 2–3 лет. Большинство опухолей диагностируется в течение 4–6 месяцев. Риск выявления рака значительно уменьшается через два года после манифестации ПНС и становится очень низким через четыре года.
Лечение пациентов с ПНС проводят по двум направлениям: 1) резекция опухоли, 2) подавление иммунной реакции. Терапия зависит от вида паранеоплатического синдрома, опухоли и наличия антител. ПНС редко улучшается после иммуномодулирующего лечения, так как в большинстве случаев нейрональные структуры уже необратимо повреждены. Основная цель лечения — регресс опухоли. У некоторых пациентов отмечается улучшение при использовании внутривенных иммуноглобулинов, стероидов, ритуксимаба или плазмафереза [1].
Нервно-мышечные паранеопластические синдромы, особенно синдром Ламберта–Итона, имеют относительно благоприятный прогноз. ПНС с повреждением центральной нервной системы обычно быстро прогрессируют и не корректируются. Иногда состояние пациента улучшается после резекции опухоли. Тем не менее, согласно многочисленным публикациям, у пациентов с ПНС прогноз лучше, чем без него. Предположительно, это является не только результатом ранней диагностики рака, но следствием более сильного иммунного ответа на опухоль [1, 4].
ПНС у детей отличаются тем, что разрушают незрелый и развивающийся мозг. Если опухоль диагностируют, своевременное лечение рака приводит к длительной и стойкой ремиссии, но неврологические осложнения ПНС не всегда обратимы. Важную роль в лечении ПНС играет детский невролог, вначале инициируя поиск опухоли, а по окончанию ее терапии корректируя неврологические последствия [8]. Учитывая редкость данных состояний, эффект лечения маленького пациента зависит не только от эрудиции невролога, но и от его умения работать с клиницистами других специальностей.
Литература
М. Ю. Бобылова* , 1 , кандидат медицинских наук
Е. С. Ильина**
Е. Ст. Ильина***, кандидат медицинских наук
* ИДНЭ им. Свт. Луки,
** ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ,
*** ФГБУ РДКБ МЗ РФ, Москва
а) Терминология:
1. Синонимы:
• Паранеопластические синдромы (ПС), паранеопластическая болезнь
2. Определение:
• Отдаленные неврологические эффекты рака, связанные с неопластическим процессом экстра-ЦНС локализации:
о Наиболее частая опухоль: мелкоклеточный рак легкого
• Лимбический энцефалит (ЛЭ) является наиболее частым клиническим паранеопластическим синдромом:
о Единственный ПС с четкими томографическими признаками
1. Общие характеристики паранеопластических синдромов:
• Лучший диагностический критерий:
о Лимбический энцефалит: повышение интенсивности сигнала от медиальных отделов височных долей, структур лимбической системы:
- Визуализационная картина такая же, как и при герпетическом энцефалите, однако характерно иное клиническое течение (подострая/хроническая стадия)
о При первичном исследовании в 20-40% изменения не наблюдаются
• Локализация изменений при ЛЭ: гиппокамп, миндалина мозжечка, поясная извилина, пириформная кора, субфронтальная кора, островок
2. КТ при паранеопластическом синдроме:
• Бесконтрастная КТ: при первичной КТ в > 95% случаев изменения не наблюдаются:
о Снижение плотности медиальных отделов височных долей (редко)
• КТ с контрастированием: обычно контрастирование не наблюдается
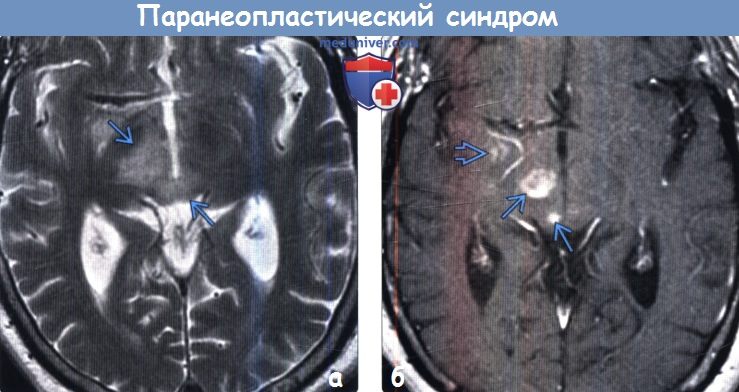
(а) МРТ, Т2-ВИ, аксиальный срез: в среднем мозге определяется гиперинтенсивная зона, отражающая стволовой энцефалит, который характеризуется появлением гиперинтенсивных зон в среднем мозге, мосте, ножках мозжечка и базальных ганглиях.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у того же пациента определяется фрагментарное контрастирование зон поражения в среднем мозге и медиальных отделах височной доли. Данному пациенту с новыми стволовыми симптомами был поставлен диагноз лимбический энцефалит. У одного и того же пациента возможно развитие нескольких паранеопластических синдромов.
3. МРТ при паранеопластическом синдроме:
• Т1-ВИ:
о Снижение интенсивности сигнала от медиальных отделов височных долей (гиппокамп, миндалевидное тело), островка, поясной извилины, субфронтальной коры, белого вещества (БВ) нижних отделов лобной доли о Возможно выявление минимального масс-эффекта
о Возможно выявление атрофии при хроническом течении
о Отсутствие кровоизлияний
• ДВИ:
о Ограничение диффузии наблюдается редко
• Т2-ВИ: повышение интенсивности сигнала от медиальных отделов височных долей (гиппокамп, миндалевидное тело), островка, поясной извилины, субфронтальной коры, белого вещества (БВ) нижних отделов лобной доли:
о Возможно выявление минимального масс-эффекта
• FLAIR: повышение интенсивности сигнала от медиальных отделов височных долей, островка, поясной извилины, субфронтальной коры, белого вещества (БВ) нижних отделов лобной доли
• Т2* GRE: отсутствие кровоизлияний:
о При визуализации продуктов распада крови предполагайте герпетический энцефалит
• Постконтрастные Т1-ВИ: часто наблюдается фрагментарный характер контрастирования
• Стволовой энцефалит: зоны гиперинтенсивного сигнала в среднем мозге, мосте, ножках мозжечка, базальных ганглиях
• Паранеопластическая мозжечковая дегенерация (ПМД): атрофия мозжечка
4. Радионуклидная диагностика:
• ПЭТ с ФДГ: гиперметаболизм глюкозы в медиальных отделах височных долей у пациентов с ЛЭ
5. Рекомендации по визуализации:
• Советы по протоколу исследования:
о МРТ с получением постконтрастных Т1-ВИ, корональных Т2-ВИ или FLAIR-изображений
о Рассмотрите возможность повторной МРТ, если на фоне отсутствия изменений при первичном исследовании сохраняется высокое клиническое подозрение
в) Дифференциальная диагностика паранеопластического синдрома:
1. Герпетический энцефалит:
• Повышение интенсивности сигнала на Т2-ВИ от медиальных отделов височных долей, структур лимбической системы
• Часто наблюдается масс-эффект, ограничение диффузии
• Быстрое начало, лихорадочное состояние
• Титры ВПГ (вСМЖ, сыворотке) на ранних этапах заболевания могут быть отрицательными
• Возможные кровоизлияния на поздней острой/подострой стадии
• Может быть неотличим от лимбического энцефалита
2. Диффузная астроцитома низкой степени злокачественности (grade II):
• Одностороннее гиперинтенсивное объемное образование
• Могут поржаться медиальные отделы височной доли
• Характерно отсутствие контрастного усиления
3. Эпилептический статус:
• Судороги могут обусловливать аномальное изменения сигнальных характеристик на Т2-ВИ/FLAIR медиальных отделов височных долей
• Характерно контрастирование коры, ограничение диффузии в ее области
• Судорожный синдром в анамнезе
4. Глиоматоз головного мозга:
• Диффузный процесс, склонность к поражению лимбической системы отсутствует
• Гиперинтенсивные на Т2-ВИ зоны в нескольких смежных долях
• Увеличение объема пораженных структур
5. Паренхимальные метастазы:
• Обычно мультифокальное поражение, характерно накопление контраста
• Часто известна первичная опухоль
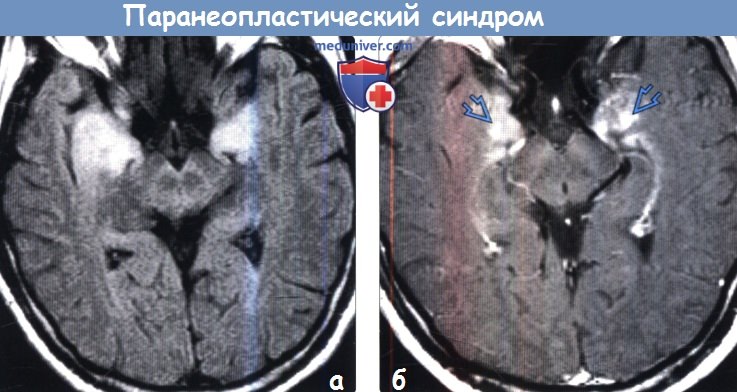
(а) MPT, FLAIR, аксиальный срез: аномальное двустороннее повышение интенсивности сигнала от медиальных отделов височных долей, что обусловлено лимбическим энцефалитом. Поскольку визуализационные признаки в этом случае имитируют герпетический энцефалит, большинству пациентов первоначально проводят противовирусную терапию до тех пор, пока титры ВПГ не окажутся отрицательными. Пара неопластический синдром развивается у менее 7 % пациентов с раковыми заболеваниями.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у этого же пациента определяется фрагментарное контрастирование медиальных отделов височных долей. Лимбический энцефалит является единственным паранеопластическим синдромом с четкими визуализационными признаками.
1. Общие характеристики:
• Этиология:
о Иммуноопосредованные механизмы развития (связаны с аутоантителами или цитотоксическими Т-клетками)
о У 60% пациентов имеются циркулирующие сывороточные аутоантитела:
- Анти-Hu (рак легких): лимбический энцефалит Анти-Та (герминогенные опухоли яичка): лимбический энцефалит, стволовой энцефалит
- Anti-Yo (молочная железа и яичники): паранеопластическая мозжечковая дегенерация
- Анти-Tr (лимфома Ходжкина): паранеопластическая мозжечковая дегенерация
- Anti-Ri (рак легких, молочной железы, яичников): опсоклонус-миоклонус синдром
о Обратимая экстралимбическая паранеопластическая энцефалопатия:
- Связана с раком молочной железы и легких
- Обратимая в условиях контроля над первичными опухолями
о Имеются сообщения о новых антигенах клеточной поверхности: потенциал-зависимые калиевые каналы (VGKC) и N-метил-D-аспартат-рецептор (NMDA-рецептор):
- Связаны с другими опухолями (тимомы, тератомы, лимфома Ходжкина)
- Являются антителоопосредуемыми и лучше реагируют на иммунотерапию (90%)
- Пациенты могут поступать в лечебные учреждения с лимбическим энцефалитом; часто возникают серьезные психические расстройства, судороги, дискинезии, расстройства вегетативной регуляции или гиповентиляция
о Новые антитела к рецептору амино-3-гидрокси-5-метил-4-и-зоксазол-пропионовой кислоты (АМРА-рецептор):
- Связаны с лимбическим энцефалитом
- Могут встречаться в сочетании с другими антителами
2. Стадирование и классификация паранеопластического синдрома:
• Паранеопластический синдром (ПС) подразделяют на поражение ЦНС, периферической НС, ЦНС/ ПНС, нервно-мышечного соединения:
о ЦНС: паранеопластическая мозжечковая дегенерация (ПМД), опсоклонус-миоклонус синдром, ретинопатия
о Периферическая НС: сенсомоторная нейропатия, вегетативная нейропатия
о Поражение как ЦНС, так и ПНС: энцефаломиелит (лимбический энцефалит, стволовой энцефалит, миелит, болезнь двигательного нейрона)
о Нервно-мышечное соединение: миастенический синдром Ламберта-Итона
• Лимбический энцефалит является наиболее частым паранеопластическим синдромом (ПС):
о Имеются сообщения о непаранеопластическом лимбическом энцефалите
• ПМД является вторым по распространенности паранеопластических синдромов (ПС)
• У одного и того же пациента возможно развитие нескольких паранеопластических синдромов (ПС)
3. Макроскопические и хирургические особенности:
• ЛЭ: плохо отграниченное от окружающих структур размягчение и изменение цвета серого вещества (СВ):
о Гиппокамп, поясная извилина, пириформная кора, лобная орбитальная поверхность височной доли, островок, миндалевидное тело; типично двустороннее поражение
• ПМД: атрофия мозжечка, истончение извилин
• Стволовой энцефалит: размягчение ствола мозга
4. Микроскопия:
• Лимбической энцефалит:
о Потеря нейронов, реактивный глиоз, периваскулярная лимфоцитарная инфильтрация, микроглиальные узелки
о Отсутствие новообразований и вирусных включений
• ПМД: потеря клеток Пуркинье, микроглиальная пролиферация, гиперплазия глии Бергмана, уменьшение числа зернистых клеток
• Стволовой энцефалит: периваскулярные воспалительные инфильтраты, глиальные узелки, нейронофагия
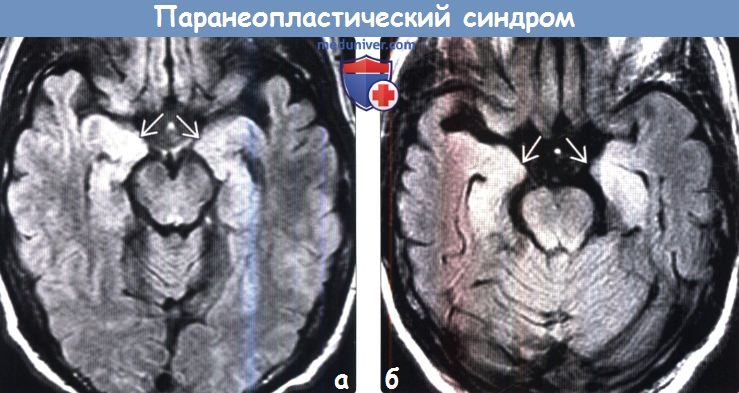
(а) МРТ, FAIR, аксиальный срез: у молодого пациента с меланомой и подострой деменцией определяется легкое асимметричное повышение интенсивности сигнала от гиппокампов.
(б) МРТ, FAIR, аксиальный срез: у пациента с подострой деменцией и аутоиммунной реакцией против потенциалзависимых калиевых каналов (VGKC) определяется повышение интенсивности сигнала от медиальных отделов обеих височных долей. Аутоиммунная реакция против VGKC может возникать при отсутствии первичной опухоли или может представлять собой паранеопластический синдром, имитируя лимбический энцефалит. Данное состояние характеризуется хорошим ответом на иммунотерапию.
д) Клиническая картина:
1. Проявления паранеопластического синдрома:
• Наиболее частые признаки/симптомы:
о ЛЭ: потеря памяти, когнитивная дисфункции, деменция, психологические изменения (тревога, депрессия, галлюцинации), судороги; подострый характер проявлений
о ПМД: атаксия, дискоординация, дизартрия, нистагм:
- У пациентов возрастом > 50 лет мозжечковая дегенерация имеет паранеопластический генез в 50% случаев, часто предшествует развитию отдаленного злокачественного поражения
о Стволовой энцефалит: дисфункция стволовых структур, включая параличи черепных нервов, нарушения зрения
о У пациентов с известной первичной опухолью необходимо исключать другие осложнения:
- Метастазы, инфекция, нарушение обмена веществ, эффект химиотерапии
• Клинический профиль:
о У 60% пациентов с ПС при поступлении в лечебное учреждение в анамнезе может отсутствовать известная первичная опухоль, у многих из них опухоль при обследовании не выявляется
о Обнаружение антинейрональных антител в сыворотке или СМЖ облегчает диагностику паранеопластического синдрома (ПС) и первичной раковой опухоли
о Первичные новообразования:
- Лимбический энцефалит:
Наиболее часто: мелкоклеточный рак легкого
Другие = желудочно-кишечный тракт, мочеполовая система (яичники > почки > матка), лимфома, молочные железы, семенники, тимус, нейробластома (у детей)
У 90% пациентов имеет место положительные тесты СМЖ (плеоцитоз, ↑ белка, олигоклональные полосы)
Вовлечение височных долей по данным ЭЭГ
- Паранеопластическая мозжечковая дегенерация:
Мочеполовая система (яичники), молочные железы, легкие, лимфома
- Опсоклонус-миоклонус синдром:
Нейробластома, рак легкого
- Миастенический синдром Ламберта-Итона:
Мелкоклеточный рак легкого
2. Демография:
• Возраст: встречается в любом возрасте, чаще всего у взрослых
• Эпидемиология: у
Редактор: Искандер Милевски. Дата публикации: 7.4.2019
Читайте также:


