По деформирующему остеоартрозе болевой синдром связан
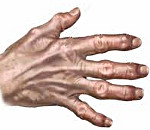
Деформирующий остеоартроз – прогрессирующее дистрофическое изменение костных суставов с первичным повреждением хрящевых тканей и последующей дегенерацией всего комплекса костно-суставного аппарата. Деформирующий остеоартроз характеризуется артралгией, функциональной недостаточностью суставов и выраженными изменениями их формы. Фармакотерапия деформирующего остеоартроза направлена на замедление прогрессирования дегенеративных процессов, уменьшение боли и улучшение функционирования суставов; в некоторых случаях показано эндопротезирование суставов. Течение деформирующего остеоартроза медленно прогрессирующее с развитием анкилоза или патологической нестабильности сустава.
- Классификация
- Симптомы деформирующего остеоартроза
- Осложнения
- Диагностика
- Лечение деформирующего остеоартроза
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Деформирующий остеоартроз - частая патология суставов, при которой нарушение регенерации соединительнотканных структур приводит к преждевременному старению суставного хряща – его истончению, шероховатости, растрескиванию, потере прочности и эластичности. Субхондральная кость обнажается и уплотняется, в ней происходят остеосклеротические изменения, образуются кисты и краевые разрастания - остеофиты.
Деформирующий остеоартроз по первичному типу развивается в изначально здоровом хряще при врожденном снижении его функциональной выносливости. Случаи вторичного деформирующего остеоартроза возникают на фоне имеющихся дефектов суставного хряща, вызванных травматизацией, воспалением костно-суставных тканей, асептическим некрозом костей, гормональными или обменными нарушениями.

Классификация
В соответствии с клинико-рентгенологической картиной в развитии деформирующего остеоартроза выделяют 3 стадии:
Авторы Kellgren и Lawrence выделяют 0 стадию деформирующего остеоартроза с отсутствием рентгенологических проявлений.
Симптомы деформирующего остеоартроза
К проявлениям деформирующего остеоартроза относятся крепитация (хруст) в суставах при движении; ограниченность подвижности суставов, связанная с уменьшением суставной щели, разрастанием остеофитов и спазмом периартикулярных мышц; необратимая деформация суставов, вызванная дегенерацией субхондральных костей.
Деформирующий остеоартроз с заинтересованностью коленных суставов (гонартроз) проявляется болью при длительной ходьбе, подъеме в лестницу, хрустом и затруднением при выполнении сгибательных и разгибательных движений. При артрозе мелких суставов кистей рук появляются плотные узелки по краям межфаланговых проксимальных и дистальных суставов (узелки Гебердена и Бушара), сопровождающиеся болезненностью и скованностью.
При генерализованной форме деформирующего остеоартроза (болезни Келлгрена, полиостеоартрозе) отмечаются множественные изменения периферических и межпозвонковых суставов. Полиостеоартроз обычно сочетается с остеохондрозом межпозвоночных дисков, спондилёзом в шейном и поясничном отделах позвоночника; периартритами и тендовагинитами.
Осложнения
Длительное прогрессирование деформирующего остеоартроза может осложняться развитием вторичного реактивного синовита, спонтанного гемартроза, анкилоза, остеонекроза мыщелка бедра, наружного подвывиха надколенника.
Диагностика
В ходе диагностики деформирующего остеоартроза пациент проходит консультацию ревматолога и исследования, позволяющие определить состояние и степень функциональной полноценности сустава по характерным клиническим критериям. Основными являются данные рентгенодиагностики, показывающие сужение суставных щелей, разрастание остеофитов, деформацию суставных участков кости: наличие кист, субхондрального остеосклероза. Для более детальной оценки изменений хряща при деформирующем остеоартрозе дополнительно проводят УЗИ, КТ позвоночника и МРТ больного сустава.
По показаниям выполняют пункцию сустава. В сложных случаях выполняют артроскопию с прицельным забором материала и морфологическим изучением биоптатов синовиальной оболочки, суставной жидкости, хрящевой ткани, выявляющим дистрофические и дегенеративные изменения сустава.
Лечение деформирующего остеоартроза
Терапия деформирующего остеоартроза включает комплексный подход с учетом этиологических обстоятельств, систематичность и длительность лечения. В первую очередь требуется разгрузить больной сустав (особенно опорный), снизить двигательную активность, избегать длительной ходьбы, фиксированных поз и ношения тяжестей, при ходьбе пользоваться тростью.
Уменьшение воспаления и боли в суставах при деформирующем остеоартрозе достигается назначением НПВС: диклофенака, нимесулида, индометацина. Сильный болевой синдром снимают внутрисуставными блокадами с введением гормональных препаратов. При риске развития язвенной болезни показаны препараты мелоксикам, лорноксикам, местно - противовоспалительные мази, гели. При медленном рассасывании внутрисуставного выпота выполняют его пункционную эвакуацию.
В начальной стадии деформирующего остеоартроза эффективны хондропротекторы (гидрохлорид глюкозамина и хондроитинсульфат), помогающие приостановить дальнейшее разрушение хряща и восстановить его структуру. При деформирующем остеоартрозе назначают локальную физиотерапию - аппликации парафина и озокеритолечение, высокочастотную электротерапию, электрофорез с новокаином и анальгином, магнитотерапию и лазеротерапию. Для укрепления мышечно-связочных структур и улучшения двигательной функции суставов показана лечебная гимнастика, кинезотерапия, регулярное санаторное лечение и бальнеотерапия.
При тяжелом инвалидизирующем поражении тазобедренного или коленного суставов выполняют эндопротезирование, в случае развития деформирующего остеоартроза голеностопных суставов эффективна операция полного обездвиживания сустава (артродез). Инновационным в лечении деформирующего остеоартроза является применение стволовых клеток, замещающих собой поврежденные клетки хрящевой ткани и активизирующих регенеративные процессы.
Прогноз и профилактика
Скорость и степень прогрессирования деформирующего остеоартроза определяется его формой, локализацией, а также возрастом и общим фоном здоровья пациента. Коксартроз может серьезно нарушить функции конечности, стать причиной нетрудоспособности и даже инвалидности. При многих формах деформирующего остеоартроза достигается устранение болевой реакции, улучшение функционирования сустава, однако полного восстановления хряща у взрослого пациента достичь невозможно.
Профилактика деформирующего остеоартроза состоит в ограничении перегрузок суставов, своевременном лечении травм (растяжений связок, ушибов), заболеваний костного аппарата (дисплазии, плоскостопия, сколиоза), регулярных занятиях гимнастикой, поддержании оптимальной массы тела.
Деформирующий остеоартроз (ДОА, в англоязычной литературе именуемое остеоартрит) – часто встречаемое заболевание суставов, развивающееся вследствие длительного воздействия различных факторов, которые постепенно дестабилизируют процессы восстановления хряща. ДОА относится к группе дегенеративно-дистрофических заболеваний соединительной ткани.
Не имея возможности полноценно восстановиться, хрящ постепенно истончается, теряет былую эластичность и жесткость, а его поверхность становится шершавой, покрытой микротрещинами. Участок кости, на которой крепится хрящ, оголяется, на его поверхности вырастают остеофиты, а по мере развития заболевания поражаются все ткани сустава.
Наиболее подвержены риску остеоартроза люди преклонного возраста, с избыточной массой тела (особенно в отношении коленных суставов), женщины в период менопаузы, работники профессий, где необходимо часто сгибать колени, профессиональные спортсмены и пациенты с наследственным дефицитом коллагена II типа.
Клинически ДОА проявляется в виде болезненности во время движения (артралгиями), снижением мобильности сустава, его деформацией и крепитацией (похрустыванием).
Формы ДОА
Выделяют две формы деформирующего остеоартроза:
- первичная: заболевание возникает в здоровом хряще (по неизвестным причинам);
- вторичная: разрушение развивается на фоне явных дефектов хряща, спровоцированных травмой, хроническим воспалительным процессом, асептическим некрозом костной ткани, гормональными или метаболическими болезнями, ожирением, последствиями артритов.
Симптомы деформирующего остеоартроза
Для всех видов ДОА, независимо от скорости развития дегенерации хряща, ведущими признаками заболевания являются боли разного типа и интенсивности в пораженных суставах. В первую очередь болезни подвержены так называемые опорные группы: коленные (гонартроз), тазобедренные (коксартроз), позвоночник и мелкие межфаланговые суставы рук и стоп.
Варианты болевого синдрома:
Недостаточность амортизационных качеств хряща и субхондральной области
Присутствуют во время нагрузки на пораженный сустав, максимума достигают во второй половине дня, их интенсивность снижается после длительного отдыха
Развитие реактивного синовита (воспаления суставной оболочки и наличие выпота в нем)
Имеют максимальную выраженность в начале нагрузки (до 20 мин) и постепенно стихают по мере движений
Боли, вызванные тендобурситом и периартрозом
Присоединение воспаления сухожилий, поддерживающих сустав
Наблюдаются при движениях, в которых задействованы данные сухожилия
Вызваны венозным застоем в подхрящевом слое надкостницы, вовлечением в процесс костного мозга
Возникают в ночное время и постепенно проходят утром при ходьбе
Также болью сопровождается вовлечение в дегенеративный процесс капсулы сустава, рефлекторный спазм прилегающих мышц и блок суставной мыши (тканей свободного участка разрушенного хряща) в межсуставной щели.
- крепитация;
- ограничение амплитуды движений (вызвано разрастанием остеофитов и мышечным спазмом);
- постепенная и необратимая деформация сустава.
Диагностика заболевания
При подозрении на дегенеративные заболевания опорно-двигательной системы необходимо обратиться к ревматологу. Установить диагноз ДОА доктор может при наличии у пациента триады признаков:
- жалобы на боль;
- изменения на рентгенограмме;
- визуальные признаки деформации сустава.
Стандартные исследования крови и мочи при данной патологии неинформативны. Единственные показатели, которые могут изменяться при наличии активного воспаления в синовиальной оболочке – скорость оседания эритроцитов (СОЭ) и С-реактивный белок.
Широкодоступным, объективным способом диагностики и оценки эффекта от проводимого лечения при ДОА служит рентгенография.
Рентгенологические признаки артроза:
- сужение суставной щели (темного промежутка между двух костей на рентгенограмме);
- субхондральный склероз (уплотнение костного участка, на который крепится хрящ);
- остеофиты – костные отростки, изменяющие площадь контакта и контур суставных поверхностей;
- кистозная перестройка костной ткани;
- повышение плотности (оссификация) прилежащих тканей.
Дополнительные методы исследования позволяют точней определить стадию заболевания, степень поражения сустава и подобрать адекватную терапию. К ним относятся:
- артроскопия с прицельной биопсией синовиальной оболочки и хряща;
- анализ синовиальной жидкости;
- УЗИ (оптимальный метод визуализации суставного хряща);
- МРТ, КТ, сцинтиграфия (проводится для дифференциальной диагностики или в предоперационный период).
Лечение деформирующего остеоартроза
Для ДОА характерно постепенное развитие с периодами обострения и затухания клинических проявлений. Заболевание прогрессирует независимо от проводимого лечения, никогда не наблюдается обратного развития дегенеративных изменений. Все методы лечения направлены на то, чтоб снизить степень дискомфорта и максимально продлить физическую активность пациента.
Существует два подхода к лечению данного заболевания – консервативное и радикальное. Оба они направлены на предотвращение развития инвалидности и улучшение качества жизни пациента.
Этот подход к лечению пациента с ДОА состоит в назначении препаратов симптоматического и структурно-модулирующего действия.
Симптоматические препараты применяются для снижения болевого и воспалительного синдрома. К ним относятся:
- нестероидные противовоспалительные средства: предпочтение отдается селективным блокаторам ЦОГ-2;
- гидролитические энзимы: системная энзимотерапия;
- глюкокортикостероиды: внутрисуставное введение пролонгированных форм, не больше 4 раз в год.
Препараты структурно-модулирующего действия призваны модифицировать течение ДОА путем замедления прогрессирования дистрофических процессов и стимуляции восстановления хрящевой ткани.
Показано применение следующих средств:
- глюкозамина сульфат в виде инъекций;
- хондроитина сульфат в таблетках;
- ингибиторы интерлейкина-1;
- гиалуроновая кислота инъекционно.
Местная терапия заболевания проводится в случае развития периартрита:
- инфильтрация болезненных участков мягких тканей глюкокортикостероидами с анестетиками;
- аппликация противовоспалительных мазей;
- фонофорез гидрокортизона и другие методы физиотерапии.
Вид ортопедической операции отличается в зависимости от рентгенологической стадии остеоартроза.
На I–II ст. рекомендовано проведение корригирующих остеотомий: удаление участков, мешающих движениям в полном объеме или в которых есть признаки злокачественного перерождения. Этот метод эффективен в 90% случаев. Продолжительность функционирования протеза превышает 10–15 лет.
На III–IV ст. проводится:
- тотальное эндопротезирование: замена сустава искусственным;
- артродез: полное обездвиживание сустава в функционально выгодном положении путем удаления суставных поверхностей с последующим сращиванием костей.
Как вспомогательные методы используются:
- лечебная физкультура;
- физиотерапия;
- санаторно-курортное лечение: особенно полезны сероводородные, грязевые и минеральные ванны.
Критерием эффективности терапии является существенное снижение болевого синдрома, замедление разрушения хряща по данным рентгенографии, УЗИ и МРТ и улучшение качества жизни пациента.
Осложнения ДОА
Одно из частых осложнений патологии – вторичный реактивный синовит.
Длительное течение деформирующего остеоартроза может приводить к ряду других последствий:
- спонтанный гемартроз: внезапное кровоизлияние внутрь суставной полости;
- анкилоз: полное отсутствие подвижности в суставе;
- остеонекроз бедренных отростков;
- внешний подвывих надколенника.
Видео
Предлагаем к просмотру видеоролик по теме статьи.

Образование: Ростовский государственный медицинский университет, специальность "Лечебное дело".
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
В четырех дольках темного шоколада содержится порядка двухсот калорий. Так что если не хотите поправиться, лучше не есть больше двух долек в сутки.
Самая высокая температура тела была зафиксирована у Уилли Джонса (США), который поступил в больницу с температурой 46,5°C.
Раньше считалось, что зевота обогащает организм кислородом. Однако это мнение было опровергнуто. Ученые доказали, что зевая, человек охлаждает мозг и улучшает его работоспособность.
Наши почки способны очистить за одну минуту три литра крови.
Во время работы наш мозг затрачивает количество энергии, равное лампочке мощностью в 10 Ватт. Так что образ лампочки над головой в момент возникновения интересной мысли не так уж далек от истины.
В стремлении вытащить больного, доктора часто перегибают палку. Так, например, некий Чарльз Йенсен в период с 1954 по 1994 гг. пережил более 900 операций по удалению новообразований.
Американские ученые провели опыты на мышах и пришли к выводу, что арбузный сок предотвращает развитие атеросклероза сосудов. Одна группа мышей пила обычную воду, а вторая – арбузный сок. В результате сосуды второй группы были свободны от холестериновых бляшек.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его "мотор" остановился на 4 часа после того как рыбак заблудился и заснул в снегу.
74-летний житель Австралии Джеймс Харрисон становился донором крови около 1000 раз. У него редкая группа крови, антитела которой помогают выжить новорожденным с тяжелой формой анемии. Таким образом, австралиец спас около двух миллионов детей.
В нашем кишечнике рождаются, живут и умирают миллионы бактерий. Их можно увидеть только при сильном увеличении, но, если бы они собрались вместе, то поместились бы в обычной кофейной чашке.
В течение жизни среднестатистический человек вырабатывает ни много ни мало два больших бассейна слюны.
Если бы ваша печень перестала работать, смерть наступила бы в течение суток.
Первый вибратор изобрели в 19 веке. Работал он на паровом двигателе и предназначался для лечения женской истерии.
Здоровая спина – это подарок судьбы, который нужно очень бережно хранить. Но кто из нас задумывается о профилактике, когда ничего не беспокоит! Мы не просто не .

Деформирующий остеоартроз – прогрессирующее дистрофическое изменение костных суставов с первичным повреждением хрящевых тканей и последующей дегенерацией всего комплекса костно-суставного аппарата. Деформирующий остеоартроз характеризуется артралгией, функциональной недостаточностью суставов и выраженными изменениями их формы. Фармакотерапия деформирующего остеоартроза направлена на замедление прогрессирования дегенеративных процессов, уменьшение боли и улучшение функционирования суставов; в некоторых случаях показано эндопротезирование суставов. Течение деформирующего остеоартроза медленно прогрессирующее с развитием анкилоза или патологической нестабильности сустава.

- Классификация
- Симптомы деформирующего остеоартроза
- Осложнения
- Диагностика
- Лечение деформирующего остеоартроза
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Деформирующий остеоартроз - частая патология суставов, при которой нарушение регенерации соединительнотканных структур приводит к преждевременному старению суставного хряща – его истончению, шероховатости, растрескиванию, потере прочности и эластичности. Субхондральная кость обнажается и уплотняется, в ней происходят остеосклеротические изменения, образуются кисты и краевые разрастания - остеофиты.
Деформирующий остеоартроз по первичному типу развивается в изначально здоровом хряще при врожденном снижении его функциональной выносливости. Случаи вторичного деформирующего остеоартроза возникают на фоне имеющихся дефектов суставного хряща, вызванных травматизацией, воспалением костно-суставных тканей, асептическим некрозом костей, гормональными или обменными нарушениями.

Классификация
В соответствии с клинико-рентгенологической картиной в развитии деформирующего остеоартроза выделяют 3 стадии:
Авторы Kellgren и Lawrence выделяют 0 стадию деформирующего остеоартроза с отсутствием рентгенологических проявлений.
Симптомы деформирующего остеоартроза
К проявлениям деформирующего остеоартроза относятся крепитация (хруст) в суставах при движении; ограниченность подвижности суставов, связанная с уменьшением суставной щели, разрастанием остеофитов и спазмом периартикулярных мышц; необратимая деформация суставов, вызванная дегенерацией субхондральных костей.
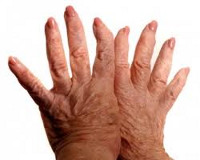
Деформирующий остеоартроз с заинтересованностью коленных суставов (гонартроз) проявляется болью при длительной ходьбе, подъеме в лестницу, хрустом и затруднением при выполнении сгибательных и разгибательных движений. При артрозе мелких суставов кистей рук появляются плотные узелки по краям межфаланговых проксимальных и дистальных суставов (узелки Гебердена и Бушара), сопровождающиеся болезненностью и скованностью.
При генерализованной форме деформирующего остеоартроза (болезни Келлгрена, полиостеоартрозе) отмечаются множественные изменения периферических и межпозвонковых суставов. Полиостеоартроз обычно сочетается с остеохондрозом межпозвоночных дисков, спондилёзом в шейном и поясничном отделах позвоночника; периартритами и тендовагинитами.
Осложнения
Длительное прогрессирование деформирующего остеоартроза может осложняться развитием вторичного реактивного синовита, спонтанного гемартроза, анкилоза, остеонекроза мыщелка бедра, наружного подвывиха надколенника.
Диагностика
В ходе диагностики деформирующего остеоартроза пациент проходит консультацию ревматолога и исследования, позволяющие определить состояние и степень функциональной полноценности сустава по характерным клиническим критериям. Основными являются данные рентгенодиагностики, показывающие сужение суставных щелей, разрастание остеофитов, деформацию суставных участков кости: наличие кист, субхондрального остеосклероза. Для более детальной оценки изменений хряща при деформирующем остеоартрозе дополнительно проводят УЗИ, КТ позвоночника и МРТ больного сустава.
По показаниям выполняют пункцию сустава. В сложных случаях выполняют артроскопию с прицельным забором материала и морфологическим изучением биоптатов синовиальной оболочки, суставной жидкости, хрящевой ткани, выявляющим дистрофические и дегенеративные изменения сустава.
Лечение деформирующего остеоартроза
Терапия деформирующего остеоартроза включает комплексный подход с учетом этиологических обстоятельств, систематичность и длительность лечения. В первую очередь требуется разгрузить больной сустав (особенно опорный), снизить двигательную активность, избегать длительной ходьбы, фиксированных поз и ношения тяжестей, при ходьбе пользоваться тростью.
Уменьшение воспаления и боли в суставах при деформирующем остеоартрозе достигается назначением НПВС: диклофенака, нимесулида, индометацина. Сильный болевой синдром снимают внутрисуставными блокадами с введением гормональных препаратов. При риске развития язвенной болезни показаны препараты мелоксикам, лорноксикам, местно - противовоспалительные мази, гели. При медленном рассасывании внутрисуставного выпота выполняют его пункционную эвакуацию.
В начальной стадии деформирующего остеоартроза эффективны хондропротекторы (гидрохлорид глюкозамина и хондроитинсульфат), помогающие приостановить дальнейшее разрушение хряща и восстановить его структуру. При деформирующем остеоартрозе назначают локальную физиотерапию - аппликации парафина и озокеритолечение, высокочастотную электротерапию, электрофорез с новокаином и анальгином, магнитотерапию и лазеротерапию. Для укрепления мышечно-связочных структур и улучшения двигательной функции суставов показана лечебная гимнастика, кинезотерапия, регулярное санаторное лечение и бальнеотерапия.
При тяжелом инвалидизирующем поражении тазобедренного или коленного суставов выполняют эндопротезирование, в случае развития деформирующего остеоартроза голеностопных суставов эффективна операция полного обездвиживания сустава (артродез). Инновационным в лечении деформирующего остеоартроза является применение стволовых клеток, замещающих собой поврежденные клетки хрящевой ткани и активизирующих регенеративные процессы.
Прогноз и профилактика
Скорость и степень прогрессирования деформирующего остеоартроза определяется его формой, локализацией, а также возрастом и общим фоном здоровья пациента. Коксартроз может серьезно нарушить функции конечности, стать причиной нетрудоспособности и даже инвалидности. При многих формах деформирующего остеоартроза достигается устранение болевой реакции, улучшение функционирования сустава, однако полного восстановления хряща у взрослого пациента достичь невозможно.
Профилактика деформирующего остеоартроза состоит в ограничении перегрузок суставов, своевременном лечении травм (растяжений связок, ушибов), заболеваний костного аппарата (дисплазии, плоскостопия, сколиоза), регулярных занятиях гимнастикой, поддержании оптимальной массы тела.
Рассмотрены патофизиология болевого синдрома при остеоартрозе и подходы к терапии с применением нестероидных противовоспалительных препаратов (НПВП). Описаны клиническая эффективность и безопасность применения нимесулида для лечения боли при остеоартрозе.
Pathophysiology of pain syndrome in osteoarthrosis and approaches to the therapy using non-steroidal anti-inflammatory preparations (NAIP) were considered. Clinical efficiency and safety of nemisulide application for relief of pain in osteoarthrosis were described.
Остеоартроз (ОА) — одно из самых распространенных заболеваний опорно-двигательного аппарата, основная причина постоянного болевого синдрома [1] и инвалидизации [2].
Болевой синдром при ОА представляется важной клинической проблемой. Манифестация боли возможна на разных стадиях процесса и не имеет четкой корреляции с рентгенологической картиной: рентгенологические проявления ОА отмечаются примерно у 30% взрослого населения, а болевой синдром развивается у 10–12% [3].
Боль может сохраняться даже после хирургического лечения. Примерно 15% больных, которым проведено эндопротезирование коленного сустава в связи с выраженным ОА, продолжают испытывать боль, несмотря на отсутствие хирургических осложнений и нормальную рентгенологическую картину [4].
В основе успешного управления симптомами ОА лежит понимание патофизиологии и тщательная клиническая оценка болевого синдрома.
Любой сустав, вне зависимости от его размеров, — это сложный орган, в состав которого входят синовиальная мембрана, синовиальная жидкость, хрящ, кость и мягкие ткани. При этом сустав — это еще и орган с едиными нейротрофическими, метаболическими, иммунными и функциональными составляющими, играющими важную роль как в патогенезе самого ОА, так и болевого синдрома при нем.
Известно, что прогредиентно протекающие дегенеративные процессы при ОА отмечаются во всех суставных структурах и объединяют потерю матрикса гиалинового хряща, ремоделирование подлежащей кости, поражение костного мозга, вовлечение связок, растяжение капсулы сустава, ослабление прилегающих к суставу мышц [5]. По мере прогрессирования ОА существенно меняется биомеханика сустава.
При ОА в процесс активно вовлекается периост из-за обнажения костной суставной поверхности [6]. Поверхность костной ткани внутри сустава, лишенная амортизирующих свойств из-за деструкции хряща, испытывает избыточную и неравномерную механическую нагрузку. В субхондральной кости появляются зоны динамической перегрузки, в которых развиваются изменения микроциркуляции. Это способствует возникновению субхондрального остеосклероза, кистовидной перестройки, изменению кривизны суставных поверхностей и образованию остеофитов. Повышение внутримедуллярного давления в субхондральной кости — это еще один источник боли при ОА.
Изменения также затрагивают связки, сухожилия, с развитием лигаментитов, теносиновитов, а также бурситов околосуставных сумок [7]. Прилегающие к суставу мышечные структуры страдают как от реактивного воспаления, развивающегося в суставах, так и от нарушения биомеханики больного сустава. В итоге повышенная механическая нагрузка на мышечный аппарат приводит к гипертонусу мышц, что также способствует нарастанию боли.
Значимая роль в патогенезе ОА отводится синовиту, деструктивно воздействующему на суставные структуры за счет активации фагоцитарных, воспалительных и иммунных реакций, способствующих высвобождению значительного числа медиаторов (цитокинов, простагландинов, матриксных металлопротеиназ, супероксидных радикалов, оксида азота и др.), играющих ключевую роль как в моделировании воспаления, так и восприятии боли [8, 9]. Воспаление синовиальной оболочки вносит существенный вклад в развитие боли, поскольку в ней достаточно широко представлены нервные окончания.
К настоящему времени накоплены данные о роли субстанции Р — нейропептида, способствующего возникновению и поддержанию боли за счет усиления продукции медиаторов воспаления в области суставов [10, 11]. По данным исследований при ОА субстанция Р обнаруживается в синовиальной жидкости и синовиальной оболочке [12, 13], периосте, подхрящевых участках костей, суставных капсулах, где синтезируется в немиелинизированных чувствительных нейронах [14], то есть в тех суставных структурах, из которых чаще и больше происходит болевых импульсов [15]. В хрящевой ткани сустава субстанция Р не обнаружена.
Еще одним проявлением ОА, усиливающим боль, является синовиальный выпот, способствующий растяжению богатой нервными окончаниями капсулы сустава [16, 17].
Кроме того, в качестве весьма специфического для суставов фактора, способствующего развитию болевого синдрома при ОА, рассматривается ангиогенез, при котором помимо роста сосудов отмечается значительный рост новых немиелинизированных чувствительных нервных окончаний [18]. При ОА процесс ангиогенеза наблюдается в синовиальной оболочке, некальцифицированных участках внутрисуставных хрящей и в остеофитах. Интересно, что в периваскулярных немиелинизированных нервных волокнах также обнаруживается субстанция Р и пептид, связанный с геном кальцитонина (CGRP), которые в совокупности способствуют медиации устойчивой жгучей боли, как ее описывают больные ОА [19].
Поскольку внутрисуставной гиалиновый хрящ не имеет ноцицепторов, он, несмотря на существенные дегенеративные процессы в нем, не может служить источником болевой импульсации. Очевидно, что боль при ОА полиэтиологична и происходит из всех выполняющих сустав структур, за исключением хряща [10, 11].
Болевой синдром при ОА может быть острым и хроническим: с периодическими обострениями и их уменьшением. Острая боль является следствием раздражения болевых рецепторов, расположенных в коже, связках, сухожилиях, сумках, костях, синовиальной оболочке, мышцах. Механизмы трансформации острой боли в хронический болевой синдром при ОА изучены недостаточно полно. Предполагается, что хронизации боли при ОА может способствовать длительное раздражение периферической ноцицептивной системы с постоянным вовлечением задних рогов спинного мозга [20]. При этом включаются принципиально иные механизмы формирования болевых импульсов. Ключевой вопрос касается связи между периферическим повреждением и воспалением структур суставов и стимуляцией выработки ЦОГ-2 в центральной нервной системе (ЦНС), где могут иметь значение как нервные, так и гуморальные механизмы. В частности, показано, что довольно продолжительная активность небольших сенсорных нейронов, обусловленная периферическим воспалением, сопровождается высвобождением глутамата/аспартата и субстанции Р в спинном мозге с последующей активацией рецепторов NMDA (N-метил-D-аспартата) в нейронах задних рогов спинного мозга [21]. Доказательством этого является повышенное содержание субстанции Р в спинномозговой жидкости больных ОА [22]. Стимуляция этих рецепторов может вызвать повышение экспрессии ряда ферментов, включая ЦОГ-2, в спинном мозге, что в итоге ведет к усилению болевого синдрома. Гуморальный же механизм воспалительной реакции, связанной с повреждением периферических суставных структур, приводит к высвобождению провоспалительных цитокинов (ФНО-α, ИЛ-1β), которые в свою очередь усиливают экспрессию ЦОГ-2.
Исходя из представлений о патогенезе ОА и болевого синдрома при нем, становится очевидным, что подавление воспаления и предотвращение деструкции суставных структур, с целью снижения синтеза провоспалительных цитокинов, простагландинов (в особенности ПГE2), ферментов синовиальной оболочки, металлопротеиназ, деградации коллагеновых волокон, протеолитической активности и т. п., является одним из приоритетных направлений в терапии ОА. Несомненно, назначение противовоспалительных препаратов не просто желательно, но и показано больным с ОА, испытывающим боль, особенно в тех случаях, когда развитие болевого синдрома тесно связано с тканевым воспалением, а простой анальгетик не оказывает должного эффекта. Подобный терапевтический подход соответствует ведущим рекомендациям национальных и международных руководств по купированию болевых синдромов у пациентов с ОА, где подчеркивается, что терапевтическим методом в таких случаях является использование парацетамола. При этом важно подчеркнуть, что парацетамол не оказывает действия на периферические ЦОГ, а посему не обладает противовоспалительным эффектом. И, кроме того, чтобы реализовать свою функцию, парацетамол должен достичь достаточного уровня концентрации в ликворе, поскольку оказывает комплексное воздействие на ЦНС, усиливая нисходящие от периферии к ЦНС процессы торможения. А это требует применения достаточной дозировки и обязательного соблюдения временного интервала между приемами (1 г трижды в день), чтобы полностью использовать потенциал препарата [27]. Эти аспекты оправдывают применение таких лекарственных препаратов, как НПВП, с учетом соотношения пользы и риска.
Нестероидные противовоспалительные препараты (НПВП) — наиболее назначаемый класс лекарственных средств, предназначенных для лечения болевых синдромов. Общими фармакологическими свойствами НПВП являются подавление биосинтеза простагландинов (ведущих факторов активации болевых рецепторов) за счет блокады изоферментов циклооксигеназы, в частности ЦОГ-2, и нормализация сниженного болевого порога. При назначении НПВП подавление синтеза простагландинов имеет место как на периферическом, непосредственно в месте повреждения и воспаления, так и на центральном уровнях, свидетельствуя о том, что и периферические и центральные механизмы принимают участие в антиноцицептивном действии этих препаратов. Центральный эффект НПВП связан с угнетением синтеза простагландинов, которые образуются в ЦНС и способствуют усилению болевого сигнала. Таким образом, ЦНС является дополнительным местом проявления антиноцицептивных эффектов НПВП.
Одним из наиболее популярных средств среди НПВП является нимесулид. Многочисленные исследования и более чем 30-летний клинический опыт применения показали, что нимесулид (Найз) обладает высокой эффективностью и хорошей переносимостью [28].
В контексте данной статьи хотелось бы прежде остановиться на бесспорных достоинствах нимесулида как препарата выбора для лечения болевых синдромов при ОА, принимая во внимание данные об их механизмах, рассмотренные ранее.
Интересны, прежде всего, ЦОГ-зависимые механизмы действия, обусловливающие эффективность и безопасность нимесулида. Поскольку нимесулид оказывает преимущественное действие на ЦОГ-2, то его эффекты очевидны как на периферии, в суставных структурах, затронутых деструктивным процессом и связанным с ним воспалением, так и в ЦНС [29, 30]. Причем исключительной особенностью нимесулида является способность не только подавлять активность ЦОГ-2, но и блокировать ее образование [31].
Хотя нимесулид и обладает преимущественным эффектом в отношении ЦОГ-2, он оказывает сбалансированное влияние на обе изоформы ЦОГ. В терапевтических концентрациях нимесулид ингибирует 88% активности ЦОГ-2 и 45% активности ЦОГ-1. При этом если воздействие на ЦОГ-1 прекращается через 24 часа после введения, то воздействие на ЦОГ-2 продолжается намного дольше [32], и это различие сохраняется при длительном применении [33, 34].
Неоспоримым преимуществом нимесулида является способность молекулы уменьшать высвобождение ФНО-α, ИЛ-6 и субстанции Р [35–37].
Примечательны ЦОГ-независимые эффекты нимесулида. В частности, в терапевтических концентрациях нимесулид влияет на продукцию токсичных окислительных радикалов и других компонентов нейтрофильной активации [38], ß-глюкуронидазы [39], что может усилить противовоспалительный и анальгетический эффект и потенциально уменьшать вероятность гастроинтестинальной ульцерогенности.
Наконец, трудно переоценить протективное действие нимесулида на суставной хрящ. Известно, что неселективные в отношении ЦОГ НПВП усугубляют тяжесть ОА при длительном применении. В наибольшей степени отрицательно влияют на хрящ производные индолуксусной кислоты (индометацин), чуть меньше — производные пропионовой кислоты (ибупрофен, напроксен и др.), что подтверждается данными рентгенографии. При этом доказано, что селективные ингибиторы ЦОГ-2, в частности нимесулид, не оказывают отрицательного влияния на синтез протеогликанов хрящевой тканью, даже при применении высоких доз [40, 41]. Напротив, нимесулид обнаруживает способность снижать в синовиальной жидкости, полученной из воспаленного сустава, уровень коллагеназы, вызывающей деградацию коллагена и протеогликанов [42].
С клинической точки зрения, многоплановость механизмов действия нимесулида, связанных или не связанных с ЦОГ, выражается в эффективности и быстром модулировании сложного воспалительного процесса и сопряженной с ним боли.
Клиническая эффективность нимесулида показана в многочисленных исследованиях. Известно, что препарат превосходит или как минимум столь же эффективен, как и классические НПВП, в отношении купирования значительного числа болевых синдромов, включая ревматоидный артрит, скелетномышечные боли в спине, послеоперационную и зубную боль, дисменорею. Преимущества нимесулида показаны и при лечении ОА. Так, использование нимесулида позволило добиться значимого уменьшения боли и улучшения самочувствия у подавляющего большинства пациентов с ОА, включенных в двойное слепое сравнительное исследование эффективности и безопасности нимесулида и диклофенака при гонартрозе и коксартрозе [43]. Этот результат представляется более значимым еще и потому, что примерно половина больных до назначения нимесулида получали другие НПВП и не отмечали при этом существенного улучшения своего состояния.
М. И. Шупина* , 1 , кандидат медицинских наук
Г. И. Нечаева*, доктор медицинских наук, профессор
Е. Н. Логинова*, кандидат медицинских наук
Т. В. Кропотина**, кандидат медицинских наук
Ю. В. Арбузова**
* ГБОУ ВПО ОмГМУ МЗ РФ, Омск
** БУЗОО ОКБ, Омск
Читайте также:


