Подвержены инфекциям дети иммунитет

Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Иммунитет - это невосприимчивость организма к различным инфекционным возбудителям, их токсинам (ядам), а так же к различным другим чужеродным органическим веществам. Работа иммунитета включает в себя запуск сложного многоступенчатого механизма, взаимодействие одновременно нескольких систем: нервной, эндокринной, регулирование обмена веществ и других сложных процессов в организме.
Какие органы формируют иммунную систему?
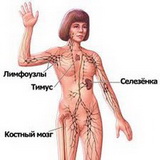
Иммунная система человека состоит из вилочковой железы, костного мозга, эмбриональной (во внутриутробном периоде) печени, лимфоидных образований кишечника, лимфатических узлов, селезенки, а также постоянно находящиеся в крови и тканях клетки костномозгового происхождения - лимфоциты, моноциты и др. Иммунная охрана организма осуществляется как клетками иммунной системы (клеточный иммунитет), так и продуктами их жизнедеятельности (гуморальный иммунитет).
Виды иммунитета
Существует несколько видов иммунитета:
• приобретенный: естественный иммунитет (активный и пассивный)
Видовой иммунитет передается по наследству. Например, человек не может заразиться определенной инфекцией от животных (чумой). Следующий вид иммунитета приобретенный: естественный иммунитет, вырабатывается при длительном контакте с возбудителями инфекции, при этом заражения не происходит. Приобретенный иммунитет, который в свою очередь бывает активным: после перенесенного заболевания (ветряная оспа или краснуха) и после введения вакцин. Пассивный иммунитет, который развивается в ответ на введение специальных сывороток с антителами (при инфекционных заболеваниях).
Особенности иммунитета у детей
Иммунитет детей имеет ряд особенностей на определенных этапах развития.
Детский иммунитет характеризуется наличием 5 основных критических периодов:
• Второй критический период в возрасте 4-6 месяцев обусловлен разрушением материнских антител. В этот период особенно важно начать вакцинацию, с последующей ревакцинацией для формирования активного иммунитета против определенных видов инфекций. В этом возрасте дети особенно подвержены воспалительным процессам органов дыхания и кишечным инфекциям, нарастает частота пищевой аллергии.
• Четвертый критический период в возрасте 4-6 лет. Характеризуется уже накопленным активным иммунитетом, который сформировался под воздействием вакцинации и перенесенных вирусных и инфекционных заболеваний. В этот период возможно формирование многих хронических заболеваний. Для предотвращения этого необходимо своевременное и правильное лечение острых процессов.
• Пятый критический период в возрасте 12-15лет. Происходит на фоне бурной гормональной перестройки для девочек 12-13 лет, для мальчиков 14-15 лет. На фоне повышенной секреции половых гормонов уменьшается объем лимфоидных органов. В этот период окончательно формируется сильный и слабый типы иммунного ответа.
В период полового созревания (пятый критический период) организм ребенка впервые сталкивается с неблагоприятными экзогенными (внешними) факторами, такими как курение, алкоголь и употребление различных синтетических наркотических средств.
Причин и факторов, снижающих иммунитет очень много. Основные из них это прежде всего неправильное питание, с низким содержанием белка и витаминов, что приводит к транзиторному снижению иммунитета, наличие хронических очагов инфекции (кариозные зубы, синусит, тонзиллит, пиелонефрит, цистит и др.), наличие хронических болезней органов пищеварения, инфекционных болезней в анамнезе, экологически неблагоприятная обстановка на территории проживания ребенка, нарушение состава кишечной микрофлоры, неадекватное использование антибиотиков.
Иммуномоделирующее лечение

Прежде чем начинать иммуномоделирующее лечение необходимо оценить и скорректировать следующие моменты:
• качество питания ребенка. Сбалансированное питание ребенка должно быть, прежде всего, разнообразным, включать белки, витамины и микроэлементы и состоять из продуктов растительного и животного происхождения.
• условия жизни ребенка, спокойная психоэмоциональная обстановка в семье, родительская любовь и ласка, также способствует правильному формированию иммунитета.
• оценка состояния внутренних органов, санация очагов хронической инфекции, для этого необходима консультация педиатра или семейного врача
Когда необходимо начать иммуномоделирующее лечение?
Использование иммунокорректирующих средств оправданно в следующих случаях:
• Ребенок слишком часто болеет, больше 6 раз в год простудными заболеваниями.
• Ребенок плохо реагирует на стандартное лечение, длительность заболевания выше, чем в среднем у детей данного возраста.
• Обычные простуды протекают, как правило, с осложнениями (бронхиты, отиты, ангины).
Прежде чем начать лечение необходимо произвести стандартное обследование состояния здоровья ребенка, включающее в себя:
• общий анализ крови
• общий анализ мочи
• биохимический анализ крови (Ig E, глюкоза, более подробно необходима консультация врача)
• обсследование у ЛОР-врача (для исключения очагов инфекции)
• анализ кала на яйца гельминтов и наличие дисбактериоза
• УЗИ внутренних органов (для оценки состояния внутренних органов).
Иммунокоррекция состоит из двух видов: неспецифической и специфической:

Неспецифическая иммуностимуляция включает в себя, прежде всего грудное вскармливание, а в дальнейшем сбалансированное питание, закаливание, правильная организация сна и отдыха.
Группы препаратов используемые для специфической иммунокоррекции
Препараты, которые могут непосредственно воздействовать на иммунную систему, делятся на 3 группы:
2. Индукторы иммунологической толерантности (эта группа препаратов способствует повышению функциональной активности иммунной системы).
3. Иммуносупрессоры (препараты поддержки иммунной системы, изменяющие некоторые специфические иммунные ответы).

Иммуностимуляторы - это препараты способствующие процессам возрастного созревания иммунной системы, включают в себя следующие группы препаратов:
• витамины (Пиковит, Гровит, Мултитабс, Киндер биовиталь, Витрум Кидс, Мултивитамол и др.)
• препараты содержащие полиненасыщенные жирные кислоты (Омега-3, рыбий жир, оливковое масло.
Индукторы иммунологической толерантности - эта группа препаратов состоит из 5 подгрупп:
• препараты растительного происхождения изготавливаются из лекарственных растений, обладающих иммуностимулирующими и адаптогенными свойствами. Данная группа препаратов может быть назначена без обследования иммунного статуса ребенка, но дозировка и длительность использования должна быть обязательно согласована с врачом.
В эту группу входят: препараты Эхинацеи пурпурной (Иммунал, настойка эхинацеи доктора Тайса), как правило, их назначают для лечения ОРВИ и для профилактики простудных заболеваний. Препараты женьшеня, радиолы розовой, элеутерококка - эти препараты желательно использовать у детей в возрасте после 6 лет.
• препараты группы интерферонов, используются в первую очередь при вирусных заболеваниях, гриппе, а также при вирусных гепатитах, герпесе. Интерфероны бывают 2 поколений: первое поколение, это препараты синтезированные из донорской крови (интерферон человеческий лейкоцитарный), в настоящее время не используется.
Второе поколение синтетические интерфероны (Гриппферон, Виферон, Кипферон)
• препараты способствующие выработке собственных интерферонов (индукторы интерферонов): Арбидол, Анаферон, Циклоферон.
Данные препараты обладают выраженным противовирусным и иммуностимулирующим действием. Препараты индукторы эндогенных (собственных) интерферонов не рекомендуется применять одновременно с препаратами из предыдущей подгруппы, так как возможна неадекватная реакция организма на сочетание этих препаратов. Использование препаратов этой группы целесообразно с первых часов болезни (как только вы заметите первые признаки начинающийся вирусной инфекции).
• препараты бактериального происхождения для повышения иммунитета
(Бронхомунал П,Бронхомунал, ИРС-19б, Ликопид, Рибомунил).
Данные медикаменты содержат фрагменты бактерий, но не несут никакой инфекционной опасности для заражения, обладая при этом иммуностимулирующим действием. Использование данных средств, требует обязательной консультации врача специалиста.
• препараты изготовленные из вилочковой железы (тимуса): Тималин, Т-активин, Тимостимулин и другие использование препаратов данной группы ограниченно и требует постоянного контроля врача иммунолога.
Необходимо помнить, что иммунитет это основная защита нашего организма. Неправильное вмешательство в работу этой тонкой системы может привести к серьезным последствиям и сделать организм вашего ребенка открытым для любых воздействий извне. Поэтому прежде чем начинать использование иммуностимулирующих средств, необходимо проконсультироваться с врачом.
Оппортунистические инфекции ЦНС могут возникать у иммуноослабленных детей, и спектр инфекций зависит от особенностей нарушения клеточного иммунитета, врожденных или ятрогенных (Cunha, 2001). Все большее число детей появляется с ятрогенной этиологией иммунной недостаточности различной степени выраженности — от тяжелого иммунного подавления при трансплантации органов до хронического применения стероидов при воспалительных состояниях.
Инфицирование оппортунистическими возбудителями, обычно непатогенными для человеческого организма, может быть необычным нарушением, вторичным при обычных вирусных патогенах. В целом большему риску подвержены дети с Т-клеточной лимфоцитарной недостаточностью, у которых может встречаться широкий спектр вирусных, бактериальных, грибковых и протозойных инфекций. Дети с В-клеточным дефицитом в меньшей степени повержены риску инфицирования ЦНС, однако возможен общеизвестный синдром хронической энтеровирусной инфекции.
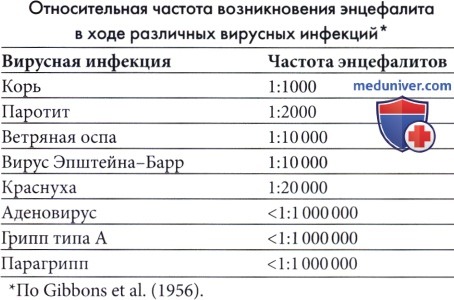
а) Замедленный тип острого коревого энцефалита при ослабленном иммунитете. Острый замедленный коревой энцефалит наблюдался в основном у пациентов с ослабленным иммунитетом (Murphy и Yunis, 1976), хотя изредка он встречается у детей с явно нормальными иммунными механизмами. В отличие от обычного постинфекционного энцефаломиелита, вирус кори в большом количестве выявляется в тканях мозга, а нуклеокапсиды видны при электронной микроскопии в ядрах глии и нейронах. Воспалительная реакция выражена в различной степени, но чаще слабая (Lacroix et al, 1995). Заболевание развивается через 2-6 месяцев после кори или контакта со случаями кори. Наиболее явным симптомом часто являются эпилептические припадки и во многих случаях первыми проявлениями является epilepsia partialis continua (Aicardi et al., 1977; Luna et al., 1990; Barthez Carpentier et al., 1992).
Быстро развивается прогрессирующее ухудшение с оглушенностью и комой и характерными очаговыми симптомами, особенно гемиплегией.
Продолжают появляться новые неврологические симптомы разной продолжительности. У некоторых пациентов отмечается ретинопатия (Haltia et al., 1977). Диагностика может быть затруднена, в связи с нормальными или слегка измененными показателями ликвора. В большинстве случаев отмечают интратекальный синтез специфических противокоревых антител и высокий титр антител против вируса кори в плазме крови и СМЖ. У детей с наиболее тяжелым подавлением иммунитета выработка антител, однако, может быть ослаблена.
КТ обычно дает нормальные результаты. Были сообщения о наличии пониженной плотности в центральном сером веществе (Colamaria et al., 1989). НА MPT могут быть участки интенсивного сигнала при Т2-режиме (Barthez Carpentier et al., 1992). ЭЭГ может показать замедление сигнала от базальных ядер с повторяющимися медленно-волновыми комплексами на уровне 1 Hz (Aicardi et al., 1977; Colamaria et al., 1989). Течение болезни имеет фатальный исход. Может произойти приостановление болезни, но у редких выживших остаются тяжелые последствия (Mustafa et al., 1993).
б) Герпесвирусные инфекции человека. Все герпесвирусные инфекции могут стать причиной тяжелого заболевания у иммунодефицитных детей с ослабленной функцией Т-лимфоцитов, включая реципиентов органов при трансплантации, ВИЧ-инфицированных детей и детей с врожденным иммунодефицитом. Заболевание может возникать в результате первичной инфекции у неиммуннизированных детей или как результат реактивации латентной инфекции в период иммунной недостаточности. Болезнь может ограничиваться одним органом или распространяться, вовлекая многие органы с высоким уровнем вирусемии в плазме. Несмотря на доступность противовирусной терапии, полное выздоровление часто зависит от улучшения функции иммунной системы.
Нарушающие зрение вирусные ретиниты вызываются в первую очередь представителями семейства вирусов герпеса; в клинические синдромы входят острый ретинальный некроз (ОРН) (Bonfioli и Eller, 2005), прогрессирующий наружный ретинальный некроз (ПНРН) (Purdy et al., 2003), мультифокальный хориоидит, серпигинозный хориоидит и другие вирусные ретинопатии (ЦМВ ретинит, смотри ниже). При активном иммунитете наиболее распространенным считается ВПГ ретинит, тогда как вирус ветряной оспы в равной степени поражает пациентов с нормальным и ослабленным иммунитетом.
В связи с плохим проникновением лекарственных форм в ткани глаза при системной терапии из-за ограниченного кровоснабжения, при лечении тяжелых заболеваний необходимы как системные назначения, так и прямое внутриглазное введение противовирусных препаратов (Scott et al., 2002).
• Цитомегаловирус. При тяжелой иммунной депрессии может развиваться диссеминированная форма цитомегаловирусной инфекции. Обычно наблюдается высокий уровень вирусемии в крови. Инфекция может поражать головной мозг, сетчатку глаза, легкие, костный мозг, печень и кишечник. При лечении могут быть эффективны ганцикловир, фоскарнет или цидофовир; однако из-за их токсичности требуется тщательный метаболический контроль. Ганцикловир относится к средствам первого выбора после фоскарнета и цидофовира; для более долгосрочной поддерживающей иммуносупрессивной терапии подходит пероральный прием валганцикловира (Kimberlin, 2002; Griffiths, 2004).
ЦМВ ретинит хорошо распознается при прогрессировании ВИЧ-инфекции; при ее наличии у новорожденных, в отличие от взрослых или более старших детей, в первую очередь поражается макула, а не периферическая сетчатка, тем самым непосредственно угрожая центральному зрению (Wren et al., 2004). Другие проявления ЦМВ инфекции в центральной нервной системе у детей с иммунодефицитом включают очаговый или генерализованный энцефалит, паралич черепных нервов, поперечный миелит, радикулит и синдром Гийена-Барре. Успех терапии зависит от ответа вовлеченного органа, также как от уровня вирусемии. У ВИЧ-инфицированных пациентов цитомегаловирусное заболевание ЦНС, включая ретинит, может принять остро симптоматическое течение, в момент начала противовирусной терапии, как проявление синдрома восстановления воспалительного иммунитета (IRIS). IRIS наиболее характерен для пациентов, которые начали лечение в стадии прогрессирующей болезни и с очень низким уровнем CD4, что требует тщательного наблюдения при лечении ЦМВ, ВИЧ и иммунной перестройке для уменьшения симптомов (Griffiths, 2004).
• Вирус простого герпеса. Тяжелая инфекция ВПГ может иметь место у детей с ослабленным иммунитетом. Чаще всего поражаются ротовая полость, кожа, легкие и кишечник, в то время специфическое поражение ЦНС редко. Высокие дозы внутривенного ацикловира должны иметь эффект, хотя возможно развитие резистентности при повторной экспозиции, особенно при низких оральных дозах. ПЦР-исследование ликвора на ВПГ имеет важное значение в постановке диагноза и контроле лечения у иммуносупрессивных пациентов (Cinque et al., 1998).
• Вирус ветряной оспы. Имеются сообщения о диссеминированном энцефаломиелите у взрослых и детей с недостаточностью иммунитета, вызванном ВВО инфекцией (Carmack et al., 1993; Herrold и Hahn, 1994). Заболевание может протекать с сыпью или без нее. Реактивация латентной инфекции ВОГ характерна при иммунной недостаточности и кожный опоясывающий герпес может иметь тяжелое течение, вплоть до диссеминированного заболевания. Диссеминированная инфекция ВОГ может привести к полиорганной недостаточности и синдрому диссеминированного внутрисосудистого свертывания.
• Вирус герпеса человека 6 и 7 типов. Реактивация ВГЧ-6 встречается приблизительно в 50% всех пересадок костного мозга и у 20-30% реципиентов паренхиматозных органов через 2-3 недели после процедуры. Клинические симптомы заключаются в лихорадке, кожной сыпи, пневмонии, подавлении костного мозга, энцефалите и отторжении трансплантата (Yoshikawa, 2003). Развитие лимбического энцефалита связано с высокой вирусной нагрузкой в крови ДНК ВГЧ-6 после трансплантации (Ogata et al., 2006). ВГЧ-7 виремия после пересадки стволовых клеток также была ассоциирована с энцефалитом (Chan et al., 2004). Эффект может быть от применения ганцикловира.
• Вирус Эпштейна-Барр. Инфекция ВЭБ способна вызывать тяжелые, часто заканчивающиеся смертью заболевания в некоторых семьях с потенциально фатальной чувствительностью к ВЭБ, передаваемой по наследству как Х-сцепленный ген. Это заболевание, известное как Х-сцепленный лимфопролиферативный синдром (ХЛС) (Grierson и Purtilo, 1987), может принимать форму смертельного инфекционного мононуклеоза, злокачественной лимфомы, приобретенной гипо- и агаммаглобулинемии и вирус-ассоциированного гемофагоцитарного синдрома (Tiab et al., 2000, Gilmour и Gaspar, 2003). Поврежденный ген XLP был определен и обозначен SH2D1A; он кодирует адаптерный белок SAP (белок сигнальной лимфоцитарной молекулосвязанной активации — SLAM-ассоциированный); измерение этого белка может быть использовано в диагностике состояния (Gilmour et al., 2000).
С XLP связан высокий уровень заболеваемости, и во всех случаях исход неблагоприятный. В настоящее время аллогенная трансплантация стволовых клеток остается единственным лечебным мероприятием (Lankester et al., 2005).
Похожий синдром моно- и поликлональной лимфоцитарной пролиферации, обусловленный ВЭБ, известный как посттрансплантационное лимфопролиферативное заболевание (ПТЛЗ), может развиваться при ослабленном иммунитете, особенно у реципиентов пересаженных органов (Randhawa et al., 1992). ПТЛЗ может проявляться полиорганными поражениями, нечасто вовлекая ЦНС. Поражение мозга у реципиентов с ПТЛЗ дает неблагоприятный прогноз; однако изолированное вовлечение ЦНС имеет лучший прогноз, чем одновременное поражение ЦНС и внечерепных органов (Buell et al., 2005). Исследование детей после трансплантации печени показало, что мониторинг вирусной нагрузки ВЭБ при раннем вмешательстве может уменьшить количество случаев ПТЛЗ (Lee et al., 2005).
Комбинированное лечение с иммунной модуляцией, противовирусными средствами и анти-В-клеточными моноклональными антителами ритуксимаба обеспечивает определенный эффект (Nozzoli et al., 2006).
У пациентов с более прогрессирующей ВИЧ-иммуносупрессией ВЭБ может привести к развитию лимфомы. Это может быть изолированная лимфома ЦНС или же поражение ЦНС при более распространенном заболевании (Nadal et al., 1994). В настоящее время проводится разработка более эффективного лечения вызываемой ВЭБ лимфомы у пациентов с ВИЧ, включая противовирусную терапию, химиотерапию и иммуномодулирующее лечение.
в) Полиомавирусная инфекция человека. JC-вирус — это человеческий нейротропный полиомавирус, который вызывает прогрессивную мультифокальную лейкоэнцефалопатию (ПМЛ), смертельное демиелинизирующее заболевание у иммунодефицитных пациентов. Сообщалось о случаях у детей с ВИЧ, после лечения злокачественных новообразований и у детей с врожденной иммунной недостаточностью (Redfearn et al., 1993; Bezrodnik et al., 1998; Angelini et al., 2001; Nuttall et al., 2004; Demir et al., 2005). Заболевание может начинаться медленно как расстройство с когнитивным нарушением или быстро прогрессировать с припадками, гемипарезом, нарушениями двигательных функций или с утратой зрения. На МРТ черепа могут быть распространенные повреждения белого и серого вещества. Исход без лечения и восстановления иммунитета обычно смертельный через несколько месяцев. Пациенты с прогрессирующей формой ВИЧ могут развить острую симптоматику ПМЛ вскоре после начала противовирусной терапии, что рассматривается как еще одно проявление синдрома воспалительного восстановления иммунитета (Nuttall et al., 2004).
г) Полиовирусная инфекция (дикий и поствакцинальный тип). Полиовирус у пациентов с ослабленным иммунитетом может вызвать развитие типичной картины паралитического полиомиелита. Имеются описания случаев при Х-сцепленной гипогаммаглобулинемии (Wright et al., 1977) и нарушении Т-клеточного звена иммунитета. В качестве исключения может иметь место более диффузное заболевание с вовлечением головного мозга и очагами кальцификации в зрительном бугре после вакцинации живым аттенуированным вирусом (Davis et al., 1977).
д) Хроническая энтеровирусная инфекция у детей с Х-сцепленной гипогаммаглобулинемией. Дети с Х-сцепленной гипогаммаглобулинемией (болезнью Брутона) часто страдают от вирусных инфекций ЦНС в сочетании с бактериальными осложнениями (гнойным менингитом). Наиболее распространенными возбудителями этих инфекций являются энтеровирусы (Cooper et al., 1983). Характерным клиническим проявлением является хронический лимфоцитарный менингит с различными признаками поражения мозга, такими как нарушение сознания и очаговые припадки или неврологический дефицит. Другие симптомы включают в себя прогрессирующую миелопатию, миелопатию, прогрессирующую до энцефалопатии, простую энцефалопатию, ретинопатию, нейросенсорную тугоухость и дерматомиозит (Rudge et al., 1996). Течение хроническое, нередко с летальным исходом. Диагностика по результатам ПЦР-исследования ликвора или же по биопсии ткани в некоторых случаях, а для контроля эффективности можно использовать количественную оценку ПЦР (Quartier et al., 2000).
Интратекальное и внутрижелудочковое введение гаммаглобулинов может помочь уменьшить симптомы, но не выводит инфекцию (Erlendsson et al., 1985; Johnson et al., 1985).
Редактор: Искандер Милевски. Дата публикации: 23.12.2018
Иммунная система человека выступает в качестве приобретенной в течение жизни защиты внутренней среды от различного рода заболеваний. Процесс формирования естественной устойчивости начинается еще в утробе матери, а после рождения проходит ряд периодов, в течение которых вырабатывается иммунитет. Ознакомиться с принципами формирования и укрепления иммунитета ребенка поможет представленная публикация.
Как формируется иммунитет у новорожденного ребенка?
В период развития плода ребенка в утробе матери осуществляется образование врожденного иммунитета. Под данным видом иммунной защиты предполагается выработка устойчивости, которая передается новорожденному от матери на генетическом уровне.
Процесс формирования защиты детского организма начинается с образования лимфоцитов типа В в период с 3 по 8 неделю беременности. Между 5 и 12 неделей беременности происходит выработка лимфоцитов типа Т. В третьем триместре у будущего малыша наступает этап образования глобулинов иммунитета. Поэтому дети, рожденные раньше положенного срока, подвержены частым простудным и инфекционным заболеваниям.
Наследственный врожденный иммунитет начинает действовать после рождения ребенка, защищая его от чужеродных вирусов и бактерий. Продолжительность действия иммунитета новорожденного составляет до 4-6 месяцев после рождения.
Сформированная в утробе матери иммунная устойчивость после появления ребенка на свет осуществляет защитные функции только на 50 процентов. Поэтому важным этапом, в течение которого закладывается основа здоровья малыша, выступает период грудного вскармливания. Переданные с молоком матери полезные вещества невозможно заменить искусственным питанием. Длительность кормления малыша материнским молоком не должна быть меньше года.

Основные этапы формирования иммунной защиты
Процесс формирования иммунитета ребенка проходит ряд периодов. Начальные этапы образования иммунной системы ребенка закладывают основу будущего здоровья человека. Поэтому во время взросления ребенка важно уделять особое внимание мероприятиям, направленным на повышение устойчивости организма малыша разного рода заболеваниям.
Основные этапы формирования иммунитета ребенка:
Первый этап начинается в первом триместре беременности, когда наблюдается первичная активность лимфоцитов типа В. Врожденный иммунитет ребенка наилучшим образом осуществляет защитные функции детского организма в первые месяцы жизни. До наступления полугода внутренняя среда ребенка оказывает сопротивление вирусам и бактериям за счет переданной от матери устойчивости.
Второй этап начинается с четырех — шести месяцев. Начиная с этого времени иммунитет новорожденного, переданный от матери, ослабевает, повышая риск проникновения болезнетворных микроэлементов во внутреннюю среду малыша. Благоприятное влияние на процесс формирования собственного иммунитета ребенка оказывает грудное вскармливание. С материнским молоком в организм малыша поступают полезные ферменты, глобулины типа А, создающие защитный барьер ребенка. В этот период времени детский организм наиболее восприимчив к заболеваниям, поэтому важно следить за его здоровьем и при необходимости провести вакцинацию от инфекций.
Третий этап начинается со второго — третьего года жизни ребенка. Он характеризуется, как первый критический период для иммунитета. Поскольку малыш начинает активно контактировать с внешним миром, повышается риск попадания во внутреннюю среду возбудителей заболеваний. Это создает основу для формирования специфической устойчивости и развития иммунной памяти малыша.
Четвертый этап имеет место после наступления ребенку пяти — семи лет. В данный период времени процесс формирования собственного иммунитета ребенка завершается. У малыша активно вырабатываются лимфоциты, действует клеточная и гуморальная защита. Благодаря сформированной иммунной памяти при повторном попадании чужеродных микроэлементов, иммунная защита оказывает активное сопротивление, что способствует предотвращению заболевания или его протеканию в более легкой форме.
Пятый этап наступает в подростковом возрасте, с 12 — 15 лет. Обозначенный период характеризуется перестройкой детского организма и изменением гормонального фона. Органы иммунной системы (лимфаузлы) изменяются в размере и снижают сопротивляемость чужеродным антителам, поэтому иммунитет ослабевает, что провоцирует проявление хронических заболеваний.

Признаки ослабленной иммунной защиты
Распознать ослабленный иммунитет у ребенка можно при обнаружении следующих признаков:
- Частые простудные заболевания, которые отличаются длительностью курса лечения;
- Наличие хронических заболеваний, провоцирующих снижение защитных функций малыша;
- Утомляемость;
- Сонливое состояние;
- Неспокойный сон;
- Развитие аллергии;
- Еще одним признаком ослабленной иммунной защиты малыша является частое воспаление и продолжительный период заживления открытых ран;
- Поднятие температурного режима без видимых причин.
При наличии одного из представленных симптомов рекомендуется обратить внимание на необходимость проведения мероприятий по укреплению ослабленной иммунной защиты малыша.

Как выработать иммунитет у ребенка?
Проводить мероприятия по укреплению защитных функций детского организма требуется с момента рождения малыша. Особое внимание важно уделять рекомендациям, позволяющим выработать иммунитет.
Общие рекомендации:
- Избегать контактирования ребенка с болеющими людьми;
- Не следует пренебрегать грудным вскармливанием новорожденных малышей;
- Выработать иммунную защиту у ребенка можно посредством прививания полноценного и здорового питания;
- Исключение стрессовых ситуаций;
- Для укрепления иммунной системы не рекомендуется самостоятельно назначать лекарственные препараты для лечения или принимать продолжительный период времени антибиотики;
- Важно соблюдать режим активности и отдыха малыша;
- Уделить внимание процедурам закаливания;
- Частые прогулки на свежем воздухе.
Поскольку использование полезных продуктов питания не помогает надлежащим образом восполнить нехватку полезных микроэлементов, дополнительному поднятию иммунитета способствует употребление препаратов, содержащих в составе комплекс полезных витаминов и минералов. Среди наиболее качественных лекарственных средств выделяют: ИРС 19, Настойка эхинацеи, Тималин, Виферон, Циклоферон, Иммунал, Йодомарин, Оциллококцинум, Имунорикс, Амиксин. Применять витаминные добавки в виде препаратов рекомендуется, соблюдая представленные советы.
Для приготовления лекарственных средств для укрепления иммунитета малышей и подростков используются: прополис, мед, женьшень, эхинацея, имбирь, лимон, орехи, сухофрукты, чеснок, алоэ, ромашка, шиповник. Приготовленные домашние лекарства на основе целебных растений и трав можно использовать для лечения или профилактики заболеваний.
Получить полезную информацию по данному вопросу можно по ссылке.
Регулярное следование представленным рекомендациям позволит выработать крепкий иммунитет детского организма с первых лет жизни и избежать развития серьезных заболеваний в течение жизни.
Читайте также:


