Принимать при инфекции при онкологии
Больные, находящиеся на лечении по поводу злокачественных новообразований, за счет измененного иммунного статуса подвержены простудным заболеваниям, которые в свою очередь еще больше истощают защитные силы организма и затрудняют терапию основного диагноза
Острые респираторные вирусные инфекции (ОРВИ), в том числе и грипп, составляющие основную долю инфекционной патологии населения всех возрастов, представляют существенную угрозу пациентам из групп риска: пожилым, беременным, детям младшего возраста и пациентам с хроническими заболеваниями, в том числе онкологическими.
Больные, находящиеся на лечении по поводу злокачественных новообразований, за счет измененного иммунного статуса подвержены простудным заболеваниям, которые в свою очередь еще больше истощают защитные силы организма и затрудняют терапию основного диагноза.
При ОРВИ на фоне онкологического процесса лечащий врач сталкивается со следующими трудностями:
- Длительность ОРВИ у иммунокомпрометированных пациентов может достигать нескольких недель, в течение которых состояние больных значительно ухудшается, и не только по иммунным показателям.
- Инфекционный процесс заставляет откладывать очередной курс химиотерапии, что сильно сказывается на прогнозе.
- Назначение противовирусной терапии может вызвать осложнения, а в частности лекарственную гепатотоксичность, так как ее эффект накладывается на гепатотоксичное действие фармакотерапии злокачественного заболевания 1 .
Таким образом, можно сказать, что необходимость в профилактике и терапии ОРВИ у онкологических пациентов неоспорима, но последнее упомянутое обстоятельство резко ограничивает выбор конкретного средства.
Вирус-специфические препараты римантадин, занамивир и осельтамивир доказали свою эффективность, которая распространяется однако только на вирус гриппа. Кроме того, эти средства имеют ряд противопоказаний, которые зачастую делают невозможным их применение у онкологических пациентов.
В случае назначения средств, действующих на определенные вирусные белки, следует учитывать также проблему резистентности, которую вырабатывают к ним вирусы 2 . Так, появились данные о повышении до 18% частоты устойчивости вирусов гриппа А (H3N2) к осельтамивиру среди детей, получавших данный препарат для лечения гриппа 3 .
В связи с вышесказанным сегодня как никогда высока потребность в противовирусных препаратах, действующих не на инфекционный агент, а на иммунные защитные механизмы.
Оптимальное противовирусное средство, которое может быть рекомендовано для онкологической практики, должно:
- не вызывать резистентности, вероятно вследствие отличного механизма действия;
- быть безопасным, в частности при длительном применении;
- иметь минимальный риск побочных эффектов при лекарственном взаимодействии.
Указанным критериям в полной мере соответствуют иммуномодулирующие средства, благодаря чему интерес к ним клиницистов-онкологов в последние годы резко возрос.
Иммуномодуляторы – это лекарственные средства, которые обладают иммунотропной активностью и в терапевтических дозах восстанавливают эффективную иммунную защиту. Растущая опухоль вызывает существенные изменения в иммунном ответе, а проводимая химио- и лучевая терапия, а также любые оперативные вмешательства вызывают или усугубляют иммунную недостаточность 4 . Поэтому использование иммуномодуляторов, в частности для лечения сопутствующих инфекций, является оправданным.
Главной особенностью релиз-активных препаратов является способность воздействовать на биологически активные молекулы мишени (эндогенные регуляторы), модифицируя их физико-химические свойства. Эффект проявляется не только на молекулярном, но и на клеточном, органном, системном и организменном уровнях.
Так, прием Эргоферона усиливает функциональную активность макрофагов, натуральных киллеров и ИФН при помощи релиз-активных антител к ИФН-γ и CD4+. На этапе цитотоксических клеточных реакций CD8+ и CD4+ Т-лимфоцитов Эргоферон поддерживает противовирусный иммунитет при участии компонента релиз-активных антител к CD4+. На более поздних этапах релиз-активные антитела к CD4+ через стимуляцию рецепторов CD4 Тх2 поддерживают гуморальный противовирусный иммунитет.
Третий компонент Эргоферона – релиз-активные антитела к гистамину – обеспечивает противовоспалительный и антигистаминный эффекты, которые проявляются уменьшением длительности и выраженности катаральных симптомов и аллергических реакций, сопутствующих инфекционному процессу 7 . Это является важным преимуществом Эргоферона перед другими противовирусными препаратами, так как позволяет снизить потребление других средств и нивелировать риск лекарственного взаимодействия при параллельно проводящейся противоопухолевой терапии.
Эргоферон применяется в клинической практике с 2011 года, и его эффективность была доказана в ходе рандомизированных клинических исследований. На данный момент завершено 3 клинических исследования и продолжаются еще 4.
Исследований по лечению ОРВИ именно у онкологических больных не проводилось. Однако в клинической практике накоплен опыт назначения Эргоферона госпитализированным больным с солидными опухолями (Шаповалова Ю.С). Учитывая актуальность проблемы отсрочек курсов химиотерапии и продления сроков госпитализации, в 2012 г. был разработан внутрибольничный протокол лечения ОРВИ у госпитализированных пациентов с солидными злокачественными новообразованиями. В него включены следующие противовирусные препараты: для лечения гриппа – ингибиторы нейраминидазы занамивир и осельтамивир, а также римантадин, умифеновир и Эргоферон; для лечения ОРВИ – умифеновир и Эргоферон. Эргоферон применялся в виде монотерапии (37 пациентов) или в комбинации с римантадином (14 пациентов) в течение первых 48 часов от начала проявления симптомов заболевания. Все пациенты выздоровели через 5-9 дней лечения; нежелательных реакций, связанных с изучаемой терапией, отмечено не было. Учитывая благоприятный профиль переносимости Эргоферона и отсутствие гепатотоксичности, его применение может быть востребовано для лечения ОРВИ у пациентов онкологического профиля, в том числе находящихся в процессе химиотерапии.
Следует также отметить, что согласно экспериментам использование релиз-активных антител к ИФН-γ не приводит к гиперпродукции ИФН-γ. Этот факт немаловажен в свете недавних исследований, показавших, что ИФН-γ в больших дозах может приводить к увеличению метастазирования в легкие и резистентности клеток меланомы к терапии 11 .
Учитывая безопасность Эргоферона, доказанную в исследованиях высокого методологического качества, можно сделать вывод, что препарат стоит рекомендовать для лечения ОРВИ у пациентов со злокачественными новообразованиями 12 .
Как доказали результаты экспериментальных и клинических исследований Эргоферон является перспективным противовирусным препаратом с принципиально новым механизмом и мишенями воздействия, и он может помочь решить проблему лечения больных в условиях изменчивости антигенных свойств вирусов и исходно скомпрометированного иммунного статуса. Комплексный препарат, сочетающий противовирусное, иммуномодулирующее, противовоспалительное и антигистаминное действие, оказывает выраженный терапевтический эффект при ОРВИ у пациентов с онкологической патологией. Препарат имеет благоприятный профиль безопасности, и его назначение позволяет снизить лекарственную нагрузку и риск лекарственного взаимодействия с противоопухолевыми препаратами.
1 Шаповалова Ю.С. Клинико-фармакологическое обоснование и опыт применения инновационного релиз-активного препарата в лечении острых респираторных вирусных инфекций. Справочник поликлинического врача. 2015;2:38-42.
2 Heaton NS et al. Genome-wide mutagenesis of influenza virus reveals unique plasticity of the hemagglutinin and NS1 proteins. Proc Natl Acad Sci USA 2013; 25.
3 Антимикробная терапия по Джею Сэнфорду. Под ред. Д.Гилберта, Р.Меллеринга мл., Дж.Элиопулоса и др. М.: ГРАНАТ, 2013.
4 Артамонова Е.В. Модификаторы биологических реакций (иммуномодуляторы, интерфероны, интерлейкины) в терапии злокачественных опухолей. Эффективная фармакотерапия. 2014; 14: 8-21.
5 Сыроешкин А.В., Никифорова М.В., Колдина А.М., Горнак А.А., Тарабрина И.В. Лекарственные препараты на основе релиз-активных антител. Справочник поликлинического врача. 2018 (3):15-20
6 Эпштейн О.И. Сверхмалые дозы (история одного исследования). М.: Изд-во РАМН, 2008.
7 Жавберт Е.С., Дугина Ю.Л., Эпштейн О.И. Противовоспалительные и противоаллергические свойства антител к гистамину в релиз-активной форме: обзор экспериментальных и клинических исследований. Детские инфекции. 2014; 1: 40-3.
8 Архивъ внутренней медицины. 2013; 14 (6): 46.
9 Шиловский И.П., Корнилаева Г. В., Хаитов М.Р. Новые возможности в терапии респираторно-синцитиальной вирусной инфекции: данные доклинического исследования препарата Эргоферон. Иммунология. 2012; 33 (3): 144-8.
11 Taniguchi K, Petersson M, Höglund P et al. Interferon gamma induces lung colonization by intravenously inoculated B16 melanoma cells in parallel with enhanced expression of class I major histocompatibility complex antigens. Proc Natl Acad Sci USA 1987; 84 (10): 3405-9.
12 Артамонова Е.В. Модификаторы биологических реакций (иммуномодуляторы, интерфероны, интерлейкины) в терапии злокачественных опухолей. Эффективная фармакотерапия. 2014; 14: 8-21.
Инфекции — главные причины смерти при раке. Они не только часто встречаются, но нередко имеют более тяжелое течение, чем у других пациентов, менее подверженных действию терапии, и иногда вызываются организмами, которые не патогенны для здоровых людей. Такая восприимчивость является следствием подавления защитных механизмов больного, вызванного опухолью и ее лечением.
Кожа и слизистые оболочки служат барьером для инфекции. Опухолевая инфильтрация и местная лучевая радиотерапия могут привести к повреждению лимфатических или венозных сосудов, что приводит к увеличению восприимчивости к локальной инфекции. Воспроизводство эпителиальных клеток в желудочно-кишечном тракте подавляется химиотерапией, из-за чего повреждается и изъязвляется слизистая, что позволяет организмам из кишечника попасть в систему воротной вены.
Кожа повреждается внутривенными иглами и канюлями, особенно туннельными подкожными каналами. Это частые источники инфекции, которые вызываются такими кожными организмами, как Staphylococcus epidermidis. В носоглоточной полости возникают инфекции, вызванные Candida albicans.
Рак при запущенной стадии иногда связан с ухудшением функций и нейтрофилов, и моноцитов. Было описано подавление хемотаксической, фагоцитарной и бактерицидной активностей.
Ослабленная замедленная гиперчувствительность довольно распространена при запущенной болезни Ходжкина, но менее часта в других случаях злокачественных опухолей. Лимфопения неизменно вызывается действием алкилирующих агентов и массивной радиотерапией. Клеточный иммунитет особенно важен при защите организма хозяина от грибов, вирусов, туберкулеза и простейших.
Интенсивная цитотоксическая химиотерапия ведет к ухудшению образования антител к бактериальным и вирусным антигенам.
Циркулирующие бактерии удаляются фагоцитарными клетками, находящимися в синусах ретикулоэндотелиальной системы, особенно в печени и селезенке. Для этой чистки важны антитела и белки системы комплемента. Спленэкто-мия увеличивает риск серьезной бактериальной инфекции, особенно пневмококковый сепсис в детском возрасте и в меньшей степени во взрослом.
Бактериемия и септицемия у больных раком
Инфекции кровяного русла довольно часты у пациентов с гранулоцитопенией. Патогенами часто являются грамотрицательные бактерии (Escherichia coli, Pseudomonas aeruginosa), стафилококки и стрептококки. Увеличивается частота инфекций, вызванных грамположительными бактериями, особенно Staphylococcus epidermidis. Пациенты с тунельными подкожными каналами особенно подвержены поражениям этим организмом.
Жар у пациента с нейтропенией при раке — показатель присутствия бактерий в крови и под кожей. Если существует очевидный источник инфекции, например инфицированный порт для инфузий, следует взять культуру бактерий и удалить канюлю. Лечение не следует откладываеть для пациента с нейтропенией. Пациенты с лихорадочной нейтропенией с относительно низким риском развития серьезных осложнений относятся к тем, кого лечат короткими циклами химиотерапии для солидных опухолей.
Эти пациенты должны быть госпитализированы. Недавние исследования показали, что пероральный прием амоксициллина-клавуланата комбинированный с пероральным приемом ципрофлоксацина так же эффективен, как и внутривенная химиотерапия в этой группе (70% пациентов). Пациенты с высоким риском (с неконтролируемым раком или на стационарном лечении интенсивной терапией) лечатся внутривенными антибиотиками, в том числе b-лактамом и аминогликозидом или цефтазидимом.
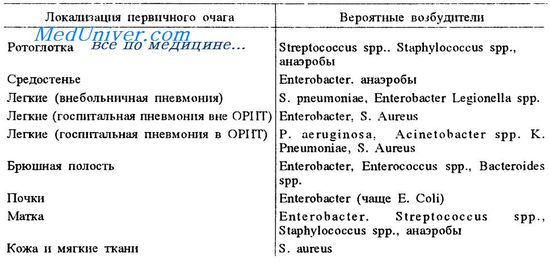
Респираторные инфекции у больных раком
У пациента с серьезным подавлением иммунитета довольно часто возникает жар с легочным инфильтратом. Главные причины этого даны в таблице.
Осложнения в постановке диагноза могут быть значительны, поскольку тесты слюнных и кровеносных культур иногда отрицательны, а более инвазивные процедуры, такие как трансбронхиальная биопсия, невозможны из-за тромбоцитопении или общего состояния пациента.
Существуют некоторые клинические особенности, которые помогают при постановке диагноза. Кавитация наиболее часто сопровождает поражения анаэробными бактериями, стафилококками и микобактериями. Инфекции Pneumocystis вызывают заметную одышку, а на рентгенограмме грудной клетки видны билатеральные инфильтраты, обычно состоящие из хилуса. Болезнь, однако, может протекать вяло и вызвать долевое уплотнение. Цитомегаловирусные инфекции встречаются главным образом у пациентов с серьезным подавлением иммунитета, в частности в течение аллогенной ВМТ. Болезнь может также вызывать миокардит, невропатию или офтальмию.
Легочные инфильтраты обычно билатеральны. Инфекции Candida вызывают широкое разнообразие изменений в рентгенограмме. Инфекции Aspergillus обычно быстро прогрессируют. Тесты культур крови обычно отрицательны, а инфильтраты возможны в одном или двух легких.
При затруднениях в постановке диагноза можно следовать следующей схеме.
У пациентов без нейтропении или тромбоцитопении исследовать посевы крови, слюны, бронхоскопические промывания и трансбронхиальную биопсию там, где это возможно. Если кровяные и слюнные культуры отрицательны, лечить антибиотиками широкого антибактериального спектра действия (обычно в комбинации с аминогликозидом, пенициллином и метронидазолом или аналогичными соединениями). Если возможной причиной инфекции является Pneumocystis, следует давать высокие дозы котримоксазола. Если ответа нет, рассмотрите ацикловир для вируса простого герпеса и противогрибковую терапию с амфотерицином или кетоконазолом. Ацикловир не эффективен против цитомегаловирусов.
Если кровяные или слюнные тесты положительны, лечите соответствующе, но если ответа нет, рассмотрите смешанные инфекции.
Пациентам с нейтропенией или тромбоцитопенией проводят бронхоскопию, но биопсия не всегда возможна, и лечение продолжают без дальнейшего диагностического исследования. До и после бронхоскопии иногда необходимы антибиотики и переливание тромбоцитов.

Инфекции мочевыводящих путей у больных раком
Инфекции часты у пациентов с затрудненным мочеиспусканием. Затруднения могут быть вызваны опухолью или ослаблением мочевого пузыря у пациентов с компрессией спинного мозга и его корешков. Диагноз ставится после исследования уринокультуры, и лечение осуществляется антибиотиками и снятием осложнений, если это возможно.
Желудочно-кишечные инфекции у больных раком
Молочница ротовой полости (инфекция, вызываемая Candida albicans) — частое осложнение химиотерапии. Она особенно распространена у пациентов с подавленным иммунитетом, у пациентов, принимающих стероиды и тех, кого лечат антибиотиками с широким спектром действия. Рот и глотка становятся очень болезненными, а белые пятна грибков видны на эри-темной основе. У плохо питающихся пациентов инфекция может проникать глубже и распространяться по пищеводу, желудку и кишечнику. Обычно эффективен пероральный прием нистатина, амфотерицина или миконазола.
Проявление вируса простого герпеса на губах часто проблематично для пациентов с лейкопенией, и повреждения могут быть довольно обширными. В данном случае необходимо местное применение ацикловира для пациентов с подавленным иммунитетом или систематический прием ацикловира при более серьезных инфекциях.
Инфекции, вызванные Candida в пищеводе, необходимо лечить пероральным приемом суспензии нистатина, но если такое лечение неэффективно, то необходимо применение кетоко-назола или короткий курс амфотерицина. Кишечные инфекции, возникающие при поражении Candida, должны лечиться амфотерицином.
Перианальные инфекции распространены среди пациентов с нейтропенией. Всегда необходимо применять профилактические меры совместно с тщательной гигиеной промежности и смягчителями стула для предотвращения запора и анальных трещин. Распространяющиеся перинеальные (паховые) инфекции могут угрожать жизни пациента, и требуется срочное лечение внутривенными антибиотиками, действующими против грамотрицательных и анаэробных бацилл.
Менингит у больных раком
Инфекции центральной нервной системы (ЦНС) довольно редки, но у пациентов с лимфомой или лейкемией иногда развивается менингит из-за Cryptococcus neoformans. Начало заболевания индивидуально у каждого и сопровождается головной болью. Микроорганизм обнаруживают при окрашивании India ink спинномозговой жидкости (CSF).
Выявление антигенов Cryptococcus в крови и CSF возможно у большинства пациентов. Состояние многих пациентов улучшается при приеме амфотерицина, некоторые вылечиваются.
Кожные инфекции у больных раком
В отличие от инфекции, представленной на портах для вливания, наиболее частое кожное заболевание — опоясывающий лишай (varicella zoster). Возникает из-за реактивации вируса varicella zoster в ганглии дорсального корешка, вызывает кожную пузырчатую сыпь, которая особенно серьезна у людей с подорванным иммунитетом, может распространяться как ветряная оспа и вызывать фатальную пневмонию. Пациентов следует лечить ацикловиром как можно быстрее.
— Многие специалисты высказываются о том, что коронавирусная инфекция COVID-19 представляет особую опасность именно для онкологических больных. Что известно об этом?
— Наши коллеги из Китая проделали (и продолжают делать!) невероятную работу: справившись с эпидемией у себя в стране, они проводят анализ многих аспектов своей деятельности в тех экстремальных условиях, в том числе исследуют, как влияет вирус на онкологических больных.
Действительно, наших пациентов можно смело причислять к группе риска. Китайские коллеги (пусть с помощью относительно небольшого числа больных с коронавирусом, имевших онкологические заболевания) выявили, что частота возникновения тяжёлых осложнений (вплоть до смерти) у наших пациентов в пять раз выше, чем у тех, кто никогда не имел злокачественной опухоли.
Эти результаты подтверждают, что необходимо быть особо настороженными как нам (онкологам. — RT), так и (прежде всего) самим пациентам с онкологией.
— С чем связана уязвимость онкологических больных?
— То сложное, иммуносупрессивное (искусственно угнетающее иммунитет. — RT) и крайне токсичное лечение рака, которое получают наши пациенты и которое чревато многими осложнениями даже в благополучные эпидемиологические периоды, значительно ослабляет собственные ресурсы организма. К примеру, в условиях лейкопении (снижения количества лейкоцитов) и лимфопении (снижение числа лимфоцитов), возникающих при проведении химиотерапии и облучения (и тем более при одновременной химиолучевой терапии), организму справиться с вирусом будет крайне сложно.
— То есть дело ещё и в пониженном иммунитете, верно?
— Говорить о снижении иммунитета мы можем в том случае, если соответствующим образом обследуем больного — делаем иммунограмму, определяем количество Т- и В-лимфоцитов (клеток иммунной системы. — RT), уровень иммуноглобулинов — и видим отклонения. У онкологических больных это, как правило, не делается.
Но во многих случаях развитие злокачественного процесса уже подразумевает некий иммунный сбой, а добавление осложнений типа лейкопении (после химиотерапии или облучения) общую картину здорово усугубляет. Не забудьте ещё и о необходимости регулярного посещения онкологического учреждения с целью лечения или контроля. Поэтому ещё раз повторю: наши пациенты действительно находятся в группе повышенного риска в плане инфицирования и тяжёлого течения болезни.
— Пациенты с какими онкологическими заболеваниями больше подвержены риску?
— Полагаю, что любой онкологический пациент, находящийся в стадии активного противоопухолевого лечения либо подлежащий ему (по результатам проведённого обследования), находится в группе повышенного риска. Если имеются осложнения лечения — риск возрастает.
Пациент, который уже полностью прошёл полагающееся лечение, у которого осложнения благополучно купированы или их вовсе не было, которому предстоит просто динамическое наблюдение при отсутствии признаков активного опухолевого процесса, тоже не должен расслабляться.
— Способен ли коронавирус увеличить риск возвращения болезни у пациентов, у которых на данный момент рак перешёл в стадию ремиссии?
— Думаю, нет. Коронавирус имеет шансы стать сезонной инфекцией, волнообразно захватывающей регионы. Да, возможно, с более тяжёлым течением, чем обычный грипп. Если бы подобная инфекция стимулировала всплеск онкологического заболевания, по весне онкоцентры задыхались бы от количества рецидивирующих пациентов. Но этого не происходит.
— Если у пациента с онкологией обнаружен коронавирус, стоит ли прерывать противоопухолевое лечение?
— Полагаю, что ни о каком продолжении противоопухолевого лечения при обнаружении коронавирусной инфекции у онкологического больного не может быть и речи.
Такой пациент должен быть изолирован и получать обычное поддерживающее лечение на дому в случае лёгкого течения заболевания либо быть госпитализирован в инфекционный стационар при более серьёзных формах заболевания. Риск тяжёлых осложнений (вплоть до смерти) в большинстве случаев будет слишком высок.
— Не опасны для онкологических больных противовирусные препараты? Можно ли их принимать для профилактики коронавируса?
— Любой препарат может нести в себе потенциальный риск побочных осложнений: от аллергических реакций до токсического воздействия на печень или другие органы.
Принимать какие-либо противовирусные препараты для профилактики коронавируса нет смысла. Во-первых, потому что пока ни один из них не подтвердил свою эффективность при коронавирусе, многие надежды не оправдались. А во-вторых, по причине возможной токсичности.
Основную профилактику мы знаем прекрасно: дистанцированность или изоляция, частое и тщательное мытьё рук, обработка всех контактных поверхностей антисептиками и так далее.
— Рекомендуете ли вы пациентам с онкологией более жёсткий карантинный режим, чем для остального населения?
— Однозначно. Нахождение дома — лучшая мера для предотвращения больших проблем, и не только для онкологических больных. Сами пациенты организовывать своё противоопухолевое лечение не должны. Они это делают под руководством и строгим наблюдением врачей-онкологов. Их задача — строго выполнять все рекомендации.
— Во многих странах в связи с пандемией коронавируса меняется порядок оказания помощи онкологическим больным. Изменилось ли что-то в работе онкологов в нашей стране?
— Онкологические центры оказывают плановую помощь, оставлять наших пациентов без планового, требующего соблюдения определённых сроков и режимов лечения никто не собирается, однако необходимые меры должны быть приняты. Связаны они прежде всего с уязвимостью онкологических пациентов.
Каждый онколог на своей линии фронта — хирург, химиотерапевт, радиотерапевт — определённым образом реорганизует работу: возможно, отменяет особо травматичные операции, переводит пациентов на таблетированную химиотерапию и так далее.
Например, в отделении лучевой терапии Ульяновского областного онкологического диспансера, которое я возглавляю, мы уже три недели работаем в особом режиме. Все пациенты, которые были запланированы на этот период, поступили на лечение. Но при этом мы постарались чётко разграничить потоки больных, не допускать скученности в отделении, с большей частотой проводить уборку, по возможности назначать укороченные, хоть и чуть более интенсивные курсы лучевой терапии — конечно, если это позволяет не превышать допустимые дозы на здоровых органах.
Кроме того, мы временно отказываемся от одновременного химиолучевого лечения, чтобы не провоцировать у пациентов развитие более выраженных осложнений — прежде всего со стороны крови. В тех ситуациях, когда курс лучевой терапии можно безболезненно отсрочить, мы это делаем.
Однако общение с коллегами из других регионов показывает, что далеко не во всех центрах были приняты какие-либо меры организационного характера — как по защите пациентов, так и по защите персонала. Как бы эта инертность (или надежда на русский авось?) не вышла боком.

Антибиотики и химиотерапия имеют много общего не только потому, что это незаменимые лекарственные средства, без которых невозможна современная жизнь человека. В фармакологической литературе антибиотики часто называют химиотерапевтическими препаратами, а процесс их лечебного применения — антимикробной химиотерапией, хоть им не присуще даже минимальное противораковое действие. Без противоопухолевых антибиотиков невозможно эффективное лечение большого спектра злокачественных новообразований, но бактериям они не страшны.
Можно ли принимать антибиотики при химиотерапии
Зачастую поводом для назначение противомикробных препаратов онкологическому больному становятся воспалительные последствия противоопухолевой химиотерапии, когда снижение иммунных защитных сил организма до минимального уровня позволило активное размножение и распространение бактерий.
Антибиотики и химиотерапия одновременно не используются, за исключением местных антибактериальных мазей при кожных воспалительных осложнениях иммуно-онкологических препаратов. Иммуно-онкологические препараты не убивают клетки, а только активируют лимфоциты для борьбы с опухолью, легкое поражение кожи аутоиммунного характера не требует снижения дозы иммунного средства. При кожной инфекции 3-4 степени начинают приём антибиотика в таблетках, а иммунный препарат отменяется, пока клинические симптомы не достигнут уровня 1-2 степени.
Антибиотики и химиотерапия решают разные проблемы больного человека: антимикробные лекарства борются с воспалительными процессами, когда по состоянию здоровья противопоказана любая химиотерапия, потому что способна усугубить тяжесть воспаления или инфекции за счёт активного подавления иммунитета.
Показания к применению антибиотиков при онкологии
В жизни онкологического больного достаточно возможностей для активизации болезнетворной микрофлоры с формированием местного или распространенного воспаления, часто с исходом в обширный гнойный процесс и сепсис из-за недостаточности иммунитета после химиотерапии. Самое частое инфекционное осложнение при онкологии — пневмония, она стала одной из ведущих причин смерти больных раком. Чуть реже после химиотерапии отмечаются инфекции полости рта, кандидоз пищевода, инфекции мочевых путей при опухолевых нарушениях их проходимости, стрептококковые поражения кожи и у 5% гнойные парапроктиты.
Вырабатывая специальные вещества, прогрессирующая злокачественная опухоль тоже активно подавляет иммунитет, но наиболее вероятная и самая частая причина инфекционных осложнений — снижение в результате химиотерапии уровня лейкоцитов, и главным образом, фракции сегментоядерных или нейтрофилов. Падение абсолютного числа нейтрофилов до 500 клеток в миллилитре крови, при норме более 1500, на 50% повышает вероятность развития инфекции.

Факторы риска развития инфекционного воспаления у онкологического больного на фоне снижения уровня нейтрофильных лейкоцитов после химиотерапии:
- мукозит 3-4 степени, когда в слизистой пищеварительного тракта в результате действия химиотерапии погибают нормальные клетки, образуя очаговые дефекты слизистого покрова, через которые в кровь внедряются болезнетворные микроорганизмы;
- энтероколит — повреждение цитостатиками слизистой кишечника нарушает баланс и состав собственной кишечной микрофлоры, место которой активно занимается другими классами бактерий и грибами;
- постоянные сосудистые катетеры, в том числе порты, на внутренней поверхности могут содержать попавшую из воздуха патогенную микрофлору;
- недостаточность печени или почек, а также тяжелые сопутствующие заболевания, обострившиеся в результате противоопухолевого лечения, меняют тканевой гомеостаз и способствуют застою крови во внутриорганной кровеносной сети, создавая идеальные условия для жизнедеятельности и размножения патогенных агентов;
- изначальное снижение сопротивляемости определенным видам микроорганизмов —инкапсулированным у страдающих злокачественными болезнями лимфоидной ткани;
- пребывание в стационаре всегда сопряжено с возможностью инфицирования постоянной госпитальной микрофлорой, потому что в больницу попадают пациенты с разнообразными заболеваниями, в том числе скрытые носители патогенной микрофлоры.
Основания для назначения антибиотиков онкологическому больному:
- на фоне снижения нейтрофилов у пациента дважды за сутки температура выше 38° или один раз больше 38,3 °, что именуется как фебрильная нейтропения;
- на рентгене выявляется пневмония при соответствующих клинических симптомах;
- обнаружен гнойной очаг в тканях, чаще всего абсцесс;
- развился синдром системной воспалительной реакции при отсутствии явной пневмонии и других воспалительных процессов или гнойных очагов.
Отдельно обсудим синдром системной воспалительной реакции, считающийся манифестацией генерализованного распространения патологической микрофлоры или признаком скрытого воспалительного очага, который не удалось обнаружить. Для диагностирования синдрома у любого человека, и не только онкобольного, достаточно выявить в любом сочетании только два признака из пяти указанных:
- повышение температуры тела пациента выше 38° или ниже 36°;
- лейкоцитоз свыше 12 тысяч или, наоборот, лейкопения менее 4 тысяч, причём даже без расчёта абсолютного числа нейтрофилов;
- тахикардия более 90 ударов в минуту;
- учащение дыхания более 20 в минуту;
- явная или только предполагаемая инфекция у пациента.
При снижении показателей белой крови в сочетании с высокой лихорадкой лечение антибиотиками должно начинаться безотлагательно, на всё предварительное обследование и установление очага инфекции, если таковой имеется, отводится не более часа. В большинстве случаев антибиотик выбирается эмпирически, потому что выявление возбудителя и определение его чувствительности к антибиотикам — длительный процесс, а времени на раздумья нет. Очень часто при фебрильной нейтропения инфекционного очага так и не находят, что также свидетельствует об эффективности антибактериальной терапии, препятствующей формированию видимого глазом воспаления.
Не существует противопоказаний для применения каких-либо групп антибиотиков или отдельных лекарств, запрещается использовать заведомо неэффективные антибактериальные препараты. Известны наиболее частые микроорганизмы, вызывающие инфекции у российских пациентов, для каждого микроорганизма известен спектр антибиотиков, к которым он должен быть чувствителен. Тем не менее, у каждого пациента исследуют кровь на стерильность и делают её посев на культурную среду, чтобы в случае неэффективности стандартной комбинаций антибиотиков изменить схему лечения на оптимальную.
Совместимость антибиотиков и химиотерапии
Не следует у пациента с лейкопенией применять антибиотики, негативно влияющие на белый росток кроветворения для исключения суммации побочных эффектов. При угнетении кроветворения наряду с лечением инфекции антибиотиками обязательно проводится стимуляция белого ростка костного мозга колоние-стимулирующим фактором, ускоряющим выработку и созревание лейкоцитов.
При химиотерапии нефротоксичными цитостатиками нецелесообразно лечить воспаление повреждающими почки антибиотиками. Пока не найдено лекарств для купирования печеночной и почечной токсичности при химиотерапии, не существует и способов восстановления повреждения печени и почек при антимикробном лечении.
Точно также не совместимы повреждающие слуховой нерв антимикробные с ототоксичными химиопрепаратами.
Нет абсолютно безопасных лекарств, тем не менее, первое на что необходимо ориентироваться при выборе антибиотика — это чувствительность к лекарству микробного агента.
Применение антибактериальных средств после курса химиотерапии
Клинические рекомендации предлагают множество комбинаций из полутора десятков антибактериальных препаратов разных групп. Терапия фебрильной нейтропении начинается с внутривенного введения комбинированного пенициллина (тазоцим) каждые 6 часов или цефалоспорина IV поколения, требующего трех инъекций на протяжении суток. Если у пациента есть указания на аллергическую реакцию на пенициллины или за три дня антимикробной терапии состояние не улучшилось, прибегают к карбапенему.

Присутствие устойчивого к метициллину стафилококка меняет начальную антибактериальную терапию на препарат выбора — ванкомицин и ему подобные, а при необходимости все вышеуказанные антибиотики становятся дополнением к нему.
Разработаны стандартные программы и лекарственные комбинации антибиотиков для купирования инфекций, вызванных несколькими бактериальными агентами, в том числе устойчивыми к резервным препаратам и с учётом возможной непереносимости больным.
Какие побочные эффекты вызывает комбинация веществ?
Комбинации антибиотиков с неодинаковым механизмом действия на бактерию решают задачу максимально быстрого купирования воспалительного процесса и одновременно способствуют замедлению формирования лекарственной устойчивости.
В комбинации предпочитают не включать лекарства с однонаправленной токсичностью или перекрестной резистентностью. Антибактериальные вещества подавляют не только патологические, но и нормальные бактерии, приводя к нарушению баланса микрофлоры в кишечнике. Освободившиеся от бактерий место занимают грибы, борьба с которыми имеет свои сложности и может затягиваться, благо, что восстанавливается подавленный химиотерапией иммунитет и лимфоциты приступают к своим основным обязанностям — защите от любых патологических агентов.
Каждый лекарственный препарат оказывает негативное влияние на организм, спектр таких проявлений хорошо изучен, но непредсказуем в каждом отдельном случае. Именно поэтому есть сомнения в необходимости профилактического назначения антибактериальных препаратов при высоком риске развития фебрильной нейтропении. Большую целесообразность видят в профилактическом введении стимуляторов кроветворения, нежели в антимикробном средстве.
Тем не менее, при крайней необходимости, а крайняя необходимость — это уже существующая инфекция или нейтропения с высокой лихорадкой, надо выбирать из двух зол меньшее. Меньшее зло — это возможные, но не обязательные побочные эффекты антимикробного средства, большее зло — перспектива сепсиса и реальная угроза жизни больного.
Лечение инфекции у здорового человека — сложная задача, лечение инфекционных осложнений химиотерапии — это кроссворд со множеством неизвестных и единственной задачей — спасение от сепсиса и смерти. Врачи нашей клиники помогут в любой ситуации, даже кажущейся безвыходной. Наш интерес — ваше здоровье, и ради этого мы готовы на многое.
Читайте также:


