Проблемы особо опасных инфекций 2014
В мире достаточно много заболеваний, которые являются редкими, лечатся сложно или совсем не поддаются терапии. Чума и холера – особо опасные инфекции, которые ведут к смертельному исходу. Кроме них, конечно же, есть и другие, подробности о которых приведены ниже. Приказ об особо опасных инфекциях был издан ВОЗ. В нем были прописаны основные профилактические меры, поведение в случае заражения и контакта с больным.
Возбудителем особо опасной инфекции является бубонная палочка, открытая еще в 1894 году французским ученым Александром Йерсеном и японским врачом-бактериологом Китасато Сибасабуро. По их заключению, этот агент переносят на себе черные и серые крысы, сурки, суслики, песчанки, мышеподобные грызуны, кошки, верблюды, некоторые виды блох.
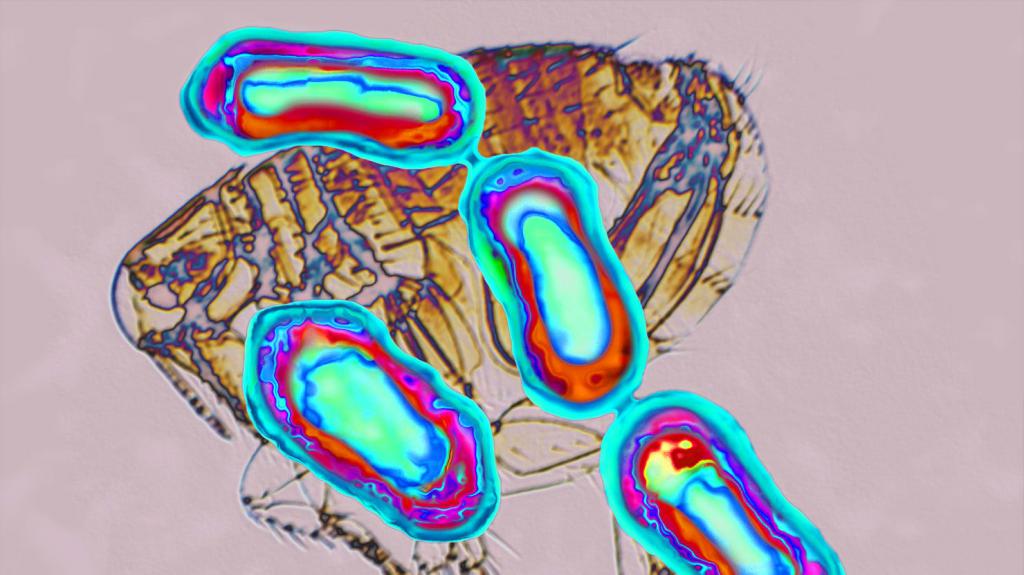
Заражение чумой происходит мгновенно при укусе блохи, заселении места жительства грызунами и иными животными – носителями бубонной палочки. Попадая через микротравмы на коже, через слизистые оболочки или конъюнктиву, вирус начинает распространяться с космической скоростью. На месте укуса (заражения) у человека возникает гниющая папула, заполненная белой мутной жидкостью. После вскрытия гнойника инфекция распространяется по всему телу. Следующей стадией развития болезни считается набухание лимфоузлов и трудности с глотанием. Буквально через несколько часов у больного отмечается резкий подъем температуры, нарушение процессов дыхания и сердцебиения, обезвоживание.
Холера
Холера – это острая кишечная инфекция, которая развивается при поражении человека вирусом вибриона. Болезнь проявляется поносом, рвотой, обезвоживанием, сухостью кожных покровов и склер, заострением черт лица, олигоанурией. Для выявления холеры применяется скрининговое исследование рвотных и каловых масс, бактериологические анализы
Холера – это особо опасный инфекционный агент, научное название которого – Vibrio cholerae. На сегодняшний день известно более 150 серогрупп холерных вибрионов, которые содержатся в сточных водах и загрязненных водоемах достаточно длительное время. Как и любая другая сложная бактерия, Vibrio cholerae устойчива к воздействиям внешней среды. Особо питательной средой для нее является скисшее молоко или мясо.
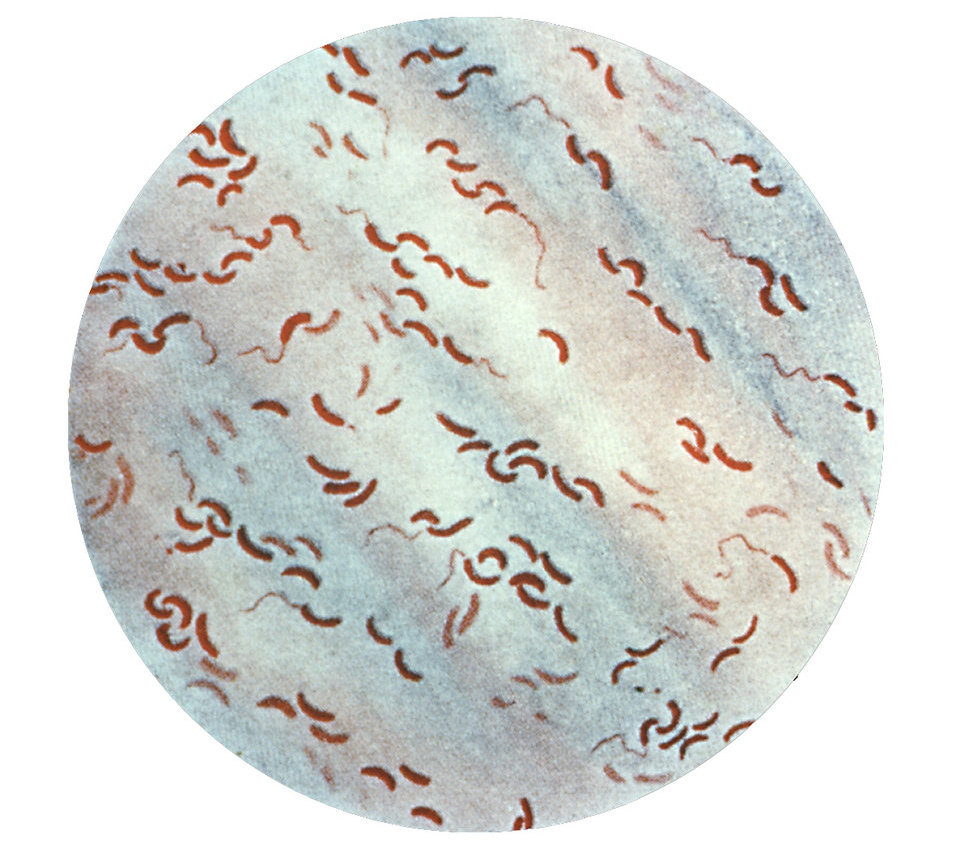
Согласно СанПин, особо опасная инфекция сразу после заражения холерным вибрионом никак себя не проявляет. Инкубационный период воздействия колеблется от нескольких часов до 5 дней включительно. Разгар холеры принято считать острым состоянием, когда вся симптоматика проявляется почти сразу. В течение 10 часов тело человека теряет порядка 20-30 % жидкости, стул является жидким и постоянным, рвотные массы могут быть источником заражения окружающих людей.
Полиомиелит
Полиомиелит – вирусная инфекция, при которой поражается серое вещество спинного мозга, что приводит к развитию множественных параличей, парезов. В зависимости от формы болезни у пациента могут наблюдаться: лихорадочные припадки, нарушение двигательной функции, расстройство пищеварения или быстрое развитие периферических параличей, деформация конечностей, астенический синдром, нарушение работы вегетативной нервной системы.
В зависимости от типа возбудителя, попавшего в кровь, различают несколько основных форм болезни:
- Спинальная. Характерны вялые параличи, парезы грудины, нижних и верхних конечностей, мышц диафрагмы, шеи и туловища.
- Бульбарная. Связана с поражением центральной нервной системы и развитием речевых расстройств – дизартрия, дисфония. Кроме этого, у больного отмечается нарушение функции глотания, жевания, сбои в работе сердца, легочные спазмы.
- Понтинная. У пациента отмечается полная или частичная утрата лицевой мимики, потеря речи, свисание угла рта на одну половину лица.
- Энцефалопатическая. Представлена тотальным поражением мозговых и спинномозговых структур.
- Смешанная. Включает в себя все известные формы болезни.
Натуральная оспа
Натуральная оспа (лат. variola, variola major) – особо опасная вирусная инфекция, передающаяся воздушно-капельным и аэрозольным (пылевым) путем от зараженного человека. Инкубационный период ВНО составляет 3-8 календарных дней. По прошествии этого периода у заболевшего отмечаются все эпидемиологические признаки сложного воспалительного процесса. О разгаре болезни свидетельствуют следующие симптомы:
- тяжелая интоксикация;
- двухволновая лихорадка;
- образование гнойных пустул на теле;
- неврологические расстройства (вследствие не спадающей высокой температуры);
- нарушение работы дыхательной и сердечно-сосудистой систем – увеличение лимфоузлов, бронхиальные стенозы, аритмия, слабость грудных мышц и трудности вдоха-выдоха.
Вирус натуральной оспы – патогенный агент внешней среды, наиболее устойчивый к влиянию температурных и иных природных факторов. Период его нахождения на открытом воздухе может значительно превышать 60 дней. Антигенами ВНО являются:
- ранний ES-антиген;
- родоспецифический LS-антиген;
- группо-специфический нуклеопротеидный NP-антиген.

Общий показатель восприимчивости живого организма к воздействию ВНО составляет 95-98 %. Проникая через слизистые оболочки, микротравмы на коже внутрь объекта, вирус начинает быстро встраиваться в ДНК-структуру, приводя к общему ослаблению иммунных процессов. Главными путями передачи являются:
- Посуда.
- Нательное белье и гигиенические принадлежности.
- Биологически активные компоненты: кровь, слюна, сперма.
- Шерсть домашних животных.
В том случае, если ВНО привел к гибели человека, его тело также является очагом особо опасной инфекции.
Желтая лихорадка
Желтая лихорадка является одной из самых опасных вирусных инфекций. Распространена в Центральной и Южной Америке, а также Африке. Всемирной организации здравоохранения (ВОЗ) ежегодно публикуется список этих стран. В год регистрируется более двухсот тысяч случаев заражения, тридцать тысяч из них с летальным исходом. Возбудителем лихорадки является РНК-содержащий вирус. Источником распространения инфекции являются животные. Заболевание распространяется по трансмиссивному механизму.

Признаки заболевания проявляются от 3 до 6 дней после заряжения. Желтая лихорадка существует в двух эпидемиологических формах:
- лихорадка джунглей – это передача инфекции от насекомого человеку;
- лихорадка населенных пунктов – это передача инфекции от человека к человеку.
Заболевание характеризуется лихорадкой, сыпью, поражением органов выделительной системы, печени. Развитие заболевания делится на несколько стадий:
- острая стадия с признаками тошноты, рвоты и повышения температуры;
- более токсичная вторая стадия с развитием желтухи и болями в животе.
По правилам ВОЗ при выезде в страны благоприятного развития вируса необходимо провести вакцинацию от данного вируса. Данная прививка действует 10 лет и по необходимости проводится повторно за 10 дней до посещения страны.
Вирус Эбола
К особо опасным инфекциям относится и вирус Эбола, которым нельзя заразиться через воздух или через пищу. Заражение может произойти только во время контакта здорового организма и биологической жидкости зараженного, не так давно умершего от этой болезни. Если говорить проще, вирус передается с кровью, слюной, потом, слезами, спермой, мочой, кишечной слизью и рвотными массами. К тому же зараженными могут быть и предметы, недавно используемые больным, на которых остались любые из вышеперечисленных продуктов жизнедеятельности организма.
До проявления симптомов человек не является заразным, даже при наличии вируса в организме. Симптомы появляются спустя 2 дня, максимум 3 недели. Болезнь сопровождается:
- высокой температурой, начиная с 38,5 °С и выше;
- головными болями;
- суставными и мышечными болями;
- болью в горле и его покраснением;
- слабостью мышц;
- отсутствием аппетита.
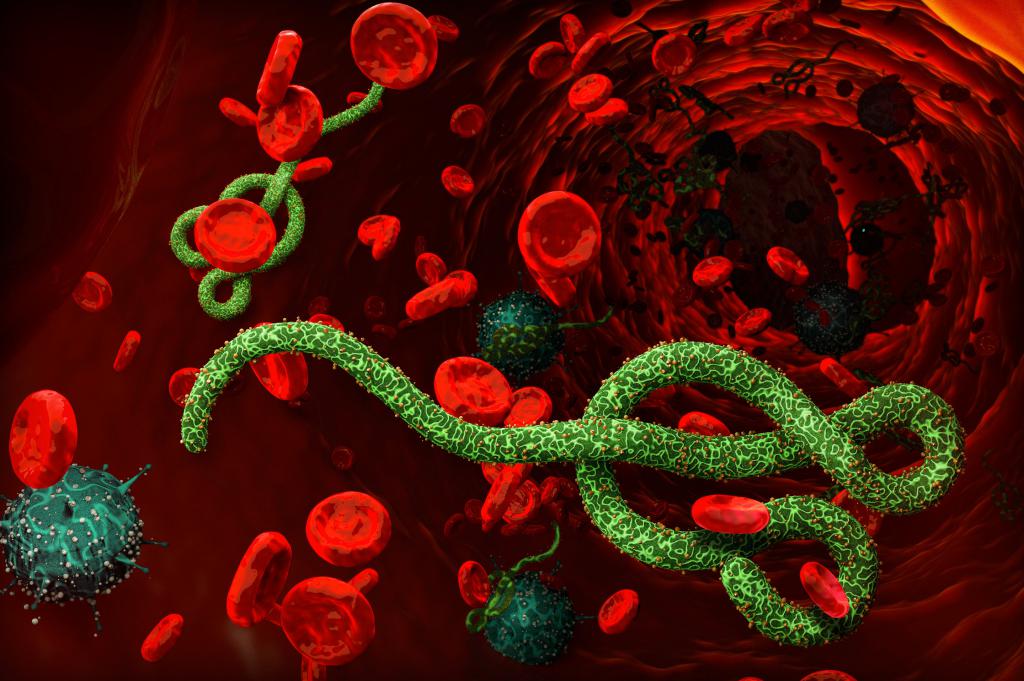
По ходу течения и развития заболевания у пациента уменьшается число клеток, ответственных за свертываемость крови. Результатом этого становится появление как внутреннего, так и внешнего кровотечения. Часто больные страдают от кровяной рвоты, поноса и сыпи. Это главные проблемы особо опасной инфекции. По данным, полученным благодаря вспышке эпидемий в 2013-1014 годах, удалось установить смертность болезни, она составляет 50 %. Но также были и вспышки болезни, в которых смертность достигала 90 %.
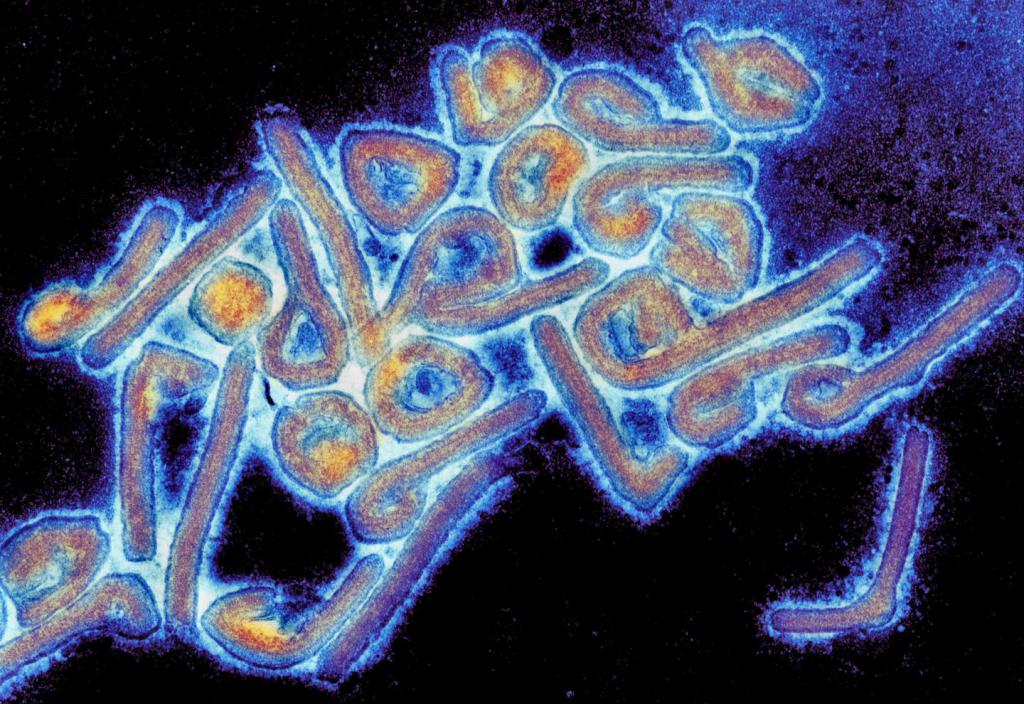
Вирус Марбург
Впервые о вирусе Марбург, или геморрагической лихорадке Марбурга, заговорили в 1967 г., после череды эпидемий, вспыхнувших в Марбурге, Белгороде и Франкфурте-на-Майне. Заражение произошло после контакта людей с африканскими зелеными мартышками. Помимо этого, переносчиками вируса являются плодоядные летучие мыши из семейства Pteropodidae. Таким образом, распространение вируса совпадает со средой обитания этих животных. Заболевание характеризуется высокой заразностью и тяжелым течением. Показатели смертности достигают 90 %. Инкубационный период составляет от 2 до 21 дня.

Первая симптоматика проявляется резко: лихорадка, сильные головные боли, миалгия в поясничной области, высокая температура. Вирусные частицы размножаются во всех органах организма, поражая лимфоидную ткань, печень, селезенку, кожу и головной мозг. Нередко отмечают локализованные некрозы органов мочеполовой системы. На следующей стадии появляются тошнота, рвота и профузная диарея, продолжающаяся до нескольких дней. С развитием болезни симптомы становятся все более тяжелыми: стремительная потеря веса, панкреатит, дисфункция внутренних органов, нарушения центральной нервной системы, сопровождающиеся галлюцинациями и бредом.
Частыми проявлениями являются желудочно-кишечные, маточные и носовые кровоизлияния. Обнаруживающаяся в моче и фекалиях кровь представляет собой опасность, т. к. служит источником заражения. Что касается летальных исходов, то смерть наступает на 8-16 день после проявления первых симптомов, ей предшествует шоковое состояние пациента и обильные кровопотери, в том числе и кровоизлияния под конъюнктиву.
Не существует специализированного лечения или вакцины. Пациентам проводят симптоматическое лечение: внутривенные вливания водно-солевых растворов, переливания крови, оксигенотерапию.
Клинические проявления заболевания идентичны с другими тяжелыми инфекциями, такими как брюшной тиф, лептоспироз, холера и другие. Точная диагностика может быть проведена только в лабораторных условиях (с соблюдением особых мер контроля и предосторожности) при помощи реакции сывороточной нейтрализации и полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР).
У выживших пациентов период восстановления имеет затяжной характер: долго сохраняется неподвижность, боли, развивается алопеция. Также сопутствующими заболеваниями могут стать энцефалит, орхит, пневмония и когнитивные нарушения. Были экспериментальные попытки лечения сывороткой, полученной от выздоравливающих, однако ее эффективность не была доказана. В настоящее время проводится тестирование ряда потенциальных вакцин, но их использование в клинических случаях станет возможным только через несколько лет.
Есть три разновидности тифа, и даже клинические симптомы у них похожи:
- Сыпной тиф – это инфекционная болезнь, разносчиками которой являются вши-паразиты. Если говорить по существу, то укус не является причиной заражения. Через ранку инфекция попадает в организм. После этого возбудитель добирается до лимфотока, а после окончания инкубационного периода – и в кровяную систему. Но все это произойдет, если место укуса будет расчесано.
- Возвратный тиф тоже является инфекционным и остропротекающим заболеванием, которое переносится паразитами. Его склонность отступать и повторно активизироваться является одной из отличительных черт этой болезни. У возбудителя тифа гибкое строение, это дает ему способность менять свой структурный вид.
- Возбудители брюшного тифа попадают в организм через продукты питания. Эту кишечную инфекцию вызывают микроорганизмы из рода сальмонелл.
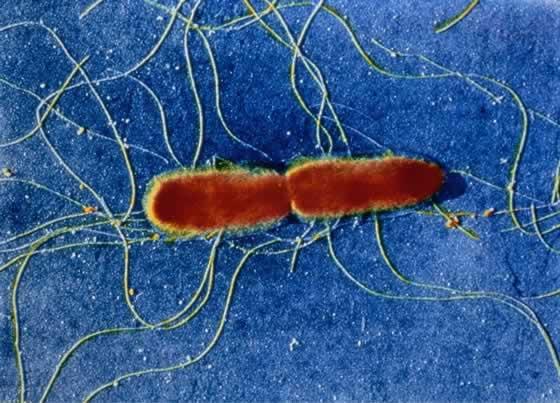
Еще одной характеристикой особо опасной инфекции называют лихорадку, которая является общим симптомом для каждого вида тифа. Сыпной тиф распознается по сыпи, головной боли и слабости. Если речь идет о возвратном тифе, то лихорадку дополнит делирий – острое расстройство психики с сильными тревожными приступами, нарушенной ориентацией и чувственным бредом. Также селезенка с печенью будут увеличены. У больного брюшным тифом наблюдаются следующие симптомы:
- Снижен аппетит.
- Общая слабость.
- Брадикардия.
- Бледно-розовая сыпь – розеолы.
- Нарушенное лихорадкой сознание.
Малярия
Малярия входит в перечень особо опасных инфекций. Это инфекционно-паразитарное заболевание, которое проявляется повышением температуры тела, малокровием, гепатомегалией и спленомегалией. Переносчиками этого вируса являются комары и иные кровососущие насекомые. Именно поэтому болезнь широко распространена в странах Южной Америки и Юго-восточной Азии.
Источником вируса являются простейшие кровососущие организмы – комары, которые заносят бактерию при впрыске антисептического вещества. После попадания заразы в кровь происходит постепенное поражение клеток печени. Оно же считается первой трансплацентарной стадией. В дальнейшем ослабленный токсическими веществами и вирусом организм перестает активно сопротивляться и открывает доступ малярии непосредственно к клеткам крови – эритроцитам.

Больной малярией человек имеет желтушность кожных покровов, низкий гемодиализ, состояние слабости, нарушение пищеварительных функций, проблемы с опорно-двигательной системой, неврологические нарушения. Разгар болезни характеризуется резким увеличением температуры тела, выраженным кислородным голоданием, изменением формы стоп и кистей рук. У маленьких детей малярия протекает особенно тяжело. Смертность от этой инфекции составляет 80 из 100 новорожденных.
Профилактика
В РФ множество заболеваний такой степени сложности, что при эпидемической вспышке с ними справиться трудно. Последствия не только тяжелые, но и могут быть с летальным исходом. Чтобы эпидемии не наносили ущерба здоровью граждан, живущих в России, медики проводят периодически профилактику особо опасных инфекций:
- Временно изолируют всех, кто заболел первым.
- Уточняют диагноз больного, чтобы не было сомнений в том, что предположение было верным.
- Собирают информацию о больном и фиксируют в медицинских бланках для архива, в дальнейшем эти записи могут взять на исследование.
- Оказывают больному первую медицинскую помощь.
- Забирают у больного для изучения в лаборатории все необходимые для анализов материалы.
- Стараются выяснить весь список тех лиц, которые успели побывать в близком контакте с заболевшим человеком.
- Всех, кто контактировал с больным, помещают в изолятор для наблюдения за ними в период карантина до тех пор, пока не станет ясно, здоров человек или тоже заразился.
- Проведение дезинфекции всех лиц, как больных, так и тех, кто был в контакте, но еще не заболел.
К числу опасных болезней относят: все виды вирусных лихорадок, холеру, чуму, новые штаммы гриппа, оспу, малярию,ТОРС.

Как уберечь людей от особо опасных инфекций? Мероприятия по профилактике болезней – пункт номер один в борьбе с инфекциями. Полезная, доступная информация повышает грамотность населения в такого рода вопросах и дает шанс защитить людей от возможного заражения.


— Наш институт создан в 1924 году на основе пастеровской станции и химико-фармакологической лаборатории Минска, — рассказывает Александр Петкевич. — То есть наши корни имеют начало в борьбе с инфекциями. В Советском Союзе мы отвечали только за две проблемы: химиотерапию, химиопрофилактику вирусных инфекций и особо опасные инфекции. В суверенной Беларуси нам пришлось заняться остальными проблемами контроля инфекций.
В России, приводит пример Александр Петкевич, есть отдельные институты: гриппа, полиомиелита, вирусных препаратов, бактериологии, контроля вакцин и сывороток, кори и краснухи и т.д. РНПЦ эпидемиологии и микробиологии — это те же институты, но под одной крышей.

Александр Петкевич рассказывает, что в коллекции инфекций хранятся десятки тысяч образцов. За некоторыми из них, например, за возбудителем лихорадки Эбола, он лично ездил в Африку. Чтобы в банке был образец, с которым можно сравнить исследуемый материал
Любая страна заинтересована в том, чтобы на своей территории поддерживать санэпидемическое благополучие, рассказывает Александр Петкевич. Для этого у Беларуси есть специальные правительственные программы и нужная инфраструктура. Но поскольку для инфекций не составляет проблемы нарушить любую, даже мегаохраняемую границу, в этом вопросе важно сотрудничать на международном уровне.
— Международное сотрудничество и стандарты — обязательный элемент нашей работы, а не просто благозвучная фраза. Границы для вирусов и бактерий прозрачны. Поэтому очень важно работать комплексно. Беларусь находится в центре Европы. Миграционные потоки с Востока на Запад очень активны. Легальных и нелегальных мигрантов — десятки и даже сотни тысяч. Еще один фактор, который нужно учитывать: над территорией Беларуси проходят миграционные пути птиц. Отсюда у нас есть возбудители экзотических африканских болезней.

По словам Александра Петкевича, на данный момент Беларусь успешно побеждает инфекции. Однако к этим победам нужно подходить взвешенно и осторожно.
— Мы можем нарушить равновесие, которое сложилось в природе. Нужно помнить, что, по последним данным, человечество существует 300 тысяч лет, а возбудители инфекций — четыре миллиарда.
В организме взрослого мужчины весом 70 кг — 2−2,5 килограмма микробов абсолютной массы. Если бы бактериальные клетки весили столько же, сколько человеческие, мы бы весили сотни килограммов. Возникает вопрос: кто в ком живет? Бактерии в нас или мы в бактериях? Мы напрасно думаем, что можем их уничтожить и победить. Это равновесие было создано до нас. Наша задача — правильно определить свои приоритеты и работать, искать технологии, которые будут преодолевать негативные последствия действий возбудителей и использовать положительные.
Павел Семижон возглавляет лабораторию биотехнологии и иммунодиагностики особо опасных инфекций. Здесь исследуют особо опасные и природно-очаговые инфекции, а также разрабатывают препараты (иммунобиологические и молекулярно-биологические), с помощью которых их можно диагностировать.

Павел Семижон
Корпус, в котором располагается лаборатория, спроектирован и построен специально для этой работы. Территория условно делится на чистую и заразную зоны.
В центре лаборатории находятся закрытые боксовые помещения, в них — закрытые боксовые линии, где проводят исследования с возбудителями особо опасных инфекций. По периметру располагаются вспомогательные помещения.
Материал с патогенами (это может быть сыворотка, кровь и т.д.) попадает на закрытые боксовые линии. После он проходит обеззараживание: сперва дезинфицирующими средствами, затем его упаковывают и направляют в автоклав. Дополнительно бокс облучается ультрафиолетом.

В таких закрытых боксах проводятся исследования с пробами биологического материала
— Например, если работа проводилась с животными, они обеззараживаются в боксах, потом в автоклаве, после чего их сдают в крематорий. Если это какие-то твердые отходы, то после обеззараживания их выбрасывают в основную сеть.
В лаборатории особо опасных инфекций обычно делают диагностику экзотических и, как правило, завозных инфекций.
За все время работы, вспоминает Павел Семижон, еще ни разу не подтвердился ни один случай особо опасных инфекций. Хотя практически каждый год поступает несколько проб с подозрениями. В 2014-м, когда в Африке наблюдалась вспышка лихорадки Эбола, их было более 15.
Под особо опасными инфекциями сотрудники лаборатории подразумевают лихорадки Эбола, Ласса и Марбург. Свиной грипп относится просто к опасным инфекциям. Впервые его обнаружили в 2009 году. Его привез студент, который приехал учиться в Беларусь из Китая.
— В то время было много проб. В итоге многие диагнозы подтверждались. В основном это были пробы от иностранных студентов. Мы предполагали, что рост начнется в августе-сентябре, когда в Беларусь прибудут иностранные студенты. Так это и получилось.

Так выглядит одно из вспомогательных помещений по периметру лаборатории
Как вычисляют людей, которые потенциально могут быть заражены болезнью? Павел Семижон объясняет:
— Контроль начинается еще во время авиаперелета. Когда возникает подъем заболеваемости в каком-то из регионов, экипажи самолетов получают инструкции. Они наблюдают, как пассажиры себя ведут, кашляют ли, есть ли рвота. Еще до прилета в пункт назначения командир сообщает, есть ли кто-то подозрительный.
В любом аэропорту, на вокзалах есть санитарно-карантинные пункты, оборудованные приборами дистанционного измерения температуры. При малейшем подозрении пассажиров снимают и помещают в инфекционные стационары. Малейшим подозрением, к слову, может стать даже прибытие из страны, где есть это заболевание.
Затем вступает в работу следующий алгоритм. Специальным транспортом человека с подозрением на заболевание отвозят в инфекционную больницу, где для него подготавливают специальный бокс-изолятор. Он оборудован отдельной вентиляционной системой и канализацией. Далее у пациента забирают материал для исследования и специальным транспортом доставляют к нам в лабораторию.

Если такая ситуация возникает, специальная оперативная группа из сотрудников лаборатории приезжает в течение 40 минут.
— Мы анализируем материал и в течение 6 часов выдаем предварительный результат, в течение 12 — окончательный. Все это время к пациенту относятся как к потенциально зараженному.
Как от возможного контакта с особо опасной инфекцией защищаются сотрудники лаборатории? Есть несколько способов.
— Сотрудники надевают специальную одежду — скафандры. В них они работают в полностью изолированных помещениях.
Второй способ — это работа в кабинетах биологической безопасности.
— В этих боксовых помещениях создается отрицательное давление за счет специальной системы вентиляции. Например, во вспомогательных помещениях оно на 5 мм ниже. В боксах, где работают с опасными инфекциями, еще ниже. Таким образом, создается перепад давлений, при котором исключается любая возможность того, что инфекционный агент попадет за пределы лаборатории. Система вентиляции оснащена несколькими ступенями фильтров тонкой очистки, что препятствует попаданию возбудителей наружу.
То есть в боксовых линиях ты как будто работаешь в реке, которая все уносит потоком через систему фильтров. Это обеспечивает защиту персонала и окружающей среды.
Как охраняется сама лаборатория?
— Все сотрудники находятся под постоянным видеонаблюдением, — рассказывает Александр Петкевич. — Умный человек не унесет ничего. Но должна быть и страховочная система. Потому везде стоят видеокамеры, войти в лабораторию можно только по электронным пропускам. К работе в боксовых помещениях, где исследуют особо опасные патогены, имеют доступ только определенные сотрудники лаборатории.

— Как ни охраняй лабораторию, все равно в Беларусь могут прилететь особо опасные инфекции с теми же птицами, о которых упоминал Александр Петкевич. Что в таком случае делать?
— Да, причем переносчиками могут быть и насекомые, и летучие мыши. Например, у нас в Беларуси обитает несколько видов летучих мышей, которые могут быть носителями таких особо опасных вирусов, как Хендра и Нипа — новых и малоизученных.
Сейчас во Всемирной организации здравоохранения активно обсуждается, что мы на пороге очередной пандемии. Поэтому ВОЗ рекомендует развивать диагностическую платформу, чтобы быть готовыми обеспечить диагностику любого заболевания. Техника нашей лаборатории позволяет это делать.
Аннотация научной статьи по экономике и бизнесу, автор научной работы — Бачинский А.Г., Низоленко Л.Ф.
Похожие темы научных работ по экономике и бизнесу , автор научной работы — Бачинский А.Г., Низоленко Л.Ф.
Universal Model of Local Epidemics Development, Caused by Particularly Dangerous Infection Agents
универсальная модель локальных эпидемий, вызываемых возбудителями особо опасных инфекций
Ключевые слова: эпидемия, математическая модель, особо опасные инфекции, меры противодействия. A.G.Bachinsky, L.F.Nizolenko
Universal Model of Local Epidemics Development, Caused by Particularly Dangerous Infection Agents
State Scientific Center of Virology and Biotechnology "Vector", Kol'tsovo, Russian Federation
Key words: epidemics, mathematical model, particularly dangerous infections, countermeasures.
Материалы и методы
Для адаптации модели к выбранному возбудителю собираются все доступные данные о патогенезе, эпидемиологии, профилактике и лечении заболевания. На их основании задаются параметры моделирования, такие как продолжительность стадий заболевания, относительная инфекционность и смертность больных, продолжительность вакцинального периода и др. Если доступны более или менее качественные данные о динамике вспышек [5, 7, 8], они используются, с одной стороны, для подбора параметров, а с другой, для верификации модели по отношению к данному возбудителю, то есть адекватного описания вспышек с учетом мер противодействия. Для перехо-
да от одной инфекции к другой достаточно задать соответствующий набор параметров. Предполагается, что такого рода относительно простая структура модели достаточна для описания основных особенностей развития эпидемий, учитывая то обстоятельство, что данные для адаптации более сложных структурированных моделей, как правило, отсутствуют.
Основные положения модели базируются на концепции моделирования эпидемий, предложенной Б.В.Боевым [4], которая, в свою очередь, основывается на работах О.В.Барояна и Л.А.Рвачева 1. принципиальное положение ее состоит в том, что инфицированный человек проходит последовательно ряд стадий заболевания, например, скрытый (латентный, инкубационный) период, стадия продромы, инфекционная стадия. Для каждой из стадий, в зависимости от времени пребывания в ней, задаются функции, определяющие вероятность (долю) ежедневного перехода в следующую стадию, выздоравливания, смертности, интенсивности выделения инфицирующего агента (инфекционности) и ряд других.
разрабатываемая модель относится к классу SEIRF, то есть в популяции некоторого населенного
пункта или региона выделяются следующие группы населения:
- не инфицированные лица, чувствительные к инфекции (иммунные и без иммунитета; находящиеся в стадии формирования иммунитета после вакцинации; лица, бывшие в контакте с уже инфицированными, в том числе выявленные и наблюдаемые/ изолированные; лица, имеющие первичные неспецифические симптомы заболевания - подозрительные - наблюдаемые или изолированные);
- инфицированные лица, находящиеся в латентной стадии, кластеризованные так же;
- инфицированные лица, находящиеся во второй стадии заболевания, обычно продромы;
- поправившиеся, имеющие стойкий иммунитет на период моделируемой вспышки;
- лица, умершие в результате заболевания.
Моделируются следующие процессы:
- естественное снижение (повышение) активности внешнего источника инфекции;
- инфицирование чувствительных лиц в зависимости от инфекционной напряженности и состояния их иммунитета;
- формирование класса контактных пропорционально числу вновь инфицированных чувствительных лиц;
- инфицирование контактных с повышенной по сравнению с остальными скоростью;
- вероятностный переход из одной стадии развития заболевания в другую;
- смерть больных. Смертность снижается, если больные подвергаются лечению.
В модели предусматривается реализация трех режимов противоэпидемических мероприятий (ПЭМ), определяющих, в основном, скорость выявления и изоляции (наблюдения) инфицированных, контактных и подозрительных лиц:
подворный обход. Обычно при реализации этого режима снимаются ресурсные ограничения, т.к. предполагается мобилизация необходимых ресурсов из других регионов.
Кроме этих трех режимов для некоторых инфекций задается массовая вакцинация, характеризующаяся охватом и периодом ее проведения, профилактический прием лекарственных препаратов, а также карантин, характеризующийся степенью активности, снижающей скорость инфицирования.
все указанные меры противодействия реализуются при наличии соответствующих ресурсов, к которым относятся квалифицированный медперсонал, места для изоляции/наблюдения больных, контактных и подозрительных на заболевание лиц, запасы профилактических и лекарственных средств. при исчерпании ресурсов, уровни активности соответствующих мер могут быть снижены вплоть до полного прекращения.
проведена верификация модели путем аппроксимации реальных данных о вспышках оспы в городах Европы расчетными данными. Ретроспективные данные включают описания вспышек оспы: Югославия в 1972 г., Брайтон в 1950-1951 гг., Билстон в 1947 г., Москва в 1959-1960 гг., Стокгольм в 1963 г., Кардифф в 1962 г. [6]. При верификации варьируемыми параметрами были только среднее число инфицированных от одного больного до и после начала проведения противоэпидемических мероприятий и параметры скорости изоляции больных и контактных [5]. Примерно таким же образом верифицировалась модель по данным о вспышках геморрагической лихорадки Эбола [7, 8] и пандемии гриппа НШ1 2009-2010 гг. (по данным официального сайта ВОЗ).
Результаты и обсуждение
Проблемы особо опасных инфекций, вып. 2, 2014
Задаются параметры этого города:
- число мед. работников, занятых в ликвидации эпидемии - 2000;
- запас доз вакцины для массовой вакцинации -100000;
- запасы лекарства (на один курс лечения) -1000;
- число мест строгой изоляции больных - 300, в провизорных госпиталях - 2500, в изоляторах для контактных - 1000.
основные моменты вспышки отображаются в протоколе расчетов: день 17 - включены ПЭМ1, день 22 - включается ПЭМ2, день 22 - начинается массовая вакцинация, день 22 - нехватка пунктов вакцинации, день 22 - нехватка мест изоляции контактных, день 22 - нехватка медбригад, день 23 - нехватка мест изоляции, день - 23 нехватка мест изоляции подозрительных, день 25 - недостаток вакцины, день 27 - включается ПЭМ3 ресурсные ограничения сняты, день 27 - введен карантин.
Кроме текущих и накопленных значений переменных модели, выдаются некоторые сводные характеристики, включающие общее число инфицированных, изолированных больных, изолированных контактных, изолированных подозрительных, человеко-дней изолированных контактных, человеко-дней изолированных подозрительных, человеко-дней изолированных больных, дней карантина, число умерших.
Для проверки влияния тех или иных ограничений на динамику вспышки, наличие каждого из ресурсов по отдельности было увеличено десятикратно. Данные по суммарному числу инфицированных приведены на рис. 2, вариант 1.
результаты приведенных расчетов показывают, что снятие любого из ресурсных ограничений по отдельности не приводит к кардинальному улучшению ситуации. Только увеличение запаса вакцины снижает число инфицированных в два раза на промежутке в 50 дней. Некоторое улучшение ситуации дает также увеличение числа мест изоляции больных или контактных лиц. Все остальные факторы влияния не оказывают.
На фоне десятикратного увеличения запасов вакцины, снимались ограничения по одному из тех остальных ресурсов, по которым наступал дефицит. В этом случае к наилучшему результату логично приводило отсутствие дефицита пунктов вакцинации, т.е. возможность проводить ее достаточно оперативно. Немного меньший эффект давало увеличение числа мест изоляции больных или контактных лиц (рис. 2, вариант 2).
День от начала расчетов ОГраНИЧеНИЯ СОХраНЯЮТСЯ При ПЭМЗ:
Сняв дефицит доз вакцины и пунктов вакцинации, опять увеличивали количество других ресурсов по отдельности. В этом случае максимальный эффект дает увеличение числа мест изоляции больных, чуть меньше - контактных (рис. 2, вариант 3).
Таким образом, расчеты показывают, что только комплекс эффективных мер противодействия способен ликвидировать вспышку в приемлемые сроки и с минимальными потерями.
Следует отметить, что возможность беспрепятственной изоляции больных и контактных лиц (одновременное отсутствие дефицита мест и медбригад для ее осуществления) даже при полном отсутствии вакцинации дает заметно лучший результат, чем вакцинация 80 % населения, если имеются проблемы с изоляцией (4190 инфицированных лиц против 6986). Но, учитывая разницу в материальных затратах на содержание мест изоляции и вакцинацию, именно массовая вакцинация по-прежнему остается оптимальной мерой противодействия эпидемии натуральной оспы.
Рис. 2. Влияние ресурсных ограничений на последствия эпидемии натуральной оспы:
потерь от эпидемий: запас вакцины, скорость вакцинации, определяемая числом пунктов вакцинации, число мест изоляции больных, число медбригад для поиска больных и контактных и.т.д.
2. Бароян О.В., Рвачев Л.А., Иванников Ю.Г. Моделирование и прогнозирование эпидемий гриппа для территории СССР. М.: ИЭМ им. Н.Ф.Гамалеи; 1977. 546 с.
3. Бароян О.В., Рвачев Л.А. Прогнозирование эпидемий гриппа в условиях СССР. Вопр. вируссл. 1978; 2:131-7.
4. Боев Б.В., Макаров В.В. Компьютерное моделирование и прогнозирование эпидемий птичьего гриппа. Ветеринарная патсл. 2005; 3:49-58.
5. Бачинский А.Г. Математическая модель локальной эпидемии натуральной оспы с учетом мер противодействия и ресурсных ограничений. 30 лет после ликвидации оспы: исследования продолжаются Кольцово: Информ-Экспресс; 2010. С. 253-80.
7. Bachinsky A.G., Nizolenko L.Ph. A Universal Model for Predicting Dynamics of the Epidemics Caused by Special Pathogens. BioMedRes. Int. 2013; 2013:467078. doi:10.1155/2013/467078.
8. Outbreak of Ebola haemorrhagic fever, Uganda, August 2000 - January 2001. Wkly Epidemiol. Rec. 2001; 76(6):41-8.
1. Baroyan O.V., Rvachev L.A. [Mathematics and Epidemiology]. M.: "Znanie"; 1977. 63p.
2. Baroyan O.V., Rvachev L.A., Ivannikov Yu.G. [Modeling and Forecasting of the Flue Epidemics in the Territory of USSR], M.; 1977. 546 p.
3. Baroyan O.V., Rvachev L.A. [Prognostication of flue epidemics in the environments of USSR]. Vopr. Virusol. 1978; 2:131-7.
4. Boev B.V., Makarov V.V. [Computer modeling and forecasting of avian flu epidemics]. Veterenar. Patol. 2005; 3:49-58.
5. Bachinsky A.G. [Computer model of local smallpox epidemics taking into account countermeasures and resource limitations. 30 years after smallpox eradication: investigations continue]. Kol'tsovo: Inform-Express; 2010. P. 253-80.
6. Serenko A.F. [Imported Onsets of Smallpox]. M.: "Medgiz"; 1962. 120 p.
7. Bachinsky A.G., Nizolenko L.Ph. A Universal Model for Predicting Dynamics of the Epidemics Caused by Special Pathogens. BioMed Res. Int. 2013; 2013:467078. doi:10.1155/2013/467078.
8. Outbreak of Ebola haemorrhagic fever, Uganda, August 2000 -January 2001. Wkly Epidemiol. Rec. 2001; 76(6):41-8.
Читайте также:


