Радионуклидная терапия для лечения метастазов в костях
- К каким проблемам приводят метастазы в костях
- Сколько живут с костными метастазами?
- Как диагностируют метастазы в костях?
- Современные методы лечения
- Противоопухолевые препараты при метастазах в костях
- Радиофармпрепараты
- Бисфосфонаты
- Лучевая терапия
- Радиочастотная аблация
- Применение костного цемента
- Хирургические вмешательства при метастазах в костях
Кости являются третьим по частоте местом локализации метастазов при различных онкологических заболеваниях, уступая только печени и легким.
Обычно появление костных метастазов говорит о том, что рак находится в запущенной стадии. Радикальное лечение в такой ситуации, как правило, невозможно, терапия носит паллиативный характер.
Чаще всего в кости метастазирует рак простаты и молочной железы.
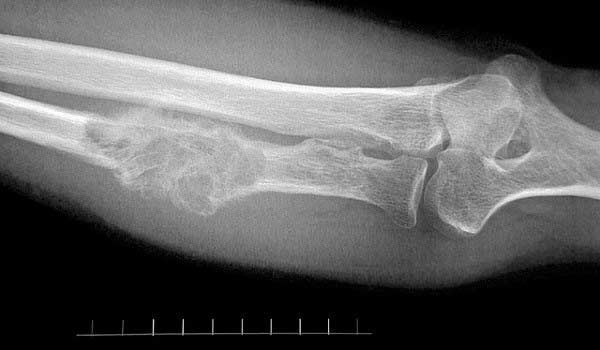
Вторичный рак костей намного более распространен по сравнению с первичными опухолями, особенно у взрослых. Кости и красный костный мозг имеют хорошее кровоснабжение, поэтому в них с легкостью проникают раковые клетки, присутствующие в кровотоке.
К каким проблемам приводят метастазы в костях
Костные метастазы приводят к мучительным болям и нарушению подвижности в суставах. Из-за ослабления костной ткани происходят патологические переломы. Чаще всего у таких больных ломается бедренная кость, очень распространены патологические переломы ребер и позвонков.
Многие злокачественные опухоли метастазируют в позвонки. При этом беспокоят сильные хронические боли в позвоночнике, которые усиливаются и не дают спать по ночам. Может возникнуть тяжелое осложнение — сдавление спинного мозга.
Из-за разрушения костной ткани в кровь поступает большое количество кальция, развивается гиперкальциемия. Она приводит к запорам, увеличению количества мочи, больной постоянно испытывает жажду, усталость. В тяжелых случаях развиваются сердечные аритмии, почечная недостаточность.
Правильное лечение помогает справиться с этими симптомами и осложнениями, улучшить состояние больного, замедлить рост опухоли и продлить жизнь.
Сколько живут с костными метастазами?
Прогноз во многом зависит от того, в каком органе находится первичная опухоль, от ее гистологического типа. Медианная выживаемость при раке простаты с метастазами в костях с момента установления диагноза составляет 12–53 месяцев (в зависимости от степени злокачественности), при раке молочной железы — 19–25 месяцев, при раке щитовидной железы — 48 месяцев, при почечной карциноме — 12 месяцев, при раке мочевого пузыря — 6–9 месяцев, при раке легких — 6–7 месяцев, при меланоме — 6 месяцев.
Гиперкальциемия сильно ухудшает прогноз, у таких больных медианная выживаемость снижается до 10–12 недель.
Как диагностируют метастазы в костях?
Наиболее информативный метод диагностики — ПЭТ-сканирование. Во время исследования в организм больного вводят радиофармпрепарат, который накапливается в опухолевой ткани и делает ее видимой на снимках, выполненных с помощью специального аппарата. Это помогает выявлять даже мелкие очаги, но иногда за рак по ошибке можно принять костные инфекции, артриты и перенесенные переломы.
МРТ полезна для выявления сдавления нервов и спинного мозга.
Анализы крови на уровень кальция и щелочной фосфатазы не могут быть основанием для диагностики костных метастазов, они применяются в комплексном обследовании, в сочетании с вышеперечисленными методами. Лабораторные анализы помогают выявить осложнение костных метастазов — гиперкальциемию.
Современные методы лечения
Многие пациенты, у которых диагностированы костные метастазы, отчаиваются и прекращают лечение, считая, что больше ничего нельзя сделать. Несмотря на то, что ремиссия, как правило, невозможна, больному все еще можно помочь. Доступны разные виды лечения, которые помогают:
- замедлить рост вторичных очагов;
- справиться с симптомами;
- улучшить общее состояние и увеличить продолжительность жизни.
Составляя программу лечения, врач учитывает симптомы, локализацию и характеристики первичной опухоли, локализацию и количество костных метастазов, наличие осложнений в виде патологических переломов и гиперкальциемии.
Противоопухолевые препараты при метастазах в костях
Назначая противоопухолевую терапию, врач в первую очередь ориентируется на первичную опухоль. Метастазы в костях состоят из клеток, характерных для органа, из которого распространился рак. В разных случаях будут эффективны те или иные виды препаратов:
Лечение проводят до тех пор, пока опухоль реагирует на него, и не возникают серьезные побочные эффекты. Если назначенные препараты перестали работать, врач подбирает другую комбинацию.
Радиофармпрепараты
Радиофармпрепараты — это радиоактивные вещества, которые после внутривенного введения достигают опухолевой ткани, накапливаются в ней и уничтожают раковые клетки. Это альтернатива традиционной лучевой терапии. Если у больного обнаружены множественные метастазы, нецелесообразно облучать каждую кость: это не очень эффективно и грозит серьезными побочными эффектами. Стоит отдать предпочтение радиофармпрепаратам: они распространяются с кровотоком по всему организму и достигают всех вторичных очагов.
В настоящее время в зарубежной литературе есть данные об успешном применении стронция-89 (Metastron), самария-153 (Quadramet), радия-223 (Xofigo). Доказано, что радиофармпрепараты эффективно помогают уменьшить боли в пораженных костях в течение нескольких месяцев. При необходимости процедуру можно повторить.
Лучше всего радиофармпрепараты работают при остеобластных метастазах, когда повышена активность остеобластов — клеток, образующих новую костную ткань.
Бисфосфонаты
Бисфосфонаты — препараты, которые подавляют активность остеокластов — клеток, разрушающих костную ткань. Они помогают справиться с болями, укрепить кость, предотвратить патологические переломы, снизить уровень кальция в крови. Однако, применять бисфосфонаты нужно с осторожностью, потому что они способны вызывать серьезные осложнения, в том числе тяжелое нарушение функции почек и остеонекроз челюсти.
Более безопасной альтернативой является деносумаб — этот препарат тоже подавляет активность остеокластов, но его механизм действия отличается от бисфосфонатов.
Лучевая терапия
Облучение помогает справиться с болями в костях и предотвратить патологические переломы. Лечение проводят в одном из двух режимов:
- Можно провести 1–2 процедуры, во время которых на кость дают большие дозы излучения. Это удобно для пациента, так как сокращается количество поездок в клинику.
- Другая схема предусматривает проведение 5–10 сеансов меньшими дозами. При этом суммарная доза получится несколько больше, чем в первом случае, у таких пациентов реже рецидивируют боли и возникает необходимость в повторном лечении.
Радиочастотная аблация
Если в кости обнаружено 1–2 метастаза, можно провести радиочастотную аблацию. Процедура болезненная, поэтому ее выполняют под общей анестезией. В опухоль под контролем КТ вводят иглу и подают на нее ток высокой частоты. Это приводит к разрушению опухолевой ткани.
Применение костного цемента
Иногда для того чтобы уменьшить боль и укрепить костную ткань, в кость вводят специальный цемент. Его применяют при метастазах в позвонках и других частях скелета. Введение костного цемента может дополнять другие виды лечения.
Хирургические вмешательства при метастазах в костях
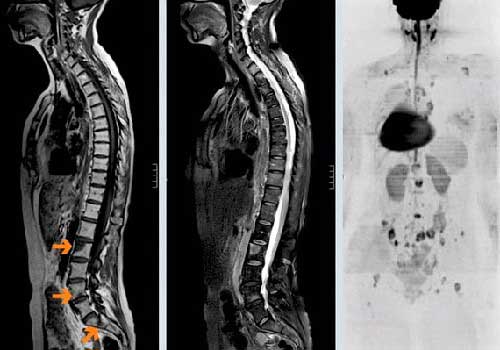
Операции при костных метастазах носят паллиативный характер. Врач применяет винты, штифты, пластины и другие конструкции, чтобы укрепить кость или восстановить ее целостность после патологического перелома. Это помогает справиться с болью и улучшить функцию пораженной части тела. Если хирургическое вмешательство противопоказано, применяют специальные шины, как при обычных переломах.
Все, на чем мы останавливались выше, касалось использования локо-регионального лучевого воздействия на метастатический очаг с использованием тех или иных методологий дистанционной лучевой терапии.
Вместе с тем есть и подход, когда лучевое воздействие может носить системный характер — это использование радионуклидной терапии.
Главное преимущество радиоизотопной терапии заключается в том, что это — системное лечение, которое в равной степени воздействует как на манифестирующие, так и на субклинические метастатические очаги.
Необходимо отметить, что защитные мероприятия в равной степени носят комплексный характер. Подтверждение того, что изотоп попал в организм и произойдет захват препарата в костях, можно осуществить в ряде случаев с использованием гамма-камеры.
Но, говоря о достоинствах радиоизотопной терапии, необходимо остановиться и на недостатках этого метода. Главная причина токсичности лечения связана с диффузным поглощением радиоизотопной дозы костным мозгом, в результате чего могут произойти значительные повреждения стволовых ростков.
Радиобиологические эффекты лечения радиоизотопами отличаются от таковых при наружном облучении: эта доза облучения подводится в течение продолжительного периода времени, но при этом она остается низкой.
Низкие дозы облучения биологически менее эффективны, чем высокие, и позволяют опухолевым клеткам восстановиться от лучевого повреждения, но клиническая достоверность данного факта в лечении костных метастазов остается сомнительной.
Изотопы для лечения метастазов
Изотопы, применяемые для лечения метастазов рака молочной железы в кости, относятся к группе костноспецифичных.
Радиоактивный фосфор (32Р) был одним из первых специфичных изотопов, используемых в медицине. Этот изотоп впервые был применен в лечении эритроцитоза, когда под его действием значительно снизилась выработка эритроцитов в результате захвата изотопа костным мозгом. 32Р является чистым бета-излучателем с периодом полураспада 14,3 дней.
Бета-частицы имеют максимальную энергию 1,7meV c проникающей способностью в несколько миллиметров. Отсутствие гамма-излучения при распаде 32Р означает невозможность визуального контроля, но в то же время исключает проблемы, связанные с радиационной защитой. Первые сведения об использовании радиоактивного фосфора в лечении костных опухолей появились в 1941 году, когда его использовали при костных метастазах рака молочной железы и остеогенной саркоме.
С тех пор периодически публиковались статьи, в которых, с одной стороны, подтверждалась эффективность 32Р, с другой — отмечалось его значительное токсическое воздействие на костный мозг. Предпринимались попытки совместного применения 32Р с тестостероном, стимулирующим костный мозг.
Последние сообщения по применению данной схемы свидетельствуют о том, что 87% пациентов отмечали значительное снижение интенсивности боли, при этом были зарегистрированы значительные проблемы с состоянием костного мозга (Maxfield et al., 1958).
Ряд авторов проводили исследования, связанные с попытками снижения миелотоксичности путем назначения 32Р-пирофосфата и 32Р-дифосфоната (Miller, 1974; Hall et al., 1975; Francis et al., 1976; Werner et al., 1980).
Малочисленные данные об использовании этих препаратов опять указывают на высокую противоболевую активность, но, с другой стороны, и на значительную костномозговую токсичность. Положительный эффект при использовании радиоактивного фосфора-32 для лечения болевого синдрома при костных метастазах рака молочной железы отмечен в исследованиях Кантина А.В. (1971), Шишкиной В.В. и соавт. (1986, 1988).
В частности, при пероральном введении фосфора-32 в дозе 74-111МBq у больных раком молочной железы с метастазами в кости положительный эффект был достигнут в 86% наблюдений. Эти результаты обнадеживают, так как авторами проанализированы результаты лечения 332 больных, при этом 46 из них получили 2 курса и 10 — 3 курса терапии.
Кроме того, Шишкина В.В. и соавт. (1988) использовали введение радиоактивного фосфора на фоне дистанционной лучевой терапией, и в сочетании с термотерапией и без нее в сравнении с изолированной дистанционной лучевой терапией. Авторы отмечают, что лучший эффект был получен при сочетанной лучевой терапии с термотерапией или без нее.
Стронций (89Sr) является химическим аналогом кальция, и при поступлении в кости включается в минеральную структуру. Стронций преимущественно накапливается в местах остеобластической активности и, в связи с этим, имеет преимущества перед фосфором. 89Sr является бета-излучателем, а проникающая способность бета-излучения составляет 8 мм. Это позволяет избирательно облучать кости в местах его захвата. Препарат назначается внутривенно.
Изучение гамма-излучения 89Sr подтверждает тот факт, что показатели захвата и удержания препарата значительно выше в костных метастазах, где повышена минерализация, т.е при остеобластическом типе метастазирования (Ben Josef et al., 1995).
В костных метастазах стронция накапливается в 2-2,5 раза больше, чем в нормальных костях. Обычная его доза составляет 150МBq. Эффективность метода может быть сопоставима с облучением половины тела при более низкой токсичности, обусловленной приходящей миелосупрессией. В настоящее время мы имеем убедительные данные о терапевтическом эффекте метастрона (хлорида стронция-89) (табл. 11.2.1.8).
Таблица 11.2.1.8. Эффективность хлорида стронция-89 в лечении костных метастазов 
Поиск новых радиофармпрепаратов привел к испытаниям таких открытых радионуклидов, как самарий и рений.
Самарий (153Sm) — новый изотоп, применение которого только изучается. Изотоп 153Sm объединяется с бисфосфонатной структурой в составе 153Sm-EDMP. Данное сочетание является новым направлением в радиоизотопной терапии, так как бисфосфонат обладает селективной способностью накапливаться в костях. Это дает возможность прицельного облучения зон метастатического поражения костей.
Самарий распадается с высвобождением как бета-частиц, так и гамма-излучения, и имеет короткий период полураспада — 46,3 час. Максимальная энергия бета-частиц — 0,81meV, что придает им относительно низкую проникающую способность (около 1 мм).
Энергия гамма-фотона (103keV) позволяет с помощью гамма-камеры получать изображение распределения и места захвата препарата. Самарий находится в стадии изучения, тем не менее, последние публикации свидетельствуют о том, что изотоп достаточно эффективен (табл. 11.2.1.9).
Таблица 11.2.1.9. Эффективность самария-153 в лечении костных метастазов 
Рений (186Re-HEDP) является бета-излучателем с максимальной энергией излучения равной 1,07meV, при этом 9% спектра составляет гамма-излучение, что позволяет выполнять диагностическое сканирование. Малая токсичность рения позволяет вводить этот изотоп повторно.
De Klerk et al. (1992, 1998) изучили фармакокинетику 186Re-HEDP у 11 пациентов (17 исследований) раком молочной железы или простаты с костными метастазами. Период полураспада 186Re в трех фракциях крови (цельная кровь, плазма и жидкость плазмы) была 40,1±5,0, 41,0±6,0 и 29,5±6,4 часа, соответственно.
Полная уринарная экскреция 186Re составила 69±15 %, из которой 71±6 % выделялось в течение первых 24 ч после инъекции. Авторы пришли к заключению, что максимально допустимая доза 186Re-HEDP у больных с метастатическим раком молочной железы составляет 2405MBq (65mCi).
Имеющиеся данные по использованию радиоактивного рения в лечении костных метастазов убеждают в эффективности этого препарата (табл. 11.2.1.10).
Таблица 11.2.1.10. Эффективность рения-186 в лечении костных метастазов 
В вопросе использования радиофармпрепаратов для паллиативного лечения костных метастазов остается ряд нерешенных проблем. В связи с этим существует разная оценка данного метода врачами онкологами. В качестве иллюстрации можно привести интересные данные, полученные в США (Papatheofanis, 1999).
Ста медицинским онкологам давали краткое клиническое резюме трех пациентов с метастатическим раком. Методы лечения включали энтеральный, парентеральный и подкожный пути введения наркотических анальгетиков; дистанционную лучевую терапию и системную изотопную терапию (стронций-89, самарий-153).
Мнение онкологов оценивалось в баллах от 1 (наиболее подходящий вариант) до 10 (наименее подходящий вариант), в зависимости от уместности каждого предложенного метода для каждого пациента. В результате системная лучевая терапия была воспринята как наименее подходящий метод паллиативного лечения метастатической костной боли по сравнению с наркотическими анальгетиками.
Некоторое расширение показаний для системной лучевой терапии было обозначено для пациента с распространенной метастатической болезнью, не смотря на литературные данные, которые говорят о том, что именно у этих больных радиоизотопная терапия дает наименьший эффект.
Онкологи оценили возможности системной лучевой терапии как низкие у больных с локализованной ранней формой метастатического процесса, в то время как по данным литературы, именно у этих пациентов эффект от лечения бывает наибольший.
В заключении автор делает вывод, что онкологи оценивают возможности системной лучевой терапии как низкие. Отношение к радиоизотопной терапии улучшается по мере увеличения распространенности заболевания. Как итог такого ошибочного мнения, системная лучевая терапия костных метастазов в повседневной практике применяется не так часто, как это должно быть на самом деле.
Для того, чтобы сформировать собственное мнение о системной лучевой терапии костных метастазов и попытаться ответить на ряд нерешенных вопросов в отношении данного метода, мы провели собственное исследование.
Лечение было проведено 43 пациентам: рак молочной железы был зарегистрирован у 29 (67,4%), предстательной железы — у10 (23,3%), почки — у 3 (6,97%) и шейки матки — у 1 (2,33%) больной. Возраст пациентов варьировал от 33 до 76 лет. Одиночные метастазы в костях были выявлены у 2 (4,65%) больных, множественные — у 37 (86,05%), сочетанное поражение костной системы и других органов отмечалось у 3 (6,98%) больных.
Радиофармпрепарат вводился внутривенно, струйно, в дозе 160 МБк. Повторная системная лучевая терапия проводилась 14 больным дважды, и 5 — трижды. Лечение с использованием хлорида стронция-89 осуществлялось преимущественно в комбинации с локальной лучевой терапией, химиотерапией и гормонотерапией, а также в самостоятельном варианте.
Эффективность лечения
Эффективность лечения оценивалась по динамике болевого синдрома, а также по объективным изменениям в метастатических очагах, определяемым с помощью контрольной рентгенографии, ЯМР-томографии, компьютерной томографии, остеосцинтиграфии.
Из 17 больных, получавших наркотические анальгетики, у 14 стало возможным либо уменьшить дозу, либо полностью отказаться от препарата. Не было эффекта от введения у 3 больных. Из 22 больных, у которых в той или иной степени была нарушена двигательная функция, ее улучшение или полное восстановление наблюдалось у четырнадцати.
Мы попытались определить эффективность хлорида стронция-89 у больных, получивших первую и повторные инъекции хлорида стронция-89.
Оценивая результаты в группе пациентов, получивших первую инъекцию радиофармпрепарата, мы отметили, что из 43 больных положительный эффект был достигнут у 40 (93%), у 2 (4,6%) эффект отсутствовал, у 1 (2,3%) больного наблюдалось ухудшение.
Наличие самого эффекта и его длительность зависели от применяемой схемы лечения. Сравнительно небольшое количество наблюдений не позволяет считать результаты достоверными, но предварительно можно сказать, что включение в схемы лечения локальной лучевой терапии позволяет добиться противоболевого эффекта практически у всех пациентов на срок не менее 3,5 месяцев.
Еще большая продолжительность (до 6 месяцев) и выраженность позитивного эффекта (у всех 9 больных) были зарегистрированы в группе больных, получивших комплексное лечение.
Объективный эффект был оценен у 31 больного. Полной репарации метастатических очагов после одной инъекции радиофармпрепарата не было отмечено ни у одного пациента. Частичная репарация наиболее часто наблюдалась при включении в план лечения локальной лучевой терапии и зарегистрирована у 8 больных.
После повторной инъекции раствора хлорида стронция-89 противоболевой эффект наблюдался у 13 пациентов из 14, и лишь у одного больного наступило усиление болей.
Следует отметить, что у 9 пациентов наблюдался полный противоболевой эффект, который практически не зависел от вида лечения, проводимого вместе с системной лучевой терапией, что, видимо, указывает на эффективность повторного введения радиофармпрепарата. Средняя длительность противоболевого эффекта составила 3,4 месяца.
При оценке объективных результатов повторного введения, мы отметили, что у 4 больных из 9 (44,4%) отмечалась положительная динамика, причем у одной больной, получавшей бисфосфонаты одновременно с системной лучевой терапией, наблюдалась полная репарация множественных костных метастатических поражений. У 4 больных регистрировалось дальнейшее прогрессиро-вание процесса, которое, однако, происходило на фоне полного отсутствия болей.
Третье введение раствора хлорида стронция-89 было проведено 5 больным. Безусловно число наблюдений слишком малое для того, чтобы делать определенные выводы, однако противоболевой эффект был зафиксирован у 4 пациентов, его средняя продолжительность составила 2,7 месяцев. Объективные результаты третьего введения были оценены у 4 больных. У двух пациентов отмечалась стабилизация метастатического процесса, у двух — дальнейшее прогрессирование.
Была отмечена умеренная гематологическая токсичность радиофармпрепарата, проявившаяся снижением количества лейкоцитов и тромбоцитов.
Пик токсичности приходился в основном на первую, а также на 4-6 недели. Интересно, что после первого введения снижение исходного уровня лейкоцитов и тромбоцитов наблюдалось приблизительно у четверти всех пациентов, и процент снижения составил для лейкоцитов 17,8% (0-73%), тромбоцитов — 9% (0-38%).
После повторных введений снижение уровня кровяных телец отмечалось практически у всех больных и составило для лейкоцитов 27,5% (0-63%) и 24,5% (0-50%), для тромбоцитов — 12,9% (0-54%) и 16% (0-26%) после второй и третьей инъекции, соответственно.
Из 43 человек умерло 8: шестеро больных — после первой инъекции, причем у 3 из них был зафиксирован противоболевой эффект, двое больных — после повторных инъекций.
В результате проведенных исследований нами было показано, что отечественный хлорид стронция-89 является эффективным препаратом системной лучевой терапии, обеспечивающим у большинства больных купирование болевого синдрома, уменьшение потребности в анальгетиках вплоть до полной их отмены, улучшение качества жизни пациентов, а также замедление прогрессирования метастатического процесса. Отмечена достаточно высокая эффективность данного радиофармпрепарата при костных метастазах как остеобластического, так и остеолитического типов.
Лучшие результаты были достигнуты при включении в схемы лечения локальной лучевой терапии и химиотерапии, хотя при повторных инъекциях радиофармпрепарата позитивный эффект был отмечен у большинства пациентов независимо от дополнительного противоопухолевого лечения.
Наши исследования подтвердили тот факт, что хлорид стронция-89 обладает умеренной гематологической токсичностью, проявляющейся снижением числа лейкоцитов и тромбоцитов, причем более выраженной после повторных введений радиофармпрепарата.
Новиков Г.А., Чиссов В.И., Модников О.П.

Основные показания к системной лучевой терапии болевого синдрома
- Метастатическое поражение костей скелета.
Цель терапии
- Борьба с болевым синдромом и дальнейшим распространением поражения костей при онкологических заболеваниях.
Важные аспекты применения Стронция-89-хлорида:
- Радионуклид обеспечивает продолжительное терапевтическое действие (4-6 месяцев).
- Препарат обладает системным лечебным эффектом, накапливаясь одновременно во всех имеющихся костных поражениях.
- Можно применять как самостоятельный метод лечения, а также в составе курса комбинированной терапии.
- Использование Стронция-89-хлорида не требует какого-либо другого предварительного лечения.
- Препарат обладает минимальной гематологической токсичностью.
- Госпитализации пациентов после введения Стронция-89-хлорида не требуется.
Что такое Стронций-89-хлорид?
Стронций-89-хлорид представляет собой лекарственный препарат для внутривенного введения, который применяется для лечения костных метастазов и купирования боли. Стронций-89-хлорид по химическому строению похож на кальций, поэтому он накапливается в местах его повышенного обмена (костные метастазы) и остается там в течение многих недель, обеспечивая лечебное действие.
Стронций-89-хлорид является препаратом для лечения костных метастазов. Он содержит небольшое количество радиоактивного стронция, который воздействует только на ту область, в которой он накапливается, обеспечивая лечение именно в тех местах, где это необходимо.
Какое действие окажет Стронций-89-хлорид?
В самом начале Вы можете не почувствовать никакого эффекта. Может даже отмечаться небольшое усиление боли в течение двух или трех дней после инъекции. Это нормально, и Вы можете немного увеличить дозу анальгетиков, которые Вы обычно принимаете.
Приблизительно спустя одну-две недели, иногда немного больше, Вы должны почувствовать, что боль уменьшается и может исчезнуть совсем. Обезболивающий эффект длится в течение нескольких месяцев (4-8 месяцев).
Существуют ли какие-либо побочные эффекты?
Нет. Вы можете употреблять обычную пищу и питье, кроме случаев, когда Вам специально скажет об этом доктор. Может наблюдаться некоторое снижение количества кровяных клеток, и Вам будет назначен общий анализ крови для контроля. Это является нормой. Если у Вас возникнут какие-либо беспокойства, Вам следует обсудить это с врачом.
Следует ли мне прекратить прием анальгетиков?
Врач может рекомендовать Вам продолжить прием анальгетиков до тех пор, пока боль не начнет уменьшаться. Затем Вы можете постепенно сокращать дозу этих препаратов иногда до полной отмены.
Можно ли получать другие виды лечения?
Врач при необходимости другого лечения скажет вам об этом. Вы можете продолжать получать инъекции гормонов или другие препараты, если это нужно.
Чем я могу заниматься?
Введение препарата не ограничивает никакой деятельности, которой Вы занимались. Как только Стронций-89-хлорид начнет действовать, Вы почувствуете, что можете быть более активным и делать то, что раньше не могли по причине сильной боли. Обычно при этом никаких проблем не возникает, однако все же соблюдайте осторожность. Если возникнут какие-либо беспокойства, обратитесь к врачу. Стронций-89-хлорид не влияет на способность водить машину или использовать другую технику.
Какие меры предосторожности мне следует соблюдать?
Действие Стронция-89-хлорида внутри Вашего организма ограничено очагами поражения, в которых он концентрируется. Поэтому нет никакой опасности для окружающих при контакте с Вами.
Следует помнить! В течение первых недель после инъекции Стронций89-хлорид присутствует в крови и моче. Поэтому важно соблюдать следующие меры предосторожности:
- по возможности пользоваться обычным туалетом, а не писсуаром и несколько раз смывать его водой;
- вытирать капли мочи салфеткой и выбрасывать ее в унитаз;
- всегда мыть руки после туалета;
- при загрязнении белья или одежды мочой немедленно выстирать его отдельно от другого белья и тщательно прополоскать;
- если Вы случайно пораните себя, нужно хорошо промокнуть капли крови и выбросить тампон в унитаз;
- если Вы пользуетесь судном, спросите у врача относительно утилизации мочи.
Что делать, если боль появится снова?
У большинства больных, которые получают Стронций-89-хлорид, его действие продолжается в течение по крайней мере нескольких месяцев. Если боль все же появилась, обратитесь к врачу. Он может назначить дополнительную инъекцию Стронция-89-хлорида или другое подходящее лечение.
Как проходит лечение?
Стронций-89-хлорид назначается только врачом и вводится квалифицированным персоналом, который сообщит Вам всю необходимую дополнительную информацию о вашем лечении. Если у вас возникнут любые вопросы или сомнения, обращайтесь к своему лечащему врачу без всяких колебаний.
Препарат вводится внутривенно. Госпитализации не требуется. С утра Вы оформляете историю болезни в нашем центре.

Метастазы в костях являются одним из самых частых клинических проявлений злокачественного опухолевого процесса и свидетельствует о четвертой стадии онкологического заболевания, что в целом ухудшает прогноз жизни.
Метастазы в кости могут определяться при многих онкологических заболеваниях, но наиболее часто они диагностируются при раке:
- молочной железы;
- предстательной железы ;
- легких;
- щитовидной железы;
- почек;
- миеломной болезни;
- при опухолях желудочно-кишечного тракта;
- при опухолях гепато-биллиарной системы (печени, желчевыводящих протоков).

При диагностике опухолевого поражения костей чаще всего выявляются вторичные изменения в позвоночнике, метастазы в тазовых костях, а также метастазы в ребрах, в трубчатых костях конечностей и метастазы в кости черепа.
Развитие и рост костных метастазов
Метастазы рака в кости характеризуются поражением костной ткани раковыми клетками, которые проникают в нее с током крови и лимфы из первичной опухоли. Кроме того, эти раковые клетки могут распространяться в другие органы и ткани, формируя в них метастазы. Поскольку кости выполняют важнейшую для организма опорно-двигательную функцию, их поражение негативно влияет на качество и прогноз жизни пациента.
Основными клетками костной ткани являются остеобласты, ответственные за образование новых клеток и рост кости, и остеокласты, отвечающие за разрушение и поглощение отработавших костных клеток.

При поражении костей метастазами нарушаются функции вышеуказанных клеток, в связи с чем, метастазы в кости в зависимости от типа поражения делятся на:
- остеолитические: при поражении остеокластов происходит истончение костной ткани, приводящее к патологическим переломами при нагрузках. При прогрессировании заболевания эти признаки могут появляться даже при малейшей нагрузке (например, при вставании с постели, при попытке сделать шаг и т.д.).
- остеобластические: при поражении остеобластов диагностируется патологическое увеличение костной ткани, образование наростов и выпячиваний на кости, ограничение подвижности суставов.
- смешанные: поражение остеобластов и остеокластов. Обнаруживаются наиболее часто у больных с метастазами в кости и проявляются истончением кости и появлением новых метастазов.
Симптоматика и характерные признаки
При небольшой площади поражения костной ткани у онкологических больных метастазы в кости клинически могут никак себя не проявлять. При отсутствии противоопухолевого лечения метастазы в кости растут, увеличиваясь в размерах и количестве. Это сопровождается появлением и, впоследствии, прогрессирующим усилением определенных признаков:
Все вышеуказанные симптомы у онкологических больных могут быть выражены по – разному, в зависимости от объема поражения костной ткани и эффективности проводимого лечения.

Диагностика метастазов в костях
Для диагностики метастазов в кости применяется ряд инструментальных методов обследования, которые можно при определенных показаниях комбинировать друг с другом, что повышает их диагностическую точность:
- Сцинтиграфия скелета основывается на накоплении раковыми клетками радиофармпрепарата (радиоактивный изотоп), который вводится внутривенно за некоторое время до исследования. Изотоп с током крови разносится по костной ткани и там, где есть метастазы в кости он поглощается опухолевыми клетками и накапливается. Сцинтиграфия скелета часто используется на первом этапе диагностики метастазов в кости.
- Рентгенография костей используется в основном как дополнительный метод дифференциальной диагностики метастазов в костях.
- Компьютерная томография является высокоинформативным методом обследования, в связи с чем широко применяется для подтверждения метастазов в кости.
- Магнитно-резонансная томография также является высокоинформативным и дорогостоящим методом обследования, помогающим в трудных клинических ситуациях оценить степень поражения костной ткани, распространение опухоли на окружающие мягкие ткани, сосуды, нервы.
- Биохимический анализ крови при метастазах в кости отражает повышенный уровень кальция в крови, повышение щелочной фосфатазы. Однако, выраженность этих нарушений в анализах крови определяется степенью костного поражения.
- Биопсия кости является самым точным методом диагностики, позволяющим определить морфологическое строение опухоли. Для верификации метастазов в кости может быть использовано как цитологическое, так и гистологическое исследование биоптата. В спорных случаях с целью верификации диагноза (когда неизвестна локализация первичной опухоли) биоматериал может быть направлен на иммуногистохимическое исследование для определения тканевой принадлежности.

Выбор метода определения метастазов в костях должен осуществляться по определенным диагностическим стандартам квалифицированным специалистом, обязательно в соответствии с клинической ситуацией и может варьировать у разных больных с одинаковым диагнозом.
Цели и методы терапии
Известно, что наличие метастатического поражения скелета повышает стадию онкопатологии, может ухудшить прогноз и качество жизни пациентов. Но, тем не менее, метастазы в кости поддаются лечению и при правильно подобранной и своевременной терапии можно достичь длительной выживаемости и улучшения качества жизни этой категории больных, что является главной целью онкологов. Для достижения этой цели необходимо:
- Уменьшить болевые ощущения за счет правильно подобранного обезболивания;
- Уменьшить размеры и количество метастазов в костях;
- Предотвратить осложнения, вызванные метастазами в кости, такие как, патологический перелом, компрессионный синдром;
- Уменьшить или предотвратить интоксикацию больного.
Лечение метастазов в кости проводится в комплексе с основным противоопухолевым лечением.
Методы лечения метастазов в кости:
- Лекарственный метод основан на применении бисфосфонатов, которые способствуют восстановлению костной ткани.
- Лучевая терапия направлена на разрушение опухолевых клеток, остановку их роста и деления. Она может осуществляться с помощью дистанционной лучевой терапии, стереотаксической лучевой терапии или сочетанием этих методов.
Кроме того, может быть назначено обезболивание, коррекция сопутствующей патологии, профилактика или лечение интоксикации пациента.

Часто больным с метастазами в кости назначается комплексное лечение, включающее все вышеуказанные методы.
Обязательно сочетать лечение метастазов в кости с основным лечением, это способствует увеличению продолжительности жизни.
Лечиться народными средствами не рекомендуется, поскольку это приведет к скорым осложнениям, ухудшению самочувствия и, самое главное, к прогрессированию болезни и потере бесценного времени жизни.
Прогноз и длительность жизни
Как уже говорилось выше, больные с метастазами рака в кости имеют IV стадию заболевания. Прогноз и продолжительность жизни этой категории пациентов варьирует в зависимости от многих факторов:
- основного диагноза (морфологического строения опухоли, степени злокачественности и т.д.)
- общего состояния больного и образа жизни;
- сопутствующей патологии и ее коррекции;
- степени распространения опухолевого процесса (размера, локализации и количества метастазов в кости, а также прорастания жизненно важных структур самой опухолью и ее метастазами);
- грамотности подобранного противоопухолевого лечения и его эффективности;
- соблюдения режима лечения и наблюдения и т.д.
Чем раньше диагностировано поражение скелета, тем эффективнее борьба с метастазами. В связи с этим, все пациенты с онкопатологией должны регулярно проходить контрольное обследование (в зависимости от своего диагноза) под наблюдением врача онколога и незамедлительно обращаться за помощью, если в промежутках между обследованиями появились какие-либо жалобы на изменение или ухудшение состояния здоровья.
Для профилактики рака
Говоря о профилактике рака, надо начинать с самого начала, а именно, ответить себе на вопросы:
- Где мы живем?
- Как мы живем?
- Что мы делаем для нашей жизни и здоровья?
В наш век доступной и открытой информации существует множество публикаций, интернет ресурсов о здоровом и правильном образе жизни, питании, отдыхе и т.д., где можно найти ответы на все интересующие нас вопросы. Нужно помнить, что наше здоровье только в наших руках, поэтому очень важно беречь его.

А что мы делаем для этого?
Как узнать, что пора обратиться к врачу, если ничего не беспокоит?
Необходимо проводить регулярные скрининговые обследования, медицинские осмотры.
Выявленный на ранней стадии рак имеет благоприятный прогноз и эффективно поддается лечению. Лечение рака направлено на уничтожение опухолевых клеток, предотвращение их роста и размножения, поэтому, чаще всего, для лечения онкопатологии используют комплекс мероприятий: хирургическое лечение, лекарственное лечение (химиотерапия, гормонотерапия, иммунотерапия), лучевую терапию. Такое комплексное лечение позволяет снизить риск возврата болезни (местного рецидива, прогрессирования), увеличивает продолжительность жизни и улучшает ее качество.
Цена, руб.
- О центре
- Специалисты
- Новости
- Партнеры
- Отзывы
- Запись на приём
- Стоимость лечения
- Консультация
- Диагностика
- FAQ
- Статьи
- Аппарат Кибернож
- Уникальность системы
- Показания к лечению
- Противопоказания
- Как происходит лечение
- Сравнение методов
- Дистанционная
- Комбинированное лечение
- Лечение
- Опухоли головного мозга
- Рак легкого
- Рак печени
- Рак почки
- Рак предстательной железы
- Рак носоглотки
- Опухоль спинного мозга
- Опухоль ЦНС у детей
- Рак поджелудочной железы
- Опухолевое поражение костей
- Метастазы
- Невралгия тройничного нерва
- Пяточная шпора
Читайте также:


