Расчет инфузионной терапии у детей при кишечной инфекции у

Острые кишечные инфекции (ОКИ) занимают второе место в структуре инфекционной заболеваемости у детей. В 2015 г. показатель заболеваемости ОКИ в Российской Федерации составил 545,89 на 100 тыс. населения, что практически не отличается от показателя 2014 г. При этом на долю ОКИ неустановленной этиологии приходится 63,44% случаев.
Сохраняются выраженные различия в эффективности диагностики ОКИ на различных территориях Российской Федерации, наряду со снижением заболеваемости по отдельным нозологиям, отмечался рост заболеваемости кампилобактериозом — на 30,3%, ротавирусной — на 14%> и норовирусной — на 26,47о инфекциями.
При инфекционной диарее тяжесть состояния больного определяется наличием и выраженностью ряда патологических симптомов. Речь, в частности, идет об общеинфекционном синдроме (лихорадке, интоксикации, вялости), синдроме дегидратации (токсикозе с эксикозом), синдроме метаболического ацидоза, синдроме местных изменений (диарее, рвоте, метеоризме, парезе кишечника). Скорость и тяжесть развития последствий обезвоживания зависит от вида обезвоживания, его выраженности и своевременности лечебных мероприятий, направленных на его устранение.
Причиной частого возникновения дегидратации (эксикоза) у детей принято считать анатомо-физиологические особенности, обусловливающие быстрый срыв адаптационных механизмов и развитие декомпенсации функций органов и систем в условиях инфекционной патологии, сопровождаемых потерей воды и электролитов. Синдром дегидратации у детей со среднетяжелыми и тяжелыми формами острых вирусных гастроэнтеритов обусловлен значительными потерями жидкости со рвотой и патологическим стулом.
Как следствие — ухудшение центральной и периферической гемодинамики, развитие патологических изменений всех видов обмена веществ, накопление в клетках и межклеточном пространстве токсических метаболитов и их вторичное воздействие на органы и ткани больных. Доказано, что основной причиной развития синдрома дегидратации является ротавирусный гастроэнтерит.
Алгоритм терапии ОКИ у детей предполагает целенаправленное воздействие, прежде всего на макроорганизм, обуславливающее коррекцию водно-электролитных расстройств и элиминацию возбудителя. Основополагающей считается патогенетическая терапия: регидратация, диетотерапия, энтеросорбция и использование пробиотиков. При водянистой диарее эксперты Всемирной организации здравоохранения (ВОЗ) признают абсолютно доказанной эффективность только двух терапевтических мероприятий — регидратации и адекватного питания (2006).
Как показал наш опыт (преподавательский и экспертный), к сожалению, именно при проведении регидратационной терапии допускают самое большое количество ошибок. Даже при парентеральном введении жидкости для купирования дегидратации в большинстве историй болезни расчет необходимой жидкости либо отсутствует, либо выполнен некорректно. При проведении оральной регидратации расчет не проводится совсем.
Однако больше всего впечатляет тот факт, что даже при наличии солидного стажа практической работы врачи различных специальностей не понимают, зачем регидратирующую соль растворять в строго определенном объеме жидкости, почему нельзя смешивать глюкозо-солевые и бессолевые растворы. Не секрет, что нередки случаи проведения необоснованной инфузионной терапии, поскольку законные представители ребенка или медицинский персонал не хотят затруднять себя проведением оральной регидратации или не имеют для этого эффективных средств.
Прежде чем приступить к коррекции дефицита жидкости при ОКИ необходимо определить степень дефицита жидкости и объем патологических потерь. Мы попытались осветить различные подходы к оценке степени синдрома дегидратации: традиционный подход российских педиатров-инфекционистов и анестезиологов-реаниматологов и широко вошедшие в повседневную практику критерии ВОЗ и ESPGHAN/ESPID (European Society for Paediatric Gastroenterology, Hepatology, and Nutrition — Европейская ассоциация детских гастроэнтерологов, гепатологов и диетологов/European Society for Paediatric Infectious Diseases — Европейская ассоциация детских инфекционистов) (2008, 2014). Тяжесть синдрома дегидратации оценивается в первую очередь по проценту потери массы тела.
Тяжесть дегидратации в процентах от массы тела ребенка до заболевания
| легкая | средняя | тяжелая | |
| Dell (1973) | 5 | 10 | 15 |
| Robson (1987) | 4-5 | 6-9 | Более 10 |
Используя критерии ВОЗ, оценивая степень дегидратации, можно сразу определить дефицит жидкости.
-
Нет признаков обезвоживания – 150 ммоль/л, уменьшенный объем эритроцита и высокое содержание гемоглобина в нем. Осмолярность плазмы и мочи повышены. Потери натрия — 3—7 ммоль/кг.
Гипотоническая (соледефицитная, внеклеточная) возникает в случае преимущественной потери электролитов (натрия, калия), встречается при преобладании рвоты над диареей. Потеря солей приводит к снижению осмолярности плазмы и перемещению жидкости из сосудистого русла в клетки (внутриклеточный отек). При этом виде дегидратации жажда умеренная. Внешние признаки дегидратации выражены слабо: кожа холодная, бледная, влажная, слизистые не столь сухие, большой родничок западает. Характерно снижение уровня натрия плазмы менее 135 ммоль/л, увеличение объема эритроцита и уменьшение концентрации гемоглобина в нем. Осмолярность плазмы и мочи понижены. Потери натрия — 8—10 ммоль/кг.
Изотоническая (нормотоническая) дегидратация считается наиболее распространенной и сопровождается одновременной потерей жидкости и солей. Как правило, содержание натрия плазмы нормальное, хотя уровень его потерь колеблется от 11 до 13 ммоль/кг. Средний объем эритроцита и концентрация гемоглобина, осмолярность плазмы и мочи — в пределах нормы.
Обычно при ОКИ не бывает изолированной вне- или внутриклеточной дегидратации. Наблюдается тотальное обезвоживание, но в большей степени из внеклеточного сектора. Симптомы гипонатриемии заключаются в развитии неврологической симптоматики: от тошноты, головной боли, потери сознания до комы, судорожного статуса и летального исхода. Тяжесть симптомов зависит как от степени гипонатриемии, так и от темпов ее нарастания. Быстрое снижение содержания внутриклеточного натрия осложняется перемещением воды внутрь клетки, что может привести к отеку головного мозга.
Как показывает клинический опыт, в большинстве случаев синдрома эксикоза имеют место пропорциональные потери воды и электролитов. В результате в 80% случаев развивается изотоническая дегидратация, в 15% — гиперосмолярная, в 5%> — гипоосмолярная.
Основной принцип оральной регидратации — дробное и постепенное введение жидкости. На наш взгляд, наиболее удобен расчет возмещаемой жидкости при оральной регидратации, принятый российским медицинским сообществом. Оральная регидратация проводится в два этапа:
- этап I — в первые шесть часов после поступления больного ликвидируют водно-солевой дефицит, возникший до начала лечения. При синдроме дегидратации первой степени количество жидкости для первичной регидратации на этом этапе составляет 40—50 мл/кг массы тела за первые шесть часов, при синдроме дегидратации второй степени — 80—90 мл/кг массы тела за первые шесть часов;
- этап II — весь последующий период проводят поддерживающую терапию с учетом суточной потребности ребенка в жидкости и солях, а также их потерь. Поддерживающую терапию проводят в зависимости от продолжающихся потерь жидкости и солей с рвотой и испражнениями. За каждый последующий шестичасовой отрезок времени ребенок должен выпить столько раствора, сколько он потерял жидкости с испражнениями и рвотными массами за предыдущие шесть часов. Этот этап регидратации продолжают до прекращения диареи. Ориентировочный объем раствора для поддерживающей регидратации — от 80 до 100 мл/кг массы тела в сутки (при массе не более 25 кг).
Необходимое количество жидкости для пероральной регидратации при синдроме дегидратации у детей, мл
| Эксикоз 1 степени | Эксикоз 2 степени | |||
| Масса тела | За 1 час | За 6 часов | За 1 час | За 6 часов |
| 5 | 42 | 250 | 66 | 400 |
| 10 | 83 | 500 | 133 | 800 |
| 15 | 125 | 750 | 200 | 1200 |
| 20 | 167 | 1000 | 266 | 1600 |
| 25 | 208 | 1250 | 333 | 2000 |
Можно воспользоваться расчетом возмещения жидкости, рекомендуемым ВОЗ для стран с развивающейся экономикой. В отсутствие значимой дегидратации реализуется план А: дети младше 24 месяцев — 50—100 мл после каждого эпизода диареи, дети старше 24 месяцев — 100—200 мл после каждого эпизода диареи. При умеренной дегидратации реализуется план В, при тяжелой — план С. Последний в странах с хорошей доступностью медицинской помощи не применяется, поскольку при серьезной дегидратации (второй-третьей степени) должна проводиться инфузионная терапия.
Оральная регидратация — план В
[youtube.player]Инфузионная терапия – это внутривенное капельное или струйное вливание медицинских растворов по определённой схеме. Лекарственные препараты, поступающие сразу в кровоток, имеют лучшую биодоступность. Тяжёлые кишечные инфекции приводят к обезвоживанию и обменным нарушениям, требующим инфузионной терапии.
Цели инфузионной терапии
Инфузионную терапию проводят для коррекции патологических изменений в организме:
- восполнение дефицита жидкости и электролитов в организме, возникающего из-за рвоты и поноса;
- восстановление кислотно-щелочного равновесия;
- выведение токсинов;
- нормализация работы сердца и сосудистого тонуса;
- улучшение микроциркуляции и тканевого дыхания;
- профилактика сгущения крови, образования тромбов.
Показания
Инфузионную терапию проводят в инфекционном стационаре или в отделении реанимации. Если вы заметили у себя один из тревожных симптомов, вызывайте скорую помощь:

неукротимая рвота;- недостаточная эффективность оральной регидратации – при частом водянистом стуле потери жидкости превышают её поступление;
- отсутствие улучшения в течение 48 часов от начала лечения;
- редкое мочеиспускание;
- сухость во рту, жажда;
- расстройство сознания;
- судороги;
- нарушения работы сердца: редкий или частый пульс, перебои, низкое артериальное давление;
- сахарный диабет – для профилактики декомпенсации заболевания.
Как проводится инфузионная терапия?
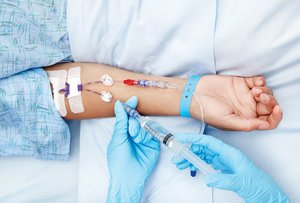
Медицинские растворы вводят в вены локтевого сгиба или кисти. Для этого используют одноразовые стерильные системы для капельного вливания. Для удобства ставят периферический катетер. В тяжёлых случаях препараты вводят струйно с помощью шприца.
Если доступа в вены на руках нет, а состояние угрожает жизни, ставят катетер в подключичную вену. Это серьёзная манипуляция, которую проводит только анестезиолог-реаниматолог. В дальнейшем медицинская сестра подключает к центральному катетеру систему для капельниц.
Инфузионная терапия включает два этапа:
- Базисный – восполнение потребности в жидкости и электролитах. Вводят физиологический раствор и 5% глюкозу.
- Корригирующий – выявление дефицита определённых элементов с помощью анализов и его коррекция. Используют многокомпонентные растворы.
Выбор препарата и схема введения зависит от характера обменных нарушений. Общий суточный объём инфузии зависит от массы тела и степени обезвоживания.
- I (лёгкая) –130-170 мл/кг
- II (средней тяжести) – 170-200 мл/кг
- III (тяжёлая) – до 220 мл/
Во время инфузионной терапии контролируют суточный диурез, относительную плотность мочи, содержание электролитов в крови, уровень гематокрита. По результатам анализов корректируют дозировку лекарств.
Группы препаратов
Кристаллоиды – это водные растворы низкомолекулярные солей, составляют основу инфузионной терапии кишечных инфекций.

Однокомпонентные растворы электролитов. Физиологический раствор натрия хлорида 0,9% назначают для восполнения объёма жидкости и дезинтоксикации. 3% гипертонический раствор используют при гипонатриемии. Для коррекции метаболического ацидоза применяют натрия бикарбонат.- Многокомпонентные растворы электролитов – восполняют дефицит жизненно важных ионов: натрия, магния, калия, кальция, хлора. Содержат два и более активных веществ: Раствор Рингера, Рингера-Локка, Реамберин, Дисоль, Ацесоль,Трисоль. Составы, по концентрации электролитов близкие к плазме, называют изоионными: Лактасол, Рингер-Лактат. Многокомпонентные растворы назначают для регидратации, дезинтоксикации и восстановления баланса жидкости и электролитов.
- 5% раствор Декстрозы – главный источник свободной жидкости; применяют, когда потери воды превышают дефицит солей.
- Поляризующая смесь – раствор глюкозы с добавлением калия и инсулина, назначают при лабораторных и клинических признаках гипокалиемии.
Это группа растворов веществ, имеющих высокую молекулярную массу. По сравнению с кристаллоидами, коллоиды медленнее выводятся из организма, дольше циркулируют в крови. Их применяют при выраженной интоксикации и низком артериальном давлении. При кишечных инфекциях назначают:

Гемодез. Основной компонент препарата поливинилпирролидон связывает и выводит токсины, улучшает микроциркуляцию, активирует почечный кровоток.- Рефортан. Действующее вещество – гидроксиэтилкрахмал. Средство препятствует образованию тромбов, уменьшает интоксикацию, повышает артериальное давление.
- Реополиглюкин. Препарат содержит декстран, при кишечных инфекциях назначают только для коррекции гипотонии.
При поражении кишечника ухудшается всасывание питательных веществ, что приводит к их дефициту в организме. Нарушается образование энергии, синтез белков.
- Инфезол – раствор аминокислот и электролитов.
- СМОФлипид – жировая эмульсия, содержит соевое и оливковое масло, комплекс триглицеридов, рыбий жир.
Противопоказания
Внутривенные вливания назначают при тяжёлом течении кишечных инфекций, поэтому все противопоказания относительны. Если нарушения гомеостаза угрожают жизни пациента, инфузионную терапию все равно проводят.
- Плохой доступ к периферическим венам. Центральный катетер ставят только по жизненным показаниям.
- Гнойнички на коже рук.
- Острое психическое расстройство, неадекватное поведение. Для проведения инфузии пациента фиксируют к кровати.
- Отказ от процедуры.
- Аллергическая реакция на препарат.
Осложнения
Внутривенная инфузия может привести к негативным последствиям. Ожидаемый эффект от лечения должен оправдывать риск возможных осложнений.
Флебиты – воспаление венозной стенки.- Тромбозы – повреждение стенки сосуда способствует тромбообразованию.
- Подкожные гематомы – кровоподтек в зоне инъекции.
- Травма соседних органов – прокол верхушки легкого при катетеризации подключичной вены.
- Аллергия на компоненты раствора – чаще возникает реакция на коллоиды и белковые препараты.
- Передозировка электролитов – бывает при недостаточном контроле над состоянием пациента.
- Отёк лёгких – развивается у пациентов с хроническими заболеваниями сердца при перегрузке жидкостью.
[youtube.player]Длительность инфузионной терапии при кишечных инфекциях в среднем составляет 3-4 дня. При улучшении самочувствия и нормализации показателей водно-солевого обмена капельницы отменяют.
Предрасполагающие факторы:
• Возраст больного – чем младше ребёнок, тем чаще возникает эксикоз и тем более он выражен;
• Неблагоприятный преморбидный фон – перинатальная патология, раннее искусственное вскармливание, гипотрофия, аллергия и пр.;
• Морфофункциональные особенности – функциональная незрелость ЖКТ и ЦНС, лабильность водно-солевого обмена, относительно больший объём внеклеточной жидкости по сравнению со взрослыми, быстрое истощение адаптационных механизмов;
• Незрелость иммунной системы – низкая выработка иммуноглобулинов, в частности секреторного IgA на слизистой оболочке ЖКТ.
Показания к парентеральной регидратации:
Ø Эксикоз III степени;
Ø Неукротимая рвота (чаще 1 раза/час) и/или учащение диареи;
Ø Резко выраженный токсикоз при любой степени обезвоживания (обычно при развитии гиповолемического или инфекционно-токсического шока);
Ø Эксикоз, не корригирующийся оральной регидратацией.
Ø В этом случае не учитывают то количество жидкости, которое давалось per os, т.к. оно практически не усвоилось. Все расчёты суточной потребности в жидкости ведут, принимая во внимание дефицит массы тела на данный момент, физиологические потребности и продолжающиеся патологические потери.
Задачи инфузионной терапии:
Ø Нормализация ОЦК, микроциркуляции и обменных процессов;
Ø Восстановление функции почек;
Ø Нормализация КЩС;
Ø Коррекция водно-электролитных нарушений;
Ø Нормализация осмоса;
Ø При необходимости – обеспечение парентерального питания, энергетических потребностей, витаминов и микроэлементов.
• При всех видах эксикоза, развивающегося на фоне ОКИ, за первые 2-е суток теряются вода и соли (Na + , Ca ++ , Mg ++ , Cl - , особенно опасно нарушение концентрации К + ), а с 3-х суток теряется и белок.
При проведении регидратационной терапии следует определить:
1. Суточный объём жидкости;
2. Возможность частичного энтерального возмещения жидкости;
3. Объём жидкости для инфузии;
4. Состав инфузионных растворов;
5. Определить стартовый раствор;
6. Скорость введения.
Определение в/в объёма инфузии:
Объём в/в вводимой жидкости должен составлять 1/2 - 2/3 от суточной потребности. При этом учитывают количество съеденной жидкой пищи и усвоенной жидкости, введённой per os. Регидрон следует чередовать с питьём кипячёной воды, лечебно-столовой минеральной воды без газа, отвара шиповника и пр. во избежание развития солевой лихорадки.
При скорости инфузии 20 кап/мин её объём составит 60 мл/час.
Расчёт инфузионной терапии в 1 день поступления больного-ФП+ЖВ+ЖТПП:
ФП – физиологическая потребность в жидкости в сутки:
До 3 мес -140 мл/кг/сутки
3-6 мес -140 мл/кг/сутки
6мес -1 год -130-110 мл/кг/сутки
1год -3 года -110 –100 мл/кг/сутки
3года – 5 лет - 100 – 90 мл/кг/сутки
5 -10 лет - 90 -70 мл/кг/сутки
10 - 14 лет - 70 – 50 мл/кг/сутки
14лет и старшие - 40-30 мл/кг/сутки
ЖВ – жидкость возмещения:
Дети до 6 месяцев
Дети от 6мес-12 мес.
Дети от12мес и старше.
ЖТПП –жидкость текущих патологических потерь:
• Потери на лихорадку – 10 мл/кг/сут. на каждый градус Цельсия свыше 37;
• Потери на одышку – 10 мл/кг/сут. на каждые 10 дыхательных движений свыше возрастной нормы;
• Потери с рвотой – 15-20 мл/кг/сут.;
• Потери с диареей:
-лёгкая – 20 мл/кг/сут.
-умеренная - 30 мл/кг/сут.
-выраженная – 40-50 мл/кг/сут.
• Парез к-ка 2ст. – 20 мл/кг/сут. (живот вздут,перистальтика снижена, рвота, газы не отходят, стула нет.)
• Парез к-ка 3ст. – 40 мл/кг/сут. ( рвота кишечным содержимым)
• Неощутимые потери – 10 мл/кг/сут.
В среднем все потери у детей до 1 года составляют 40-50 мл/кг/сут.
Расчёт инфузионной терапии в последующие дни поступления больного-
• Стартовый раствор при II степени эксикоза – 10% глюкоза, а при развитии гиповолемического шока – реополиглюкин.
Считается, что 10% раствор глюкозы является более эффективным, чем её изотонический 5% раствор, поскольку он быстрее нормализует ОЦК, АД и восстанавливает диурез. 5% глюкозу применяют только в случае неуправляемой гипергликемии, когда в/в вводится более 30 г сухого вещества (300 мл 10% раствора глюкозы).
Из солевых растворов используют: ацесоль, трисоль, р-р Рингера, физ. раствор.
• Соотношение глюкозо-солевых и коллоидных растворов –
• Соотношение глюкозы и солевых растворов: дети до 1 года – 2:1
дети старше 1 года – 1:1
• удельный вес коллоидов должен составлять 1/4 от общего объёма инфузии, иногда до 1/3, но не более 10-15 мл/кг/сутки всего.
Все коллоиды считают как кристаллоиды (солевые растворы) по содержанию в них электролитов, если они приготовлены на физиологическом растворе, а не на 5% растворе глюкозы.
Применяют следующие коллоиды:
- Реополиглюкин – обладает волемическим действием (повышает ОЦК), улучшает реологические свойства крови и микроциркуляцию, сорбирует токсины;
- Полиглюкин – резко повышает ОЦК и стабилизирует АД, но повышает вязкость крови и ухудшает микроциркуляцию, особенно в почках;
- Стабизол - повышает ОЦК и стабилизирует АД
- Рефортан - повышает ОЦК и стабилизирует АД
- 5-10% альбумин – повышает ОЦК и АД, восполняет потери белка при гипопротеинемии
- Плазма – улучшает реологические свойства крови, корригирует ДВС-синдром.
Не следует в течение 1-х суток вводить в/в разные коллоиды.
Коррекция электролитных нарушений:
Восстановление потерь К + :
Ø Истинный дефицит К + равен сумме полученного результата и физиологических потребностей в нём, т.е. 1,5-2 ммоль/кг/сут. (1,5-2 мл/кг/сут. 7,5% р-ра KCl).
Ø Суточная доза препаратов К + вводится в/в капельно в 3-4 приёма в концентрации не более 1%, т.е. 10-12 мл 7,5% раствора KCl на каждые 100 мл р-ра глюкозы.
Ø В течение первого часа можно ввести не более 1/2 ммоль = 40 мг = 0,5 мл 7,5% раствора KCl, а в сутки обычно не более 120 мг/кг (3 мл/кг).
Ø Скорость инфузии препаратов К + не должна составлять более 30 кап/мин.
Противопоказания к восстановлению потерь К + :
1. Эксикоз II-III степени (сначала корригируют обезвоживание);
2. ОПН в стадию олигоанурии при диурезе менее 1/3 от возрастной нормы (сначала восстанавливают функции почек);
3. Острая надпочечниковая недостаточность (синдром Уотерхауса-Фридериксена) из-за развития гиперкалиемии;
4. AV-блокада (по данным ЭКГ).
Для коррекции метаболического ацидоза применяются:
-Гидрокарбонат натрия (сода), 4% от4.0 до 7.0мл/кг/веса, в/в капельно, или медленно струйно.
Абсолютным показанием для назначения гидрокарбоната натрия является клиника гиповолемического шока, снижение рН крови ниже 7.2.
Коррекция метаболического алкалоза:
• Метаболический алкалоз (рН > 7,45) – встречается редко, в основном из-за передозировки NaHCO3. Кроме того, он может наблюдаться при потере кислых радикалов (Cl - и Na + ) во время частой рвоты, а также при потере К + . Внеклеточный метаболический алкалоз обычно сочетается с внутриклеточным ацидозом и гипокалигистией.
Для коррекции метаболического алкалоза применяются:
-Препараты К + (4% или 7,5% раствор КCl) с 5-10% глюкозой и инсулином (поляризующая смесь) в/в капельно или струйно очень медленно;
-5% аскорбиновая кислота (витамин С) в дозе 1 мл/год жизни в/в струйно;
-Диакарб в дозе 25-50 мг/кг/сут.;
-21,07% раствор аргинина гидрохлорида - 0,5-1,5 мл/кг/сут. в/в капельно (противопоказан при олигоанурии из-за возможного повышения уровня мочевины в сыворотке крови);
-0,1% раствор НCl – 2-2,5 мл/кг/час в/в капельно.
Контрольные параметры при проведении инфузионной терапии:
Ø ЧСС и характер пульса;
Ø Частота дыхания;
Ø Температура тела аксиллярная и конечностей (определяют их похолодание);
Ø Уровень сознания;
Ø Цвет кожи, слизистых, губ и ногтей (состояние микроциркуляции);
Ø Ионограмма (Na + , К + , Са ++ , Mg ++ , Cl - , HCO3 - );
Ø Биохимические показатели (общий белок, мочевина, креатинин, глюкоза);
Ø Коагулограмма (протромбин, фибриноген и др.).
Критерии эффективности регидратации:
• Уменьшение или прекращение текущих патологических потерь (рвоты, диареи и др.);
• Относительная плотность мочи – 1010-1015;
• ЦВД – 2-10 мм.вод.ст.
| До 2 лет | 50-100 мл после каждого жидкого стула |
| 2 года и старше | 100-200 мл после каждого жидкого стула |
Осложнения инфузионной терапии:
Ø Отек мозга или легких:
· Избыточное введение жидкости;
· Быстрое введение даже правильно рассчитанного объёма жидкости;
· Недостаточное введение коллоидов при гипопротеинемии.
• Введение сердечных гликозидов, глюкокортикостероидов, диуретиков;
• Ингаляция этилового спирта или 10% водного или спиртового раствора антифомсилана (пеногасители);
[youtube.player]В статье изложены современные подходы к регидратационной терапии при острых кишечных инфекциях у детей, в том числе с использованием комплексных методов, направленных на коррекцию не только синдрома обезвоживания, но и микроэкологических нарушений, ассоци
The article covers modern approaches to fluid therapy in acute intestinal infections in children, including use of complex methods directed not only to correction of dehydration syndrome, but also micro-ecological disorders associated with infectious affection of the intestine.
Дегидратационный синдром является ведущим патогенетическим фактором при ОКИ у детей, обуславливая тяжесть заболевания. Поэтому особую значимость для практического здравоохранения приобретает оперативность и правильность оценки степени дегидратации у ребенка, больного ОКИ [9]. Фундаментальные исследования Н. В. Воротынцевой, В. В. Малеева, В. И. Покровского по оценке выраженности обезвоживания на основе оценки острой потери массы тела пациента сохраняют свою актуальность до настоящего времени: эксикозу I степени соответствует потеря до 5% массы тела, что составляет до 50 мл/кг жидкости, эксикозу II степени — потеря 6–10% массы тела (60–100 мл/кг), эксикозу III степени — потеря более 10% массы тела (110–150 мл/кг). Обезвоживание с потерей массы тела более 20% не совместимо с жизнью [10]. Однако применительно к педиатрической практике определение дефицита массы тела ребенка на фоне болезни не всегда возможно ввиду интенсивного роста детей, поэтому оценка степени дегидратации проводится на основе клинических данных. В этой связи в настоящее время широкое распространение получили рекомендации Европейского общества педиатров, гастроэнтерологов и диетологов (European Society for Paediatric Gastroenterology Hepatology and Nutrition, ESPGHAN) от 2014 г. [11]. Однако в них предусмотрена клиническая оценка только внешнего вида, состояния глазных яблок и слизистых оболочек, а также наличие у ребенка слез. Более полная клиническая шкала M. H. Gorelick дополнительно включает определение времени капиллярной реперфузии (в норме не более 2 секунд), снижение диуреза, основные гемодинамические показатели (частота и наполнение пульса) и показатели нарушения дыхания [12]. Существуют и другие шкалы клинической оценки выраженности обезвоживания. Однако значимость каждого из симптомов обезвоживания в клинической практике может быть не всегда достаточно высокой, особенно при эксикозе I степени, что делает их наиболее применимыми при эксикозе II степени (табл. 1).
При ОКИ у детей преобладает изотонический тип обезвоживания, характеризующийся пропорциональной потерей жидкости и электролитов, в первую очередь натрия. При этом не отмечается изменения осмотического давления воды во внутриклеточном и внеклеточном пространствах, что затрудняет его определение лабораторными методами [15].
Объективизация диагностики степени выраженности обезвоживания у детей возможна с применением алгоритма, включающего клинические (увеличение времени капиллярной реперфузии, определяемая клинически сухость слизистых оболочек), анамнестические (выраженность диареи и рвоты), инструментальные (оценка влажности кожных покровов) и лабораторные (дефицит буферных оснований сыворотки крови) данные [16].
Также одним из важных аспектов патогенеза, являющегося закономерным для ОКИ любой этиологии, является развитие нарушений микрофлоры желудочно-кишечного тракта (ЖКТ). Ранее было показано, что при дизентерии Зонне у 67,8–85,1% пациентов, при сальмонеллезе — у 95,1%, иерсиниозе — у 94,9%, ротавирусной инфекции — у 37,2–62,8% нарушения со стороны микрофлоры ЖКТ носят выраженный характер [17–19].
Дестабилизация микробиоценоза ЖКТ на фоне течения инфекционного процесса приводит к снижению колонизационной резистентности микрофлоры, повышению выраженности воспалительных реакций со стороны слизистой оболочки кишки и снижению темпов репаративных процессов в кишечнике, что приводит к усугублению интоксикационного синдрома за счет высвобождения токсинов не только патогенных возбудителей, но и представителей условно-патогенной микрофлоры (УПФ), доля которых при ОКИ возрастает [20].
Основные патогенетические аспекты ОКИ обосновывают и терапевтические подходы — регидратационную и пробиотическую терапию, от своевременности и адекватности назначения которых зависят длительность заболевания и его исходы [10].
При развитии дегидратации основным принципом ведения таких больных является быстрое возмещение потерь жидкости и солей, а также увеличение буферной емкости крови. Общепризнано, что в педиатрической практике следует отдавать предпочтение оральной регидратации, как менее травматичной и более физиологичной для ребенка [21]. Международная практика применения оральной регидратации при ОКИ получила широкое применение с 70-х годов XX века, а ее включение в стандарты ведения больных позволило сократить число случаев госпитализации на 50–60% и значительно, на 40–50%, снизить летальность детей [22]. Однако первые рекомендации, которые можно отнести к регидратационной терапии и включающие в себя назначение рисового отвара, кокосового сока и морковного супа, относятся к периоду более 2500 лет назад и принадлежат древнеиндийскому врачу Sushruta [23]. В 1874 г. во Франции доктором Luton было обосновано назначение дополнительной воды для лечения детей, больных ОКИ. Впервые раствор, в состав которого вошли глюкоза, натрий и хлор, предложил использовать доктор Robert A. Phillips, после открытия механизма потенцирования глюкозой всасывания в кишечнике ионов натрия и калия [23]. В нашей стране в 30–50-х годах XX века проводилась разработка методов регидратационной терапии ОКИ М. С. Масловым (1928, 1945, 1955), В. И. Моревым (1937), В. Е. Балабан (1937). Основные принципы оральной регидратации, состав растворов и методы организации помощи больным ОКИ в нашей стране были разработаны Центральным научно-исследовательским институтом эпидемиологии под руководством В. И. Покровского [10].
Общий терапевтический подход к оральной регидратации предусматривает раннее назначение регидратационных растворов и проводится в два этапа:
- 1-й этап — восполнение потерь, произошедших до момента обращения за медицинской помощью. Назначается суммарное количество жидкости 50–80 мл/кг в течение 6 ч;
- 2-й этап — поддерживающая регидратация, задачей которой является восполнение текущих потерь жидкости при ОКИ. В сутки назначается 80–100 мл/кг жидкости. Длительность второго этапа оральной регидратации продолжается до момента выздоровления или появления показаний для парентеральной коррекции обезвоживания [24].
Согласно действующим современным подходам, для проведения оральной регидратации рекомендовано использование готовых форм растворов, сбалансированных по электролитному составу и осмолярности (75 мэкв/л натрия и 75 мэкв/л глюкозы и осмолярностью 245 мосм/л), при этом значению осмолярности растворов, рекомендуемых для педиатрического применения, уделяется огромное значение.
На заре внедрения метода в рутинную клиническую практику в 1970 г., Всемирная организация здравоохранения рекомендовала для проведения оральной регидратации составы с общей осмолярностью 311 ммоль/л. Несмотря на их эффективность в коррекции обезвоживания главным недостатком данных базовых растворов было отсутствие положительного влияния на диарейный синдром. Одним из достижений, предложенным в 2004 г. ВОЗ, было снижение осмолярности растворов для оральной регидратации до 245 ммоль/л, а концентрации натрия до 75 ммоль/л и глюкозы до 75 ммоль/л. Принципиальным отличием гипоосмолярных формул для оральной регидратации является то, что у предыдущих растворов осмолярность была выше по сравнению с плазмой крови, что не способствовало снижению объема каловых масс при диарее и могло приводить к развитию гипернатриемии [25–28]. В 2001 г. Seokyung Hahn был сделан метаанализ 15 рандомизированных клинических исследований, проведенных в различных странах мира, который показал, что применение растворов для оральной регидратации со сниженной осмолярностью оптимизирует всасывание воды и электролитов в кишечнике в большей степени, чем использование гиперосмолярных растворов, при этом не было зарегистрировано случаев клинически значимой гипонатриемии, за исключением случаев холеры [29].
Также было показано, что данный тип растворов уменьшает потребность в инфузионной терапии, снижает выраженность диарейного синдрома и рвоты и позволяет уменьшить объемы растворов при проводимой оральной регидратации, что является важным преимуществом для педиатрии [16].
Необходимо учитывать, что коррекция обезвоживания должна проводиться с использованием и бессолевых растворов, среди которых предпочтение следует отдать питьевой воде (не минеральной!), возможно использование пектинсодержащих отваров (яблочный компот без сахара, морковно-рисовый отвар). Соотношение глюкозосолевых растворов и питьевой воды должно быть 1:1 при водянистой диарее, 2:1 при выраженной рвоте, 1:2 при инвазивных диареях [24].
Тяжелые формы ОКИ, отсутствие эффекта от оральной регидратации или наличие обильной рвоты, отеков, развитие функциональной (острой) почечной недостаточности являются показаниями для проведения парентеральной регидратации, которая может быть осуществлена с использованием одного из современных отечественных растворов — 1,5% раствора меглюмина натрия сукцината, доказавшего свою эффективность в интенсивной терапии данных состояний [30].
Патогенетическое обоснование необходимости применения пробиотических лекарственных средств при ОКИ не вызывает сомнения как в отечественной, так и в зарубежной литературе. Пробиотическую терапию рекомендовано назначать в составе комплексной стартовой терапии вне зависимости от этиологии заболевания и в как можно более ранние сроки. Данные препараты показаны также всем пациентам в периоде реконвалесценции с целью восстановления параметров микробиоценоза. Их применение при ОКИ у детей является не только патогенетически обоснованным, но и относится к самому высокому уровню доказательности — А — в соответствии с принципами доказательной медицины [31]. Данный факт был подтвержден в 2010 г. результатами метаанализа, включившего в себя результаты 63 рандомизированных контролируемых клинических исследований. В нем было показано, что использование пробиотиков достоверно уменьшает продолжительность диареи в среднем на 24,76 часа и сокращает частоту стула, при этом данные препараты характеризуются высоким профилем безопасности [32].
Одним из патогенетических механизмов, позволяющих рекомендовать пробиотики при ОКИ, является их положительное влияние на муциновый слой слизистой оболочки ЖКТ. На фоне течения инфекционного процесса наблюдается изменение физических характеристик данного барьера — снижение вязкости за счет разрушения дисульфидных связей между цистеиновыми мостиками суперструктуры данного геля, что может приводить к транслокации микроорганизмов из просвета кишечника в ткани. Данные процессы развиваются под действием патогенных микроорганизмов, имеющих соответствующие факторы патогенности в виде ферментов, разрушающих слизь (нейраминидаза, гиалуронидаза, муциназа). Длительное, в том числе в постинфекционном периоде, изменение физических свойств муцинового слоя приводит к риску развития воспалительных заболеваний кишечника [33]. Микроорганизмы, относящиеся к компонентам нормальной микрофлоры ЖКТ человека, а также продукты их обмена оказывают потенцирующее действие на состояние муцинового слоя посредством целого ряда механизмов, в том числе генетических [34, 35].
Современный взгляд на терапию пробиотиками подразумевает штамм-специфичный подход, который включает в себя установление в клинических исследованиях терапевтических эффектов, характерных для определенных генетически сертифицированных штаммов и дальнейшее их использование с учетом штамм-специфичных свойств пробиотиков в различных клинических ситуациях [36, 37].
Применительно к острым кишечным инфекциям у детей рабочая группа ESPGHAN в 2014 г. на основе анализа опубликованных систематических обзоров и результатов рандомизированных клинических исследований, в том числе плацебо-контролируемых, опубликовала меморандум, в котором разделила все пробиотические штаммы на пробиотики с положительной рекомендацией, с отрицательной рекомендацией и пробиотики с недостаточными доказательствами их эффективности. К рекомендованным штаммам (несмотря на низкий уровень доказательной базы по мнению экспертов) для терапии ОКИ у детей были отнесены Lactobacillus GG, Saccharomyces boulardii, Lactobacillus reuteri штамм DSM 17938 (исходный штамм ATCC 55730), а также термически инактивированный штамм Lactobacillus acidophilus LB, который формально к пробиотикам как живым микроорганизмам с заданными полезными свойствами отнесен быть не может, однако он показал свою эффективность при острых инфекционных гастроэнтеритах [38].
Штамм Lactobacillus reuteri DSM 17938 устойчив к следующим антимикробным средствам (возможен совместный прием пробиотиков Lactobacillus reuteri Protectis с этими средствами): амоксициллин, ампициллин, Аугментин, диклоксациллин, оксациллин, пенициллин G, феноксиметилпенициллин, цефуроксим, цефалотин, ванкомицин, доксициклин, тетрациклин, фузидовая кислота, ципрофлоксацин, энрофлоксацин, налидиксовая кислота, метронидазол. Lactobacillus reuteri DSM 17938 чувствительны к цефотаксиму, неомицину, стрептомицину, кларитромицину, эритромицину, рокситромицину, клиндамицину, хлорамфениколу, рифампицину, имипенему, линезолиду, виргиниамицину.
При этом Lactobacillus reuteri DSM 17938 характеризуется хорошим профилем безопасности, что подтверждено Продовольственной и сельскохозяйственной организацией ООН (Food and Agriculture Оrganization of the United Nations, FAO) и ВОЗ в 2002 г.
Клиническая эффективность Lactobacillus reuteri DSM 17938 показана при функциональных коликах у детей первого года жизни, в составе комплексной эрадикационной терапии H. рylori-инфекции, профилактики антибиотик-ассоциированной диареи, при метаболическом синдроме, в терапии аллергических заболеваний. Эффективность данного штамма подтверждена в 163 клинических исследованиях у 14 000 пациентов, из которых 114 — рандомизированные, двойные/слепые или слепые плацебо-контролируемые исследования, 47 — открытые исследования, 56 исследований проводились среди 7300 детей 0–3 лет жизни.
Однако наиболее хорошо изучены клинические эффекты данного штамма при ОКИ, что послужило причиной включения его в рекомендации ESPGHAN. Так, в многоцентровом рандомизированном простом слепом клиническом исследовании, проведенном среди госпитализированных с острым гастроэнтеритом детей, получавших традиционную терапию с или без 1 × 10 8 КОЕ Lactobacillus reuteri DSM 17938 на протяжении 5 дней, было показано, что назначение данного пробиотического штамма сокращает продолжительность диареи через 24 и 48 ч (50% в основной группе против 5% в группе сравнения, p
А. А. Плоскирева 1 , кандидат медицинских наук
А. В. Горелов, доктор медицинских наук, профессор, член-корреспондент РАН
ФБУН ЦНИИЭ Роспотребнадзора, Москва
[youtube.player]Читайте также:


