Ревматическая полимиалгия диагностические критерии
Ревматическая полимиалгия — воспалительное заболевание опорно-двигательного аппарата, развивающееся только во второй половине жизни человека, характеризующееся сильными болями стереотипной локализации (область шеи, плечевой и тазовый пояс), нарушениями движений, значительным повышением лабораторных показателей воспаления, а также наступлением ремиссии при назначении ГК в небольших дозах.
Ревматическая полимиалгия в 15% случаев сочетается с гигантоклеточным (височным) артериитом (болезнью Хортона). МКБ-10: М35.3 Ревматическая полимиалгия; М31.5 Гигантоклеточный артериит с ревматической полимиалгией. Эпидемиология. Частота выявления новых случаев ревматической полимиалгии за год в различных странах колеблется от 4,9 до 11,1 на 100 000 всех жителей (от 12,7 до 68,3 на то же количество жителей в возрасте 50 лет и старше).
Отмечена тенденция к меньшей распространённости заболевания в странах, расположенных ближе к экватору. В возрасте моложе 50 лет ревматическая полимиалгия не встречается. Пик заболеваемости приходится на седьмую декаду жизни. Примерно в 2 раза чаще болеют женщины. Профилактика не разработана. Скрининг нецелесообразен в связи с редкостью заболевания.
Классификация. Выделяют изолированную ревматическую полимиалгию и ревматическую полимиалгию, сочетающуюся с гигантоклеточным артериитом.
Диагностика. Клинические проявления
• Заболевание в большинстве случаев развивается остро, полная картина (пик болезни) формируется за 2—4 нед.
Возникают сильные боли, охватывающие область шеи, плечевые суставы и плечи, тазобедренные суставы и бёдра. Боли в области плечевого и тазового пояса двухсторонние и симметричные, постоянные, усиливаются при движениях. В покое боли на время уменьшаются, но возникают при каждом изменении положения тела. Из-за этого резко нарушается сон. Типична скованность, наиболее выраженная утром после сна или любого длительного периода неподвижности.
Постоянным признаком ревматической полимиалгии являются ограничения движений в плечевых, тазобедренных суставах, а также в области шеи. Из-за болей существенно нарушаются са мообслуживание (трудно причесаться, умыться, одеться, поднять и удержать что-либо руками, сесть на низкое сиденье и встать с него), а также способность к передвижению. В ряде случаев больные вынуждены проводить в постели. Приём анальгетиков и НПВП существенно не влияет на состояние больных ревматической полимиалгией.
• У ряда больных развивается слабо выраженный артрит лучезапястных, коленных, ключично-акромиальных суставов и очень редко — мелких суставов кистей или стоп. Как правило, число воспалённых суставов не превышает 1—3, симметричность поражения отсутствует. Боли в поражённых суставах обычно невелики, они намного меньше, чем в плечевом и тазовом поясе. Нередко припухлость суставов и болезненность при движениях в них можно заметить только при целенаправленном осмотре.
• У отдельных больных развивается слабовыраженный синдром карпального канала с типичными проявлениями в виде онемения в кончиках I—IV пальцев кистей, а иногда ладонный фасциит: умеренный отёк кисти, формирование сгибательных контрактур пальцев, уплотнение и болезненность ладонной фасции и сухожилий-сгибателей пальцев.
• Нередко отмечается лихорадка, обычно субфебрильная, но иногда доходящая до 38°С и выше. Лихорадка никогда не предшествует типичным болевым ощущениям, а обычно присоединяется в их разгаре, утяжеляя состояние больных. Во многих случаях довольно быстро возникает снижение массы тела, иногда значительное, что обычно сопровождается потерей аппетита. Характерны также общая слабость, сниженное настроение.
• У больных ревматической полимиалгией могут отмечаться явные или скрытые признаки гигантоклеточного артериита (см. ниже). Целенаправленное выявление этих признаков должно осуществляться у каждого больного ревматической полимиалгией, так как наличие артериита определяет прогноз и требует применения незамедлительного назначения существенно большей дозы кортикостероидов, чем при изолированной ревматической полимиалгии.
Рекомендуемое обследование в стационаре
• Лабораторные исследования: общий анализ крови, общий анализ мочи, биохимическое исследование (щелочная фосфатаза, КФК, кальций и фосфор, РФ, общий белок и его фракции).
♦ Общий анализ крови. У всех больных с первых дней заболевания резко повышаются СОЭ - 40 мм/ч и более, а также уровень СРБ. Степень увеличения этих показателей воспаления обычно соответствует выраженности болевого синдрома и нарушений движений. У многих больных возникает гипохромная анемия.
♦ Биохимическое исследование. У трети больных выявляется небольшое повышение уровня трансаминаз и щелочной фосфатазы в крови (активность этих ферментов нормализуется вскоре после начала приёма ГК).
Диагноз
• Общепринятых критериев диагностики ревматической полимиалгии не существует.
• Применяют следующие диагностические признаки заболевания.
1) возраст пациента в начале болезни не менее 50 лет;
2) боли по крайней мере в 2 из следующих 3 областей: плечевой, тазовый пояс и шея;
3) двусторонняя локализация болевых ощущений в плечевом и тазовом поясе;
4) преобладание указанной локализации болей во время пика болезни;
5) увеличение СОЭ более 35 мм/ч;
6) быстрый и яркий эффект преднизолона в суточной дозе не более 15 мг в день;
7) отсутствие признаков РА.
Для диагностики ревматической полимиалгии необходимо наличие всех указанных признаков.
• При постановке диагноза важно оценивать результат применения ГК. Практически у всех больных уже через несколько дней после ежедневного приёма преднизолона (обычно в дозе 15 мг в день) радикально улучшается состояние, нормализуются СОЭ и другие лабораторные показатели воспаления. Поэтому больных нужно обязательно осмотреть после назначения преднизолона.
Отсутствие ожидаемой положительной динамики может указывать на ошибочность диагноза. Дифференциальная диагностика проводится с парапротеинемическими гемобластозами (миеломная болезнь и др.), псориатическим артритом, РА, полимиозитом, системными васкулитами, заболеваниями мягких тканей опорно-двигательного аппарата, остеомаляцией, гиперпаратиреозом, острыми инфекциями, сопровождающимися миалгиями.
Показания к консультации других специалистов. При обнаружении признаков гигантоклеточного артериита может возникнуть необходимость в консультации окулиста, ангиолога, в проведении ультразвукового сканирования магистральных артерий шеи, конечностей и аорты, а также в проведении биопсии височной артерии.
Показания к госпитализации в ревматологическое отделение. Необходимость дополнительного обследования пациента, которое невозможно осуществить в амбулаторных условиях, — серьёзные сопутствующие заболевания, уточнение состояния которых требуется перед или во время начала терапии ГК.
Лечение
Цели терапии: достижение ремиссии, а в дальнейшем - выздоровления. Обучение. Пациента следует информировать об основных правилах приёма ГК, о диете и наиболее частых побочных реакциях.
Немедикаментозное лечение. При ревматической полимиалгии немедикаментозная терапия не проводится.
Медикаментозное лечение
• Единственным эффективным средством лечения ревматической полимиалгии являются ГК. Их назначение считается обязательным, так как это значительно снижает риск присоединения гигантоклеточного артериита.
• Начальная доза преднизолона составляет обычно 15 мг в день и обязательно распределяется на 2 — 3 приёма. Если положительный эффект очевиден, но ко 2-3-й неделе лечения не отмечается полной клинико-лабораторной ремиссии заболевания, доза преднизолона может быть увеличена до 20 мг. В отдельных случаях, когда выраженность ревматической полимиалгии умеренная, начальная суточная доза преднизолона может составлять 10 мг.
• После развития ремиссии подавляющую дозу преднизолона сохраняют ещё в течение 1 мес, а затем начинают постепенно снижать до полной отмены препарата. Снижение проводится на 1,25 мг через каждые 7-10 дней при условии отсутствия признаков обострения заболевания до достижения 10 мг/сут; затем по 1 мг в день каждые 4 нед.
• В случае развития обострения необходимо временное повышение дозы преднизолона на величину, достаточную для достижения ремиссии заболевания. Обострения чаще возникают во время приёма небольших поддерживающих доз препарата, могут неоднократно повторяться.
• В процессе снижения дозы преднизолона следует тщательно наблюдать за динамикой симптомов; контролировать СОЭ каждые 4 нед в течение первых 2-3 мес; затем каждые 8-12 нед в течение 12 мес после завершения лечения.
• Полного выздоровления (с отменой преднизолона) удаётся достичь у всех больных, но время, необходимое для этого, бывает различным: от 6 мес до 2—3 лет. Известны единичные случаи рецидивов болезни.
• Попытки применения гидроксихлорохина, метотрексата, азатиоприна и циклоспорина для лечения ревматической полимиалгии (в качестве стероидосберегающих средств) оказались либо неуспешными, либо их результаты противоречивы.
Прогноз у преобладающего большинства больных изолированной ревматической полимиалгией благоприятен (выздоровление). Если не применяются ГК, ревматическая полимиалгия обычно принимает хроническое, волнообразное течение; известны отдельные случаи спонтанного выздоровления (как правило, не ранее чем через 6—12 мес).
Клиническая картина РПМ состоит из комбинации признаков поражения опорно-двигательного аппарата и изменений лабораторных показателей воспаления, которые наблюдаются у всех пациентов, а также общих (конституциональных) нарушений, возникающих часто, но не постоянно [6]. Клинические особенности РПМ отображены в следующих положениях.
• Основными клиническими симптомами являются боль и скованность в плечевом и тазовом поясе, шее, которые в большинстве случаев носят симметричный характер.
• Симптомы в большей степени выражены в утреннее время.
• Общеконституционные симптомы – слабость, вялость, общее недомогание, депрессия, потеря веса, субфебрильная температура тела.
• Характерны артралгии и артриты суставов кистей, теносиновиты кисти.
• Несмотря на наличие миалгий, отсутствует мышечная слабость, боль не уменьшает силу в конечностях, не отмечаются мышечные атрофии/гипотрофии.
• Определяется болезненность мышц при пальпации от слабой до умеренной.
• Уменьшение диапазона движений в суставах, возможно, из-за боли.
• Могут присоединяться симптомы гигантоклеточного артериита (болезни Хортона). Единого мнения по вопросу взаимосвязи РПМ и болезни Хортона нет. Она может быть начальным симптомом, возникать одновременно и появляться позже. Приблизительно у 15% пациентов с РПМ развивается гигантоклеточный артериит, и 40-50% больных с гигантоклеточным артериитом имеют РПМ [3].
• Лабораторные характеристики и особенности РПМ сгруппированы ниже.
• Существенное повышение СОЭ >50 мм/ч и уровня С-реактивного белка (СРБ). СРБ при этом – более чувствительный показатель, чем СОЭ.
• Анемия – нормохромная, нормоцитарная (анемия хронического заболевания).
• Миозит-специфические ферменты: нормальные значения креатинфосфокиназы, миоглобина, альдолазы.
• Ревматоидный фактор негативный (следует помнить о возможности позитивного ревматоидного фактора у 5% лиц без признаков ревматического заболевания), антитела к циклическому цитруллинированному пептиду – негативные.
• Антинуклеарные антитела – негативные.
• Наблюдается значительное повышение уровня интерлейкина-6, что коррелирует с выраженностью воспаления.
• Может отмечаться незначительное повышение уровня печеночных ферментов (АлАТ, АсАТ, ГГТП).
С помощью инструментальных методов исследования установлено, что клиническая симптоматика РПМ обусловлена главным образом воспалительными изменениями суставов и околосуставных тканей. Магнитно-резонансная томография, ультразвуковое исследование (УЗИ) и позитронно-эмиссионная томография позволяют выявить у больных РПМ признаки бурсита в области плечевых и тазобедренных суставов, а также шейного отдела позвоночника [7, 8]. Наиболее характерными являются поддельтовидный бурсит, теносиновит бицепса, трохантерный (вертлужный) бурсит, выпот в плечевом и/или тазобедренном суставах. Описан также синовит плечевых и тазобедренных суставов. При гистологическом исследовании синовиальной оболочки у больных РПМ наблюдается слабо выраженная воспалительная инфильтрация с преобладанием макрофагов и CD4 Т-клеток [10].
На сегодняшний день не существует единственного клинического, лабораторного или инструментального признака, наличие которого позволяло бы подтвердить диагноз РПМ. Диагностика проводится на основании совокупности проявлений болезни. Наиболее типичные из них используются в качестве диагностических критериев, предложенных Европейской группой по изучению РПМ [8]. Они включают обязательные необходимые критерии, к которым относят возраст ≥50 лет, двустороннюю боль в плечах (появившуюся менее 12 нед назад), повышение СОЭ/уровня CРБ. Критерии следует применять лишь в тех случаях, когда диагноз другого заболевания не представляется более обоснованным [4]. Для верификации диагноза и решения вопроса о назначении глюкокортикоидов (ГК) у таких пациентов могут быть использованы два набора критериев.
При отсутствии данных УЗИ диагноз может быть подтвержден на основании 4 признаков: утренней скованности более 45 мин, боли или ограничения подвижности в тазобедренном суставе, отсутствия ревматоидного фактора и АЦЦП, отсутствия поражения других суставов. Максимально возможная сумма баллов по данным 4 критериям составляет 6. Для подтверждения диагноза РПМ достаточно 4 баллов.
Второй набор классификационных критериев используется при наличии результатов УЗИ и, помимо указанных основных 4 параметров, включает 2 дополнительных. Каждый дополнительный критерий представляет собой набор сонографических признаков. Первый из них предусматривает наличие как минимум поддельтовидного бурсита и/или теносиновита бицепса и/или синовита плечевого сустава (заднего или аксиллярного отдела), а также синовита тазобедренного сустава и/или трохантерного бурсита. Второй определяется как наличие двустороннего поддельтовидного бурсита, теносиновита бицепса или синовита плечевых суставов. Каждый из дополнительных критериев оценивается в 1 балл. Поэтому при использовании второго набора классификационных критериев максимально возможная сумма баллов составляет 8, и в этом случае для подтверждения диагноза РПМ необходимо набрать 5 баллов (табл.).

На сегодняшний день существует множество расхождений в подходах к лечению РПМ, которые включают вопросы дозирования ГК и целесообразности использования базисных болезнь-модифицирующих антиревматических препаратов [5].
К сожалению, у большинства пациентов (29-45%), страдающих РПМ, не удается достичь адекватного ответа на терапию ГК в течение первых 3-4 недель. При этом приблизительно у 50% больных наблюдаются различные побочные эффекты на фоне лечения этой группой препаратов. Целью Американской коллегии ревматологов (ACR) и Европейской антиревматической лиги (EULAR) являлось обеспечение клиницистов кратким, четко изложенным современным руководством, которое поможет стандартизировать подходы к лечению и улучшить прогнозы для пациентов с данным заболеванием [9]. Как обычно, при создании подобных рекомендаций эксперты ACR и EULAR руководствовались доказательной методологией с использованием классов рекомендаций и уровней доказательств [2]. Алгоритм лечения РПМ, основанный на рекомендациях (EULAR/ACR 2015), представлен на рисунке.

Экспертами тщательно проработана и обобщена вся база исследований по РПМ, а после детальной оценки и обсуждения изложена в окончательном варианте данных рекомендаций [9].
1. На старте терапии больных РПМ настоятельно рекомендуется использовать ГК вместо нестероидных противовоспалительных препаратов (НПВП), за исключением возможного кратковременного применения НПВП и/или анальгетиков в случаях, когда болевой синдром ассоциирован с другой патологией (к примеру, сопутствующим остеоартритом).
2. Настоятельно рекомендуется использовать минимально эффективную индивидуальную длительность ГК-терапии у больных РПМ.
3. Условно рекомендуется применять минимально эффективную дозу ГК в диапазоне 12,5-25 мг преднизолона (или эквивалента) как стартового лечения РПМ. Вопрос о назначении более высокой стартовой дозы ГК в границах этого диапазона может рассматриваться у пациентов с высоким риском развития рецидива и низким риском возникновения побочных эффектов; в то же время у пациентов с сопутствующими заболеваниями (например, сахарным диабетом, остеопорозом, глаукомой и др.) и другими факторами риска для ГК-ассоциированных побочных эффектов может быть предпочтительным назначение более низких доз ГК. Условно отрицается использование начальных доз ≤7,5 мг/сут и высказаны настоятельные возражения против применения начальных доз >30 мг/сут.
4. Настоятельно рекомендуется индивидуализация графиков постепенной отмены ГК, основанных на регулярном мониторинге состояния пациента, активности заболевания, лабораторных маркеров и негативных событий. Предложены следующие принципы снижения доз:
a) стартовое снижение: рекомендуется медленно уменьшать дозу ГК до 10 мг/сут в пересчете на преднизолон на протяжении 4-8 нед;
b) терапия рецидивов: рекомендуется увеличить дозу перорального преднизолона до уровня, предшествовавшего рецидиву, и в последующем уменьшать ее постепенно (в течение 4-8 нед) до дозы, во время приема которой случился рецидив;
c) снижение дозы в период ремиссии: после достижения ремиссии необходимо уменьшать дозу перорального преднизолона на 1 мг каждые 4 нед (либо на 1,25 мг, используя, к примеру, схему 10/7,5 мг через день и т.д.) на протяжении того времени, пока сохраняется ремиссия.
5. Условно рекомендуется рассмотреть возможность внутримышечного введения метилпреднизолона как альтернативы применению пероральных ГК. Выбор между пероральным и внутримышечным введением остается на усмотрение врача. Рекомендации не могут четко указать фенотип пациента, который бы нуждался во внутримышечном введении ГК. Предложен следующий график отмены внутримышечного метилпреднизолона:
• метилпреднизолон (депо-форма) внутримышечно 120 мг каждые 3 нед до 9-й недели;
• на 12-й неделе – 100 мг, с последующими 3-месячными интервалами;
• далее доза снижается на 20 мг каждые 12 нед до 48-й недели;
• после этого доза снижается на 20 мг каждые 16 нед до полного прекращения.
6. Условно рекомендуется использовать одноразовый, а не раздельный прием ежедневных доз ГК для лечения РПМ. Разделять дозу препарата на несколько приемов следует в случае выраженного интенсивного болевого синдрома в ночное время суток.
7. Условно рекомендуется учесть возможность раннего назначения метотрексата в дополнение к ГК, в частности у пациентов с высоким риском развития рецидива и/или длительной терапии, а также в случаях имеющихся факторов риска, сопутствующих заболеваний и/или приема сопутствующих препаратов, когда высока вероятность возникновения осложнений ГК-терапии или побочных эффектов ГК. В клинических испытаниях метотрексат применялся перорально в дозах 7,5-10 мг/нед.
8. Настоятельно не рекомендуется использовать ингибиторы фактора некроза опухолей для лечения РПМ в связи с отсутствием доказательной базы. В настоящее время продолжается только одно рандомизированное клиническое исследование с тоцилизумабом (clinicaltrials.gov NCT01396317), а также в другом исследовании сравниваются секукинумаб, канакинумаб и ГК (clinicaltrials.gov NCT01364389).
9. Условно рекомендуется рассмотреть вопрос о создании индивидуальной программы упражнений для пациентов с РПМ, направленных на поддержку мышечной массы и функции, а также снижение риска падений.
10. Применение растительных препаратов в терапии РПМ не рекомендуется.
Особенно категорически авторы документа выступают против использования китайских травяных препаратов Yanghe и капсул Biqi у пациентов с РПМ. Данное заявление связано в первую очередь с тем, что вышеуказанные средства не одобрены Управлением по контролю качества пищевых продуктов и лекарственных препаратов США (FDA), а также Европейским агентством лекарственных средств (EMA).
Настоящие рекомендации [9] Американской коллегии ревматологов и Европейской антиревматической лиги предназначены прежде всего для врачей-клиницистов, и предполагается, что они окажут им определенную помощь в ведении пациентов с РПМ.
1. Бунчук Н.В. Ревматические заболевания пожилых. – М.: МЕДпресс-информ, 2010. – 272 с.
2. Ватутин Н.Т., Смирнова А.С., Тарадин Г.Г., ЭльХатиб М.А. Обзор рекомендаций по лечению ревматической полимиалгии (EULAR/ACR 2015). Архивъ внутренней медицины. 2016; 1: 3-5.
3. Глазунов А.В., Жиляев Е.В., Толдиева Ф.А. Ревматическая полимиалгия и височный артериит. Клиническая геронтология. 2006; 6: 34-46.
4. Олюнин Ю.А. Ревматическая полимиалгия. Consilium medicum. 2013; 15(9): 53-57.
5. Сатыбалдыев А.М. Лечение ревматической полимиалгии. Современная ревматология. 2013; 1: 66-72.
6. Щедрина И.С., Троицкая М.П., Овчаренко С.И. Ревматическая полимиалгия: сложности диагностики. Лечащий врач. 2011; 4: 33-36.
7. Blockmans D., de Ceuninck L., Vanderschueren S. et al. Repetitive 18-fluorodeoxyglucose positron emission tomography in isolated polymyalgia rheumatica: a prospective study in 35 patients. Rheumatology (Oxford) 2007; 46 (4): 672–677.
8. Dasgupta B., Cimmino M., Maradit-Kremers H. et al. 2012 provisional classification criteria for polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann Rheum Dis. 2012; 71(4): 484-492.
9. Dejaco C., Singh Y., Perel P. et al. 2015 Recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism. American College of Rheumatology collaborative initiative Ann Rheum Dis. 2015; 74: 1799–1807.
10. Meliconi R., Pulsatelli L., Uguccioni M. et al. Leukocyte infiltration in synovial tissue from the shoulder of patients with polymyalgia rheumatica. Quantitative analysis and influence of corticosteroid treatment. Arthritis Rheum. 1996; 39 (7): 1199-1207.
11. Spiera R., Westhovens R. Provisional diagnostic criteria for polymyalgia rheumatica: moving beyond clinical intuition? Ann Rheum. Dis. 2012; 71 (4): 475-476.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Ключевые слова: ревматическая полимиалгия, классификационные критерии, глюкокортикоиды, острофазовые показатели крови.
Для цитирования: Башкова И.Б., Бусалаева Е.И. Ревматическая полимиалгия: редко диагностируемое, но нередко встречающееся заболевание. РМЖ. Медицинское обозрение. 2017;1:48-52.
Rheumatic polymyalgy: frequent disease, which is rarely diagnosed
Bashkova I.B.1, Busalaeva E.I. 1,2
1 Chuvash State University named after I.N. Ulyanov, Cheboksary
2 Institute for Advanced Training of Doctors, Cheboksary
Rheumatic polymyalgia (RPM) is an inflammatory disease of the musculoskeletal system with typical manifestations, the most noticeable of which is a combination of pains in proximal muscle groups with a high acute phase inflammatory response, high efficacy of small doses of prednisolone, and which develops exclusively in people over 50 years old. The modern classification criteria are designed to facilitate the timely diagnosis, though careful collection of anamnesis and examination of the patient are of a great importance too. Differential diagnostics of RPM is given. Despite the classic debut and the further course of the disease, timely diagnosis is significantly delayed, which is due to low awareness of doctors about this pathology. A clinical case in a patient aged over 50 years is presented. The patient had a bilateral pain in the shoulder area and an increase in the acute phase blood values, the morning stiffness for more than 45 minutes, bilateral synovitis of the shoulder joints, no increase in the level of rheumatoid factor and anti-bodies to the cyclic citrullinated peptide, which allowed diagnosing RPM. A good effect of using prednisolone was an additional sign. Inadequate knowledge of physicians regarding the possible development of RPM in elderly patients, became the reason for a late verification of the diagnosis. After the appointment of glucocorticoids, the patient returned to the initial body weight within a month. The subfebrility and arthritis of peripheral joints was fully relieved, the volume of active movements in the joints was restored.
Key words: rheumatic polymyalgia, classification criteria, glucocorticoids, acute phase blood values.
For citation: Bashkova I.B., Busalaeva E.I. Rheumatic polymyalgy: frequent disease, which is rarely diagnosed // RMJ. MEDICAL REVIEW. 2017. № 1. P. 48–52.
Статья посвящена проблеме ревматической полимиалгии. Приводится дифференциальная диагностика ревматической полимиалгии. Описан клинический случай данного заболевания.

Пациентка М., 71 год, самостоятельно обратилась на прием к ревматологу с жалобами на сильные боли, охватывающие область шеи и верхнего плечевого пояса. Боли носили двусторонний, постоянный характер, усиливались при движении, в т. ч. и ночью, при каждом изменении положения тела, кратковременное облегчение состояния приносил прием простых анальгетиков или НПВП. Также беспокоила скованность, наиболее выраженная утром после пробуждения (сохранялась более 1 ч) или любого длительного периода неподвижности. Болевой синдром сопровождался ограничением активных движений в суставах, пациентка нуждалась в посторонней помощи при выполнении элементарных бытовых и гигиенических действий. Еще одной жалобой было онемение пальцев кистей и трудности при сжатии кистей в кулак. Из конституциональных проявлений обращали на себя внимание повышение температуры тела до 37,5° С (на протяжении последних 4–5 нед.) и похудание на 5 кг за 4 мес.
С 2010 г. наблюдалась у терапевта по поводу двустороннего коксартроза, проводились краткосрочные курсы приема симптоматических препаратов медленного действия (хондроитина сульфат) и нестероидных противовоспалительных препаратов (НПВП). Прогрессирующий характер поражения тазобедренных суставов и стойко сохраняющийся болевой синдром стали причиной последовательного проведения тотального эндопротезирования обоих суставов (2013, 2014 г.). В амбулаторных условиях дальнейшее лечение остеоартроза не проводилось.
Резкое ухудшение состояния – с июня 2017 г., когда впервые отметила появлений болей в суставах и мышцах верхнего плечевого пояса и области шеи. В течение нескольких недель интенсивность суставно-мышечных болей нарастала, присоединились ночные боли, затруднения при самообслуживании, стала отмечать ежедневное повышение температуры тела до субфебрильных цифр. Появление онемения пальцев обеих кистей, парастезий (усиливались по ночам) послужило поводом к обращению к неврологу. При обследовании выявлен синдром запястного канала (туннельная нейропатия срединного нерва), носивший двусторонний характер. В июле 2017 г. в условиях травматологического отделения одного из городских стационаров были выполнены пластика карпальной связки левой кисти и невролиз срединного нерва слева. Значимого улучшения самочувствия пациентки в послеоперационном периоде не последовало, было предложено выполнение аналогичного оперативного вмешательства на другой кисти, от проведения которого она отказалась. Следует обратить внимание, что в условиях стационара не было обращено должного внимания на резкое повышение острофазовых показателей крови (СОЭ по методу Вестергрена – 78 мм/ч, СРБ – 53 мг/л).
Интенсивный суставно-мышечный синдром с конституциональными проявлениями, сохранение высокого лабораторного воспалительного ответа, отсутствие эффекта от приема НПВП послужили поводом к обращению пациентки к ревматологу в сентябре 2017 г. При объективном осмотре: состояние средней степени тяжести, выражение лица страдальческое. Нуждается в посторонней помощи при раздевании. Диффузный отек кистей, кисти с трудом сжимаются в кулак. Выявлено ограничение активных движений в обоих плечевых суставах, при заведении рук за спину и за голову, болезненность при пальпации в области бугорков головок плечевых костей, лучезапястных суставов. Узелки Гебердена и Бушара в области межфаланговых суставов кистей. Послеоперационные рубцы по передненаружной поверхности обоих бедер. По внутренним органам и системам – без особенностей.
По результатам дообследования: ревматоидный фактор (РФ) – 1,0 Ед/л, антитела к циклическому цитруллинированному пептиду (АЦЦП) – менее 7 Ед/мл (при верхней границе – до 17). Тиреотропный гормон – 4,02 мМЕ/л (при верхней границе – до 3,4) в отсутствие изменения сывороточного уровня тиреоидных гормонов. В протеинограмме отмечалось повышение содержания альфа-2-глобулинов в отсутствие изменения уровня общего белка. Уровни КФК, ЛДГ, трансаминаз, щелочной фосфатазы, кальция оставались в пределах референсных значений. Антинуклеарные антитела не обнаружены.
При проведении УЗИ плечевых суставов выявлены двусторонний синовит плечевых суставов, бурсит сумки подлопаточной мышцы, более выраженный справа.
Таким образом, у пациентки в возрасте старше 50 лет с двусторонними болями в области плечевого пояса и повышением острофазовых показателей крови (обязательные критерии) определялись дополнительные критерии: утренняя скованность более 45 мин (2 балла), отсутствие повышения в сыворотке крови РФ и АЦЦП (2 балла), двусторонний синовит плечевых суставов по результатам УЗИ (1 балл), что позволило расценить это состояние как РПМ.
Дополнительным признаком стал также хороший эффект от приема преднизолона в дозе 15 мг/сут, отмеченный через 3 сут от начала приема ГК.
Недостаточная осведомленность врачей в отношении возможного развития у пожилых пациентов РПМ послужила поводом для поздней верификации диагноза (спустя 4 мес. от дебюта заболевания) и необоснованного проведения хирургического вмешательства. Необходимо также отметить, что диффузный умеренно выраженный отек правой кисти со сгибательной контрактурой пальцев, вероятно, за счет ладонного фасциита и парастезии пальцев полностью купировались на фоне лечения ГК. Спустя 1 мес. от начала терапии ГК наблюдалось снижение уровней СОЭ до 35 мм/ч (по методу Вестергрена) и СРБ до 12 мг/л. Пациентка в течение 1 мес. вернулась к исходной массе тела. Полностью купированы субфебрилитет и артрит периферических суставов, восстановился объем активных движений в суставах, в посторонней помощи не нуждается.
В таблице 2 представлены основные заболевания, которые включаются в круг дифференциально-диагностического поиска при установлении диагноза РПМ, и их отличительные особенности, позволяющие исключить данные состояния. 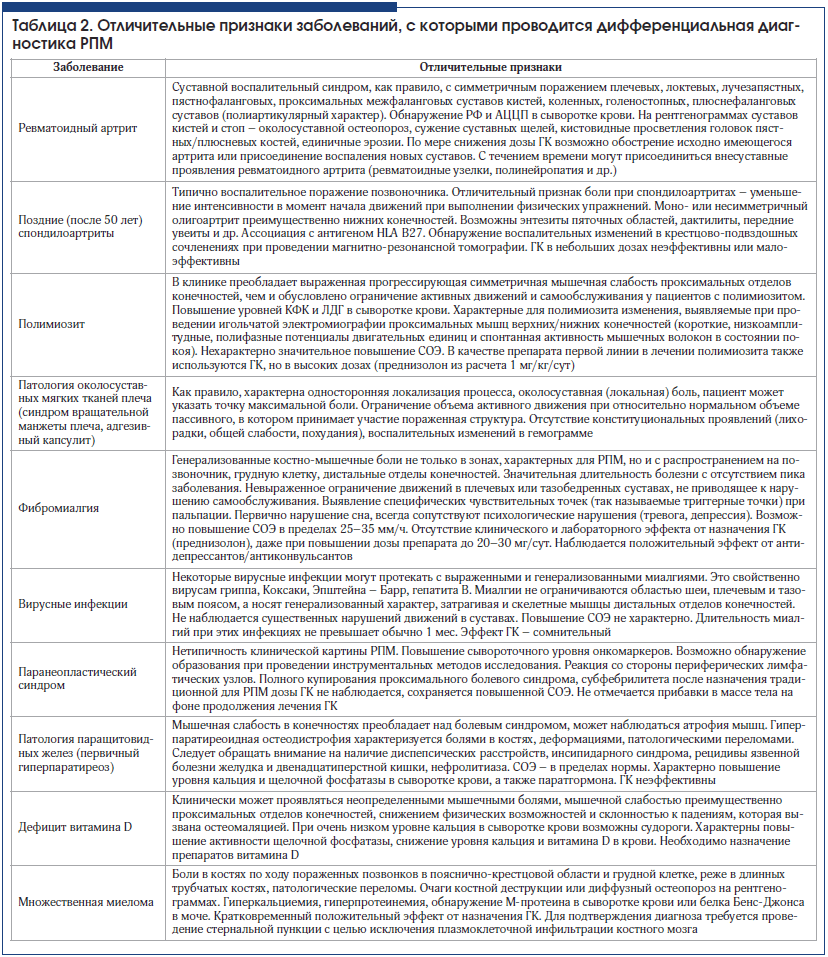
Только для зарегистрированных пользователей
Читайте также:


