Санитарные правила по цитомегаловирусной инфекции
ГЛАВНЫЙ ГОСУДАРСТВЕННЫЙ САНИТАРНЫЙ ВРАЧ РОССИЙСКОЙ ФЕДЕРАЦИИ
от 27 июля 2011 года N 106
Об утверждении СП 3.1.2950-11 "Профилактика энтеровирусной (неполио) инфекции
В соответствии с Федеральным законом от 30.03.99 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения" (Собрание законодательства Российской Федерации, 1999, N 14, ст.1650; 2002, N 1 (ч.1), ст.2; 2003, N 2, ст.167; 2003, N 27 (ч.1), ст.2700; 2004, N 35, ст.3607; 2005, N 19, ст.1752; 2006, N 1, ст.10; 2006, N 52 (ч.1) ст.5498; 2007, N 1 (ч.1) ст.21; 2007, N 1 (ч.1) ст.29; 2007, N 27, ст.3213; 2007, N 46, ст.5554; 2007, N 49, ст.6070; 2008, N 24, ст.2801; 2008, N 29 (ч.1), ст.3418; 2008, N 30 (ч.2), ст.3616; 2008, N 44, ст.4984; 2008, N 52 (ч.1), ст.6223; 2009, N 1, ст.17) и постановлением Правительства Российской Федерации от 24.07.2000 N 554 "Об утверждении Положения о государственной санитарно-эпидемиологической службе Российской Федерации и Положения о государственном санитарно-эпидемиологическом нормировании" (Собрание законодательства Российской Федерации, 2000, N 31, ст.3295; 2004, N 8, ст.663; 2004, N 47, ст.4666; 2005, N 39, ст.3953)
постановляю:
1. Утвердить санитарно-эпидемиологические правила СП 3.1.2950-11 "Профилактика энтеровирусной (неполио) инфекции" (приложение).
Приложение. Санитарно-эпидемиологические правила СП 3.1.2950-11. Профилактика энтеровирусной (неполио) инфекции
УТВЕРЖДЕНЫ
постановлением Главного
государственного санитарного врача
Российской Федерации
от 27 июля 2011 года N 106
Санитарно-эпидемиологические правила
СП 3.1.2950-11
1.1. Настоящие санитарно-эпидемиологические правила (далее - санитарные правила) разработаны в соответствии с законодательством Российской Федерации.
1.2. Настоящие санитарные правила устанавливают основные требования к комплексу организационных, санитарно-противоэпидемических (профилактических) мероприятий, направленных на предупреждение и распространение энтеровирусной инфекции (ЭВИ) среди населения на территории Российской Федерации.
1.3. Соблюдение санитарных правил является обязательным для граждан, юридических лиц и индивидуальных предпринимателей.
1.4. Контроль за выполнением настоящих санитарных правил проводится органами, осуществляющими функции по контролю и надзору в сфере обеспечения санитарно-эпидемиологического благополучия населения, в соответствии с законодательством Российской Федерации.
2.1. Энтеровирусные (неполио) инфекции (ЭВИ) представляют собой группу острых инфекционных заболеваний вирусной этиологии, вызываемых различными представителями энтеровирусов.
2.2. Основными возбудителями ЭВИ являются вирусы Коксаки А (24 серотипа), Коксаки В (6 серотипов), ECHO (34 серотипа) и неклассифицированные энтеровирусы человека 68-71 типов.
Энтеровирусы отличаются высокой устойчивостью во внешней среде, способны сохранять жизнеспособность в воде поверхностных водоемов и влажной почве до 2 месяцев.
2.3. Источником инфекций является человек (больной или носитель). Инкубационный период составляет в среднем от 1 до 10 дней. Среди заболевших ЭВИ преобладают дети.
ЭВИ свойственна высокая контагиозность для неиммунных лиц.
Передача ЭВИ осуществляется при реализации фекально-орального механизма (водным, пищевым и контактно-бытовым путями) и аэрозольного механизма (воздушно-капельным и пылевым путями).
2.4. ЭВИ распространена повсеместно. Заболевание встречается в виде спорадических случаев, локальных вспышек (чаще в детских коллективах), эпидемий.
Причиной формирования локальных очагов с групповой заболеваемостью может являться занос инфекции в учреждение, на территорию и возможность ее распространения в условиях несоблюдения требований санитарного законодательства как по условиям размещения, так и по состоянию систем водопользования и организации питания.
Эпидемиологическую значимость представляет вода открытых водоемов, загрязненная сточными водами, как в качестве источников питьевого водоснабжения, так и используемая в качестве рекреационных зон для купания населения.
2.5. Отмечается преимущественно летне-осенняя сезонность заболеваемости ЭВИ. Локальные вспышки ЭВИ могут регистрироваться в течение всего года, часто вне зависимости от сезонного эпидемического подъема заболеваемости.
2.6. ЭВИ характеризуются полиморфизмом клинических проявлений и множественными поражениями органов и систем: серозный менингит, геморрагический конъюнктивит, увеит, синдром острого вялого паралича (ОВП), заболевания с респираторным синдромом и другие.
Один и тот же серотип энтеровируса способен вызывать развитие нескольких клинических синдромов и, наоборот, различные серотипы энтеровирусов могут вызвать сходные клинические проявления болезни. Наибольшую опасность представляют тяжелые клинические формы с поражением нервной системы.
Выраженный полиморфизм клинических проявлений и отсутствие патогномоничных основных симптомов значительно осложняет клиническую диагностику ЭВИ, особенно его спорадических случаев, поэтому при установлении диагноза заболевания необходим тщательный сбор эпидемиологического анамнеза и проведение лабораторных исследований.
2.7. Обследованию на ЭВИ подлежат лица при наличии у них одного или нескольких из следующих клинических симптомов/синдромов:
- очаговая неврологическая симптоматика;
- менингеальные симптомы;
- сепсис новорожденных небактериальной природы;
- ящуроподобный синдром (HFMD-экзантема полости рта и конечностей);
- герпангина, афтозный стоматит;
- миокардит;
- геморрагический конъюнктивит;
- увеит;
- миалгия;
- другие (в том числе респираторный синдром, гастроэнтерит, экзантема при возникновении групповой заболеваемости в детском организованном коллективе).
2.8. Диагноз заболевания ЭВИ устанавливается на основании клинических признаков болезни, результатов лабораторного исследования, эпидемиологического анамнеза.
2.9. По степени достоверности диагноза случаи заболевания ЭВИ классифицируются как подозрительные, вероятные или подтвержденные:
подозрительным считается случай ЭВИ при наличии одного или нескольких из перечисленных в п.2.7 симптомов (синдромов) и, возможно, лихорадки;
вероятным считается случай ЭВИ при наличии характерных клинических проявлений и связи заболевания с зарегистрированным эпидемическим очагом;
В статье проанализированы опубликованные данные по вопросам адекватной диагностики антенатальной и постнатальной цитомегаловирусной инфекции (ЦМВИ), а также лечению острых ЦМВИ у беременной, плода и новорожденного. Представлены отечественные клинические р
The article gives analysis of the data on the issues of relevance of diagnostics of antenatal and postnatal cytomegaloviral infection (CMVI), as well as treatment of acute CMVI in the pregnant, fetus and newborns. National clinical guidelines on diagnostics and treatment of congenital CMVI developed by the Russian Association of antenatal medicine in 2016, were presented; as well as the first unofficial international guidelines on the issues of diagnostics and treatment of congenital CMVI.
Цитомегаловирус (ЦМВ) — чрезвычайно распространенный вирус, поражающий людей всех возрастов и формирующий пожизненную персистенцию в организме инфицированного человека. Считается, что в большинстве случаев персистенция начинается в ранние годы жизни и протекает латентно, не оказывая выраженного патологического влияния на состояние здоровья инфицированного. С другой стороны, доказано, что персистенция вируса может сопровождаться хроническим воспалением, формировать разнообразные многочисленные иммунные дисфункции и определять развитие вторичных иммунных, аутоиммунных и дегенеративных нарушений. Различного рода иммунокомпрометации могут приводить к рецидивам размножения вируса и многообразным клиническим проявлениям с поражением любых органов и систем в любом возрасте.
Особое значение имеют врожденные инфекции детей, которые отличаются высоким риском развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией (ЦМВИ), что определяет потребность в своевременном пренатальном выявлении беременных и плодов с высоким риском развития врожденной ЦМВИ и ранней диагностике и лечении инфекций у новорожденных.
Теоретические дискуссии по вопросам адекватной диагностики антенатальной и постнатальной ЦМВИ, а также лечению острых ЦМВИ у беременной, плода и новорожденного продолжаются с 1990-х гг., но отсутствие единых руководящих принципов затрудняет практическую работу врачей. Российской ассоциацией специалистов перинатальной медицины в 2016 г. выработаны отечественные клинические рекомендации по диагностике и лечению врожденной ЦМВИ. Созданная в рамках 5-й Международной конференции по ЦМВИ (Брисбен, Австралия, 19 апреля 2015) международная группа экспертов на основе консенсусных дискуссий и обзора литературы выработала первые неофициальные международные рекомендации по вопросам диагностики и лечения врожденной ЦМВИ, которые опубликованы в Lancet Infect Dis в марте 2017. Все эти рекомендации будут нуждаться в постоянном обновлении по мере поступления дополнительных данных.
ЦМВ — двухцепочечный ДНК-вирус, член семейства герпес-вирусов (β-герпесвирус человека). Синтез вирусного генома ДНК происходит в ядре клетки-хозяина. Исследования последних лет подтверждают гипотезу о том, что штаммы ЦМВ могут варьировать в их вирулентности, тропизме и патогенном потенциале, который, в свою очередь, вероятно, связан с генетической изменчивостью ключевых для патогенеза генов. Внешняя оболочка вируса содержит множественные гликопротеины, кодируемые вирусом. Гликопротеин B и гликопротеин H, по-видимому, являются основными факторами для формирования гуморального иммунитета — антитела к ним способны нейтрализовать вирус. Эти гликопротеины используют сегодня при разработке анти-ЦМВ-вакцин [3].
Вирус распространяется различными способами: через продукты крови (переливание, трансплантация органов), грудное вскармливание, пролиферацию в местах контактов (кожа, любые слизистые оболочки), перинатально и половым путем. ЦМВИ может протекать в виде первичной инфекции ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни [4].
При острой ЦМВ-инфекции могут поражаться практически все типы клеток человеческого организма — эндотелиальные клетки, эпителиальные клетки, клетки гладкой мускулатуры, фибробласты, нейронные клетки, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и пр. Все типы клеток поражаются и в мозге: нейроны, астроциты, клетки эпендимы, выстилающие желудочки, макроглия, эндотелий капилляров, оболочек, микроглия, сплетения сосудистой оболочки, дендриты и аксоны — т. е. вирус в мозге не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения нервной системы у больных [5].
Считается, что ЦМВ реплицируется в эндотелиальных клетках с низкой скоростью, вызывая преимущественно подострые инфекции, однако истинная скорость репликации вируса в клетках определяется эффективностью цитотоксического Т-клеточного иммунитета и степенью иммуносупрессии хозяина. Так, например, на моделях ЦМВИ у животных продемонстрировано, что отсутствие CD4 Т-клеток сопровождалось более тяжелым и стремительным заболеванием ЦМВИ. Известно также, что ВИЧ-инфицированные новорожденные имеют очень высокую частоту врожденной ЦМВИ с высоким риском смерти, неврологических дефектов и прогрессии ВИЧ-инфекции [6–7].
Особое свойство ЦМВИ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [7].
Доказано, что и первичные и латентные ЦМВИ сами могут индуцировать хронические воспалительные системные реакции с устойчивой иммунной активацией, запускать и поддерживать аутоиммунные процессы, усиливать аллореактивность Т-клеток после трансплантации и, возможно, участвовать в комплексе причин повышения частоты нейродегенеративных состояний с возрастом человека (Jones R. P. The debility cascade in neurological degenerative disease). Установлено также, что ЦМВ-индуцированные иммунные изменения в пожилом возрасте могут отвечать, например, за замедленную элиминацию вируса гриппа из легких, сниженный поствакцинальный иммунитет на гриппозные вакцины, измененную реакцию организма на терапию интерферонами [8].
Многие годы риск развития врожденных инфекций плода ассоциировали преимущественно с первичной инфекцией матери, однако к настоящему моменту не вызывает сомнения, что большая доля врожденных ЦМВИ (до 75%) встречается в условиях рецидивирующей во время беременности материнской инфекции. Допускаются также и экзогенные реинфекции с новыми штаммами ЦМВ — доказательства основываются на молекулярных данных, подтверждающих получение нового штамма вируса.
Вместе с тем степень риска вертикального инфицирования плода в условиях первичной инфекции матери рассматривают по-прежнему как чрезвычайно высокую — в 30–50% случаев острой первичной инфекции беременной развивается врожденная инфекция ребенка. Показано, что ранее существовавший материнский иммунитет хоть и не гарантирует полной защиты, тем не менее обеспечивает снижение риска врожденной ЦМВИ при следующих беременностях на 69% [9].
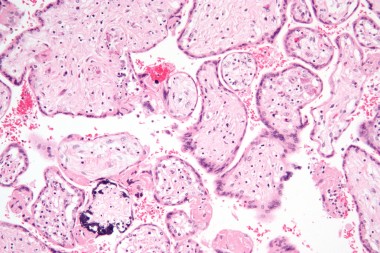
Недавними исследованиями установлено, что ЦМВ может поражать амниотическую мембрану, ухудшая цитотрофобласт-индуцированный лимфангиогенез и ремоделирование сосудов в плаценте и задерживая правильное развитие клеток — предшественников трофобласта, одновременно вызывает врожденную провоспалительную иммунную реакцию. Это приводит к гипоксии плода, задержке внутриутробного развития и возможным последующим гипоксическим повреждениям головного мозга. Степень поражения плода определяется сроками антенатального инфицирования и вирусной нагрузкой в размножающихся клетках — чем меньше гестационный возраст, тем более выражена альтерация (разрушение) тканей с формированием пороков развития [10]. Особенно быстро ЦМВ достигает максимума в астроцитарных и глиальных клетках, при этом максимальная экспрессия вируса найдена в глиальных клетках развивающегося мозга мышат (что объясняет микрогирию, микроцефалию и другие пороки ЦМВ-инфицированного мозга детей). По мере увеличения срока гестации в клинической картине инфекционного заболевания плода преобладают симптомы системного воспаления с выраженной пролиферацией и экссудацией. У 1/3 умерших от ЦМВИ новорожденных (из них 60% — недоношенные) при морфологическом исследовании выявляют различные пороки развития. У 43% — признаки генерализованной внутриутробной инфекции с геморрагическими и ишемическими инфарктами (в том числе в головном и спинном мозге) [11].
Способность вируса реплицироваться в любых клетках человеческого организма определяет многообразие клинических форм болезни; ЦМВ может вызывать как генерализованные инфекции, так и поражения отдельных органов: печени, головного мозга, сердца, легких, мочеполовых органов, желудочно-кишечного тракта и др.
У беременных острая первичная ЦМВИ протекает чаще бессимптомно (25–50%) или малосимптомно — с неспецифическими проявлениями (обычно лихорадка, астения и головная боль).
Как первичная, так и рецидивирующая ЦМВИ матери может стать причиной антенатальных ультразвуковых признаков поражения плода в результате трансплацентарной инфекции. Самые частые УЗИ-признаки: задержка роста плода, вентрикуломегалия, микроцефалия, перивентрикулярная гиперэхогенность, кальцификаты в мозге, плевральный выпот или асцит, гепатоспленомегалия, гиперэхогенный кишечник и мекониальный илеус и др. Эти УЗИ-аномалии эмбриона прогнозируют тяжелую генерализованную манифестную врожденную ЦМВИ новорожденного с высоким риском формирования инвалидизирующих исходов болезни и смерти. Поэтому первичная острая ЦМВИ во время беременности может являться показанием к ее искусственному прерыванию. Установлено, что около 4% детей с антенатальной ЦМВИ умрут в утробе матери или вскоре после рождения, среди остальных около 60% будут иметь когнитивные дефекты, нейросенсорную потерю слуха и другие неврологические и прочие проблемы [11–12].
Сегодня установлено также, что нейросенсорная тугоухость является прогрессирующим заболеванием и может формироваться в течение 5–6 лет жизни даже у детей, родившихся с бессимптомной ЦМВИ (это связывают с многолетней репликацией ЦМВ в перилимфе), что требует соответствующей длительности наблюдения ребенка.
При инфицировании в поздние сроки гестации ЦМВИ у новорожденного может проявляться и как генерализованная инфекция, и как поражение отдельных органов с нетяжелыми транзиторными симптомами болезни, например, умеренной гепатомегалией, изолированным снижением количества тромбоцитов или повышенным уровнем аланинаминотрансферазы. Возможна и клинически бессимптомная ЦМВИ с изолированной нейросенсорной тугоухостью.
У 10% всех новорожденных в течение первого месяца жизни возникают инфекционные заболевания в результате в основном семейных контактов, в том числе грудного вскармливания. Экскреция ЦМВ с грудным молоком в течение первых недель после родов бывает низкой, достигает максимума к 4–8 неделям, завершается к 9–12 неделям. Считается, что риск трансмиссии вируса коррелирует с вирусной нагрузкой в молоке, передача максимальна при высокой экскреции. У доношенных детей в результате инфицирования ЦМВ через молоко матери формируется, как правило, субклиническое течение инфекции без остаточных явлений; в клинической картине более вероятно развитие энтероколита и транзиторного холестатического гепатита с минимальным цитолизом. Недоношенные дети (вес
И. Я. Извекова 1 , доктор медицинских наук, профессор
М. А. Михайленко
Е. И. Краснова, доктор медицинских наук, профессор
ФГБОУ ВО НГМУ МЗ РФ, Новосибирск
Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ И. Я. Извекова, М. А. Михайленко, Е. И. Краснова
Для цитирования: Лечащий врач № 4/2018; Номера страниц в выпуске: 90-95
Теги: новорожденные, беременность, инфекция, персистирование
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК - 2015
Общая информация
Цитомегаловирусная инфекция (синонимы: цитомегалия, вирусная болезнь слюнных желез, инклюзионная цитомегалия, болезнь с включениями; salivarygland virus disease – англ.) хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса от латентной инфекции до клинически выраженного генерализованного заболевания [1,2].
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |


Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
У ВИЧ-инфицированных в 3 и 4 стадии: клиника манифестных форм с поражением легких, ЦНС, глаз (ретинит), ЖКТ, печени.
Иммунограмма: снижение CD4+, CD8+, снижение CD4\CD8.
Дифференциальный диагноз
Алгоритм дифференциальной диагностики при цитомегаловирусной болезни


Лечение
Диета: стол № 15 с коррекцией в зависимости от клинической формы.
• меглюмина акридонацетат в таблетках: по 0,45 г (3 табл.) на прием 1 раз в сутки per os по схеме 1,2,4,6,8,11,14,17,21,23 дни., в инъекциях 12,5% - 2 мл в/м, 1 раз №10.
Латентная ЦМВИ: лечение не проводится.
• Панавир 0,004% раствор 5 мл в/в медленно №5 по схеме три инъекции с интервалом 48 часов, две последующие – с интервалом 72 часа и суппозитории ректальные Панавир 200 мкг, по 1 свече на ночь 3-х кратно в течении 1-ой недели с интервалом 48 часов и 2-х кратно в течении 2-ой недели с интервалом 72 часа. Курс лечения 11 дней.
• Валганцикловир 900 мг в сутки или Ганцикловир 5 мг/кг/сутки в течение месяца, перенёсшим ЦМВ – ретинит на фоне ВААРТ до повышения CD4 – лимфоцитов более 100 кл/мкл, сохраняющегося не менее 3 месяцев. Поддерживающий курс у этих больных при других манифестных формах ЦМВИ должен быть не менее одного месяца.
С десенсибилизирующей, противотёчной, противовоспалительной целью при генерализованной ЦМВИ с поражением ЦНС: кортикостероидные препараты: преднизолон 2-5 мг\кг в сутки;
• Рингер раствор для инфузий, 200 мл и 400мл;

Цитомегаловирусная инфекция – широко распространенная вирусная инфекция, характеризующаяся многообразием проявлений от бессимптомного течения вплоть до тяжелейших генерализованных форм с поражением внутренних органов и центральной нервной системы. Во время трансплацентарной передачи инфекции возможно поражение плода.
Уровень инфицирования цитомегаловирусной инфекцией и степень зараженности организма зависит от социально-экономических условий, этнической принадлежности, практики медицинского обслуживания новорожденных и детей младшего возраста, времени вступления в половые отношения.
Доля носителей ЦМВ в России составляет около 90%.
Попадая в клетки человеческого организма, цитомегаловирус способен оставаться в нем пожизненно.
Возбудитель (Cytomegalovirus hominis) относится к вирусам герпеса (семейство Herpesviridae)
Резервуаром и источником инфекции является только человек. Вирус может находиться в слюне, молоке, моче, испражнениях, семенной жидкости, в секрете шейки матки.
У 20-30% здоровых беременных женщин ЦМВ присутствует в слюне, 3-10 % - в моче, 5-20% - в цервикальном канале или вагинальном секрете.
Кровь около 1% доноров содержит цитомегаловирус.
Хотя, вирусные частицы могут быть обнаружены по всему телу, цитомегаловирус, чаще всего, ассоциирован со слюнными железами.
Cпособы передачи инфекции
Цитомегаловирусная инфекция распространяется не только через слюну при близких контактах, но и во время полового контакта, через кровь, от беременной матери плоду, а также контактно-бытовым путем.
Наибольшую опасность для плода представляет первичная инфекция на ранних сроках беременности. Возбудитель, проникший в плод через кровь в ранние сроки беременности, вызывает формирование врожденных пороков развития.
При наличии инфекции в канале шейки матки у беременной, заражение плода может происходить в родах, во время прохождения плода по родовым путям.
Основной путь заражения ребенка до года – передача вируса через грудное молоко.
Источником заражения детей до 5-6 лет являются матери, выделяющие вирус со слюной или мочой.
Дети, находящиеся в организованных коллективах заражаются чаще контактно-бытовым путем.
Заражение в возрасте 16-30 лет происходит, как правило, при близком контакте через поцелуи и половым путем.
Переливание крови и другие манипуляции с кровью также могут приводить к заражению цитомегаловирусом.
Симптомы цитомегаловирусной инфекции
В здоровом организме вирус никак себя не проявляет, но может быть смертельно опасен для людей с иммунодефицитами: для ВИЧ-инфицированных, больных, после трансплантации органов, а также ожидающих трансплантацию, новорождённых.
При врожденной цитомегаловирусной инфекции характер поражения плода зависит от срока его заражения. Особенно опасно острое инфицирование матери в первые 20 недель беременности.
К чему может привести заражение в ранние сроки беременности?
Внутриутробная гибель плода;
Грубые врожденные пороки (анэнцефалия, микроцефалия, гидроцефалия, нарушение строения легких, бронхиального дерева, аномалии строения почек и др.).
Врожденные пороки в большинстве случаев несовместимы с жизнью.
При заражении ЦМВ в более поздние сроки беременности формирования пороков развития не происходит.
К чему приводит заражение ребенка цитомегаловирусом во время родов?
Клинические признаки, как правило, появляются через 1-2 месяца после родов.
Поражение легких (пневмония);
Увеличение печени, селезенки;
Поражение желудочно-кишечного тракта;
Заболевание может носить длительный рецидивирующий характер.
Максимальная летальность от цитомегаловирусной инфекции приходится на 2-4 месяц.
Профилактика цитомегаловирусной инфекции
Во время консультирования беременных женщин, или планирующих беременность необходимо информировать о главных источниках и путях инфицирования (половые контакты с инфицированными ЦМВ партнерами, физический контакт при ежедневном уходе за ребенком дома или профессиональный контакт с детьми младшего возраста в стационарах, домах ребенка, дошкольных учреждениях).
Для снижения риска первичного заражения ЦМВ беременным женщинам, использовать барьерные контрацептивы при половых контактах, соблюдать правила личной гигиены (мыть руки после прикосновения к дверным ручкам, прикосновения к игрушкам, испачканными слюной , мочой ребенка), не рекомендуется доедать или допивать за детьми, использовать совместную посуду, нельзя облизывать соску. Необходимо избегать поцелуев в губы детей грудного возраста, которые могут выделять вирус со слюной.
При планировании переливания крови недоношенному ребенку или взрослому человеку с ослабленной иммунной системой, необходимо осуществлять проверку крови и ее компонентов на наличие ДНК ЦМВ.
СМОТРЕТЬ ДРУГИЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
Год утверждения 2016
Профессиональные ассоциации
Оглавление
1. Краткая информация
Цитомегаловирусная болезнь (ЦМВБ) – хроническая антропонозная инфекция с многообразием клинических форм.
Возбудитель ЦМВБ – Cytomegalovirus hominis из семейства Herpesviridae.
Особенности цитомегаловируса (ЦМВ):
- крупный геном;
- репликация без повреждения клетки;
- малая цитопатогенность в культуре ткани;
- медленная репликация;
- сравнительно низкая вирулентность;
- существенное подавление клеточного иммунитета.
При постнатальной ЦМВБ входные ворота - слизистые оболочки.
Патогенетические особенности ЦМВ-инфекции:
- вирус поражает эпителий легких, печени, кишки, почек, мочевого пузыря, молочных и слюнных желез, генитального тракта;
- может инфицировать нервные, гладко мускульные и клетки стромы костного мозга;
- в микрососудах вызывает продуктивное поражение, приводящее к их стенозу и облитерации;
- хронический резервуар вируса - моноциты, лимфоциты, эндотелиальные и эпителиальные клетки;
- периоды локальной активизации с выделением вируса из носоглотки или урогенитального тракта;
- манифестация и тяжесть течения зависит от глубины иммуносупрессии, преимущественно от количества СD4-лимфоцитов.
При аутопсии выявляют:
- фиброзирующий альвеолит, фиброз легких;
- эрозивно-язвенное с выраженным фиброзом подслизистого слоя поражение пищевода и толстой кишки, реже желудка и тонкой кишки;
- массивное, часто двустороннее некротическое поражение надпочечников;
- энцефаловентрикулит с преимущественным поражением стенок желудочков и близлежащих структур, некроз спинного мозга, сетчатки глаза.
У большинства больных патологический процесс генерализован.
Клинически выраженная ЦМВБ:
- одно из серьезных осложнений при трансплантации;
- частое оппортунистическое заболевание при ВИЧ;
- у 10 – 40% больных СПИД, не получающих АРВТ;
- в 3 – 7% в популяции больных ВИЧ-инфекцией на АРВТ;
- причина посттрансфузионных гепатитов, гинекологической патологии, синдрома и болезни Бадда-Киари;
- ко-фактор развития системных васкулитов, хронических диссеминированных заболеваний легких, криоглобулинемии, ЗНО, атеросклероза, кардиомиопатии, ДЦП, эпилепсии, синдрома Гийена-Барре, синдрома хронической усталости, аутизма;
- возможна у взрослых без выраженных иммунологических нарушений.
Источник инфекции – человек.
Специфические антитела указывают на присутствие вируса в организме.
Доля серопозитивных взрослых 73 – 98%.
У здоровых беременных ЦМВ находят:
- в слюне 20 – 30%;
- в моче 3 – 10%;
- в цервикальном канале или вагинальном секрете 5 – 20%.
- в грудном молоке 20 – 60% серопозитивных матерей;
- в сперме 35% пациентов сохраняется 22 месяца;
- в 1% донорской крови.
- половой - критический возраст заражения 16 – 30 лет;
- парентеральный – частота передачи при переливании крови и компонентов 0.14 – 10.0 на 100 доз, с каждой гемотрансфузией риск возрастает на 5 – 12%;
- вертикальный – 0.2 – 2.5% всех родившихся младенцев;
- контактно-бытовой с аспирацией возбудителя через слюну.
Частота сероконверсии (в год):
- 24% у матерей, имеющих старшего ребенка до 3-х лет или до 6 лет, посещающего детский сад;
- 50% у родителей выделяющего ЦМВ ребенка до 2-х лет;
- 2% у доноров;
- 8% у сотрудников детских отделений больниц, домов ребенка, дошкольных учреждений, родителей дошкольников;
- 2% у молодых людей.
Цитомегаловирусная болезнь (B25):
В25.0+ Цитомегаловирусный пневмонит (J7.1*)
В25.1+ Цитомегаловирусный гепатит (К77.0*)
В25.2+ Цитомегаловирусный панкреатит (К87.1*)
В25.8 Другие цитомегаловирусные болезни
В25.9 Цитомегаловирусная болезнь неуточненная
- Врожденная и приобретенная;
- Антенатальная, интранатальная и постнатальная;
- Латентная, персистирующая, активная (низкой, средней, высокой степени);
- Первичного или повторного заражения (острая инфекция, реактивация вируса и реинфекция).
2. Диагностика
Скрининговое обследование на ЦМВ:
- Планирующие беременность;
- Беременные;
- Реципиенты крови, органов и тканей;
- После полового контакта с серопозитивным партнером;
- Женщины с отягощенным акушерским анамнезом;
- Пациенты с гепатитом, панкреатитом, менингоэнцефалитом, пневмонией, поражением глаз, ЖКТ;
- Пациенты с иммунодефицитом;
- Доноры крови, органов и тканей, спермы.
- окружение пациента организованными дошкольниками;
- близкий бытовой контакт с больным инфекционным мононуклеозом или вирусовыделителем; лихорадящим пациентом; болеющим ОРЗ/фарингитом;
- половые контакты без барьерных контрацептивов с серопозитивным партнером;
- гемотрансфузии в последние 6 месяцев;
- длительная волнообразная лихорадка неправильного типа выше 38,5ºС, выраженная слабость, быстрая утомляемость, сонливость, потеря аппетита, существенное снижение веса, реже – потливость по ночам, артралгии, миалгии.
2.2 Физикальное обследование
- осмотр кожных покровов и видимых слизистых ЛОР и половых органов, глаз;
- осмотр и пальпация лимфоузлов;
- пальпация живота с определением размеров и консистенции печени и селезенки;
- аускультация легких;
- очаговая неврологическая симптоматика и менингеальный синдром
Первичная диагностика:
- Клинический анализ крови с лейкоцитарной формулой;
- Общий анализ мочи;
- БАК: общий билирубин и его фракции, АлАТ, АсАТ, ЩФ, ГГТП, амилаза, холестерин, мочевина, креатинин;
- Протеинограмма;
- Протромбиновый индекс (ПТИ)
Серологические маркеры ЦМВ:
- антитела классов IgG и IgM в сыворотке крови;
- индекс авидности антител IgG по ИФА/ иммуноблоту (ИБ)/ твердофазному хемилюминисцентному ИФА.
Острую ЦМВ-инфекцию подтверждают IgM антитела + сероконверсия IgG и/или низкоавидные IgG антитела.
При первичном заражении:
- анти-ЦМВ IgM вырабатываются на 5 – 7 день;
- анти-IgM исчезают через 1 – 2 месяца;
- низкоавидные анти-IgG появляются через 10 – 14 дней, затем авидность увеличивается до высокой;
- низкоавидные анти-IgG исчезают через 1 – 3 месяца;
- высокоавидные антитела IgG циркулируют в крови пожизненно.
При острой ЦМВБ специфичность выявления анти-ЦМВ IgM антител методом ИФА - 30%, чувствительность - 88%, что при отсутствии антител требует повторного анализа через 2 недели для установления факта появления IgG (сероконверсии), а при наличии анти-ЦМВ IgG антител определяют их авидность.
При латентной инфекции в крови присутствуют только высокоавидные IgG антитела.
При активной ЦМВ-инфекции можно обнаружить IgM антитела и высокоавидные IgG антитела.
Титр IgG антител не отражает степени репликативной активности ЦМВ и не позволяет выставить активную ЦМВ-инфекцию для назначения противовирусной терапии.
Метод выбора - твердофазный хемилюминисцентный ИФА, чувствительнее и специфичнее стандартного ИФА.
Золотой стандарт выявления антител класса IgМ – ИБ с чувствительностью и специфичностью 100%.
Маркер активной репликации вируса - антитела к антигену рр65 (ранний белок), рр72 (предранний белок), позже появляются антитела к белку рp28.
Молекулярно-биологическое исследование
Выявление ДНК ЦМВ в биологических жидкостях, определение количества ДНК ЦМВ в крови, ликворе методом ПЦР.
Клиническое и прогностическое значение ДНК в биологических жидкостях:
Определение антигенов ЦМВ в биологическом материале при РИФ, иммуноцитохимическим методом, mRNA NASBA.
Для обнаружения предраннего и раннего белков вируса рр72 и рр65 в слюне и моче используют РИФ, исследование длится 24 – 36 часов.
Антиген pp65 в лейкоцитах при иммуноцитохимии позволяет установить активную ЦМВ-инфекцию, вирусный белок pp65 опережает клинику, титр коррелирует с развитием клинических симптомов.
Определения антигена pp67 методом mRNA NASBA специфичнее pp65-антигенемии и позволяет использовать замороженные или лизированные образцы крови.
Методы выявления антигенов уступают чувствительности ПЦР.
Диагностика на этапах противовирусной терапии (ПВТ) и диспансерного наблюдения
Контрольный клинический анализ крови с лейкоцитарной формулой;
Общий анализ мочи;
БАК: общий билирубин и его фракции, АлАТ, АсАТ, ЩФ, ГГТП, амилаза, холестерин, мочевина, креатинин;
Контрольное молекулярно-биологическое исследование: ДНК ЦМВ в крови и моче, определение количества ДНК ЦМВ в крови, ликворе при положительной качественной ПЦР.
На этапе первичной диагностики:
УЗИ органов брюшной полости и забрюшинного пространства.
Фибробронхоскопия при признаках поражения дыхательной системы с цитологией бронхоальвеолярной жидкости и её исследования на ДНК ЦМВ и ДНК иных возбудителей.
Рентгенографии органов грудной клетки при признаках поражения дыхательной системы.
ЭКГ при признаках поражения сердечно-сосудистой системы.
ФГДС при признаках поражения ЖКТ (амбулаторно с местной аппликационной анестезией или седацией после консультации и сопровождения анестезиолога).
КТ или МРТ головного мозга при наличии общемозговой или очаговой неврологической симптоматики, интоксикации и лихорадкой в продромальном периоде.
На этапе постановки диагноза:
Выявление ЦМК в биопсийных и аутопсийных препаратах гистологическим методом, чувствительность 50%, для повышения чувствительности и специфичности в препаратах определяют вирусный антиген или ДНК ЦМВ.
При наличии показаний - консультации смежных специалистов:
- офтальмолога,
- невропатолога,
- гастроэнтеролога,
- пульмонолога,
- кардиолога.
При показаниях - люмбальная пункция с определением в ликворе уровня общего белка и фракций, микроскопия, определение цитоза, ДНК ЦМВ и ДНК иных возбудителей.
Плевральная пункция при экссудативном плеврите с исследованием жидкости на ДНК ЦМВ и ДНК иных возбудителей.
При мононуклеозоподобном варианте необходимо исключить:
- другие герпес-вирусные инфекции;
- острую ВИЧ-инфекцию;
- стрептококковый тонзиллит;
- дебют онкогематологического заболевания.
При патологии органов дыхания дифференциальный диагноз:
- бактериальный бронхит;
- респираторно-синцитиальная вирусная инфекция;
- коклюш;
- трахеобронхит, вызванный вирусом простого герпеса 1 типа;
- микоплазменная пневмония;
- хламидийная пневмония.
При иммуносупрессии исключить:
- пневмоцистную пневмонию;
- туберкулез;
- грибковые инфекции;
- герпетическую инфекцию;
- бактериальный сепсис.
При выраженных нейрокогнитивных расстройств дифференцировать:
- ВИЧ-энцефалит;
- многоочаговая лейкоэнцефалопатия;
- нейросифилис.
Полинейропатия и полирадикулопатия ЦМВ-этиологии требует дифференцировки:
- полирадикулопатия, вызванная герпес-вирусами 2 и 6 типов;
- синдром Гийена-Барре;
- токсическая лекарственная, алкогольная или наркотическая полинейропатия.
При ретините и хориоретините исключают:
- токсоплазмоз;
- инфекции, вызванные вирусами простого и опоясывающего герпеса.
3. Лечение
На выбор тактики оказывают влияние следующие факторы:
- период болезни;
- клиническая форма;
- тяжесть заболевания;
- возраст больного;
- характер осложнений;
- доступность и возможность лечения в соответствии с необходимым видом оказания медицинской помощи.
Персональная ответственность за интерпретацию и использование настоящих рекомендаций лежит на лечащем враче.
- подавление репликации вируса;
- снижение тяжести и продолжительности болезни;
- предотвращение осложнений.
ПВТ проводится всем пациентам с первичным эпизодом или рецидивом для минимизации осложнений, сокращения длительности заболевания и вероятности рецидива.
Метод выбора ПВТ - ганцикловир или валганцикловир независимо от локализации и степени тяжести заболевания.
- Индукционный курс: часовое в/в/капельное введение 5 мг/кг ганцикловира в 100 мл физраствора или 5% глюкозы 2 раза в сутки 14 – 21 дней.
- Поддерживающий курс: 6 мг/кг ганцикловира 5 раз в неделю или 5 мг/кг ганцикловира ежедневно. Продолжительность курса индивидуальна.
Лечение ЦМВ-ретинита:
- орально 900 мг валганцикловира 2 раза в сутки 21 день;
- поддерживающая терапия – 900 мг валганцикловира 1 раз в сутки до купирования симптомов и исчезновения ДНК ЦМВ из крови.
Активная ЦМВ-инфекция у беременной: 1 мл/кг/сут антицитомегаловирусного иммуноглобулина человека в/в каждые 2 недели № 3.
Всем инфицированным ЦМВ пациентам, независимо от локализации и степени тяжести заболевания терапия синтетическими индукторами интерферона (по выбору):
- 250 мг (4 – 6 мг/кг) оксодигидроакридинилацетата натрия в/м, № 5 – 7 с интервалом 48 часов за 10 – 15 дней; при необходимости введение 500 мг через 18 – 36 часов;
- меглюмина акридонацетат № 3 каждые 24 часа, затем № 3 каждые 48 часов. В ремиссию еженедельно 250 мг 1 месяц, повторение курса через 4 – 5 недель.
Дезинтоксикационная, метаболическая, антиоксидантная терапии.
Дезинтоксикационная терапия направлена на купирование синдрома интоксикации.
Метаболическая терапия адеметионином 800 – 1600 мг в/в/струйно ежедневно 2 недели, затем по 2 – 4 таблетки в день.
Антиоксидантная терапия: 0,1г альфа-токоферола ацетата ежедневно 1 – 2 месяц в сочетании с препаратами селена.
Купирование воспалительных и токсических проявлений заболевания, предупреждение осложнений.
При повышении температуры более 38,0ºС - жаропонижающие средства.
- производные пропионовой кислоты;
- анилиды;
- производные уксусной кислоты и родственные соединения.
Читайте также:
- Инфекции крови и симптомы у собак
- Меры профилактики и защиты медперсонала от инфекций
- Белый кал у ребенка 2 года причины чем лечить дисбактериоз
- Анальная лихорадка на острове
- Общая схема микробиологической диагностики острых кишечных инфекций


