Системная красная волчанка и эпилептические припадки

wolfana, пишет 31 августа 2012, 20:57
Щелково, 47 лет
У кого-нибудь имеется вдобавок к СКВ ещё и эпилепсия или эпилептический синдром?
Врачи предполагают у меня (по моим описаниям) абсансы (бессудорожные приступы эпилепсии), говорят, что судорожные приступы могут быть в перспективе, но из-за СКВ и кучи осложнений опасаются мне прописывать что-то серьезное. Пока попаду к эпилептологу, который возмет на себя ответственность за мое лечение - изведусь вся.
Кто-нибудь принимает что-нибудь ещё (от эпилепсии) кроме препаратов, обычно сопровождающих СКВ?
У меня соббсно с эпиприступа и началсь хождение по врачам. СКВ стоит с 2006г, но кроме невынашивания, никаких признаков не проявлялось. И вот после очередной (непервой, заметьте) поездки в декабре 2010 в Египет, случился приступ.
Потом еще было 5 или 6 приступов, пока не подобрали препарат и дозу.
А до этого с 1994 года были приступы "де-жа-вю", и оказалось, что они и были началом эпи-побочки СКВ.
Так что начинайте принимать, а то потом приступы с частичной потерей "оперативной памяти" (забываешь ближайшие по времени незначительные факты, но с возвратом) - не очень прямо скажем приятная вещь! Препараты , которые я принимала, никакой побочки на СКВ не давали, ну разве что Тегретол, от которого вылезла жуткая сыпь и тромбоциты упали - это была аллергическая реакция, никак не отразившаяся на АНФ, атДНК и пр. ат.
Я принимаю Ламиктал. Вполне безобидный препарат. В Питере на него региональная льгота, и я получаю его в аптеке бесплатно.

Спасибо за ответ.
Областной эпилептолог не обнаружила у меня эпилепсию. По поводу ЭЭГ она сказала, что 15 минут не дают полноценной картины, чтобы ставить такой диагноз. Рекомендует сделать ночной видео-ЭЭГ, но склоняется к тому, что у меня всего лишь проявления нарушения сна и, возможно, АПНОЭ
Мне перед постановкой диагноза делали не просто ЭЭГ, а 4-часовой мониторинг ЭЭГ. Я должна была не спать всю ночь, а потом утром приехать в клинику и там сделать во сне. Я тогда так волновалась, что кажется вообще не спала на процедуре. Но врачи сказали, что я прваливалась в сон немного несколько раз, и этого было достаточно.

Мне моя эпилептолог сказала, что дневной 4-х часовой ЭЭГ тоже непоказателен. Ещё лучше - суточный ЭЭГ. Но может быть, это касается только слабовыраженных и потому - сомнительных - симптомов, а если приступы сильные, то достаточно и 3-4 часов.
Дело не в дневном или ночном, надо делать во время сна 4 часа как минимум.

О том и речь, что показательной можно считать ЭЭГ длительностью более 8 часов
Здравствуйте! У меня эпилепися с 13 лет, с 26 СКВ.Сейчас мне 32. Приступы ночные, во сне. Один раз уже на фоне СКВ был дневной. Раньше пила финлепсин, потом топомакс. У врачей есть серьезное подозрение, что моя скв лекарственная, т.е. спровоцированная лекарствами от эпилепсии и неправильным лечением в начале скв((Но с эти ничего не сделать уже. Последни 5 лет пью кеппру. Очень хороший препарат, нет побочных эффектов. Дорогой правда , моя доза на месяц 8 т.р. стоит. Однако мне повезло и я оформила льготу. Получаю в поликлинике бесплатно. У меня есть очень хороший врач эпилептолог, наблюдаюсь у нее с детства, думаю благодаря ей форма эпилепсии переросла в доброкачественную (т.е. приступы на терапии редкие, интеллект сохранен). Так что если вам понадобиться, обращайтесь, дам контакты (живу в Москве и врач тоже).

Сегодня я снова была у эпилептолога. Уже с результатами 9-ти часового ЭЭГ-видеомониторинга, подтвердившего наличие эпилептической активности, и МРТ. За этот год и состояние у меня изменилось - стала появляться спутанность в мыслях и рассеивание сознания, всего на несколько секунд, но зато всё чаще, до нескольких раз в день. Теперь уже точно поставили эпилепсию и назначили трилептал, как наиболее подходящий при СКВ.
Но я возобновила тему не ради этого "отчета" :)
Эпилептолог меня сразила, рассказав, что более чем в половине случаев СКВ рядом идет эпилепсия, причем дебют эпилепсии всегда предшествовал дебюту СКВ. Она рассказала, что всегда, когда обнаруживались и эпилепсия и СКВ выясняется, что сначала (обычно ещё в детстве) появлялись приступы эпилепсии (не обязательно припадки с судорогами, а также и случаи выпадения сознания, типа тех, что я описала, это тоже - приступы эпилепсии, если эпиактивность подтверждалась при ЭЭГ). А потом, спустя годы, случался дебют СКВ (не обязательно обострение: у меня были боли в суставах, которые сами прошли, а обострение только через несколько лет случилось).
Ещё она сказала, что если у ребёнка случались приступы эпилепсии, то следует потом почаще проверять его (её) на аутоиммунные заболевания.

Исследуем причины и методы лечения системной красной волчанки, трудного диагностируемого аутоиммунного заболевания, симптомы которого возникают внезапно и могут привести к инвалидности и даже смерти в течение десяти лет.
Что такое системная красная волчанка
Системная красная волчанка – это сложное хроническое воспалительное заболевание аутоиммунного характера, которое влияет на соединительную ткань. Поэтому оно атакует различные органы и ткани, имеет системный характер.

Воспалительная реакция, которую приносит заболевание, влияет на функции пораженных органов и тканей, и если болезнь не контролировать, то она может привести к их уничтожению.
Обычно, заболевание развивается медленно, но может также возникнуть очень внезапно и развиваться как форма острой инфекции. Системная красная волчанка, как уже упоминалось, является хронической болезнью, от которой не существует лечения.
Её развитие является непредсказуемым и протекает с чередованием ремиссий и обострений. Современные методы лечения, хотя и не гарантируют полного излечения, дают возможность контролировать заболевания и позволяют больному вести почти обычную жизнь.
Наиболее подверженных риску развития заболевания представители этнических групп африканских стран Карибского бассейна.
Причины волчанки: известны только факторы риска
Все причины, которые ведут к развитию системной красной волчанки, – неизвестны. Предполагается, что не существует одной конкретной причины, а к заболеванию приводит комплексное влияние различных причин.
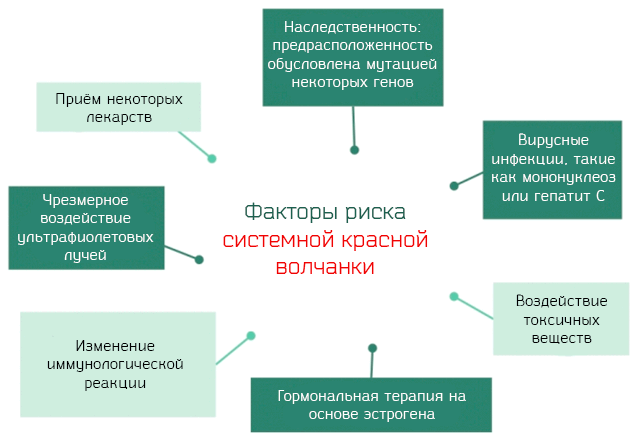
Однако, известны факторы, предрасполагающие к заболеванию:
Конечно, обладание генами, которые предрасполагают к развитию системной красной волчанки, ещё не гарантирует развитие заболевания. Существуют некоторые условия, которые действуют как спусковой крючок. Эти условия относятся к числу факторов риска развития системной красной волчанки.
Опасности окружающей среды. Таких факторов много, но все связаны со взаимодействием человека и окружающей среды.
Наиболее распространенными являются:
- Вирусные инфекции. Мононуклеоз, парвовирус B19, ответственный за кожную эритему, гепатита C и другие, могут вызвать системную красную волчанку у генетически предрасположенных лиц.
- Воздействие ультрафиолетовых лучей. Где ультрафиолетовые лучи – это электромагнитные волны, не воспринимаемые человеческим глазом, с длиной волны меньше, чем фиолетовый свет, и с более высокой энергией.
- Лекарства. Существует множество препаратов, как правило, используемых при хронических заболеваниях, которые могут вызвать системную красную волчанку. В эту категорию можно отнести около 40 препаратов, но наиболее распространенными являются: изониазид, используется для лечения туберкулеза, идралазин для борьбы с гипертонией, хинидиназин, используемый для лечения аритмических заболеваний сердца и др.
- Воздействие токсичных химических веществ. Наиболее распространенными являются трихлорэтилен и пыли кремнезема.
Гормональные факторы. Многие соображения заставляют нас думать, что женские гормоны и, в частности, эстроген играют важную роль в развитии болезни. Системная красная волчанка – это типичная для женщин болезнь, которая, обычно, появляется в годы полового развития. Исследования, проведенные на животных, показали, что лечение с помощью эстрогена вызывает или ухудшает симптомы волчанки, в то время как лечение мужскими гормонами улучшает клиническую картину.
Нарушения в иммунологических механизмах. Иммунная система, в нормальных условиях, не атакует и защищает клетки организма. Это регулируется с помощью механизма, который известен под названием иммунологической толерантности в отношении аутологичных антигенов. Процесс, который регулирует всё это, чрезвычайно сложный, но, упростив его, можно сказать, что в процессе развития иммунной системы, под влиянием лимфоцитов, могут появиться аутоиммунные реакции.
Симптомы и признаки волчанки
Трудно описать общую клиническую картину системной красной волчанки. Причин тому много: сложность заболевания, его развитие, характеризующееся чередованиями периодов длительного покоя и рецедивов, большое количество поражаемых органов и тканей, изменчивость от человека к человеку, индивидуальный прогресс патологии.
Всё это делает системную красную волчанку единственной болезнью, для которой вряд найдётся два полностью идентичных случая. Конечно, это значительно усложняет диагностику заболевания.
Волчанка сопровождается появлением очень расплывчатых и неспецифических симптомов, связанных с возникновением воспалительного процесса, который очень похож на проявление сезонного гриппа:
После начальной стадии и повреждения органов и тканей развивается более специфическая клиническая картина, которая зависит от областей тела, пострадавших от воспалительного процесса, поэтому могут возникнуть наборы симптомов и признаков, показанных ниже.
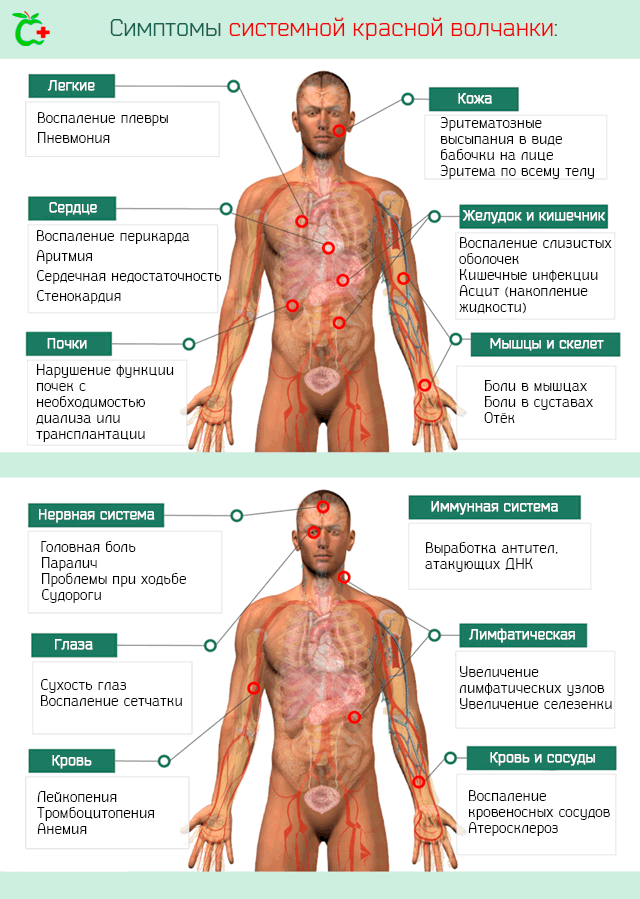
Также страдают слизистые оболочки рта и носа, где могут развиться очень болезненные поражения, которые плохо поддаются лечению.
Иммунная система. Болезнь определяет следующие иммунологических расстройств:
- Положительность на антитела, направленные против ядерных антигенов или против внутренних белков ядра, которые включают в себя ДНК.
- Положительность на антитела против ДНК.
- Положительность на антифосфолипидные антитела. Это категория аутоантител, направленных против белков, которые связывают фосфолипиды. Предполагается, что эти антитела способны даже в условиях тромбоцитопении вмешиваться в процессы свертывания крови и вызывать образование тромба.
Лимфатическая система. Симптомы, которыми характеризуется системная красная волчанка, когда поражает лимфатическую систему, это:
- Лимфаденопатия. То есть увеличение лимфатических узлов.
- Спленомегалия. Увеличенная селезенка.
Почки. Нарушения в работе почечной системы иногда называют волчаночный нефрит. Она может пройти несколько стадий – от легкой до тяжелой. Волчаночный нефрит требует скорейшего лечения, поскольку может привести к потере функции почек с необходимостью диализа и трансплантации.
Сердце. Вовлечение сердечной мышцы может привести к развитию различных заболеваний и их симптомов. Наиболее частыми являются: воспаление перикарда (мембрана, которая окружает сердце), воспаление миокарда, серьезная аритмия, нарушения в работе клапанов, сердечная недостаточность, стенокардия.
Кровь и кровеносные сосуды. Наиболее ощутимым следствием воспаления кровеносных сосудов является затвердение артерий и преждевременное развитие атеросклероза (образования бляшек на стенках сосудов, что сужает просвет и препятствует нормальному току крови). Этому сопутствует стенокардия, а в тяжелых случаях инфаркта миокарда.
Тяжелая системная красная волчанка влияет на концентрацию клеток крови. В частности, большой может иметь:
- Лейкопению – снижение концентрации лейкоцитов, вызванное, в основном, уменьшением лимфоцитов.
- Тромбоцитопению – снижение концентрации тромбоцитов. В связи с этим возникают проблемы со свертыванием крови, что может привести к серьезным внутренним кровотечением. В некоторых случаях, а именно у тех пациентов, у которых из-за болезни появляются антитела к фосфолипидам, ситуация диаметрально противоположная, то есть высокий уровень тромбоцитов, что ведёт к риску развития флебита, эмболии, инсульта и др.
- Анемия. То есть низкая концентрация гемоглобина в результате снижения количества циркулирующих в крови эритроцитов.
Легкие. Системная красная волчанка может вызвать воспаление плевры и легких, а затем плеврит и пневмонию с соответствующей симптоматикой. Также возможно скопление жидкости на уровне плевры.
Желудочно-кишечный тракт. Больной может иметь желудочно-кишечные боли из-за воспаления слизистых оболочек, которые покрывают внутренние стенки, кишечные инфекции. В тяжелых случаях воспалительный процесс может привести к перфорации кишечника. Также возможны скопления жидкости в брюшной полости (асцит).
Центральная нервная система. Заболевание может вызвать как неврологическую, так и психиатрическую симптоматику. Очевидно, что неврологическая симптоматика является наиболее грозной и, в определенных ситуациях, может поставить под серьезную угрозу саму жизнь пациента. Основным неврологическим симптомом является головная боль, но могут возникнуть паралич, трудности при ходьбе, судороги и эпилептические припадки, накопление жидкости во внутричерепной полости и увеличение давления, и др. Психиатрические симптомы включают расстройства личности, расстройства настроения, тревожность, психоз.
Глаза. Наиболее распространенным симптомом является сухость глаз. Также могут возникнуть воспаления и нарушения функции сетчатки, но эти случаи редки.
Диагностика аутоиммунного заболевания
Из-за сложности заболевания и неспецифичности симптомов диагностировать системную красную волчанку очень трудно. Первое предположение в отношении диагноза формулируется, как правило, врачом общей практики, окончательное подтверждение дают иммунолог и ревматолог. Именно ревматолог затем осуществляет контроль за пациентом. Также, учитывая большое количество повреждаемых органов, может потребоваться помощь кардиолога, невролога, нефролога, гематолога и так далее.
Сразу скажу, что ни один тест не может, сам по себе, подтвердить наличие системной красной волчанки. Заболевание диагностируется путём объединения результатов нескольких исследований, а именно:
- Анамнестическая история пациента.
- Оценка клинической картины и, следовательно, симптомов, испытываемых пациентом.
- Результаты некоторых лабораторных тестов и клинических исследований.
В частности, могут быть предписаны следующие лабораторные испытания и клинические исследования:
Анализ мочи. Используется для выявления белка в моче, чтобы получить полную картину функционирования почек.
Рентген грудной клетки для исследования на наличие воспаления легких или плевры.
Эходоплерография сердца. Чтобы убедиться в правильной работе сердца и его клапанов.
Терапия системной красной волчанки
Лечение системной красной волчанки зависит от степени выраженности симптомов и конкретных пораженных органов, и, таким образом, доза и вид препарата является предметом постоянного изменения.
В любом случае, обычно используют следующие лекарства:
- Все нестероидные противовоспалительные препараты. Служат для того, чтобы снять воспаление и боль, снизить жар. Тем не менее, они имеют побочные эффекты, если принимать их в течение длительного времени и в высоких дозах.
- Кортикостероиды. Имеют большую эффективность в качестве противовоспалительных средств, но побочные эффекты очень серьёзные: увеличение веса, гипертония, сахарный диабет и потеря костной массы.
- Иммунодепрессанты. Препараты, которые подавляют иммунный ответ и используются при строгих формах системной красной волчанки, которая затрагивает жизненно важные органы, такие как почки, сердце, центральная нервная система. Они эффективны, но имеют много опасных побочных эффектов: увеличение риска развития инфекций, повреждение печени, бесплодие и увеличения вероятности развития рака.
Риски и осложнения волчанки
Осложнения от системной красной волчанки связаны с теми нарушениями, к которым приводит повреждение затронутых заболеванием органов.
Также к осложнением следует добавить дополнительные проблемы, вызванные побочными эффектами терапии. Например, если патология затрагивает почки, в долгосрочной перспективе может развиваться почечная недостаточность и необходимость диализа. Кроме того, нефрологическую волчанку следует держать строго под контролем, и поэтому есть необходимость в иммуносупрессивной терапии.
Системная красная волчанка является хроническим заболеванием, от которого не существует никакого лечения. Прогноз зависит от от того, какие органы и в какой степени повреждены.
Конечно, хуже, когда вовлечены жизненно важные органы, такие как сердце, мозг и почки. К счастью, в большинстве случаев, симптоматика заболевания довольно сдержанная, и современные методы лечения могут справиться с заболеванием, что позволяет пациенту вести почти нормальный образ жизни.
В любом случае, если ребенок выживает после родов, симптомы системной красной волчанки сохранятся не более 2 месяцев, пока в крови младенца будут присутствовать антитела матери.
Острую системную красную волчанку в настоящее время почти все авторы относят к коллагенозам. Поражения нервной системы при этой болезни, как, и при узелковом периартериите, обусловлено изменениями мезенхимальной ткани, главным образом сосудов центральной и периферической нервной системы.
Острая красная волчанка была вначале описана как лихорадочное заболевание с кожными явлениями. Дальнейшие исследования обнаружили, что при этой болезни поражаются различные внутренние органы. Чаще всего страдают серозные оболочки, лимфатические узлы, почки, сердце, сосуды, в том числе и сосуды мозга.
Поражения периферических нервов обычно не столь тяжелы, как при узелковом периартериите, но боли и чувствительность периферических нервов к давлению встречаются очень часто.
Диффузное поражение коллагена стенок сосудов вызывает самые различные синдромы со стороны центральной нервной системы: эпилептические припадки, параличи, афазии, психические нарушения, поражения черепных нервов. Чаще всего наблюдаются эпилептические припадки. Руссель, Газерик и Цакер отметили судорожные припадки в 15% из 144 наблюдений острой красной волчанки, собранных в литературе. Среди 28 больных, находившихся под их наблюдением, у 7 были эпилептические припадки. У 2 из них припадки возникли до появления других признаков красной волчанки, у 3 - на высоте заболевания, а у 2 - только в терминальной фазе болезни.
Подобно эпилепсии кожным высыпаниям могут предшествовать другие синдромы поражения нервной системы: хореиформный гиперкинез, гемиплегия, миелит. У некоторых больных появляется менингеальный синдром.
Психические нарушения наблюдаются довольно часто. Тумулти отметил такого рода расстройства у 25 из 105 больных. Т. А. Невзорова и О. М. Виноградова описали состояние спутанности, дезориентации, параноидные и галлюцинаторные синдромы.
На дне глаз нередко обнаруживаются отек сетчатки, периваскулярный эксудат, реже - кровоизлияния.
Спинномозговая жидкость в большинстве случаев нормальна. Только у отдельных больных описано небольшое повышение белка и нерезко выраженный плеоцитоз. Бертран и Бонне наблюдали больного с белково-клеточной диссоциацией в ликворе.
Основным патогистологическим изменением при острой красной волчанке является фибриноидный некроз коллагена. Последний сочетается с незначительным воспалением, локализующимся в небольших, но многочисленных очагах. В мозгу обнаруживаются поражения мелких артерий и артериол в виде субинтимального фибриноидного некроза коллагена, который распространяется между мышечными волокнами, а также между мышечной и адвентициальной оболочкой. Деструкция мышечных и соединительнотканных элементов приводит к некрозу стенки сосуда и закрытию его просвета вследствие пролиферации эндотелия. Вокруг сосудов видны небольшие инфильтраты, состоящие из мононуклеаров и полинуклеаров.
В результате этих процессов в мозгу возникают более или менее рассеянные очаги размягчения, петехиальные кровоизлияния, иногда субарахноидальные кровоизлияния.
Глазер, Меламед обнаружили многочисленные мелкие рубцы в коре мозга, создающие картину гранулематозной атрофии. Каждый из этих рубцов является следствием микроинфаркта серого вещества Мозга с реактивным глиозом. Белое вещество мозга поражается реже. Этими изменениями в коре мозга можно объяснить частое появление при красной волчанке эпилептических припадков. Следует подчеркнуть, что пато-гистологические изменения сосудов мозга нередко не дают клинических симптомов.
Течение болезни в общем неблагоприятное, лишь у некоторых больных наступает ремиссия. При этом явления со стороны периферических нервов могут улучшиться. Симптомы со стороны центральной нервной системы менее склонны к ремиссии . Прогноз болезни хуже в случаях, в которых имеются признаки поражения головного мозга.
Диагноз в значительной мере опирается на наличие кожных явлений, но в отдельных случаях их может и не быть. Большое значение имеет обнаружение в крови клеток красной волчанки, которые очень редко обнаруживаются при других болезнях.
Современная терапия красной волчанки состоит в назначении гормональных препаратов (кортизон, преднизон). Такое лечение у части больных ведет к более или менее длительной ремиссии. У большинства больных, несмотря на лечение, болезнь неуклонно продолжает прогрессировать и приводит к летальному исходу.
Описан клинический случай ишемического инсульта у пациентки 7 лет с системной красной волчанкой, сочетающейся с антифосфолипидным синдромом. Была определена природа неврологических нарушений. Адекватная коррекция антикоагулянтами позволила форсировать реп
A clinical case of ischemic stroke in a 7-year-old patient with systemic lupus erythematosus combined with antiphospholipid syndrome is described. The nature of these disorders was determined. An appropriate correction through anticoagulation treatment made possible to speed up the repair of the central nervous system and to prevent further recurrence of thrombosis.
Ишемический инсульт (ИИ) в настоящее время признан одной из ведущих причин инвалидизации и смертности взрослого населения. ИИ — это острое нарушение мозгового кровообращения, приводящее к развитию стойкого очагового неврологического дефицита. До недавнего времени бытовало мнение о том, что случаи возникновения ИИ у детей казуистически редки, между тем согласно данным наиболее крупного канадского регистра (Canadian Pediatric Ichemic Stroke Pegistry) заболеваемость артериальным ИИ в детском возрасте составляет 2,7 на 100 000 детей в год, при этом 25–30% всех случаев приходится на неонатальный период и 50% случаев на возраст до одного года [1]. По данным В. П. Зыкова и соавт. [2] заболеваемость детей церебральным инсультом в Южном округе г. Москвы составляет 2,14 на 100 000 в год, а распространенность — 6,94 на 100 000, при этом в перинатальном периоде заболеваемость ИИ наиболее высокая и достигает 1 на 4000 новорожденных, что соответствует заболеваемости инсультом взрослых в течение 4–5 десятилетий жизни. Общая смертность от инсультов в детском возрасте составляет 0,6 на 100 000 [2].
Исход ИИ у большинства детей неблагоприятный: 3–12% детей погибают в остром периоде, у 61–74% детей сохраняются стойкие неврологические симптомы. Повторные эпизоды нарушения мозгового кровообращения по ишемическому типу встречаются в среднем у 8–42% пациентов [1, 3].
Причины возникновения ИИ у детей существенно отличаются от таковых у взрослых, наиболее частыми являются невоспалительные васкулопатии (локальная артериальная диссекция, болезнь моя-моя, лекарственная васкулопатия и др.), первичные и вторичные васкулиты с вовлечением центральной нервной системы (ЦНС), кардиоэмболизм у детей с болезнями сердца, приобретенные и врожденные тромбофилии, метаболические и др. [2, 4].
Среди системных заболеваний соединительной ткани, характеризующихся наличием системного васкулита, наиболее высокий риск развития ИИ отмечается при системной красной волчанке (СКВ), он превышает популяционный в 2–3 раза, и его наиболее высокие показатели наблюдаются у детей в возрасте от одного года до 17 лет и пациентов молодого возраста [5, 6]. Развитие ИИ при СКВ сопряжено с наличием как традиционных, так и нетрадиционных факторов риска: мужского пола, молодого возраста, отягощенного по сердечно-сосудистым заболеваниям семейного анамнеза, артериальной гипертензии, курения, диабета, гиперлипидемии, нейролюпуса, поражения клапанов сердца, серозита, снижения активности комплемента, выявления аутоантител, приема азатиоприна [7, 8]. Важная роль в генезе ряда нейропсихических симптомов и, в частности, ИИ при СКВ принадлежит антифосфолипидным антителам (аФЛ) [9, 10]. аФЛ — это гетерогенная популяция антител, из которых три группы — волчаночный антикоагулянт (ВА), антитела к кардиолипину (аКЛ) и антитела к β2-гликопротеину-1 (анти-β2-ГП1) — включены в перечень диагностических критериев антифосфолипидного синдрома (АФС), проявляющегося венозным и/или артериальным тромбозом и/или рецидивирующим синдромом потери плода. Таким образом, АФС представляет собой приобретенную аутоиммунную тромбофилию, которая нередко сочетается с другими аутоиммунными заболеваниями, наиболее часто с СКВ.
В различных публикациях продемонстрировано, что клинические проявления ИИ у детей характеризуются рядом особенностей. Так, в отличие от взрослых, у них часто отсутствуют такие классические симптомы, как гемипарез, нарушение речи. Частыми проявлениями ИИ у детей наряду с гемиплегией/гемипарезом являются эпизоды сильной головной боли, нарушение сознания, судорожный синдром, центральный парез лицевой мускулатуры, нарушение речи [2, 11]. Указанные клинические симптомы нередко получают неправильную оценку, что определяет ошибочность тактики ведения пациентов и неблагоприятный прогноз.
Следует отметить, что при СКВ трактовка имеющихся у больного признаков поражения нервной системы представляет особенно большие трудности в силу их патогенетической разнородности и чрезвычайного клинического многообразия. Классификация, опубликованная в 1999 г. исследовательским комитетом Американского ревматологического колледжа (American College of Rheumatology, ACR), включала 12 синдромов поражения ЦНС и 7 синдромов поражения периферической нервной системы. Возможные патогенетические механизмы их развития включают тромбоэмболизм, васкулопатию мелких сосудов и, в редких случаях, истинный церебральный васкулит [12]. Кроме того, неврологическая симптоматика может быть обусловлена метаболическими нарушениями, инфекцией, побочным действием лекарств, в частности, стероидов, сопутствующей патологией и др. Выбор оптимальной тактики лечения в каждом конкретном случае требует глубокого анализа и комплексного обследования.
С целью демонстрации трудности диагностики и лечения больной СКВ и АФС с поражением нервной системы приводим клиническое наблюдение.
Больная В., 7 лет, поступила в Университетскую детскую клиническую больницу Первого МГМУ им. И. М. Сеченова в апреле 2014 г. с жалобами на нарушение речи, частые головные боли. Ранний анамнез — без особенностей. Наследственный анамнез по тромбозу не отягощен.
В феврале 2014 г. девочка была госпитализирована в стационар по месту жительства, с жалобами на ежедневные подъемы температуры до 39,8 °C, боли в суставах. При обследовании выявлены лимфаденопатия, гепатоспленомегалия, полисерозит, в анализах крови — повышение СОЭ до 40–52 мм/ч, лейкопения (лейкоциты 3,8 × 10 9 /л), анемия (Нв — 92 г/л). Проводился онкологический поиск, по результатам пункции костного мозга патологии не выявлено. Получила повторный курс антибактериальной терапии (препараты пенициллинового ряда, затем макролиды) без эффекта.
Через месяц в марте 2014 г. на фоне высокой лихорадки отмечались повторные эпизоды генерализованных тонико-клонических судорог с потерей сознания (ребенок находился в сопоре в течение 5 дней). По данным магнитно-резонансной томографии: выраженный отек головного мозга, по результатам электроэнцефалографии — генерализованная эпилептиформная активность.
По данным лабораторного обследования признаков активности СКВ выявлено не было: АТ к ДНК — 24 МЕ/МЛ (норма 0–20 МЕ/мл), АНФ — отр., однако уровни аФЛ в сыворотке крови превышали нормальные значения: аКЛ-IgG — 15 МЕ/мл (норма 0–7), аКЛ-IgМ — 24 МЕ/мл (норма 0–10), ВА — положительный.
Данные анамнеза, клинико-лабораторного и инструментального обследования девочки были расценены как проявления системной красной волчанки высокой степени активности с поражением суставов, серозных оболочек, Кумбс-положительной гемолитической анемией и лейкопенией в сочетании с антифосфолипидным синдромом, клиническим проявлением которого был ишемический инсульт, а лабораторными маркерами — ВА, анти-β2-ГП I и аКЛ. Обнаружение трех типов аФЛ указывало на возможность рецидива тромботических осложнений.
С целью уточнения степени риска рецидива тромбоза и определения длительности и интенсивности антитроботической терапии и профилактики было проведено исследование полиморфизмов генов свертывания крови. У девочки выявлены гетерозиготные формы мутаций в гене метилентетрагидрофолатредуктазы (MTHFR Ala 222Val CT) и ингибитора активатора плазминогена I (PAI-I (SERPINE) — 675 5G/4G).
Таким образом, поражение нервной системы у данной больной главным образом было обусловлено тромботическим процессом в рамках тромбофилии, обусловленной носительством аФЛ и наличием полиморфизмов генов свертывания крови и являющейся значимым неблагоприятным фактором прогноза у данной пациентки. С учетом этого дальнейшая тактика ведения больной была направлена на улучшение микроциркуляции и предотвращение рецидива тромбоза. Была назначена активная антитромботическая терапия низкомолекулярным гепарином (фраксипарином п/к 0,3 мл/сутки). Помимо этого проводилась сосудистая, нейротрофическая и метаболическая терапия нарушений ЦНС (Актовегин, Кортексин, Вазобрал, Пикамилон, Элькар, Семакс в возрастных дозировках).
При повторной госпитализации через 4 месяца состояние девочки расценивалось как удовлетворительное. Отмечено существенное улучшение неврологического статуса. Сознание — ясное, на вопросы отвечает адекватно, социальный контакт — хороший. Эмоционально-поведенческая сфера — по возрасту, периодически астенические проявления. ЧМН — легкая анизокория слева. Когнитивная сфера — речь: увеличение объема экспрессивной и импрессивной речи, инкременция объема механической и ассоциативной памяти, однако сохраняются парциальный дефицит сферы мышления, внимания с астеническим компонентом. Вместе с тем девочка учится в массовой школе, объем информации усваивает. Двигательная сфера: тонус ближе к физиологическому, объем движений не ограничен, сохраняются незначительные проявления правостороннего гемипареза в виде пирамидных знаков и утомляемости от физической нагрузки, координаторные пробы выполняет, статические без дефицита, в локомоторных — незначительная дисметрия справа. Тазовые функции: центральная регуляция сформирована, периферическая не нарушена. Вегетативное обеспечение — ваготония. За истекший после последней госпитализации срок судорожных проявлений не отмечалось.
При повторной МРТ головного мозга отмечены проявления перенесенного ишемического инсульта в виде атрофии в височно-теменной области и резидульной вентрикуломегалии. По данным ЭЭГ умеренно выраженные эпилептиформные изменения ЭА, преобладающие в задних отделах мозга, при гипервентиляции отмечаются фокальные изменения в задневисочной области.
С учетом отсутствия активности патологического процесса доза преднизолона была снижена до 10 мг/сут (0,3 мг/кг/сут), продолжено лечение варфарином (МНО 1,8–1,9).
Дальнейшее наблюдение девочки в течение полутора лет продемонстрировало полное нивелирование неврологической симптоматики, что еще раз доказало значительные репаративные способности детского мозга при правильной терапевтической коррекции. Последовательное проведение антитромботической профилактики позволило предотвратить возможные новые эпизоды нарушения мозгового кровообращения.
В представленном клиническом наблюдении продемонстрирована сложность трактовки тяжелой неврологической симптоматики, возникшей на фоне высокой клинико-лабораторной активности СКВ, которая проявлялась длительной потерей сознания, рецидивирующими генерализованными тонико-клоническими судорогами и очаговой симптоматикой. Результаты дополнительных исследований позволили определить тип поражения ЦНС в виде ишемического инсульта в бассейне средней мозговой артерии и установить факторы риска его развития (наличие аФЛ и полиморфизмов генов свертывания крови). Установление генеза имеющихся нарушений детерминировало корректный объем терапевтических мероприятий, включающих применение прямых, а в последующем и непрямых антикоагулянтов. Этот подход позволил не только улучшить репарацию ЦНС, но и превентировать возможные рецидивы тромбоза.
Литература
- DeVeber G. Canadian Pediatric Ichemic Stroke Pegistry // Paediatr Child Health. 2000: A17.
- Зыков В. П., Комарова И. Б., Чучин М. Ю., Ушакова Л. В., Степанищев И. Л. Ишемический инсульт у детей. Учебное пособие. М., 2011. 72 с.
- Fox C. K., Fullerton H. J. Recent Advances in Childhood Arterial Ischemic Stroke // Curr Atheroscler Rep. 2010, 112, 217–224.
- Poisson S. N., Schardt T. Q., DIngman A., Bernard T. J. Etiology and treatment of arterial ischemic stroke in children and young adults // Curr Treat Options Neurol. 2014, 16 (10), 315.
- Holmqvist M., Simard J. F., Asplund K., Arkema E. V. Stroke in systemic lupus erythematosus: a meta-analysis of population-based cohort studies // RMD Open. 2015, 16; 1 (1): e000168.
- Wang I. K., Muo C. H., Chang Y. C., Liang C. C., Lin S. Y., Chang C. T., Yen T. H., Chuang F. R., Chen P. C., Huang C. C., Sung F. C. Risks, subtypes, and hospitalization costs of stroke among patients with systemic lupus erythematosus: a retrospective cohort study in Taiwan // J Rheumatol. 2012; 39 (8): 1611–1618.
- Fernández-Nebro A., Rúa-Figueroa Í., López-Longo F. J., Galindo-Izquierdo M., Calvo-Alén J., Olivé-Marqués A., Ordóñez-Cañizares C., Martín-Martínez M. A., Blanco R., Melero-González R., Ibáñez-Rúan J., Bernal-Vidal J. A., Tomero-Muriel E., Uriarte-Isacelaya E., Horcada-Rubio L., Freire-González M., Narváez J., Boteanu A. L., Santos-Soler G., Andreu J. L., Pego-Reigosa J. M. EAS-SER (Systemic Diseases Study Group of Spanish Society of Rheumatology). Cardiovascular Events in Systemic Lupus Erythematosus: A Nationwide Study in Spain From the RELESSER Registry // Medicine (Baltimore). 2015; 94 (29): e1183.
- Ballocca F., D’Ascenzo F., Moretti C., Omedè P., Cerrato E., Barbero U., Abbate A., Bertero M. T., Zoccai G. B., Gaita F. Predictors of cardiovascular events in patients with systemic lupus erythematosus (SLE): a systematic review and meta-analysis // Eur J Prev Cardiol. 2015, 22 (11): 1435–1441.
- Yu H. H., Lee J. H., Wang L. C., Yang Y. H., Chiang B. L. Neuropsychiatric manifestations in pediatric systemic lupus erythematosus: a 20-year study // Lupus. 2006; 15 (10): 651–657.
- Hawro T., Bogucki A., Krupiska-Kun M., Maurer M., Woniacka A. Intractable headaches, ischemic stroke, and seizures are linked to the presence of anti-β2 GPI antibodies in patients with systemic lupus erythematosus // PLoS One. 2015, 17; 10 (3): e0119911.
- Mallick A. A., Ganesan V., Kirkham F. J., Fallon P., Hedderly T., McShane T., Parker A. P., Wassmer E., Wraige E., Amin S., Edwards H. B., Tilling K., O’Callaghan F. J. Childhood arterial ischaemic stroke incidence, presenting features, and risk factors: a prospective population-based study // Lancet Neurol. 2014; 13 (1): 35–43.
- Böckle B. C., Jara D., Aichhorn K., Junker D., Berger T., Ratzinger G., Sepp N. T. Cerebral large vessel vasculitis in systemic lupus erythematosus // Lupus. 2014; 23 (13): 1417–1421.
Н. С. Подчерняева, доктор медицинских наук, профессор
Л. Г. Хачатрян 1 , доктор медицинских наук, профессор
Ю. О. Костина, кандидат медицинских наук
О. В. Шпитонкова, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва
Читайте также:


