Ювенильный хронический артрит этиология

- 7 Августа, 2018
- Ревматология
- Волощук Наталя
В современной педиатрии одной из актуальных проблем выступает диагностирование и лечение болезней суставов воспалительного характера. Среди всех ревматических заболеваний, развивающихся в детском возрасте, самым распространенным является ювенильный хронический артрит (ЮХА). Он представляет собой аутоиммунное заболевание, характеризующееся длительным воспалением сустава у ребенка до шестнадцати лет, что возникает по неизвестным причинам.
Эта болезнь является серьезной и требует своевременного лечения, а также постоянного поддержания особого образа жизни. Проблемой недуга выступает сложность определения всех мест воспаления и выбор соответствующих медицинских препаратов для их устранения.
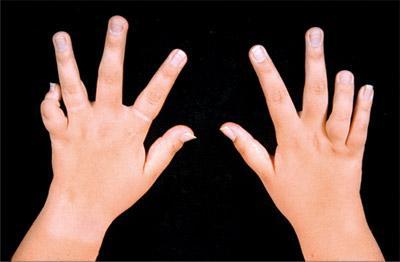
Описание
ЮХА относится к аутоиммунным болезням суставов. Он носит хроническую форму и обуславливается длительным протеканием с периодическими проявлениями патологических процессов. Независимо от того какие суставы поражаются, у ребенка наблюдается болезненность и отек тканей. Это приводит к скованности при движениях, деформации суставов и вывихам.
Данный вид артрита имеет продолжительность больше трех месяцев. В медицине прослеживается связь его появления с перенесенными ОРВИ, прививками, приемом гаммаглобулина, травмами и т. д.
При этом заболевании иммунная система ребенка по неизвестным причинам воспринимает ткани организма как чужеродные и хочет их уничтожить. При этом развивается воспаление негнойного характера синовиальных оболочек, что способствует увеличенному выделению суставной жидкости. Со временем синовиальные оболочки спаиваются с суставным хрящом, вызывая его эрозию. Из-за этого хрящ разрушается. Продолжительность процесса может быть разной у всех больных.
Этиология и эпидемиология
Развивается чаще всего ювенильный хронический артрит у детей в возрасте от двух до шести лет. Недуг встречается в 0,4 случаев из одной тысячи детей или 16:100000 детей до шестнадцати лет. Больше всего страдают от заболевания девочки.
Отмечается, что близкие родственники заболевших, как правило, имеют коллагенозы и ревматоидные артриты. Смертельный исход от болезни составляет 1 %. Очень часто ЮХА приводит к инвалидизации.
Разновидности заболевания
В медицине существует классификация ювенильных артритов:
- Пауциартикулярный ЮХА. Он характеризуется поражениями от одного до четырех суставов одновременно: коленного, голеностопного, локтевого и лучезапястного. Чаще всего болеют девочки до пяти лет.
- Спондилоартрит ювенильный. Обуславливается поражением коленного, голеностопного и бедренного суставов, а также воспалением сухожилий.
- Полиартикулярный ювенильный хронический артрит, при котором поражаются более четырех суставов, чаще всего верхних и нижних конечностей. Болезнь считается опасной, а при постановке диагноза на ранних стадиях заболевания возникают трудности.
- Системный ЮХА, характеризующийся отсутствием симптомов на ранней стадии. Проявляется недуг ночными лихорадками, зудящими высыпаниями, увеличением гланд.
Опасность болезни
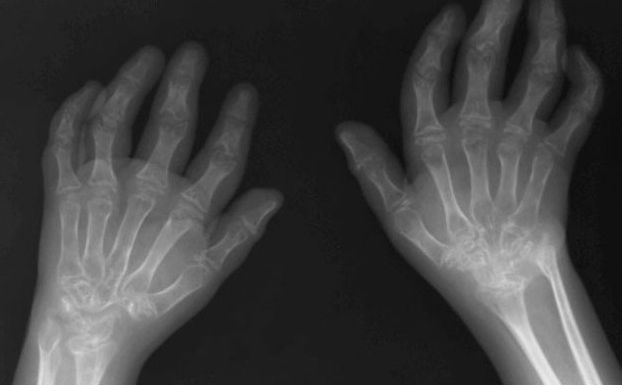
Такие болезни, как ЮХА, считаются тяжелыми, но, к счастью, редко приводят к смерти. Основную же опасность представляет разрушение хряща в суставе, в результате чего может наступить инвалидность. Ювенильный артрит может способствовать и потере зрения.
Но при правильном и своевременном лечении заболевания можно достичь ремиссии. Для этого необходимо придерживаться определенного образа жизни, постоянно находиться под наблюдением специалистов и принимать медикаментозные препараты, чтобы не было рецидивов.
Причины
Поскольку данный вид артрита относится к группе аутоиммунных болезней, то основной причиной его развития являются нарушения в иммунной системе ребенка. Толчком к появлению недуга на фоне сниженного иммунитета могут стать определенные факторы:
- Попадание в организм вирусной или бактериальной инфекции.
- Повреждение сустава вследствие травм.
- Генетическая предрасположенность к болезни.
- Переохлаждение или перегрев.
- Последствия плановых прививок.
- Заболевания эндокринной системы.
Признаки и симптомы
Родители должны пристально наблюдать за здоровьем своих детей, обращая внимание на первые признаки артрита, поскольку от этого зависит оперативность назначения медикаментозного лечения. ЮХА распознать тяжело, поэтому рекомендуется при первых жалобах обратиться к медику для проведения обследования и постановки диагноза.
При данном заболевании возможно замедление роста ребенка, иногда суставы могут развиваться с разной скоростью, в результате чего у ребенка может отличаться длина конечностей.
В медицине принято выделять основные признаки артрита:
- Появление в ночное время лихорадки, сопровождающейся пятнистой сыпью.
- Слабость и быстрая утомляемость, частые приступы головной боли.
- Болевые ощущения в суставах, их припухлость. Но при этом маленькие дети не жалуются на боль.
- Со временем происходит деформация суставов, внутренних органов, увеличение лимфатических узлов.
Типичным признаком для недуга выступает патология шейного отдела позвоночника и челюстных суставов, что часто приводит к недоразвитию либо нижней, либо верхней челюсти.
Диагностика
Перед тем как врач скажет, чем лечить артрит, ему необходимо поставить точный диагноз. Для этого нужна консультация не только педиатра, но и ревматолога, травматолога, а также окулиста, который проведет обследование глазного яблока. После этого назначают анализы крови, иммунологических показателей. Также внимательно изучается анамнез и история болезни. Ювенильный артрит может иметь генетическую природу, поэтому необходимо выяснить, нет ли в семье страдающих болезнями суставов. Проводят такие исследования:
- УЗИ внутренних органов;
- рентгенография, КТ суставов, забрюшинного пространства и грудной клетки;
- электрокардиограмма и пункция костного мозга;
- исследование желудка и пищевода;
- эзофагогастоскопия.
Лечение
Рассматривая вопрос о том, чем лечить артрит, необходимо отметить, что лечится он как медикаментами, так и вспомогательной терапией. Опытный врач назначает четыре группы медицинских препаратов, которые имеют разные действия на организм.
Сюда относят противовоспалительные нестероидные средства, которые нацелены на купирование болей и воспаления сустава, способствуют восстановлению его функций. Также применяются глюкокортикоиды, иммунодепрессанты и биологические агенты. Но их отмена часто провоцирует обострение недуга. Поэтому рекомендуется принимать лекарственные средства даже в период ремиссии, чтобы заболевание снова не обострилось.
Вспомогательное лечение
Не менее важным при лечении такого заболевания, как ювенильный хронический артрит, является вспомогательная терапия, которая включает:
- двигательную активность и лечебную физкультуру (плаванье, пешие прогулки и т. д.);
- соблюдение диеты;
- физиотерапию (электрофорез, криотерапия, лазер и прочее);
- массаж для восстановления кровообращения;
- ортопедическую коррекцию.
Хирургическое вмешательство может быть произведено в том случае, когда суставы не выполняют своих функций из-за деструктивного поражения. В этом случае проводят эндопротезирование сустава, артропластику и прочее.
Необходимо отметить, что ювенильный хронический артрит нельзя полностью вылечить. Но регулярное наблюдение у специалиста и правильно подобранное лечение дает возможность получить ремиссию на длительный временной период, улучшив тем самым качество жизни.
Цели лечения
Поскольку данное заболевание полностью не излечивается, медики назначают терапию, имеющую определенные цели. К ним относят:
- снижение воспалительного процесса;
- купирование суставного синдрома;
- сохранение функций суставов;
- снижение побочных эффектов от лечения медицинскими препаратами.
Очень важно замедлить разрушение сустава и избежать дальнейшей инвалидизации человека, достичь длительной ремиссии и, конечно же, улучшенить качество жизни пациентов.

Профилактика
Первичной профилактики заболевания не существует, так как причины его появления до конца не изучены. Вторичная профилактика нацелена на предупреждение рецидивов недуга.
Рекомендуется систематические наблюдение у ревматолога, который при помощи лабораторных анализов поможет распознать обострение болезни как можно раньше. Тогда врачом будет предложено усиленное лечение, направленное на снижение прогрессирования недуга. Также необходимо избегать перегрева и переохлаждения организма, защититься от инфекций.
От плановых вакцинаций врачи рекомендуют отказываться, чтобы не спровоцировать развитие ювенильного артрита, симптомы которого описаны выше. Ребенку необходимо правильно питаться, исключив из рациона жирную, острую и мучную пищу.
Образ жизни больного
Как было сказано, больному артритом ребенку нельзя делать прививки, но Манту никакой опасности не представляет, несмотря на введение в организм туберкулина. Детям нельзя давать препараты, которые направлены на стимуляцию иммунной системы. Пациентов с ювенильным артритом необходимо ограничить:
- от сильных физических нагрузок;
- перегрева и переохлаждения;
- контакта с инфекциями и вирусами;
- взаимодействиями с различными животными, которые могут переносить инфекции;
- эмоциональных и психологических нагрузок;
- перемены климата.
Прогноз
При данном заболевании наблюдаются частые рецидивы, которые неблагоприятно влияют на прогноз заболевания. Часто наступает инвалидизация. Ребенок становится ограниченным в физической активности, не может полностью себя обслуживать и самореализовать. Это происходит чаще всего, когда недуг проявился в раннем возрасте.
У таких пациентов часто развивается патология органов зрения (глаукома, катаракта и др.) спустя пять лет после начала заболевания. Через 11 лет после первого проявления недуга у некоторых детей наблюдалось развитие увеита, из них у 15 % наступала полная слепота. Одним из серьезных осложнений при ЮХА является амилоидоз и тяжелая функциональная недостаточность.
У половины всех больных прогноз можно считать благоприятным, поскольку ремиссия может продолжаться несколько лет. У трети пациентов наблюдается постоянно рецидивирующее течение болезни. Смертность при ЮХА невысока, и зависит от развития амилоидоза или осложнений неинфекционного характера из-за проведения глюкокортикоидной терапии длительный период времени.
Все вышеперечисленное говорит о том, что некоторые больные требуют с ранних сроков развития патологии постоянного наблюдения и лечения, чтобы предотвратить развитие серьезных нарушений, которые в будущем могут повлиять на физическую и социальную адаптацию человека.
Таким образом, причины ювенильного артрита не установлены на сегодняшний день. Заболевание проявляется в детском возрасте (до 16 лет) и часто ведет к инвалидности. По МКБ-10 недуг имеет номер М08-М09. В настоящее время продолжается изучение возможных причин развития болезни.

Примечание. Обозначения аминокислотного кода: А = Ala, D = Asp, Е = Glu, G = Gly, I = ILe, К = Lys, L = Leu, Q = Gin, R = Arg Рис. 56.
Детерминанты предрасположенности к ЮРА
Предполагают, что один или несколько экзогенных или аутоантигенных пептидов могут присоединяться к этому гену предрасположенности к ЮРА и вызывать это заболевание. Интересно, что вирусный гликопротеин Эпштейна—Барра (гликопротеин 110) содержит идентичную последовательность аминокислот. Таким образом, можно допустить, что ЮРА — это полиэтиологическое заболевание, в основе которого лежит изменение реактивности больных, их сверхчувствительности к различным факторам внешней среды, но с единым иммунопатологическим механизмом. ПАТОГЕНЕЗ. В основе патогенеза ЮРА лежит активация иммунокомпетентных клеток, аутоиммунные реакции и формирование иммунных комплексов. Для подобного утверждения имеются определенные доказательства, которые представлены в таблице 59.
Основные признаки участия иммунологических механизмов в патогенезе ювенильного ревматоидного артрита

В соответствии с последними научными данными можно предполагать следующий механизм развития ЮРА (рис. 57).

Схема патогенеза ювенильного ревматоидного артрита
; ИЛ — интерлейкин, Нр — нейтрофилы, М — моноциты, Л — лимфоциты, Ф — фагоциты, ПГ — простагландины, ЛТ — лейкотриены, С — серотонин, Г — гистамин Этиологический фактор (вирус Эпштейна—Барра, микоплазмы, бактерии и др.) действует в двух направлениях. Во-первых, этиологический фактор (или его антигены) локализуется на синовиальной оболочке сустава, вызывая местную иммунную реакцию с образованием измененных (агрегированных) IgG, обладающих аутореактивностью (аутоантигенностью). При этом агрегированные IgG распознаются как чужеродные антигены. В результате этого синовиальная оболочка сустава набухает, становится гиперемированной, в полости сустава значительно увеличивается количество синовиальной жидкости. Следовательно, в результате местной иммуновоспалительной реакции возникает синовит. Во-вторых, антигенные детерминанты (вирусные частицы, пептидогликан бактериальной стенки и др.) этиологического фактора присоединяются к антигенным детерминантам гипервариабельной зоны гаплотипа DR-6eTa-l HLA-антигенов, вызывая активацию 1а-антиген-позитивных клеток, которые выделяют интерлейкин-1, активирующий Т-лимфоциты-хелперы, и представляют данные антигены для взаимодействия с рецепторами распознавания Т-клеток-хелперов. В дальнейшем активированные Т-лимфоциты-хелперы секретируют лимфокины и интерлейкины.
Классификация ювенильного ревматоидного артрита
(А.В. Долгополова и соавторы, 1980)

Показатели активности ювенильного ревматоидного артрита

Степень активности процесса определяется числом баллов: I степень — 8 баллов; II — 9—16 баллов; III — 17—24 балла. Стадии болезни, характеризующие прогрессирование ЮРА, определяются исключительно рентгенологически и во всем мире оцениваются принципиально одинаково (табл. 62). При оценке стадий заболевания необходимо иметь в виду, что при ЮРА изменения разных суставов находятся в различных рентгенологических стадиях, поэтому в диагнозе конкретного больного отражается стадия, соответствующая максимальным изменениям любого сустава. При оценке функциональной способности больного используют следующие градации: 1) функциональная способность сохранена; 2) нарушена по состоянию опорно-двигательного аппарата: а) способность к самообслуживанию сохранена; б) способность к самообслуживанию частично утрачена; в) способность к самообслуживанию утрачена полностью; 3) нарушена по состоянию глаз или внутренних органов.
Рентгенологические стадии ювенильного ревматоидного артрита
(Steinbroker и соавторы, 1949, с изменениями)

Клинические особенности течения суставной формы ювенильного ревматоидного артрита

Критерии дифференциальной диагностики артритов у детей

ЛЕЧЕНИЕ. Основной целью лечебных воздействий при ЮРА является подавление активности и прогрессирования процесса, восстановления, по возможности, функций суставов и профилактика обострения. Главным принципом терапии является прежде всего применение комплекса лечебных средств, воздействующих на разные стороны патогенеза. Второй принцип — длительность и этапность лечения. И, наконец, третий принцип — дифференцированное лечение в зависимости от формы болезни, ее течения и активности. Основные направления лечения ЮРА складываются из применения медикаментозных препаратов, физиотерапии, ЛФК и санаторно-курортного лечения. Медикаментозное лечение больных ЮРА включает в себя применение противовоспалительных препаратов быстрого действия (нестероидные противовоспалительные препараты) и базисных препаратов (медленного действия), воздействующих на основные иммунные звенья патологического процесса (препараты золота, Д-пеницилламин, цитостатические иммунодепрессанты, хинолиновые производные и др.). Для лечения преимущественно суставной формы ЮРА применяют в основном нестероидные противовоспалительные препараты (НПВП), которые ингибируют активность простагландинсинтетазы и тем самым блокируют синтез простагландинов, очень важного фактора воспаления при ЮРА. Среди препаратов этой группы сохраняет значение ацетилсалициловая кислота, которую назначают по 0,2 г на год жизни или по 50—75 мг на 1 кг массы тела 4 раза в сутки, обязательно после еды. Она может применяться при ЮРА, но, учитывая, что в данной ситуации необходимо использовать препарат длительно, его применение нежелательно, поскольку он обладает определенными побочными эффектами. Главный из них — воздействие на пищеварительный канал (вплоть до язвообразования). Известны также такие эффекты, как появление шума в ушах, неприятные ощущения в голове, потливость. Поэтому практически при лечении ЮРА в настоящее время препарат используется редко. Более широкое применение в настоящее время получили производные индола. Они используются в виде препарата индометацина (метиндол, индоцид). Препарат (драже по 25 мг) применяется обычно в начальной дозе 1—3 мг на 1 кг в сутки 3—4 раза после еды. По своей активности индометацин является одним из самых активных НПВП, однако он тоже обладает определенным побочным действием на пищеварительный тракт, у некоторых больных он вызывает головные боли, может повышать артериальное давление, поскольку довольно активно подавляет синтез ПГ, являющихся депрессорными веществами. В настоящее время имеется препарат продленного действия — метиндолретард в таблетках по 75 мг. Наиболее эффективны при длительном применении производные уксусной кислоты. Это вольтарен и наш отечественный аналог — ортофен. Вольтарен назначают детям из расчета 2—3 мг на 1 кг в сутки. Преимущество вольтарена заключается в его лучшей переносимости, по активности он не превосходит индометацин. Другим достоинством вольтарена является наличие его в форме для парентерального введения. В настоящее время имеется препарат длительного действия — вольтарен-ретард по 100 мг в драже. Следующая группа — это производные пропионовой кислоты, куда входит бруфен (ибупрофен), напроксен (напросин) и флугалин (флюрбипрофен). Все они обладают меньшей противовоспалительной активностью, чем индометацин, но имеют минимальную токсичность. Бруфен применяют по 10—15 мг на 1 кг массы тела в сутки в 3—4 приема. Лечение ЮРА начинается с НПВП, потому что они производят быстрый противовоспалительный эффект. На процессы, лежащие в основе заболевания, на основные иммунологические изменения, которые происходят при ЮРА, они практически не влияют, поэтому, помимо противоспалительных препаратов, особенно если имеется тяжелая картина болезни, необходимо использовать так называемую базисную терапию. Применяя базисные препараты, прежде всего нужно учитывать медленное развитие лечебного эффекта. Важной особенностью их является возможность выраженного подавления клинических и лабораторных, в том числе иммунных, проявлений болезни. Третьей особенностью этих препаратов является замедление темпов деструкции суставов. Последнее важное свойство базисных препаратов — сохранение признаков улучшения и даже ремиссии в течение нескольких месяцев после отмены препарата. Это свойство объясняется кумулятивными свойствами этих лекарств. С одной стороны, конечно, очень хорошо, что и после отмены лекарство действует, но, с другой стороны, кумулятивность базисных лекарственных препаратов может давать нежелательный и серьезный побочный эффект. Больным преимущественно суставной формой ЮРА, при минимальной активности и медленно прогрессирующем течении, можно назначать хинолиновые производные (делагил, плаквенил). Делагил (хлорохин) назначают в суточной дозе 5 мг на 1 кг, плаквенил — до 8 мг на 1 кг, чаще всего — однократно на ночь после еды. Клинический эффект наступает, как правило, на 4-й неделе с начала применения, а максимальное действие — через 4—6 месяцев, поэтому препараты применяются длительно. Назначение хинолиновых препаратов требует систематического контроля окулиста, поскольку может развиваться ретинопатия. Из базисных лекарственных препаратов на первом месте по клиническому эффекту стоят препараты золота (кризанол, санокрезин, миокризин и др.). Кризанол представляет собой масляную взвесь кальциевой соли золота и содержит ! 7 мг металлического золота в 1 мл 10%-го раствора. Начинается лечение с первой инъекции в 10 мг 1 раз в неделю. При хорошей переносимости доза увеличивается, следующая, уже полная, доза — 17 мг, потом 34, 50 мг, и так при поддерживающей дозе 50 мг 1 раз в 2 недели или 1 раз в месяц, это лечение продолжается длительно, до года. Эффект наступает далеко не сразу, раньше 2—3 недель ожидать клинического улучшения нельзя, поэтому начинать самостоятельное лечение базисными препаратами нецелесообразно. Начинают его вместе с НПВП. Препараты золота у 30—40% больных ЮРА дают выраженные токсико-аллергические реакции. В процессе лечения могут наступать нарушения функции почек, печени, поэтому за больными, получающими эти препараты, необходим тщательный врачебный контроль. Учитывая серьезные побочные эффекты препаратов золота, их применение в педиатрической практике весьма ограничено. Следующим по эффективности из базисных препаратов можно поставить Б-пеницилламин (купренил, дистамин, троловол). Этот препарат воздействует на иммунокомпетентные клетки, снижает уровень РФ, уменьшает степень фиброзных изменений в тканях. Лечение начинают с небольшх доз — 150—300 мг в сутки, постепенно увеличивая дозу. Эффект от лечения наступает через 2—3 недели, продолжительность курса — несколько месяцев. Примерно такой же активностью обладают иммунодепрессанты, в частности, цитостатики. Обычно цитостатики используются в тех случаях, когда отсутствует эффект от перечисленных выше средств. Наиболее распространенным препаратом в лечении ЮРА в качестве базисного является хлорбуин (лейкеран), он менее токсичен, чем циклофосфамид, хотя тоже может давать неприятные осложнения. В частности, особенно остерегаются осложнений со стороны крови (цитопения). Необходимо помнить, что при длительном лечении этими препаратами может проявиться, правда, не всегда доказуемый эффект — канцерогенность. ' Особое место в терапии ЮРА занимают кортикостероиды, которые обладают выраженным противовоспалительным и иммуносупрессивным действием. К сожалению, кортикостероиды лишь временно подавляют активность процесса, вырабатывая гормональную зависимость. Кортикостероидная терапия показана лишь при наличии генерализованного суставного процесса и суставно-висцеральной форме ЮРА. При расчете на преднизолон доза кортикостероидов составляет 1 мг на 1 кг в сутки. Максимальная доза назначается на 4—6 недель с последующим переходом на поддерживающую дозу, которая составляет 1/3—1/4 максимальной дозы. При необходимости длительного применения кортикостероидов приходится считаться с их выраженным побочным действием. В особо тяжелых случаях (наличие висцеритов, максимальная активность процесса, резистентность к проводимой терапии) показана так называемая пульс-терапия с использованием сверхвысоких доз кортикостероидов. Для такой терапии используют метилпреднизолон (метипред), который в течение трех дней вводят внутривенно медленно (на 20—50 мл изотонического раствора натрия хлорида) в дозе 25—30 мг на 1 кг (но не более 1 г). Некоторые авторы рекомендуют в третьей инъекции вводить циклофосфамид в дозе 0,4 г на 1 кв. м поверхности тела. Важная роль в лечении ЮРА отводится методам местного воздействия на суставы. С этой целью чаще всего применяют аппликации диметилсульфоксида (ДМСО). Препарат назначают в виде аппликации 50%-го водного раствора (на дистиллированной или кипяченой воде) на пораженный сустав в течение 30—60 мин, ежедневно по 1—2 процедуры. Курс лечения — 10—20 аппликаций. ДМСО обладает противовоспалительными, противоотечными, антисептическими, спазмолитическими и антикоагулянтными свойствами. Под влиянием ДМСО снижается уровень простагландинов Е и F2, подавляется хемотаксис нейтрофилов, повышается фагоцитоз, улучшается микроциркуляция. Учитывая, что ДМСО является хорошим проводником лекарственных веществ, в раствор добавляют анальгин (из расчета 25 мг на 1 мл 50%-го раствора), новокаин и гепарин. Можно также добавлять индометациновую мазь. Кроме того, в качестве местного лечения используют внутрисуставное введение кортикостероидов. Наиболее широко применяют гидрокортизона ацетат, кеналог или метипред. Гидрокортизон обычно вводят в крупные суставы по 60—125 мг, в средние — по 50—75 мг, в мелкие — по 12—25 мг. Данный способ лечения приводит к быстрому и выраженному уменьшению симптомов синовита. В последнее время в качестве терапевтического метода используется химическая синовэктомия — введение в полость сустава веществ, оказывающих коагулирующее действие на синовиальную оболочку. У детей применяется преимущественно варикоцид, который вызывает поверхностный некроз синовиальной оболочки. Разнообразное лекарственное лечение проводится на фоне обязательных физиотерапевтических процедур; при уменьшении болевого синдрома необходима ЛФК, при снижении активности — санаторно-курортное лечение (Евпатория и др.).
В статье даны современные представления о ювенильном артрите, подробно изложены варианты течения, клиническая и инструментальная картина данного заболевания. Рассмотрены вопросы дифференциальной диагностики хронического синовита и полиартрита у детей.
The article contains current concepts about juvenile arthritis. Detailed description of the clinical course variants, clinical and instrumental picture of the disease was given. The issues of differential diagnosis of chronic synovitis and polyarthritis in children were also presented.
В настоящее время принято считать, что ювенильный идиопатический артрит (ЮИА) — это часто встречаемое хроническое воспалительное заболевание суставов у детей мультифакторной природы, которое характеризуется длительным прогрессирующим течением, приводящим к развитию контрактур и потере функции суставов. В основе заболевания лежит хронический прогрессирующий воспалительный процесс внутреннего слоя капсулы сустава (синовиальная оболочка), который приводит к деструкции хряща и костной ткани. Распространенность заболевания в различных странах составляет от 16 до 150 случаев на 100 000 населения. ЮИА достоверно встречается чаще таких известных заболеваний, как лейкемия, сахарный диабет, воспалительные заболевания кишечника [1, 11, 19].
Суставное поражение при полиартрите (более 5 суставов) кардинально отличается от олигоартрита и носит, как правило, симметричный характер с вовлечением суставов верхних и нижних конечностей, в том числе шейного отдела позвоночника и височно-челюстных суставов. Заболевание более характерно для девочек, однако встречаются тяжелые формы и среди мальчиков. Выделяют два пика заболевания: первый — от года до пяти лет, второй — от десяти до четырнадцати лет. Для детей раннего возраста наиболее характерен дебют с поражением одного-двух суставов, с быстрым вовлечением большего числа суставов в течение первых шести месяцев болезни. Первые проявления артрита могут быть не столь яркими, поэтому зачастую начало ЮИА несколько смазано. Одним из проявлений заболевания в этом возрасте может быть дактилит с последующим развитием картины полиартрита. Для данной подгруппы детей нехарактерно наличие ревматоидного фактора (РФ), однако степень суставного поражения остается не менее агрессивной, чем у взрослых с РФ+. При этом сохраняется риск поражения глаз, который тесно взаимосвязан с повышенным титром антинуклеарного фактора (АНФ). Для детей старшего возраста более характерно манифестное начало заболевания с поражением нескольких групп суставов одновременно. Чаще всего дебют полиартрита клинически проявляется артритом мелких суставов кистей или стоп, хотя в дальнейшем заболевание может иметь распространенную форму с вовлечением практически всех групп суставов, включая шейный отдел позвоночника и тазобедренные суставы. Именно данную подгруппу можно подразделить на два подтипа по наличию РФ. Некоторые дети данной подгруппы могут быть носителями гена HLADR4 и/или иметь антитела к циклическому цитруллинированному пептиду (анти-CCP), которые, как показали некоторые исследования, могут напрямую отражать степень агрессивности течения заболевания, однако доля таких детей крайне мала (менее 5%). При поражении шейного отдела позвоночника чаще всего развиваются передний атлантоаксиальный подвывих, эрозии зубовидного отростка, артрит С1-С2 и апофизарных суставов шейного отдела, что является отличительной чертой данной патологии [8, 9, 12].
Системный артрит может не иметь стойкого суставного синдрома или картины олиго-полиартрита, а проявляется гектической лихорадкой, кожным синдромом, лимфаденопатией, полисерозитом и гепатоспленомегалией. Системный воспалительный процесс протекает с крайне высокой степенью лабораторной активности в виде лейкоцитоза, тромбоцитоза, повышения уровня трансаминаз, прогрессирующей анемии, значительного ускорения СОЭ, высокого уровня СРБ, диспротеинемии. Суставной синдром в дебюте может ограничиваться артралгиями или интермиттирующим экссудативным артритом суставов верхних или нижних конечностей. Стойкий артрит может развиваться через несколько месяцев от начала заболевания или даже по истечении одного-двух лет болезни. Нередко встречается бессимптомное вовлечение тазобедренных, височно-челюстных суставов и суставов шейного отдела позвоночника с развитием множественного артроза. При длительном сроке болезни большинство детей, как правило, имеют полиартрит и двусторонний асептический некроз головок бедренных костей. Одним из главных жизнеугрожающих осложнений системного артрита является развитие картины синдрома макрофагальной активации (МАС). Данное осложнение встречается с частотой 6,7–13%, а смертность составляет по данным разных источников до 22%. В основе данного осложнения лежит неконтролируемая активация макрофагов и Т-лимфоцитов с системной гиперпродукцией цитокинов, которая клинически проявляется панцитопенией, печеночной недостаточностью, коагулопатией и неврологической симптоматикой [10, 24, 26].
Кроме классификации ювенильного артрита по числу пораженных суставов, с целью определения варианта течения и прогнозирования исхода заболевания применяют также и другие предложенные критерии: определение стадии анатомических изменений, функциональных нарушений и степени лабораторной (воспалительной) активности.
На сегодняшний день скрининг инструментальной диагностики суставной патологии включает рентгенографическое исследование и ультразвуковое сканирование. Первичная оценка полученных данных инструментального обследования и сопоставление их с клинической картиной являются одной из основных задач лечащего врача. Однако, в связи с многочисленностью нозологических форм суставной патологии, специалистам в области ортопедии и ревматологии все чаще и чаще приходится прибегать к дополнительным методам обследования. Наибольшую популярность и диагностическую значимость среди специалистов имеют магнитно-резонансная и компьютерная томографии, артрография, трехфазная остеосцинтиграфия и диагностическая артроскопия с биопсией синовиальной оболочки. Однако доступность и коммерческая составляющая данных видов исследований ограничивают их применение в амбулаторном звене, к тому же диагностическая артроскопия — это полноценное оперативное вмешательство. Поэтому первичная оценка характера суставного поражения должна быть основана на простых и дешевых инструментальных методах, таких как рентгенография и ультразвуковое сканирование, при оценке которых врачом должны быть четко определены цели и методы дополнительной диагностики.
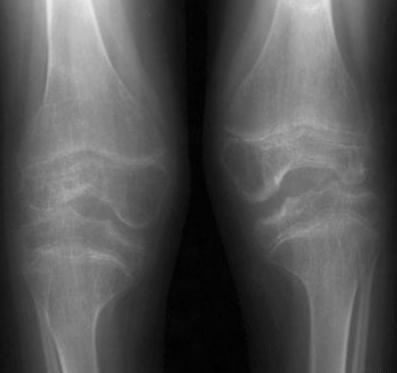
Как известно, ЮИА — это хроническое воспалительное заболевание синовиальной оболочки, распространяющееся на все структуры сустава, в том числе костную и хрящевую ткани. Инструментальная диагностика основана на методах визуализации характерных признаков хронического воспалительного процесса, при оценке которых должен учитываться существующий ряд анатомо-физиологических особенностей костной и хрящевой тканей у детей. Рентгеновское изображение костей и суставов детей отличается от изображения их у взрослых целым рядом особенностей, которые характеризуются непрерывными этапами энхондрального костеобразования, что определяет видоизменения формы и контура определенной части костей, собственно структуры костной ткани. Реакция костной ткани у детей на течение хронического воспалительного процесса характеризуется быстрым развитием остеопороза, асимметрией и неравномерностью оссификации хрящевых моделей, а также ускоренным ростом эпифизов, образующих сустав. Нередким является образование очагов дистрофии костной ткани, участков асептического некроза. Специфические изменения костной ткани суставов, подверженных РА, позволили Штейнброкеру в 1988 г. систематизировать данные рентгеновской картины и представить их как стадии анатомических изменений, которые также нашли широкое применение в детской практике:
- I стадия. Эпифизарный остеопороз, уплотнение периартикулярных мягких тканей, ускорение роста эпифизов пораженных суставов.
- II стадия.Те же изменения плюс сужение суставной щели, единичные костные узуры (эрозии).
- III стадия. Распространенный остеопороз, выраженная костно-хрящевая деструкция, вывихи, подвывихи, системное нарушение роста костей.
- IV стадия. Изменения, присущие I–III стадии и фиброзный, костный анкилоз.
Спектр дифференциальной диагностики моно-, олигоартрита у детей представлен в табл. 2 и 4.
.jpg)
Диагностика и лечение гнойно-воспалительных заболеваний скелета у детей остаются весьма актуальными проблемами, в частности, для педиатрии и детской хирургии. Зачастую остеомиелит, равно как септический артрит, в ранние сроки у детей может представлять собой труднодиагностируемую патологию, несмотря на широкой спектр методов визуализации. За последнее десятилетие отмечено увеличение количества заболеваний с атипичными и тяжелыми формами, что нередко приводит к развитию осложнений и росту инвалидизации. Кроме того, характер клинического течения и инструментальные признаки остеомиелита имеют свои особенности у детей в зависимости от возраста. Считается, что остеомиелит — это воспаление костного мозга и прилегающей костной ткани локального или распространенного характера с формированием некротического очага — секвестра. В некоторых странах остеомиелит встречается с частотой от 2 до 13 на 100 000 детей, частота септического артрита в 2–3 раза реже. Остеомиелит может быть острый или хронический, по природе инфекционного агента — специфический или неспецифический, по пути проникновения — экзогенный или эндогенный. Для острого остеомиелита характерно развитие очага некроза кости в зонах, богатых кровоснабжением, с густой сетью анастомозов — это области метафизов и эпифизов. Для детей до двухлетнего возраста, исключая новорожденных, более характерна эпифизарная форма остеомиелита с картиной септицемии, в то время как для детей старшего возраста — метафизарная форма, течение которого может иметь локальную форму. Ранняя рентгенологическая картина формирования очага некроза наблюдаются у детей с 3-го по 10-й день от начала заболевания. Хронический остеомиелит у детей, как правило, является следствием нелеченного острого остеомиелита или возникает вторично на участках измененной костной ткани. Однако большую роль в возникновении хронического остеомиелита играют изменения иммунного гомеостаза и средовые факторы. Наиболее часто мишенью хронического остеомиелита являются длинные трубчатые кости.
Диагностика остеолитической патологии нередко представляет собой трудности в случаях вялотекущего характера течения воспалительного процесса в связи с полиморфизмом клинико-инструментальной картины. Использование спиральной компьютерной томографии, магнитно-резонансной томографии, трехфазной остеосцинтиграфии не всегда позволяет поставить правильный диагноз, поэтому в некоторых случаях биопсия фокуса имеет решающее значение (рис. 1).
Окончание статьи читайте в следующем номере.
А. Н. Кожевников*, 1, кандидат медицинских наук
Н. А. Поздеева*, кандидат медицинских наук
М. А. Конев*
В. В. Селизов*
А. В. Москаленко*
К. А. Афоничев*, доктор медицинских наук
Г. А. Новик**, доктор медицинских наук, профессор
* ФГБУ НИДОИ им. Г. И. Турнера МЗ РФ, Санкт-Петербург
** ГБОУ ВПО СпбГМПУ МЗ РФ, Санкт-Петербург
Читайте также:


