Заболевание легких при системной красной волчанке
Рассмотрены вопросы поражения легких при системной красной волчанке, ревматоидном артрите, системной склеродермии, полимиозите/дерматомиозите, синдроме Шегрена, смешанном заболевании соединительной ткани, гранулематозе Вегенера, синдроме Черджа–Стросса, с
Aspects of lungs lesion with exanthematous lupus erythematosus, rheumatoid arthritis, Addison’s keloid, polymyositis/dermatomyositis, Sj?gren’s sicca syndrome, mixed connective tissue disease, necrotizing respiratory granulomatosis, Churg–Strauss syndrome, Goodpasture’s syndrome and Bechterew’s disease have been analysed.
В основе поражения легких (ПЛ) при системных аутоиммунных заболеваниях (САЗ) лежат расстройства механизмов иммунорегуляции и гиперреактивность организма. Макрофаги и лимфоциты являются ключевыми клетками, участвующими в инициации и сохранении иммунного ответа в легких. Альвеолярные макрофаги — резиденты легочной ткани — поглощают чужеродные агенты, проникшие через слизистые поверхности легких и бронхов. Кроме того, эти клетки служат в качестве антигенпредставляющих клеток для Т-лимфоцитов. Относительно небольшое число лимфоцитов присутствуют в нормальной паренхиме легких. Однако после стимуляции соответствующим антигеном окружающей лимфоидной ткани лимфоциты мигрируют в легкие и принимают участие в воспалительной реакции.
Проведение специальных исследований, включавших компьютерную томографию высокого разрешения (КТВР) и биопсию легкого, выявило, что при САЗ встречаются различные гистологические формы поражения интерстиция легких (табл.).
Системная красная волчанка (СКВ) — системное аутоиммунное заболевание неизвестной этиологии, характеризующееся гиперпродукцией органоспецифических аутоантител к различным компонентам клеточного ядра с развитием иммуновоспалительного повреждения тканей и внутренних органов.
Ревматоидный артрит (РА) — системное аутоиммунное заболевание соединительной ткани с преимущественным поражением суставов по типу хронического прогрессирующего эрозивно-деструктивного полиартрита и внесуставными проявлениями.
ПЛ при РА было впервые описано в 1948 г., когда Эллман и Болл установили диффузный фиброз легких у трех пациентов. Легочные проявления при РА включают поражение плевры, образование ревматоидных узелков в легких, ИПЛ, легочный васкулит, альвеолярные кровоизлияния, бронхообструктивные изменения. Почти у половины больных РА при вскрытии выявляется плеврит. Экссудативный плеврит может быть односторонним или двусторонним и сохраняться в течение многих месяцев. Наличие плеврального выпота вызывает нарушение легочной функции. Как правило, плевральная жидкость бывает экссудативной с низким содержанием глюкозы и низким уровнем комплемента. Чаще у пациентов с РА встречается сухой плеврит и является находкой при рентгенологическом исследовании.
Ревматоидные узелки (РУ), как единичные, так и множественные, могут быть обнаружены в легочной паренхиме больных РА. РУ легких у пациентов с РА были впервые описаны Каплан в 1953 г. РУ могут появиться до, во время или после начала РА. ИПЛ характеризуется хроническим воспалением стенок альвеол и скоплением больших мононуклеарных клеток в альвеолах. Довольно часто у больных РА встречается сочетание ИПЛ и подкожных ревматоидных узелков. Прогноз для пациентов с РА с ИПЛ неблагоприятен. Легочный васкулит является одним из редких легочных проявлений РА. Альвеолярные кровоизлияния, не часто встречающиеся у больных РА, приводят к кровохарканью и анемии. У пациентов с РА отмечается высокая частота поражения бронхов. ПЛ может быть результатом токсического воздействия препаратов, используемых в терапии РА. Для того чтобы обеспечить оптимальный эффект от лечения, врач всегда должен учитывать возможную легочную патологию при оценке состояния пациентов с РА [1–3].
Системная склеродермия (ССД) — диффузное заболевание соединительной ткани с прогрессирующим фиброзом, распространенными вазоспастическими нарушениями и характерными изменениями кожи, опорно-двигательного аппарата и внутренних органов. Среди висцеральных проявлений ССД ПЛ занимает важное место.
Плеврит при ССД наблюдается реже, чем при РА и СКВ. В то же время у больных ССД значительно выше частота ИПЛ, при этом морфологическое исследование показывает выраженный фиброз интерстициальной ткани и утолщение межальвеолярных перегородок. Исследование функции внешнего дыхания (ФВД) демонстрирует снижение диффузионной способности легких (ДСЛ) даже при отсутствии каких-либо клинических симптомов и рентгенологических изменений.
У пациентов с ССД выявляется рестриктивный тип нарушения вентиляции легких. У большинства больных ССД с ЛФ наблюдается гистологическая картина обычной интерстициальной пневмонии (ОИП), однако во многих случаях встречается гистопатологический тип неспецифической интерстициальной пневмонии (НИП).
Развитие ЛФ инициируется микрососудистыми изменениями, которые приводят к повреждению эндотелиальных клеток и поражению альвеолярного эпителия. Это приводит к активации каскада свертывания (рис.).
Экспрессия аутоантител является предиктором поражения внутренних органов, в частности ПЛ. Наличие антител к Scl-70 (антисклеродермальные антитела с молекулярной массой 70 кДа, антитела к топоизомеразе I) в значительной степени является фактором риска развития ИПЛ, в то время как антицентромерные антитела (АЦА) говорят о низкой вероятности развития рентгенологических признаков ЛФ.
У пациентов с ССД встречается легочная гипертензия (ЛГ). ЛГ может быть изолированной, возникшей вследствие поражения сосудов, или вторичной — при поражении паренхимы легких или левых отделов сердца. ЛГ развивается у 5–7% больных, чаще на поздних стадиях лимитированной формы ССД. Предиктор ЛГ — изолированное уменьшение ДСЛ. Более редко встречаются аспирационная пневмония, причиной которой является дисфункция пищевода, а также спонтанный пневмоторакс, лекарственный пневмонит [1–3, 6–8].
Полимиозит/дерматомиозит (ПМ/ДМ) — группа хронических диффузных заболеваний поперечнополосатой мускулатуры, основным проявлением которых выступает мышечная слабость.
Около 40% пациентов с ПМ/ДМ имеют патологию легочной системы. Одной из причин этого является поражение мышц. Поражение межреберных мышц и высокое стояние диафрагмы приводят к уменьшению экскурсии грудной клетки и появлению вентиляционных нарушений по рестриктивному типу. В отличие от других САЗ, ПЛ при ПМ/ДМ не затрагивает в первую очередь дыхательные пути или плевру. Наиболее распространенной патологией является аспирационная пневмония, которая возникает по причине слабости мышц глотки и верхней трети пищевода.
Болезнь Шегрена (БШ) — системное аутоиммунное заболевание неизвестной этиологии, характеризуется поражением секретирующих эпителиальных желез, с вовлечением преимущественно слюнных и слезных желез (ксеростомия, ксерофтальмия).
Поражение экзокринных желез верхних дыхательных путей часто приводит к сухости носовых ходов и бронхов. Наиболее распространенным проявлением ПЛ, связанным с БШ, является лимфоцитарный пневмонит, поражающий нижние доли. У пациентов с БШ может развиться плеврит (с или без выпота), ИПЛ с очагами лимфоидной инфильтрации. При развитии неходжкинских лимфом метастатические поражения легких встречаются часто, реже наблюдают формирование MALT-ткани (mucosal-associated lymphoid tissue) с развитием первичной MALT-лимфомы [1–3, 12, 13].
Смешанное заболевание соединительной ткани (синдром Шарпа) (CЗСТ) — аутоиммунное заболевание, характеризующееся наличием отдельных признаков СКВ, ССД, РА, ПМ/ДМ в сочетании с высоким титром антител к экстрагируемому ядерному антигену — U1-RNP.
ИПЛ и ЛГ довольно часто встречаются у больных с СЗСТ, при этом нередко имеют субклиническое течение. Обследование пациентов с СЗСТ показало повышение уровня иммунных комплексов (ИК) и увеличение потребления комплемента. ИК-опосредованное повреждение альвеолярно-капиллярной мембраны и легочной ткани может играть важную роль в патогенезе ИПЛ при СЗСТ. При исследовании показателей функции внешнего дыхания больные с СЗСТ демонстрируют снижение диффузионной способности легких (ДСЛ) и рестриктивный тип нарушения вентиляции. Прогноз ИПЛ у пациентов с СЗСТ более благоприятный, чем при РА и ССД. ЛГ является основной причиной смерти больных с СЗСТ [1–3, 14, 15].
Гранулематоз Вегенера (ГВ) — системный некротический васкулит мелких вен и артерий с образованием гранулем в сосудистых стенках и окружающих тканях дыхательных путей, почек и других органов.
ПЛ развивается у большинства пациентов с ГВ. Клинические проявления ПЛ при ГВ разнообразны, начиная от бессимптомных узелков в легких и кончая фульминантным альвеолярным кровотечением. ГВ может сопровождаться образованием опухолевидных инфильтратов с неровными краями, которые могут распадаться и образовывать полости. Плеврит, легочное кровотечение и увеличение лимфатических узлов средостения встречаются редко. Поражение трахеальных или бронхиальных стенок обычно проявляется гранулематозным утолщением слизистой оболочки или подслизистого слоя, при этом возникает обструктивный тип нарушения вентиляции легких. Частое осложнение — коллапс бронхов и постобструктивная пневмония. Инфильтраты, которые могут увеличиваться и уменьшаться, первоначально часто неправильно диагностируются как пневмония. Примерно в 20% случаев развивается прогрессирующая легочная недостаточность, связанная с ЛФ, пневмонией или пневмонитом, индуцированным циклофосфамидом. ДСЛ, как правило, уменьшена, но при развитии диффузных альвеолярных геморрагий наблюдают ее рост. Описаны случаи развития бронхоплевральных свищей [1–3].
Синдром Чарджа–Строса (СЧС) — эозинофильное, гранулематозное воспаление респираторного тракта и некротизирующий васкулит, поражающий мелкие и средние сосуды, часто сочетающийся с астмой и эозинофилией.
Легкие — это наиболее поражаемый орган при данном синдроме; более 90% пациентов с синдромом СЧС в анамнезе имеют астму. При рентгенологическом исследовании легких выявляются очаги консолидации, распределяющиеся по периферии, которые часто бывают преходящими. Могут появляться узелки, при распаде не образующие полости. Другие менее распространенные проявления ПЛ включают утолщение междольковой перегородки и утолщение бронхиальной стенки. Плевральные выпоты образуются редко.
Существуют три фазы развития СЧС: продромальная фаза, которая характеризуется наличием аллергических заболеваний (как правило, астма или аллергический ринит), может продолжаться от нескольких месяцев до многих лет; эозинофилия/фаза инфильтрации тканей, в которой может наблюдаться удивительно высокая периферическая эозинофилия, а также инфильтрация эозинофилами тканей легких, желудочно-кишечного тракта и других органов; васкулитная фаза, в которой некротический васкулит поражает широкий спектр органов — сердце, легкие, периферические нервы и кожу. Диагноз приходится верифицировать с другими васкулитами, в первую очередь ГВ [1–3].
Синдром Гудпасчера (СГ) (геморрагический легочно-почечный синдром) — прогрессирующее аутоиммунное заболевание легких и почек, характеризующееся образованием антител к базальным мембранам капилляров клубочков почек и альвеол и проявляющееся сочетанием легочных и почечных геморрагий.
Патоморфологически в легких наблюдается картина венулитов, артериолитов, капилляритов с выраженными явлениями деструкции и пролиферации; поражение капилляров наблюдается преимущественно в межальвеолярных перегородках, развивается альвеолит с геморрагическим экссудатом в альвеолах.
В большинстве случаев ПЛ и почек происходит одновременно. Клинические проявления ПЛ включают в себя кашель, одышку и кровохарканье, которое может появляться на несколько месяцев раньше признаков поражения почек. В развитии альвеолита при СГ огромное значение имеет активация альвеолярных макрофагов. В активированном состоянии они выделяют около 40 цитокинов. Цитокины I группы (хемотаксины, лейкотриены, интерлейкин-8) усиливают поступление полиморфноядерных лейкоцитов в легкие. Цитокины II группы (факторы роста — тромбоцитарный, макрофагальный) способствуют перемещению в легкие фибробластов. Альвеолярные макрофаги продуцируют также активные формы кислорода, протеазы, повреждающие легочную ткань.
Исследование жидкости бронхоальвеолярного лаважа (ЖБАЛ) не является диагностическим при СГ, но может использоваться для подтверждения наличия диффузной альвеолярной геморрагии у пациентов с гломерулонефритом и легочными инфильтратами, но без кровохарканья. ЖБАЛ, которая остается геморрагической после многократных промываний, позволяет подтвердить диффузный геморрагический синдром, особенно при сопутствующем снижении гематокрита.
Гистологическое и иммунологическое исследование биоптатов легочной ткани при СГ характеризуется признаками геморрагического альвеолита, гемосидероза и интерстициального фиброза, а также линейных отложений иммуноглобулина G (IgG) и С3-компонента комплемента на базальных мембранах легочных альвеол.
Рентгено-компьютерное исследование легких при СГ демонстрирует наличие легочных инфильтратов в прикорневой области с распространением на нижние и средние отделы легких. Исследование легочных тестов выявляет рестриктивный тип нарушения вентиляции легких (снижение жизненной емкости легких — ЖЕЛ), но по мере прогрессирования заболевания присоединяются обструктивные изменения (снижение объема форсированного выдоха за 1 сек — ОФВ1, индекса Тиффно) [1–3].
Болезнь Бехтерева (ББ, анкилозирующий спондилит, АС) — хроническое системное заболевание, характеризующееся воспалительным поражением суставов позвоночника, околопозвоночных тканей и крестцово-подвздошных сочленений с анкилозированием межпозвоночных суставов и развитием кальцификации спинальных связок.
ПЛ у больных АС встречается в 50–85% случаев и обусловлено анкилозирующим процессом в грудном отделе позвоночника, снижением дыхательной экскурсий грудной клетки, утомлением и слабостью дыхательных мышц. У больных АС чаще всего развивается эмфизема легких, затем ИПЛ, хроническая обструктивная болезнь легких (ХОБЛ), апикальный фиброз, бронхоэктазия и поражение плевры. Апикальный пневмофиброз, который встречается нечасто (3–4%), требует проведения дифференциальной диагностики с туберкулезными изменениями. Фиброз верхней доли легкого обычно протекает бессимптомно, но может вызывать кашель, отделение мокроты и одышку.
При АС чаще встречается рестриктивный тип нарушения вентиляции легких. У больных АС с хронической обструктивной болезнью легких (ХОБЛ) исследование ФВД демонстрирует обструктивные вентиляционные изменения [1, 16, 17].
Таким образом, при САЗ могут наблюдаться различные типы легочной патологии. Развитие ПЛ обусловлено особенностями патофизиологических характеристик основного заболевания. Основные легочные проявления САЗ включают заболевания плевры, ИПЛ, поражение бронхиального дерева. При РА и СКВ чаще, чем при других САЗ, встречается поражение плевры. ИПЛ в настоящее время все больше признается как самое частое и серьезное проявление САЗ. ПЛ у больных с САЗ оказывает существенное негативное воздействие на качество жизни (КЖ): у больных снижаются показатели КЖ, характеризующие физический, психоэмоциональный статус и социальную активность.
ПЛ при САЗ имеет большое значение в формировании облика заболевания, при этом во многом определяет его тяжесть и прогноз. Наряду с базисной терапией САЗ, ПЛ необходимо рассматривать как важную мишень для терапевтического воздействия.
Литература
- Ревматология, национальное руководство. Под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008.
- Castelino F. V., Varga J. Interstitial lung disease in connective tissue diseases: evolving concepts of pathogenesis and management // Arthritis Research & Therapy. 2010; 12: 213.
- Bouros D., Pneumatikos I., Tzouvelekis A. Pleural involvement in systemic autoimmune disorders // Respiration. 2008; 75: 361–371.
- Kriegel M. A., Van Beek C., Mostaghimi A. et al. Sterile empyematous pleural effusion in a patient with systemic lupus erythematosus: a diagnostic challenge // Lupus. 2009; 18: 581–585.
- Pego-Reigosa J. M., Medeiros D. A., Osenberg D. A. Respiratory manifestations of systemic lupus erythematosus: old and new concepts // Best Pract Res Clin Rheumatol. 2009; 23: 460–480.
- Varda J., Abraham D. Systemic sclerosis: a prototypic multisystem fibrotic disorder // J Clin Invest. 2007; 117: 557–567.
- Yanaba K., Hasegawa M., Takehara K. et al. Comparative study of serum surfactant protein-D and KL-6 concentrations in patients with systemic sclerosis as markers for monitoring the activity of pulmonary fibrosis // J Rheumatol. 2004; 31: 1112–1120.
- McNearney T. A., Revelle J. D., Fischbach M. et al. Pulmonary involvement in systemic sclerosis: associations with genetic, serologic, sociodemographic, and behavioral factors // Arthritis Rheum. 2007; 57: 318–326.
- Tillie-Leblond I., Wislez M., Valeyre D. et al. Interstitial lung disease and anti-Jo-1 antibodies: difference between acute and gradual onset // Thorax. 2008; 63: 53–59.
- Chen I. J., Jan Wu Y. J., Lin C. W. et al. Interstitial lung disease in polymyositis and dermatomyositis // Clin Rheumatol. 2009; 28: 639–646.
- Fujisawa T., Suda T., Nakamura Y. et al. Differences in clinical features and prognosis of interstitial lung diseases between polymyositis and dermatomyositis // J Rheumatol. 2005; 32: 58–64.
- Ito I., Nagai S., Kitaichi M. et al. Pulmonary manifestations of primary Sjögren’s syndrome: a clinical, radiologic, and pathologic study // Am J Respir Crit Care Med. 2005; 171: 632–638.
- Parambil J. G., Myers J. L., Lindell R. M. et al. Interstitial lung disease in primary Sjögren’s syndrome // Chest. 2006; 130: 1489–1495.
- Bodolay E., Szekanecz Z., Devenyi K. et al. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. 2005; 44: 656–661.
- Kinder B. W., Shariat C., Collard H. R. et al. Undifferentiated connective tissue disease-associated interstitial lung disease: changes in lung function // Lung 2010; 188: 143–149
- Quismorio F. P. Jr. Pulmonary involvement in ankylosing spondylitis // Curr Opin Pulm Med. 2006; 12: 342–345.
- Lee C. C., Lee S. H., Chang I. J. et al. Spontaneous pneumothorax associated with ankylosis spondylitis // Rheumatol. 2005; 44: 1538–1541.
Д. В. Бестаев 1 , кандидат медицинских наук
Е. Л. Насонов, доктор медицинских наук, профессор, академик РАН
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
Системная красная волчанка
Системная красная волчанка
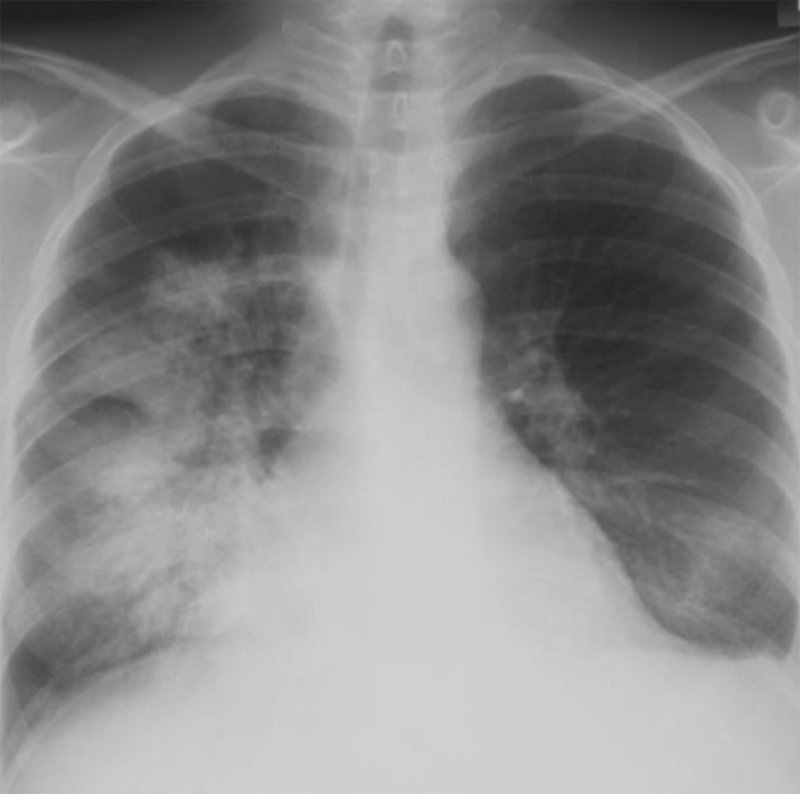
Рисунок 1. Поражение легких при системной красной волчанке. На рентгенограмме, выполненной у больного с кровохарканьем, обусловленного обширным легочным кровотечением, в прикорневой зоне и среднем легочном поле справа определяется высокоинтенсивная, нечетко ограниченная инфильтрация, также в нижней доле слева визуализируется начальная инфильтрация. Слева отмечается небольшой плевральный выпот
Ревматоидный артрит
Системная склеродермия
Гранулематоз Вегенера
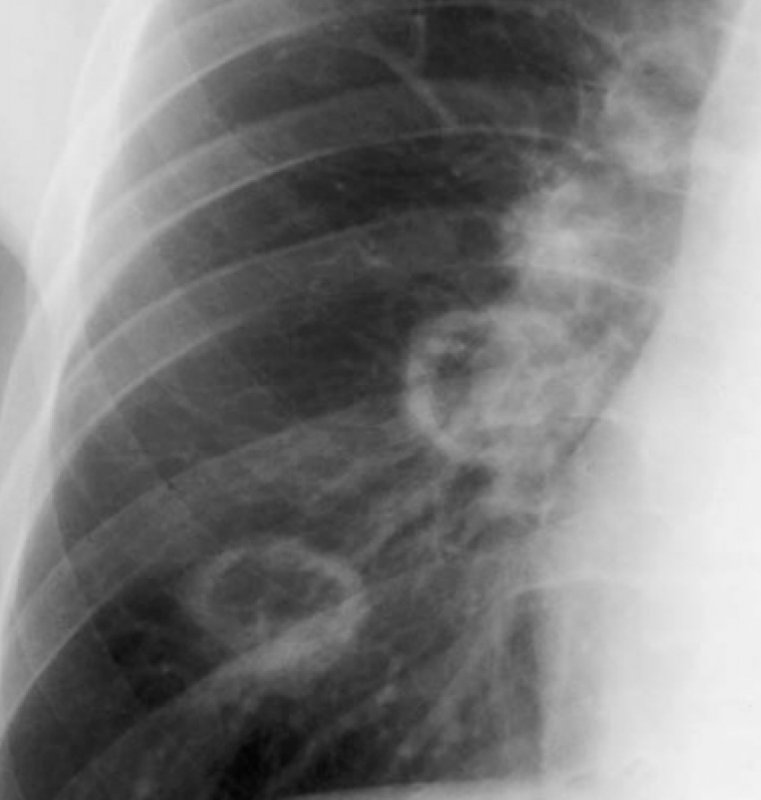
Гранулематоз Вегенера – системный некротизирующий васкулит, при котором происходит поражение верхних дыхательных путей с развитием изъязвлений (стоматит, трахеит, синусит, ринит), также возникает гломерулонефрит. На рентгенограмме легких могут обнаруживаться множественные инфильтраты неправильной округлой формы, размером до нескольких сантиметров. По мере развития заболевания в инфильтратах происходит распад – на их месте формируются тонкостенные полости (рисунок 2). При гранулематозе Вегенера могут возникать легочные кровотечения (на рентгенограмме в легких отмечаются инфильтративные изменения, как правило распространенные и двусторонние).
Гранулематоз Вегенера
Рисунок 2. Гранулематоз Вегенера (увеличенный фрагмент рентгенограммы в прямой проекции – нижнее правое легочное поле). На фоне тени правого корня определяются 4 полостных образования в легком
Анкилозирующий спондилоартрит (Болезнь Бехтерева)
Синдром Чарга-Стросса
Синдром Гудпасчера
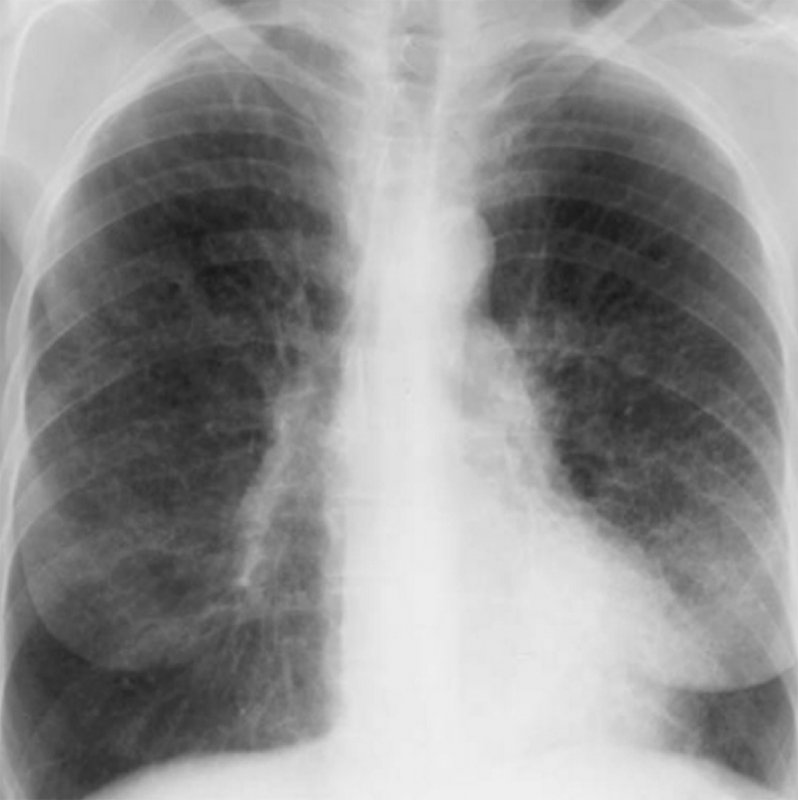
Синдром Гудпасчера – системный капиллярит, характеризующийся преимущественным поражением базальных мембран гломерулярного аппарата по типу гломерулонефрита (с гематурией) и альвеол легких по типу геморрагического пневмонита (с легочными кровотечениями). Рентгенологическая картина характеризуется появлением участков альвеолярной инфильтрации в легких. На рисунке 3 продемонстрированы интерстициальные изменения в легких, характерные для этой патологии.
Синдром Гудпасчера
Рисунок 3. Синдром Гудпасчера: Интерстициальные изменения в легких. Усиление интерстициального компонента легочного рисунка с обеих сторон, определяются ретикулярные и множественные мелкоочаговые тени. Изменения наиболее выражены в нижних и средних отделах легочных полей
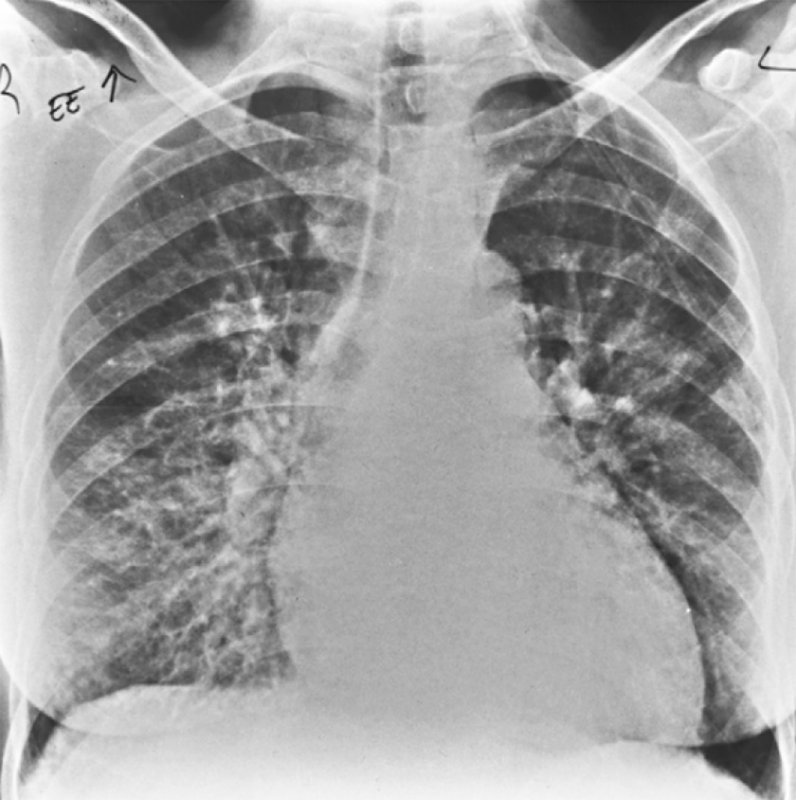
Острый пневмонит
Рисунок 4. Острый пневмонит при системной красной волчанке. В нижнем и среднем отделе правого легкого определяется усиление рисунка с образованием ретикулярных теней и неоднородной инфильтрации. Гистологическое исследование биоптата показало васкулит и кровоизлияние
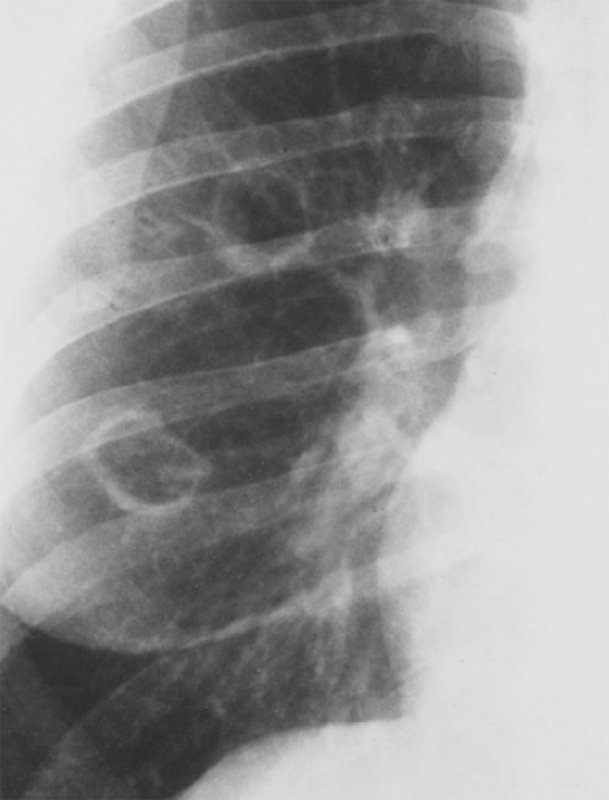
Ревматоидные узелки в легких
Рисунок 5. Ревматоидные узелки. Увеличенный фрагмент рентгенограммы в прямой проекции – правое легочное поле. На снимке определяются 2 полостных образования в легком
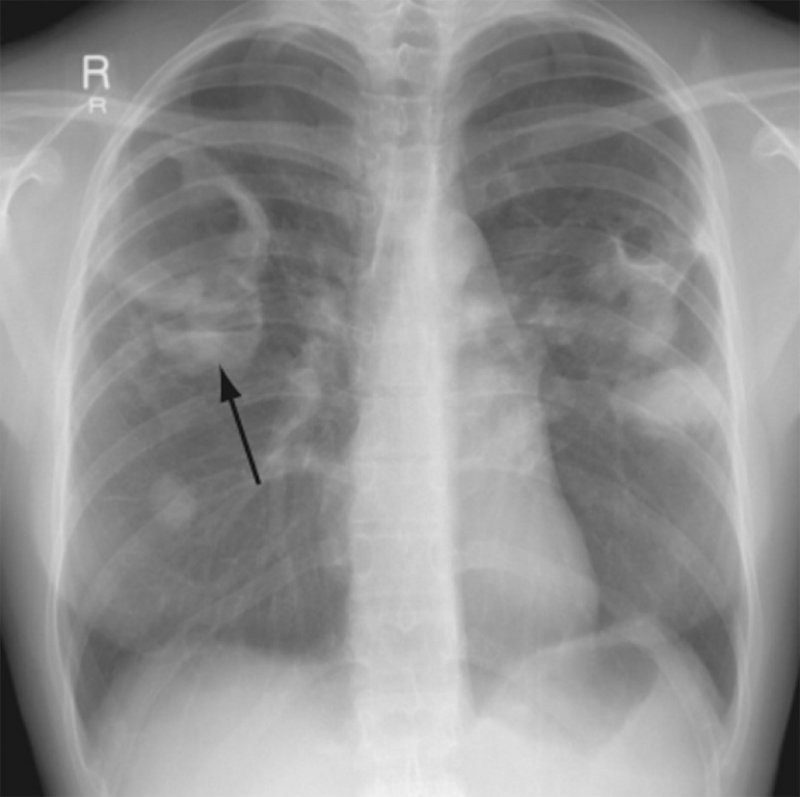
Гранулематоз Вегенера
Рисунок 6. Гранулематоз Вегенера. В обоих легких определяются множественные новообразования. В наиболее крупных образованиях видны полости с утолщенными стенками, а в образованиях среднего размера визуализируется уровень содержимого жидкость/газ
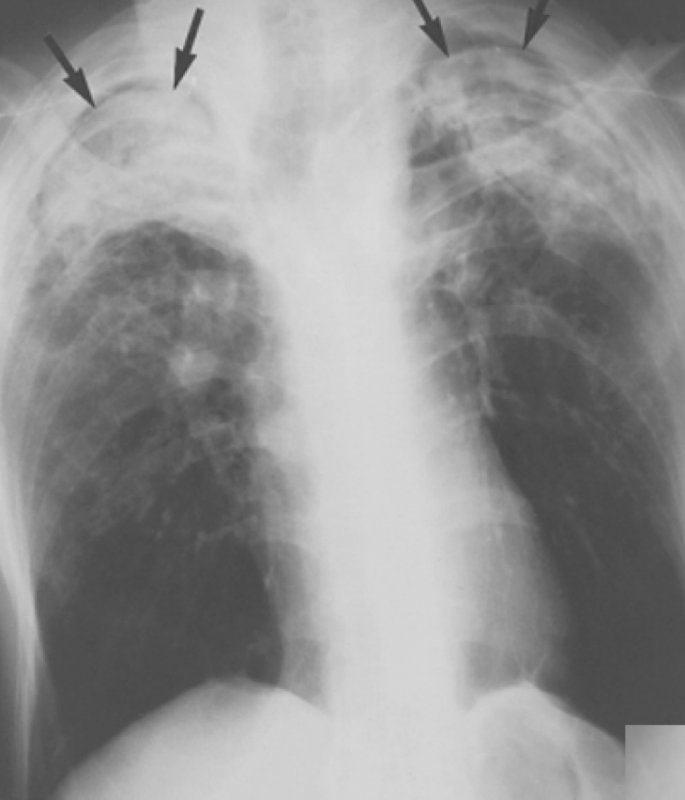
Полости в легких с мицетомами
Поражение легких
В 50—80% случаев при СКВ наблюдается сухой или выпотной плеврит. Больных беспокоят боль в грудной клетке, небольшой сухой кашель, одышка. При небольшом количестве выпота плеврит может протекать незаметно и лишь при рентгенологическом исследовании выявляют утолщение плевры или жидкость в плевральных полостях обычно с обеих сторон, приподнятость диафрагмы. Наблюдается и довольно массивный выпот, достигающий 1—2 л.
Описаны случаи СКВ, когда выпот с обеих сторон достигал III ребра и по жизненным показаниям приходилось проводить повторные пункции. Неадекватное лечение обычно приводит к образованию массивных спаек и облитерации плевральных полостей, что в дальнейшем резко снижает жизненную способность легких. Из-за массивных спаек диафрагма деформируется, снижается ее тонус, она подтягивается вверх с образованием высокого стояния с обеих сторон, но чаще справа.
Плеврит при волчанке — важный диагностический признак, так же как и подтянутая диафрагма. В выпоте можно обнаружить LE-клетки, низкий уровень комплемента и высокое содержание иммуноглобулинов. По составу выпот представляет собой экссудат, содержащий более 3% белка, 0,55% глюкозы. При патологоанатомическом исследовании практически у всех больных находят признаки спаечного плеврита, значительное утолщение плевры. Микроскопически в плевре выявляют скопления макрофагов и лимфоцитов. В отдельных случаях возможен периваскулярный фибриноидный некроз с нейтрофильной и мононуклеарной инфильтрацией.
Поражение легких при СКВ — проявление классического васкулита, хотя непосредственно легочный васкулит довольно редкая патология, встречается в небольшом проценте случаев. N. Rothfield (1983) наблюдала легочный васкулит у 2% больных и всегда в сочетании с артериитом почечных сосудов и сосудов желудочно-кишечного тракта.
Люпус-пневмонит развивается обычно в период обострения СКВ с вовлечением в процесс других органов и систем. Клиническая картина скудна, нередко ограничивается выраженной одышкой, болью в грудной клетке, сухим кашлем у 50% больных. Редко отмечается кровохарканье. Рентгенологически характерно диффузное усиление легочного рисунка. Образование инфильтратов в легких не столь часто. Высокое стояние диафрагмы, обусловленное наличием плевро-диафрагмальных сращений и собственно легочным процессом, составляет важный рентгенологический диагностический признак люпус-пневмонита (рис. 4.12). Жизненная емкость легких у таких больных значительно снижена, выявляются признаки гипоксемии.

Рис. 4.12. Волчаночный пневмонит, дисковидный ателектаз над правым куполом диафрагмы.
При сканировании иногда определяются кистевидные образования в нижних отделах легких. При высокой лихорадке, кашле с мокротой необходимо проводить дифференциальную диагностику с разнообразной вторичной инфекцией (бактериальной, вирусной, грибковой). Наиболее затруднительна диагностика с туберкулезом, особенно у больных, длительно леченных кортикостероидами.
В ряде случаев приходится проводить чрезбронхиальную биопсию. В диагностике может помочь также проведение кожных тестов, исследование полученного плеврального экссудата.
Поражение сердца и сосудов
Наиболее часто при СКВ наблюдается перикардит. Перикард, по данным разных авторов, вовлекается в процесс в 25—51% случаев [Насонова В. А., 1972;
Иванова М. М., 1985; Dubois E., 1964]. Характерен сухой перикардит, в отдельных случаях может наблюдаться значительный выпот вплоть до тампонады сердца. Сухой перикардит диагностируют на основании жалоб (боль за грудиной, сердцебиения, затруднение глубокого вдоха), объективных данных (тахикардия, приглушенность тонов, иногда шум трения перикарда). Вспомогательное значение имеют показатели ЭКГ и ФКГ (снижение вольтажа, отрицательный зубец Т, высокочастотный шум). Выявление небольшого выпота облегчает эхокардиографию.
Значительный выпот определяется клинически и рентгенологически (рис. 4.13).

Рис. 4.13. Выпотной перикардит в период одного из обострении у больной с хроническим течением системной красной волчанки.
При длительном течении СКВ у больных с рецидивирующим (даже сухим) перикардитом развиваются массивные спайки.. Для этой группы больных характерна даже вне обострения СКВ стойкая боль за грудиной, в боку, усиливающаяся при смехе, чиханье, длительно может выявляться шум трения перикарда. В редких случаях отмечаются массивные перикардиальные наложения с облитерацией перикарда столь выраженной, что требуется хирургическое вмешательство.
Миокардит обычно наблюдается у больных с высокой степенью активности. Клиническая картина диффузного миокардита, данные ЭКГ и ФКГ не имеют специфических черт и соответствуют критериям этой патологии. Важно то обстоятельство, что эффективны лишь кортикостероиды, сердечная недостаточность не купируется препаратами дигиталиса, которые могут быть лишь вспомогательным средством в адекватной кортикостероидной терапии.
Нерезко выраженное поражение миокарда иногда не диагностируется из-за других более тяжелых проявлений СКВ (цереброваскулит, нефрит) и купируется терапией, адекватной общей активности болезни.
При патологоанатомическом исследовании поражение миокарда выявляют довольно часто: находят очаговые инфильтраты из лимфоцитов и плазматических клеток; могут быть даже очаговые некрозы, рубцовые изменения. В сосудах миокарда обнаруживают отложения фибрина. Поражается проводящая система сердца. Наблюдается атриовентрикулярная блокада.
Эндокардит в последние годы диагностируется при жизни довольно часто. Клинически эндокард изолированно не поражается. Как правило, вовлекаются все оболочки сердца и обязательно перикард.
При эндокардите выслушивается грубый систолический шум на верхушке и других проекционных точках сердца (чаще в точке Боткина), выявляют и диастолический шум, ослабление I тона на верхушке. Классический эндокардит Либмана—Сакса в основном патоморфологический признак СКВ, реже клинически выявляют пороки сердца. Бородавчатые изменения обнаруживают чаще при микроскопическом исследовании, но они могут быть видны и макроскопически. Чаще поражается митральный клапан. Сотрудниками Института ревматологии АМН СССР [Котельникова Г. П. и др., 1977] описано 4 случая митрального порока сердца у больных с достоверной СКВ. Имеются сообщения также о поражении аортального и трикуспидального клапана.
Из сосудов при СКВ поражаются в основном артерии среднего и мелкого калибра. Степень и выраженность поражения сосудов варьируют. Полагают, что антитела к ДНК, преципитирующие в контриммуноэлектрофорезе, ассоциируются с артериитом, а различия в клинической патологии сосудов обусловлены составом иммунных комплексов, в которые входят антитела с разной аффинностью.
Кожные васкулиты представлены эритематозными высыпаниями, дигитальными капилляритами, ишемическими некрозами кончиков пальцев кистей, а также сетчатым ливедо.
Поражается и венозное звено. Тромбофлебиты конечностей как проявление васкулита наблюдались нами у 25% больных, возникли, как правило, в период обострения СКВ и поддавались только лечению кортикостероидами.
Поражение крупных сосудов при СКВ требует дополнительного изучения.
К настоящему времени имеется небольшое число сообщений о вовлечении в процесс аорты и ее ветвей, подключичной артерии и коронарных сосудов, тромбозах магистральных сосудов конечностей с гангреной. В Институте ревматологии РАМН мы наблюдали двух больных с тромбозом глубоких вен плеча. В одном случае консервативное лечение было эффективным, в другом потребовалось извлечение тромба хирургическим путем. Нередко наблюдаются тромбофлебиты поверхностных вен плеча и передней поверхности груди.
Коронарные артерии вовлекаются в процесс не столь редко. В ранние сроки болезни коронарит связан с высокой активностью СКВ. Описаны случаи инфаркта миокарда у молодых женщин [Фоломеева О. М., Котельникова Г. П., 1979]. В поздние сроки коронарит связан с возможностью развития атеросклероза при длительной терапии кортикостероидами. Имеются'сообщения, что коронароатеросклероз возникает уже через год терапии кортикостероидами. Существует четкая корреляция поражения коронарных артерий с высоким АД. Инфаркт миокарда при большой давности СКВ является наиболее частой причиной смерти в описаниях последних 10 лет. В связи с этим рекомендуется интенсивное лечение гипертензии с момента ее выявления.
Читайте также:
- Инфекционная больница в миорах на
- Что относится к антропонозным инфекциям
- Инфекционные заболевания и бактериологическое оружие
- Когда можно делать прививки после инфекционного мононуклеоза
- Какие бывают грибковые инфекции в интимной зоне


