Домарадский и в хеликобактериоз
Бактерия Хеликобактер пилори (Helicobacter pylori) является одной из самых распространенных инфекций человека. В мире не менее 50% населения инфицировано Хеликобактер пилори. В России этот микроорганизм выявляется у 80% людей старше 18 лет [1, 2].
Открытие инфекции Хеликобактер пилори в 1983 году вызвало революционные изменения представлений о причинах развития многих распространенных заболеваний желудочно-кишечного тракта. Авторам этого открытия, австралийским ученым Робину Уоррену и Барри Маршалу, в 2005 году была присуждена Нобелевская премия по физиологии и медицине [3].

Изображение является художественным. Подготовлено на основе описания
бактерии Helicobacter pylori, приведенного в источниках 4, 5.
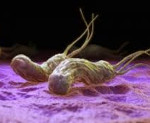
Хеликобактер пилори представляет собой спиралевидно изогнутую палочку, на одном конце которой имеются жгутики. Местом обитания Хеликобактер пилори в организме человека служит желудок и двенадцатиперстная кишка. Бактерия либо свободно передвигается в слое слизи с помощью жгутиков, либо прикрепляется к эпителиальным клеткам слизистой оболочки. Хеликобактер пилори — один из немногих микробов, приспособившихся к обитанию в условиях высокой кислотности желудочного сока [4, 5].
Пути передачи инфекции
Несмотря на интенсивное изучение, пути передачи инфекции Хеликобактер пилори остаются не до конца изученными. Считается, что микроорганизм передается от человека к человеку при близком контакте через слюну (поцелуи, облизывание сосков при кормлении детей) и фекально-оральным путем (несоблюдение правил личной гигиены). Бактерия также может передаваться через воду и продукты питания. Большинство людей заражаются Хеликобактер пилори еще в детском возрасте. Источниками инфекции чаще всего являются инфицированные родители, братья и сестры, сверстники в детских садах и школах [4, 5, 6, 7].
Иммунный ответ организма человека в подавляющем большинстве случаев не уничтожает Хеликобактер пилори. Без лечения человек остается инфицированным на протяжении всей жизни. Однако после успешного лечения, особенно у взрослых, риск повторного заражения невелик и составляет несколько процентов в год [5, 8].
Вопреки частому заблуждению, Хеликобактер пилори не является безобидным микроорганизмом. Присутствие этой бактерии в слизистой оболочке приводит к ее повреждению, возникновению воспаления и развитию хронического хеликобактерного гастрита. При этом хронический гастрит развивается у ВСЕХ пациентов, инфицированных Хеликобактер пилори. Это объясняет чрезвычайно широкое распространение этого заболевания [9].
В свою очередь, вызванный инфекцией Хеликобактер пилори хронический гастрит служит патологическим фоном, на котором возникают такие серьезные заболевания верхнего отдела желудочно-кишечного тракта, как язвенная болезнь желудка и двенадцатиперстной кишки, а также рак желудка. Язвенная болезнь развивается приблизительно у 10% пациентов, инфицированных этой бактерией [4, 5, 9]. На сегодняшний день Хеликобактер пилори рассматривается как опасный для человека канцерогенный фактор. Связь данной инфекции и рака желудка считается доказанной и признана Всемирной организацией здравоохранения [10].
Стрессы, неправильное питание и алкоголь не являются причинами хронического гастрита и язвенной болезни!
Диагностика
Существует несколько методов диагностики инфекции Хеликобактер пилори. Выбор того или иного теста осуществляется врачом и обычно зависит от конкретной ситуации.
Если пациенту выполняется гастроскопия с забором образцов слизистой оболочки (биоптатов), то наиболее подходящими методами служат гистологическое исследование биоптатов, а также специальный уреазный тест, позволяющий выявить наличие данной инфекции за несколько минут [1].
Если гастроскопия не проводится, то Хеликобактер пилори может быть выявлена с помощью мочевинного дыхательного теста. Пациент выпивает специальный раствор мочевины, которая распадается в желудке при наличии там Хеликобактер пилори. Продукты распада мочевины с помощью специальных приборов определяются в выдыхаемом воздухе.
Также бактерия может быть выявлена с помощью анализов крови (антитела к Хеликобактер пилори) и кала (тест на антигены Хеликобактер пилори) [1, 4, 11].
Лечение
Лечение инфекции Хеликобактер пилори(антихеликобактерная терапия) направлено на ее полное уничтожение (эрадикацию) в слизистой оболочке желудка и двенадцатиперстной кишке. С этой целью могут применяться специальные схемы, состоящие из 3–4 препаратов. Антихеликобактерная терапия может быть назначена только врачом и должна проводиться согласно современным отечественным и международным рекомендациям. Курс лечения обычно составляет 10–14 дней [12, 13].
Схемы антихеликобактерной терапии обычно включают препараты нескольких групп [12, 13]:
лекарственные средства, снижающие секрецию соляной кислоты (ингибиторы протонной помпы);
препараты висмута (висмута трикалия дицитрат – Де-Нол®).
Эффективность висмута трикалия дицитрата (Де-Нол®) в отношении Хеликобактер пилори впервые была показана нобелевским лауреатом Барри Маршаллом [14]. Де-Нол® обладает мощным антибактериальным действием в отношении Хеликобактер пилори и значительно повышает эффективность антибиотиков, входящих в схемы лечения этой инфекции [4, 15, 16, 17, 18, 19]. В отличие от многих антибиотиков, устойчивость Хеликобактер пилори к препарату Де-Нол® не развивается никогда [20]. Помимо бактерицидного, этот препарат оказывает на слизистую оболочку желудка и двенадцатиперстной кишки выраженное защитное (цитопротективное) действие. Де-Нол® способствует ускорению заживления дефектов слизистой оболочки, улучшению кровообращения и выделения слизи, оказывает противовоспалительное действие [4, 15, 21].
Эффективность современных схем лечения инфекции Хеликобактер пилори составляет 80–90%. Обычно через 1–1,5 месяца после завершения лечения врач рекомендует пройти повторное исследование для оценки эффективности уничтожения инфекции. Если бактерия не была уничтожена, может быть назначена вторая схема терапии, содержащая антибиотики [12].
Изучено влияние пребиотического комплекса на результаты эрадикационной антихеликобактерной терапии и показана его эффективность по предупреждению развития антибиотикоассоциированной диареи у пациентов, имеющих прогностические факторы неблагоприятного тече
Influence of prebiotic complex on the results of eradication anti-helicobacter therapy was studied, and its efficiency in prevention of antibiotic-associated diarrhea in patients having forecasting factors of adverse clinical course of early post-eradication period was shown.
Инфекция Helicobacter pylori (Н. pylori) является ведущей причиной хронических заболеваний желудка и двенадцатиперстной кишки. Эрадикация Н. pylori является основным стандартом лечения хеликобактер-ассоциированных заболеваний гастродуоденальной зоны, что отражено в международных соглашениях (Маастрихтские соглашения 1–3, соответственно 1996, 2000 и 2005 гг.) [1].
Следует иметь в виду, что хеликобактериоз проявляется не только местными эрозивно-язвенными поражениями гастродуоденальной зоны, но и оказывает системное влияние на организм человека. Инфицирование макроорганизма и длительное персистирование H. pylori нарушает микроэкологию пищеварительного тракта и может рассматриваться в качестве фактора, инициирующего и усугубляющего нарушения микробиоценоза толстой кишки [2, 3]. При H. pylori-позитивной язвенной болезни дисбиоз кишечника выявляется у 92% пациентов (НИИ питания РАМН), выраженность дисбиотических изменений достоверно связана со степенью обсемененности H. pylori [4]. Антихеликобактерная терапия, включающая применение антибиотиков, также приводит к угнетению облигатной микрофлоры и последующей колонизации слизистой оболочки желудочно-кишечного тракта патогенной и условно-патогенной микрофлорой [5].
Дисбиоз толстой кишки может стать причиной развития вторичного иммунодефицита (местного и общего), что в свою очередь вызывает снижение защитных сил организма и является важным фактором в патогенезе H. pylori-ассоциированной патологии. При этом важно, что сопутствующие дисбиотические изменения кишечника могут достигать определенного критического уровня и превращаться в самостоятельный фактор агрессии. В этих условиях прогредиентно нарастает выраженность клинических симптомов воспалительных заболеваний гастродуоденальной области, удлиняются сроки их существования, утяжеляется общее состояние, ухудшаются показатели результатов лечения и качество жизни пациентов, клиническое течение приобретает часто рецидивирующий характер [6, 7].
Иммуногенная функция нормофлоры заключается в стимуляции синтеза иммуноглобулинов, интерферона, цитокинов; в активировании созревания системы фагоцитирующих мононуклеаров; в повышении содержания комплемента и пропердина, активности лизоцима; выработке бактериальных модулинов. В качестве медиаторов действия бактериальных метаболитов выступают гистамин, серотонин, простагландины, лейкотриены, короткоцепочные жирные кислоты. Воздействие микробных метаболитов и медиаторов их действия направлено на модуляцию пролиферации, дифференцировки, апоптоза и метаболических реакций эукариотических клеток. Нормофлора способна воздействовать на дифференцировку Т-хелперов и таким образом влиять на соотношение про- и противовоспалительных цитокинов. S. Roos, C. Johnson (2003 г.) показали, что некоторые штаммы лактобактерий обладают кислотоустойчивостью и антагонизмом к H. pylori in vivo и in vitro. Lactobacilli spp., как и Bifidobacterium spp., выделяют бактериоцины, способные ингибировать рост H. pylori и нарушать адгезию микроба к эпителиальным клеткам желудка [8–10].
Исследования последних лет показали, что препараты, улучшающие микробиоценоз кишечника, не только повышают эффективность эрадикационной терапии, но и предупреждают развитие и позволяют в значительной степени снизить побочные эффекты антибиотиков, входящих в стандартные схемы антихеликобактерной терапии, такие как антибиотикоассоциированная диарея, тошнота, неприятный привкус в ротовой полости и т. п. [10–14].
Независимо от индивидуальных различий в составе кишечной микрофлоры, кишечный микробиоценоз у каждого человека функционирует как единая экосистема и целостный метаболический орган, который обеспечивает необходимое количество и профиль конечных метаболитов, среди которых наиболее важную роль играют короткоцепочечные жирные кислоты (КЦЖК). КЦЖК — основной продукт микробной ферментации анаэробными бактериями углеводов, жиров и белков. К ним относятся уксусная (С2), пропионовая (С3), изомасляная, масляная (С4), изовалериановая, валериановая (С5), изокапроновая и капроновая (С6) кислоты [7, 15, 16].
Неразветвленные КЦЖК — уксусная, пропионовая и масляная — образуются при анаэробном брожении углеводов, тогда как метаболизм белков ведет к образованию разветвленных кислот — изомасляной (из валина) и изовалериановой (из лейцина). В течение суток синтезируется более 300 ммоль/л КЦЖК. Максимальная концентрация КЦЖК достигается в проксимальных отделах толстой кишки 70–140 ммоль/л — самом мощном биокорректорном участке желудочно-кишечного тракта. В дистальной части содержание КЦЖК снижается до 20–70 ммоль/л [16].
КЦЖК участвуют в регуляции большинства физиологических эффектов облигатной микрофлоры толстой кишки. Так, они являются основным источником питания для колоноцитов, обеспечивая их энергией (на 70%), стимулируют регенерацию эпителия, обладают антибактериальной активностью, обеспечивают баланс микробной экосистемы, препятствуя ее контаминации патогенной микрофлорой, поддерживают детоксицирующую функцию печени за счет участия в энтерогепатической циркуляции желчных кислот, обладают антиканцерогенным и антивирусным действием, оказывают влияние на экспрессию генов в колоноцитах, являются активным модулятором иммунной системы, регулируют моторную функцию кишечника (табл. 1) [16–18].
- Контроль структурной и функциональной целостности клеточного состава толстой кишки и всего организма.
- Модулирует распознавание и уничтожение собственных мутантных, в том числе и опухолевых клеток, а также вторгшихся микроорганизмов и образуемых ими токсических веществ, способных нарушить генетический гомеостаз.
- Продукция медиаторов межклеточного взаимодействия:
- снижение секреции провоспалительных цитокинов, таких как фактор некроза опухоли альфа, оксид азота, гамма-интерферон, интерлейкины ИЛ-2, ИЛ-1;
- стимулирование высвобождения противовоспалительного цитокина ИЛ-10 из моноцитов.
- Ингибирование адгезии эндотелиальных лейкоцитов посредством модуляции экспрессии ФМА-1 и МАСЭ-1 и активации макрофагального ядерного фактора NF-каппа-би.
- Уменьшает гамма-интерферон-индуцируемое высвобождение белка-10 в субэпителиальных миофибробластах кишечника человека.
- Снижает кишечную продукцию СЛК-зависимого ИЛ-8 и кишечную экспрессию Toll-подобного рецептора 4, который считается важным компонентом врожденного иммунитета и который, при избыточной продукции, приводит к проявлению воспалительных заболеваний кишечника.
Основными продуцентами бутирата являются не бифидо- и лактобактерии, а эубактерии, пептококки, фузобактерии и клостридии (поэтому большинство пробиотиков не влияют на синтез масляной кислоты). Эта КЦЖК активно абсорбируется в цитоплазму колоноцита, где в митохондриях из нее образуется АТФ. 70% энергии идет на обеспечение локальных процессов в толстой кишке, а оставшиеся 30% этой энергии расходуются на нужды целого организма. Рецептор-опосредованным путем масляная кислота инициирует активацию и/или ингибирование локальных и системных иммунных реакций [16].
В России с 2011 г. для лечения различных заболеваний ЖКТ применяется препарат Закофальк®. В состав препарата входит масляная кислота и инулин в дозе 250 мг, которые помещены в полимерную мультиматриксную капсулу NMX. В отличие от ранее известных про- и пребиотиков, которые стимулируют рост нормофлоры толстой кишки, что опосредованно приводит к образованию КЦЖК, в первую очередь ацетата и пропионата, Закофальк® напрямую доставляет масляную кислоту и инулин в толстую кишку в заданном количестве. Пребиотический комплекс Закофальк® обеспечивает возможность реализации сложного каскада иммунобиологических, метаболических и других свойств, присущих нормально функционирующему микробно-тканевому комплексу кишечника.
Инулин, (C6H10O5)n, органическое вещество из группы полисахаридов (фруктанов), полимер D-фруктозы, построенный из остатков D-фруктофуранозы, связанных 2,1-бета связями.
Что касается медицинской классификации инулина, в большинстве публикаций его относят к группе растворимых пищевых волокон (не целлюлозный полисахарид). Кроме того, способность инулина избирательно стимулировать бифидо- и лактобактерии, являющиеся представителями нормальной микрофлоры кишечника, позволяет назвать данное вещество истинным пребиотиком.
При попадании в пищеварительный тракт инулин проходит в неизмененном виде в желудок и тонкую кишку. В толстой кишке фруктоолигосахариды являются питательным субстратом исключительно для бифидобактерий и отдельных видов лактобацилл, которые обладают ферментной системой бета-фруктозидаз, позволяющей им расщеплять фруктоолигосахариды до масляной кислоты. Таким образом, инулин выступает не только как селективный пребиотический фактор для микрофлоры толстой кишки, но и как промоутер синтеза эндогенной масляной кислоты.
Растительные волокна инулина, будучи нерастворимыми в тонкой кишке, в толстой кишке создают дополнительные площади (помимо поверхности слизистой оболочки), к которым фиксируются сахаролитические бактерии. Благодаря этому в просвете толстой кишки во много раз возрастает число мест для адгезии и формирования микроколоний лакто- и бифидобактерий, что приводит к значительному увеличению количества присутствующих на единицу объема кишки микроорганизмов, и, как следствие этого, резко возрастает метаболическая активность кишечного содержимого с образованием различных важных для организма энергетических и пластических субстанций. Lactobacilli spp., как и Bifidobacterium spp., выделяют бактериоцины, способные ингибировать рост Н. pylori и нарушать адгезию микроба к эпителиальным клеткам желудка.
Масляная кислоты С3Н7СООН является органической кислотой, вырабатывающейся в просвете толстой кишки в процессе бактериальной ферментации неперевариваемых пищевых углеводородов. Бутират используется организмом в качестве энергетического субстрата для обеспечения процессов пролиферации и дифференцировки колоноцитов, для энергообеспечения ферментативных процессов индигенной флоры. Именно эта кислота контролирует механизмы, инициирующие апоптоз ненужных в функциональном отношении колоноцитов и раковых клеток, модулирует экспрессию генов, регулирующих клеточный цикл, нивелирует действие супероксидных радикалов. Масляная кислота играет основную роль в обеспечении локальных и системных иммунных механизмов: путем активации локальных макрофагов для увеличения презентации антигенов B-лимфоцитам и увеличения производства секреторного иммуноглобулина А местно и системно, модулирования цитокиновых профилей и активации синтеза интерферона. Масляная кислота, являясь универсальным сигнальным химическим носителем передачи информации в организме человека, регулирует адаптивные реакции не только на уровне микробиоценоза толстой кишки (предупреждает развитие кишечного дисбиоза), но и оказывает общее иммуномодулирующее действие.
Клинически манифестной формой кишечного дисбиоза при проведении эрадикационной терапии является антибиотикоассоциированная диарея. На базе городских поликлиник г. Москвы было проведено открытое сравнительное рандомизированное многоцентровое исследование по изучению влияния препарата Закофальк® на эффективность и переносимость эрадикационной терапии.
Целью настоящего исследования было изучение влияния пребиотического комплекса Закофальк® на результаты эрадикационной терапии и его эффективности по предупреждению развития антибиотикоассоциированной диареи при проведении антихеликобактерной терапии у пациентов, имеющих прогностические факторы неблагоприятного течения раннего постэрадикационного периода.
В рамках сравнительного открытого рандомизированного исследования было обследовано 115 человек (мужчин — 52, женщин — 63), средний возраст 42,5 лет (20–65 лет).
Критерии включения: больные язвенной болезнью, ассоциированной с Н. pylori, в стадии обострения с наличием язвенного дефекта в желудке или в двенадцатиперстной кишке; наличие не менее двух факторов риска развития антибиотикоассоциированной диареи (постинфекционный синдром раздраженного кишечника, сахарный диабет 2-го типа, указание в анамнезе на проведение антибактериальной терапии вне связи с основным заболеванием в течение ближайших 6 месяцев, хронические заболевания гепатобилиарной системы и поджелудочной железы, длительный прием гормональных или химиотерапевтических препаратов, синдром короткой тонкой кишки, дивертикулярная болезнь толстой кишки, онкологические заболевания толстой кишки в анамнезе).
Обследование включало: клиническое наблюдение в динамике, проведение эзофагогастродуоденоскопии с взятием гастробиоптатов слизистой оболочки края язвы с последующей их гистобактериоскопией и проведением уреазного теста (до и через 4 недели от окончания эрадикационной терапии). В ходе исследования анализировались результаты исследования состава кишечной микрофлоры. Исследование иммунного статуса включало определение в сыворотке крови IgG, IgM, IgA, IgE.
После включения в исследование больные были рандомизированы на две группы. Пациенты основной группы (60 человек) помимо препаратов эрадикационной терапии (Нексиум 20 мг 2 раза + кларитромицин 500 мг 2 раза + амоксициллин 1000 мг × 2 раза 14 дней) получали Закофальк® 3 таблетки в сутки, а больные группы сравнения (55 человек) — ту же терапию, но без применения препарата Закофальк®. До начала терапии нарушений кишечной моторики (поносов либо запоров) ни у кого не было.
Через 7 дней от включения в исследование при повторном опросе и осмотре синдром кишечной диспепсии, индуцированный проведением эрадикационной терапии, был отмечен у 34 (68%) пациентов группы сравнения: вздутие — 25, урчание — 28; жидкий стул до 3 раз в сутки — 25, жидкий стул более 3 раз в день — 9. Девять пациентов этой группы (18%) в течение первой недели лечения отказались от дальнейшего приема антибиотиков. При этом в основной группе, пациенты которой получали Закофальк®, не было зафиксировано возникновение диареи, а вздутие или урчание живота было отмечено лишь у 14 пациентов (23,3%). По завершении антибиотикотерапии на 14-й день лечения 41 (82%) пациент группы сравнения отмечал послабления стула от 3 до 5–7 раз в сутки. У 7 (11,7%) пациентов основной группы отмечалось учащение дефекаций до 5 раз в сутки. Таким образом, включение препарата Закофальк® в схему эрадикационной терапии улучшает переносимость лечения антибиотиками даже у пациентов с высоким риском антибиотикоассоциированной диареи (табл. 2).
Исходный уровень сывороточных иммуноглобулинов не имел значимых отличий в основной группе и группе сравнения, средние его значения были незначительно снижены. Уровень IgE был повышен только у больных язвенной болезнью двенадцатиперстной кишки с наличием участков лимфоидной гиперплазии в антральном отделе желудка, средний его уровень в основной группе составил 64,25 ± 11 кЕ/л и 55 ± 12 кЕ/л в группе сравнения. После проведения эрадикационной схемы лечения с включением препарата Закофальк® у пациентов основной группы наблюдалась небольшая тенденция к повышению уровня IgA до 3,0 ± 0,5 г/л (исходный 0,65 ± 0,2 г/л) и значительное снижение IgE до 43 ± 11 кЕ/л. У пациентов группы сравнения такой тенденции не наблюдалось. Повышение сывороточного IgA может отражать повышение секреторного IgA на слизистой оболочке желудка, что свидетельствует об усилении реакций местного иммунитета. Снижение уровня IgE, по-видимому, связано с усилением протективной и детоксицирующей функций эндосимбиотных бактерий. Повышение сывороточных IgA и снижение IgE после лечения препаратом Закофальк® сочеталось со стабильным исчезновением клинических признаков обострения и эндоскопически подтвержденным рубцеванием язв у всех пациентов основной группы (табл. 3).
При микробиологическом исследовании фекалий в исходном периоде достаточно выраженные изменения соотношения представителей кишечной микрофлоры выявлены у большинства обследованных больных в обеих группах, в первую очередь отмечалось снижение уровня бифидо- и лактобактерий. После курса эрадикационной терапии у пациентов, принимавших Закофальк®, выявлено достоверное увеличение количества бифидобактерий и лактобактерий, а также достоверное уменьшение количества патогенных и условно-патогенных бактерий. В группе сравнения обращает внимание угнетение микробного роста представителей нормальной кишечной микрофлоры и увеличение степени дисбиоза кишечника. Таким образом, полученные данные в очередной раз подтверждают отрицательное влияние стандартной эрадикационной терапии на микробный состав кишечника, что имеет особое значение для пациентов с сопутствующими заболеваниями ЖКТ, увеличивающими риск развития кишечного дисбиоза и его клиническое проявление — антибиотикоассоциированной диареи (табл. 4, 5).
Достижение эрадикации H. pylori было зафиксировано у 52 (86,7%) пациентов основной группы и у 17 (31%) из группы сравнения, что может зависеть от более четкого соблюдения комплаентности терапии, а также способности препарата Закофальк® потенцировать противовоспалительный эффект антибиотиков.
Проводилась морфологическая оценка из краев язвенных дефектов до начала антихеликобактерной терапии и по ее завершении. Полученные данные свидетельствуют, что включение в терапию препарата Закофальк® приводит к улучшению клеточного состава слизистой оболочки в краях язвы. Так, значительно уменьшается нейтрофильная и лимфоцитарная и плазмоцитарная инфильтрация, что свидетельствует об уменьшении воспалительного и иммуно-воспалительных процессов (табл. 6, 7).
Результаты исследования показывают несомненное преимущество комплексного лечения язвенной болезни, ассоциированной с H. pylori, с включением пребиотика Закофальк® по сравнению со стандартной эрадикационной схемой.
На основании полученных данных можно сделать следующие выводы:
- Антихеликобактерная терапия сопровождается развитием антибиотико-ассоциированных нарушений кишечной микрофлоры у большинства пациентов.
- Назначение препарата Закофальк® снижает риск развития осложнений антихеликобактерной терапии; способствует улучшению показателей собственно эрадикации.
- Эффект препарата Закофальк® проявляется клиническим улучшением, нормализацией состава микрофлоры кишечника, а также восстановлением ее метаболической активности.
- Включение препарата Закофальк® позволяет существенно потенцировать противовоспалительный эффект эрадикационной терапии.
Литература
Л. И. Буторова*, кандидат медицинских наук
Т. А. Плавник**
Н. Г. Кадникова***
С. Р. Рекель****
* ГИУВ МО РФ; ГБУЗ ГП № 209 ДЗМ, Москва
** ГБУЗ ГП № 195 ДЗМ, Москва
*** ПК № 230 ДЗМ, Зеленоград
**** ФГБУ ПК № 2 УДП РФ, Москва
Хеликобактериоз — это латентное или манифестировавшее инфекционное заболевание, при котором слизистая желудка колонизируется хеликобактериями. Обычно протекает бессимптомно. При клинической манифестации проявляется болями, чувством тяжести и дискомфорта в эпигастрии, диспепсией, учащением дефекации. Для длительного течения характерны признаки анемизации: слабость, быстрая утомляемость, головокружения, головные боли. Диагностируется с помощью ИФА, ПЦР, дыхательного теста, эзофагогастродуоденоскопии и анализа биоптата. Стандартные схемы лечения предполагают назначение блокаторов протонного насоса, антибактериальных препаратов и солей висмута.
МКБ-10
Общие сведения
Инфицирование хеликобактерией (Helicobacter pylori) наблюдается почти у 60% населения планеты. По данным наблюдений в сфере клинической гастроэнтерологии, распространенность хеликобактериоза напрямую зависит от материального уровня жителей: в развивающихся государствах этот показатель выше, чем в развитых, в семьях с годовым доходом более 70 тыс. долларов инфицированность встречается спорадически.
Кислотоустойчивые бактерии были впервые выделены из слизистой желудка австралийскими учеными Дж. Уорреном и Б. Маршаллом в 1982 году. Наиболее часто хеликобактериоз выявляется после 60 лет, повышенной восприимчивостью к хеликобактерной инфекции обладают больные с ослабленным иммунитетом.

Причины хеликобактериоза
Заболевание вызывается микроаэрофильной грамотрицательной бактерией Helicobacter pylori, реже другими видами хеликобактера, тропными к желудочному эпителию и устойчивыми в кислотной среде. Источниками заражения являются пациенты, страдающие явным или латентным хеликобактериозом, носители микроорганизма, домашние и сельскохозяйственные животные, у которых высеиваются другие разновидности хеликобактерий (H. acinonychis, H. felis, H. salomonis, H. mustelae).
Основными путями инфицирования являются алиментарный и водный. Возможно контактно-бытовое заражение при пользовании общими с носителем или больным посудой, полотенцами, зубной щеткой и другими предметами личной гигиены. Новорожденным детям возбудитель хеликобактериоза чаще всего передается контактно-бытовым способом. Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Патогенез
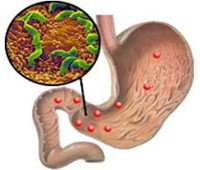
Механизм развития хеликобактериоза определяется особенностями колонизации бактерией слизистой желудка. Инфицирующей считается доза патогена от 10 тыс. до 1 млрд. микробных тел. Хеликобактерии адгезируются к желудочным эпителиоцитам, скапливаясь преимущественно в межклеточных промежутках, с помощью жгутиков мигрируют к участкам выделения мочевины и гемина, необходимых для жизнедеятельности возбудителей. Расщепление мочевины микробной уреазой до аммиака и двуокиси углерода позволяет создать вокруг колонии слой, защищающий хеликобактера от соляной кислоты.
Аммиак, цитотоксины и высокоактивные энзимы (муциназа, липаза, протеаза), продуцируемые микробом, разрушают слизисто-бикарбонатный барьер и оказывают повреждающее воздействие на желудочный эпителий. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно с минимальными патоморфологическими изменениями слизистой или остро с инфильтрацией эпителиальной оболочки, активацией системы простагландинов, выраженной клинической симптоматикой воспаления.
Хронический гастрит с инфильтрацией лимфоцитами антрального эпителия является продолжением острого процесса или следствием активации возбудителя при снижении иммунитета у пациентов с первично-латентной формой хеликобактериоза. Значительный дисбаланс между недостаточным защитным действием слизисто-бикарбонатного слоя и высокой агрессивностью желудочного сока приводит к формированию язвы желудка, дисплазии эпителиоцитов. Поражение двенадцатиперстной кишки и пищевода возможно только при желудочной метаплазии их эпителия.
Симптомы хеликобактериоза
Почти у 90% пациентов инфицирование H. pylori длительное время протекает бессимптомно и выявляется при обследовании по поводу других болезней ЖКТ. В случае быстрой первичной манифестации возбудителя у больных развивается острый период хеликобактериоза, который длится около 10 дней. Основными жалобами являются периодические боли в эпигастральной области, чувство тяжести, дискомфорта после приема пищи, тошнота. Может наблюдаться учащение дефекации, изменение характера стула. Пациенты жалуются на отрыжку, изжогу и вздутие живота.
Общее состояние больных обычно остается удовлетворительным, иногда отмечается кратковременный субфебрилитет, снижение работоспособности. После стихания острых проявлений хеликобактериоза отмечается периодический абдоминальный дискомфорт, тошнота и снижение аппетита. При хроническом течении заболевания и атрофическом поражении слизистой желудка возникают признаки анемии — частые головные боли и головокружения, бледность кожных покровов, снижение АД и тахикардия.
Осложнения
Наиболее частое последствие хеликобактериоза — усиление выработки соляной кислоты и гастрина, снижение факторов защиты, приводящее к возникновению хронического гастрита типа В. По мере прогрессирования заболевания формируются участки атрофии слизистой оболочки желудка, снижается кислотность. Хеликобактерная инфекция является причиной 95% язв двенадцатиперстной кишки, 80% язв желудка. В современных исследованиях доказана связь патологии с развитием гастроэзофагеальной рефлюксной болезни.
При хеликобактериозе снижается выработка внутреннего фактора Касла, что нарушает всасывание витамина В12 и вызывает мегалобластную анемию. При этом у пациентов, кроме типичных признаков анемии, возникают патогномоничные симптомы — лакированный язык, фуникулярный миелоз (поражение периферической нервной системы). Наиболее опасное осложнение патологии — метаплазия и дисплазия атрофированной слизистой, значительно повышающая риск рака желудка.
Диагностика
Постановка диагноза хеликобактериоза во время клинического осмотра пациента затруднена, что объясняется полиморфностью и неспецифичностью жалоб. Диагностический поиск включает комплексную лабораторно-инструментальную оценку состояния желудочно-кишечного тракта больного. Наиболее информативными для диагностики являются такие методы, как:
- Серологические реакции. Определение антител к хеликобактеру в крови с помощью иммуноферментного анализа используется для подтверждения инфицирования H. Pylori. Тест позитивный, если концентрация антител превышает 1,1 ед/мл, при значениях в диапазоне 0,9-1,1 единиц в 1 мл фиксируют сомнительный результат, который не исключает наличия хеликобактериоза.
- Дыхательный тест. Измерение концентрации меченых изотопов углерода в выдыхаемом воздухе после приема раствора мочевины основано на ферментативной активности H. Pylori и применяется для экспресс-диагностики. Диагностически значимым считается содержание 13С изотопов более 1,7%. Дыхательный тест на хеликобактер также назначают для контроля лечения.
- Эзофагогастродуоденоскопия. Визуализация верхних отделов ЖКТ при помощи гибкого эндоскопа — основной метод диагностики, позволяющий оценить состояние эпителия. При хеликобактериозе в ходе ЭГДС обнаруживается гиперемия и отечность слизистой тела желудка, пилорического отдела и верхней части 12-перстной кишки. Дополнительно производится эндоскопическая биопсия.
- Исследование биоптатов. Фрагмент патологически измененной слизистой оболочки используют для последующего быстрого уреазного теста — определения наличия хеликобактера. Изменение цвета индикатора с желтого на красный свидетельствует о положительном результате. В сомнительных случаях проводят цитоморфологическое исследование для изучения клеточного состава.
- Дополнительные анализы. В общем анализе крови в острой фазе хеликобактериоза выявляют умеренный лейкоцитоз и повышение СОЭ, при длительном течении болезни обнаруживают снижение показателей эритроцитов и гемоглобина, макроцитоз. Биохимический анализ крови без патологических изменений. Для определения хеликобактерной инфекции могут выполнять бактериологическое исследование — культивирование материала на специальных питательных средах.
В первую очередь дифференциальную диагностику заболевания проводят с функциональной диспепсией. Основными диагностическими критериями, свидетельствующими в пользу хеликобактериоза, являются наличие воспалительных изменений слизистой желудка и двенадцатиперстной кишки, выявление H. Pylori с помощью инвазивных методов исследования. В остром периоде болезнь нужно дифференцировать с кишечными инфекциями. Кроме гастроэнтеролога для обследования пациента привлекают инфекциониста.
Лечение хеликобактериоза
Выбор тактики зависит от клинического течения патологии. Выявленным носителям инфекции рекомендовано наблюдение. При развитии на фоне хеликобактерной инфекции гастрита, язвы желудка или двенадцатиперстной кишки, желудочной MALT-лимфомы назначается одна из трехкомпонентных, четырехкомпонентных или усеченных схем эрадикации хеликобактера. Консервативное лечение обычно длится 10-14 дней. С учетом решений Маастрихтских согласительных конференций и рекомендаций Научного общества гастроэнтерологов России для терапии хеликобактериоза могут применяться:
- Ингибиторы протонной помпы. Антисекреторные препараты блокируют Н+/К+-АТФазу париетальных клеток желудка, за счет чего угнетается продукция соляной кислоты. Снижение кислотности желудочного сока позволяет уменьшить его агрессивное воздействие на слизистую оболочку.
- Антибактериальные средства. При выборе препарата учитывают резистентность хеликобактера. Для элиминации патогена используют комбинацию макролидов или нитрофуранов с полусинтетическими пенициллинами или нитроимидазолами, тетрациклины, производные рифампицина.
- Коллоидные соли висмута. Висмут-содержащие препараты оказывают бактерицидное действие на хеликобактер. Усиливают защитные факторы слизистой желудка: формируют на поверхности эпителия защитную пленку, стимулируют секрецию бикарбонатов и простагландина Е2.
Прогноз и профилактика
Исход заболевания зависит от обратимости морфологических изменений слизистой ЖКТ и своевременности начатого лечения. У пациентов без сопутствующей патологии, прошедших полный курс антихеликобактерной терапии, прогноз благоприятный: возможна полная санация эпителия, нормализация кислотности. Профилактика хеликобактериоза включает соблюдение правил личной гигиены, рациональный режим питания (прием пищи 4-5 раз в день, исключение жареной, очень острой еды, копченостей), лабораторное обследование людей, которые были в контакте с инфицированным H. Pylori.
Читайте также:


