Грамположительный и грамотрицательный сепсис
Предположительная этиология сепсиса в зависимости от локализации первичного очага
Локализация первичного очага
Наиболее вероятные возбудители
Легкие (нозокомиальная пневмония, развившаяся вне ОРИТ)
Streptococcus pneumoniae, Enterobacteriaceae (Klebsiella spp., E.coli), Staphylococcus aureus
Легкие (нозокомиальная пневмония, развившаяся в ОРИТ)
Pseudomonas aeruginosa, Staphylococcus aureus, Enterobacteriaceae, Acinetobacter spp.
Staphylococcus aureus, Streptococcus spp., Enterobacteriaceae
Enterobacteriaceae (E.coli, Klebsiella spp., Enterobacter spp., Proteus spp.), Enterococcus spp.
Ротоглотка и синусы
Streptococcus spp, Staphylococcus spp.
Streptococcus pneumoniae, Haemophilus influenzae
Staphylococcus epidermidis, Staphylococcus aureus;
Реже– Enterococcus spp., Candida spp.
Патогенез.Сепсис - это бактериальное инфекционное заболевание, с ациклическим течением, которое развивается у лиц с резко сниженными защитными силами организма при наличии инфекционного очага в организме (абсцесс, перитонит, абсцедирующая пневмония, пиелонефрит, гнойный отит, гнойный отоантрит, флебит и перифлебит пупочных сосудов, остеомиелит, гнойный артрит и др.) и протекает системной воспалительной реакцией и полиорганной недостаточностью.
При наличии инфекционного очага в организме (абсцесс, перитонит, абсцедирующая пневмония, пиелонефрит, гнойный отит, гнойный отоантрит, флебит и перифлебит пупочных сосудов, нозокомиальные пневмонии, развивающиеся в ОРИТ, длительное нахождение катетера в магистральных сосудах, остеомиелит, гнойный артрит и др.) в кровь поступают микроорганизмы и токсины. В ответ на это активизируются гуморальные и клеточные механизмы иммунной системы. Развитие органно-системных повреждений при сепсисе, прежде всего, связано с генерализованным повреждением эндотелия сосудистого русла токсинами и различными продуктами распада микроорганизмов, высвобождением большого количества медиаторов воспаления: цитокинов (ФНО-α, ИЛ-1, ИЛ-6, ИЛ-8, ИЛ-10 и др.), белков каскада комплемента (С3а, С5а), факторов свертывания (ФАТ, фактор Хагемана), кининов (брадикинин), серотонина, гистамина, эндорфинов, метаболитов арахидоновой кислоты (лейкотриены, простагландины), протеаз (эластаза, коллагеназа, лизоцим), активных кислородных радикалов (супероксиды, перекись водорода), протеинов адгезии (селектины, ICA,M CD11b/CD18 b и др.). В ответ развиваются системный воспалительный ответ (СВО), ДВС синдром, нарушение перфузии органов и тканей, что ведет к развитию септического шока и полиорганной недостаточности.
Для развития бурного СВО необходимым условием является значительная депрессия механизмов противоинфекционной защиты организма, и, прежде всего, нейтрофильного, макрофагального и его звеньев. Диссеминация микроорганизмов может вообще отсутствовать или быть кратковременной, трудноуловимой. Экзо- и эндотоксины бактерий также могут активировать их гиперпродукцию из макрофагов, лимфоцитов, эндотелия. Суммарные эффекты, оказываемые медиаторами, формируют синдром системной воспалительной реакции [1, 3, 5, 7, 9,10, 11]. СВО – стадийная активация клеток (нейтрофилов, моноцитов/макрофагов, лимфоцитов, тромбоцитов, эндотелиоцитов), продуцирующих цитокины и другие медиаторы и формирующих цитокиновую сеть. При чрезмерной активации это приводит к генерализации воспаления и явлениям системной альтерации. Помимо клинических проявлений (ССВО или SIRS-критерии), СВО имеет дополнительные лабораторные диагностические признаки: повышение концентрации прокальцитонина, белков – реактантов острой фазы воспаления (C-реактивный белок, фибронектин, другие белки-адаптогены) и цитокинов (IL-6, IL-8). При наличии ССВО очевидна высокая предрасположенность организма к возникновению сепсиса.
В развитии СВО выделяют три основных этапа.
1-й этап. Локальная продукция цитокинов в ответ на действие микроорганизмов.
Истинный фагоцитоз в организме осуществляют макрофаги. Процесс фагоцитоза осуществляется и нейтрофилами. Основной функцией нейтрофилов является инициация воспалительной реакции. Биологически активные вещества, декретируемые нейтрофильными гранулоцитами, всегда имеют провоспалительную направленность и делятся на цитокины, работающие в очагах острого воспаления (IL8, IL1, ФНО, ГМ-КСФ и Г-КСФ) и участвующие в регуляторной цепи взаимодействий при хроническом воспалении (ИЛ6, γ-ИФН, трансформаторный ростовой фактор). Нейтрофилы располагают широким спектром поверхностных адгезивных молекул. С их помощью они взаимодействуют с клетками эндотелия сосудов, иммунной системы, тканей органов и со структурными элементами. Цитокиновая сеть занимает особое место среди медиаторов воспаления, контролирует процессы реализации иммунной и воспалительной реактивности. Основными продуцентами цитокинов являются Т-клетки и активированные макрофаги, а также, в той или иной степени, другие виды лейкоцитов, эндотелиоциты посткапиллярных венул (ПКВ), тромбоциты и различные типы стромальных клеток. Цитокины вначале действуют в очаге воспаления и на территории реагирующих лимфоидных органов,выполняя ряд защитных функций, участвуя в процессах заживления ран и защиты клеток организма от патогенных микроорганизмов [1, 3, 5, 9,10, 11, 16].
2-й этап. Выброс малого количества цитокинов в системный кровоток.
Роль выхода содержимого нейтрофильных гранул в процессе воспаления огромна: индуцируются агрегация тромбоцитов, выход гистамина, серотонина, протеаз, производных арахидоновой кислоты, факторов, активирующих свертывание крови, систем комплемента, кининов и др. Малые количества медиаторов способны активировать макрофаги, тромбоциты, выброс из эндотелия молекул адгезии, продукцию гормона роста. Развивающаяся острофазовая реакция контролируется провоспалительными медиаторами (интерлейкинами: IL-1,IL-6,IL-8, фактором некроза опухоли-TNF и др.) и их эндогенными антагонистами, такими как IL-4,IL-10,IL-13, растворимые рецепторы к TNF и др., получившие название антивоспалительных медиаторов. За счет поддержания баланса и контролируемых взаимоотношений между про- и антивоспалительными медиаторами в нормальных условиях создаются предпосылки для уничтожения патогенных микроорганизмов, поддержания гомеостаза. К системным адаптационным изменениям при остром воспалении можно отнести стрессорную реактивность нейроэндокринной системы, лихорадку, выход нейтрофилов в циркуляцию из сосудистого и костномозгового депо, усиление лейкоцитопоэза в костном мозге, гиперпродукцию белков острой фазы в печени, развитие генерализованных форм иммунного ответа.
3-й этап. Генерализация воспалительной реакции.
В случае неспособности регулирующих систем к поддержанию гомеостаза деструктивные эффекты цитокинов и других медиаторов начинают доминировать, что приводит к нарушению проницаемости и функции эндотелия капилляров, запуску синдрома ДВС, формированию отдаленных очагов системного воспаления, развитию моно- и полиорганной дисфункции. В качестве факторов системного повреждения могут выступать любые нарушения гомеостаза, способные восприниматься иммунной системой как повреждающие или потенциально повреждающие. На этой стадии синдрома СВР с позиций взаимодействия про- и антивоспалительных медиаторов возможно условное выделение двух периодов .
Первый (начальный) период гипервоспаления, характеризующийся выбросом сверхвысоких концентраций провоспалительных цитокинов, окиси азота, сопровождается развитием шока и ранним формированием синдрома полиорганной недостаточности (ПОН). Однако уже в данный момент происходит компенсаторное выделение антивоспалительных цитокинов, скорость их секреции, концентрация в крови и тканях постепенно нарастают с параллельным снижением содержания медиаторов воспаления. Развивается компенсаторный антивоспалительный ответ, сочетающийся со снижением функциональной активности иммуннокомпетентных клеток - период " иммунного паралича". У некоторых больных в силу генетической детерминации или изменённой под действием факторов внешней среды реактивности сразу происходит формирование устойчивой антивоспалительной реакции.
Запускающими септический ответ факторами могут являться компоненты клеточной стенки, такие как пептидогликан и тейхоевая кислота, стафилококковый протеин А и стрептококковый протеин М, расположенные на поверхности клеток, гликокаликс, экзотоксины. С практической точки зрения чрезвычайно важно отметить, что скорость реакций септического каскада резко возрастает в условиях гипоксии из-за экспрессии цитокиновых рецепторов на поверхности клеток.
В генезе острой сосудистой недостаточности, лежащей в основе септического шокового синдрома, ведущая роль отводится окиси азота (NО), концентрация которой увеличивается в десятки раз в результате стимуляции макрофагов ТNF, IL-1, IFN, а в дальнейшем секреция осуществляется и клетками гладкой мускулатуры сосудов и сами моноциты активируются под действием NО. В нормальных условиях NО выполняет роль нейротрансмиттера, участвует в вазорегуляции, фагоцитозе. Характерно, что нарушения микроциркуляции при сепсисе носят неоднородный характер: зоны дилатации сочетаются с участками вазоконстрикции.
Полиорганная недостаточность – патологическое состояние, которое формируется и прогрессирует в результате тяжелой неспецифической реакции организма на повреждение или инфекцию и сопровождается несостоятельностью двух и более органно-функциональных систем. При развитии ПОН устанавливается качественно иное патологическое состояние организма, опасность которого определяется скоростью возникновения и углубления дисфункции определенных органных систем.
Для ПОН характерно поражение всех органов и тканей организма агрессивными медиаторами с временным преобладанием симптомов той или иной органной дисфункции – легочной, сердечной, почечной и других органных систем. Сроки выявления и динамика формирования отдельных синдромов весьма вариабельны, дисфункции разных органов могут встречаться в различных сочетаниях. Применительно к характеристике тяжелого сепсиса важно наличие дисфункции иммунной системы и развитие ее крайней формы – иммунной недостаточности [1, 5, 9,15]. В результате дисфункции печени, почек, кишечника появляются новые факторы повреждающего воздействия. В роли таковых выступают промежуточные и конечные продукты нормального обмена в высоких концентрациях (лактат, мочевина, креатинин, билирубин), накопленные в патологических концентрациях компоненты и эффекторы регуляторных систем (калликреин-кининовой, свертывающей, фибринолитической, ПОЛ, нейромедиаторы), продукты извращенного обмена (альдегиды, кетоны, высшие спирты), вещества кишечного происхождения типа индола, скатола, путресцина.
Патофизиология сепсиса и септического шока
Симптомы и течение. Инкубационный период продолжается от нескольких часов до нескольких дней. При эндогенной инфекции длительность инкубационного периода определить трудно. По клиническому течению различают:
· острейший (молниеносный) сепсис, протекающий бурно с развитием септического шока и приводящий к летальному исходу в течение 1-2 дней;
· острый сепсис, который продолжается до 4 недель;
· подострый, длящийся до 3-4 мес;
· рецидивирующий сепсис, протекающий в виде обострений и ремиссий, длится до 6 мес;
· хрониосепсис может продолжаться до года и более.
Сепсис различается также видом возбудителя (стафилококковый, пневмококковый, сальмонеллезный, анаэробный). Воротами инфекции и местом первичного очага [1, 3, 5, 7, 10, 12, 13, 16] (рис. 1).
Клиническая картина сепсиса многообразна. Она складывается из симптомов общей интоксикации и проявлений болезни, обусловленных первичным очагом и метастазами. Сепсис, как правило, начинается остро, однако он всегда предполагает наличие входных ворот, а также явного или скрытого первичного очага. Входными воротами могут быть кожа, слизистые, пупочная ранка, пупочные сосуды, кишечник, легкие и др.
Признаки, связанные с воротами инфекции и первичным очагом, не всегда обнаруживаются достаточно отчетливо, особенно при скрытых очагах инфекции (эзофагит, флебит). Может иметь место интоксикация, проявляющаяся в типичных случаях лихорадкой, чаще интермиттирующего типа с резко выраженным ознобом (в момент прорыва возбудителя в кровь). Реже бывает лихорадка постоянного типа. Лихорадка держится на высоких цифрах. Состояние больного быстро становится тяжелым. Кратковременное возбуждение в начале болезни быстро сменяется заторможенностью. Нарастает анемия.
Кожа имеет бледновато-субиктеричный цвет. На коже, как следствие развития тромбогеморрагического синдрома и септических заносов, появляется экзантема в виде пустул, пузырьков, мелких и более крупных кровоизлияний. Геморрагии могут быть также в конъюнктиву склер и слизистые оболочки полости рта. Развиваются артриты, остеомиелиты, миозиты и абсцессы мышц. Пульс учащается до 120-150 уд/мин, лабильный, наблюдается одышка, не связанная с поражением органов дыхания. АД снижается, границы сердца расширены, тоны приглушены. При поражении клапанов сердца выслушиваются органические шумы. Возможны инфаркты легкого, абсцесс и гангрена легкого, гнойный плеврит.
Очень часто в результате эмболий развивается геморрагический нефрит. Занос инфекции в почки может сопровождаться циститами, пиелитами, паранефритами.
В головном мозге наблюдаются абсцессы с разнообразной общей и очаговой симптоматикой. Вовлекаются в процесс и мозговые оболочки (гнойный менингит). Меняются данные лабораторных исследований- прогрессирует анемия (за счет гемолиза и угнетения кроветворения), число лейкоцитов значительно повышается, однако в тяжелых случаях вследствие резкого угнетения кроветворных органов может наблюдаться и лейкопения. Характерен нейтрофилез со сдвигом ядерной формулы влево (до юных и миелоцитов); СОЭ значительно повышена (до 30-60 мм/ч и более). Отмечается повышенное содержание билирубина (до 35-85 мкмоль/л) и остаточного азота в крови. Свертываемость крови и протромбиновый индекс понижены (до 50-70%), снижено также содержание кальция и хлоридов в крови. Содержание общего белка снижено, особенно за счет альбуминов, уровень глобулинов (альфа- и гамма-глобулины) повышен. В моче - белок, лейкоциты, эритроциты, цилиндры, содержание хлоридов понижено, мочевины и мочевой кислоты - повышено. Описанные изменения характерны для острого сепсиса, вызванного различными возбудителями. Непременными симтомами развёрнутой картины сепсиса являются признаки ПОН (табл. 2).
Этиология сепсиса отражается на клинической симптоматике. Острейший (молниеносный) стафилококковый сепсис наблюдается редко, но протекает исключительно тяжело, с потрясающим ознобом, высокой лихорадкой, тяжелейшей интоксикацией, цианозом, быстрым падением АД. Может привести к смерти больного в течение 1-2 дней. Метастазов при этой форме не обнаруживается. Чаще стафилококковый сепсис протекает в острой форме.
Воротами инфекции служат поражения кожи и подкожной клетчатки (фурункул, карбункул, пустула, импетиго, панариций) или слизистых оболочек зева, респираторного тракта и мочевых путей. Температурная кривая гектического, неправильного, реже постоянного типа. На коже отмечаются геморрагии, ломкость сосудов повышена, может быть гнойничковая сыпь, кровоизлияния в слизистые оболочки. Рано увеличиваются печень и селезенка. Часто наблюдаются многочисленные гнойные метастазы (в почках, эндокарде, в мышцах), остеомиелиты, панариции, артриты. Стафилококковый гной густой, гомогенный, желтоватого цвета. В крови лейкоцитоз со сдвигом формулы влево, СОЭ повышена. Стафилококковый сепсис может принимать рецидивирующее течение, когда лихорадка и обострения (что связано с формированием новых очагов) сменяются ремиссиями. Эта картина наблюдается до полугода и больше. Хронический стафилококковый сепсис может длиться несколько лет, сопровождается множественными метастазами и приводит к амилоидозу внутренних органов.
При сепсисе, обусловленном Pseudomonas aeruginosa (синегнойная палочка), на первый план выступают признаки общей интоксикации, хотя развивается он как осложнение локализованной инфекции (раны, ожоги и др.). При этом часто отделяемое ран окрашивает повязки в сине-зеленый цвет, такого же цвета могут быть фибринозные налеты на раневой поверхности. Обильное жидкое отделяемое имеет гнилостный запах. Сепсис развивается чаще при ожогах III и IV степени, после флегмон, перитонитов и др. Лихорадка и другие проявления общей интоксикации резко выражены и быстро нарастают. Вторичные очаги (метастазы) могут локализоваться в легких, суставах, мочеполовых органах.
Анаэробный сепсис чаще начинается с локальных поражений в области головы и шеи (язвенно-некротический гингивит, поражение миндалин, глотки, синуситы, отиты, остеомиелиты), а также после операций на органах брюшной полости. Сепсис начинается бурно, протекает тяжело. Температура тела достигает 40°С и выше, температурная кривая чаще гектическая. Может развиться септический шок. Для вторичных очагов характерно быстрое абсцедирование. Развиваются абсцессы мозга (85% всех абсцессов связано с анаэробной инфекцией), абсцесс печени, легких. Чаще это связано с инфекцией В. fragilis, который обладает уникальной среди анаэробов способностью вызывать абсцедирование без участия других микробов. Это связано с наличием особого капсульного полисахарида. При других анаэробных инфекциях абсцессы могут формироваться лишь в присутствии других синергически действующих микроорганизмов.
Клинические и лабораторные критерии органной недостаточности при сепсисе
Сепсис- тяжёлое инфекционное заболевание, вызываемое разными возбудителями и их токсинами, проявляющееся своеобразной реакцией организма с однотипной, несмотря на различие возбудителей, клинической картиной.
•В зависимости от принципа, положенного в основу классификации сепсиса, существует несколько её вариантов: Различают первичный и вторичный сепсис.
-Первичный сепсис(криптогенный). Встречают относительно редко. Происхождение его не ясно. Предполагают связь с аутоинфекцией (хроническим тонзиллитом, кариозными зубами, дремлющей инфекцией).
- Вторичный сепсис развивается на фоне существования в организме гнойного очага: гнойной раны, острого гнойного хирургического заболевания, а также после оперативного вмешательства.
• По локализации первичного очага: хирургический, гинекологический, урологический, отогенный, одонтогенный сепсис и т.д.
•По виду возбудителя: стафилококковый, стрептококковый, колибациллярный, синегнойный, анаэробный. Иногда выделяют грамположительный и грамотрицательный сепсис.
•По источнику: раневой, послеоперационный, воспалительный сепсис (флегмона, абсцесс, остеомиелит и т.д.), сепсис при внутренних болезнях (ангина, пневмония и др.).
•По времени развития: ранний (до 14 дней с момента повреждения) и поздний (более 14 дней с момента повреждения).
•По типу клинического течения: молниеносный, острый, подострый, хронический сепсис.
-Молниеносный сепсисхарактеризуется быстрой генерализацией воспалительного процесса и уже в течение нескольких часов (12-24 ч) после повреждёния можно выявить его клинические симптомы. Длительность течения составляет 5-7 дней, чаще наступает летальный исход, даже при своевременном лечении.
- Острый сепсис характеризуется более благоприятным течением, клинические симптомы проявляются в течение нескольких дней. Длительность течения составляет 2-4 нед.
- Подострый сепсис продолжается 6-12 нед, исход благоприятный.
-Если не удаётся ликвидировать острый сепсис, процесс переходит в хроническую стадию. Хронический сепсистечёт годами с периодическими обострениями и ремиссиями.
•По характеру реакций организма: гиперергический, нормергический, гипергический сепсис.
•По клинико-анатомическим признакам: септицемия (без метастазов) и септикопиемия (со вторичными метастатическими гнойными очагами).
Этиология- Возбудителями сепсиса могут быть почти все существующие патогенные и условно патогенные бактерии. Наиболее распространены стафилококки, стрептококки, синегнойная палочка, протей, анаэробная флора и бактероиды.
Главные жалобы - чувство жара и озноб, связанные с высокой лихорадкой, которую нельзя связать с нарушением оттока отделяемого из гнойного очага. При сепсисе без метастазов амплитуда температурной кривой обычно небольшая , а при сепсисе с метастазами чаще возникает гектическая или ремитирующая лихорадка с сильными ознобами и проливными потами.
Остальные жалобы менее постоянны. Больных беспокоят общая слабость, потеря аппетита, бессонница, иногда профузная диарея. В части случаев больные эйфоричны, возбуждены и не отдают себе отчёта в тяжести своего заболевания. Другие пациенты пассивны и находятся в состоянии прострации.
Объективное исследование- Общий вид септического больного достаточно характерен. Лицо обычно осунувшееся, землистого, иногда желтоватого цвета. Язык сухой и обложен налётом. На теле часто видна петехиальная сыпь. У длительно болеющих возникают пролежни.
Пульс обычно учащён. АД нормальное или несколько снижено. При развитии септического шока давление может снижаться менее 70-80 мм рт.ст. При выслушивании сердца иногда определяют диастолический шум аортальной недостаточности (при этом обычно снижается диастолическое АД). Со стороны дыхательной системы выявляют одышку, кашель, хрипы.
Течение сепсиса характеризуется прогрессивным ухудшением общего состояния и истощением больного. Гибель пациентов наступает вследствие прогрессирующей интоксикации и истощения, присоединившей-ся септической пневмонии, развития вторичных гнойников в жизненно важных органах, поражения клапанов сердца, острых расстройств кровообращения и т.д.
Лабораторные данные- При исследовании крови обнаруживают лейкоцитоз со значительным сдвигом лейкоцитарной формулы влево, прогрессирующее снижение содержания гемоглобина и количества эритроцитов, возможна тромбоцитопения. Резко увеличивается СОЭ.
Важное исследование для выявления бактериемии - посев крови, его проводят не менее 3 раз ежедневно в течение 3 дней подряд.
В моче определяют протеинурию, эритроцитурию, лейкоцитурию и цилиндрурию.
Септический шок- острые расстройства кровообращения, происходящие при поступлении в кровеносное русло значительных порций микроорганизмов и их токсинов - септический шок.
1.Общие симптомы системной воспалительной реакции.
•Температура выше 38 ?С или ниже 36 ?С.
•ЧСС более 90 в мин.
•Частота дыхательных движений более 20 в мин или рСО2меньше 32 мм. рт.ст.
2.Признаки органной недостаточности.
•Лёгкие - необходимость ИВЛ или инсуфляции кислорода для поддержания р02выше 60 мм рт.ст.
•Печень - содержание билирубина свыше 34 мкмоль/л или активность аминотрансфераз более чем в 2 раза выше по сравнению с нормальными величинами.
•Почки - повышение концентрации креатинина свыше 0,18 ммоль/ л или олигурия меньше 30 мл/ч на протяжении 30 мин и более.
• Сердечно-сосудистая система - снижение АД ниже 90 ммрт.ст, приводящее к необходимости применения симпатомиметиков.
•ЦНС - заторможённость или сопорозное состояние сознания при отсутствии черепно-мозговой травмы или нарушений мозгового кровообращения.
Лечение сепсиса должно быть местным (хирургическим) и общим.
Особенности местного лечения
При сепсисе существует ряд особенностей лечения первичного и вторичных очагов инфекции.
Особое значение придают удалению некротизированных тканей из очага вплоть до ампутации конечности на необходимом уровне. После операции целесообразно применение ультразвука, лазера, обработки пульсирующей струёй антисептика.
Не менее ответственным при вскрытии очагов считают вопрос о том, оставить ли рану открытой или наложить глухой шов с активным дренированием. На этот вопрос однозначного ответа нет.
В настоящее время распространены методы глухого или частичного шва раны в сочетании с длительным промыванием её растворами антибиотиков и антисептиков и одновременной вакуумной аспирацией отделяемого.
Очень важно не только санировать очаг, но и обеспечить правильную иммобилизацию (гипс, аппарат), а также как можно раньше (конец 2-й - начало 3-й нед) предусмотреть возможность наложения вторичных швов или кожной пластики.
После вскрытия гнойный очаг превращается в гнойную рану, общие принципы её лечения общеизвестны, при терапии необходимо учитывать фазность процесса. Использование гипербарической оксигенации и управляемых абактериальных сред позволяет улучшить эффект местного лечения ран.
Общее лечение -Лечение сепсиса комплексное и состоит из антибиотикотерапии, инфузионно-трансфузионной терапии, респираторной поддержки, иммунокоррекции, компенсации функций органов и систем.
С первого дня без учёта посева из раны назначают комбинацию из двух антибиотиков первой очереди (например, полусинтетические пенициллины + аминогликозиды) или один препарат из группы антибиотиков второй очереди (амоксициллин + клавулановая кислота, цефалоспорины, полусинтетические аминогликозиды).
Эффективными способами детоксикации в остром периоде считают форсированный диурез и пролонгированную гемофильтрацию при по- лиорганной недостаточности.
Для поддержания дыхательной функции используют дыхание кислородом, а по показаниям ИВЛ.
Нормализации электролитного и кислотно-основного состояния достигают введением растворов с ионами К+, при метаболическом ацидозе внутривенно вводят раствор гидрокарбоната натрия.
Парентеральное питание осуществляют путём внутривенной инфузии белковых препаратов и жировых эмульсий, а также концентрированных растворов глюкозы с инсулином.
Гипопротеинемию и анемию корригируют переливанием крови, нативной плазмы, свежезамороженной плазмы, альбумина, протеина и др.
Для коррекции нарушения свёртывания крови и протеолиза по показаниям вводят апротинин, препараты кальция, гепарин натрий (надропарин кальций).
В большом мире, перефразируя классиков, делаются серьезные дела: запускаются космические корабли, покоряются земные полюса, изобретаются лекарства от неизлечимых болезней. В то же время в микромире тоже кипят нешуточные страсти: вирусы и бактерии пытаются выжить в условиях жестких реалий и тотальной медицинской охоты.
Бактерии: кто они?
Микроорганизмы широко распространены как в окружающем мире, так и внутри человеческого тела.
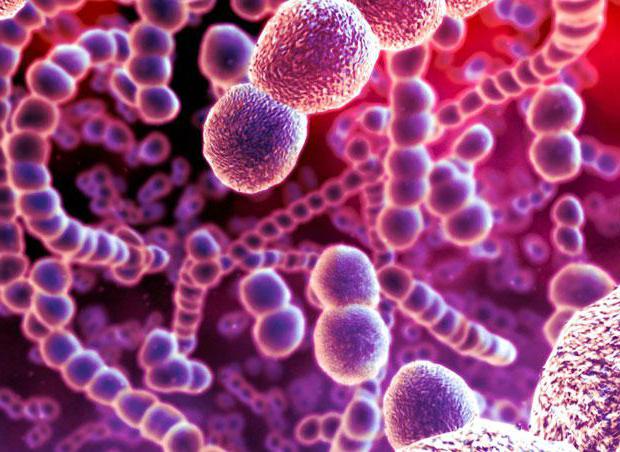
Отличия по Граму
Впервые термин "грамположительные и грамотрицательные бактерии" в науку ввел датский ученый Грам.
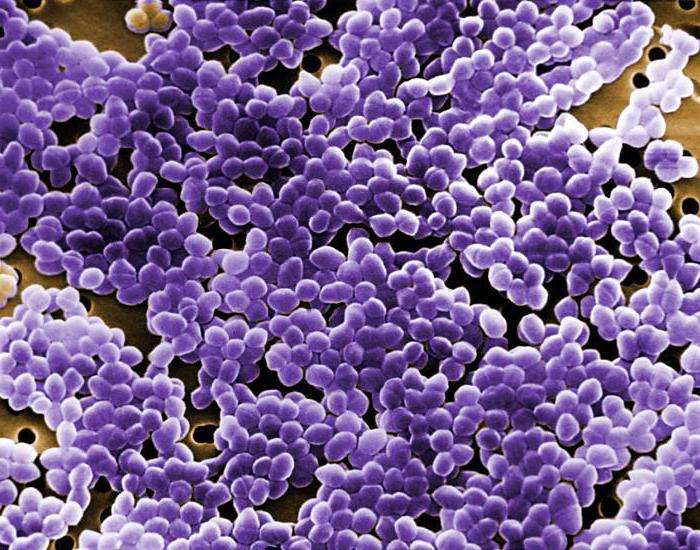
Использовав при окрашивании микроорганизмов специальный краситель генцианвиолет, бактериолог заметил, что одна группа бактерий поддается окраске, в отличие от второй. Позже ученый выяснил, что причиной этому стала клеточная стенка. Таким образом, окрашиваемые субстанции получили название грамположительные бактерии, а те, которые на краситель не реагировали – грамотрицательные.
Грамположительный мир
Эти микроорганизмы окрашиваются способом Грама в фиолетовый цвет. Смысл процедуры состоит в том, что толщина защитного слоя бактериальной клетки довольно высока, за счет чего краситель удерживается. Грамположительные бактерии представлены стафилококками, стрептококками. Кроме того, грамположительные бактерии – возбудители таких опасных недугов, как газовая гангрена, столбнячная инфекция, сибирская язва. От грамотрицательных бактерий они отличаются по строению и толщине клеточной стенки. Именно она определяет внешний вид микроорганизмов: спиралевидный холерный вибрион, шаровидная кокковая форма. Бактериальная клетка отличается от клеток млекопитающих наличием жесткого защитного каркаса, состоящего из плотного биополимерного слоя, и химическим составом. Этим обусловлена реакция бактерий на действие антибиотиков.
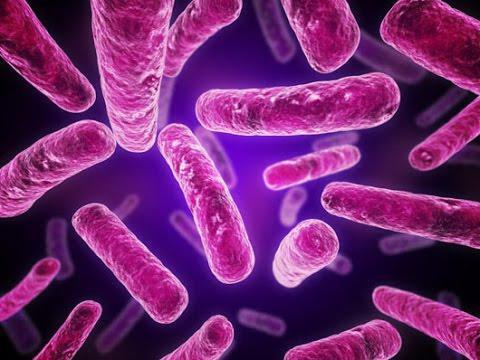
Грамположительные бактерии имеют толстый ригидный слой (клеточную стенку). Защитная оболочка состоит из полипептидов и полисахаридов. До 70% стенки составляет муреиновый мешок. В его состав входят: лизин, ацетилглюкозаминин, ацетилмурамовая кислота, диаминопимелиновая и тейхоевые кислоты.
Основные виды грамположительных бактерий
Большинство опасных для человека микроорганизмов – грамположительные бактерии. Они вызывают такие заболевания, как ботулизм или столбняк, эти болезни плохо поддаются лечению. Кроме того, микоплазму, которую не относят к этому типу, также произвели на свет грамположительные бактерии.
Виды грампозитивных микроорганизмов:
- кокки: клетки, соединенные между собой с помощью целлюлозы; в основном это анаэробные молочнокислые стрептококки;
- палочки: спорообразующие представлены анаэробными клостридиями; не способные образовывать споры – молочнокислые лактобациллы;
- коринеморфы: отличаются склонностью к изменению формы – это стрептомицетовые и пропионовокислые бактерии.
Подобные микроорганизмы вызывают массу недугов. Стафилококки провоцируют грибковые инфекции. Особенно опасен золотистый стафилококк.
Стрептококковые микроорганизмы вызывают фарингиты, рожу, реже пневмонию, сепсис.
Энтерококки часто поражают мочевыводящие пути, сердечную мышцу и провоцируют нагноения в ранах.
Заражение пневмококком зачастую проходит в сопровождении острых симптомов. Синуситы, отиты, внезапные генерализированные пневмонии – вот список заболеваний, вызванных этим возбудителем.
Что касается палочек, то самая известная из них – дифтерийная палочка, выделяющая смертельно опасные токсины и относящаяся к коринебактериям. Помимо нее, палочками вызываются сибирская язва и ботулизм.
Газовую гангрену вызывают бактерии под названием клостридии. Заболевание столбняком также обязано своим существованием этому виду бактерий. Причем столбнячные споры очень живучи: выдерживают длительное кипячение и замачивание в дезинфицирующих растворах.
Грамотрицательные микроорганизмы
В отличие от грампозитивных собратьев, они не окрашиваются в характерный цвет.
Напомним, что грамположительные бактерии, строение которых отличается более плотной клеточной оболочкой, не теряют фиолетовый цвет даже во время промывания. Тогда как грамотрицательные прокариоты поддаются полному обесцвечиванию. Но при этом контрастный сафранин окрашивает эти бактерии в розовато-красные цвета. Несмотря на более тонкую стенку, которая прочнее, нежели у иного вида бактерий, грамотрицательные микроорганизмы сложнее поддаются действию антител.
Заболевания, вызываемые грамотрицательными бактериями
Грамположительные и грамотрицательные бактерии отличаются реакцией на антибиотики. Более устойчивой к ним является вторая группа микроорганизмов.
Многие виды представляют собой объект пристального внимания медицины. Это бактерии, вызывающие венерические болезни: гонорею, сифилис, хламидийные инфекции. Грамотрицательные патогены, провоцирующие респираторные заболевания - моракселла катаралис, проблемы с дыханием - легионелла, клебсиелла. Также эти устойчивые бактерии вызывают менингит, нарушения пищеварения или язвенную болезнь желудка (сальмонелла, хеликобактер пилори, эшерихия коли). По форме бактерии довольно разнообразны: спириллы, палочки, спирохеты, вибрионы, трубчатые чехлы.
Знания о микроорганизмах – на пользу медицине
Информация о возбудителях различных болезней, как грамположительных, так и грамотрицательных, значительно упростила лечение многих недугов. Понимание того факта, что мембрана грамотрицательных бактерий прочнее остальных, позволила ученым выяснить их важное свойство: устойчивость ко многим видам антибиотиков. Кроме прочего, знания о мутациях и приспосабливании микроорганизмов к лекарственным препаратам также улучшили качество лечения бактериальных инфекций. Немаловажным аспектом является информация о том, что прежде всего влияют на организм токсины, выделяемые грамположительными и грамотрицательными видами бактерий.
Но наука не стоит на месте, и уже разработаны медикаменты, которые способны справиться с мембранной защитой грамотрицательных микроорганизмов. При этом имеет значение состояние макроорганизма в целом: его иммунный ответ и объемы воспалительных процессов.
Помимо заболеваний, бактерии приносят пользу: с их помощью можно готовить полезные кисломолочные продукты, очищать сточные воды, использовать в животноводстве.
Читайте также:


