Какие стрептококки вызывают ревматизм
ВНИМАНИЕ! САЙТ ЛЕКЦИИ.ОРГ проводит недельный опрос. ПРИМИТЕ УЧАСТИЕ. ВСЕГО 1 МИНУТА.
Ревматизм представляет собой воспалительное заболевание, возникающее как аутоиммунное следствие инфекции, вызванной b-гемолитическими стрептококками группы А.
Этиологическая связь стрептококков группы А с ревматизмом подтверждается клиническими и эпидемиологическими данными. В острой фазе ревматизма всегда обнаруживаются иммунологические признаки перенесенной ранее стрептококковой инфекции и повышение титров антител к стрептококковым антигенам.
Обычно ревматизм обостряется после перенесенной стрептококковой инфекции. Первичные и повторные атаки ревматизма можно предотвратить с помощью антибактериальной терапии (бициллина, пенициллина).
Воротами инфекции при начале ревматического процесса служит глотка.
Выявлена перекрестная реактивность некоторых стрептококковых антигенов с тканями сердца. В основе патогенеза ревматизма находится аутоиммунный механизм (с генетической предрасположенностью и без нее).
В диагностике ревматизма используют серологические исследования, в которых определяют титры антител к О-стрептококку (антистрептолизиновый тест, к гиалуронидазе, антидезоксирибонуклеазе). При однократном исследовании повышенным сяитают титры не менее 250 ед Тодда у взрослых и 333 ед – у детей в возрасте старше 5 лет.
Используют антистрептозимовый тест. Это РПГА, в которой используют эритроцитарный антигенный диагностикум. Определение антител к внеклеточным стрептококковым антигенам служит чувствительным индикатором недавно перенесенной стрептококковой инфекции.
Streptococcus pneumoniae(пневмококк). Этот стрептококк имеет тропизм к легочной ткани, что обусловлено наличием специфических адгезинов; имеет вытянутую ланцетовидную форму. Располагается попарно, окружен полисахаридной капсулой. Под капсулой расположен М-белок, придающий типовую специфичность. Грамположителен, спор и жгутиков не имеет, на кровяном агаре образует мелкие колонии с зоной гемолиза зеленого цвета (a-гемолиз). Разлагает инулин.
Антигенная структура
Имеет полисахаридный антиген клеточной стенки; по К антигену – 90 сероваров.
Факторы патогенности
По данным ВОЗ пневмококковая инфекция является одной из ведущих причин детской смертности в мире, вызывая до 700 тыс. летальных случаев ежегодно у детей моложе 5 лет.
Пневмококки образуют пневмолизин – мембраноповреждающий токсин, протомеры токсина адсорбируются холестерином, входящим в состав билипидного слоя мембраны, далее протомеры олигомеризуются в гептамеры, которые после ряда конформационных изменений проникают через цитоплазматическую мембрану, через образовавшуюся пору (в виде ножки) происходит вход и выход небольших молекул и ионов, что ведет к осмотическому лизису эритроцитов; имеют лейкоцидин; М-белок и капсула обеспечивают способность к адгезии и устойчивость к фагоцитозу. Имеется гиалуронидаза и фермент пептидаза, которая расщепляет секреторный иммуноглобулин А, нейроминидаза.
Важное значение имеет субстанция С – холинсодержащая тейхоевая кислота клеточной стенки, специфически взаимодействующая с С-реактивным белком, в результате чего происходит активация системы комплемента и высвобождение медиаторов острой фазы воспаления, которые аккумулируются в легочной ткани, что стимулирует миграцию полиморфноядерных фагоцитов и развитие воспаления.
Инфекции вирулентным сероваром 3 могут сопровождаться образованием полостей в паренхиме легких. Из первичного очага возбудитель может проникать в плевральную полость и перикард или гематогенно диссеминировать и вызывать менингиты, эндокардиты, поражения суставов.
Резистентность
Характериситка заболевания
Патогенез
Пневмококки персистируют в верхних дыхательных путях. При ослаблении иммунитета они попадают в нижние дыхательные пути, возникает эндогенная инфекция, особенно если есть предрасполагающие факторы: застойные явления в легких; снижение уровня секреторных иммуноглобулинов А, активности макрофагов, разрушение сурфактанта легких.
В связи с выделением патогенных пневмококков от больного или носителя возможно воздушно-капельное заражение чувствительных людей, т.е. экзогенная инфекция. Пневмококки могут вызывать менингит.
Клиническая картина
Лабораторная диагностика
Материал для диагностического исследования берут в зависимости от формы пневмококковой инфекции: при пневмонии – мокроту, при сепсисе – кровь, при гнойном заболевании – гной, при отите – отделяемое из слухового прохода. Материал важно забрать до начала этиотропного лечения. Для обнаружения антител исследуют сыворотку крови.
Экспресс-методы (обнаружение возбудителя в патологическом материале):
1.Микроскопическое исследование – мазок из патологического материала с окраской по Граму. Обнаруживаются грамположительные капсульные диплококки.
3.Обнаружение антигена в сыворотке крови или ликворе (методы – РСК, латекс-агглютинация, встречный иммуноэлектрофорез).
Экспресс-методы являются ориентировочными, так как не всегда обнаружение пневмококка свидетельствует о его этиологической роли (часто возможно носительство), и возбудитель не обнаруживается после начала этиотропного лечения.
Бактериологический метод. Материал (не позднее 1-2 часов с момента забора) засевают на 5%-й кровяной агар, культивируют в эксикаторе со свечой (источник СО2) 20-24 часа при температуре 37°С; далее отбирают подозрительные колонии, дающие a-гемолиз, микроскопируют (окраска по Граму), отсевают в сывороточный бульон; определяют чистоту культуры (окраска по Граму).
Серологический метод. Определяют противокапсульные антитела и их динамику в сыворотке крови в реакциях с аутоштаммами; используют также РСК и РПГА с эталонными штаммами пневмококка.
Биологический метод. Внутрибрюшинно заражают белых мышей исследуемым материалом (чаще мокротой). Погибших мышей вскрывают, делают мазки-отпечатки, посев крови и органов на кровяной агар с последующей идентификацией возбудителя.
Лечение
Все стрептококки серогруппы А чувствительны к β-лактамным антибиотикам, включая бензилпенициллин, в меньшей степени – к макролидам и азалидам
Бензилпенициллин (пенициллин G) остается препаратом выбора для лечения внегоспитальных пневмококковых пневмоний, хотя к резистентность к нему постепенно увеличивается. Также для лечения пневмоний используют другие β-лактамы (амоксициллин, цефалоспорины), макролиды и азалиды, фторхинолоны (левофлоксацин).
Профилактика
Для предупреждения развития хронических стрептококковых инфекций, связанных с персистенцией возбудителя и образованием L-форм, необходимо проведение адекватной антибиотикотерапии. За детьми, перенесшими повторные ангины, скарлатину устанавливают диспансерное наблюдение.
Специфическая профилактика пневмококковых заболеваний проводится с помощью вакцин, приготовленных из высокоочищенных капсульных полисахаридов тех серовариантов, которые чаще вызывают заболевания. В настоящее время имеются две такие вакцины – 23-валентная пневмококковая полисахаридная вакцина (PPSV23, Пневмо23) и 7-валентная конъюгированная пневмококковая вакцина (PCV7), которая рекомендуется для вакцинации детей моложе 5 лет.
9.3. Семество Leuconostaceae
Семество Leuconostaceae включает род Leuconostoc.
9.3.1. Бактерии рода Leuconostoc
Бактерии рода Leuconostoc выделены из клинического материала Handwerger в середине 80-х годов прошлого века.
Leuconostoc – грамположительные, каталазонегативные, неспорообразующие, неподвижные, факультативно анаэробные кокки, широко распространенные в окружающей среде.
Классификация
Род Leuconostoc включает 9 видов, из них L. mesenteroides и L. lactis выделяют чаще из молока и молочных продуктов, L. pseudomesenteroides и L. citreum обнаруживаются на растениях, овощах, молочных продуктах, L. gelidum и L. carnosum выделяются из мяса и мясных продуктов, L. fallax – из консервированных, L. argentinum – выделен в Аргентине из непастеризованного молока. Эти микроорганизмы чаще выделяют при инфекциях у больных с иммунодефицитами (при злокачественных новообразованиях, длительной катетеризации, из интраабдоминальных абсцессов, абсцессов печени, из раневого отделяемого при послеоперационных инфекциях).
Факторы патогенности
К факторам патогенности данных возбудителей относится лейкоцидин (бактерицин), инактивирующий протеолитические ферменты и бактерицидный в отношении лактобактерий.
Лабораторная диагностика
Клиническое значение имеет выделение микроорганизмов рода Leuconostoc только из заведомо стерильных источников (кровь, ликвор, перитонеальная и суставная жидкость). Материал засевают на кровяной агар, где микроорганизмы дают рост мелких колоний с альфа-гемолизом. При идентификации учитываются следующие признаки: каталазный тест отрицательный, образуют газ на средах с глюкозой, не вызывают гидролиз аргинина, растут при температуре 10 о С.
Лечение
Пенициллин, ампициллин, клиндамицин.
9.4. Семество Enterococсаeae
Семество Enterococсаeae включает род Enterococcus, включающий более 10 видов. Наиболее часто от человека выделяют 2 основных вида – E. faecalis и E. faecium. Это условно-патогенные микроорганизмы, вызывающие оппортунистические инфекции мочевыводящих путей, желчных путей, абсцессы брюшной полости, подострый септический эндокардит, сепсис. Данные возбудители отличаются весьма широким спектром резистентности к антибиотикам. E. faecium обычно более устойчив, чем E. faecalis.
9.4.1. Род Enterococcus
Род Enterococcus объединяет кокковидные бактерии, которые в мазках располагаются попарно или короткими цепочками. Спор не образуют, некоторые виды подвижны (имеют жгутики); капсул не имеют. Факультативные анаэробы, хемоорганотрофы, метаболизм ферментативный, расщепляют углеводы с образованием кислоты; каталазоотрицательны, иногда восстанавливают нитраты в нитриты.
Хорошо растут в интервале 10-45°С на простых питательных средах, устойчивы к действию окружающей среды, выдерживают нагревание до 60°С в течение 30 минут. Теллурит калия, азид натрия, желчные соли, кристаллический фиолетовый, налидиксовая кислота, пенициллин, неомицин, цефалоспорины не угнетают роста энтерококков, что используется для создания элективных питательных сред и проведения микробиологической диагностики.
На средах с теллуритом калия дают черные колонии вследствие восстановления теллура.
На кровяном агаре образуют негемолитические или α-гемолитические колонии.
В качестве селективных и дифференциально-диагностических сред применяют желчно-щелочной агар (растут только энтерококки), молочную среду с метиленовым синим (определяют восстановление метиленового синего), среду с трифенилтетразолий-хлоридом (ТТХ). На последней среде оценивают гемолиз и способность восстанавливать ТТХ.
Представители рода Enterococcus относятся к серогруппе D согласно серологической классификации Р. Ленсфильд
Энтерококки обладают генетически детерминированной устойчивостью к многим β-лактамам, включая пенициллиназоустойчивые пенициллины и цефалоспорины. Также они проявляют умеренный уровень резистентности к фторхинолонам и аминогликозидам. Штаммы энтерококков, продуцирующие β-лактамазу, обычно устойчивы к аминогликозиду гентамицину.
Увеличивается частота обнаружении изолятов энтерококков, устойчивых к ванкомицину. Механизм данного вида резистентности связан с изменением структуры клеточной стенки энтерококков.
Кроме того, в организме человека энтерококки устойчивы и к сульфаниламидам, включая бисептол.
Отсюда при подозрении на энтерококковую инфекцию (например, при подостром септическом эндокардите) проводят посевы материала на селективные и дифференциально-диагностические среды для энтерококков и идентифицируют ихпо вышеуказанным свойствам. Видовая идентификация возбудителей возможна также с помощью автоматизированных систем биохимической идентификации микроорганизмов, а также генетическими методами (ПЦР).
Лечение данных инфекций представляет сложную задачу. Используются комбинации антибиотиков, наиболее эффективных в отношении энтерококков. Они включают пенициллин, ампициллин или ванкомицин в сочетании с аминогликозидами (стрептомицином или гентамицином).
В течение многих лет острая ревматическая лихорадка (ревматизм) была наиболее распространенным ревматическим заболеванием и наиболее частой причиной пороков сердца. Но в последнее время наблюдается значительное уменьшение количества больных благодаря разработке эффективных профилактических мер (главным образом применение антибиотиков во время стрептококковой инфекции). Современные врачи гораздо чаще имеют дело с последствиями перенесенного в детстве ревматизма (острой ревматической лихорадки), относящегося ко времени, когда не была широко распространена профилактика антибиотиками, чем непосредственно с болезнью.
Острая ревматическая лихорадка представляет собой заболевание соединительной ткани, преимущественно поражающее сердечно-сосудистую систему (пороки сердца – нарушение работы клапанов, кардит – воспаление сердца), нервной системы и кожи (появление особенных ревматических узелков, пятен красного цвета, имеющих форму круга). Такое заболевание в основном поражает людей молодого возраста (7-15 лет) после инфицирования организма определенной инфекцией (бета-гемолитическим стрептококком группы А).
Многие ошибочно считают ревматическую лихорадку болезнью суставов. Ревматическое поражение суставов является полностью обратимым и протекает кратковременно. При этом поражение сердца, наоборот, приводит к пороку сердца и раннему прекращению трудовой деятельности. В 20-25 % случаев развивается порок сердца. Порок сердечного клапана может протекать совсем без симптомов в течение нескольких лет, выявить его можно во время профилактического осмотра либо при развитии осложнения (к примеру, сердечной недостаточности или аритмии).
Симптомы ревматизма
Как правило, симптомы острой ревматической лихорадки проявляются спустя две-три недели после перенесенной инфекции, вызванной стрептококками (в большинстве случаев – ангины, реже – инфекции кожи – пиодермии). Самочувствие ухудшается, поднимается температура, появляется болезненность, покраснение и припухание суставов (артрит). Как правило, участвуют средние и крупные суставы (коленные, плечевые, локтевые), в редких случаях – мелкие суставы стоп и кистей. Могут появляться мигрирующие боли (они изменяют местоположение, могут находиться в разных суставах). Продолжительность воспаления суставов (артрита) составляет не более одной недели – десяти дней.
Одновременно с артритом развивается ревмокардит – поражение суставов. При этом могут появиться как незначительные изменения, выявить которые можно только при специальном обследовании, так и тяжелые поражение, сопровождающиеся сердцебиением, одышкой, отеками, болью в сердце.
Опасность ревмокардита состоит в том, что даже при легком течении заболевания воспаление влияет на сердечные клапаны (структуры внутри сердца, которые разделяют сердечные камеры, необходимые для обеспечения правильного тока крови). Происходит сморщивание, потеря эластичности и разрушение клапанов. Итогом этого становится то, что клапаны либо не могут полностью раскрыться, либо неплотно смыкаются. В итоге развивается клапанный порок. Чаще всего развитие ревмокардита приходится на возрастной период 12-25 лет. В более позднем возрасте первичное ревматическое поражение клапанов сердца встречается очень редко.
В 15 % случаев развивается ревматическое поражение нервной системы (в детском возрасте – чаще). Ребенок в результате становится рассеянным, капризным, раздражительным. Он начинает быстро уставать, у него возникают проблемы с памятью, изменяется походка, почерк, речь.
Анулярная эритема - проявление острой ревматической лихорадки в виде кольцевидных высыпаний на коже, а также ревматические (подкожные) узелки, которые, на сегодняшний день, встречаются редко.
Причины ревматизма
Факторы риска ревматизма
Ослабленные пациенты и люди, чьи родственники переносили какие-либо ревматические болезни, в том числе и патологию, о которой идет речь, имеют высокий риск заболеть. Чаще всего острая ревматическая лихорадка развивается у детей от 7 до 15 лет. Маленькие дети и взрослые болеют значительно реже. Случаи возникновения болезни у детей до трех лет крайне редки.
Необходимо помнить, что ревматическая лихорадка входит в группу социальных болезней. При неблагополучных жизненных условиях (грязь, переохлаждения и т.д.), плохом питании вероятность развития этого заболевания значительно повышается.
Профилактика ревматизма
Первичная профилактика острой ревматической лихорадки (т.е. предупреждение ее появления у здоровых людей) состоит в грамотном лечении стрептококковой инфекции (фарингита, ангины и стрептококковых инфекций кожи). При стрептококковой инфекции обязательно принимать антибиотики! Продолжительность терапии антибиотиками (обычно это производные пенициллина) не должна быть меньше десяти дней (если курс будет более коротким, появляется вероятность того, что инфекция сохранится). В современной практике лечения стрептококковых тонзиллитов не используют такие препараты, как бисептол, тетрациклин, офлоксацин, левомицетин.
Вторичная профилактика, направленная на предотвращение повторных атак острой ревматической лихорадки, предполагает применение в течение не меньше пяти лет бензатин бензилпенициллина (ретарпен, экстенциллин) - антибиотика продленного действия.
В повседневной жизни не стоит пренебрегать простыми правилами: придерживаться распорядка дня, регулярно правильно питаться, заниматься физкультурой и спортом, проводить закаливания, на время изолировать человека с температурой. Закаленный организм лучше сопротивляется проникновению стрептококковой инфекции. Стрептококк широко представлен в окружающем нас мире: он присутствует в пыли, грязном белье, носовых платках. Из этого можно сделать вывод о важности проветривания и влажной уборки помещений, регулярной смены белья. Нужно своевременно лечить хронический тонзиллит, кариозные зубы.
Диагностика ревматизма
Выявление острой ревматической лихорадки основано в большинстве случаев на проведении анализа клинической картины заболевания. Очень важно определить стрептококковую инфекцию (инфекцию кожи, ангину) не позднее чем за шесть недель до начала поражения суставов. Довольно специфический признак острой ревматической лихорадки – это сочетание суставных и сердечных симптомов.
Крайне важно найти возбудителя заболевания, для чего нужно проводить посевы миндалин и т.п.
Требуется проведение следующих лабораторных анализов: повышение содержания в крови С-реактивного белка, увеличение СОЭ - скорости оседания эритроцитов.
Для подтверждения диагноза очень важно проведение ЭКГ – электрокардиографии и ЭхоКГ – исследование сердца с помощью ультразвука.
Лечение ревматизма
Основа лечения острой ревматической лихорадки – неукоснительное соблюдение режима если болезнь активна, назначают строгий постельный режим) и применение различных медикаментов с целью избавления от симптомов и предотвращения рецидивов (повторных атак). Если у пациента кардит (сердечное воспаление), ему может потребоваться снижение потребления соли.
Чтобы избавиться от микроорганизма стрептококка, который является причиной болезни, прописывают антибиотики. Используют антибиотики пенициллинового ряда; если у пациента непереносимость этой группы, назначают макролиды. В течение последующих пяти лет с момента подавления активности болезни необходимо принимать антибиотики продолжительного действия.
Важной составной частью лечения ревматизма являются нестероидные противовоспалительные препараты, такие как ибупрофен, диклофенак, позволяющие снизить активность воспаления. Дозировка препаратов и продолжительность их применения оговариваются в каждом конкретном случае и зависят от того, в каком состоянии находится больной.
Если в организме задерживается жидкость, прописывают мочегонные препараты (диуретики).
Сформированные пороки лечат в зависимости от степени их выраженности, наличия сердечной недостаточности, поражения клапанов и проч. Зачастую применяются антиаритмические препараты, которые устраняют или предупреждают нарушения сердечных ритмов, нитраты, диуретики и др.
Если порок тяжелый, необходимо проведение операции на сердечных клапанах – пластика или протезирование пораженного клапана.



Люди много веков назад уловили связь между тяжелыми простудами, ангинами и последующим возникновением проблем с суставами и общим недомоганием. Однако научное изучение ревматизма началось только с конца XIX века. Сегодня уже ясно – это поражение всей соединительной ткани, которая имеется в организме, и воспаление связано с нашим собственным иммунитетом.
Считается, что острая ревматическая лихорадка наиболее часто бывает у детей школьного возраста, хотя возможен ревматизм у взрослых. Обычно это лица 18 - 25 лет. Воспалительный процесс возникает в соединительной ткани, составляющей каркас внутренних органов, покрывающей суставные поверхности костей и формирующей клапаны сердца. Причиной болезни считают изменения в иммунной системе, которые запускает особый микроб – бета-гемолитический стрептококк А-группы. Причем ревматизм развивается не у всех, кто переболел стрептококковыми ангинами, скарлатиной или фарингитом, а только у части людей, имеющих наследственную предрасположенность.
При ангине токсины бактерий, а затем и антитела, которые организм вырабатывает в ответ на инфекцию, поражают волокна соединительной ткани в сердце, провоцируя воспаление внутренней оболочки сердца – эндокардит, или сердечной мышцы – миокардит. Кроме того, поражаются сердечные клапаны.
Помимо сердца, антитела, которые производит иммунная система, атакуют хрящи и связки в суставах, волокна соединительной ткани в сосудах, почках. Кроме этого, антитела повреждают и нервную систему. Такой процесс развивается, если у иммунной системы изначально есть дефект, то есть человек генетически предрасположен к ревматизму.

Симптомы ревматизма у взрослых
Ожидать первые признаки болезни можно через 2 - 3 недели после острой ангины, скарлатины или фарингита, которые вызваны стрептококком. Важно подчеркнуть, что симптомы ревматизма у взрослых начинаются не с поражений суставов или сердца, а с приступа лихорадки. На фоне общего нарушения самочувствия, слабости и разбитости температура повышается от 37 до 38,5 - 39 °С, сопровождается сильным ознобом и обильным потом.
Температура может держаться до 5 суток, и на фоне нее воспаляются суставы – они отекают, кожа над ними краснеет, возникает боль, которая не утихает даже в покое. Чаще всего повреждаются симметрично оба колена, либо голеностопные, плечевые или локтевые суставы. Но воспаление быстро переходит с одних суставов на другие – пару дней болят колени, затем локти, затем голеностопы. Причем после приема противовоспалительных препаратов боль и воспалительный процесс быстро исчезают. По мере снижения температуры утихает и артрит.
Некоторые пациенты отмечают на коже сыпь в виде розовых колец (эритема), которая не зудит и быстро проходит. В редких случаях в области затылка или воспаленных суставов могут возникать узелки под кожей, похожие на зернышки риса или горошины.

Ключевое проявление ревматизма – это серьезные поражения сердца (кардиты). От того, насколько сильно поражены оболочки сердца, клапаны и крупные сосуды, во многом зависит дальнейший прогноз для больного. Возможен:
-
эндокардит – воспаление внутренней выстилки сердца и клапанов;
миокардит – это поражение самой сердечной мышцы;
панкардит – когда в той или иной степени страдают все оболочки сердца.
Основные проявления – сердцебиение (тахикардия) и боль в области сердца, имеющая ноющий, щемящий или колющий характер. На фоне боли возникает одышка при малейшей нагрузке, аритмии (нарушения ритма). Почти у 1/4 больных, особенно при несвоевременном лечении, формируется порок сердца, так как воспалительный процесс разрушает сердечные клапаны.
По словам врача-невролога высшей категории Урюпинской ЦРБ Евгения Мосина, ревматизм затрагивает и нервную систему, у неврологов есть даже отдельный термин для описания болезни – нейро-ревматизм. Повреждения нервной системы возможны как в период ревматической лихорадки (из-за острых нарушений мозгового кровообращения, психозов или ревматического невроза), так и спустя некоторое время, из-за воспалительного процесса соединительнотканных элементов в нервной системе (миелиты, энцефалиты или невриты).
Самое частое неврологическое проявление ревматизма – это хорея (поражение подкорковых центров мозга, отвечающих за движения). Для этой патологии характерны подергивания рук и ног, имеющие хаотичный характер. Из-за сокращения мышц на лице возникает ощущение, что человек гримасничает, хотя он не контролирует эти действия. Может нарушаться внятность речи, страдает почерк, сложно держать в руках столовые приборы. В среднем, симптомы, как отмечает Евгений Юрьевич, сохраняются до трех месяцев.

- хондроитин и коллаген - важные строительные элементы суставных хрящей и соединительных тканей;
- муравьиный спирт и сабельник болотный оказывают сильнейшее противовоспалительное действие, улучшают кровообращение, снимают отеки и боль.
При ежедневном использовании препарата его эффективность только нарастает.
Длительность острой ревматической лихорадки длится до 6 - 12 недель. В этот период процесс воспаления проходит последовательные стадии развития, от обратимых начальных изменений до тяжелых, фатальных осложнений.
Самое неприятное при ревматизме то, что после затухания процесса, в первые 4 - 5 лет ремиссии, возможны новые вспышки воспаления. Они связаны с повторными эпизодами микробных ангин и фарингитов.
Ревматизм, или ревматическая лихорадка, относится к числу наиболее частых осложнений глоточных инфекций, вызванных СГА (ангины, фарингита, скарлатины). По данным статистических исследований разных стран, случаи возникновения болезни во всем мире варьируют от 55 до 1100 на 100 000.
Сам по себе ревматизм представляет собой болезнь с острым или хроническим рецидивирующим течением. Основным проявлением его является системное поражение всех элементов соединительной ткани с преимущественной локализацией патологического процесса в тканях сердца. Острая ревматическая лихорадка, или первичный ревматизм (по классификации А.И. Нестерова), в ряде случаев обретает хроническое течение, часто сопровождающееся появлением необратимых изменений в клапанном аппарате сердца.
Ревматизм относится к болезням преимущественно детского, юношеского и молодого возраста (7-20 лет), возникающим вслед за глоточными стрептококковыми инфекциями, поражающими в основном эту возрастную группу. Первые клинические признаки ревматизма появляются после глоточных инфекций по прошествии латентного периода длительностью от 2 до 5 недель, в течение которых происходит превращение глоточной инфекции в острую ревматическую лихорадку.
а) Этиология. Даже при острых ярко выраженных случаях первичного и рецидивах возвратного (по классификации А.И. Нестерова) ревматизма этиологическая роль стрептококка А бактериологически выявляется не всегда. В 30-40-е годы прошлого столетия Н.Д. Стражеско, один из открывателей стрептококковой этиологии ревматизма, и его современники — клинические микробиологи в первую неделю заболевания или возникновения рецидива болезни высевали гемолитический стрептококк, нередко в чистой культуре, практически от всех больных. Однако спустя два десятилетия (с начала 60-х годов) со слизистых оболочек носоглотки СГА могли быть высеяны только от отдельных больных, причем чаще всего в виде единичных колоний. Это, несомненно, связано с мощным действием пенициллина и его производных, назначаемых для лечения острых глоточных заболеваний, санации хронических очагов инфекции и профилактики рецидивов ревматизма.
Между тем отсутствие роста стрептококков А в посевах носоглоточной слизи, низкий процент выделения гемокультур явились одной из основных причин возникшей в 70-е годы XX в. дискуссии среди отечественных клиницистов и ревматологов об этиологической роли стрептококков при ревматизме.
В настоящее время вопрос об этиологической роли этих бактерий при ревматизме больше не обсуждается. Анализ архивных материалов и многочисленных отечественных и зарубежных публикаций позволяет говорить о преобладании при ревматизме СГА М-серотипов 1; 3; 5; 6; 14; 18; 19 и 24. Представители этих серотипов СГА характеризовались образованием на кровяном агаре крупных мукоидных колоний, поскольку клетки стрептококка имели большую гиалуроновую капсулу, в бульонных культурах преобладали короткие цепочки. Характерной чертой ревматогенных изолятов является высокая контагиозность стрептококков.
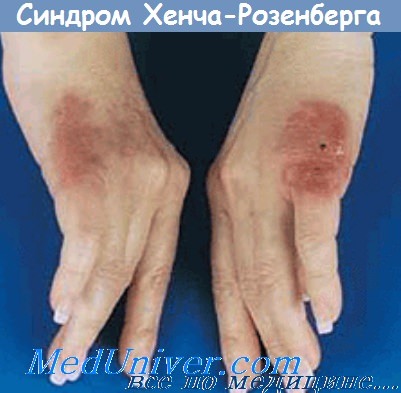
Синдром Хенча-Резенберга - рецидивирующий ревматизм
б) Патогенез. В проблеме ревматизма одним из наиболее сложных и наименее изученных разделов является патогенез болезни. Отчасти это объясняется тем, что в возникновении, течении и исходе ревматизма участвуют два равнозначных по своему значению фактора: один из них — человек с повышенной предрасположенностью к заболеванию ревматизмом, а второй — стрептококк М+ серотипа, содержащего фактор ревматогенности, входящий в обширную серологическую группу А стрептококков.
Только в середине 80-х — начале 90-х годов прошлого века группой ученых Рокфеллеровского университета под руководством J.B. Zabriski в В-лимфоцитах больных ревматизмом обнаружили генетически наследуемый аллоантиген, который оказался способным вызывать изменение иммунной системы человека в сторону наследственно передаваемой предрасположенности к заболеванию ревматизмом. Таким образом, был обнаружен генетический маркер, который, согласно результатам международных исследований, определяется у 98-100% больных ревматизмом с генетически обусловленной или приобретенной слабостью механизмов защиты в отношении стрептококковой инфекции.
В последние десятилетия XX в. появился ряд публикаций, посвященных изучению свойств пиогенных стрептококков, в частности конкретизации ревматогенных М-серотипов СГА и выявлению факторов, определяющих их ревматогенные свойства.
При поиске фактора ревматогенности стрептококков основное внимание исследователей было обращено на перекрестно реагирующие антигены, определяемые только у некоторых М-серотипов класса глоточных штаммов. Перекрестно реагирующие антигены характеризуются антигенной общностью отдельных структурных элементов стрептококка с антигенными детерминантами тканей тех органов, которые являются мишенью при ревматизме.
Так, например, групповой полисахаридный антиген содержит общие антигенные детерминанты с антигенами галактопротеина клапанов сердца человека, антигенами кардиолипинов сердечной мышцы, кардиомиоцитами и фибробластами соединительной ткани сердца. Установлена гомология у молекул М-протеина с тропомиозином и молекулами сарколеммы мышечных тканей сердца.
Содержание в различных структурных фрагментах возбудителя и в тканях органов, поражаемых патологическим процессом, идентичных антигенных детерминант, вызывающих образование антител, которые реагируют одновременно с возбудителем болезни и аутоантигенами, носит название молекулярной (антигенной) мимикрии.
Феномен молекулярной мимикрии лежит в основе образования кардиальных аутоантител при ревматизме, которые, вступая в реакцию с аутоантигенами тканей сердца, образуют иммунные комплексы. В клетках тканей происходит разрушение лизосом, сопровождаемое нарушением васкуляризации очага поражения с экссудацией, развитием продуктивного воспаления в очаге поражения и снижением фагоцитоза.
Приобретенные аутоиммунные изменения сердца прогрессируют при повторных инфицированиях организма ревматогенными штаммами стрептококка. В миокарде образуются гранулемы Ашоффа—Талалаева, на клапанах — бородавчатый эндокардит, на задней стенке левого предсердия — аурикулит (поражение ушка).
Таким образом, в настоящее время наиболее обоснованной является иммунопатологическая теория патогенеза ревматизма, в основе которой лежат аутоиммунные процессы, инициируемые образованием перекрестно реагирующих антител, вызванных наличием общих антигенных детерминант в клетках этиологического фактора болезни — СГА ревматогенного М+ серотипа и тканях поражаемых им органов человека.
в) Клиническая картина первичного ревматизма отличается большим разнообразием клинических проявлений, затрудняющих постановку диагноза. Эти трудности усугубляются еще тем, что ревматизм не имеет ни одного клинического и лабораторного патогномоничного признака. Поэтому ревматологи в основном пользуются синдромной диагностикой, основанной на результатах всестороннего клинико-лабораторного обследования больного.
Только в 1944 г. американский ревматолог Джонс (T.D. Jones) для диагностики острой ревматической лихорадки (ОРЛ) рекомендовал комплекс клинико-лабораторных тестов, которые вскоре дополнил А.И. Нестеров, и они под наименованием диагностических критериев Джонса-Нестерова вошли в клиническую практику, получив высокую оценку со стороны пользовавшихся ими врачей.
Однако в 1989 г. исследовательская группа ВОЗ предложила для диагностики ревматизма видоизмененную, более расширенную систему критериев Джонса, которая в частности давала значительно большие возможности для выявления связи диагностируемой болезни с предшествующей ей стрептококковой инфекцией.
Данные критерии предусмотрены только для диагностики ОРЛ (первичного ревматизма) и не предполагают их применения для определения формы (активная, неактивная), характера течения (острый, подострый, интермиттирующий, субклинический) и степени тяжести кардита. На основании критериев Джонса при рассмотрении их в разных сочетаниях можно легко представить себе разнообразие клинических проявлений ОРЛ.

г) Эпидемиология. Начиная с 1950 г. заболеваемость ревматизмом во всех индустриально развитых странах начала заметно снижаться, очевидно, вследствие введения препаратов пенициллина для лечения стрептококковых глоточно-респираторных инфекций и предупрежден и я рецидивов ревматизма.
В 70-е годы прошлого столетия ревматизм был отнесен к категории редко встречающихся болезней, что, к сожалению, привело к значительной утрате интереса к этой болезни как в нашей стране, так и за рубежом. Но в 80-е годы во многих странах Европы, в Советском Союзе и США уровень заболеваемости первичным ревматизмом совершенно неожиданно стал возрастать. В это же время, по данным ВОЗ, на поражения сердца, связанные со стрептококковой инфекцией приходилось 50% всей его патологии, которые впоследствии стали основной причиной операций на сердце в США.
В последние годы отмечается дальнейший рост заболеваемости ревматизмом. В ряде стран зарегистрированы эпидемические вспышки ревматизма. В период с 1980 по 1990 г. в США было зарегистрировано 8 крупных вспышек первичного ревматизма и множество спорадических и групповых (по 2-3 человека) заболеваний.
Инспектирование ряда крупных детских медицинских учреждений ведущими педиатрами и кардиологами выявило увеличение уровня заболеваемости первичным ревматизмом в 5-12 раз в 24 штатах США. Подъем заболеваемости был связан с появлением в популяции новых для нее стрептококков М-серотипов 1;3;5;6 и 18.
В Советском Союзе в послевоенные годы (конец 40-х — начало 50-х годов) распространенность ревматизма составляла 15 случаев на 1000, а первичная заболеваемость — 1,5 на 1000 среди лиц 7-20 лет. В большинстве случаев первичный ревматизм протекал тяжело с выраженным суставным синдромом и тяжелым ревмокардитом, сопровождающимся сердечно-сосудистой недостаточностью.
В 60-70 гг. прошлого столетия заболевания первичным ревматизмом встречались только во время эпидемических вспышек в закрытых или полузакрытых коллективах, в интернатах для детей инвалидов, военных училищах и среди военнослужащих по призыву.
За последние 30 лет первичная заболеваемость ревматизмом снизилась с 0,58 до 0,045 случаев на 1000 населения. В то же время определилась явная тенденция к увеличению частоты (у заболевших) подострого, затяжного и латентного течения.
В настоящее время на ревматические болезни приходится 14-15% от всех хронических заболеваний, регистрируемых в РФ. С каждым годом этот показатель увеличивается на 0,2-0,5%. Основной контингент больных ревматизмом — люди в возрасте 30-50 лет. Из них 6% — инвалиды. Отмечена связь между уровнем пораженно-сти населения ревматизмом и климато-географическим районам проживания.
д) Лечение. С начала заболевания с целью эрадикации персистирующих в организме СТА назначают антибактериальную терапию. Учитывая высокую чувствительность стрептококка к пенициллину и его производным, препаратом первого выбора является пенициллин. Больному назначают курс терапии бензил-пенициллином в виде внутримышечных инъекций в суточной дозе 3-6 млн. ЕД (для подростков и взрослых); продолжительность лечения — 14 дней. Больным с хроническим декомпенсированным тонзиллитом продолжительность курса увеличивают до 3 недель. Можно применять также полусинтетические пенициллины, в частности амоксициллин, в дозе 1,5-2,0 г/сут — 1-3 приема; курс лечения — 2 недели.
Больным с непереносимостью препаратов пенициллина назначают эритромицин или другие препараты группы макролидов. В завершение курса антибиотикотерапии в целях профилактики обострений тонзиллита больным назначают дюрантные препараты пенициллина. Эти же препараты рекомендуются больным возвратным ревматизмом для предупреждения стрептококковых инфекций и рецидивов ревматизма — вторичная профилактика.
Редактор: Искандер Милевски. Дата публикации: 19.11.2019
Читайте также:


