Лечение стрептококка агалактия не антибиотиками
Часть микрофлоры организма составляют условно-патогенные бактерия, такие как стрептококки группы В рода агалактия. В норме они присутствуют в теле человека в низких концентрациях, не оказывая влияния на работу его органов и систем. Воспаление начинается при их интенсивном размножении, под воздействием внешних или внутренних провоцирующих факторов (изменения гормонального фона, падение иммунитета).
Что такое стрептококк агалактия
Группа условно-патогенных бактерий, называемая стрептококками, в небольших концентрациях может присутствовать в организме человека, не вызывая развития инфекции или воспаления. Все микроорганизмы рода Streptococcus по характеру роста на питательных средах подразделяют на гемолитические, негемолитические и зеленящие. Стрептококки из рода агалактия (Streptococcus agalactiae) относятся к грамположительным бета-гемолитическим стрептококкам группы В.
Бактерия попадает в организм после начала половой жизни, обитает во влагалище, прямой кишке, урогенитальном тракте и носоглотке. Существует риск заражения ребенка от инфицированной матери во время родоразрешения или незадолго до его начала). Показателями нормы считают концентрации не более 10 в 4 степени КОЕ/мл. Инфекции, вызываемые стрептококками этого типа при росте их концентраций, особенно опасны для новорожденных и людей пожилого возраста, для которых они чреваты уросепсисом, перитонитом и пневмонией, инфекциями костей и кожи.
К основным путям попадания бактерии рода агалактия в организм относят половой, бытовой, воздушно-капельный, пищевой, и пренатальный или интранатальный (от матери к новорожденному). Активное размножение стрептококков происходит на фоне нарушения баланса нормальной микрофлоры из-за ряда следующих факторов:
- ослабление иммунитета;
- нарушение правил интимной личной гигиены;
- регулярные спринцевания (у женщин);
- гормональные сбои;
- ношение нижнего белья из синтетических тканей;
- незащищенный сексуальный контакт.
Стрептококк агалактия у мужчин активизируется либо после секса без использования презерватива, либо на фоне дисбактериоза кишечника после антибиотикотерапии или в следствие влияния иных факторов. После первоначального инфицирования носитель становится способен передавать бактерию возбудителя своим половым партнерам (самый распространенный путь передачи инфекции).
Отдельную группу риска представляют собой новорожденные. По статистике, носителями стрептококка Agalactiae является около 30% всех здоровых женщин, у которых во время беременности на фоне гормональных изменений могут обостряться вызываемые патогенным микроорганизмом инфекции (циститы, уретриты и др.). Угроза заражения ребенка растет при следующих обстоятельствах:
- возраст матери старше 20 лет;
- аборты или выкидыши в медицинском анамнезе матери;
- преждевременные роды (до 37 недели);
- амнионит;
- хроническая инфекция мочеполовых путей;
- задержка внутриутробного развития;
- лихорадочный синдром во время родов.

Микроорганизмы типа агалактия при интенсивном размножении вызывают инфекционные заболевания мочеполовой системы, сопровождающиеся воспалительным процессом. Активность бактерии сопровождается выделением следующих соединений и токсичных веществ:
- Некротоксинов и летальных токсинов, провоцирующих некроз тканей.
- Лейкоцидина, разрушающего клеточный иммунитет.
- Стрептолизина, способствующего разрушению тканей.
- Амилаза, гиалуронидаза, протеиназа, способствующие распространению стрептококковой инфекции.

Симптомы увеличения концентрации стрептококка агалактии
Бактерия стрептококк агалактия в моче или влагалищном мазке в увеличенных концентрациях свидетельствует о текущем воспалительном инфекционном процессе. В зависимости от типа инфекции, проявляется характерная симптоматика:
- При инфицировании мочевыделительных путей – зуд или жжение в области половых органов, цервикального канала, учащенные болезненные мочеиспускания, отечность и покраснение половых губ или анальных складок, боли в нижней части живота, выделения из мочеиспускательного канала.
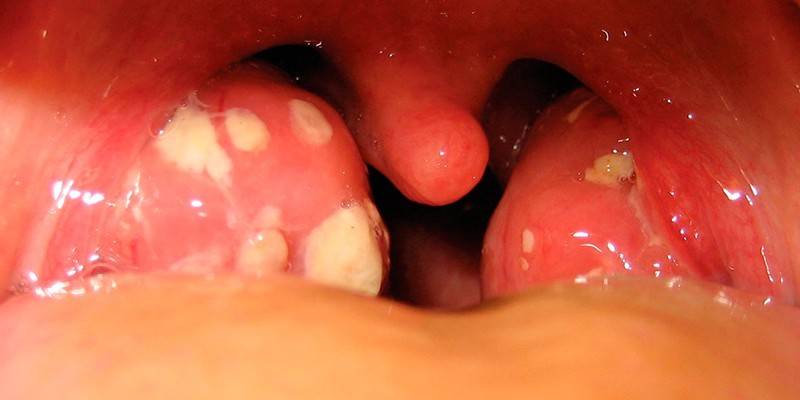
- При стрептококковом тонзиллите (ангине), фарингите и др. бактериальных инфекциях дыхательных путей – лихорадка, признаки тяжелой общей интоксикации, поражение слизистых.
Чем опасен стрептококк агалактия при беременности
Согласно статистике, стрептококки в мазке у женщин почти в 40% случаев обнаруживаются во время беременности. На фоне сниженного иммунитета максимально активное размножение агалактии наблюдается на 33-37 неделе, поэтому на этих сроках обязательно назначаются анализы для выявления возбудителя и его обезвреживания (при необходимости). Факторами, увеличивающими риск инфицирования, являются:
- обнаружения стрептококков этой группы в моче;
- диагностированная угроза преждевременных родов;
- диагностирование стрептококковой инфекции у предыдущих детей.
У беременной женщины агалактии могут вызывать воспаления мочеполовой системы, легких, спровоцировать следующие опасные осложнения беременности и родовой деятельности:
- эндометрит (воспаление внутренней оболочки матки);
- преждевременное отхождение околоплодных вод;
- хориоамнионит (воспаление плодных оболочек);
- выкидыш на любом сроке;
- преждевременное родоразрешение;
- сепсис, менингит, эндокардит(воспаление внутренней оболочки сердца) у новорожденного.
Диагностика
Обнаруживается стрептококк агалактия в мазке из влагалища, уретры или прямой кишки, который может быть назначен при обнаружении кокковой флоры в анализе мочи. После обследования биоматериала методом лабораторной микроскопии проводят посев на питательную среду, помогающий точно идентифицировать тип бактериального заражения, степень концентрации микроорганизмов и их устойчивость к антибактериальным препаратам.
Дополнительно назначаемыми анализами являются скрининг-тесты: ИФА (иммуноферментный анализ) и метод ПЦР (полимеразно-цепной реакции). Остальные лабораторные и инструментальные методы диагностики (общий и биохимический анализ крови, мочи, УЗИ и пр.) назначаются для выявления заболеваний, развитие которых вызвано активным размножением Streptococcus agalactiae.
Лечение streptococcus agalactiae
Необходимость медикаментозного лечения возникает при обнаружении концентраций стрептококков этой группы до 10 в четвертой степени КОЕ/мл и выше, даже если инфекция протекает скрыто. При воспалении мочеполовых органов терапию проходят оба половых партнера, при инфекции смешанного типа возможен прием антибиотиков разных фармакологических групп, при хронической форме заболевания пациенту с острой стадией болезни рекомендован прием иммуностимуляторов, ферментов, прохождение курса физиотерапии.
В зависимости от типа инфекции антибактериальные препараты назначаются в форме средств для перорально приема или в иных лекарственных формах (например, вагинальные таблетки или свечи Флуомизин, Тержинан, Гексикон,). Активность по отношению к агалактии проявляют пенициллины (Оксациллин, аминопенициллины), макролиды (Эритромицин) и Цефалоспорины (Цефазолин).
Если существует опасность заражения ребенка во время родов, матери назначаются внутривенные инъекции, проводимые прямо при родоразрешении, может рекомендоваться антибактериальная санация родовых путей перед родами. После курса антибиотиков и выведения бактерии требуется терапия с применение пробиотиков или энтеросорбентов (например, Атоксила) для восстановления естественной нормальной микрофлоры кишечника.
Профилактика
К профилактическим мерам предотвращения стрептококкового заражение является соблюдение правил личной гигиены и безопасности половых контактов, мероприятия по поддержанию естественного иммунитета, нормального баланса микрофлоры:
- полноценное питание;
- активный образ жизни, занятия спортом;
- здоровый режим дня;
- прием витаминов;
- закаливание организма, избегание переохлаждения;
- полноценный отдых;
- отказ от вредных привычек.


Streptococcus agalactiae — представитель большой группы микроорганизмов, отличающихся характерными морфологическими, тинкториальными, культуральными и биохимическими свойствами. Этот условно-патогенный микроб является естественным обитателем организма человека и локализуется преимущественно в кишечнике, носоглотке и влагалище. Стрептококк способствует развитию заболеваний лишь при определенных негативных условиях, ослабляющих иммунную защиту и снижающих общую резистентность организма.
Стрептококк агалактия — нормальный обитатель влагалища здоровой женщины. В количестве, не превышающем 10 4 колониеобразующих единиц, микробы безвредны для организма. Недуг развивается только в случае активного размножения бактерий и приобретения ими болезнетворных свойств. Это происходит при развитии иммунодефицита или переохлаждении. Одномоментное внедрение ударной дозы патогенов заканчивается патологическим процессом. Обнаружение во влагалищных выделениях значительного числа микробов – признак неспецифического воспаления.
У мужчин стрептококк агалактия входит в состав нормоценоза кишечника и носовой полости. При исследовании кала на дисбактериоз количество микробов не должно превышать 10 5 или 10 6 . Микробиологическое исследование отделяемого слизистой носа на микрофлору обнаруживает у здоровых людей стрептококк в количестве 10 3 или 10 4 . Streptococcus agalactiae, проникая в мужские половые органы, вызывает острую форму заболевания.
Стрептококк агалактия представляет серьезную опасность для беременных женщин и новорожденных детей, особенно, недоношенных. В последние годы отмечается рост заболеваемости среди пожилых лиц, у которых инфекция протекает в форме сепсиса, воспаления легких или перитонита. В группу риска также входят лица с тяжелыми соматическими заболеваниями, ослабляющими их иммунитет.
Диагностика патологии, вызванной Streptococcus agalactiae, основывается на данных, полученных в ходе микробиологического исследования влагалищного секрета, мочи, кала. Всем больным показано этиотропное противомикробное лечение антибиотиками из группы пенициллинов, макролидов, цефалоспоринов, а также патогенетическая и симптоматическая терапия, назначенная врачом с учетом индивидуальных особенностей организма.
Этиология
Streptococcus agalactiae — бактерия специфической шарообразной или эллипсоидной формы, способная существовать как в присутствии кислорода, так и без него. Микробы аспорогенны, неподвижны, имеют капсулу и обладают группоспецифическим полисахаридом.

Streptococcus agalactiae под микроскопом
Микроорганизмы окрашиваются по Грамму в синий цвет и располагаются в мазке парами и цепочками. Они требовательны к питательным средам. Растут стрептококки исключительно на средах, содержащих кровь, сыворотку и глюкозу. Эти вещества они используют в качестве источника энергии. Инкубируют посевы в термостате при 37 °С, хотя бактерии способны расти и в более широком диапазоне температур. На кровяном агаре спустя сутки образуются сероватые, очень мелкие колонии с зоной полного просветления по периферии. В бульоне бактерии растут в виде диффузной мути и осадка на дне пробирки.
Патогенные свойства бактерии обусловлены следующими факторами:
- Стрептолизином, разрушающим окружающие ткани, в особенности клетки крови и сердца;
- Лейкоцидином, угнетающим иммунитет и уничтожающим иммунокомпетентные клетки;
- Некротоксином, вызывающим отмирание тканей и воздействующим на работу всего организма;
- Ферментами, обеспечивающими адгезию, инвазию, распространение микробов по организму, поражение здоровых тканей и развитие патологического процесса.
Стрептококки резистентны к замораживанию, высушиванию, прямым солнечным лучам. Погибают бактерии под воздействием антибиотиков, антисептиков и дезинфектантов.
Патогенетические звенья инфекции:
- Внедрение микроба в организм,
- Колонизация слизистой оболочки,
- Возникновение очага воспаления,
- Боль и отек,
- Бактериемия,
- Общее недомогание,
- Интоксикационный синдром,
- Дегидратация,
- Помутнение сознания,
- Регионарный лимфаденит.
Эпидемиология
В природе Streptococcus agalactiae широко распространены. В организме человека они колонизирует слизистую кишечника, носа, глотки, органов выделительной и половой систем. От 15 до 40 % женщин репродуктивного возраста являются бактерионосителями.
Существует три варианта пребывания стрептококка во влагалище:
- Безвредное существование бактерий в организме,
- Бактериальный вагиноз,
- патологический процесс.
Если бактерий в мазке из цервикального канала мало, а лактобактерий много, говорят о первом варианте. Когда количество стрептококков превышает количество молочнокислых бактерий, а число лейкоцитов в поле зрения находится в пределах 50, это признак дисбиоза влагалища. Если лейкоцитов гораздо больше, значит, имеет место воспалительный процесс, протекающий в форме цервицита, кольпита, эндометрита.
Пути распространения инфекции:
- Контактный — через общие бытовые предметы, при поцелуе, объятии,
- Самозаражение – микробы из анальной зоны могут проникать во влагалище,
- Вертикальный — заражение плода во время беременности или новорожденного в родах,
- Половой — во время коитуса без презерватива,
- Воздушно-капельный — при чихании, кашле, близком общении с больным человеком,
- Пищевой — при употреблении обсемененных продуктов питания,
- Гематогенный занос инфекции из первичных очагов – почек или носоглотки.
Новорожденные инфицируются в первые часы и сутки после рождения. Это может случиться и раньше: в пре- и интранатальном периоде.
Для Streptococcus agalactiae характерна осенне-зимняя сезонность. Эти микроорганизмы активизируются в тот момент, когда организм ослаблен вирусами. На фоне ОРВИ чаще всего развивается вторичная бактериальная инфекция.
Факторы, способствующие активации стрептококка и его размножению:
- Гормональный сбой,
- Иммунодефицит,
- Тяжелые соматические заболевания,
- Частое использование лубрикантов,
- Ношение нижнего белья из синтетических материалов,
- Эндокринопатии,
- Вирусные инфекции,
- Дисбиоз кишечника,
- Неправильное подмывании наружных половых органов,
- Редкая смена нижнего белья,
- Использование некачественных гигиенических средств,
- Половой акт без презерватива,
- Стрессы,
- Переохлаждения,
- Состояния после хирургических вмешательств,
- Длительная и бесконтрольная антибиотикотерапия,
- Лечение цитостатиками или гормонами,
- Физическое перенапряжение,
- Сложная экологическая обстановка.
В мужской организм бактерии попадают при незащищенном половом контакте с женщиной-бактерионосителем или в результате дисбиоза кишечника. Инфицирование происходит во время занятий нетрадиционными видами секса. Мужчина-носитель инфекции сам не болеет, но заражает своих партнерш.
При беременности изменяется гормональный фон, что выражается в повышенной секреции прогестерона, угнетающего локальную иммунную защиту. Подобные процессы позволяют сохранить беременность. При этом повышается риск развития инфекционных патологий и обострения хронических заболеваний органов репродуктивной системы.
Клиника
Инфекция, вызванная данным микроорганизмом, у лиц репродуктивного возраста обычно протекает бессимптомно. Клинические признаки воспаления органов мочевыделительной и репродуктивной систем вполне узнаваемы.
Streptococcus agalactiae способен вызвать воспаление мочевого пузыря, уретры, легких, эндокарда, суставов, мозговых оболочек.

- Цистит проявляется режущей болью при мочеиспускании, отсутствием удовлетворения от его опорожнения, императивными позывами, появлением мутной мочи с хлопьями. Острая форма патологии сопровождается интоксикацией, слабостью, цефалгией, резкой потерей работоспособности.
- Симптомами уретрита у мужчин являются: боль при мочеиспускании, неприятные ощущения, чувство жжения в уретре, усиливающиеся после эякуляции, обильное слизисто-гнойное отделяемое, гиперемия устья и отек губок уретры по утрам.
- Бактериальный вагиноз, обусловленный увеличением во влагалище стрептококка, проявляется жжением и зудом в промежности, ноющей болью внизу живота, болезненностью при половом сношении, отеком половых губ, обилием желтоватой слизи.
У женщины инфекция часто протекает скрыто, бессимптомно. Стрептококки очень опасны для появившихся на свет малышей. Если произошло заражение внутри утробы матери, ребенок рождается с лихорадкой, гематомами, выделением крови изо рта, тяжелым дыханием. При инфицировании плода развивается сепсис, воспаление легких, мозговых оболочек, сердечной мышцы. Больные дети погибают практически сразу после рождения.
Причиной антенатальной гибели плода также может стать Streptococcus agalactiae. Патологоанатомы на вскрытии обнаруживают признаки гипоксии, увеличенное кровенаполнение органов, петехиальные геморрагии на эпикарде, отечность мозга, размягчение и разжижение тканей. На плодных оболочках определяется очаговая лейкоцитарная инфильтрация.
Диагностика
Заболевание диагностируют на основании результатов анализов. Лабораторная диагностика — основной способ обнаружения Streptococcus agalactiae.

-
В микробиологической лаборатории исследуют мазки из цервикального канала, влагалища, зева, мочу, кал. Окрашенные препараты микроскопируют и обнаруживают кокковую флору. В лаборатории готовят жидкие и плотные питательные среды, содержащие стимуляторы роста для стрептококков и вещества, подавляющие постороннюю микрофлору. На основании полученных в ходе исследования данных о

Лечебные мероприятия
Чтобы избавиться от патологии и ее основных проявлений, необходимо воздействовать на первопричину — убить бактерии. Для этого больным назначают противомикробные препараты — антибиотики. В тяжелых случаях показано патогенетическое лечение, включающее дезинтоксикацию и коррекцию водно-электролитного баланса. Симптоматическая терапия заключается в применении жаропонижающих, антигистаминных, антисептических средств. Дополнительно проводят лечение иммуномодуляторами и иммуностимуляторами.

После купирования интоксикации назначают физиопроцедуры – электрофорез, УВЧ, индуктотермию, СВЧ-терапию, аэроионотерапию, ингаляции, а также массаж грудной клетки, иглоукалывание, ЛФК.
Большое значение в лечении патологии имеет режим. Больным рекомендуют находиться в постели, особенно лицам с выраженным интоксикационным синдромом. Активные движения в разгар болезни замедляют процесс выздоровления и повышают риск развития серьезных осложнений. Дезинтоксикационные мероприятия включают правильный питьевой режим — употребление в сутки до трех литров воды. При отсутствии эффекта от лечения и ухудшении общего состояния больным показана госпитализация в стационар.
Своевременное и правильное лечение делает прогноз инфекции благоприятным. В противном случае заболевание приобретает затяжное течение, развиваются тяжелые осложнения, возможен смертельный исход.
Профилактика
Мероприятия, предупреждающие развитие стрептококковой инфекции:
- Укрепление иммунитета,
- Правильное питание,
- Личная гигиена,
- Борьба с табакокурением,
- Профилактический прием витаминов,
- Оптимальная физическая нагрузка,
- Полноценный сон,
- Отказ от употребления спиртных напитков,
- Санация очагов хронической инфекции,
- Соблюдение санитарно-гигиенических норм и правил,
- Ношение одежды по сезону,
- Защита организма от переохлаждения и сквозняков.
Streptococcus agalactiae в определенном количестве постоянно обитает в организме здоровых людей. Его активация и быстрое размножение очень опасны. Микроб разрушает эритроциты и способствует развитию воспаления там, где его количество максимально. При своевременном обнаружении стрептококка и правильном этиотропном лечении прогноз на выздоровление улучшается, и значительно снижается риск развития опасных для жизни осложнений.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Применение антибактериальных препаратов будет максимально эффективным, когда медикаментозная терапия является целенаправленной, то есть этиотропной: если возбудителем заболевания являются стрептококки, то следует применять антибиотики от стрептококков.
Для этого необходимо бактериологическое исследование – чтобы выделить и идентифицировать конкретную бактерию, подтвердив ее принадлежность к роду грамположительных бактерий Streptococcus spp.
Какие антибиотики убивают стрептококк?
Эффективными в отношении стрептококков могут быть препараты бактерицидного действия, способные не только преодолеть факторы их вирулентности – ферменты-антигены, цитотоксины (приводящие к β-гемолизу), поверхностные адгезивные белки, позволяющие стрептококку противостоять фагоцитозу – но и обеспечить эрадикацию патогена in vivo. И для того чтобы антибиотик мог искоренить бактерии, он должен проникать через их внешние мембраны и поражать уязвимые структуры клеток микроорганизма.
Основные названия антибактериальных фармакологических средств, которые считаются лучшими антибиотиками от стрептококка:
Антибиотики от гемолитического стрептококка или антибиотики против стрептококка группы А – β-гемолитического стрептококка группы А штамма Streptococcus pyogenes – включают и антибиотики от стрептококка в горле (поскольку указанный штамм вызывает стрептококковый фарингит и тонзиллит): β-лактамные карбапенемы – Имипенем (другие торговые названия – Имипенем с циластатином, Тиенам, Циласпен), Меропенем (Мепенам, Меробоцид, Инемплюс, Дорипрекс, Синерпен); антибиотики группы линкозамидов Клиндамицин (Клиндацин, Климицин, Клинимицин, Далацин); Амоксиклав (Амоксил, А-Клав-Фармекс, Аугментин, Флемоклав Солютаб).
Антибиотики от стрептококка пневмония – колонизирующей носоглотку комменсальной бактерии Streptococcus pneumoniae, часто называемой пневмококком включают все вышеперечисленные препараты, а также цефалоспориновые антибиотики IV поколения Цефпиром (Кейтен) или Цефепим.
Воспаление внутренней оболочки сердца чаще всего является следствием патогенного воздействия зеленящего стрептококка – альфа-гемолитического типа Streptococcus viridans. Если он с кровью попадает в сердце, то способен вызывать подострый бактериальный эндокардит (особенно у людей с поврежденными сердечными клапанами). Лечение зеленящего стрептококка антибиотиками проводят с помощью Ванкомицина (торговые названия – Ванкоцин, Ванмиксан, Ванкорус) – гликопептидного антибиотика.
Чувствительность стрептококков к антибиотикам – фактор успешного лечения
Прежде чем перейти к характеристике отдельных антибактериальных средств, используемых при стрептококковых инфекциях, следует подчеркнуть, что важнейшим фактором эффективности лечения является чувствительность стрептококков к антибиотикам, которой определяется способность лекарственных средств уничтожать бактерии.
Нередко эффективность антибиотикотерапии настолько мала, что возникает вопрос – почему антибиотик не убил стрептококк? Данные бактерии – в частности, Streptococcus pneumoniae – за последние два десятка лет продемонстрировали значительное повышение резистентности, то есть сопротивления антибактериальным препаратам: на них не действует тетрациклин и его производные; почти треть их штаммов не поддаются воздействию эритромицина и пенициллина; выработалась устойчивость к некоторым препаратам группы макролидов. А фторхинолоны изначально менее эффективны при стрептококковой инфекции.
Снижение чувствительности стрептококков к антибиотикам исследователи связывают с трансформацией отдельных штаммов в результате генетического обмена между ними, а также с мутациями и усилением естественного отбора, так или иначе спровоцированного теми же антибиотиками.
И речь идет не только о порицаемом медиками самолечении. Лекарство, назначенное врачом, тоже может оказаться бессильным перед стрептококковой инфекцией, поскольку в большинстве случаев антибактериальный препарат назначают без выявления конкретного возбудителя, так сказать, эмпирически.
Кроме того, антибиотик не успевает убить стрептококк, если пациент раньше времени прекращает принимать препарат, сокращая длительность курса лечения.
Полезная информация также в материале – Антибиотикорезистентность
Код по АТХ
Фармакологическая группа
Фармакологическое действие
Показания к применению антибиотиков от стрептококков
Штаммы, серотипы и группы стрептококков весьма многочисленны, как и вызываемые ими воспалительные заболевания, которые распространяются от слизистой глотки до оболочек головного мозга и сердца.
Список показаний к применению антибактериальных средств включает: перитонит, сепсис, септицемию и бактериемию (в том числе неонатальную); менингит; скарлатину; импетиго и рожу; стрептодермию; лимфаденит; синусит и острый средний отит; пневмококковые фарингит, тонзиллит, бронхит, трахеит, плеврит, бронхопневмонию и пневмонию (в том числе нозокомиальную); эндокардит. Эффективны при инфекционных воспалениях мягких и костной тканей (абсцессах, флегмонах, фасцитах, остеомиелите) и поражениях суставов стрептококкового происхождения с ревматической лихорадкой в острой форме.
Данные антибиотики используются в лечении пиелонефрита и острого гломерулонефрита; воспаления мочеполовых органов; внутрибрюшной инфекции; послеродовых инфекционных воспалений и т.д.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Форма выпуска
Форма выпуска антибиотиков Имипенем, Меропенем, Цефпиром и Ванкомицин – стерильный порошок во флаконах, предназначенный для приготовления раствора, который вводится парентерально.
Амоксиклав выпускается в трех формах: таблетки для перорального применения (по 125, 250, 500 мг), порошок для приготовления принимаемой внутрь суспензии и порошок для приготовления раствора для инъекций.
А Клиндамицин имеет форму капсул, гранул (для приготовления сиропа), раствора в ампулах и 2% крема.

[11], [12], [13], [14], [15], [16]
Фармакодинамика
Бета-лактамные антибиотики Имипенем и Меропенем, относящиеся к карбапенемам (классу органических соединений, известных как тиенамицины), проникают в бактериальные клетки и мешают синтезу жизненно важных компонентов их клеточных стенок, что приводит к разрушению и гибели бактерий. От пенициллинов эти вещества несколько отличаются строением; кроме того, в состав Имипенема входит натрия циластатин, который тормозит его гидролиз почечной дегидропептидазой, что продлевает воздействие препарата и повышает его эффективность.
Сходный принцип действия имеет Амоксиклав – комбинированный препарат с аминопенициллином амоксициллином и клавулановой кислотой, которая является специфическим ингибитором β-лактамаз.
Фармакодинамика Клиндамицина базируется на связывании с субъединицей 50 S рибосом клеток бактерий и угнетении белкового синтеза и роста РНК-комплекса.
Цефалоспориновый антибиотик четвертого поколения Цефпиром также нарушает выработку гетерополимерных пептидогликанов (муреинов) каркаса стенок бактерий, приводя к разрушению пептидогликановых цепочек и лизису бактерий. А механизм действия Ванкомицина кроется как в ингибировании синтеза муреинов, так и в нарушении синтеза РНК бактерий Streptococcus spp. Преимущество данного антибиотика в том, что он, не имея в своей структуре β-лактамного кольца, не подвергается воздействию защитных ферментов бактерий – β-лактамаз.

[17], [18], [19], [20], [21], [22], [23], [24], [25], [26], [27]
Фармакокинетика
Меропенем проникает в ткани и биологические жидкости, но связывание с белками плазмы не превышает 2%. Расщепляется с образованием одного неактивного метаболита. Две трети препарата элиминируется в первоначальном виде; при в/в введении период полувыведения составляет 60 минут, при в/м инъекции – около полутора часов. Выводится из организма почками в среднем через 12 часов.
В фармакокинетической характеристике Клиндамицина отмечается его 90%-ая биодоступность и высокая степень связывания с альбуминами крови (до 93%). После приема внутрь максимальная концентрация препарата в крови достигается примерно через 60 минут, после введения в вену – через 180 минут. Биотрансформация происходит в печени, часть метаболитов терапевтически активны. Выведение из организма длится около четырех суток (через почки и кишечник).
Цефпиром вводится путем инфузии, и хотя с белками плазмы крови препарат связывается менее чем на 10%, в течение 12 часов терапевтическая концентрация в тканях удерживается, а биодоступность составляет 90%. Данный препарат в организме не расщепляется и выводится почками.
После перорального приема Амоксиклава в кровь амоксициллин и клавулановая кислота попадают примерно через час, а выводятся вдвое дольше; связывание с белками крови 20-30%. При этом накопление препарата отмечается в синусах верхней челюсти, легких, плевральной и спинномозговой жидкостях, в среднем ухе, брюшной полости и органах малого таза. Амоксициллин почти не расщепляется и выводится почками; метаболиты клавулановой кислоты экскретируются через легкие, почки и кишечником.
Для фармакокинетики Ванкомицина характерно связывание с белками плазмы крови на уровне 55% и проникновение во все биологические жидкости организма и через плаценту. Биотрансформация препарата незначительна, а период полувыведения составляет в среднем пять часов. Две трети вещества выводится почками.

[28], [29], [30], [31], [32], [33], [34], [35], [36], [37]
Использование антибиотиков от стрептококков во время беременности
Безопасность применения антибиотиков-карбапенемов (Имипенема и Меропенема) беременными производителями не установлена, поэтому их использование во время беременности допускается только значительном перевесе пользы для будущей матери над потенциальным негативным воздействием на плод.
Таков же принцип использования беременным и кормящим Клиндамицина и Амоксиклава.
При беременности применять Цефпиром запрещается. Запрет на использование Ванкомицина касается первого триместра беременности, а на более поздних сроках применение допускается только в крайних случаях – при наличии угрозы жизни.
Противопоказания
Основные противопоказания к применению:
Имипенем и Меропенем – наличие аллергии и повышенная чувствительность к препаратам, детский возраст до трех месяцев;
Клиндамицин – воспаление кишечника, недостаточность печени или почек, детский возраст до года;
Цефпиром – непереносимость пенициллина, беременность и лактация, возраст пациентов младше 12-ти лет;
Амоксиклав – повышенная чувствительность к пенициллину и его производным, застой желчи, гепатит;
Ванкомицин – нарушения слуха и кохлеарный неврит, недостаточность почек, первый триместр гестации, лактационный период.

[38], [39], [40], [41], [42], [43]
Побочные действия антибиотиков от стрептококков
Наиболее вероятные побочные действия Имипенема, Меропенем и Цефпирома включают:
болезненность в месте укола, тошноту, рвоту, диарею, кожные высыпания с зудом и гиперемией, снижение уровня лейкоцитов и повышение содержания мочевины в крови. Также может быть гипертермия, головная боль, нарушение дыхания и сердечного ритма, судороги, нарушение микрофлоры кишечника.
Кроме уже перечисленных, побочные эффекты Клиндамицина могут проявляться в виде привкуса металла во рту, гепатита и холестатической желтухи, повышения уровня билирубина в крови, боли в эпигастральной области.
Применение Амоксиклава может сопровождаться тошнотой, рвотой и диареей, острым воспалением кишечника (псевдомембранозным колитом) из-за активизации оппортунистической инфекции – клостридий, а также экссудативной эритемой кожи и развитием токсической некротизации эпидермиса.
Аналогичные побочные действия могут проявлять при лечении зеленящего стрептококка антибиотиками-гликопептидами (Ванкомицином). Кроме того, данный антибиотик может негативно повлиять на слух.

[44], [45], [46]
Способ применения и дозы
Способ применения препаратов зависит от их формы выпуска: таблетки принимают внутрь, растворы для инъекции вводятся парентерально.
Имипенем может вводиться в вену (медленно, в течение 30-40 минут) и в мышцу, но внутривенное введение практикуется чаще. Разовая доза взрослым составляет 0,25-0,5 г (в зависимости от заболевания), количество инъекции – три-четыре в течение суток. Дозы для детей определяют по массе тела – по 15 мг на каждый килограмм. Максимальная суточная доза для взрослых – 4 г, для детей – 2 г.
Меропенем вводят в вену – струйно или капельно: через каждые 8 часов по 0,5-1 г (при менингите – по 2 г). Для детей до 12 лет дозировка из расчета 10-12 мг на каждый килограмм массы тела.
Капсулированный Клиндамицин принимается внутрь – по 150-450 мг четыре раза в сутки в течение десяти дней. Для детей больше подходит сироп: до года – по половине чайной ложки трижды в день, после года - по чайной ложке. Инъекции Клиндамицина – внутривенные капельные и внутримышечные – назначаются в суточной дозе от 120 до 480 мг, (делится на три введения); продолжительность парентерального применения – 4-5 дней с переходом на прием капсул до окончания курса лечения, общая продолжительность которого составляет 10-14 дней. Клиндамицин в форме вагинального крема используют раз в сутки в течение недели.
Антибиотик от стрептококков Цефпиром вводят только внутривенно, а доза зависит от патологии, которую вызвал стрептококк – по 1-2 г дважды в течение суток (через 12 часов); максимально допустимая доза – 4 г в сутки.
Амоксиклав взрослым и детям старше 12-ти лет вводится внутривенно четыре раза в сутки по 1,2 г; детям до 12-ти лет – по 30 мг на килограмм массы тела. Курс лечения – 14 дней с возможным переходом (по состоянию) на прием таблеток. Таблетки Амоксиклав принимают во время еды по 125-250 мг или по 500 мг два-три раза в сутки в течение 5-14 дней.
Разовая доза Ванкомицина, который требует очень медленного в/в введения, для взрослых составляет 500 мг (через каждые шесть часов). Для детей дозу рассчитывают: на каждый килограмм веса ребенка – по 10 мг.

[47], [48], [49], [50]
Читайте также:


