Острая язвенная болезнь желудка хеликобактер ассоциированная
ЯБ является полиэтиологическим заболеванием, но открытие учеными J.R. Warren, B. Marshal (1983) роли Helicobacter pylori (Hp) в развитии ЯБ привело, с начала 80-х годов, к значительному переосмыслению этиологии и патогенеза данного заболевания [4,9,16,33].
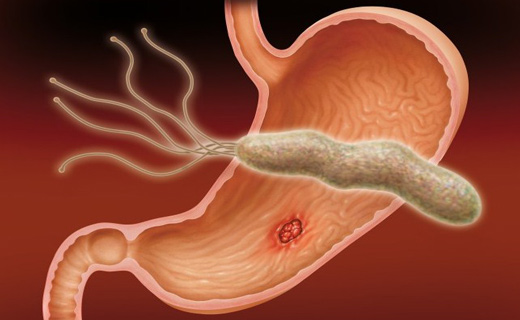
Helicobacter pylori в настоящее время является основным инфекционным агентом, приводящим к развитию ЯБ. По своим биологическим свойствам Hp относится к микроорганизмам с окислительным типом метаболизма, вырабатывающим ферменты: уреазу, каталазу, оксидазу, щелочную фосфатазу, глютамин, аминопептидазу, ДНК-азу и цитотоксин, повреждающие эпителиальные клетки, образуя в них адгезивный бактериальный слой, тем самым участвуя в развитии язвенных поражений желудка [4,35,69,70,81]. Цитотоксин способствует продвижению бактерий в межклеточное пространство и образованию колоний, тем самым вызывая повреждение слизистой оболочки желудка (СОЖ) [34,55,67]. Уреаза вызывает расщепление мочевины, что приводит к образованию углекислого газа и аммиака, которые нейтрализуют соляную кислоту и, являясь важным фактором повреждения, воздействуют как на слой слизи, так и на клетки желудочного эпителия, продуцируя провоспалительные агенты [31]. Кроме того, Hp секретируют поверхностные белки и фактор активации тромбоцитов, которые являются медиаторами воспаления, активируют моноциты, несущие рецепторы к ИЛ-2 и вырабатывают свободные радикалы кислорода, тем самым способствуя выделению протеаз, фосфолипаз, разрушающих слизистый гель, вызывая хронический воспалительный процесс и иммунный ответ [40,41,43,75,85]. При этом уменьшается количество и вязкость слизи, снижается секреция соляной кислоты и пепсина вплоть до ахлоргидрии, что способствует устойчивой колонизации Hp, тем самым вызывая развитие неопластических процессов в стенке желудка [55].
Под влиянием Нр и активирования лейкоцитов происходит повреждение сосудистого эндотелия, нарушение микроциркуляции и трофики СОЖ, что ведет к развитию воспалительных, дистрофических и некробиотических изменений [58,77], определяя высокую частоту рецидивов язв после их заживления [6,10,12].
К предраковым состояниям относят рецидивирующие и длительно незаживающие формы язвенной болезни с ахлоргидрией [80], каллезные язвы, торпидное течение процесса рубцевания язвенного дефекта, полиповидные изменения СОЖ [10,11,16,25,31,35,62], сопутствующие атрофические и диспластические изменения [1,36,54]. Согласно рекомендациям Международного координационного комитета ВОЗ по гистологической классификации предраковых заболеваний желудка (1978), введено понятие дисплазия, в которое входят клеточная атипия, нарушение дифференцировки и структуры СОЖ.
При неблагоприятном течении ЯБ, ассоциированной с Hp и активном воспалительном процессе в СОЖ под влиянием факторов окружающей среды, вредных привычек, генетической предрасположенности усиливаются процессы пролиферации, что ведет к развитию и прогрессированию предраковых изменений в эпителии органа [9,22,63,83,87]. По данным ряда исследований, повреждения клеток СОЖ, вызывающих метапластические, диспластические изменения в эпителии желудка, связаны с аутоиммунной агрессией индуцированной Hp [6,9,22,23,40]. В зонах кишечной метаплазии и железистом эпителии СОЖ с признаками дисплазии выявляют кишечные антигены. Таким образом, ученые полагают, что трофические расстройства и диспластические изменения эпителия желудка сопровождаются антигенной перестройкой по кишечному типу [36], поэтому у больных ЯБ, ассоциированной с Hp, нередко выявляются данные патоморфологические нарушения на фоне кишечной метаплазии [80].
Данные о частоте малигнизации язв желудка вариабельны и противоречивы: от 4,6-28 % до 60 % [16,28], что объясняется сложностями дифференциальной диагностики ЯБ и первично-язвенной формы рака, встречаемой в 10-15 % всех случаев язв желудка [5].
Рак желудка (РЖ) является одним из наиболее распространенных форм рака и второй причиной онкологической смертности во всем мире [71]. В мире ежегодно диагностируется приблизительно от 700 000 до 900 000 новых случаев [71]. В России РЖ занимает третье место в структуре злокачественных заболеваний, а по показателям смертности - второе [18,30,38,39].
Показатели заболеваемости РЖ во всем мире отличаются друг от друга географически, причем в развитых странах в течение нескольких десятилетий отмечается снижение числа заболевших [45]. Выживаемость больных РЖ в мире варьируется в пределах 15 % при диагностике заболевания на более поздних стадиях и 65 % - при идентификации болезни на ранних стадиях.
В 1994 году Международное агентство по изучению рака включило Hp в список канцерогенов первой группы [83].
РЖ, как правило, выявляется в поздней стадии и зачастую хирургическое лечение его бывает неэффективным [18,19,25,28,29,38], поэтому в последние годы пытаются выявлять предраковые изменения СОЖ на ранних этапах с применением новых и усовершенствованных методов исследований.
Также, активно изучается эрадикация Hp как метод предупреждения развития предраковых состояний и профилактики РЖ [25,35,37,86]. Имеются сведения о том, что эрадикация Hp сопровождается обратным развитием морфологических изменений, таких, как атрофия, метаплазия, дисплазия, однако эти сведения носят противоречивый характер и требуют дальнейшего изучения [12,24,35,50,57].
Современный способ ФГДС в сочетании с методикой инсуфляции воздуха в полость желудка для расправления складок позволяет оценить состояние слизистой и под визуальным контролем взять биопсийный материал со дна язвы, ее краев и окружающей СОЖ, при этом опухолевидное изъязвление, ригидность стенки желудка, не раздуваемой воздухом, являются симптомами малигнизации язвы желудка. Для ранней диагностики кишечной метаплазии в СОЖ может использоваться метод хромогастроскопии с применением метиленовой сини. Ультразвуковое исследование желудка выявляет процессы, сопровождающиеся утолщением стенки органа в результате отека, фиброза, кровоизлияния, опухоли. Также, используются анализы крови больных ЯБ на основные биохимические показатели - уровень лактатдегидрогеназы и ß2-макроглобулина, определение уровня сывороточного гастрина, увеличение которого свидетельствует о наличии инфекционного агента в стенке желудке и атрофического гастрита. Гистологический метод кроме верификации микробного обсеменения СОЖ, позволяет оценить ее состояние воспаления, атрофии, метаплазии или малигнизации. Также, для выявления Hp используют высокочувствительный, специфичный метод гибридизации дезоксирибонуклеиновой кислоты (ДНК) в парафиновых срезах, а также ХЕЛПИЛЛ-тесты. Иммунологическая диагностика позволяет определять антитела в сыворотке крови больных с помощью серологических методов - реакции агглютинации, непрямой гемагглютинации, преципитации с помощью иммуноферментного анализа (ИФА), а также, более специфичного и чувствительного теста с применением иммунного блоттинга выявляют антитела классов IgM, IgG, IgA в сыворотке крови к антигенам Hp и секреторные IgM, IgG в слюне и содержимом желудка, а также патогенность штаммов бактерии с CagA-статусом [42]. Современные экспресс-тесты с помощью твердофазного ИФА за несколько минут позволяют провести качественную оценку гуморального иммунного ответа на комплекс антигенов Hp. С 2000 года применяется тест-система для определения концентрации антигена Hp в кале с помощью количественного ИФА, цитогенетический метод FISH, а также тест URINELISA Hp Antibodi, основанный на твердофазном ИФА для определения микроба в моче больного ЯБ [15]. После расшифровки генома Hp стало известно, что онкогенными являются специфические участки ДНК некоторых штаммов микроба. Молекулярный метод идентификации штаммов Hp с применением полимеразной цепной реакции основан на выявлении фрагмента различных генов (cagA, ureC, vacA) микроорганизма в биоптатах СОЖ, зубном налете, слюне, копрофильтрате, желудочном соке [14,16].
Несмотря на положительный эффект от стандартных схем лечения ЯБ, частота случаев рецидивирующих, длительно незаживающих, рецидивирующих язв как риск развития предраковых изменений и РЖ в наше время остается высокой [25,28]. Эффективное, комплексное лечение ЯБ с сопутствующим неблагоприятным фоном должно приводить к восстановлению иммунного статуса и целостности эпителиального пласта в зоне язвенного дефекта в оптимальные сроки, восстанавливая функции желез, слизи, способствуя полноценной эрадикации Hp и дальнейшему предупреждению малигнизации язв [87].
Рецензенты:
- Магазов Р.Ш., д.м.н., профессор, академик Академии наук Республики Башкортостан, г. Уфа.
- Сыртланова Э.Р., д.м.н., главный врач поликлиники №33, г. Уфа.
Работа получена 20.10.2011.
Терапию начинают одним из вариантов трёхкомпонентной терапии. При его неэффективности рекомендуют повторные терапевтические меры. Вам необходимо узнать у врача, как лечить язву желудка с Helicobacter pylori с использованием другого варианта трёхкомпонентной или четырёхкомпонентной схемы или после окончания комбинированной эрадикационной терапии продолжают лечение ещё в течение 5 нед при двенадцатиперстной и 7 нед при желудочной локализации язв с использованием одного из следующих препаратов: ранитидина (0,3 гр. на ночь), фамотидина (0,04 г на ночь).
Не ассоциированная язва с Helicobacter pylori
Форма ассоциированая с Helicobacter pylori в 95% случаев язвенной болезни двенадцатиперстной кишки и 87% желудка. Терапия лекарствами проводят по рекомендациям Российской гастроэнтерологической ассоциации и Российской группы по изучению данного типа бактерий. Всё-таки как лечить язву с H. pylori ассоциированную и не ассоциированную данными микроорганизмами? Комплексная терапия больных с язвой желудка направлено на эрадикацию Н. pylori и включает в себя антибактериальные лекарства и ингибиторы секреции соляной кислоты. Ингибиторы секреции соляной кислоты обеспечивают оптимальный уровень рН для действия антибактериальных препаратов и устраняют агрессивное действие соляной кислоты на процесс рубцевания очагов. Обычно используют блокаторы Н2-рецепторов гистамина (ранитидин, фамотидин) и блокаторы "протонного насоса" (омепразол, лансопразол, пантопразол).
Как лечить: разные схемы против язвы
Трёхкомпонентная схема излечения язвы включает или блокатор "протонного насоса" (омепразол, пантопразол, лансопразол), или блокатор Н2-рецепторов гистамина (ранитидин, фамотидин), или препарат висмута в сочетании с двумя противомикробными препаратами.
Блокатор Н+,К+-АТФазы омепразол (20 мгр 2 р.), или пантопразол (увеличить дозировку вдвое), или лансопразол (30 мг дважды). Таким методом как лечить не ассоциированную форму болезни? В течение 7 дней в комбинации с:
- метронидазолом (0,4 гр. 3 р. в сутки) и кларитромицином (250 мг 2 раза);
- амоксициллином (1000 мг два р. ежедневно) и кларитромицином (500 мг дважды за день) или амоксициллином (также, но 3 р.) и метронидазолом (столько же по 400 мг).
Висмута трикалия дицитрат (де-нол) или висмута субсалицилат (120 мг 4 р. в сутки) в течение 7 дней в сочетании с:
- тетрациклином (500 мг 4 раза каждый день) и метронидазолом (250 мг четырежды) при лечении язвы желудка,
- кларитромицином (250 мг два р. в сутки) и амоксициллином (вдвое больше по дозе.) или амоксициллином (500 мг 3 р.) и метронидазолом (250 мг 4 р. ежедневно).
среди разных вариаций возможна и такая схема терапии Helicobacter pylori. Ранитидина висмута цитрат (400 мг 2 в сутки) в течение 7 дней в сочетании с:
- кларитромицином (500 мг дважды за день) и метронидазолом (так же) или тетрациклином (500 мг 4) и метронидазолом (вдвое меньше) для излечения от болезни.
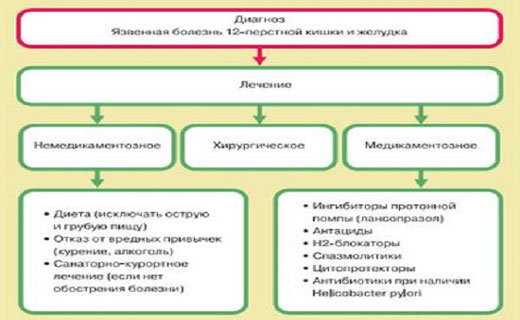
Четырёхкомпонентная схема включает антисекреторный препарат (ингибитор Н+,К+-АТФазы или блокатор Н2-рецепторов гистамина), препарат висмута и два противомикробных препарата.
Ингибитор Н+,К+-АТФазы (омепразол 20 мг, лансопразол 30 мг или пантопразол 40 мг по 2 раза) в сочетании с коллоидным субцитратом висмута 120 мг 4 р. каждый день, тетрациклином 500 мг 4 раза в сутки и метронидазолом 250 мг четырежды (или тинидазолом вдвое больше по дозе, но дважды за сутки) для терапии язвы желудка.
Оценку эрадикации осуществляют не ранее 4-6-й недели после окончания курса антихеликобактерного лечения и как минимум двумя диагностическими методами. Как еще проводить терапию, если использованная схема не привела к эрадикации? В первую очередь это означает, что бактерии приобрели устойчивость к одному из компонентов схемы (производным нитроимидазола, макролидам) и применять эту схему ещё раз не следует. Если и другая схема лечения не приводит к эрадикации, следует определять чувствительность штамма Н. pylori ко всему спектру используемых антибиотиков. Появление бактерии в организме больного спустя год после расценивают как рецидив инфекции и для его устранения применяют более эффективные схемы терапии.
Как избавиться от не ассоциированной с Helicobacter pylori?
Применяют все группы антисекреторных лекарств: антациды, холиноблокаторы, блокаторы Нг-рецепторов гистамина, блокаторы Н+,К+-АТФазы в обычной дозировке. чтобы узнать, как лечить не ассоциированную язву с Helicobacter pylori, обратитесь за помощью к вашему доктору. Он подберет адекватные медикаменты для терапии.
Хирургические мероприятия для восстановления желудка. Абсолютные показания: осложнения (перфорация язвы, профузное желудочно-кишечное кровотечение, стеноз, сопровождающийся выраженными эвакуаторными нарушениями). Относительные показания: многократные профузные желудочно-кишечные кровотечения в анамнезе, крупные каллёзные пенетрирующие болезни, резистентные к лекарственному методу. Не знаете, как лечить болезнь при обсеменении желудка бактерией HP ассоциированного и не ассоциированного типа? Обратитесь за консультацией к вашему лечащему врачу. Принимать какие-либо лекарства самостоятельно нельзя, назначение доктором должно быть только после постановки диагноза.
Лечение язвенной болезни, не ассоциированной с helicobacter pylori
До внедрения в практику ингибиторов протонного насоса (омепразол, париет, эзомепразол и др.) основными средствами лечения язвенной болезни служили блокато-ры Н2-гистаминорецепторов (ранитидин, фамотидин и др.). Еще раньше (до изобретения блокаторов Н2-гиста-минорецепторов) основой лечения язвенной болезни являлись препараты висмута (викалин, субнитрат висмута).
Базисное, основное лечение язвенной болезни проводится антисекреторными препаратами, препаратами висмута или сукральфатом. Продолжительность лечения противоязвенными антисекреторными препаратами составляет не менее 4–6 недель при язве двенадцатиперстной кишки и не менее 6–8 недель при язве желудка. Антацидные препараты и прокинетики назначают в дополнение к базисной терапии как симптоматические средства для устранения изжоги и боли.
Применение блокаторов Н2-гистаминорецепторов
Ранитидин принимают по 300 мг в сутки однократно вечером (в 19–20 часов) или по 150 мг 2 раза в день. Дополнительно могут назначаться антацидные препараты (маалокс, фосфалюгель, гастал и др.) или прокинетики (мотилиум и др.) как симптоматические средства.
Фамотидин принимают по 40 мг в сутки однократно вечером (в 19–20 часов) или по 20 мг 2 раза в день. Дополнительно — антацидный препарат (гастал и др.) или прокинетик (мотилиум и др.).
Применение ингибиторов протонного насоса
Омепразол (син.: омез) по 20 мг на прием. Париет (син.: рабепразол) по 20 мг на прием. Эзомепразол (син.: нексиум) по 20 мг на прием.
В качестве базисного средства лечения язвенной болезни также может быть назначен комплексный препарат ранитидин висмут цитрат. Лекарство назначает по 400 мг 2 раза в сутки (при язве двенадцатиперстной кишки прием не менее 4 недель, при язве желудка — 8 недель).
Де-нол, препарат висмута, принимают по двум возможным схемам:
по 240 мг 2 раза в сутки за 30 мин до еды или через 2 часа после еды;
по 120 мг 4 раза в сутки — до завтрака, обеда, ужина
Сукральфат (син.: вентер) для лечения язвенной болезни назначают по 1 г 4 раза в сутки — по 1 г за 30 минут
или за 1 час до еды (перед завтраком, обедом, ужином) и вечером через 2 часа после еды или перед сном; курс лечения 4 недели, и далее при необходимости продолжают прием препарата по 2 г в сутки в течение 8 недель.
Суточную дозу, продолжительность лечения, необходимость включения в схему лечения антацида (алмагель и др.) или прокинетика (мотилиум и др.) определяет врач.
Комбинированное применение базисных противоязвенных препаратов и антацидов (алмагель, маалокс, ру-тацид и др.), способных быстро нейтрализовать избыток соляной кислоты в полости желудка, довольно быстро устраняет изжогу и боль. В то же время необходимо знать, что антацидные препараты замедляют всасывание других препаратов, поэтому их следует принимать отдельно: интервал между приемом антацидного и другого препарата должен составлять не менее 2 часов.
Используя ту или иную схему, вполне возможно достичь хороших результатов лечения, однако в том и состоит искусство врача, чтобы назначать индивидуальную терапию каждому пациенту для достижения наилучших результатов с наименьшими потерями (добиться быстрой и стойкой ремиссии при минимуме побочных эффектов и минимуме финансовых затрат).
Ингибиторы протонного насоса (омепразол и др.) являются сегодня наиболее мощными средствами подавления факторов желудочной агрессии. В то же время установлено, что не всегда следует максимально снижать уровень соляной кислоты и пепсина в желудке. Во многих случаях достаточно использовать ранитидин или фамотидин (они дешевле омепразола и париета). При необходимости врач может на 3–4 дня увеличить дозу ранитидина или фамотидина, что ускоряет заживление язвенного дефекта, но самостоятельно менять схему лечения нельзя из-за увеличения риска возникновения побочных действий.
Возможно сочетанное применение омепразола с ра-нитидином или фамотидином, однако такую схему может назначить лишь опытный специалист.
При назначении медикаментозной терапии имеет значение размер язвенного дефекта: если размеры язвы двенадцатиперстной кишки превышают 9 мм, а размеры язвы желудка превышают 7 мм, то лучше применять более сильные лекарственные средства (омепра-зол и др.).
Хороший эффект может быть получен также при использовании препаратов висмута или при приеме сукральфата. Де-нол (коллоидный субцитрат висмута) можно назначать по двум схемам: или 2 раза в сутки по 240 мг (интервал 12 часов) за 30 минут до завтрака и ужина; или 4 раза в сутки по 120 мг — перед завтраком, обедом, ужином и перед сном.
Сукральфат (вентер) принимают 4 раза в сутки: по 1 г перед завтраком, обедом, ужином и на ночь. Лечение де-нолом или вентером целесообразно проводить при небольших по размерам, неосложненных язвах, при нерезко выраженных симптомах (прежде всего боли и изжоги). В то же время при более выраженных симптомах — боль, изжога — или более значительных размерах язвенного дефекта де-нол и вентер рекомендуется сочетать с ранитидином (или фамотидином).
При лечении пожилых пациентов учитывают возрастные нарушения циркуляции крови в стенках желудка. Для улучшения кровообращения в мелких кровеносных сосудах желудка из противоязвенных препаратов показан прием коллоидного субцитрата висмута (де-нол). Дополнительно лицам пожилого возраста целесообразно принимать актовегин, улучшающий обменные процессы в тканях организма, и солкосерил, обладающий раноза-живляющим действием.
Данный текст является ознакомительным фрагментом.
| Авторы: НОГР / Лазебник Л.Б. / Ткаченко Е.В. / Абдулхаков Р.А. / Бордин Д.С. / Гриневич В.Б. / Минушкин О.Н. / Пасечников В.Д. / Радченко В.Г. / Рустамов М.Н. / Сайфутдинов Р.Г. / Самсонов А.А. / Сарсенбаева А.С. / Ситкин С.И. / Старостин Б.Д. / Яковенко Э.П. |
ШИФР по МКБ-10: Язва желудка - К 25 Язва двенадцатиперстной кишки - К 26
Язвенная болезнь — хроническое рецидивирующее заболевание, основным морфологическим проявлением которого является язва желудка или двенадцатиперстной кишки, как правило, развивающаяся на фоне хронического гастрита, ассоциированного с Helicobacter pylori.
- Клинический.
- Эндоскопический, при язве желудка в обязательном порядке для исключения малигнизации — прицельная биопсия (5-7 фрагментов) дна и краев язвы.
- Рентгенологический, для выявления осложнений (пенетрация, перфорация, стеноз, малигнизация).
- По показаниям — определение кислотообразующей и кислотонейтрализующей функций желудка (внутрижелудочная рН-метрия).
1. Биохимические методы:
1.1. Быстрый уреазный тест (определение активности уреазы в биоптате слизистой оболочки желудка).
1.2. Уреазный дыхательный тест с 13С-мочевиной.
1.3. Аммонийный дыхательный тест (недостаточно информативен).
2. Морфологические методы:
2.1. Гистологический метод — выявление Helicobacter pylori в биоптатах слизистой оболочки антрального отдела и тела желудка.
2.2. Цитологический метод — выявление Helicobacter pylori в слое пристеночной слизи желудка.
3. Бактериологический метод с выделением чистой культуры и определением чувствительности к антибиотикам.
4. Иммунологические методы:
4.1. Выявление антигена Helicobacter pylori в кале (слюне, зубном налете, моче) с применением моноклональных антител.
4.2. Валидированный серологический тест с IgG.
5. Молекулярно-генетические методы:
5.1. Полимеразная цепная реакция (ПЦР) (для изучения биоптатов слизистой оболочки Желудка). ПЦР проводится не столько для выявления Helicobacter pylori, сколько для верификации штаммов Helicobacter pylori (генотипирование), в том числе молекулярно-генетических особенностей, определяющих степень их вирулентности и чувствительности к кларитромицину или другим антибиотикам.
Для первичной диагностики Helicobacter pylori может использоваться любой метод при условии отсутствия лечение ИПП, Н2-блокаторами, антибиотиками или препаратами висмута в течение месяца перед проведением теста. Если у больного не предполагается проведение ЭГДС, предпочтение отдается неинвазивным тестам (13С-дыхательный тест, определение антигена Нр в кале). Диагностика Helicobacter pylori на фоне приема указанных препаратов возможна путем выявления антител к Helicobacter pylori в крови (IgG), при условии, что ранее эрадикация Helicobacter pylori у больного не проводилась.
Для первичной диагностики Helicobacter pylori необходимо использовать минимум два метода, например, цитологический + биохимический уреазный тест, либо гистологический + дыхательный уреазный тест с изотопом 1ЗС. Уреазный тест может давать ложноположительные результаты при заселении верхних отделов желудочно-кишечного тракта грамотрицательными бактериями, способными продуцировать уреазу (Proteus vulgaris, Proteus mirabilis и др.).
Контроль эффективности эрадикации проводится не ранее, чем через месяц после завершения приема лекарств (ИПП, Н2-блокаторы, антибиотики, препараты висмута). Для этого может быть использован любой метод, за исключением определения антител к Helicobacter pylori в крови.
Выбор варианта лечения зависит от наличия индивидуальной непереносимости больными тех или иных препаратов, а также чувствительности штаммов Helicobacter pylori к препаратам. Применение стандартной тройной терапии на основе кларитромицина и ИПП возможно в регионах, где резистентность к нему менее 15—20%. Схемы тройной терапии с метронидазолом не рекомендуются из-за высокой распространенности резистентных штаммов Helicobacter pylori в популяции. В этой ситуации применение других рекомендованных антибиотиков делает их средством выбора.
Проведенные в последние годы исследования свидетельствуют о том, что распространенность резистентных к кларитромицину штаммов Helicobacter pylori в разных регионах России отличается и составляет от 7,6% до 40%.
При неосложненной язвенной болезни двенадцатиперстной кишки прием ИПП после завершения эрадикационной терапии может быть прекращен.
При язвенной болезни желудка и осложненной язвенной болезни двенадцатиперстной кишки рекомендуется продолжение приема ИПП до заживления язвенного дефекта.
Эрадикационную терапию больному с состоявшимся язвенным кровотечением следует начинать сразу после возобновления питания через рот.
Антациды могут применяться как в комплексной терапии в качестве симптоматического средства, так и в виде монотерапии — до проведения диагностики Helicobacter pylori и рН-метрии.
Лечение должно начинаться с соблюдения рекомендаций по изменению стиля жизни и соблюдения диеты и исключения продуктов, вызывающих или усиливающих неприятные ощущения.
Первый вариант. Один из ингибиторов протонной помпы в стандартной дозировке (омепразол 20 мг, лансопразол30 мг, пантопразол 40 мг, эзомепразол 20 мг, рабепразол 20 мг 2 раза в день) и амоксициллин (1000 мг 2 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день) или джозамицином (1000 мг 2 раза в день) или нифурателом (400 мг 2 раза в день) в течение 10-14 дней.
Использование высоких доз ИПП (двойная доза два раза в день) повышает эффективность трехкомпонентной терапии.
Добавление пробиотиков Saccharomyces boulardii к стандартной антихеликобактерной терапии в стандартной дозе в течение 10-14 дней и более улучшает переносимость антибиотиков, повышает эффективность эрадикации Helicobacter pylori и комплайенс пациентов.
Добавление пробиотиков, содержащих некоторые штаммы Lactobacillus acidophilus и/или Bifidobacterium spp., к стандартной антихеликобактерной терапии в стандартных дозах в течение одного месяца улучшает переносимость антибиотиков, повышает эффективность эрадикации Helicobacter pylori и комплайенс.
Добавление некоторых пребиотиков, содержащих, например, ди-, олиго- и полисахариды (фруктоолигосахариды [ФОС], гуммиарабик, лактитол), к стандартной антихеликобактерной терапии в стандартных дозах в течение одного месяца улучшает переносимость терапии, повышает эффективность эрадикации Helicobacter pylori и комплайенс.
Второй вариант (четырехкомпонентная терапия). Препараты, используемые при первом варианте (один из ИПП в стандартной дозировке, амоксициллин в сочетании с кларитромицином, или джозамицином, или нифурателом) с добавлением четвертого компонента — висмута трикалия дицитрата 120 мг 4 раза в день или 240 мг 2 раза в день пррдолжительностью 10-14 дней.
Третий вариант (при аллергии к препаратам пенициллинового ряда) — классическая квадротерапия.
Один из ИПП в стандартной дозировке, висмута трикалия дицитрат по 120 мг 4 раза в день, метронидазол по 500 мг 3 раза в день, тетрациклин 500 мг 4 раза в день в течение 10—14 дней.
Четвертый вариант (рекомендуется только в ситуациях, при которых полноценная терапия невозможна, - поливалентная аллергия к антибиотикам, сопутствующая патология гепатобилиарной системы и категорический отказ пациента от приема антибиотиков).
- A. Висмута трикалия дицитрат по 120 мг 4 раза в день (или 240 мг 2 раза в день) за 30—40 минут до приема пищи и на ночь в течение 28 дней. При наличии болевого синдрома — короткий курс ИПП.
- Б. Один из ингибиторов протонной помпы в стандартной дозировке в сочетании с 30%-ным водным раствором прополиса (100 мл два раза в день натощак) в течение 14 дней.
- B. Один из ингибиторов протонной помпы в стандартной дозировке в сочетании со щелочной углекислой хлоридной-гидрокарбонатной натриевой или хлоридной-натриевой питьевой минеральной водой (по 150—200 мл три раза в день за 90 минут до приема пищи в дегазированном и подогретом до 38 °С виде) и пробиотиками, содержащими некоторые штаммы Lactobacillus acidophilus и Bifidobacterium spp., в стандартных дозах в течение одного месяца. (Прим.: прием щелочной углекислой хлоридной-гидрокарбонатной натриевой или хлоридной натриевой питьевой минеральной воды в течение одного месяца возможен и в качестве адъювантной терапии к стандартной эрадикационной схеме).
- Г. Один из ингибиторов протонной помпы в стандартной дозировке в сочетании с пробиотиками, содержащими некоторыми штаммы Lactobacillus acidophilus и Bifidobacterium spp. в стандартных дозах в течение одного месяца.
Пятый вариант (при наличии атрофии слизистой оболочки желудка с ахлоргидрией, подтвержденной при внутрижелудочной рН-метрии).
Амоксициллин (1000 мг 2 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день), или нифурателом (400 мг 2 раза в день), или джозамицином (1000 мг 2 раза в день) и висмута трикалия дицитрат (120 мг 4 раза в день или 240 мг 2 раза в день) продолжительностью 10—14 дней.
Проводится при отсутствии эрадикации Helicobacter pylori после лечения больных одним из вариантов терапии первой линии.
Первый вариант (классическая квадротерапия). Один из ИПП в стандартной дозировке, висмута трикалия дицитрат по 120 мг 4 раза в день, метронидазол по 500 мг 3 раза в день, тетрациклин 500 мг 4 раза в день в течение 10—14 дней.
Второй вариант. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день) в сочетании с нитрофурановым препаратом: нифурателом (400 мг 2 раза в день) или фуразолидоном (100 мг 4 раза в день), и висмута трикалия дицитрат (120 мг 4 раза в день или 240 мг 2 раза в день) продолжительностью 10-14 дней.
Третий вариант. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза в день или 1000 мг 2 раза в день), левофлоксацин (500 мг 2 раза в день) в течение 10—14 дней.
При отсутствии эрадикации Helicobacter pylori после лечения препаратами второй линии рекомендуется подбор терапии только после определения чувствительности Helicobacter pylori к антибиотикам.
При сохранении язвенного дефекта по результатам контрольной эзофагогастродуоденоскопии на 10—14-й день от начала лечения рекомендовано продолжить цитопротективную терапию висмута трикалия дицитратом (120 мг 4 раза в день или 240 мг 2 раза в день) и/или ИПП в половинной дозе в течение 2—3 недель. Пролонгированная терапия висмута трикалия дицитратом показана также в целях улучшения качества послеязвенного рубца и скорейшей редукции воспалительного инфильтрата.
Проведение эрадикации Helicobacter pylori беременным не показано.
Отсутствие Helicobacter pylori должно быть подтверждено двумя методами при обязательном условии отсутствия терапии ИПП, Н2-блокаторами, антибиотиками или препаратами висмута в течение месяца перед проведением теста.
Антисекреторные препараты: один из ингибиторов протонной помпы (омепразол 20 мг 2 раза в день, лансопразол 30 мг 1—2 раза в день, пантопразол 40 мг 1—2 раза в день, эзомепразол 20—40 мг 1—2 раза в день, рабепразол 20 мг 1—2 раза в день) или блокаторы Н2-рецепторов (фамотидин 20 мг два раза в день) в течение 2—3 недель
Гастропротекторы: висмута трикалия дицитрат (120 мг 4 раза в день), сукральфат по 0,5—1,0 г 4 раза в день, мизопростол 200 мкг 4 раза в день — 14—28 дней
Антациды могут применяться в комплексной терапии в качестве симптоматического средства и в монотерапии (до проведения рН-метрии и диагностики Helicobacter pylori).
АСК – ацетилсалициловая кислота
ГЭР – гастроэзофагеальный рефлюкс
ГЭРБ – гастроэзофагеальная рефлюксная болезнь
ЖКТ – желудочно-кишечный тракт
ИПП – ингибитор протонной помпы
ФД функциональная (неязвенная) диспепсия
Нр – Helicobacter pylori
ПЦР – полимеразная цепная реакция
НПВП – нестероидные противовоспалительные заболевания
ХГ – хронический гастрит
XIII съездом НОГР (Санкт-Петербургским) 12 марта 2013 года, утверждены также:
Читайте также:


