Стрептококк агалактия препарат выбора

Streptococcus agalactiae (стрептококк агалактия) — вид грамположительных факультативно анаэробных β-гемолитических бактерий. По классификации R. Lancefield является стрептококком серогруппы B, распространённая аббревиатура GBS и др. Клетки Streptococcus agalactiae, как и другиих стрептококков, имеют сферическую форму. Чаще всего встречаются парами. Не образует спор. Все штаммы Streptococcus agalactiae обладают группоспецифическим полисахаридом, который состоит из глюкозы, галактозы, N–ацетилглюкозамина и рамнозы.
Инфекции Streptococcus agalactiae наиболее опасны для новорожденных. Однако в последние годы отмечается относительный рост числа заболеваний, вызываемых Streptococcus agalactiae у пожилых лиц, у которых они чаще всего вызывают инфекцию кожи и костей, сепсис без явного источника его происхождения, уросепсис, пневмонию и перитониты.
Streptococcus agalactiae — стрептококк, встречающийся у некоторых лиц в составе нормальной микрофлоры кишечника, у 20-30 % здоровых женщин — в урогенитальном тракте. Передача инфекции от инфицированной матери происходит, как правило, незадолго до родов или непосредственно во время родов. В первые часы и сутки после рождения ребенок также может инфицироваться, однако это случается значительно реже по сравнению с пре– и интранатальным заражением. Streptococcus agalactiae новорожденных не всегда приводит к развитию инфекционного процесса у новорожденных. Факторами риска заболевания ребенка, рожденного инфицированной Streptococcus agalactiae женщиной, являются: возраст беременной ( 12 часов), задержка внутриутробного развития и наличие инфекции Streptococcus agalactiae у ранее рожденных детей.
Стандартную антибиотикопрофилактику проводят бензилпенициллином (в дозе 5 млн ЕД в/в с момента начала родовой деятельности, переходя в дальнейшем на дозу 2,5 млн ЕД каждые 4 часа до окончания родов) или ампициллином (в/в, первоначально в дозе 2 г на введение, а затем – по 1 г каждые 4 часа). При аллергии к пенициллинам их заменяют клиндамицином или эритромицином, но чаще в этих случаях рекомендуют цефазолин (в/в, начиная с 2 г на введение, затем по 1 г каждые 8 часов до окончания родов). При высоком риске развития анафилаксии на бета-лактамные антибиотики может быть использован ванкомицин в/в по 1 г каждые 12 часов до окончания родов.**
* Prevention of perinatal group В streptococcal disease: Revised Guidelines from CDC // Morb. Mortal. Wkly Rep. 2002. Vol. 51. Р. 10–22.
** Садова Н.В., Заплатников А.Л., Шипулина О.Ю., Подкопаев В.Н., Шаргородская А.В., Карасева Л.Н., Скачкова Т.С., Смирнова В.С., Фомина С.Г. Современные возможности этиотропного лечения и профилактики врожденных инфекций // РМЖ. 2016. №6. С. 348-350.
При подозрении на инфекцию Streptococcus agalactiae препаратом выбора является ампициллин. Предпочтителен внутривенное введение. При менингите дозы ампицилина увеличивают. При неинвазивных формах инфекции Streptococcus agalactiae продолжительность монотерапии составляет 10 суток, при вызванных Streptococcus agalactiae неосложненных менингитах — две недели, артритах и остеомиелитах — 3–4 недели, эндокардите и вентрикулите — не менее 4 недель.
Из представленных в данном справочнике антибактериальных средств в отношении Streptococcus agalactiae активны: ципрофлоксацин, норфлоксацин, левофлоксацин, моксифлоксацин, ванкомицин, клиндамицин, азитромицин.
Обнаружение Streptococcus agalactiae у взрослых пациентов, не относящихся к группам риска (беременных женщин и др.) в относительно небольшом количестве (10*3. 10*4 КОЕ на мл) не требует специального лечения, в особенности антибиотикотерапии, если иного не назначит лечащий врач, консультация с которым в данном случае необходима.

Streptococcus agalactiae — представитель большой группы микроорганизмов, отличающихся характерными морфологическими, тинкториальными, культуральными и биохимическими свойствами. Этот условно-патогенный микроб является естественным обитателем организма человека и локализуется преимущественно в кишечнике, носоглотке и влагалище. Стрептококк способствует развитию заболеваний лишь при определенных негативных условиях, ослабляющих иммунную защиту и снижающих общую резистентность организма.
Стрептококк агалактия — нормальный обитатель влагалища здоровой женщины. В количестве, не превышающем 10 4 колониеобразующих единиц, микробы безвредны для организма. Недуг развивается только в случае активного размножения бактерий и приобретения ими болезнетворных свойств. Это происходит при развитии иммунодефицита или переохлаждении. Одномоментное внедрение ударной дозы патогенов заканчивается патологическим процессом. Обнаружение во влагалищных выделениях значительного числа микробов – признак неспецифического воспаления.
У мужчин стрептококк агалактия входит в состав нормоценоза кишечника и носовой полости. При исследовании кала на дисбактериоз количество микробов не должно превышать 10 5 или 10 6 . Микробиологическое исследование отделяемого слизистой носа на микрофлору обнаруживает у здоровых людей стрептококк в количестве 10 3 или 10 4 . Streptococcus agalactiae, проникая в мужские половые органы, вызывает острую форму заболевания.
Стрептококк агалактия представляет серьезную опасность для беременных женщин и новорожденных детей, особенно, недоношенных. В последние годы отмечается рост заболеваемости среди пожилых лиц, у которых инфекция протекает в форме сепсиса, воспаления легких или перитонита. В группу риска также входят лица с тяжелыми соматическими заболеваниями, ослабляющими их иммунитет.
Диагностика патологии, вызванной Streptococcus agalactiae, основывается на данных, полученных в ходе микробиологического исследования влагалищного секрета, мочи, кала. Всем больным показано этиотропное противомикробное лечение антибиотиками из группы пенициллинов, макролидов, цефалоспоринов, а также патогенетическая и симптоматическая терапия, назначенная врачом с учетом индивидуальных особенностей организма.
Этиология
Streptococcus agalactiae — бактерия специфической шарообразной или эллипсоидной формы, способная существовать как в присутствии кислорода, так и без него. Микробы аспорогенны, неподвижны, имеют капсулу и обладают группоспецифическим полисахаридом.

Streptococcus agalactiae под микроскопом
Микроорганизмы окрашиваются по Грамму в синий цвет и располагаются в мазке парами и цепочками. Они требовательны к питательным средам. Растут стрептококки исключительно на средах, содержащих кровь, сыворотку и глюкозу. Эти вещества они используют в качестве источника энергии. Инкубируют посевы в термостате при 37 °С, хотя бактерии способны расти и в более широком диапазоне температур. На кровяном агаре спустя сутки образуются сероватые, очень мелкие колонии с зоной полного просветления по периферии. В бульоне бактерии растут в виде диффузной мути и осадка на дне пробирки.
Патогенные свойства бактерии обусловлены следующими факторами:
- Стрептолизином, разрушающим окружающие ткани, в особенности клетки крови и сердца;
- Лейкоцидином, угнетающим иммунитет и уничтожающим иммунокомпетентные клетки;
- Некротоксином, вызывающим отмирание тканей и воздействующим на работу всего организма;
- Ферментами, обеспечивающими адгезию, инвазию, распространение микробов по организму, поражение здоровых тканей и развитие патологического процесса.
Стрептококки резистентны к замораживанию, высушиванию, прямым солнечным лучам. Погибают бактерии под воздействием антибиотиков, антисептиков и дезинфектантов.
Патогенетические звенья инфекции:
- Внедрение микроба в организм,
- Колонизация слизистой оболочки,
- Возникновение очага воспаления,
- Боль и отек,
- Бактериемия,
- Общее недомогание,
- Интоксикационный синдром,
- Дегидратация,
- Помутнение сознания,
- Регионарный лимфаденит.
Эпидемиология
В природе Streptococcus agalactiae широко распространены. В организме человека они колонизирует слизистую кишечника, носа, глотки, органов выделительной и половой систем. От 15 до 40 % женщин репродуктивного возраста являются бактерионосителями.
Существует три варианта пребывания стрептококка во влагалище:
- Безвредное существование бактерий в организме,
- Бактериальный вагиноз,
- патологический процесс.
Если бактерий в мазке из цервикального канала мало, а лактобактерий много, говорят о первом варианте. Когда количество стрептококков превышает количество молочнокислых бактерий, а число лейкоцитов в поле зрения находится в пределах 50, это признак дисбиоза влагалища. Если лейкоцитов гораздо больше, значит, имеет место воспалительный процесс, протекающий в форме цервицита, кольпита, эндометрита.
Пути распространения инфекции:
- Контактный — через общие бытовые предметы, при поцелуе, объятии,
- Самозаражение – микробы из анальной зоны могут проникать во влагалище,
- Вертикальный — заражение плода во время беременности или новорожденного в родах,
- Половой — во время коитуса без презерватива,
- Воздушно-капельный — при чихании, кашле, близком общении с больным человеком,
- Пищевой — при употреблении обсемененных продуктов питания,
- Гематогенный занос инфекции из первичных очагов – почек или носоглотки.
Новорожденные инфицируются в первые часы и сутки после рождения. Это может случиться и раньше: в пре- и интранатальном периоде.
Для Streptococcus agalactiae характерна осенне-зимняя сезонность. Эти микроорганизмы активизируются в тот момент, когда организм ослаблен вирусами. На фоне ОРВИ чаще всего развивается вторичная бактериальная инфекция.
Факторы, способствующие активации стрептококка и его размножению:
- Гормональный сбой,
- Иммунодефицит,
- Тяжелые соматические заболевания,
- Частое использование лубрикантов,
- Ношение нижнего белья из синтетических материалов,
- Эндокринопатии,
- Вирусные инфекции,
- Дисбиоз кишечника,
- Неправильное подмывании наружных половых органов,
- Редкая смена нижнего белья,
- Использование некачественных гигиенических средств,
- Половой акт без презерватива,
- Стрессы,
- Переохлаждения,
- Состояния после хирургических вмешательств,
- Длительная и бесконтрольная антибиотикотерапия,
- Лечение цитостатиками или гормонами,
- Физическое перенапряжение,
- Сложная экологическая обстановка.
В мужской организм бактерии попадают при незащищенном половом контакте с женщиной-бактерионосителем или в результате дисбиоза кишечника. Инфицирование происходит во время занятий нетрадиционными видами секса. Мужчина-носитель инфекции сам не болеет, но заражает своих партнерш.
При беременности изменяется гормональный фон, что выражается в повышенной секреции прогестерона, угнетающего локальную иммунную защиту. Подобные процессы позволяют сохранить беременность. При этом повышается риск развития инфекционных патологий и обострения хронических заболеваний органов репродуктивной системы.
Клиника
Инфекция, вызванная данным микроорганизмом, у лиц репродуктивного возраста обычно протекает бессимптомно. Клинические признаки воспаления органов мочевыделительной и репродуктивной систем вполне узнаваемы.
Streptococcus agalactiae способен вызвать воспаление мочевого пузыря, уретры, легких, эндокарда, суставов, мозговых оболочек.

- Цистит проявляется режущей болью при мочеиспускании, отсутствием удовлетворения от его опорожнения, императивными позывами, появлением мутной мочи с хлопьями. Острая форма патологии сопровождается интоксикацией, слабостью, цефалгией, резкой потерей работоспособности.
- Симптомами уретрита у мужчин являются: боль при мочеиспускании, неприятные ощущения, чувство жжения в уретре, усиливающиеся после эякуляции, обильное слизисто-гнойное отделяемое, гиперемия устья и отек губок уретры по утрам.
- Бактериальный вагиноз, обусловленный увеличением во влагалище стрептококка, проявляется жжением и зудом в промежности, ноющей болью внизу живота, болезненностью при половом сношении, отеком половых губ, обилием желтоватой слизи.
У женщины инфекция часто протекает скрыто, бессимптомно. Стрептококки очень опасны для появившихся на свет малышей. Если произошло заражение внутри утробы матери, ребенок рождается с лихорадкой, гематомами, выделением крови изо рта, тяжелым дыханием. При инфицировании плода развивается сепсис, воспаление легких, мозговых оболочек, сердечной мышцы. Больные дети погибают практически сразу после рождения.
Причиной антенатальной гибели плода также может стать Streptococcus agalactiae. Патологоанатомы на вскрытии обнаруживают признаки гипоксии, увеличенное кровенаполнение органов, петехиальные геморрагии на эпикарде, отечность мозга, размягчение и разжижение тканей. На плодных оболочках определяется очаговая лейкоцитарная инфильтрация.
Диагностика
Заболевание диагностируют на основании результатов анализов. Лабораторная диагностика — основной способ обнаружения Streptococcus agalactiae.

-
В микробиологической лаборатории исследуют мазки из цервикального канала, влагалища, зева, мочу, кал. Окрашенные препараты микроскопируют и обнаруживают кокковую флору. В лаборатории готовят жидкие и плотные питательные среды, содержащие стимуляторы роста для стрептококков и вещества, подавляющие постороннюю микрофлору. На основании полученных в ходе исследования данных о

Лечебные мероприятия
Чтобы избавиться от патологии и ее основных проявлений, необходимо воздействовать на первопричину — убить бактерии. Для этого больным назначают противомикробные препараты — антибиотики. В тяжелых случаях показано патогенетическое лечение, включающее дезинтоксикацию и коррекцию водно-электролитного баланса. Симптоматическая терапия заключается в применении жаропонижающих, антигистаминных, антисептических средств. Дополнительно проводят лечение иммуномодуляторами и иммуностимуляторами.

После купирования интоксикации назначают физиопроцедуры – электрофорез, УВЧ, индуктотермию, СВЧ-терапию, аэроионотерапию, ингаляции, а также массаж грудной клетки, иглоукалывание, ЛФК.
Большое значение в лечении патологии имеет режим. Больным рекомендуют находиться в постели, особенно лицам с выраженным интоксикационным синдромом. Активные движения в разгар болезни замедляют процесс выздоровления и повышают риск развития серьезных осложнений. Дезинтоксикационные мероприятия включают правильный питьевой режим — употребление в сутки до трех литров воды. При отсутствии эффекта от лечения и ухудшении общего состояния больным показана госпитализация в стационар.
Своевременное и правильное лечение делает прогноз инфекции благоприятным. В противном случае заболевание приобретает затяжное течение, развиваются тяжелые осложнения, возможен смертельный исход.
Профилактика
Мероприятия, предупреждающие развитие стрептококковой инфекции:
- Укрепление иммунитета,
- Правильное питание,
- Личная гигиена,
- Борьба с табакокурением,
- Профилактический прием витаминов,
- Оптимальная физическая нагрузка,
- Полноценный сон,
- Отказ от употребления спиртных напитков,
- Санация очагов хронической инфекции,
- Соблюдение санитарно-гигиенических норм и правил,
- Ношение одежды по сезону,
- Защита организма от переохлаждения и сквозняков.
Streptococcus agalactiae в определенном количестве постоянно обитает в организме здоровых людей. Его активация и быстрое размножение очень опасны. Микроб разрушает эритроциты и способствует развитию воспаления там, где его количество максимально. При своевременном обнаружении стрептококка и правильном этиотропном лечении прогноз на выздоровление улучшается, и значительно снижается риск развития опасных для жизни осложнений.
Часть микрофлоры организма составляют условно-патогенные бактерия, такие как стрептококки группы В рода агалактия. В норме они присутствуют в теле человека в низких концентрациях, не оказывая влияния на работу его органов и систем. Воспаление начинается при их интенсивном размножении, под воздействием внешних или внутренних провоцирующих факторов (изменения гормонального фона, падение иммунитета).
Что такое стрептококк агалактия
Группа условно-патогенных бактерий, называемая стрептококками, в небольших концентрациях может присутствовать в организме человека, не вызывая развития инфекции или воспаления. Все микроорганизмы рода Streptococcus по характеру роста на питательных средах подразделяют на гемолитические, негемолитические и зеленящие. Стрептококки из рода агалактия (Streptococcus agalactiae) относятся к грамположительным бета-гемолитическим стрептококкам группы В.
Бактерия попадает в организм после начала половой жизни, обитает во влагалище, прямой кишке, урогенитальном тракте и носоглотке. Существует риск заражения ребенка от инфицированной матери во время родоразрешения или незадолго до его начала). Показателями нормы считают концентрации не более 10 в 4 степени КОЕ/мл. Инфекции, вызываемые стрептококками этого типа при росте их концентраций, особенно опасны для новорожденных и людей пожилого возраста, для которых они чреваты уросепсисом, перитонитом и пневмонией, инфекциями костей и кожи.
К основным путям попадания бактерии рода агалактия в организм относят половой, бытовой, воздушно-капельный, пищевой, и пренатальный или интранатальный (от матери к новорожденному). Активное размножение стрептококков происходит на фоне нарушения баланса нормальной микрофлоры из-за ряда следующих факторов:
- ослабление иммунитета;
- нарушение правил интимной личной гигиены;
- регулярные спринцевания (у женщин);
- гормональные сбои;
- ношение нижнего белья из синтетических тканей;
- незащищенный сексуальный контакт.
Стрептококк агалактия у мужчин активизируется либо после секса без использования презерватива, либо на фоне дисбактериоза кишечника после антибиотикотерапии или в следствие влияния иных факторов. После первоначального инфицирования носитель становится способен передавать бактерию возбудителя своим половым партнерам (самый распространенный путь передачи инфекции).
Отдельную группу риска представляют собой новорожденные. По статистике, носителями стрептококка Agalactiae является около 30% всех здоровых женщин, у которых во время беременности на фоне гормональных изменений могут обостряться вызываемые патогенным микроорганизмом инфекции (циститы, уретриты и др.). Угроза заражения ребенка растет при следующих обстоятельствах:
- возраст матери старше 20 лет;
- аборты или выкидыши в медицинском анамнезе матери;
- преждевременные роды (до 37 недели);
- амнионит;
- хроническая инфекция мочеполовых путей;
- задержка внутриутробного развития;
- лихорадочный синдром во время родов.

Микроорганизмы типа агалактия при интенсивном размножении вызывают инфекционные заболевания мочеполовой системы, сопровождающиеся воспалительным процессом. Активность бактерии сопровождается выделением следующих соединений и токсичных веществ:
- Некротоксинов и летальных токсинов, провоцирующих некроз тканей.
- Лейкоцидина, разрушающего клеточный иммунитет.
- Стрептолизина, способствующего разрушению тканей.
- Амилаза, гиалуронидаза, протеиназа, способствующие распространению стрептококковой инфекции.

Симптомы увеличения концентрации стрептококка агалактии
Бактерия стрептококк агалактия в моче или влагалищном мазке в увеличенных концентрациях свидетельствует о текущем воспалительном инфекционном процессе. В зависимости от типа инфекции, проявляется характерная симптоматика:
- При инфицировании мочевыделительных путей – зуд или жжение в области половых органов, цервикального канала, учащенные болезненные мочеиспускания, отечность и покраснение половых губ или анальных складок, боли в нижней части живота, выделения из мочеиспускательного канала.
- При стрептококковом тонзиллите (ангине), фарингите и др. бактериальных инфекциях дыхательных путей – лихорадка, признаки тяжелой общей интоксикации, поражение слизистых.
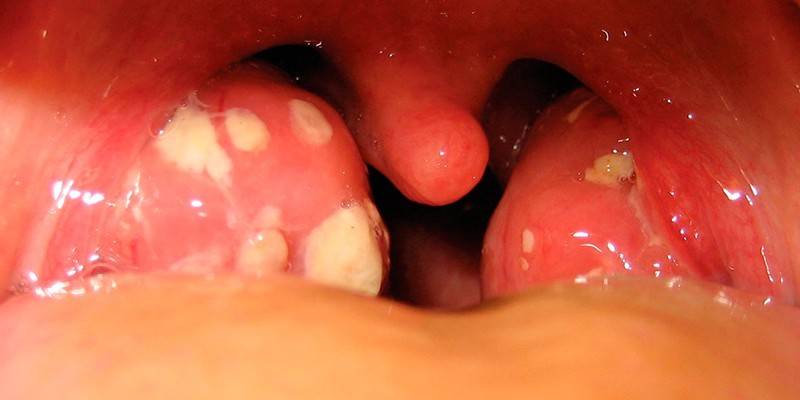
Чем опасен стрептококк агалактия при беременности
Согласно статистике, стрептококки в мазке у женщин почти в 40% случаев обнаруживаются во время беременности. На фоне сниженного иммунитета максимально активное размножение агалактии наблюдается на 33-37 неделе, поэтому на этих сроках обязательно назначаются анализы для выявления возбудителя и его обезвреживания (при необходимости). Факторами, увеличивающими риск инфицирования, являются:
- обнаружения стрептококков этой группы в моче;
- диагностированная угроза преждевременных родов;
- диагностирование стрептококковой инфекции у предыдущих детей.
У беременной женщины агалактии могут вызывать воспаления мочеполовой системы, легких, спровоцировать следующие опасные осложнения беременности и родовой деятельности:
- эндометрит (воспаление внутренней оболочки матки);
- преждевременное отхождение околоплодных вод;
- хориоамнионит (воспаление плодных оболочек);
- выкидыш на любом сроке;
- преждевременное родоразрешение;
- сепсис, менингит, эндокардит(воспаление внутренней оболочки сердца) у новорожденного.
Диагностика
Обнаруживается стрептококк агалактия в мазке из влагалища, уретры или прямой кишки, который может быть назначен при обнаружении кокковой флоры в анализе мочи. После обследования биоматериала методом лабораторной микроскопии проводят посев на питательную среду, помогающий точно идентифицировать тип бактериального заражения, степень концентрации микроорганизмов и их устойчивость к антибактериальным препаратам.
Дополнительно назначаемыми анализами являются скрининг-тесты: ИФА (иммуноферментный анализ) и метод ПЦР (полимеразно-цепной реакции). Остальные лабораторные и инструментальные методы диагностики (общий и биохимический анализ крови, мочи, УЗИ и пр.) назначаются для выявления заболеваний, развитие которых вызвано активным размножением Streptococcus agalactiae.
Лечение streptococcus agalactiae
Необходимость медикаментозного лечения возникает при обнаружении концентраций стрептококков этой группы до 10 в четвертой степени КОЕ/мл и выше, даже если инфекция протекает скрыто. При воспалении мочеполовых органов терапию проходят оба половых партнера, при инфекции смешанного типа возможен прием антибиотиков разных фармакологических групп, при хронической форме заболевания пациенту с острой стадией болезни рекомендован прием иммуностимуляторов, ферментов, прохождение курса физиотерапии.
В зависимости от типа инфекции антибактериальные препараты назначаются в форме средств для перорально приема или в иных лекарственных формах (например, вагинальные таблетки или свечи Флуомизин, Тержинан, Гексикон,). Активность по отношению к агалактии проявляют пенициллины (Оксациллин, аминопенициллины), макролиды (Эритромицин) и Цефалоспорины (Цефазолин).
Если существует опасность заражения ребенка во время родов, матери назначаются внутривенные инъекции, проводимые прямо при родоразрешении, может рекомендоваться антибактериальная санация родовых путей перед родами. После курса антибиотиков и выведения бактерии требуется терапия с применение пробиотиков или энтеросорбентов (например, Атоксила) для восстановления естественной нормальной микрофлоры кишечника.
Профилактика
К профилактическим мерам предотвращения стрептококкового заражение является соблюдение правил личной гигиены и безопасности половых контактов, мероприятия по поддержанию естественного иммунитета, нормального баланса микрофлоры:
- полноценное питание;
- активный образ жизни, занятия спортом;
- здоровый режим дня;
- прием витаминов;
- закаливание организма, избегание переохлаждения;
- полноценный отдых;
- отказ от вредных привычек.

Стрептококки серогруппы В (СГВ) давно известны как возбудители мастита крупного и мелкого рогатого скота и получили название Streptococcus agalactiae. Ранее, до 1937 г. включительно, этот микроорганизм рассматривался как комменсал организма человека. С 60-х годов этот вид, как патоген человека, изредка начали выделять при самых различных нозологических формах инфекции: эндокардите, пиелонефрите, менингите, пневмониях, абсцессе, перитоните, родовом сепсисе, сепсисе новорожденных, фарингите и т.д. В течение 1970–1980 гг. СГВ становится одним из частых возбудителей гнойно-септических инфекций у новорожденных и матерей в США и Западной Европе. В начале 90-х годов в нашей стране также появляются первые публикации о роли этого вида стрептококка в патологии беременности и при гнойно-воспалительных заболеваниях новорожденных. До настоящего времени официальной регистрации заболеваний вызываемых этим микроорганизмом в Российской Федерации не проводится.
Стрептококки этого вида, согласно современной номенклатуре по определителю Bergay, входят в род Streptococcus семейства Sreptococcaeae, вид S.agalactiae. В основе современной классификации стрептококков лежит деление на серологические группы по классификации Ленсфильд. S.agalactiae отнесены к серогруппе В и являются ее единственными представителями. СГВ – неоднородная популяция, состоящая из ряда серотипов и их сочетаний. В настоящее время выделено 9 серотипов, обозначаемых римскими цифрами: I, II, III ,IV, V, VI, VII, VIII. Тип I разделен на подтипы Ia и Ib.
Место обитания патогена – организм человека, крупный и мелкий рогатый скот, возможность передачи его от животных к человеку и наоборот не доказана. Локализация СГВ у человека – ЖКТ (толстая кишка), влагалище, уретра, иногда микроорганизм может колонизировать зев. Факторы патогенности: способность к адгезии и инвазии, устойчивость к фагоцитозу, гемолизин, гиалуронидаза, пептидаза (нарушает хемотаксис полиморфноядерных лейкоцитов к месту инфекции СГВ).
СГВ могут вызывать у людей тяжелые инфекции. Наиболее чувствительны к ним новорожденные, беременные женщины, больные диабетом, хронические больные, дети с дистрофией, пожилые люди, лица с пониженным иммунитетом. С СГВ могут быть связаны самопроизвольные аборты, преждевременные роды, хориоамниониты, пиелонефриты, инфекции мочеполовых путей, эндокардит, сепсис, а также осложнения после кесарева сечения, менингиты, маститы и эндометриты у родильниц. У новорожденных детей СГВ в основном вызывает сепсис, менингит и пневмонию. Передача возбудителя новорожденному может происходить интранатально и постнатально. По данным зарубежных источников в последние годы отмечается относительный рост числа заболеваний, вызываемых СГВ у пожилых лиц на фоне некоторого снижения заболеваемости среди новорожденных детей. Наблюдаемое явление связывают, c одной стороны, с активной профилактикой этой инфекции в родильных домах, а с другой, с увеличением числа пациентов пожилого возраста со сниженным иммунитетом. У последних СГВ обычно вызывают инфекцию кожи и костей, сепсис без явного источника его происхождения, уросепсис, пневмонию и перетониты. Нередко перечисленные инфекции возникают у таких пациентов повторно.
Важную роль в развитии СГВ инфекций у новорожденных детей играют факторы, предрасполагающие к заболеванию, так называемые “факторы риска”, которые условно можно разделить на две группы:
- cвязанные с особенностями родов или колонизацией СГВ матерей;
- имеющие непосредственное отношение к новорожденным.
К первой группе можно отнести присутствие СГВ на слизистой шейки матки у беременных женщин, массивность колонизации (выделения патогена одновременно из нескольких обследованных локусов), случаи СГВ инфекций детей в анамнезе у рожениц, преждевременные роды, длительный безводный период, подъем температуры во время родов, хориоамнионит, бактериурия, обусловленная СГВ.
Ко второй группе – факт и массивность колонизации новорожденных СГВ, недоношенность и малый вес при рождении, рождение посредством кесарева сечения, внутриутробное инструментальное исследование плода, длящееся более 12 часов.
Пенициллин по-прежнему остается наиболее эффективным и распространенным препаратом для лечения инфекций вызываемых стрептококками. Наряду со стрептококками серогруппы А, СГВ сохраняют свою чувствительность к данному антибиотику, хотя у штаммов СГВ в незначительном числе случаев отмечается устойчивость к пенициллину G. Помимо пенициллина, у стрептококков выявлена высокая чувствительность к ампициллину, эритромицину, клиндамицину, линкомицину, оксациллину и меропонему. Первые три поколения цефалоспринов за исключением цефокситина и моксалактама обладают более широким спектром активности по сравнению с пенициллином. Отмечена также высокая чувствительность СГВ к ряду сравнительно новых препаратов с широким спектром активности: тиенамицину, мезлоциллину, азлоциллину и пиперациллину. У штаммов СГВ установлена частая устойчивость к аминогликозам, налидиксовой кислоте, тетрациклину, хлорамфениколу, бацитрацину, триметоприму и метромнидазолу. Тем не менее при сочетанном применении аминогликозидов с пенициллином или ампициллином в экспериментальных исследованиях на лабораторных животных выявлен синергетический эффект таких комбинаций. В последние годы в зарубежной литературе появляются сообщения о выделении штаммов СГВ устойчивых к бета-лактамным антибиотикам. Природу этого явления связывают с появлением в клетках микроорганизмов генов ответственных за синтез пенициллин связывающих белков (ПСБ). По данным ряда зарубежных исследователей число штаммов СГВ резистентных к эритромицину может колебаться от 5,9 до 32,0% и число штаммов устойчивых к клиндамицину от 6,9 до 14,3%. Применение лечебных бактериофагов для профилактики и лечения СГВ инфекции в настоящее время невозможно из-за отсутствия активных специфических бактериофагов.
Показания к обследованию. Рождение ребенка с СГВ–инфекцией в анамнезе у роженицы, СГВ–бактериурия во время данной беременности, угроза преждевременных родов, подъем температуры во время родов (≥ 38°C), безводный период продолжительностью более 18 ч.
Материал для исследования. Кровь, СМЖ, мокрота, плодная жидкость, суставная жидкость, фрагменты пораженных тканей, мазки из ротоглотки, мазки/соскобы со слизистой влагалища, ректальные мазки.
Этиологическая диагностика включает выделение возбудителя и выявление его ДНК.
Сравнительная характеристика методов лабораторной диагностики. Выделение возбудителя в диагностике СГВ–инфекций является “золотым стандартом” и представляет собой важный этап в ряду диагностических мероприятий. Применяется стандартное культуральное исследование с использованием, например, 5% кровяного агара. Своевременное выделение возбудителя с определением чувствительности к антибиотикам во многом определяет эффективность лечения и профилактики данного заболевания.
При подозрении на инфекцию исследуют разнообразный биологический материал. В случае определения носительства СГВ у беременных женщин исследуются мазки со слизистой влагалища и прямой кишки на 35–37 нед. беременности. Если нет возможности провести посев сразу, возможно использование транспортных сред. Время необходимое для выделения и идентификации СГВ обычно составляет от 4 до 5 дней.
Выявление специфического фрагмента ДНК S.agalactiae методом ПЦР проводят при исследовании различного биологического материала. Соскобы эпителиальных клеток с боковых стенок влагалища, перианальные мазки на 34–36 неделях беременности исследуют для выявления колонизации влагалища и/или прямой кишки S.agalactiae; кровь, СМЖ новорожденного – для диагностики септических состояний; мазки из ротоглотки – у новорожденных с клиническими симптомами пневмонии для подтверждения диагноза. Преимуществом данного исследования является то, что оно позволяет выполнить тестирование в течение нескольких часов и тем самым ускорить принятие клинических решений по профилактике и лечению заболевания. Диагностическая чувствительность исследования составляет 81%, диагностическая специфичность – 97,6%. Выявление ДНК S.agalactiae методом ПЦР могут быть выполнены в качественном и количественном формате. Количественный формат теста позволяет использовать исследование для оценки степени колонизации СГВ выбранного локуса. Однако выявление специфического фрагмента ДНК S.agalactiae методом ПЦР не позволяет выявить жизнеспособные микроорганизмы и соответственно определить у них чувствительность к антибиотикам.
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 - 2020

! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Читайте также:


