Стрептококк группы в при родах
Стрептококки группы B (Strept. Agalactiae) — это бактерии, которые обнаруживаются в нижних отделах кишечника 10-35% здоровых мужчин и во влагалище и/или нижних отделах кишечника 10-35% здоровых женщин. Стрептококки группы B не нужно путать со стрептококками группы A, которые вызывают воспаление горла. Лица, у которых стрептококки группы B обнаруживаются в организме, но не вызывают никаких симптомов, называются носителями этих бактерий. Носительство стрептококков группы B не контагиозно, т. е. не передается при контакте от человека к человеку. Эти микробы являются нормальной частью микрофлоры организма. В большинстве случаев они не вызывают никаких проблем. Однако при определенных условиях стрептококки группы B могут вызывать тяжелые инфекции. Такое состояние называется Б-стрептококковой болезнью (БСБ).
Кто может заболеть Б-стрептококковой болезнью?
- В США ежегодно от 15 до 18 тысяч новорожденных и взрослых заболевает тяжелой БСБ, вызывая сепсис, воспаление дыхательных путей и другие опасные инфекции.
- Около половины всех случаев БСБ поражает новорожденных, попадая в их организм во время родов из организма матери-носительницы.
- Стрептококки группы B вызывают септические инфекции у беременных женщин, попадая в полость матки, в околоплодные воды, в разрезы матки после кесарева сечения, в мочевые пути. Ежегодно в США регистрируется более 50 тысяч случаев таких инфекций у беременных.
- 35-40% БСБ поражает пожилых людей или хронически больных.

Стрептококки группы B и Ваш малыш
Около 8000 новорожденных заболевает тяжелой БСБ ежегодно. До 800 их этих детей умирает, а до 20% из тех кто выживает после Б-стрептококкового менингита остаются инвалидами.
У новорожденных БСБ является самой частой причиной сепсиса (заражения крови) и менингита (инфекции оболочек мозга и спиномозговой жидкости) и одной из частых причин пневмонии новорожденных. БСБ является более частой причиной заболеваний, чем такие общеизвестные инфекции как краснуха, врожденный сифилис и spina bifida. Многие из тех, кто выживает, особенно после менингита, впоследствии страдают такими осложнениями как потеря слуха или зрения, различные степени умственной отсталости и церебральный паралич.
В подавляющем большинстве случаев дети вступают в контакт со стрептококками группы B во время родов; кроме того микробы могут попасть в полость матки при преждевременном разрыве оболочек (подтекание вод). Младенцы вступают в контакт с микробами в случае перехода бактерий из влагалища в полость матки. Кроме того, заражение может произойти в процессе прохождения ребенка через родовые пути. Младенцы заражаются, заглатывая околоплодные воды, зараженные микробами, или вдыхая бактерии. Существует предположение, что стрептококки группы Б могут переходить через целые оболочки и поражать внутриутробного плода. В таких случаях они могут быть причиной преждевременных родов, мертворождений и выкидышей.
Фактором риска БСБ является недоношенность, в связи с общей слабостью организма и незрелостью иммунной системы. Недоношенные дети, заболевающие БСБ имеют больший риск стойких осложнений и/или смерти. Однако, поскольку большинство детей рождается в срок, 70% случаев БСБ возникает у доношенных новорожденных.
Большинство (80%) случаев БСБ новорожденных возникает в течение первой недели жизни. Большинство детей заболевает в течение нескольких часов после рождения. При раннем начале заболевания у детей возникают следующие симптомы: нарушения терморегуляции, хрипы, судороги, нарушения дыхания, необычные поведенческие отклонения, гипертонус или выраженный мышечный гипотонус.
Кроме того БСБ может развиться у младенцев в сроки от недели до нескольких месяцев после рождения (позднее начало БСБ). Менингит чаще развивается при позднем начале БСБ. Около половины случаев позднего начала БСБ связано с матерью-носительницей стрептококков группы B. У остальных детей источник инфицирования остается неизвестен. Для позднего начала БСБ характерны следующие симптомы: мышечный гипертонус или гипотонус, постоянный плач, лихорадка, отказ от кормления.
Для уточнения причины заболевания проводятся посевы крови, рентгеновское обследование и другие тесты.
Стрептококки группы B у беременных
Стрептококки группы B являются частью нормальной микрофлоры влагалища и не являются заболеванием, передающимся половым путем. Носительство стрептококков группы B не связано с повышенной сексуальной активностью.
Центр иммунологии и репродукции рекомендует проведение обследование на стрептококк группы B всем беременным женщинам. Первое обследование желательно сделать в первом триместре беременности, особенно если в прошлом были выкидыши или преждевременные роды. Повторное обследование желательно сделать в 35-37 недель беременности. Данное обследование может помочь спасти жизнь Вашему ребенку.
Положительный результат тестов означает, что мать является носительницей стрептококка группы B. Это не означает, что мать болеет стрептококковой болезнью, или что ее ребенок обязательно заболеет. Положительный результат теста поможет врачу и беременной женщине правильно спланировать дальнейшее ведение беременности и родов (профилактическое применение антибиотиков). Результаты обследования должны быть готовы к моменту поступления в роддом.
- Положительные результаты обследования на стрептококки группы B;
- БСБ у ребенка после предыдущих родов;
- стрептококки группы B в моче (симптомная или бессимптомная бактериурия);
- разрыв оболочек (подтекание вод) в сроки ранее 18 часов до родов;
- схватки или разрыв оболочек в сроки беременности менее 37 недель;
- лихорадка в родах;
- возраст младше 20 лет.
Профилактика БСБ
Для снижения риска развития БСБ у новорожденных наиболее эффективным оказалось профилактическое назначение антибиотиков роженице. Лучше, если введение антибиотиков начнется не позднее 4-6 часов до родоразрешения. Если женщина относится к группе риска, то чем раньше начнется введение антибиотиков в родах, тем ниже риск развития БСБ.
Для снижения риска развития БСБ рекомендуется профилактическое назначение антибиотиков всем женщином у которых роды начинаются или воды изливаются ранее 37 недель беременности.
Поскольку антибиотики могут оказывать побочное действие, которое в большинстве случаев достаточно слабо выражено, но в редких случаях может быть достаточно серьезным, решение о назначении антибиотиков принимает врач, учитывая баланс положительных и отрицательных факторов применения этих препаратов. Роженица обязательно должна сообщить врачам об аллергических реакциях на антибиотики в прошлом.
Кесарево сечение не снижает риск развития БСБ.
К сожалению, ни одна схема профилактики не эффективна на 100%.
Некоторые женщины, у которых в последствии развивается БСБ не имеют факторов риска. Поэтому мы настоятельно рекомендуем тестировать всех беременных на носительство стрептококков группы B.
Существует ли вакцина против БСБ?
В настоящее время во многих лабораториях проводится работа над созданием вакцины против стрептококков группы B. Можно надеятся, что внедрение такой вакцины в практику поможет спасти многих новорожденных и снизить риск преждевременных родов.
Женщины, у которых в прошлом были проблемы, связанные со стрептококками группы B, должны сообщить об этом врачам женской консультации и роддома. Профилактика БСБ может предотвратить развитие БСБ при последующих беременностях, и дети будут рождаться здоровыми и свободными от стрептококков.
Кормление грудью не является фактором риска передачи стрептококка от матери к ребенку. Женщины-носительницы могут кормить своих детей грудью. Конечно, руки и соски должны быть чистыми.
Профилактика антибиотиками может предотвратить развитие БСБ у 95% женщин-носительниц. Помните об этом!

Авива Ромм: Стрептококк группы В во время беременности — что делать маме?
Сегодня невозможно открыть журнал или газету без того, чтоб не наткнуться на статью о важности формирования микробиома для здоровья человека. Если вы получили хоть какое-то представление о микробиоме, то вы уже, скорее всего, знаете, что антибиотики — один из факторов, негативно влияющих на микробиом.
Возможно, вы читали также, что у малышей антибиотики повышают риск экземы, аллергии и астмы в детском возрасте, и риск ожирения и диабета впоследствии. Поэтому неудивительно, что беременных женщин и даже многих медиков тревожит широкое применение антибиотиков, а профилактическое назначение их в родах, если у беременной был обнаружен стрептококк группы В, тоже вызывает вопросы. При этом для матери это вопросы сложные:что опаснее — риск развития серьёзной инфекции у ребёнка, если в родах не применять антибиотики, или риск повредить микробиому ребёнка, если антибиотики использовать?
Эта статья отвечает на множество вопросов, заданных мне беременными, объясняет, что такое стрептококк группы В, оценивает риски осложнений для ребёнка при отсутствии лечения, а также рассказывает о достоверности и безопасности самых распространённых тестов на стрептококк группы В, применяемых в беременность, и об альтернативных методов профилактики и лечения.
Что такое стрептококк группы В?
Давайте начнём с азов (на случай, если вы не в теме). Стрептококк группы В (СГВ) — один из миллиардов микроорганизмов, населяющих желудочно-кишечный тракт человека. Мигрируя из тонкого кишечника, он колонизирует прямую кишку, мочевой пузырь и (у многих женщин) влагалище. Таким образом, он часто определяется в вагинальных и ректальных мазках. Непохоже, чтоб СГВ играл особо положительную роль для нашего здоровья, но при наличии здоровой кишечной флоры он не наносит нашему организму никакого вреда. То, что женщина колонизирована СГВ, не означает, что она инфицирована, это означает лишь присутствие бактерии в организме.Такова ситуация у 15% — 30% беременных.
В 70-е годы СГВ был признан главной причиной серьёзных инфекционных заболеваний у новорожденных, включая пневмонию, сепсис и менингит.Чаще всего бактерии передаются новорожденному вертикальным путём (во время родов) либо при попадании бактерий в околоплодные воды с разрывом плодного пузыря. Недоношенные детки и детки женщин с преждевременным излитием вод, имеют повышенный риск развития инфекции СГВ. СГВ также проникает через оболочки, поэтому кесарево сечение от него не спасает; при этом, как и любая операция, КС несёт дополнительные риски. У беременной СГВ может спровоцировать выкидыш, инфекцию мочеполовых путей; он также повышает риск преждевременных родов, преждевременного излития вод и рождения мёртвого ребёнка.
Если беременная, колонизированная СГВ, в родах не получает антибиотики, риск передачи СГВ ребёнку возрастает примерно до 50%. Обратите внимание, что у большинства этих деток инфекция не развивается. Риск развития у такого ребёнка серьёзной инфекции СГВ, угрожающей жизни, составляет по данным Центра контроля и профилактики заболеваний (Centers for Disease Control and Prevention — CDC) от 1 дo 2%.
Уровень смертности при раннем развитии инфекции СГВ у доношенных детей составляет от 2 дo 3% (я знаю, что это звучит ужасно, и я всегда говорю своим пациенткам, что если это ваш ребёнок, это 100%) и от 20 до 30% для недоношенных детей (родившихся до полных 33 недель беременности). Ежегодно (в США — прим.пер.) отмечается 1600 случаев раннего инфицирования СГВ, из них примерно 800 заканчиваются гибелью ребёнка. И это несмотря на профилактическое применение антибиотиков в родах.
Инфицирование СГВ может стать причиной длительного пребывания в отделении реанимации новорожденных, до 44% детей, переживших вызванный СГВ менингит, имеют впоследствии значительные проблемы со здоровьем, включая отставание в развитии, параличи, судорожные припадки, частичную или полную потерю слуха и зрения.
При антибактериальной терапии в родах у ребёнка СГВ-колонизированной матери риск инфицирования снижается почти на 80%. Статистики, говорящей о том, сколько из этих детей будут иметь потом последствия в виде аллергии, астмы, ожирения или диабета, нет.
Как & Когда возникает у малыша инфекция СГВ?
Различают раннее и позднее начало инфекции СГВ. Симптомы раннего начала возникают в первые часы жизни и далее в течение всей первой недели. В одном из крупных исследований, на которое ссылается доктор Ребеккак Дреккер ( Rebecca Drekker, PhD) в своём блоге Evidence Based Birth, говорится, что из 148 000 детей, родившихся между 2000 и 2008 годами, те 94 малыша, у которых развилась ранняя инфекция СГВ, были диагностированы в течение первого часа жизни. И это заставляет предположить, что развитие инфекции началось ещё дородов. Для профилактики раннего инфицирования СГВ используется антибактериальная терапия (профилактическое введение антибиотиков во время родов).
Позднее возникновении инфекции СГВ обычно связано с пребыванием в медицинских учреждениях (внутрибольничная инфекция) и проявляется в течение трёх первых месяцев жизни. Почти у 45% медработников на коже живёт СГВ, через прикосновение этот возбудитель может быть передан новорожденным. Постоянное и тщательное мытьё рук играет огромную роль в профилактике позднего инфицирования.
У кого появляется СГВ? Какие детки инфицируются СГВ?
Хотя любая женщина может быть колонизирована СГВ, для некоторые женщины попадают в группу риска. Туда входят женщины моложе 20 лет, женщины с большим количеством сексуальных партнёров и женщины, пользующиеся тампонами. Активная сексуальная жизнь или сексуальный контакт незадолго до сдачи анализа, оральный секс (куннилингус) и недостаточное мытьё рук обычно связывают с большей вероятностью положительного теста на СГВ. По непонятным мне причинам афроамериканки чаще бывают колонизированы СГВ. Новые исследования в области микробиома предполагают, что нарушенная кишечная флора может способствовать колонизации СГВ. Чуть позже мы этого коснёмся.
В то время как любой малыш матери, колонизированной СГВ, может быть инфицирован, имеются факторы, повышающие этот риск: рождение до срока 37 недель, афроамериканские корни, повышение температуры у женщины в родах, преждевременное излитие вод, длительный безводный период, хориоамнионит (инфекция плодных оболочек), внутренний электронный мониторинг (с расположением датчиков в полости матки или фиксированных к коже головки плода) .
Какие тест стоит сделать. Насколько они достоверны?
Золотой стандарт при определении СГВ — одновременное взятие влагалищного и ректального мазков; это может сделать акушер гинеколог, семейный врач или акушерка. Самое лучшее время для этого — период с 35 до 37 недели. Tакое исследование вдвое эффективнее в плане прогнозирования и профилактики перинатальных заболеваниях, чем обследования на более ранних сроках; хотя у каждой женщины уровень колонизации микроорганизмами индивидуален, и, соответственно, иногда СДВ можно выявить раньше, но рекомендации по борьбе с СГВ, опубликованные в 2002 году, рекомендуют обязательный скрининг на СГВ между 35 и 37 неделями беременности.
СГВ обнаруживается в моче у 2%-7% беременных. Положительный результат анализа мочи на СГВ на ранних сроках беременности тоже является распространённым диагностическим методом; такой результат говорит о высоком уровне колонизации СГВ во влагалище и прямой кишке и является фактором риска раннего инфицирования новорожденного СГВ. Таким образом, это считается показанием к применению антибиотиков в родах. Антибактериальная терапия СГВ в выделительной системе не уничтожает СГВ половых путей и желудочно-кишечного тракта; часто после окончания лечения происходит реколонизация, поэтому лечение в беременность не отменяет назначение антибиотиков во время родов.
Вышеупомянутые обследования считаются надёжными, ложноположительные результаты бывают редко. Так что если ваш тест положительный, вы колонизированы. Тест проводится в 35-37 недель, чтобы дать организму запас ещё в 5 недель — если тест положительный, он с высокой вероятностью останется положительным и в следующие 5 недель, что позволит организовать профилактические мероприятия во время родов. Отрицательный результат, однако, не означает, что у вас нет СГВ; он может быть ложноотрицательным, то есть не определять существующую инфекцию. Также вы можете быть инфицированы после прохождения теста; таким образом, при отрицательном результате в беременность женщина может иметь положительный результат во время родах. И множество женщин, которые на самом деле были колонизированы СГВ, не получают антибиотиков в родах, так как в беременность тесты не определили СГВ.
FDA (государственная служба США, отвечающая за испытания лекарственных препаратов и допуск их к производству и продаже) одобрила экспресс-тест, с помощью которого СГВ у беременной определяется в течение часа. Обычно тест рекомендуют использовать в родах, если неизвестно, колонизирована ли та СГВ, а результаты срочно нужны по медицинским показаниям (например, в случае преждевременного излития вод). Некоторые исследования утверждают, что надёжность теста достигает 91%, то есть она выше, чем обследование на 35-37 неделе, которое выявляет до 69% всех случаев. Так как у СГВ выработалась устойчивость к антибиотикам, особенно к тем, которые назначают женщинам с аллергией к пенициллину, одновременно с тестом на СГВ рекомендуется сделать посев микрофлоры на чувствительность к антибиотикам.
Не забить ли мне на этот тест, чтоб у меня не нашли СГВ?
Не обойтись ли мне без теста, чтоб не получить положительный результат? — такой вопрос мне задают многие женщины; а многие акушерки, принимающие роды дома, так и делают. Но необходимо учитывать одну вещь: если вы не знаете, есть ли у вас СГВ, и рожаете в роддоме или вас госпитализируют в процессе домашних родов, то при наличии любых факторов риска, включая отошедшие воды, длительный безводный период (более 18 — 24 часов в зависимости от протокола) или подъём температуры, вы получите антибиотики. С другой стороны, если тест на СГВ дал отрицательный результат, антибиотики вам не назначат, и вам не надо будет принимать никаких решений. Таким образом, отрицательный результат может стать преимуществом и успокоить вас, если вы переживаете о наличии СГВ.
А какое лечение и подходит ли оно мне?
С 2002 года всем беременным рекомендовано обследование на СГВ на сроке между 35 и 37 неделями, а также внутривенное введение антибиотиков во время родов женщинам с положительным результатом (обычно это пенициллин или ампициллин, для аллергиков подбирается альтернативный препарат).
Aльтернатива внутривенному введению антибиотиков, используемая в Европе и развивающихся странах, но в США применяемая только домашними акушерками, — это хлоргексидин (антисептический раствор, уничтожающий СГВ). В то время как одни исследования показали, что хлоргексидин снижает колонизацию и инфицирование новорожденных до уровня, сравнимого с уровнем при лечении антибиотиками, другие исследования демонстрируют лишь некоторое снижения уровня колонизации, не влияющее на уровень возникновения раннего СГВ. Необходимо дополнительно исследовать, может ли этот экономичный и простой в использовании метод стать альтернативой рутинному внутривенному введению антибиотиков во время родов для профилактики СГВ. Хлоргексидин также малоэффективен в случае преждевременного излития вод, так как он не препятствует распространению бактерий. Американские акушерки обычно используют раствор хибикленс (Hibiclens), содержащий хлоргексидин.
Имейте в виду, что хибикленс и хлоргексидин не можгут выборочно уничтожить СГВ, они также убивает и нормальную вагинальную флору, обычно на долгие часы после применения. Таким образом, вы избегаете антибиотиков, но не достигает главной цели — сохранения здоровой влагалищной флоры, которая колонизирует ребёнка во время родов.
А если у меня сначала был положительный тест, а следующий тест — отрицательный?
Что касается СГВ во время беременности, то если в эту беременность у вас был хоть один положительный тест на СГВ, то даже при последующих отрицательных тестах вы всё равно находитесь в группе риска, и вам будет рекомендованное внутривенное введение антибиотиков во время родов (заметьте, что если у вас был положительный тест в прошлую беременность, а в эту — отрицательный, то вам антибиотики в родах не потребуется, если только ваш ребёнок не был инфицирован СГВ; в этом случае антибиотики в родах рекомендованы). Так что даже если вы применяете натуральный подход, пытаясь снизить у себя уровень колонизации, в роддоме или в родильном центре по протоколу вам всё равно назначат антибиотики.
Могу ли я отказаться от антибиотиков? Чем я рискую в этом случае?
Вы имеете право отказаться от профилактического введения антибиотиков во время родов. В случае отказа существует низкий (2-3%) риск, что у ребёнка разовьётся раннее инфицирование СГВ; но этот небольшой риск всё равно вдвое выше, чем при использовании антибиотиков.
Я встречала ситуации, где с возникали юридические осложнения, включая привлечение социальных служб для определения, не имеет ли места преступная халатность и жестокое обращение с детьми; и это просто в случае отказа родителей от профилактического назначения антибиотиков в родах. В одном из случаев родителей вынудили дать новорожденному антибиотики на том основании, что мать отказалась от антибиотиков в родах, и это при том, что у ребёнка не было никаких признаков инфекции. В то время, как, скорее всего, вы не встретитесь с такой радикальной ситуацией, настоятельно рекомендуем при наличии положительного результата на СГВ обсудить тактику ведения родов с врачом или акушеркой заранее, а не непосредственно в родах; так вы избежите неприятных сюрпризов.
Важно полностью осознавать все риски СГВ перед тем, как отказываться от профилактического введения антибиотиков во время родов. Также не существует натуральных средств для борьбы с СГВ у женщин с положительным результатом теста в случае признаков инфекции или длительного безводного периода (более 24 часов); ребёнок с признаками инфекции СГВ ДОЛЖЕН получить немедленное лечение сильными антибиотиками. Помните, что если у вас положительный тест на СГВ, то при отказе от антибиотиков в родах, на вас будут давить, чтобы вы согласились на введение ребёнку антибиотиков после рождения.
Может ли здоровый микробиом защитить от СГВ?
Здоровая вагинальная флора и хороший кишечный микробиом могут снизить вероятность колонизации СГВ и в результате снизить вероятность инфицирование ребёнка. Бактерия Lactobacillus известна тем, что препятствует заселению кишечника СГВ. Бактерии Lactobacillus reuteri и Lactobacillus rhamnosisэффективно поддерживают здоровую вагинальную флору. Я рекомендую ежедневный приём 1-2 капсул пробиотиков во время беременности, особенно в третьем триместре, это важно не только в плане профилактики СГВ, приём пробиотиков в третьем триместре также снижает у детей уровень таких осложнений как аллергия, экзема и астма.
Основная классификация стрептококков делит их на 20 типов, названных латинскими буквами. Иногда допускаются и русские обозначения. Для человека опасны стрептококки групп A, B и D (А, Б и Д). Каждая может вызывать серьезные осложнения. Стрептококк группы В является частью микрофлоры организма, но при определенных условиях тоже приводит к тяжелым заболеваниям.
Что такое стрептококк группы Б
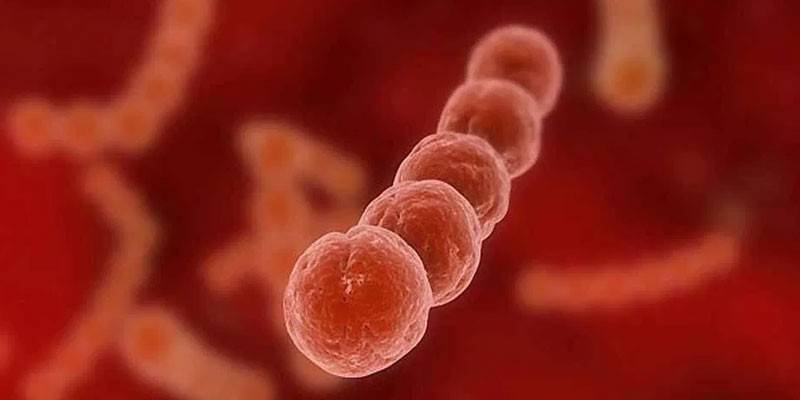
Английское название этого микроорганизма выглядит как Group B Streptococcus (сокращенно – GBS). Микроорганизм относится к категории грамположительных (сохраняющих цвет при окраске по методу Грама) стрептококковых бактерий – Streptococcus agalactiae. Этот стрептококк является бета-гемолитическим. Гамма-гемолитический GBS не причиняет кровяным клеткам вреда, альфа-гемолитический – приводит к частичному их разрушению. Бета-гемолитический стрептококк считается самым опасным, поскольку вызывает полный гемолиз эритроцитов – разрушение с выделением гемоглобина.
Streptococcus agalactiae – это аэробные бактерии, представляющие собой недлинные ленты синего цвета. Они неподвижны и не образуют споры. У некоторых из таких бактерий есть капсула, из-за чего могут возникнуть трудности при лечении инфекции. Сложности бывают связаны и со следующими факторами агрессии этих бактерий:
- Эритрогенин. Это стрептококковый экзотоксин, который провоцирует шок при одноименной инфекции.
- Гемолизин. Данное вещество и вызывает разрушение эритроцитов. Также оно токсически действует на лейкоциты, нарушает функцию тромбоцитов.
- Стрептокиназа. Этот фактор агрессии вызывает дисбаланс между свертывающей и противосвертывающей системами организма.
- Белок типа М. Угнетает иммунитет, повреждает клетки организма.
В организме человека эти бактерии встречаются на слизистой поверхности влагалища у женщин (обсеменение чаще происходит путем загрязнения из прямой кишки) и в нижних отделах кишечника у всех взрослых людей. Своему биологическому хозяину микроорганизм не доставляет дискомфорта при нормальном иммунитете. В случае его снижения, например, при хронических заболеваниях, развивается стрептококковая инфекция группы Б (Б-стрептококковая болезнь, БСБ).
Особенно опасна ситуация носительства GBS у женщины детородного возраста, поскольку она способна заразить ребенка во время беременности или родов. Эти бактерии могут вызывать и следующие заболевания:
- вульвовагинит;
- уретрит;
- цистит;
- послеродовой эндометрит;
- менингит и менингоэнцефалит;
- остеомиелит длинных костей и артрит;
- сепсис новорожденных;
- пневмонию;
- внутрибольничные инфекции.
Пути передачи
Существует несколько способов заражения этой бактерией. Отдельно стоит отметить носительство GBS. Инфекция в этом случае отсутствует, поскольку бактерия никак себя не проявляет из-за крепкого иммунитета, но передаваться другим людям она может. Возможные пути заражения:
- Вертикальный. Заражение ребенка происходит в процессе беременности или родов от матери из-за колонизации прямой кишки или влагалища стрептококками группы В. По статистике стрептококковая инфекция развивается только у одного такого новорожденного из 200.
- Горизонтальный. Это более распространенный (классический) путь передачи возбудителя, связанный с его выходом во внешнюю среду. Инфицирование может происходить во время полового акта с носителем или больным, использования общих бытовых предметов, через слюну, при чихании или кашле зараженного.
Симптомы
У большинства мужчин и женщин стрептококки никак себя не проявляют. Инфекции начинают развиваться только при ослаблении иммунных сил организма. Возможные формы протекания заболевания:
- послеродовой сепсис;
- диабетическая стопа (присоединение инфекции и развитие гнойного воспаления ступни при сахарном диабете);
- гнойный артрит;
- инфекции крови, кожи и мягких тканей;
- перитонит;
- пневмония;
- инфекции мочевых путей, костей, суставов;
- абсцессы;
- перитонит;
- менингит;
- эндокардит.
Существует два варианта стрептококковой инфекции группы Б у новорожденных: ранняя и поздняя. Первая развивается в течение 24 ч. после рождения. Вероятность летального исхода составляет 30–50%. БСБ проявляется в виде:
- бактериемии;
- пневмонии;
- респираторного дистресс-синдрома;
- сепсиса;
- сердечно-сосудистой недостаточности.
Поздние стрептококковые инфекции группы В проявляются у новорожденных на 2–14 сутки, а иногда в течение первых 3 месяцев. Такие дети при рождении выглядят здоровыми. Симптомы формируются в течение первой недели жизни. Чаще болезнь протекает в форме менингита. Риск смерти составляет 15–25%. Симптомы поздней инфекции группы В:
- плохое питание;
- ворчащие звуки;
- проблемы с дыханием;
- голубоватая кожа – цианоз из-за недостатка кислорода;
- судороги;
- диарея;
- рвота;
- аномалии сердечного ритма и артериального давления;
- повышение температуры тела.
Стрептококк группы Б при беременности
У сотен десятков женщин, являющихся носителями GBS, ежегодно рождаются здоровые дети. Факторы риска заражения ребенка В-стрептококком со стороны матери:
- возраст менее 20 лет;
- разрыв мембраны за 18 ч. до родов;
- хирургические или гормональные вмешательства во время беременности;
- стрептококковая инфекция у предыдущего ребенка;
- положительный результат анализа на БСБ;
- разрыв оболочек или схватки на сроке менее 37 недель;
- лихорадка во время родов;
- стрептококки группы Б в моче.
Заражение большинства новорожденных происходит во время родов. Бактерии могут проникнуть в матку и при преждевременном разрыве амниотической оболочки. То же происходит при переходе стрептококков из влагалища в маточную полость. Младенец заражается и при заглатывании околоплодных вод, в которые попали микробы. Это опасно мертворождением, выкидышами, преждевременными родами. Возможные осложнения для рожденного ребенка:
- сепсис;
- менингит;
- пневмония;
- краснуха;
- сифилис;
- потеря слуха или зрения;
- эпилептические припадки;
- умственная отсталость;
- церебральный паралич;
- инвалидизация на всю оставшуюся жизнь.
Беременные должны регулярно обследоваться на стрептококк группы В. Анализ делают несколько раз на протяжении всего периода вынашивания ребенка:
- Первый раз исследование проводится в первом триместре. Особенно это касается женщин, у которых в анамнезе есть выкидыши или преждевременные роды.
- Повторно анализ делают на 35–37 неделе вынашивания плода.
При положительном результате врач спланирует дальнейшее ведение беременности. Метод профилактики инфекции у ребенка – введение женщине антибиотиков не позднее 4–6 часов до родоразрешения. Такая процедура обязательно назначается пациенткам, чьи роды начинаются ранее 37 недели и у которых был выявление стрептококк группы В. Если родоразрешение будет осуществляться посредством кесарева сечения, то введение антибиотиков не требуется до момента отхождения вод и начала родов.

Осложнения
У взрослых стрептококковая инфекция группы Б вызывает различные заболевания, каждое из которых имеет свои последствия. Список возможных осложнений для беременных женщин включает:
- инфекции матки или плаценты;
- выкидыш;
- гибель плода;
- эндометрит;
- инфекции мочевых путей;
- боль в животе, кровотечение, гнойные выделения из влагалища и лихорадка спустя несколько дней после рождения ребенка.
Диагностика
Лабораторная диагностика GBS имеет сложности, поскольку бактерии, которые ее вызывают, культивируются в особых условиях. Для их обнаружения в крови применяют специальные питательные среды, такие как кровяной агар и сахарный бульон. Используемые методы диагностики:
- окраска мазка по методу Грама;
- мазок женской вагинальной и ректальной области на 35–37 неделе у беременных женщин;
- люмбальная пункция при подозрении на менингит;
- рентген грудной клетки для оценки наличия пневмонии;
- анализ мочи (в случае дизурии или учащенного мочеиспускания);
- серологическое исследование на выявление в крови антител к GBS.
Лечение
Основой терапии выступает внутривенное введение антибиотиков. Стоит отметить, что они неэффективны для профилактики ранней начальной стрептококковой инфекции перед родовым процессом, поскольку стрептококки могут быстро расти. По этой причине женщины, у которых эта бактерия была обнаружена в моче, антибактериальные препараты получают во время самих родов. Введение антибиотиков беременным, не знающим о статусе стрептококков группы В, показано и в следующих случаях:
- если с момента отхождения вод прошло 18 и более часов;
- при преждевременных родах (ранее 37 недели);
- на фоне лихорадки во время родоразрешения.
Выбор определенного антибиотика осуществляют после получения результатов анализа на выявление возбудителя инфекции. До этого момента врач назначает препараты широкого спектра действия, чаще – пенициллины. При ранней стрептококковой инфекции группы Б у новорожденных начинают срочное лечение антибиотиками. Курс длится 10–14 дней. Такая терапия эффективна, но некоторым детям требуется реанимация. Взрослым в зависимости от тяжести состояния и индивидуальных симптомов дополнительно могут назначить:
- Иммуномодуляторы: Лизобакт, Иммунал, Имунорикс. Используются с целью повышения защитных сил организма.
- Стрептококковый бактериофаг. Назначается в более тяжелых случаях. Это иммунобиологический препарат, который приводит к лизису (разрушению) бактериальных клеток.
В отношении стрептококка группы В эффективны цефалоспорины, оксациллины и пенициллины. Последние назначаются чаще и являются препаратами первой линии выбора при стрептококковой инфекции. Только пенициллин как антибиотик против стрептококка действительно эффективен, поскольку к нему не выработалась устойчивость этой бактерии. Кроме того, такой препарат имеет низкую вероятность развития побочных эффектов даже при использовании высокой дозы.
При лечении сепсиса новорожденных часто используют сочетание Гентамицина (антибактериальный препарат из группы аминогликозидов) и Ампициллина. Показания к применению Ампициллина:
- менингит;
- септицемия;
- перитонит;
- сальмонеллез;
- скарлатина;
- хламидиоз у беременных;
- пиелонефрит;
- гонорея;
- цервицит;
- инфекции мочевыводящих путей.
Преимущество Ампициллина – разрешен с месячного возраста, но только в форме суспензии. Кроме того, по показаниям его можно применять и во время беременности. Недостаток – нельзя использовать этот антибиотик во время лактации. При лечении пенициллинами чаще удается избежать побочных эффектов, но для небольшой части пациентов они являются аллергенными. В таком случае используют другие антибактериальные средства:
Последний препарат относится к группе цефалоспоринов. Активное вещество антибиотика блокирует биосинтез клеточных стенок микробов, приводя к их гибели. Недостаток Цефазолина – плохо всасывается из желудочно-кишечного тракта. По этой причине антибиотик применяется внутривенно или внутримышечно. Концентрация активного компонента Цефазолина выше в желчи, чем в крови. Это является преимуществом препарата при лечении острых холециститов. Другие показания к использованию Цефазолина:
- сепсис;
- перитонит;
- заражение крови;
- воспаление оболочки сердца;
- инфекции суставов и костей;
- инфекции мочевыводящих или дыхательных путей.
Еще один риск при лечении антибиотиками – появление диареи и тошноты. Кроме того, такие препараты негативно влияют на микрофлору кишечника. По этой причине врачи не назначают антибактериальные средства без серьезной необходимости, что особенно касается новорожденных. Некоторые специалисты ждут 12 ч. после рождения, чтобы посмотреть, как будет меняться состояние ребенка. Только потом окончательно принимают решение о назначении антибиотиков.
Прогноз
При определении прогноза учитываются возраст пациента и наличие у него других заболевания. Здесь можно привести некоторые данные статистики:
- Смертность среди беременных с инфекцией стрептококков группы В имеет низкие показатели. Если женщина является носителем этих бактерий, то она может заразить ими ребенка.
- Вероятность инфицирования новорожденного без введения беременной антибиотиков перед или во время родов составляет 1:200. При проведении антибиотикотерапии риск инфицирования понижается до 1:4000.
- Смертность среди взрослых с инвазивной стрептококковой инфекций группы Б составляет 5–47% в зависимости от общего состояния. Вероятность летального исхода выше у пожилых, поскольку большинство из них имеют первичные заболевания.
Профилактика
Для предотвращения заражения ребенка беременные должны регулярно проходить скрининг, в том числе и анализ на стрептококк группы В. Тестирование позволяет снизить количество летальных исходов среди новорожденных. К мерам предупреждения GBS относят и следующее:
- соблюдение личной гигиены;
- введение женщине антибиотиков во время родов при положительном результате анализа на Streptococcus agalactiae;
- использование антибактериальных препаратов у детей, рожденных от матерей-носителей;
- взятие мазка из входа во влагалище у беременных на 35–37 неделе беременности;
- проведение через каждые 4 часа на протяжении 2 дней клинического мониторинга детей, у которых типичные симптомы Б-стрептококковой болезни отсутствуют сразу после рождения.
Читайте также:


