Дыхание через трахеостому. Операция на плевре при туберкулезе
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Для цитирования: Наумов В.Н., Шайхаев А.Я., Токаев К.В. ХИРУРГИЧЕСКАЯ ТАКТИКА В УСЛОВИЯХ СОВРЕМЕННОГО ТЕЧЕНИЯ ТУБЕРКУЛЕЗА ЛЕГКИХ. РМЖ. 1998;17:11.
Хирургические методы используют в лечении больных туберкулезом органов дыхания более 100 лет. Разработаны методики оперативного лечения как ограниченных, так и распространенных форм туберкулеза, применяющиеся в сочетании с противотуберкулезной химиотерапией. До 1990 г. оперативное лечение преимущественно проводили при ограниченных поражениях легких. В настоящее время в связи с учащением случаев лекарственной полирезистентности микобактерий туберкулеза приоритет отдается хирургическому лечению распространенных прогрессирующих процессов в легких.
Surgical interventions are used in the treatment of patients with pulmonary tuberculosis over 100 years. Surgical techniques in combination with antituberculosis drug therapy both for restrictive and disseminated tuberculosis have been developed. Before 1990, surgery was made chiefly in restrictive pulmonary diseases. Due to the greater cases of Mycobacterium tuberculosis multiresistance, surgery for disseminated progressive processes in the lung is of high priority.
В.Н. Наумов — профессор, доктор мед.наук, руководитель отдела хирургии ЦНИИ туберкулеза РАМН
А.Я. Шайхаев — доктор мед. наук, ведущий научный сотрудник ЦНИИ туберкулеза РАМН
К.В. Токаев — доктор мед. наук, ведущий научный сотрудник ЦНИИ туберкулеза РАМН, Москва
V.N. Naumov — Prof., MD, Head, Department of Surgery, Central Research Institute of Tuberculosis, Russian Academy of Medical Sciences A.Ya.
A.Ya. Shaikhayev — MD, Leading Researcher, Central Research Institute of Tuberculosis, Russian Academy of Medical Sciences
K.V. Tokayev — MD, Leading Researcher, Central Research Institute of Tuberculosis, Russian Academy of Medical Sciences, Moscow
В России наблюдается рост показателей заболеваемости туберкулезом, в том числе с бактериовыделением, и смертности от него на 70% и более по сравнению с 1990 г. Особое значение имеет увеличение числа больных с тяжелыми остропрогрессирующими формами заболевания, первичной полирезистентностью микобактерий туберкулеза (МБТ) и вторичным иммунодефицитом, которые способствуют развитию эпидемии туберкулеза, а ее последствия, представленные в прогнозах для населения России и других стран мира, крайне неблагоприятны . Антибактериальная комбинированная полихимиотерапия при этих формах туберкулеза часто малоэффективна вследствие лекарственной резистентности МБТ, нарушений иммунитета и др. Поэтому особенно остро встает проблема повышения противоэпидемической роли фтизиохирургии, а также разработки методов спасения обреченных на неблагоприятный исход больных, как правило, молодого и среднего возраста.
Таблица 1. Виды оперативных вмешательств (в %) по поводу туберкулеза органов дыхания, проведенных в ЦНИИТ РАМН за период с 1975 по 1996 г.
Сроки выполнения
1975 – 1990 гг. (n=6416)
1992 – 1996 гг. (n=1008)
кавернопластика, торакопластика, ЛЭП)
Исторический путь развития хирургических методов лечения больных туберкулезом легких и плевры в мире и в России насчитывает более 100 лет. Хирургия туберкулеза легких стала важной проблемой во всем мире еще в доантибактериальный период. В нашей стране Н. Г. Стойко выполнял операции торакопластики, начиная с 1917 г. В 1936–1938 гг. Л.Л.Богуш в Нижнем Новгороде успешно проводил операции перевязки легочных вен, удаления доли пораженного туберкулезом легкого. К 60-м годам эпидемиологическая ситуация в Европе и Америке значительно улучшилась, и количество операций стало уменьшаться. В Советском Союзе в связи с сохраняющейся высокой распространенностью туберкулеза с 1961 г. была принята государственная программа по его хирургическому лечению. При областных противотуберкулезных диспансерах (ПТД) были открыты типовые хирургические отделения, подготовлены специалисты-фтизиохирурги.
Таблица 2. Эффективность хирургических вмешательств при туберкулезе органов дыхания, проведенных в 1992 – 1996 гг., в ЦНИИТ РАМН
Названия операций
Клинический эффект, %
Летальность, %
Количество операций по поводу торакального туберкулеза постоянно увеличивалось и к 1989 г. достигло 28 000 в год. Были разработаны методы хирургического лечения как ограниченных, так и распространенных туберкулезных поражений легких, исключая остро прогрессирующие формы, в том числе казеозную пневмонию.
Начиная с 90-х годов отмечено нарастание частоты развития остропрогрессирующих форм туберкулеза легких, включая казеозную пневмонию, плохо поддающихся противотуберкулезной терапии. Происшедшие изменения в клиническом течении туберкулеза легких потребовали коррекции хирургической тактики и разработки новых хирургических методов лечения, применимых при остропрогрессирующих формах туберкулеза.
Таблица 3. Пневмонэктомия при двустороннем туберкулезном поражении
В настоящее время фтизиохирургия должна ориентироваться в первую очередь на совершенствование методов хирургического лечения больных с заразными прогрессирующими формами туберкулеза, чтобы предотвратить рост резервуара инфекции и добиться снижения показателя смертности. Совершенствование методов химиотерапии, особенно внедрение новых программ противотуберкулезной терапии, новых мощных антибиотиков широкого спектра и иммуномодуляторов, совершенствование хирургической и анестезиологической техники, использование новых технических средств открывают новые возможности для расширения показаний к операциям у ранее бесперспективных больных, даже с двусторонними деструктивными процессами. Таким образом, сформировались условия для пересмотра хирургической тактики.
Табл. 1 показывает изменения в структуре хирургических операций у больных туберкулезом легких, проведенных в хирургическом отделе ЦНИИ туберкулеза РАМН за последние 20 лет.
Частичные, экономные и комбинированные резекции легких при ограниченных туберкулезных процессах ранее были основными во фтизиохирургической службе по стране и составляли более 80 % всех операций при туберкулезе. Показания к этим видам операций и техника их выполнения хорошо отработаны, прошли испытание временем и не претерпели существенных изменений. Общее сокращение числа частичных резекций с 27,4 до 13,9 % объясняется не столько поздней выявляемостью ограниченных форм туберкулеза (снижение роли профилактических осмотров, флюорографии), но и социально-экономическими причинами. Эффективность частичных резекций легких в нашей клинике остается на уровне 98,4 % (табл. 2) .
В арсенале фтизиохирургических вмешательств значительное место вновь приобретают нерезекционные методы лечения: варианты эндокавитарного, в том числе лазерного лечения, экстраплеврального пневмолиза (ЭПП), кавернотомия, кавернопластика, торакопластика, вскрытие полости эмпиемы, торакомиопластика, сроки выполнения которых необоснованно затягиваются на местах. Этот вид операций в нашей клинике составляет от 19,5 до 21,7 %. Основные показания к этим операциям остались прежними: большие (в том числе двусторонние) каверны на фоне обширной диссеминации как основной источник интоксикации при неэффективности полихимиотерапии и прогрессирующем течении заболевания, когда радикальные операции противопоказаны из-за распространенности процесса или ограниченности функциональных резервов пациента. В последние годы уменьшилось число пациентов, которым показана одномоментная кавернопластика. При этом наиболее часто использовались ЭПП, одно- и двухэтапные кавернотомии как самостоятельные (11 %) операции, которые не сопровождались серьезными осложнениями и у 85,7 % больных позволили прекратить бацилловыделение и стабилизировать распространенный туберкулезный процесс. Новый вариант открытого ЭПП весьма щадящий, выполняется с резекцией участков 2–3 ребер (в зоне над каверной), преимущественно из подмышечного доступа с последующим местным лечением каверны путем пункций с введением антибиотиков, использованием различных видов физического воздействия. Такие операции можно проводить в качестве предварительного эффективного лечения с целью стабилизации двустороннего туберкулезного процесса и подготовки к радикальному оперативному вмешательству на стороне основного поражения. Авторы использовали этот вид операций более чем у 40 больных, а за последние 5 лет – у 18 человек при поражении единственного легкого. Кроме того, ЭПП у 21 пациента сочетался с одномоментными этапными (в том числе комбинированными) вмешательствами на контрлатеральном легком. Разработанные в нашей клинике и используемые в настоящее время операции уникальны в мировой практике и могут сыграть еще большую роль в излечении распространенных прогрессирующих деструктивных форм туберкулеза.
Важным разделом современной фтизиохирургии является разработка методов предоперационной подготовки с целью стабилизации туберкулезного процесса, лечение сопутствующих заболеваний: интенсивное местное лечение (пункции, дренирование каверн, внутрилегочное и внутрикавитарное введение препаратов), коррекция легочно-сердечной недостаточности, компенсация сахарного диабета и др.. Прослеживается тенденция использования современных, иммунокорригирующих средств, методов экстракорпоральной детоксикации для эффективного и быстрого способа подготовки к обширным вмешательствам вплоть до плевропульмонэктомии у больных, которые ранее считались неоперабельными и некурабельными.
Классическая плеврэктомия, в том числе и с резекцией легкого, при эмпиеме плевры составила 1,2% против 2,3 % в 80-е годы.
Объясняется это не только уменьшением числа пациентов с постпневмотораксной эмпиемой плевры, но и возрастанием числа больных с хроническими экссудативными плевритами, в излечении которых роль хирургических методов часто незаслуженно принижается.
По данным ПТД, в последние годы увеличился поток больных с экссудативными плевритами среди вновь выявленных больных туберкулезом легких. Общая лечебная сеть отправляет их в ПТД, а последние практически не учитывают, что в случаях хронизации воспалительного процесса в плевре оперативное лечение (в сроки до года от начала заболевания) эффективно и позволяет полностью восстановить функцию дыхания. Поэтому фтизиохирургам следует ориентироваться на раннее (через 4 – 8 мес от момента начала заболевания) применение реконструктивных операций при хронических плевритах и начальных стадиях хронической эмпиемы плевры. Эффективность при этом достигает 98,1%. На операцию удаления легкого (пневмонэктомия, плевропневмонэктомия, доудаление остатков легкого) приходится сейчас 16,2 % вместо 13,4 % в прошлые годы. Послеоперационная летальность достигает 8,1 – 9,2%, эффективность – 86,3 %. Показания для пневмонэктомии при так называемом стабильном одностороннем распространенном деструктивном туберкулезе в настоящее время имеются значительно реже (не более 15%). Оказывается, удельный вес пневмонэктомий обусловлен ростом (до 55%) числа остропрогрессирующих форм фиброзно-кавернозного туберкулеза и его осложнений (пиопневмоторакса, легочных кровотечений), случаев полирезистентности МБТ, когда современная полихимиотерапия уже неэффективна и бесперспективна. При этом пневмонэктомия как одномоментная операция может быть выполнена только у 62,5 % пациентов. Эффективность операции удаления всего легкого при относительно стабильном варианте клинического течения составляет 92%, без летальных исходов. В остальных случаях пневмонэктомия является заключительным этапом комплексного хирургического лечения больных двусторонним осложненным прогрессирующим деструктивным туберкулезом легких (табл. 3) .
Эффективность этапной пневмонэктомии составляет 82,6 % при летальности 10–12,4 % случаев (см. табл. 2). Метод более эффективен, чем одномоментная пульмонэктомия у аналогичных групп больных.
Ключевым моментом новой хирургической тактики при развившихся осложнениях, таких как бронхиальные, торакальные свищи, остеомиелиты ребер, двусторонние осложненные процессы, является трансстернальная трансперикардиальная окклюзия главных бронхов и легочных сосудов на стороне основного поражения. При этом одновременно на стороне меньшего поражения (практически единственного легкого!) осуществляют такие вмешательства, как ЭПП с тампонадой, этапные кавернотомии, реже – частичные резекции. На стороне основного поражения одновременно производят вскрытие полости эмпиемы и каверны с открытой тампонадой. Для предотвращения тяжелой дыхательной недостаточности одномоментно производят трахеостомию с последующей длительной искусственной вентиляцией легких (иногда до 1 – 1,5 мес). Комплексное лечение после первого хирургического этапа, включающее использование полихимиотерапии, экстракорпоральных методов детоксикации, различных типов лазеров, УФО, парентерального питания, позволяет в большинстве случаев подготовить таких пациентов к заключительной операции – удалению легкого.
Таким образом, гармоничное применение всего арсенала фтизиохирургических вмешательств, которые могут выполняться у значительного числа нуждающихся, по нашему убеждению, позволяет значительно снизить резервуар инфекции, расширить возможности хирургического излечения наиболее тяжелой группы больных туберкулезом органов дыхания всех возрастов и определяет хирургическую тактику, соответствующую требованиям времени.
1. Богуш Л.К. Хирургическое лечение туберкулеза легких .- М., 1979.
2. Репин Ю.М. Хирургия отягощенных форм туберкулеза .- Л., 1984.
3. Перельман М.И., Стрельцов В.П., Наумов В.Н. / Органощадящие оперативные вмешательства во фтизиопульмонологии .- М., 1989 -. С.4-7.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Поделитесь статьей в социальных сетях
Авторизируйтесь или зарегистрируйтесь на сайте для того чтобы оставить комментарий.
Дыхание через трахеостому. Операция на плевре при туберкулезе
Проведенное нами изучение температурного режима в трахее показало резкое снижение температуры при дыхании через трахеостомическую канюлю по сравнению с естественным дыханием. Это послужило основанием для применения при искусственной вентиляции подогрева смеси до 30—34°. Накопление и аспирация бронхиального отделяемого после этого производилось значительно реже и в небольших количествах.
Длительное дыхание на респираторах предусматривает на много дней отключение речи больного. С целью сохранения речи больного при искусственной вентиляции легких нами предложена модифицированная трахеостомическая канюля (1967). Принципиально, для осуществления речевой функции, мы используем подведение воздуха в подсвязочное пространство не из легких, а извне. Такое нагнетание воздуха производится независимо от вдоха и выдоха. Возникающий при этом голос не отличается от обычного естественного.
Единого суждения в вопросе о времени прекращения послеоперационной искусственной вентиляции нет. В легочной хирургии, когда нередко операции производятся при наличии уже существующей выраженной легочно-сердечной недостаточности, перевод больного на самостоятельное дыхание представляет особые трудности.
Мы считаем, что при стабильном общем состоянии через 1—2 часа после отключения аппарата: устойчивости пульса, артериального давления, анализа газов крови и частоты дыхания, а также при небольшой гиперкапнии (до 48—50 мм рт. ст.) можно решать вопрос о постепенном отключении респиратора. В процессе перевода на самостоятельное дыхание целесообразно на ночь оставлять больных на искусственной вентиляции. Этим обеспечивался полноценный сон и отдых. Уже при полном переводе на самостоятельное дыхание еще длительный период времени необходимо продолжать интенсивную оксигенотерапию.
Наши наблюдения показали, что метод длительной искусственной вентиляции легких в послеоперационном периоде для лечения острой дыхательной недостаточности в разных возрастных группах (от одного года до 60 лет) является высоко эффективным. Использование послеоперационной искусственной вентиляции легких позволяет расширить показания к вмешательствам в группе больных повышенного операционного риска.
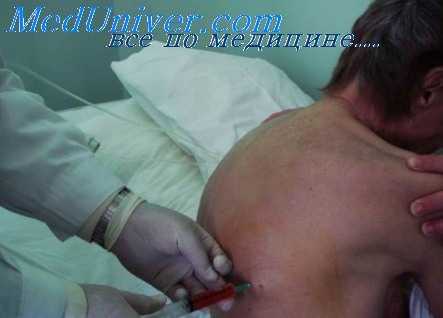
Операция на плевре при туберкулезе
В 1954 г. Л. К. Богуш впервые в нашей стране выполнил операцию на плевре больному туберкулезной эмпиемой.
В тот период поражения плевры при туберкулезе имели значительное распространение, будучи этиологически связанными главным образом с лечением искусственным пневмотораксом. Патогенетически эти поражения обусловлены реактивным воспалением в стенках плевральной полости, вызванным раздражением вдуваемым в нее воздухом. Результатом является образование панцирного плеврита, на фоне которого возможно развитие эмпиемы вследствие вторичного инфицирования содержимого плевральной полости.
Такой характер изменений преобладал в клинике ввиду широкого применения лечебного пневмоторакса, нередко поддерживаемого годами вопреки рецидивирующим пневмоплевритам. Значительно реже врачи наблюдали специфическое воспаление плевры в связи с контактным или лимфогематогенным распространением на нее туберкулезного процесса либо при спонтанном пневмотораксе. Казалось бы, современные методы антибактериальной терапии должны свести к минимуму туберкулезную патологию плевры, поскольку сфера применения искусственного пневмоторакса резко сократилась.
Однако публикации в литературе свидетельствуют о том, что туберкулезная эмпиема не исчезла даже в тех странах, где ведется успешная борьба с туберкулезом.
Морфологические данные позволили нам четко разделить два вида операций на плевре. Для вмешательства, заключающегося в освобождении легкого от сковывающего его панциря, может быть сохранено предложенное его автором наименование «декортикация легкого». Для удаления всего плеврального мешка наиболее приемлем термин «плеврэктомия».
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Пересмотр классических представлений о трахеостомии
Авторы: Крюков А.И. 1, 2 , Кунельская Н.Л. 3 , Кирасирова Е.А. , Тарасенкова Н.Н. , Горбан Д.Г. 4 , Мирошниченко Н.А. 5 , Мамедов Р.Ф. 1
1 ГБУЗ НИКИО им. Л.И. Свержевского ДЗМ, Москва
2 ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, Москва
3 ГБУЗ «НИКИО им. Л.И. Свержевского» ДЗ г. Москвы, Россия
4 ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России, Москва
5 ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, Москва, Россия
Для цитирования: Крюков А.И., Кунельская Н.Л., Кирасирова Е.А. и др. Пересмотр классических представлений о трахеостомии. РМЖ. 2011;6:381.
Несмотря на многовековую историю трахеостомии, до настоящего времени не существует единого мнения в отношении названия операции – «трахеостомия» или «трахеотомия», а также деталей ее выполнения. Принципиальное различие между трахеостомией и трахеотомией заключается в том, что в первом случае края трахеи подшиваются к коже передней поверхности шеи и таким образом формируется стойкая трахеостома. При трахеотомии после продольного или поперечного вскрытия просвета трахеи трахеостома не формируется [1,3,12].
Трахеостомия выполняется в плановом порядке больным, находящимся на искусственной вентиляции легких (ИВЛ), либо с целью восстановления дыхательной функции больным с дыхательной недостаточностью на фоне декомпенсированного стеноза гортани и трахеи (экстренная, срочная, отсроченная трахеостомия). Причины, вызывающие стеноз дыхательных путей, многочисленны: пролонгированная интубация гортани и трахеи, травмы головы и шеи, опухолевые процессы верхних дыхательных путей, операции на щитовидной железе, системные заболевания и другие [6,8].
По статистике наиболее часто стеноз дыхательных путей возникает в результате интубационной травмы. При проведении ИВЛ морфологические изменения в слизистой оболочке и хрящах трахеи различны – от повреждения эпителиального покрова с формированием эрозий и язв слизистой оболочки до полного трансмурального некроза стенки и прилежащих структур с формированием патологических соустий трахеи с окружающими структурами (пищевод, артерии, вены). Большое значение в патогенезе развития рубцового стеноза имеет общее состояние организма. Дыхательная реанимация часто проводится на фоне шока различного генеза, который проявляется нарушением микроциркуляции, в том числе в трахеальной стенке, а также снижением устойчивости различных тканей к инфекции и нарушением регенерации [4,5,7,11].
Для диагностики стеноза гортани и трахеи большое значение имеют эндоскопические методы, которые позволяют своевременно и объективно оценить характер и уровень патологических изменений, степень сужения дыхательных путей, наличие эрозий, язв, грануляций, рубцов, хондромаляцию [2].
В настоящее время большое внимание уделяется предотвращению послеоперационных осложнений после трахеостомии. Важную роль здесь играет правильный подбор антибактериальной терапии, местное ведение послеоперационной раны (уход за трахеостомой), а также адекватное протезирование дыхательных путей. Трахеальная канюля, являясь инородным телом, провоцирует и поддерживает воспалительный процесс в трахее. Воспаление и некроз хрящей трахеи в области трахеостомы нередко обусловлены инфицированием трахеостомической раны или возникновением пролежней и некроза от давления трахеостомической трубки. Поперечный размер трахеостомической трубки не должен превышать 2/3 поперечника просвета трахеи. Правильно подобранная трахеостомическая канюля и адекватный уход за трахеостомой предотвращает возникновение осложнений или сводит их к минимуму [4,9,10].
В данной статье мы обобщили результаты многолетнего опыта лечения пациентов с различными формами стеноза гортани в Отделе реконструктивной хирургии полых органов шеи МНПЦ оториноларингологии Департамента здравоохранения Москвы.
Показания к трахеостомии
• стеноз гортани и трахеи II–III степени различной этиологии;
• необходимость продленной ИВЛ (более 3–5 суток) для исключения воздействия интубационной трубки на структуры гортани;
• необходимость адекватной санации трахеобронхиального дерева.
Техника операции трахеостомии
Термины «верхняя» и «нижняя» трахеостомия ориентированы на положение перешейка щитовидной железы. Однако его положение часто варьирует, поэтому вскрытие трахеи в области 2–4 полуколец может в зависимости от расположения перешейка оказаться верхней, средней или нижней трахеостомией.
У больных, находящихся в отделениях интенсивной терапии, оптимальным сроком проведения трахеостомии от момента начала ИВЛ являются 3–5–е сутки под эндотрахеальным комбинированным наркозом с мышечными релаксантами. Положение больного в обратной позе Тренделенбурга: горизонтально на спине с максимально отведенной кзади головой и валиком под плечами. Чрезмерное запрокидывание головы приводит к смещению трахеи в краниальном направлении, изменению анатомических ориентиров. В этих случаях возможно ошибочное выполнение трахеостомии через 4–6 полуколец. Также при переразгибании головы возможно смещение плечеголовного артериального ствола выше яремной вырезки, что рискованно из–за опасности его повреждения при выделении передней стенки трахеи.
Оптимальным местом наложения трахеостомы считается рассечение у взрослых 2–3 полуколец трахеи, у детей – 3–4 полуколец.
Плохим прогностическим фактором следует считать выполнение высокой трахеостомии, когда происходит повреждение 1–го хрящевого полукольца трахеи или перстневидного хряща, что приводит к его перихондриту, а в последующем – к рубцовому сужению подголосового отдела гортани. Доказано, что фенестрация стенки трахеи приводит к деформации и сужению трахеального просвета на этом уровне [5].
При проведении операции трахеостомии учитываются индивидуальные конституциональные особенности телосложения больного (гиперстеник, астеник, нормостеник), степень выраженности подкожно–жировой клетчатки, возможность разгибания шейного отдела позвоночника.
При операции под эндотрахеальным наркозом инфильтрационная анестезия передней поверхности шеи не обязательна, срединный разрез кожи и клетчатки шеи проводится от уровня дуги перстневидного хряща до яремной вырезки грудины. Тупо, изогнутыми зажимами, послойно выделяется передняя стенка трахеи. Не следует выделять трахею на большом протяжении, особенно ее боковые стенки, так как при этом существует вероятность нарушения кровоснабжения этого участка трахеи и повреждение возвратных нервов. У пациентов с длинной тонкой шеей перешеек щитовидной железы следует смещать кверху; у больных с толстой и короткой шеей и загрудинным расположением щитовидной железы перешеек смещается книзу за грудину. При невозможности смещения перешейка щитовидной железы, его пересекают между двумя зажимами, обшивают синтетическими рассасывающими нитями на атравматической игле. Тщательный гемостаз осуществляется с помощью коагуляционного пинцета. Трахеостому формируют на уровне 2–4 полуколец трахеи. Величина разреза трахеи должна соответствовать размеру канюли (последняя не превышает 8–9 мм); увеличение длины разреза может привести к развитию подкожной эмфиземы, а уменьшение – к некрозу слизистой оболочки и прилегающих хрящей трахеи. Для улучшения стойкости трахеостомы края кожи без особого натяжения подводят к краям разреза трахеи. Формируется стойкая трахеостома, преимущества которой перед несформированной трахеостомой выявляются при смене трахеостомической канюли. Эта манипуляция у пациентов с короткой толстой шеей и несформированной трахеостомой может привести к тому, что трахеальная канюля окажется между слизистой оболочкой и хрящами трахеи, может произойти самопроизвольное выпадение трахеальной трубки при кашле и смене повязки, что может вызвать асфиксию и смерть больного. В просвет трахеи вводят трахеостомические одно– или двухманжеточные термопластические трубки необходимого диаметра с манжетой низкого давления. Особенностью этих трубок является соответствие угла трахеостомической трубки в 105 градусов, естественному анатомическому изгибу шеи. Применение таких трубок позволяет максимально уменьшить риск развития осложнений, связанных с раздражением, вызываемым соприкосновением дистального конца трубки со стенкой трахеи.
Сразу же после окончания операции выполняется санационная фибробронхоскопия (ФБС) для того, чтобы избежать обтурации просвета трахеи и бронхов сгустками крови, попавшими туда во время проведения операции (рис. 1).
Особенности трахеостомии у больных со стенозом гортани и трахеи
различной этиологии
Трахеостомия у больных с рубцовым
(постинтубационным) стенозом
Клинические проявления постинтубационного стеноза гортани и трахеи (одышка и стридорозное дыхание) проявляются чаще всего через 2–4 недели после экстубации или деканюляции. К этому времени пациенты, как правило, уже выписаны из стационара, что приводит к запоздалой диагностике заболевания. Однако декомпенсация дыхания наступает в короткий срок. Провести хотя бы минимальное обследование у таких больных не представляется возможным.
У больных, перенесших оро– или назотрахеальную интубацию трахеи, стенозы могут развиться на уровне складкового или подскладкового отделов гортани, в шейном отделе трахеи – на уровне фиксации раздувной манжетки интубационной трубки. Трахеальный стеноз может сформироваться на уровне бывшей трахеостомы (западение стенок трахеи, грануляции, рубец задней стенки), на месте фиксации раздувной манжетки трахеостомической трубки или в дистальном отделе трахеи.
Трахеостомию у больных с постинтубационным стенозом часто приходится выполнять в вынужденном положении больного (сидя, полулежа), под местной анестезией, что серьезно осложняет доступ к передней стенке трахеи и требует навыка и хирургического опыта.
Особую сложность представляет операция ретрахеостомии у больных с выраженным нарушением дыхательной функции. Это обусловлено тем, что передняя стенка трахеи не определяется при пальпации, рубцами она может быть смещена в ту или иную сторону. Изначально необходимо выделить неизмененные участки гортанно–трахеального комплекса, вскрыть трахею на этом уровне, а затем по проводнику, которым может служить зажим или расширитель Труссо, вскрывать трахею на уровне рубцового сужения до неизмененного участка. Если ориентирование затруднено, то расположение трахеи можно уточнить по аспирационной пробе. Если при пункции в шприц с жидкостью при аспирации попадает воздух, то игла находится в полости трахеи. В этом случае целесообразно вскрытие передней стенки трахеи «по игле».
По возможности следует проводить одномоментную трахеопластику с целью стойкого расширения суженного участка трахеи. Интраоперационно и в послеоперационном периоде обязателен эндоскопический контроль расположения трахеостомической трубки и выполнения санации трахеи.
Трахеостомия у больных с параличом гортани при повреждении возвратных гортанных нервов
У пациентов, перенесших струмэктомию, трахеостомию предпочтительно проводить под эндотрахеальным наркозом ввиду отсутствия анатомических ориентиров на передней поверхности шеи. По прошествии 6 и более месяцев после струмэктомии ткани передней поверхности шеи представляют собой единый рубцовый конгломерат. Трахея, запаянная в рубцах, часто смещена в сторону от средней линии. Найти и выделить трахею из рубцов технически сложно. Интубационную трубку проводят в трахею через суженную голосовую щель по гибкому бронхоскопу. Трахею необходимо выделять тупо, стараясь не повредить ушитых во время предыдущей операции крупных сосудов. Далее ход операции традиционный. По завершении операции в рану необходимо ввести резиновые дренажи для предотвращения возникновения и нагноения гематом, возникающих после струмэктомии.
Трахеостомия у больных с острой травмой шеи
У больных с травмой шеи (тупой, резаной, колотой, огнестрельной) необходимо перед проведением трахеостомии определить характер, глубину и протяженность повреждения гортани, трахеи и пищевода. Трахеостомия выполняется под местной анестезией, после чего пациента переводят на управляемое дыхание. При наличии показаний вторым этапом выполняют реконструктивную операцию в необходимом объеме: ларингоэпиглотопексию, ларинготрахеопексию, трахеопексию, трахеопластику, ушивание ткани поврежденной щитовидной железы. Для дилатации сформированного просвета гортани и трахеи, профилактики аспирации рекомендуется использование гортанных стентов обтураторов и трахеостомической трубки соответствующего диаметра.
Осложнения трахеостомии
Осложнения трахеостомии делятся на интраоперационные, ранние и поздние послеоперационные.
1. Интраоперационные осложнения:
• эмфизема мягких тканей шеи, лица, грудной клетки, средостения;
• асфиксии, остановка дыхания, резкое падение артериального давления;
• повреждение крупных сосудов и ткани щитовидной железы;
• разрывы трахеи и пищевода.
2. Ранние послеоперационные осложнения:
• эрозивные кровотечения;
• аспирация кровяных сгустков;
• подкожная эмфизема.
3. Поздние послеоперационные осложнения:
• гнойно–некротические изменения тканей в области трахеостомы;
• эрозивное кровотечение из крупных сосудов шеи;
• аспирационная пневмония.
Послеоперационный уход
за трахеостомой
Для предупреждения послеоперационных осложнений после трахеостомии применяют комплексную местную и посиндромную терапию, включающую: ингаляции, рациональную антибиотикотерапию и коррекцию органных и системных расстройств.
Наблюдение больных осуществляется отоларингологом с первых суток после наложения трахеостомы до деканюляции. Профилактика развития осложнений проводится по следующим направлениям:
• своевременная профилактика гнойно–септических осложнений в области трахеостомы;
• динамическое эндоскопическое наблюдение за состоянием слизистой оболочки гортани и трахеи;
• своевременное выявление и лечение постинтубационных изменений гортани и трахеи.
С целью профилактики гнойно–воспалительных осложнений в послеоперационном периоде местно применяются антибактериальные препараты с обязательным учетом видового состава микрофлоры, высеваемой из трахеобронхиального дерева. Для лечения больных с трахеобронхитом следует назначать ферменты, разжижающие мокроту.
Лечение больных с постинтубационным отечным ларингитом включает противоотечную, гормональную терапию, ингаляции, муколитики, антибактериальные и десенсибилизирующие препараты. Физиотерапия назначается в виде магнито–лазерного воздействия или электрофореза с хлористым кальцием на область гортани (6–8 сеансов).
Комплексная терапия больных с нарушением разделительной функции гортани включает общую и местную метаболическую, сосудистую, противовоспалительную, противоотечную, антиоксидантную, стимулирующую терапию, а также физиотерапевтические процедуры (электрофорез, магнитотерапия на область гортани и трахеостомы, курсом 7–10 сеансов), фонопедические упражнения, направленные на улучшение дыхательной и разделительной функций гортани.
При образовании гематомы в области трахеостомы следует назначать мази, содержащие гепариноид, а при начавшемся рубцевании – противорубцовую терапию. Перевязки выполняются 2 раза в сутки, смена трахеостомической канюли осуществляется 1 раз в 2 суток.
Эндоскопические методы в лечении больных, перенесших трахеостомию
Лечебная эндофибробронхоскопия направлена на:
• лечение эрозивно–язвенных повреждений гортани и трахеи,
• удаление рубцово–грануляционного «козырька» над верхним краем трахеостомы,
• удаление грануляций слизистой оболочки гортани и трахеи,
• ликвидацию воспалительного процесса в гортани, трахее и легких.
При развитии эрозивно–язвенного трахеита выполняется лечебная бронхоскопия, с помощью которой в трахею вводятся различные лекарственные вещества: антисептики, щелочные растворы, ферменты, препараты, улучшающие реологические свойства бронхиального секрета. Препараты вводятся в виде ингаляций или эндотрахеальных инстилляций.
Эндоскопические оперативные методы в качестве самостоятельного способа лечения постинтубационных изменений верхних дыхательных путей используются при наличии грануляций, внутрипросветных перегородок (пристеночных, серповидных, полулунных, кольцевидных «мембран»), рубцово–грануляционного «козырька» над верхним краем трахеостомы. Методика их удаления зависит от количества и размеров грануляций. При малых размерах грануляций производят электрокоагуляцию с помощью коагулятора. Если размеры образования превышают 3 мм, то на их основание набрасывают диатермическую петлю, которую затягивают у основания и путем подачи коротких разрядов высокочастотного тока отсекают и извлекают.
Язвы, образующиеся на месте удаленных грануляций, эпителизируются на 3–5–е сутки, поэтому контрольное эндоскопическое исследование следует выполнять не ранее этого срока.
Рубцово–грануляционный «козырек» над трахеостомой служит показанием к удалению, если его размеры превышают 0,5 см в диаметре. Удаление «козырька» производится с помощью коагулятора, затем проводится отсроченная деканюляция. Перед деканюляцией больных выполняется ларинготрахеобронхоскопия с целью оценки состояния и подвижности голосовых складок, размеров голосовой щели и подскладкового пространства.
Для облегчения адаптации больного к измененным условиям дыхания следует правильно проводить поэтапную деканюляцию с постепенным уменьшением диаметра трахеостомической трубки. Наружное отверстие в трахеостомической трубке закрывается пробкой на время контрольного периода. После удаления канюли на область трахеостомы накладываются мазевые повязки. Трахеостомические дефекты, как правило, закрываются самостоятельно. После деканюляции проводится обязательное динамическое наблюдение за больным в течение 3–х месяцев, с контрольной эндотрахеофиброскопией через 10 дней, через 20 дней и через 1,5 месяца после деканюляции.
Показания к деканюляции:
• наличие у больного адекватного самостоятельного дыхания;
• нормальная эндоскопическая картина слизистой оболочки гортани и трахее, отсутствие признаков воспаления и грануляционного процесса;
• проведение контрольного периода в течение 3 дней с закрытой трахеостомической трубкой диаметром 6 мм;
Показания к отсроченной (7–10 дней) деканюляции:
• односторонний парез гортани со стенозом I–II степени;
• постинтубационный отечный ларингит со стенозом I–II степени;
• нарушение разделительной функции гортани I–II степени;
• наличие рубцово–грануляционного «козырька» над верхним краем трахеостомы диаметром 0,6 см и более;
• грануляции, рубцовые мембраны, соединительнотканные перемычки в области гортани и трахеи, которые нуждаются в эндоскопическом удалении.
Противопоказания к деканюляции:
• двусторонний парез гортани, со стенозом гортани III степени;
• эрозивно–язвенный трахеит III степени;
• рубцовая деформация трахеи, с сужением просвета гортани и трахеи более чем на 1/3;
• нарушение разделительной функции гортани;
• хондроперихондрит гортани и трахеи;
• трахеомаляция;
• наличие тяжелой сопутствующей патологии.
Предлагаемый подход к операции «трахеостомия» позволяет в значительной степени сократить риск возникновения возможных послеоперационных осложнений, восстановить дыхательную функцию, а также значительно сократить сроки лечения, в целом повысить эффективность реабилитации данной категории больных.
Показания к операции на плевре при туберкулезе. Обследование перед операцией на плевре
Для решения вопроса о показанности операции на плевре необходимо как выяснить ее возможность с точки зрения общего состояния больного, так и определить ее целесообразность и техническую выполнимость в аспекте топографо-морфологических изменений в области предстоящего оперативного вмешательства. В частности, речь идет о способности коллабированного легкого к расправлению.
С самого начала надо разделить обнаруживаемые изменения по тому признаку, связаны ли они с коллапсом легкого и, следовательно, обратимы после расправления последнего или обусловлены стойкими патологическими процессами в легочной ткани. На таком делении будет основываться суждение о расправимости легкого и необходимости резекции легочной ткани, а также ее объеме.
Обследование начинают с более простых методов, которые, позволяя получить некоторые данные, дают возможность в то же время установить необходимость и порядок более сложных исследований.
Напротив, сочетание их с бронхоэктазиями или дефектами контрастирования более крупных бронхов — сегментарных, долевых — вплоть до их «ампутации» указывает на наличие в легком пневмосклеротических изменений.
Бронхография позволяет также диагностировать мелкие бронхиальные свищи и определить ход свищевого канала. Плеврография имеет в этом отношении меньшее значение, поскольку при мелких свищах особенно прикрытых фибрином, контрастное вещество, введенное в плевральную полость, в них просто не попадает. Диагностическая ценность плеврографии вообще сомнительна, так как контраст не проникает ни в завороты плевральной полости, прикрытые или заполненные фибрином, ни в наиболее труднодоступные для хирурга места в области реберно-диафрагмальных синусов, где стенки полости обычно сращены между собой.
Для оценки склеротических изменений в легком может быть применен способ А. Алтыпармакова — определение сократительной способности стенок бронхов во время бронхографии но изменению диаметра их просвета при кашлевых толчках. При резком уменьшении просвета можно считать, что функция бронхов сохранена и, следовательно, выраженных фиброзных изменений в коллабированном легком нет, то есть такое легкое сохранило способность к расправлению. Метод оценки субъективен со всеми присущими этому отрицательными чертами.
В ряде случаев, особенно при небольшом коллапсе легкого, удается наблюдать проникновение контрастного вещества в кортикальные отделы легкого. Это, разумеется, не настоящая капиллярная фаза, которую получают при исследовании неподжатой обычной легочной ткани, и на ангиопульмонограммах в этих случаях констатируют лишь некоторое затемнение. Тем не менее, при выпадении одной только этой фазы нельзя еще утверждать, что имеется истинная облитерация капиллярной сети легкого, поскольку в этих случаях возможно спадение ее, вызванное коллапсом, или даже временный спазм сосудов. Как и при бронхографии, такая картина свидетельствует о пневмосклеротических изменениях лишь при сочетании ее с деформацией, сужением, задержкой контраста или отсутствием контрастирования более крупных ветвей.
С теми же оговорками должны трактоваться данные сканнирования легких.
Вряд ли можно получить существенную помощь для диагностики состояния легкого от применения электроплетизмографии — метода регистрации абсолютной величины электрического сопротивления легочной паренхимы и его пульсовых колебаний. Хотя величина электрического сопротивления зависит от воздушности легочной ткани и в этом аспекте может быть полезна для суждения о наличии пневмосклероза, следует, однако, учитывать наличие на коллабированном легком панциря, а в самом легком — участков с обратимой гиповентиляцией, вызванной перегибами бронхов и образованием краевых ателектазов. Эти изменения, ликвидирующиеся при расправлении легкого, могут обусловить ложное истолкование данных электроплетизмографии до операции.
Туберкулезный плеврит
Туберкулезный плеврит - это воспаление плевры туберкулезной этиологии, протекающее как в сухой форме, так и с накоплением экссудата в плевральной полости. Основные симптомы туберкулезного плеврита – колющая боль в боку, сухой кашель, одышка, субфебрильная или фебрильная температура тела, недомогание. При постановке диагноза учитывается рентгенологическая картина, результаты пробы Манту, обнаружение МБТ в мокроте или плевральном экссудате, данные плевроскопии. Лечение туберкулезных плевритов осуществляется туберкулостатическими препаратами, кортикостероидами, НПВС; при массивной экссудации показана серия плевральных пункций для аспирации выпота; в фазе рассасывания назначается ЛФК, физиопроцедуры.
МКБ-10
Общие сведения
Причины
В большинстве случаев туберкулезный плеврит развивается на фоне активного туберкулеза легких: очагового, инфильтративного, диссеминированного, туберкулеза ВГЛУ, первичного туберкулезного комплекса и пр. Изредка возникает как самостоятельная клиническая форма в отсутствие признаков туберкулезного поражения других органов. У больного туберкулезом плевритом может осложниться спонтанный или искусственный пневмоторакс (коллапсотерапия).
Микобактерии туберкулеза проникают в плевральную полость одним их трех возможных способов: контактным путем (из легочных очагов распада субплевральной локализации), лимфогенным путем (при распространении по лимфатическим путям) и гематогенным путем (по системе кровеносных сосудов при наличии бактериемии). Источником распространения МБТ в плевру служат внутригрудные лимфатические узлы или реактивировавшиеся очаги туберкулеза в легком. Необходимым условием развития туберкулезного плеврита является специфическая сенсибилизация плевральных листков.
Благоприятствуют возникновению туберкулезного процесса в плевре следующие факторы:
- переохлаждение
- гиповитаминозы и недостаточное питание
- прием ГКС и иммунодепрессантов
- сопутствующие заболевания (онкопатология, сахарный диабет)
- тесный контакт с больным туберкулезом.
Патогенез
В ответ на внедрение МБТ развивается воспалительный отек, гиперемия и утолщение плевральных листков. Вскоре на них появляются множественные милиарные бугорки, иногда – более крупные очаги с казеозным некрозом. Указанные изменения сопровождаются выраженной экссудативной реакцией – пропотеванием и накоплением жидкости в плевральной полости. Характер экссудата (фибринозный, серозный, кровянистый, гнойный) зависит от патоморфологических изменений в плевре.
Классификация
В зависимости от наличия/отсутствия и характера выпота туберкулезные плевриты бывают фибринозными (сухими) и экссудативными (выпотными). В последнем случае может встречаться серозный, геморрагический, холестериновый, гнойный экссудат.
- Фибринозный (сухой) плеврит протекает с минимальным количеством экссудата, в котором повышено содержание фибрина. Жидкая часть экссудата быстро рассасывается, а фибрин откладывается на плевральных листках. Со временем между плевральными листками образуются фиброзные тяжи, полость плевры частично или полностью облитерируется – сухой плеврит переходит в адгезивный (слипчивый) плеврит.
- Экссудативный (выпотной) плеврит. Самый частый вариант туберкулезного плеврита - экссудативный. Количество выпота обычно значительное, экссудат быстро прибывает вновь после аспирации в ходе торакоцентеза. По преобладающему клеточному составу различают следующие виды экссудата: лимфоцитарный, эозинофильный и нейтрофильный. При резком повышении проницаемости капилляров плевры и выходе большого числа эритроцитов характер экссудата становится серозно-геморрагическим или геморрагическим. Холестериновый экссудат имеет густую консистенцию, желтый цвет, в нем определяется большое количество холестерина. Серозно-гнойный и гнойный экссудат обычно образуется при обширной казеозно-некротической реакции плевры.
По локализации различают верхушечный, междолевой, костальный, наддиафрагмальный, парамедиастинальный туберкулезный плеврит. Обычно поражение одностороннее, двусторонний плеврит туберкулезной этиологии развивается редко (1,5%). В клиническим плане наиболее значимо выделение следующих видов туберкулезного плеврита: аллергического, перифокального, туберкулеза плевры и гнойного плеврита. В течении туберкулезного плеврита выделяют 3 периода:
- 1) накопления экссудата и нарастания клинических проявлений
- 2) стабилизации
- 3) рассасывания экссудата и стихания клинических признаков.
Симптомы туберкулезного плеврита
Аллергический плеврит
Аллергическая форма плеврита возникает у лиц с первичным туберкулезом, имеющих повышенную чувствительность к туберкулину и склонных к выраженной гиперергической реакции. Клиника разворачивается остро: резко повышается температура тела, фебрилитет сохраняется в течение 10-14 дней. Поскольку в это время происходит быстрое накопление серозного выпота, возникает одышка, боль в боку, тахикардия. Резорбция экссудата происходит в течение месяца, однако при большом объеме выпота этот процесс может принимать затяжное течение. Одновременно с плевритом (иногда до или после него) появляются фликтены, узловатая эритема, полиартрит.
Перифокальный плеврит
Перифокальный туберкулезный плеврит начинается подостро или исподволь. Нередко пациенты связывают появление симптомов с предшествующим переохлаждением или ОРВИ. Больных беспокоит сухой кашель, покалывание в груди, непостоянный субфебрилитет. Усиление боли в боку провоцируется глубоким дыханием, положением на больном боку, надавливанием на межреберья. Болевой синдром нередко принимается за миозит, плексит, межреберную невралгию, стенокардию, а при иррадиации в живот – за приступ острого холецистита.
Если перифокальный плеврит протекает с накоплением серозного экссудата, клиническая картина становится более выраженной: повышенная температура тела определяется постоянно, возникает тахикардия, одышка, потливость. Течение перифокального туберкулезного плеврита затяжное (4-6 недель), часто рецидивирующее.
Туберкулезный плеврит
Туберкулез плевры может протекать в форме диссеминированного, очагового процесса, казеозно-некротической реакции. Может сопровождаться накоплением серозного, серозно-гнойного или гнойного выпота. Течение туберкулеза плевры упорное и длительное. Начало заболевания подострое или малосимптомное. Преобладают симптомы интоксикации и лихорадка.
Особой разновидностью экссудативного туберкулезного плеврита служит эмпиема плевры. Клиническая картина характеризуется интоксикацией тяжелой степени: температурой тела выше 39°С, ознобами, ночными потами, выраженной слабостью. Постепенно нарастает одышка и тахикардия, появляются тянущие боли в боку, снижается масса тела. Возможно образование бронхоплеврального свища, о чем свидетельствует откашливание гнойного экссудата. Длительно существующий гнойный плеврит может осложниться флегмоной грудной стенки, образованием плевроторакального свища, амилоидозом внутренних органов.
Диагностика
Различные формы туберкулезного плеврита имеют свои характерные физикальные, аускультативные, рентгенологические и лабораторные данные. Поэтому при малейших подозрениях на туберкулезную этиологию заболевания пациент должен быть проконсультирован фтизиатром.
- На аллергический характер туберкулезного плеврита указывает выраженная эозинофилия в крови и плевральном экссудате. В ходе диагностической плевральной пункции получают серозный экссудат, однако МБТ в нем, как правило, не обнаруживаются. При проведении видеоторакоскопии может определяться гиперемия плевральных листков.
- При фибринозном плеврите пораженная сторона грудной клетки отстает при дыхании, выслушивается шум трения плевры, определяется укорочение перкуторного звука. При проведении рентгенографии легких обнаруживаются плевральные наслоения (шварты). По данным УЗИ плевральной полости экссудат не выявляется или определяется в скудном количестве.
- Иная картина типична для экссудативного туберкулезного плеврита. Физикальное обследование выявляет сглаженность (при большом объеме экссудата – выбухание) межреберий, притупление перкуторного звука над областью скопления экссудата, смещение структур средостения в здоровую сторону. В острой фазе изменения гемограммы характеризуются значительным лейкоцитозом и ускорением СОЭ, лимфо- и эозинопенией. При рентгенологическом и ультразвуковом исследовании определяется свободная жидкость в полости плевры. Детальная оценка состояния легочной ткани возможна только после эвакуации экссудата. Диагноз гнойного плеврита подтверждается при получении гнойного экссудата во время плевральной пункции.
Плеврит туберкулезной этиологии требует дифференциации с плевритами, сопровождающими пневмонию, мезотелиому плевры, рак легкого, ТЭЛА, застойную сердечную недостаточность, коллагенозы. В сомнительных случаях верификации диагноза способствует:
Лечение туберкулезного плеврита
Лечение стационарное. В период экссудации и лихорадки назначается постельный режим. Рекомендуется питание с ограничением соли и жидкости, большим количеством белка и витаминов. При любом клиническом варианте туберкулезного плеврита назначается терапия 3-4-мя противотуберкулезными препаратами (изониазид, рифампицин, этамбутол, пиразинамид, стрептомицин) не менее чем на 9 месяцев. При выраженной экссудации и гиперергии проводится курс лечения кортикостероидами (преднизолоном) – это позволяет добиться прекращения дальнейшего накопления выпота.
В случае продолжающейся экссудации проводятся повторные плевральные пункции с введением химиопрепаратов в полость плевры. Добиться скорейшего расправления легкого и облитерации плевральных листков помогает дренирование плевральной полости с наложением активной вакуумной аспирации. В период резорбции экссудата применяются НПВС, электрофорез, дыхательная гимнастика.
При наличии бронхоплеврального свища требуется его хирургическое закрытие. При туберкулезной эмпиеме плевры может выполняться интраплевральная торакопластика, плеврэктомия с декортикацией легкого.
Прогноз и профилактика
При своевременном и полноценном лечении туберкулезного плеврита прогноз благоприятный. Летальность от туберкулеза плевры (главным образом от хронической эмпиемы плевры) составляет 1-2%. У пациентов, не получавших лечение, или получавших его не в полном объеме, в ближайшие три года может развиться диссеминированный туберкулез легких. Профилактика туберкулезного плеврита такая же, как и при других клинических формах инфекции (проведение вакцинации и туберкулинодиагностики среди детей и подростков, профилактической флюорографии среди взрослого населения, исключение контактов с больными туберкулезом и т. д.).
Читайте также:
