Эпителий желез желудка. Клетки желудка. Гормоны желудка.
Добавил пользователь Skiper Обновлено: 08.01.2026
Изучены изменения слизистой оболочки желудка при 28 нейроэндокринных опухолях различного цитогенеза и степени дифференцировки. Использовались обычные и ИГХ методы для выявления эндокринноцитов и оценки пролиферативной активности Ki-67. По клинико-анатомическим признакам выявлено 4 G-клеточных, 2 ЕС-клеточных, 1 D-клеточная (мультицентричная) и 21 ЕСL-клеточная опухоль. При G-клеточных опухолях в слизистой оболочке фундального отдела имелась выраженная гиперплазия и гипертрофия париетальных и главных клеток в сочетании с длительно незаживающими рецидивирующими эрозивно-язвенными пептическими поражениями других отделов желудочно-кишечного тракта. ЕС-клеточные опухоли возникали чаще в антро-пилорическом отделе на фоне хронического атрофического гастрита с типичной кишечной метаплазией и гиперплазией кишечных ЕС клеток открытого типа. D-клеточные опухоли (соматостатиномы) желудка сопровождались тотальной атрофией главных желез фундального отдела с кишечной метаплазией и выраженной диффузной и аденоматозной гиперплазией D клеток слизистой оболочки желудка. В основе формирования полипов фундального отдела слизистой оболочки при ECL-клеточных НЭО лежат своеобразные изменения покровно-ямочного и железистого эпителия в виде «глобоидной» гиперплазии, метаплазии и дисплазии с накоплением крупных глобулей слизи в цитоплазме клеток и трансформацией их в перстневидно-клеточные элементы. В случаях низкодифференцированных нейроэндокринных и смешанных адено-нейроэндокринных карцином в опухолях на фоне таких изменений возникают очаги перстневидно-клеточного рака. Выявление «глобоидной гиперплазии» в биопсийном материале позволит заподозрить и в более ранние сроки выявлять ECL-клеточные нейроэндокринные опухоли желудка разной степени дифференцировки, а также начальные формы перстневидноклеточного рака и разработать адекватные методы профилактики и лечения.
1. Дерижанова И.С. Опухоли диффузной эндокринной системы – карциноиды. – Ростов-на-Дону: Изд-во Ростовского ун-та, 1991. – 288с.
2. Дерижанова И.С., Салмн А. Изменения слизистой оболочки желудка при раках желудка различного генеза // Арх. Пат. – 1996. – № 4. – С. 32-35.
3. Кит О.И. Нейроэндокринные, клинические и морфологические аспекты рака желудка. – Новочеркасск: Изд-во «Лик», 2014. – 187 с.
5. Delle Fave G., O'Toole D., Sundin A., Taal B., et al. ENETS Consensus Guidelines Update for Gastroduodenal Neuroendocrine Neoplasms. Neuroendocrinology. 2016; 103(2): 119–124.
6. La Rosa S, Inzani F, Vanoli A, Klersy C, Dainese L, Rindi G, Capella C. Bordi C, Solcia E. Histologic characterization and improved prognostic evaluation of 209 gastric neuroendocrine neoplasms // Human Pathology. 2011. 42(10). P. 1373-1384.
7. LI Xin-gong, DING Hong-ji, LI Ai-ying , et al. Histologic study of Globoid Dysplasia in the Adjacent Gastric Mucosa of Signet Ring Cell Carcinoma// Chinese Journal of Clinical and Experimental Pathlogy. 1994. 01.
8. Rindi G, Arnold R, Bosman FT, et al Nomenclature and classification of neuroendocrine neoplasms of the digestive system. In: Bosman FT, Carneiro F, Hruban RH, Theise ND (eds). WHO classification of tumours of the digestive system. IARC Press, Lyon: International Agency for Research on Cancer: 2010, pp. 13-15.
9. Vanella L, Zahner E, Annibale B. et al. Risk for gastric neoplasia in patients with chronic atrophic gastritis. A critical reappraisal // World J Gastroenter. 2012, 18: 1279-1285.
Нейроэндокринные опухоли желудка (НЭО) – согласно классификации ВОЗ, определяются как опухоли диффузной эндокринной системы. В прошлом они составляли 2–3 % всех гастроинтестинальных карциноидов и 0,3 % всех желудочных неоплазий. Согласно последним эпидемиологическим данным доля НЭО желудка в структуре НЭО ЖКТ составляет от 5 % (в Канадских исследованиях) до 23 % (в Австрийских) [5]. Такие различные колебания обусловлены разным подходом в диагностике НЭО в различных странах и в разнообразии клинико-анатомических особенностей, что диктует целесообразность в поиске новых диагностических признаков. В зависимости от клинико-патологических признаков, стадии процесса, НЭО имеют очень различное поведение, варьируясь от индолентных форм до жизнеугрожающих [3].
В слизистой оболочке желудка (СОЖ) идентифицировано 8 типов эндокринных клеток закрытого и открытого типов: G, продуцирующие гастрин, ECL, гистаминсохраняющие, – наиболее многочисленная группа, P/D1, содержащие грелин и обестатин; D, секретирующие соматостатин; ЕС (желудочные и кишечные), вырабатывающие серотонин, и А, содержащие глюкагон. Имеются определенные закономерности в распределении эндокринноцитов в СОЖ – антральные и прилежащие пилорические железы – зона расположения G, D, EC, A клеток; фундальные – ECL, P/D1, EC, D; в очагах кишечной метаплазии превалируют EC клетки кишечного типа.
Соответственно классификациям ВОЗ гастроэнтеропанкреатические НЭО делятся на хорошо дифференцированные (типы I, II, III ECL – клеточные и не ECL-клеточные) и плохо (низко) дифференцированные эндокринные карциномы (PDECs) [8]. Все НЭО 1 типа ведут себя как доброкачественные опухоли. НЭО 2,3 типов часто имеют признаки злокачественности и приводят больных к смерти. Отмечены переходы от высоко- до умеренно- и низкодифференцированных опухолей [6].
Наиболее частыми НЭО являются ECL-клеточные опухоли (I–III типов).
Хорошо дифференцированные желудочные опухоли (тип I ECL-клеточные НЭО) представляют большую часть эндокринных опухолей желудка, встречаются чаще у женщин (соотношение М:Ж – 1:2,5). Опухоли развиваются менее чем у 1 % больных, на фоне гипергастринемии, вызванной хроническим атрофическим гастритом, типа А или хеликобактерным. Больные, имеющие I тип ECL-клеточных НЭО, также страдают пернициозной анемией или другими аутоиммунными заболеваниями. Опухоли такого типа обычно малы, часто множественны, состоят из относительно мономорфных клеток, группирующихся в кластеры или трабекулы. Большинство опухолей располагается в СО, очень редко отмечается инвазия в более глубокие отделы желудочной стенки. Постоянно при этом наблюдается ECL-клеточная гиперплазия и дисплазия в окружающей СОЖ. Тип II ECL-клеточных опухолей составляет 6–8 % всех эндокринных опухолей желудка, соотношение мужчин и женщин 1:1. Они развиваются у больных с гипергастринемией, вызванной гастрин-продуцирующими опухолями, вызывающими развитие синдрома Золлингера – Эллисона (ЗЭС). Такие опухоли могут сопровождаться или не сопровождаться синдромами МЭН 1 типа. Желудочные опухоли обычно множественные, связаны с гиперплазией ECL клеток с дисплазией или без нее. В противоположность опухолям I типа в окружающей СО желудка нет хронического атрофического гастрита типа А. Опухоли II типа локализуются обычно в области тела и фундуса, но могут располагаться и в антральном отделе. Эти опухоли более часто злокачественны. Больные с синдромом МЭН 1 типа и СЗЭ в 20–30 % имеют риск развития НЭО II типа, в то время как при спорадических СЗЭ риск возникновения составляет 0–1 %.
Тип III ECL клеточных опухолей часто называют «спорадическими», так как считается, что ему не предшествует какая-либо патология желудка, нет связи с гипергастринемией. Они составляют 13–23 % всех гастроинтестинальных НЭО, чаще встречаются у мужчин (соотношение М:Ж – 2,8:1). Они обычно солитарны, но описаны также и множественные опухоли. К моменту диагностики имеют большие размеры и нередко – метастазы. Это наиболее злокачественный вариант из трех типов ECL клеточных опухолей. Даже мельчайшие эндокринные опухоли III типа могут метастазировать. Многие авторы рассматривают их как высокодифференцированные нейроэндокринные раки [1].
Четвертая группа – плохо дифференцированные нейроэндокринные карциномы, делятся по аналогии с опухолями легких на мелко- и крупноклеточные варианты.
Предопухолевыми процессами для ECL клеточных новообразований являются ECL клеточная гиперплазия и дисплазия. Однако гиперплазия эндокринных клеток выявляется не только при НЭО, но и при других эпителиальных опухолях желудка [4].
Диагностика НЭО СО желудка базируется, главным образом, на результатах гистологического исследования биопсированного материала. Однако, ввиду того, что эти новоообразования часто располагаются в глубоких отделах слизистой оболочки, в биоптаты попадает не опухолевая ткань, а окружающая СОЖ, что затрудняет своевременное распознавание этих неоплазм. В анамнезе таких пациентов часто имеются указания на неоднократное проведение биопсий СОЖ, тем не менее правильный диагноз нередко ставится лишь после гистологического исследования операционного материала. Изменения СОЖ при НЭО этого органа не могут считаться достаточно полно изученными, в то же время они отражают влияние продуцируемых опухолевыми клетками биологически активных веществ на экзокринные элементы СО. Наиболее подробно изучены изменения СОЖ при гастриномах и серотониномах, но они не описаны при ECL клеточных опухолях. Однако литературные данные свидетельствуют, что при динамическом наблюдении за развитием НЭО I типа, на фоне хронического атрофического гастрита в условиях гиперпластических и диспластических изменений ECL клеток, в СО тела желудка часто выявляются гиперпластические полипы [10]. Какие-либо особенности строения их по сравнению с другими отделами желудка не отмечены. Остается неясным вопрос – случайным или закономерным является их развитие при ECL-клеточных неоплазмах. В то же время правильная оценка изменений СОЖ, обусловленных дисгормональными нарушениями при НЭО, позволит заподозрить и диагностировать эти новообразования в более ранние сроки.
Определенные трудности вызывает также определение цитогенеза НЭО. Большинство из них сочетают в себе несколько типов клеток и продуцируют не только гормоны, но и про-гормоны и другие вещества, что не всегда позволяет выявить их при иммуногистохимическом исследовании. Но анализируя изменения окружающей СОЖ и проводя тщательный клинико-анатомический анализ, возможно определить цитогенез НЭО.
Цель исследования. Изучить изменения СО при НЭО желудка различного цитогенеза и степени дифференцировки.
Материалы и методы. Исследованы биоптаты слизистой желудка и операционный материал (эндоскопически иссеченные опухоли и резецированные отделы желудка) 28 больных с НЭО желудка. Кусочки опухолей и СОЖ из различных отделов по обычной методике заливались в парафин. Гистологические срезы окрашивались гематоксилином-эозином, алциановым синим в сочетании с PAS-реакцией. Для выявления нейроэндокринных элементов и пролиферативного индекса использовались ИГХ методики с антителами к хромогранину А (Thermo scientific, разведение 1:400), синаптофизину (клон SP11, Thermo scientific, разведение 1:100), NSE (клон V1-H14, DBS, разведение 1:75), Ki-67 (клон SP6, Thermo scientific, разведение 1:200).
Результаты. Изученные опухоли распределялись следующим образом: производные G клеток – 4, ЕС – 2, D – 1, ЕСL клеток – 21; из них НЭО I типа – 6; 5 опухолей расценены как доброкачественные аденонейроэндокринные опухоли, 4 – НЭО III типа (высокодифференцированные нейроэндокринные карциномы), 2 – низкодифференцированные нейроэндокринные карциномы, 4 – смешанные аденонейроэндокринные карциномы. Следует отметить трудности разграничения отдельных форм НЭО желудка в практике, так как не все критерии их характеристики отражены в классификации НЭО желудка и поджелудочной железы ВОЗ 2010 г. Некоторые классификационные формы, например «доброкачественная - адено-нейроэндокринная опухоль» (синоним «муко-, или аденокарциноид»), представлены лишь в предшествующих классификациях. Имеется тавтология – например, при прогрессии заболевания – «нейроэндокринная опухоль превращается в карциному (тоже опухоль)».
Клинически НЭО при эндоскопическом исследовании чаще всего расценивались как «полипоз» (15 наблюдений) или «опухоли» (6). Правильный диагноз после первой биопсии был поставлен лишь в 25 % наблюдений, после повторных биопсий – еще в 28,5 %, в остальных случаях – лишь после исследования операционного материала. 26 раз в разные сроки до окончательного установления диагноза больным удаляли и гистологически выявляли гиперплазиогенные железистые полипы. У 13 больных нейроэндокринные опухоли были множественными, сочетаясь с выраженной гиперплазией эндокринноцитов в сохранившихся железах, нередко с формированием микроопухолей в разных участках слизистой оболочки.
G-клеточные опухоли располагались в антро-пилорическом отделе, сопровождались развитием пептических эрозий и язв СО желудка, осложняющихся кровотечениями, не поддающимися лечению обычными методами. В фундальном отделе у всех больных имелась выраженная гиперплазия и гипертрофия обкладочных клеток, что, наряду с клинической картиной (повышение уровня гастрина в крови, рецидивирующие язвы СО с кровотечениями и перфорацией) являлось подтверждением секреции опухолевыми клетками гастрина.
ЕС-клеточные опухоли возникали на фоне атрофического гастрита с типичной классической кишечной метаплазией СО. В цитоплазме опухолевых клеток имелась грубая зернистость, интенсивно окрашивающаяся с антителами к хромогранину и дающая слабо выраженную или даже отрицательную реакцию с антителами к синаптофизину. В очагах кишечной метаплазии выявлялись типичные кишечные энтерохромаффинные клетки открытого типа с длинными цитоплазматическими отростками, распространящимися в просвет желез.
В одном наблюдении D-клеточных опухолей, развившихся на фоне МЭН I типа, протекающих с явлениями синдрома «соматостатиномы» (ожирение, диабет, желчнокаменная болезнь), имелась выраженная атрофия СО фундального отдела с полным отсутствием специализированных желез и кишечной метаплазией, диффузной и очаговой гиперплазией эндокринноцитов с новообразованием огромного количества нейроэндокринных опухолей разных размеров – от микроскопических до 3–5–8 мм диаметром, занимающих всю поверхность СО фундального отдела. При электронной микроскопии в цитоплазме опухолевых клеток обнаружены типичные соматостатиновые гранулы.
Все ЕСL-клеточные опухоли располагались в зоне фундальных желез (тело, дно желудка), состояли из относительно мономорфных клеток, формирующих тяжи, трабекулы, железисто-подобные структуры. При всех ЕСL- клеточных опухолях постоянно отмечалась своеобразная гиперплазия покровно-ямочного и железистого эпителия СО. Эпителиальные клетки были резко увеличены в размерах за счет накопления в цитоплазме крупных скоплений слизи («глобулей»), размеры которых варьировали. Эти изменения соответствовали понятиям «глобоидная гиперплазия», «глобоидная метаплазия», «глобоидная дисплазия», отличающимся между собой числом и размерами «глобулей». В случаях «глобоидной гиперплазии» в цитоплазме обнаруживались многочисленные вакуоли слизи, не обнаруживаемые в цитоплазме обычных цилиндрических клеток покровно-ямочного и железистого эпителия; при «глобоидной метаплазии» в цитоплазме формировались две-три крупные вакуоли, деформирующие клетку. При глобоидной «дисплазии» цитоплазма содержала одну крупную вакуоль, которая оттесняла ядро к периферии, сдавливая его, что придавало сходство клетке с перстнем, так в эпителиальном пласте возникали перстневидные клетки.
Такие клетки то полностью замещали фовеолярный эпителий, то формировали гиперплазиогенные полипы над опухолями. Слизь в этих клеточных элементах имела различный характер – то была резко PAS положительной, то смешанной желудочно-кишечной. На этом фоне появлялись очень крупные бокаловидные клетки, то с кишечной алцианофильной, то со смешанного характера слизью. В 3 случаях низкодифференцированных нейроэндокринных и смешанных адено-нейроэндокринных карцином в опухолях на фоне таких изменений возникали очаги перстневидно-клеточного рака.
Аналогичные изменения возникали не только над опухолевыми элементами, но и в пограничных отделах СОЖ при хроническом гастрите с частичной атрофией фундальных желез и замещении обкладочных и главных клеток псевдопилорическими железами, постоянно сочетаясь с гиперплазией ЕСL клеток в базальных отделах. Гиперплазированный фовеолярный эпителий распространялся экзофитно вверх, формируя папиллярные структуры, и эндофитно вниз, принимая штопорообразный вид, параллельно в шейках желез отмечалась резко выраженная пролиферация низкодифференцированных клеток, отчетливо выявляемая при помощи маркера Ki-67.
Эпителий желез желудка. Клетки желудка. Гормоны желудка.
Эпителий желез желудка. Клетки желудка. Гормоны желудка.
Эпителий желез желудка представляет собой высокоспециализированную ткань, состоящую из нескольких клеточных дифферонов, камбием для которых служат малодифференцированные эпителиоциты в области шеек желез. Эти клетки интенсивно метятся при введении Н-тимидина, часто делятся митозом, составляя камбий как для поверхностного эпителия слизистой оболочки желудка, так и для эпителия желудочных желез. Соответственно этому дифференцировка и смещение вновь возникающих клеток идут в двух направлениях: в сторону поверхностного эпителия и в глубину желез. Обновление клеток в эпителии желудка происходит за 1-3 суток.
Значительно медленнее обновляются высокоспециализированные клетки эпителия желудочных желез.
Главные экзокриноциты вырабатывают профермент пепсиноген, который в кислой среде превращается в активную форму пепсин — главный компонент желудочного сока. Экзокриноциты имеют призматическую форму, хорошо развитую гранулярную эндоплазматическую сеть, базофильную цитоплазму с секреторными гранулами зимогена.
Париетальные экзокриноциты — крупные, округлой или неправильно угловатой формы клетки, расположенные в составе стенки железы кнаружи от главных экзокриноцитов и мукоцитов. Цитоплазма клеток резко оксифильна. В ней содержатся многочисленные митохондрии. Ядро лежит в центральной части клетки. В цитоплазме есть система внутриклеточных секреторных канальцев, переходящих в межклеточные канальцы. В просвет внутриклеточных канальцев выступают многочисленные микроворсинки. По секреторным канальцам из клетки на апикальную ее поверхность выводятся ионы Н и Сl, образующие соляную кислоту.
Париетальные клетки секретируют также внутренний фактор Кастла, необходимый для всасывания витамина Bi2 в тонкой кишке.
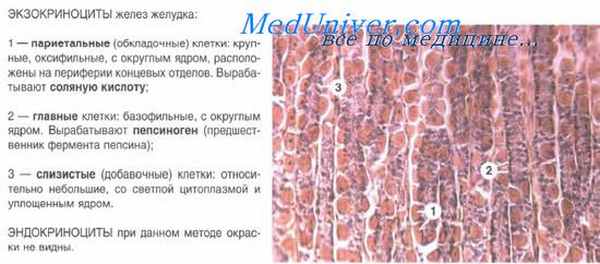
Мукоциты — слизистые клетки призматической формы со светлой цитоплазмой и уплотненным ядром, смещенным в базальную часть. При электронной микроскопии в апикальной части слизистых клеток выявляется большое количество секреторных гранул. Располагаются мукоциты в главной части желез, преимущественно в теле собственных желез. Функция клеток — выработка слизи.
Эндокриноциты желудка представлены несколькими клеточными дифферонами, для названия которых приняты буквенные сокращенные обозначения (ЕС, ECL, G, P, D, А и др.). Для всех этих клеток характерна более светлая цитоплазма, чем у других эпителиальных клеток. Отличительным признаком эндокринных клеток является наличие в цитоплазме секреторных гранул. Поскольку гранулы способны восстанавливать нитрат серебра, эти клетки называют аргирофильными. Они интенсивно окрашиваются также бихроматом калия, с чем связано другое название эндокриноцитов — энтерохромаффинные.
На основании строения секреторных гранул, а также с учетом их биохимических и функциональных свойств эндокриноциты классифицируются на несколько видов.
ЕС-клетки самые многочисленные, располагаются в теле и дне железы, между главными экзокриноцитами и секретируют серотонин и мелатонин. Серотонин стимулирует секреторную деятельность главных экзокриноцитов и мукоцитов. Мелатонин участвует в регуляции биологических ритмов функциональной активности секреторных клеток в зависимости от световых циклов.
ECL-клетки вырабатывают гистамин, который действует на париетальные экзокриноциты, регулируя продукцию соляной кислоты.
G-клетки называют гастринпродуцирующими. В большом количестве они встречаются в пилорических железах желудка. Гастрин стимулирует деятельность главных и париетальных экзокриноцитов, что сопровождается усиленной выработкой пепсиногена и соляной кислоты. У людей с повышенной кислотностью желудочного сока отмечается увеличение количества G-клеток и их гиперфункция. Имеются данные о том, что G-клетки вырабатывают энкефалин — морфиноподобное вещество, впервые обнаруженное в мозгу и участвующее в регуляции чувства боли.
Р-клетки секретируют бомбезин, который усиливает сокращения гладкой мышечной ткани желчного пузыря, стимулирует выделение соляной кислоты париетальными экзокриноцитами.
D-клетки вырабатывают соматостатин — ингибитор гормона роста. Он угнетает синтез белков.
ВИП-клетки продуцируют вазоинтестинальный пептид, расширяющий кровеносные сосуды и снижающий артериальное давление. Этот пептид стимулирует также выделение гормонов клетками островков поджелудочной железы.
А-клетки синтезируют энтероглюкагон, расщепляющий гликоген до глюкозы подобно глюкагону А-клеток островков поджелудочной железы.
В большинстве эндокриноцитов секреторные гранулы находятся в базальной части. Содержимое гранул выделяется в собственную пластинку слизистой оболочки и далее попадает в кровеносные капилляры.
Мышечная пластинка слизистой оболочки образована тремя слоями гладких миоцитов.
Подслизистая основа стенки желудка представлена рыхлой волокнистой соединительной тканью с сосудистыми и нервными сплетениями.
Мышечная оболочка желудка состоит из трех слоев гладкой мышечной ткани: наружного продольного, среднего циркулярного и внутреннего с косым направлением мышечных пучков. Средний слой в области привратника утолщен и образует пилорический сфинктер. Серозная оболочка желудка образована поверхностно лежащим мезотелием, а ее основу составляет рыхлая волокнистая соединительная ткань.
В стенке желудка расположены подслизистое, межмышечное и подсерозное нервные сплетения. В ганглиях межмышечного сплетения преобладают вегетативные нейроны 1-го типа, в пилорической области желудка больше нейронов П-го типа. К сплетениям идут проводники от блуждающего нерва и из пограничного симпатического ствола. Возбуждение блуждающего нерва стимулирует секрецию желудочного сока, тогда как возбуждение симпатических нервов, наоборот, угнетает желудочную секрецию.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эпителий желез желудка. Клетки желудка. Гормоны желудка.
Гастрин – гормон, участвующий в регуляции пищеварения. Он вырабатывается G-клетками диффузной эндокринной системы желудочно-кишечного тракта, которые располагаются в слизистой желудка, двенадцатиперстной кишке, а также в поджелудочной железе.
Синонимы русские
Пилорин, пилорогастрин, секретин желудочный.
Синонимы английские
Метод исследования
Твердофазный хемилюминесцентный иммуноферментный анализ.
Единицы измерения
Пг/мл (пикограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Исключить из рациона кофеинсодержащие напитки в течение 8 часов до исследования.
- Исключить прием антихолинергических препаратов в течение 24 часов до исследования (по согласованию с врачом).
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Гастрин (от греч. gaster – "желудок") – гормон, участвующий в регуляции пищеварения. Он вырабатывается G-клетками, относящимися к диффузной эндокринной системе желудочно-кишечного тракта, которые располагаются в слизистой желудка, двенадцатиперстной кишки, а также в поджелудочной железе. В организме человека гастрин представлен тремя формами. Условия для выработки гастрина – понижение кислотности желудка, потребление белковой пищи, растяжение стенок желудка. G-клетки также отвечают за активность блуждающего нерва. Действие гастрина направлено на париетальные клетки слизистой оболочки желудка, вырабатывающие соляную кислоту. Кроме того, он влияет на выработку желчи, секрета поджелудочной железы и на моторику желудочно-кишечного тракта, рост эпителия и эндокринных клеток. Нормальным является усиление выработки соляной кислоты при приеме пищи и снижение ее уровня по окончании переваривания. Повышение уровня соляной кислоты по механизму обратной связи уменьшает выработку гастрина.
Синдром Золлингера-Эллисона развивается при усиленной выработке гастрина. Причиной этого является гастринома – опухоль, чаще злокачественная, продуцирующая гастрин, при этом секреция не угнетается повышением кислотности желудка. Опухоль может быть расположена в пределах желудочно-кишечного тракта (в поджелудочной железе, двенадцатиперстной кишке, желудке) или вне его (в сальнике, яичниках). Клиническая картина синдрома Золлингера – Эллисона включает в себя устойчивые к обычной терапии язвы желудочно-кишечного тракта, нарушение функционирования кишечника (диарею). Гастринома часто встречается при синдроме Вермера (МЭН-1) – наследственном заболевании, при котором опухолевая трансформация затрагивает паращитовидные железы, гипофиз и поджелудочную железу.
К тому же секреция гастрина значительно увеличивается при пернициозной анемии – болезни Аддисона – Бирмера, – когда нарушается синтез внутреннего фактора Кастла, ответственного за всасывание витамина В12, и разрушаются париетальные клетки стенки желудка. Помимо фактора Кастла, эти клетки секретируют соляную кислоту. Клиническая картина заболевания определяется атрофическим гастритом и дефицитом витамина В12 (анемия, нарушение регенерации эпителия, кишечные нарушения, неврологические симптомы).
Другие заболевания желудочно-кишечного тракта также увеличивают выработку гастрина, но в меньшей степени, чем вышеописанные состояния.
Для чего используется исследование?
- Для диагностики синдрома Золлингера – Эллисона (гастриномы).
- Для контроля за течением синдрома Золлингера – Эллисона и за эффективностью его лечения.
- Для диагностики синдрома Аддисона – Бирмера (пернициозной анемии).
- Для контроля за течением синдрома Аддисона – Бирмера и за эффективностью его лечения.
- Чтобы установить причину нехватки витамина В12.
- Чтобы оценить состояние пищеварительной системы.
- Для дифференциальной диагностики гиперпаратиреодизма и синдрома Золлингера – Эллисона.
Когда назначается исследование?
- При симптомах синдрома Золлингера – Эллисона (при язвенной болезни желудочно-кишечного тракта, устойчивой к обычной терапии, стойкой стеаторее или диарее).
- При диагностированном синдроме Золлингера – Эллисона.
- При состояниях, увеличивающих риск возникновения синдрома Золлингера – Эллисона (при синдроме Вермера).
- При симптомах синдрома Аддисона – Бирмера.
- При диагностированном синдроме Аддисона – Бирмера.
- При симптомах нехватки витамина В12 (анемии, нарушении регенерации эпителия, кишечных, неврологических нарушениях).
Что означают результаты?
Референсные значения: 13 - 115 пг/мл.
Причины повышения уровня гастрина:
- заболевания желудочно-кишечного тракта (пилоростеноз, язвенная болезнь желудка и двенадцатиперстной кишки, хроническая печеночная недостаточность, хронический атрофический гастрит),
- ваготомия,
- синдром Золлингера – Эллисона (гастринома),
- синдром Аддисона – Бирмера (пернициозная анемия),
- длительный прием антацидов и препаратов, снижающих выработку соляной кислоты (ингибиторов протонной помпы),
- хроническая почечная недостаточность.
Низкий уровень гастрина имеет диагностическое значение при предшествующем высоком уровне, например после удаления гастриномы.
Что может влиять на результат?
Прием пищи и некоторых препаратов (антацидов, например "Альмагеля", "Маалокса", "Ренни", ингибиторов протонной помпы, например омепразола, омеза, париета).
Важные замечания
Необходимо помнить, что препараты, снижающие выработку соляной кислоты и нейтрализующие ее действие, повышают выработку гастрина и при их отмене возможно резкое повышение кислотности желудочного сока.
Лечение гастрита
Гастрит – это воспалительное заболевание слизистой оболочки желудка , которое приводит к развитию дистрофических изменений, замещению функционального железистого эпителия соединительной тканью и утрате основных функций органа. Патология распространена у взрослых и детей во всех странах мира – несбалансированное питание, агрессивные факторы внешней среды, нервно-эмоциональное напряжение, а также наличие специфических микроорганизмов определяют высокий уровень заболеваемости.
Виды гастрита
Существует два основных варианта воспалительного процесса в зависимости от его активности:
- Острый (коррозивный). Чаще всего развивается как реакция на серьезное воздействие – химический ожог, прием токсических веществ, алкоголя и некоторых лекарственных средств , употребление некачественной пищи или напитков. Также острый гастрит может быть вторичным проявлением системных воспалительных заболеваний, нарушений метаболизма, инфекционных процессов. Различают несколько подвидов острого воспаления слизистой желудка в зависимости от причины и степени выраженности инфильтрации.
- Хронический. Длительное влияние различных негативных факторов приводит к формированию постоянного повреждающего воздействия на ткань желудка. Железистый эпителий постепенно перестает вырабатывать желудочный сок, а процессы восстановления нарушаются. Хронический гастрит может периодически обостряться и переходить в активную фазу. Если вовремя не назначить лечение, это может стать причиной развития более серьезных заболеваний – язвенных дефектов или раковых структур.
Хронический гастрит бывает трех типов:
- Аутоиммунный (А). Нарушение работы иммунной системы приводит к атаке на собственные клетки организма. Антитела, которые вырабатываются в специфических структурах желудка, вызывают атрофию слизистой при хроническом гастрите этого типа.
- Бактериальный (В). Наиболее частая причина развития хронического гастрита – спиралевидный микроорганизм Helicobacter pylori, который при неблагоприятных условиях активизируется и приводит к изменению нормальной работы желудочных тканей.
- Рефлюкс (С). Хронический гастрит может развиваться также вследствие обратного заброса желчных кислот в полость желудка.
По локализации процесса заболевание делится на:
- антральный гастрит – в пилорическом отделе;
- гастрит тела желудка;
- пангастрит – диффузные изменения.
Также выделяют отдельные формы патологии:
- Поверхностный. Наиболее легкий вариант течения гастрита – болезнь не затрагивает железы желудка, вырабатывающие кислоты.
- Эрозивный. Характеризуется развитием дефектов слизистой и подслизистого слоя – появлением эрозий. Чаще других связан с деятельностью хеликобактера и в варианте хронического гастрита становится причиной язвенной болезни .
- Гиперацидный. Отличается повышенной продукцией соляной кислоты и развитием агрессивной среды в желудке, которая вызывает вторичные повреждения.
- Атрофический. Замещение железистого эпителия фибротическими структурами приводит к недостаточной активности желудочного сока и нарушениям функции пищеварения.
- Флегмонозный. Связан с гнойным расплавлением тканей желудка.
Существуют специфические и редкие формы острого или хронического гастрита – радиационный, грибковый, паразитарный, аллергический (эозинофильный), полипозный, НПВС-ассоциированный. Также есть вторичные – при язве или раке желудка.
![стадии гастрита]()
Признаки и лечение гастрита
Острый гастрит характеризуется большой площадью поражения, резким воспалением и быстрым нарастанием симптомов.
Типичная клиническая картина включает в себя такие жалобы:
- резкие боли в животе;
- изжога;
- тошнота;
- обильная рвота;
- появление кровянистых примесей;
- головокружение;
- выраженная острая слабость;
- повышение температуры тела;
- метеоризм;
- нарушения стула – диарея.
Хронический гастрит , в отличие от острого гастрита , может длительно протекать абсолютно бессимптомно. Большинство людей долго считают себя здоровыми, однако периодически могут появляться неспецифические симптомы:
- неприятный запах изо рта;
- отрыжка;
- тяжесть после еды;
- болезненность при длительном голодании;
- тупые боли в области верхней трети живота;
- ощущение жжения в области желудка;
- тошнота;
- отсутствие аппетита;
- диарея;
- метеоризм.
Хронический гастрит проявляется неприятными ощущениями, которые обычно усиливаются после нарушения диеты – употребления жареной пищи, копченостей, острых блюд. Также могут проявляться симптомы анемии или витаминной недостаточности вследствие нарушений всасывания питательных веществ – бледность, ломкость волос и ногтей, утомляемость, нарушения гормонального фона.
Диагноз устанавливается на приеме у гастроэнтеролога, для его подтверждения и определения типа гастрита врачу необходимо получить результаты дополнительных исследований. фиброгастродуоденоскопия (ФГДС) является «золотым стандартом» – только визуализация морфологической структуры и биопсия слизистой являются доказательством наличия острого или хронического гастрита . Также необходимо проведение теста на активность Helicobacter pylori, анализа кала на скрытую кровь. Другие методы диагностики позволяют установить тяжесть течения заболевания и его влияние на все системы организма.
Лечение необходимо начинать сразу – острый гастрит может стать причиной развития желудочно-кишечного кровотечения или других опасных для жизни состояний, а хронический гастрит часто осложняется язвами желудка или двенадцатиперстной кишки.
Лечение хронического гастрита
Тактика терапии этой формы заболевания зависит от этиологического фактора. Если установлено наличие инфекции Helicobacter pylori, назначается антихеликобактерное лечение. Схема включает в себя антибиотики, ингибиторы протонной помпы (ИПП), препараты с содержанием висмута.
Симптоматическое лечение гастрита включает в себя такие назначения:
- Диета. Важно исключить все механические, термические и химические повреждения слизистой. Блюда должны быть приготовлены на пару, сварены или запечены в духовке.
- Заместительная терапия. Хронический гастрит с недостаточной функцией желез, вырабатывающих кислоты, требует назначения натурального желудочного сока, соляной кислоты, ферментных препаратов.
- Антациды. Варианты патологии с гиперфункцией желудка подразумевают создание дополнительной защиты его слизистой при остром или хроническом гастрите . Применяются препараты, которые нейтрализуют соляную кислоту, – карбонат кальция и магния, другие.
- Обволакивающие вещества. Медицинские препараты, отвар семян льна и народные средства создают защитную оболочку , которая препятствует повреждению слизистой при выявлении хронического гастрита .
- Антисекреторные препараты. Уменьшают выработку собственной соляной кислоты. Класс включает в себя ИПП и блокаторы H2-гистаминовых рецепторов. Лекарства подобных групп назначаются длительным курсом.
- Железо и витамин В12. Если в клиническом анализе крови выявлены признаки анемии, необходимо компенсировать осложнение, которое вызвал хронический гастрит .
- Антигистаминные средства. Назначение блокаторов специфических Н1-гистаминовых рецепторов оправдано, если гастрит связан с аллергическими реакциями.
Лечение острого гастрита
Терапия острого простого гастрита часто требует неотложных мероприятий. Основная задача начальных этапов лечения – устранение повреждающего фактора и нормализация кислотно-основного состояний желудочной среды.
Может понадобиться промывание желудка или голодание в течение суток, потом назначается строгая диета. Важно исключить все агрессивные факторы, такие как курение, употребление спиртных напитков, а также прекратить прием лекарственных средств, если это не опасно для здоровья.
Медикаментозная терапия острого гастрита обычно ограничивается приемом симптоматических средств:
- водно-солевые растворы для восстановления баланса жидкости;
- спазмолитики и обезболивающие – при выраженном болевом синдроме;
- противорвотные – в случаях регулярных рвотных позывов.
Если вовремя отреагировать на проблему и соблюдать все назначения гастроэнтеролога, прогноз для выздоровления благоприятный. Однако запущенные случаи острой формы переходят в хронический гастрит и могут беспокоить пациентов длительное время в течение жизни.
Лечение эрозивного гастрита
Эрозии образуются как следствие повышенного кислотообразования, а также агрессивности желудочной среды. Поэтому лечение эрозивного острого или хронического гастрита в первую очередь должно состоять из мероприятий, которые способны нормализовать кислотный баланс в желудке и остановить образование дефектов слизистой. Обязательно соблюдение строгой диеты – исключаются все продукты питания, которые могут дополнительно раздражать слизистую. Также назначаются медицинские препараты:
- ингибиторы протонной помпы;
- блокаторы Н2-гистаминовых рецепторов;
- антацидные средства;
- ферментные препараты;
- прокинетики.
Если достоверно доказана связь эрозивного гастрита с хеликобактерной инфекцией, назначаются антибиотики, способные уничтожить болезнетворные микроорганизмы.
![лечение эрозивного гастрита]()
Состояние обострения хронического гастрита с образованием эрозий часто связано с проявлениями желудочного кровотечения, которое необходимо остановить. Могут быть назначены инъекции разнообразных кровоостанавливающих средств.
Реабилитация после купирования острого периода заболевания включает в себя терапию минеральными водами – для этого существуют специальные санаторно-курортные учреждения.
Лечение атрофического гастрита
Считается, что железистые клетки, которые трансформировались в соединительнотканные структуры, навсегда теряют свои функции и не подлежат восстановлению. Аутоиммунные процессы в организме тяжело поддаются воздействию – иммунотерапия и назначение гормональных средств не дают ожидаемых результатов. Поэтому основное направление лечения атрофического хронического гастрита – это поддержание нормальных функций желудка в пищеварительных процессах, заместительная ферментная терапия и коррекция возникающих осложнений основного заболевания.
Если выявлено значительное содержание Helicobacter pylori, также проводится эрадикация микроорганизма по общепринятым в гастроэнтерологии схемам.
Основные группы препаратов, которыми компенсируется атрофический хронический гастрит:
- вспомогательные средства для пищеварения – ферменты желудочного сока и поджелудочной железы;
- защита для слизистой – препараты с содержанием висмута или алюминия;
- лекарства, которые улучшают моторику желудочно-кишечного тракта;
- противоанемические – вещества с железом или витамином В12 в составе.
Хронический гастрит требует формирования новых привычек и образа жизни, однако при правильном подходе нарушение функции желудка полностью компенсируется.
Помните, что откладывать визит к врачу и надеяться на то, что болезненные симптомы пройдут сами по себе, нельзя. При первых же признаках нарушения работы ЖКТ записывайтесь на прием к врачу в нашем медицинском центре. Чем раньше начато лечение, тем более положительными будут результаты.
![]()
Врач гастроэнтеролог, врач УЗИ, зам. главного врача по клинико-экспертной работе.
график работы специалиста:
понедельник 10.00-14.00 среда 9.30-14.30 четверг 9.30-14.30 пятница 13.00-16.00 суббота 9.00-15.00 ![]()
Врач гастроэнтеролог детский высшей категории
график работы специалиста:
понедельник 13.00-15.00 Стоимость услуг гастроэнтерологии и эндоскопии
Код услуги Услуга Цена, рублей 11.1 Прием врача гастроэнтеролога первичный 1800 11.2 Прием врача гастроэнтеролога первичный с выдачей листка нетрудоспособности 2000 11.3 Прием врача гастроэнтеролога повторный 1600 11.3.1 Консультация врача эндоскописта 1200 11.4 Тест на диагностику инфекции «Helicobacter pylori» 1100 11.5 Экспресс-Тест на диагностику инфекции «Helicobacter pylori» 1000 11.6 Тест на диагностику инфекции «Helicobacter pylori» системой ХЕЛИК-СКАН М 1300 11.7 Взятие биоматериала и экспресс-тест диагностики инфекции «Helicobacterpylori» во время ФиброГастроскопии 1400 11.8 Забор материала для гистологического иследования при эзофагогастроскопии, колоноскопии, бронхоскопии (без стоимости гистологического исследования) 800 11.9 Эзофагогастродуоденоскопия (ЭГДС) диагностическая 3500 11.12 Колоноскопия (видеоколоноскопия) диагностическая 6900 11.16 Колоноскопия диагностическая с терминальной илеоскопией (осмотр дистальной части тонкой кишки) 7900 11.19 Ректоскопия (осмотр прямой кишки) диагностическая 2500 11.20 Ректосигмоскопия диагностическая (осмотр сигмовидной кишки) 3000 11.23 Эндоклипирование (без стоимости расходного материала) до 3-х клипс 4000 11.23.1 Эндоклипирование (без стоимости расходного материала) за каждую последующую клипсу 1500 11.24 Эндоскопическое лигирование (без стоимости расходного материала) 4000 11.25 Стоимость клипсы (за ед.) 2500 11.26 Стоимость лигатуры (за ед.) 4700 11.27 Бронхоскопия диагностическая 4000 11.30 Запись исследования на флеш-накопитель (в стоимость входит флешка) 350 11.31 Эндоскопическое удаление доброкачественных новообразований первой категории (без стоимости седации и гистологического исследования) 3700 11.32 Эндоскопическое удаление доброкачественных новообразований второй категории (без стоимости седации и гистологического исследования) 5900 11.33 Эндоскопическое удаление доброкачественных новообразований третьей категории (без стоимости седации и гистологического исследования) 9300 11.34 Эндоскопическое удаление доброкачественных новообразований нескольких отделов кишки (без стоимости седации и гистологического исследования) 16000 11.35 Установка внутрижелудочного баллона (без стоимости седации) 47000 11.36 Снятие внутрижелудочного баллона (без стоимости седации) 26500 ![распечатай купон и получи скидку 10%]()
Наша клиника приобрела экспертный УЗИ аппарат с мощными возможностями, качественной визуализацией и исключительной надежностью. Canon Aplio i800– одна из лучших ультразвуковых диагностических систем в мире.
Стойка - главное аппаратное ядро любого кабинета врача-эндоскописта. Аппаратура Pentax представляет из себя синтез высокопроизводительных видеосистем и эндоскопов для обеспечения превосходных диагностических и терапевтических возможностей и удобства специалиста.
Гастропанель
Комплекс тестов (разработка финской компании BIOHIT), позволяющих выявить наличие Helicobacter pylori—ассоциированного гастрита, определить локализацию патологического процесса в желудке (антральный отдел, тело желудка) и оценить характер изменений (является ли гастрит атрофическим). Программная обработка данных (GastroSoft, BIOHIT) позволяет предоставить наиболее вероятную интерпретацию результатов, предполагаемый диагноз, расчёт рисков и рекомендации.
Антитела к Helicobacter pylori, IgG. Исследование антител к Helicobacter pylori проводится для диагностики Helicobacter pylori—ассоциированного гастрита. H.pylori – это бактерии, колонизирующие желудок человека; их находят в слизистом слое, покрывающем эпителий желудка. Инфекция Helicobacter pylori – наиболее распространенная причина развития хронического гастрита (другим механизмом развития гастритов, в том числе тяжелых атрофических гастритов, является аутоиммунный механизм). Частота встречаемости этой инфекции очень высока, в определенной степени зависит от бытовых условий и общего уровня жизни и достигает в развивающихся странах среди взрослого населения 100%, в развитых странах 20-60%. Обычно инфицирование происходит в детстве и может продолжаться пожизненно. H.pylori, по всей вероятности, не проникают в ткани, но вызывают постоянное локальное воспаление слизистой оболочки (хронический поверхностный или неатрофический гастрит), увеличивая риск развития язв желудка или 12-перстной кишки. Такой хронический воспалительный процесс у некоторых пациентов может впоследствии привести к атрофии и нарушению функций слизистой оболочки - атрофическому гастриту со снижением кислотности желудка. Хотя инфекция H.pylori поддается лечению и может быть устранена, измененная до стадии атрофии слизистая оболочка редко восстанавливается до нормального состояния. Атрофический гастрит связан с риском развития язв и рака желудка и нарушением всасывания витамина В12, железа, магния, кальция, цинка и др., что может приводить к анемии, неврологическим нарушениям, остеопорозу, депрессии. Уровень антител к H.pylori > 30 ед/мл говорит о текущей или недавно перенесенной инфекции и связан с риском наличия гастрита тела желудка. После завершения эрадикационной терапии Helicobacter pylori, при ее успешности, уровень антител возвращается к норме в течение нескольких месяцев.
Пепсиногены – предшественники основного пищеварительного фермента желудка (пепсина). Они образуются в клетках слизистой оболочки желудка и выделяются в просвет желудка, где превращаются в активный фермент пепсин, участвующий в переваривании белков пищи. Выделяют 2 вида пепсиногенов - пепсиноген I и пепсиноген II. Пепсиноген I продуцируется преимущественно железами слизистой оболочки фундальной части желудка, пепсиноген II – железами слизистой фундальной, кардиальной, антральной частей желудка, а также и дуоденальной слизистой. Пепсиногены превращаются в пепсин под действием соляной кислоты желудочного сока, при этом для пепсиногена I оптимальна высокая кислотность (рН=1,5-2,0), а для пепсиногена II более низкая (рН=4,5). В небольших концентрациях пепсиногены попадают в кровь. Исследование уровня пепсиногенов в сыворотке крови и расчет их соотношения используют для оценки состояния слизистой оболочки желудка.
Пепсиноген I. Уровень пепсиногена I в крови отражает состояние слизистой тела желудка. Хроническая инфекция Helicobacter pylori или аутоиммунное заболевание могут вызывать разной степени тяжести атрофию слизистой тела желудка (атрофический гастрит тела желудка). Развитие атрофии слизистой тела желудка приводит к снижению количества клеток фундального отдела, продуцирующих пепсиноген I , и понижению концентрации пепсиногена I в крови ниже 30 мг/л. При наличии воспаления тела желудка без атрофических изменений (гастрит тела желудка) уровень пепсиногена I чаще имеет тенденцию к повышению.
Пепсиноген II. Уровень пепсиногена II в крови отражает состояние всей слизистой желудка. Его концентрация увеличивается при воспалении слизистой (гастрите), причиной которого наиболее часто является инфекция Helicobacter pylori, в других случаях – некоторые лекарственные препараты, бактериальные, вирусные или паразитарные инфекции, желчный рефлюкс, острая пища или алкоголь. Уровень выше 10 мг/л часто соотносится с воспалением. При атрофии слизистой тела желудка уровень пепсиногена II , в отличие от пепсиногена I, относительно стабилен или может слегка увеличиваться.
Соотношение пепсиногенов I/II является чувствительным и специфичным маркером атрофии слизистой тела желудка. Его используют в комплексе с исследованием пепсиногена I для диагностики атрофии слизистой тела желудка. При атрофическом гастрите тела желудка отношение пепсиногенов I/II снижается ниже 3.
Гастрин-17. Гастрин - полипептидный гормон желудочно-кишечного тракта, регулирующий секрецию соляной кислоты, моторику и пролиферацию клеток слизистой желудка. Выявляется в крови в разных формах (гастрин-71, -52, -34, -17, -14, -6). Гастрин-17 — доминирующая форма гастрина в здоровой слизистой антрального отдела. Он вырабатывается почти исключительно G-клетками антрального отдела желудка в ответ на стимулирующие факторы (секреция гастрина возрастает в ответ на снижение кислотности в желудке, прием белковой пищи, растяжение антральной части желудка и др.). Аномально высокая концентрация гастрина-17 натощак может свидетельствовать о снижении кислотности желудочного сока (гипо- и ахлоргидрии) и быть признаком атрофического гастрита тела желудка. При нормальной кислотности желудочного сока уровень гастрина натощак ниже 7 пмоль/л. Легкое снижение кислотности обычно вызывает повышение уровня гастрина-17 натощак до 7-10 пмоль/л, гипохлоргидрия – до 10-20 пмоль/л, ахлоргидрия –выше 20 пмоль/л.
При высокой кислотности желудка гастрин-17, напротив, вследствие обратной регуляции, может быть на недетектируемом уровне (при рН желудочного сока ниже 2,5 уровень гастрина-17 обычно менее 1 пмоль/л). Повышенная секреция кислоты связана с риском осложнения гастроэзофагальным рефлюксом. Хроническое кислотное раздражение пищевода при такой патологии может приводить к язвенному эзофагиту (воспалению пищевода) и так называемому пищеводу Барретта, который при отсутствии лечения является фактором риска рака пищевода. Низкий уровень гастрина-17 натощак ( 5 ммоль/л) – значительно снижает или исключает вероятность синдрома Барретта.
Концентрация гастрина-17 в крови натощак может быть низкой не только вследствие высокой кислотности, но также и при атрофии слизистой оболочки антрального отдела – из-за снижения числа клеток, синтезирующих гастрин-17. Чтобы дифференцировать пациентов с атрофическим гастритом антрального отдела от тех, у кого низкий уровень гастрина-17 натощак ( № 978 *);
3. Стимуляционная проба № 978 * (отдельно).
*Обращаем ваше внимание, что стимуляционная проба ( № 978 Гастрин-17 стимулированный ) заказывается отдельно.
Интерпретация:
В отчете по результатам комплекса проведенных исследований приводится наиболее вероятная интерпретация полученных результатов, расчетные риски и рекомендации.
Читайте также: