Функции эстрадиола и прогестерона. Синтез эстрогенов и прогестинов
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Москва, Россия
Кафедра гериатрической стоматологии стоматологического факультета ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России
Роль половых гормонов в патогенезе хронического генерализованного пародонтита (обзор литературы)
Журнал: Российская стоматология. 2014;7(1): 3‑7
Янушевич О.О., Сырбу О.Н. Роль половых гормонов в патогенезе хронического генерализованного пародонтита (обзор литературы). Российская стоматология. 2014;7(1):3‑7.
Yanushevich OO, Syrbu ON. The role of sex hormones in pathogenesis of chronic generalized periodontitis (a review of the literature). Russian Stomatology. 2014;7(1):3‑7. (In Russ.).
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Москва, Россия
Давно известно, что половые гормоны оказывают влияние на течение пародонтита, метаболизм костной ткани и заживление ран. Цель этой обзорной статьи — выявление связи между половыми гормонами и пародонтитом, а также анализ влияния половых гормонов на пародонт в разные периоды жизни. Из изученных публикаций следует, что половые гормоны играют ключевую роль в прогрессировании заболеваний пародонта и заживлении его ран. Более того, эти эффекты представляется возможным дифференцировать по полу, а также периоду жизни пациента. Влияние дефицита половых гормонов может быть минимизировано при помощи профессиональной гигиены полости рта и заместительной гормональной терапии.
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Москва, Россия
Кафедра гериатрической стоматологии стоматологического факультета ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России
Гормоны являются специфическими регуляторными молекулами, которые определяют размножение, рост и развитие организма, поддержание его внутренней среды, а также производство, использование и хранение энергии [12]. Гормоны ответственны как за физиологические, так, при определенных условиях, и патологические изменения почти во всех типах тканей тела.
Целевые рецепторы для воздействия ряда гормонов, таких как андрогены, эстрогены, прогестерон, были обнаружены в тканях пародонта [21]. Следовательно, системный дисбаланс эндокринной системы играет важную роль в патогенезе заболеваний пародонта.
Стероидные половые гормоны, такие как эстроген и эстрадиол, влияют на минеральный обмен в костной ткани. Среди других гормонов, ответственных за обмен веществ в костной ткани — прогестерон, тестостерон и дигидротестостерон (ДНТ), андростендион, дигидроэпиандростендион, а также и половой гормон связывающий глобулин [23]. Среди перечисленных гормонов эстрогены, прогестерон и тестостерон в наибольшей степени связаны с патогенезом заболеваний пародонта.
Эстроген и прогестерон отвечают за физиологические изменения в организме женщины на определенных специфических этапах ее жизни, начиная с периода полового созревания. Эстроген вызывает некоторые характерные для пубертатного периода изменения, а прогестерон действует синергически с эстрогеном в области формирования менструального цикла, а также подавляет секрецию фолликулостимулирующего гормона передней доли гипофиза [23]. Оба гормона также способствуют анаболизму белка и росту организма [24, 25]. Оба гормона оказывают воздействие на различные органы и системы, включая полость рта [17, 20, 25]. В частности, эстрогены могут влиять на дифференцировку клеток многослойного чешуйчатого эпителия, а также синтез и поддержание коллагеновых волокон [28]. Рецепторы к эстрогену, найденные в остеобластоподобных клетках, обеспечивают механизм прямого воздействия на костную ткань [8, 26, 27]. Эти рецепторы также расположены в периостальных фибробластах и фибробластах собственной пластинки [15] и периодонтальной связки (PDL), обеспечивая прямое действие половых гормонов на различные ткани пародонта. Клинически у пациентов с достаточным уровнем эстрогена в крови отмечено отсутствие воспалительных изменений пародонта при более высоком уровне зубного налета, в сравнении с пациентами со сниженным уровнем эстрогена [24]. Таким образом, активность медиаторов воспаления может тормозиться достаточным уровнем эстрогена, это может быть связано с участием эстрадиола и прогестерона в продукции простагландинов (ПГ).
Снижение секреции эстрогенов у женщин приводит к нарушению факторов, определяющих состояние эндотелия кровеносных сосудов. Есть основания предполагать, что важным моментом запуска воспалительно-дистрофического процесса в пародонте является поражение гистогематического барьера в его тканях, прежде всего эндотелиальной выстилки микрососудов. Именно эндотелий первым реагирует при воспалении, ишемии и дистрофии. При развитии воспаления в пародонте у женщин с гипоэстрогенемией в эндотелиальных клетках происходит набухание и вакуолизация митохондрий с переходом в гигантские, изогнутые формы, что является признаком их защитной реакции от лизиса. При средней и тяжелой степени хронического пародонтита довольно часто отмечается наличие тромбоцитов в просвете капилляров, истончение, а в некоторых случаях и прерывистость базальной мембраны [1, 4, 5].
Результаты проведенных исследований свидетельствуют о том, что нормальный уровень циркулирующего в крови эстрогена имеет важное значение для защиты пародонта. В ряде исследований выявлены следующие виды влияния эстрогенов на пародонт:
— ингибируют высвобождение провоспалительных цитокинов клетками мозга человека;
— уменьшают уровень Т-клеточного воспаления;
— подавляют синтез лейкоцитов в костном мозге;
— ингибируют хемотаксис полиморфно-ядерных нейтрофилов (ПМН);
— стимулируют фагоцитоз ПМН [11, 15, 20, 21, 25].
Прогестерон — другой половой гормон, который оказывает непосредственное влияние на пародонт. Экспериментальные, эпидемиологические и клинические данные показали, что прогестерон активно участвует в костном метаболизме и может играть важную роль в процессах костной резорбции и формирования кости [8, 9, 18, 19]. Отмечено, что прогестерон может оказывать свое действие непосредственно на кости, воздействуя на рецепторы остеобластов или, косвенно, конкурентно влияя на рецепторы глюкокортикоидов [21, 23]. Установлены следующие эффекты воздействия прогестерона на пародонт:
— увеличение производства ПГ;
— увеличение содержания полиморфно-ядерных лейкоцитов и ПГЕ2 в десневой жидкости [29];
— редуцирование противовоспалительного действия глюкокортикоидов;
— влияние на синтез коллагена и других белков;
— изменение метаболизма фибробластов PDL;
— увеличение проницаемости сосудов [1, 4, 9, 12, 16, 23—25].
Андрогены — гормоны, ответственные за маскулинизацию. Тестостерон может быть произведен и в коре надпочечников, однако тестостерон, синтезированный в яичках, является наиболее активной формой. Его секреция регулируется АКТГ и гонадотропными гормонами гипофиза. Андроген коры надпочечников — андростендион — превращается в тестостерон и эстрогены и представляет собой важный источник эстрогенов у мужчин, а также у женщин в постменопаузе. Специфические рецепторы к этому гормону были выявлены в пародонтальной ткани [25]. Известно, что количество рецепторов в фибробластах имеет тенденцию к увеличению при воспалительном процессе в деснах. Считается, что увеличение матричного синтеза в пародонтальной ткани происходит под влиянием тестостерона [34]. Тестостерон также принимает участие в костном метаболизме, играя важную роль в поддержании костной массы [33].
Весьма эффективным способом изучения влияния андрогенов на костный метаболизм является оценка наличия биохимических маркеров костной реконструкции в костной ткани под воздействием этих гормонов. Одним из маркеров ремоделирования костной ткани, который используется для этой цели, является остеопротегерин (OPG), который ингибирует образование и активацию остеокластов путем нейтрализации их родственного лиганда [26, 27]. Воздействие OPG выражается в снижении потери плотности костной ткани, наблюдаемом при прогрессировании заболеваний пародонта. Обнаружено, что сывороточная концентрация OPG значительно увеличивается с возрастом и положительно коррелирует с величиной индексов свободного тестостерона и эстрадиола [26]. Итак, наблюдаются следующие варианты воздействия андрогенов на пародонт:
— стимулируют матрицу синтеза остеобластов и фибробластов пародонтальной связки;
— стимулируют пролиферацию и дифференцировку остеобластов;
— снижают продукцию интерлейкина (IL-6) при воспалении;
— подавляют секрецию ПГ;
— повышают концентрацию OPG [2, 15, 20, 21, 23—26].
В результате проведенных исследований установлено, что возраст, а также высокая концентрация андрогенов и эстрогенов стимулируют синтез OPG, тогда как паратгормон снижает концентрацию OPG в сыворотке крови мужчин [26]. Эти данные позволяют предположить, что OPG является важным паракринным медиатором костного метаболизма у пожилых мужчин, и подчеркивают роль андрогенов в гомеостазе костной ткани у мужчин. Исследования также показали, что функции этих гормонов регулируются в пародонте, посредством стимулирующего воздействия различных факторов роста на синтез ДHT. М. Soory и соавт. [24, 25] обнаружили значительную стимуляцию синтеза ДHT инсулиноподобным фактором роста в тканях десен и культивируемых фибробластах. Этот факт позволяет представить возможный механизм развития санирующих воспалительных изменений в пародонте посредством метаболизма андрогенов. Те же авторы позже исследовали действие IL-1 на метаболизм андрогенов в тканях десны человека с признаками хронического воспаления и PDL. При воздействии IL-1 наблюдалось двукратное увеличение синтеза DHT и 3,5-кратное увеличение образования 4-андростендиона в десневой ткани; в PDL отмечено 9-кратное увеличение синтеза DHT и 6-кратное увеличение синтеза 4-андростендиона. Наблюдавшееся преобладание метаболического потенциала PDL по сравнению с тканями десны под воздействием IL-1 отражает механизм биохимических процессов при воспалительных заболеваниях пародонта [25]. Андрогены также взаимодействуют с другими важными медиаторами воспаления, в частности с IL-6. Этот цитокин играет важную роль в возникновении тканевых повреждений при заболеваниях пародонта и секретируется клетками многих типов, в том числе фибробластами ротовой полости. В 1998 г. Е. Orwoll и соавт. [23] исследовали степень влияния ДHT на экспрессию и регулирование синтеза IL-6 в фибробластах десны. Проведя исследование иммуноферментного анализа, они отметили, что увеличение концентрации ДHT ведет к прогрессивному снижению синтеза IL-6 в клетках десен как у здоровых людей, так и у пациентов с воспалением и гиперплазией десен [23].
В целом, андрогены могут защищать ткани пародонта посредством положительного анаболического действия на их клетки, отрицательного воздействия на присутствие и концентрацию медиаторов воспаления, а также ингибирующего действия на функции остеокластов.
Несколько факторов могут повлиять на степень и характер воздействия половых гормонов на пародонт. К ним относятся пол, возраст и гормональные препараты.
Вполне понятно, что пол играет важную роль в изменении плотности костной ткани скелета человека. Известно также, что женщины гораздо чаще, чем мужчины страдают от остеопороза. Е. Lau и соавт. [31] сообщили, что женщины составляют 80% среди пациентов с остеопорозом, что коррелирует с более высокой частотой переломов бедра у женщин, которые также чаще подвержены гормональному дисбалансу в течение всей жизни. Системные сдвиги метаболизма, обусловленные гипоэстрогенемией, непосредственно влияют на пульпу зуба, на ткани пародонта, способствуют развитию остеопороза во всем скелете, в том числе и в костной ткани челюстей. Причем при гипоэстрогенемии потеря губчатой субстанции кости челюстей происходит быстрее, а затем развивается более медленная потеря кортикальной костной ткани, что более характерно для возрастных изменений. Кроме того, при изучении влияния пола на заболевания пародонта было установлено, что женщины болеют чаще, чем мужчины [6, 7, 10, 22], при этом многие авторы представили противоречивые данные [6, 10, 13, 18, 22]. Это несоответствие, по-видимому, связано с тем фактом, что женщины более склонны обращаться за стоматологической помощью, чем мужчины [10, 22]. В наблюдении, которое подтверждает этот постулат, у мужчин и женщин отмечено наличие одинакового качественного и количественного состава поддесневых бактерий, которые являются наиболее важным фактором риска развития заболеваний пародонта [2—4, 30]. При исследовании роли половых гормонов в процессе заживления ран возникает вопрос об их влиянии на этот процесс у мужчин и женщин в силу очевидного различия качественного и количественного состава половых гормонов. Что касается анатомических различий пародонта между полами, при сравнении формы и высоты остаточного альвеолярного отростка была обнаружена более низкая высота остаточного гребня у женщин в сравнении с мужчинами [14].
Это может быть связано с уменьшением количества циркулирующих эстрогенов у женщин в период менопаузы, что влечет за собой потерю высоты альвеолярной кости, а также снижение плотности костной ткани [18]. Указанные эффекты у женщин коррелируют именно с концентрацией гормонов, а не с повышенной восприимчивостью пародонтальных тканей, поскольку доказано, что у мужчин и женщин в тканях пародонта, как правило, имеется одинаковое количество рецепторов к половым гормонам [25].
Биологические изменения в тканях пародонта в зависимости от возрастных особенностей продукции половых гормонов более характерны для женщин. На самом деле, половое созревание, менструальный цикл, беременность, менопауза, а также использование оральных контрацептивов предопределяют большую склонность женщин к дисбалансу гормонов, чем обусловлено значительно большее количество проведенных у женщин исследований.
В среднем менопауза у женщин европейской расы наступает в возрасте 45—50 лет, таким образом 30—40% всей жизни современной женщины приходится на климактерический период [15, 21]. Большинство периодов гормональной перестройки организма является нормальным физиологическим процессом, однако изменение или колебания уровня эстрогенов может привести к ухудшению самочувствия и снижению качества жизни [4, 24]. Эстрогены оказывают непосредственное влияние на различные органы и системы организма. Рецепторы гормонов обнаружены в костной ткани, клетках головного мозга, сердечной мышце, в базальном слое эпителия и соединительной ткани десны и в других тканях полости рта, включая сосуды [17, 23, 25]. Эстрогены воздействуют на клеточную пролиферацию, дифференцировку, кератинизацию десневого эпителия. Колебания уровня половых гормонов во время менопаузы считаются факторами как воспалительных изменений в десне, так и дистрофии, гипертрофии и атрофии. Важно, однако, отметить, что эти колебания негативно влияют на состояние здоровья у мужчин [23]. Явления остеопороза, наблюдающееся у женщин в пре- и менопаузе и, реже, у мужчин пожилого и старческого возраста, оказывают следующие воздействия на состояние пародонта:
— плохое заживление ран;
— пониженное содержание костного минерала в челюстях;
— увеличение частоты пародонтоза и выпадения зубов [2, 15, 20, 21, 23—25].
У женщин в пременопаузе основной циркулирующий в крови эстроген — 17β-эстрадиол [23, 30]. По мере приближения периода менопаузы уровень эстрогена у женщин начинает снижаться в основном в конце фолликулярной и лютеиновой фаз менструального цикла. Постепенно уровень циркулирующих в крови эстрогенов уменьшается, а концентрации фолликулостимулирующего и лютеинизирующего гормонов возрастают. Следовательно, эффекты эстрогена, перечисленные выше, уменьшается, соответственно снижается противовоспалительное действие этого гормона на пародонт [2, 4, 25].
Прогестерон — другой половой гормон, который играет важную роль в костном метаболизме во время пре- и постменопаузы [22]. Считается, что недостаточность функции яичников и связанные с этим изменения, а вовсе не возраст, являются преобладающей причиной потери костной массы в течение первых двух десятилетий после менопаузы [25]. Проведенные исследования показали, что прогестерон может конкурировать с глюкокортикоидами за рецепторы остеобластов и, таким образом, ингибировать индуцированный глюкокортикоидами остеопороз.
Менопауза также влияет на концентрацию циркулирующих в крови андрогенов. До менопаузы 50% циркулирующего андростендиона является производным яичников и 50% — надпочечников. С угасанием функции яичников концентрация циркулирующих андрогенов снижается примерно на 50%. Было высказано предположение, что периферийные превращения андрогенов в эстрогены могут быть основным фактором защиты костей [32], поскольку, как уже упоминалось ранее, эстрогены оказывают ингибирующее действие на остеокласты. Также установлена положительная корреляция высокой концентрации тестостерона с плотностью костей, что подтверждается низким уровнем данного андрогена у пациентов с остеопорозом [18, 26].
Таким образом, половые гормоны оказывают серьезное влияние на возникновение, течение и прогрессирование заболеваний пародонта, а также заживление ран полости рта. Характер и степень воздействия гормонов зависят от пола, возраста и периода жизни пациента. Очевидно, что не все пациенты одинаково реагируют на одну и ту же концентрацию половых гормонов в крови. Следует отметить, что отрицательное влияние снижения концентрации половых гормонов на заболевания пародонта может быть минимизировано высоким уровнем гигиены полости рта и заместительной гормональной терапией.
Несмотря на достаточно большое количество исследований, посвященных данной тематике, истинный механизм воздействия половых гормонов на течение заболеваний пародонта еще предстоит выяснить.
Описание исследования
Эстрогены – это подкласс стероидных женских половых гормонов. За их продукцию у женщин отвечает фолликулярный аппарат, у мужчин – яички (в них вырабатывается до 20% общего количества гормона) Также у лиц обоего пола эстрогены синтезирует кора надпочечников, кожа, жировая ткань, волосяные фолликулы, кости, мозг.
Функция гормона в женском организме – обеспечение нормального развития и работы репродуктивной системы, в мужском – нормализация функционирования яичек и предстательной железы.
В человеческом организме присутствуют три формы эстрогенов – эстрон (Е1), эстрадиол (Е2), эстриол (Е3). Наиболее активным из них является эстрадиол, затем эстриол. Самой малоактивной второстепенной формой эстрогенов является эстрон. Эстрон, эстрадиол и эстриол образуются в результате сложной реакции взаимодействия андрогенов (стероидных мужских гормонов) и ферментов.
Прогестагены – это подкласс стероидных женских половых гормонов. В женском организме их продуцирует желтое тело яичников, плацента и в небольшом количестве кора надпочечников. Функцией этих гормонов является обеспечение наступления и сохранения беременности. При их участии происходит образование нормального секреторного эндометрия, в процессе чего внутренняя слизистая оболочка матки переходит из пролиферативной фазы в фазу секреторную. Кроме того прогестрагены подавляют синтез эстрогенов, андрогенов, гонадотропных гормонов (подкласса тропных гормонов, вырабатываемых передней долей гипофиза и плацентой).
В мужском организме выработка прогестагенов происходит в небольшом количестве. Они являются промежуточным продуктом продукции кортизола и тестостерона. Как самостоятельное биологически активное вещество, прогестагены участвуют в функционировании центральной нервной системы. За синтез этих гормонов отвечают кора надпочечников и яички.
Эстрадиол – наиболее активная форма эстрогена, вырабатывается гранулезами и является их основным гормоном. Его образование происходит из предшественника тестостерона. Кроме того, гранулезы синтезируют эстрон, но количество его меньше, чем эстрадиола. Печень и плацента преобразуют эстрон в эстриол. Гранулезы продуцируют также прогестерон (этот гормон необходим для овуляции), однако совсем в незначительных количествах. Главным «производителем» прогестерона являются клетки желтого тела, контроль которых осуществляет лютеинизирующий гормон (его вырабатывает гипофиз). На цикличность секреторной активности этих клеток оказывает влияние половой цикл женщин.
При содействии эстрогенов проходят следующие процессы:
- развитие эмбриона и формирование его половых признаков;
- половое созревание;
- развитие женских половых признаков;
- установление полового цикла женщин;
- развитие мышц и железистого эпителия матки;
- формирование молочных желез;
- регуляция полового поведения (поведения, связанного с реализацией половой потребности);
- развитие женской половой клетки (овогенез);
- оплодотворение и имплантация яйцеклетки;
- нормальные роды.
Геномный эффект эстрогенов проявляется в подавлении процесса разрушения (резорбции) костной ткани, оказании общего анаболического действия (т. е. гормоны способствуют образованию новых веществ или структур), хотя оно и менее выраженное, чем у андрогенов. Действие негеномного механизма эстрогенов направлено:
- на задержке солей, азота и воды в организме;
- на активацию NO-синтетазы – фермента, ускоряющего реакцию окисления азота в коронарных сосудах, что является своеобразной профилактикой развития ИБС (ишемической болезни сердца) у женщин;
- на модулирование выделения инсулина и соблюдение кальциевого баланса внутри клеток.
Многофункциональность эстрогенов объясняется распространенностью их рецепторов на мембранах различных видов клеток организма (кровяных, нервных, костных, секреторных, мышечных, клеток соединительной ткани). Поэтому резкое падение их уровня в женском организме при климаксе является причиной изменения работы различных систем.
Действие прогестерона направлено на ослабление готовности маточной мускулатуры к сокращению, т. о. гормон выступает «гарантом» сохранения беременности. В малых количествах он участвует в процессе овуляции. Прогестерон также подавляет процесс выработки корой надпочечников альдостерона, стимулирует процесс выведения натрия с мочой.
Увеличение концентрации прогестерона может стать причиной повышения температуры тела на 0,5-0,7°C (т. е. он при повышении уровня обладает термогенным эффектом). При попадании в печень прогестерон частично теряет активность за счет быстрого образования конъюгированных (связанных) соединений, в результате чего образуются биологически неактивные продукты. Прегнандиол – основной из них, накапливается в жировой ткани и является источником прогестерона в случае прекращения его синтеза организмом. Способностью прегнандиола накапливаться в жировой клетчатке объясняется стабильность его уровня в моче при введении внутримышечно больших доз гестерона (женского полового гормона), хотя прогестерон из крови при этом быстро исчезает. На сегодняшний день принята следующая схема преобразования прогестерона в печени: прогестерон → прегнандион → прегненолон → прегнандиол.
Следствием нарушения выработки эстрогенов может быть
- нарушение функций яичников;
- нарушение менструального цикла;
- замедление или ускорение полового развитие;
- функциональные нарушения придатка и яичек;
- нарушения в развитии половых клеток;
- снижение репродуктивной способности;
- увеличение одной или обеих молочных желез;
у представителей обоих полов:
- остеопороз;
- жировая дистрофия печени;
- ожирение;
- бесплодие.
Подготовка к исследованию
Данный тест предназначен для обследования лиц старше 16 лет.
Для исследования необходимо отобрать порцию суточной мочи. Для ее хранения и транспортировки используется стерильный контейнер с крышкой, который можно получить в пункте отбора проб медицинской компании «Наука» или приобрести самостоятельно в аптеке.
Подготовка к тестированию подразумевает отказ от мочегонных средств и алкоголя за сутки до исследования. В этот же промежуток времени нежелательны физические (в т. ч. спортивные тренировки) и эмоциональные нагрузки.
При записи на исследование необходимо указать отсутствие/наличие беременности. Небеременным женщинам рекомендуется сдавать анализ на 3-5 день менструального цикла (если нет других рекомендаций лечащего врача).
Предварительный сбор мочи осуществляется в тщательно вымытую и высушенную 2-3-хлитровую емкость.
Алгоритм действий следующий:
1. Первая порция утренней мочи не собирается, но засекается время опорожнения мочевого пузыря.
2. Вся остальная выделяемая в течение суток моча собирается в подготовленную емкость. Банка с биоматериалом сохраняется в холодильнике. Последнее (утреннее) мочеиспускание должно по времени совпасть с первым, произведенным сутки назад.
3. Объем собранной мочи тщательно измеряется, перемешивается. Из общей емкости в контейнер, на котором указывается измеренное количество в мл, отливается 30-50 мл мочи и, при невозможности быстрой отправки в лабораторию, ставится на хранение в холодильник (температура хранения от 2 до 8⁰ С).
Важно! Для получения максимально корректных результатов исследования биоматериал должен быть доставлен в лабораторию в день, когда сбор закончен.
Обратите внимание! Для анализа достаточно отобранного в контейнер объема мочи, всю ее нести не нужно!
Показания к исследованию
Цель исследования – определение и контроль концентрации гормонов, диагностика состояний, связанных с гормональными нарушениями.
Обследование женщин проводится:
- при нарушении менструального цикла;
- при нарушении функций яичников;
- при замедленном или преждевременном половом развитии.
- при функциональных нарушениях придатков яичек;
- при нарушении развития мужских половых клеток (сперматозоидов);
- при снижении фертильности (способности к производству нормального потомства);
- при гинекомастии (увеличении одной или обеих молочных желез).
Обоим полам обследование рекомендовано:
- при остеопорозе (хронически прогрессирующем системном заболевании скелета, характеризуемом снижением плотности костной ткани и усилением хрупкости костей);
- при ожирении;
- при жировой дистрофии печени (патологическом накоплении триглицеридов в печеночных клетках);
- при бесплодии.
Интерпретация исследования
Тест количественный. Исследование проводится по 4 показателям:
- эстрадиолу (мкг/сут.);
- эстрону (мкг/сут.);
- эстриолу (мкг/сут.);
- прегнандиолу (мг/сут.).
Уровень эстрогенов измеряется в микрограммах в сутки (мкг/сут), прегнандиола – в миллиграммах в сутки (мг/сут).
Половые гормоны
Репродуктивная функция у обоих полов полностью контролируется и регулируется гормонами. Основные половые гормоны разделены на два класса – эстрогены (женские) и андрогены (мужские). И у мужчин, и у женщин присутствуют оба вида гормонов, но в совершенно разных количествах. Так, например, суточная выработка мужского гормона тестостерона у мужчин в 20-30 раз больше чем у большинства женщин. В свою очередь, женский половой гормон эстрадиол, в небольших количествах есть и у мужчин. У женщин, кроме двух основных классов гормонов присутствует ещё один класс: гестагены, главный представитель этого класса – прогестерон. У мужчин половые гормоны образуются в ткани семенников, у женщин они синтезируются яичниками, кроме того, независимо от пола, небольшое количество гормонов вырабатывается в коре надпочечников. Считается, что эстрогены в большей степени отвечают за память, а андрогены – за познавательные функции, настроение, половое влечение. Избыток и, наоборот, дефицит гормонов одинаково неблагоприятно сказываются на здоровье. Так, дефицит и переизбыток тестостерона препятствуют созреванию яйцеклетки.
Прогестерон – основная функция состоит в подготовке организма женщины к беременности. Он необходим для поддержания беременности и тонуса гладкой мускулатуры матки. Предотвращает избыточное разрастание слизистой матки и оказывает влияние на ткань молочных желез (стимулирует рост и развитие железистой ткани молочных желез, способствует подготовке их к лактации).
Каждый месяц эстроген заставляет внутренний выстилающий слой матки – эндометрий – расти и обновляться, в то время как лютеинизирующий гормон (ЛГ) способствует высвобождению яйцеклетки в одном из яичников. На месте высвободившейся яйцеклетки образуется так называемое жёлтое тело, которое вырабатывает прогестерон. Прогестерон вместе с гормоном, выделяемым надпочечниками, останавливает рост эндометрия и подготавливает матку к возможной имплантации оплодотворенной яйцеклетки. Если оплодотворения не происходит, желтое тело исчезает, уровень прогестерона падает и наступает менструальное кровотечение. Если же оплодотворенная яйцеклетка прикрепляется к стенке матки, желтое тело продолжает производить прогестерон. Через несколько недель плацента берет на себя функцию желтого тела по выработке прогестерона, являясь основным источником этого гормона во время беременности.
Анализ используется для выявления причин бесплодия, диагностики внематочной или патологической беременности, контроля за состоянием плода и плаценты во время беременности и чтобы определить, была ли у пациентки овуляция.
Тестостерон – основной мужской половой гормон, отвечающий за формирование вторичных половых признаков и половую функцию. Его синтез стимулируется и контролируется лютеинизирующим гормоном (ЛГ), вырабатываемым гипофизом. Уровень тестостерона подвержен значительным колебаниям в течение суток, своего пика он достигает между 4 и 8 часами утра, а минимум приходится на вечерние часы (между 16:00 и 20:00).
Кроме того, его концентрация возрастает после физических нагрузок и уменьшается с возрастом. В особенно большом количестве он вырабатывается у подростков в период полового созревания. У мужчин тестостерон синтезируется яичками и надпочечниками, а у женщин – надпочечниками и в небольшом количестве яичниками.
Тестостерон способствует развитию вторичных половых признаков, таких как увеличение полового члена, рост волос на теле, развитие мышечной массы и низкий голос. У взрослых мужчин он регулирует сексуальные инстинкты и поддержание мышечной массы. Тестостерон также присутствует в организме женщины, хотя и в меньшей концентрации. От него зависят либидо (сексуальное влечение), способность к оргазмам, уровень инсулина, стройная фигура, развитие мышечной массы, костная ткань. Тестостерон отвечает за активность и переносимость эмоциональных нагрузок. В постменопаузу, когда исчезнут эстрогены и гестагены, именно тестостерон будет еще некоторое время поддерживать плотность костной ткани, сердечно-сосудистую систему и поможет легче переносить климактерический синдром.
Анализ назначается при мужском и женском бесплодии или пониженном половом влечении, замедленном либо преждевременном половом созревании у мальчиков и эректильной дисфункции у мужчин, при болезнях гипоталамуса, гипофиза, опухолях яичек.
Лютеинизирующий гормон (ЛГ) – гормон передней доли гипофиза, отвечает за бесперебойную работу всей системы половых желез, равно как и за выработку мужских и женских половых гормонов - прогестерона и тестостерона. У женщин ЛГ воздействует на клетки оболочки яичника и жёлтое тело, стимулирует овуляцию и активирует в клетках яичников синтез эстрогенов и прогестерона, у мужчин - на клетки семенников, активируя в них синтез тестостерона, благодаря чему, в частности, происходит созревание сперматозоидов.
Анализ проводится для диагностики бесплодия и оценки функционального состояния репродуктивной системы.
ФСГ (фолликулостимулирующий гормон) регулирует выработку половых гормонов, но сам не является таковым, поскольку вырабатывается не половыми железами, а гипофизом. В организме ФСГ регулирует деятельность половых желез: способствует образованию и созреванию половых клеток (яйцеклеток и сперматозоидов), влияет на синтез женских половых гормонов (эстрогенов).
У женщин ФСГ влияет на формирование фолликула . Достижение максимального уровня ФСГ приводит к овуляции . У мужчин ФСГ стимулирует рост семявыносящих канальцев , увеличивает уровень тестостерона в крови, тем самым обеспечивая процесс созревания сперматозоидов и либидо . У мужчин ФСГ стимулирует рост семявыносящих канальцев , увеличивает уровень тестостерона в крови, тем самым обеспечивая процесс созревания сперматозоидов и либидо .
Определение уровня фолликулостимулирующего гормона (ФСГ) проводится для оценки функции гипофиза, репродуктивной функции (как женщин, так и мужчин), а так же при нарушениях полового созревания у детей и подростков. Анализ назначается для определения причин нарушения менструального цикла различного генеза, диагностика дисфункциональных маточных кровотечений, дифференциальная диагностика центральных и периферических форм заболеваний женской половой системы, контроля эффективности гормонотерапии.
Пролактин – один из гормонов, синтезируемых гипофизом – железой контролирующей метаболизм, а также процессы роста и развития организма. Пролактин необходим для нормального развития молочных желез и обеспечения лактации - он увеличивает выработку молозива, способствует его созреванию и превращению в зрелое молоко. Он также стимулирует рост и развитие молочных желез, увеличение числа долек и протоков в них. Также он контролирует секрецию прогестерона и тормозит выработку фолликулостимулирующего гормона (ФЛГ), обеспечивая нормальный менструальный цикл, тормозя овуляцию и наступление новой беременности. В норме этот физиологический механизм предотвращает беременность следующим ребенком в период кормления грудью предыдущего и может предотвращать менструации в период кормления. В крови мужчин и небеременных женщин пролактин, обычно, присутствует в малых количествах. В повседневной жизни пролактин повышается во время сна, физической нагрузки и полового акта. Но у мужчин чрезмерное повышение его уровня способно нарушать половую функцию угнетая созревание сперматозоидов в яичках и вызывая бесплодие.
Анализ используется для диагностики бесплодия и нарушения половой функции, исследования функции гипофиза, выяснения причины галактореи (выделения молока или молозива вне связи с процессом кормления ребёнка), головных болей и ухудшения зрения.
Хорионический гонадотропин человека (ХГЧ) – это гормон, который вырабатывается в плодной оболочке человеческого эмбриона. ХГЧ является важным показателем развития беременности и её отклонений. Его производят клетки хориона (оболочки зародыша) сразу после его прикрепления к стенке матки (это происходит лишь через несколько дней после оплодотворения). Зародыш на этом этапе беременности представляет собой заполненный жидкостью микроскопический пузырёк, стенки которого состоят из быстро размножающихся клеток. Из одной части этих клеток и развивается будущий ребёнок (эмбриобласт), в то время как из клеток, находящихся снаружи зародыша, образуется трофобласт – та часть плодного яйца, с помощью которого оно прикрепляется к стенке матки. В дальнейшем из трофобласта образуется хорион.
Хорион выполняет функцию питания зародыша, являясь посредником между организмом матери и ребенка. Кроме того, он вырабатывает хорионический гонадотропин, который, с одной стороны, влияет на формирование ребенка, с другой – специфическим образом воздействует на организм матери, обеспечивая благополучное протекание беременности. Появление этого гормона в организме будущей матери на начальной стадии беременности и объясняет важность теста для ранней диагностики беременности.
Хорионический гонадотропин стимулирует секреторную функцию жёлтого тела яичников, которое должно продуцировать гормон прогестерон, поддерживающий нормальное состояние внутренней оболочки стенки матки – эндометрия. Эндометрий обеспечивает надёжное прикрепление плодного яйца к организму матери и его питание всеми необходимыми веществами. Благодаря достаточному количеству хорионического гонадотропина жёлтое тело, в норме существующее лишь около 2 недель в течение каждого менструального цикла, при успешном зачатии не подвергается рассасыванию и остаётся функционально активным в течение всего срока беременности. Причём именно у беременных под влиянием хорионического гонадотропина оно производит очень большие количества прогестерона. Кроме того, ХГЧ стимулирует продукцию эстрогенов и слабых андрогенов клетками яичников и способствует развитию функциональной активности самого хориона, а в дальнейшем и плаценты, которая образуется в результате созревания и разрастания хориональной ткани, улучшая её собственное питание и увеличивая количество ворсин хориона.
Таким образом, роль хорионического гонадотропина заключается в специфическом и многостороннем воздействии на организм женщины и плода в целях успешного протекания беременности.
На основании анализа на хорионический гонадотропин определяется присутствие в организме женщины хорионической ткани, а значит, и беременность. Анализ используется, в том числе, для диагностики многоплодной, внематочной и неразвивающейся беременности, выявления задержек в развитии плода, угрозы самопроизвольного аборта, недостаточности функции плаценты. Может назначаться, как часть комплексного обследования по выявлению пороков развития плода, а также для контроля за эффективностью искусственного аборта.
Свободный В-ХГЧ – Бета-субъединица хорионического гонадотропина человека – одна из составляющих молекулы специфического гормона – хорионического гонадотропина, образующегося в оболочке человеческого эмбриона. При отсутствии беременности результат теста на бета-ХГЧ будет отрицательным. Обнаружение бета-ХГЧ позволяет предположить, что после оплодотворения прошло уже как минимум 5-6 дней.
Анализ проводят в целях ранней диагностики беременности (3–5-дневной задержки менструации), выявления её осложнений и диагностики заболеваний, связанных с нарушением секреции ХГЧ.
Эстрадиол — пожалуй, основной и один из наиболее активных женских половых гормонов группы эстрогенов. Относится к типично женским гормонам, поскольку, в женском организме в значительном количестве, вырабатывается яичниками, реализуя большое количество физиологических функций. У мужчин эстрадиол тоже вырабатывается, но в очень малом количестве, и имеет скорее вспомогательные функции.
В женском организме эстрадиол играет исключительно важную роль в регуляции менструального цикла и функционировании всей половой системы. В детском и пубертатном периодах, гормон отвечает за рост и развитие всех органов, относящиеся к репродуктивной сфере. Под его влиянием происходят циклические изменения в тканях половых органов, а также формирование вторичных женских половых признаков (рост молочных желез, оволосение лобка и подмышек и т.д.). У взрослых женщин эстрадиол стимулирует течение первой фазы менструального цикла, вызывает рост и пролиферацию (активное деление клеток) эндометрия, таким образом, подготавливая его к внедрению плодного яйца, и наступлению беременности. Во время беременности эстрадиол усиливает обмен веществ во всех тканях организма. По мере развития беременности он начинает вырабатываться плацентой всё в большем и большем количестве, обеспечивая т.о. повышенные потребности в скорости обмена веществ и кровотоке у женщины. В мужском организме эстрадиол участвует в формировании спермы, т.е. необходим для зачатия. Но, всё же, для мужчин его роль не настолько значительна, как для женщин.
Определение уровня эстрадиола у женщин фертильного возраста проводится при диагностике большого числа заболеваний и состояний, таких как бесплодие, нарушения менструального цикла, отсутствие овуляций, поликистозе и опухолях яичников и т.п, а также для оценка функций плаценты на ранних сроках беременности и мониторинга при экстракорпоральном оплодотворении. Используется при диагностике и лечении остеопороза. У мужчин анализ проводится при низком качестве спермы и бесплодии, заболеваниях надпочечников и печени.
Андростендион – основной стероидный гормон, является промежуточным продуктом и основой для образования тестостерона и эстрона. Синтезируется, у мужчин и женщин, корой надпочечников и половыми железами. У обоих полов, уровень андростендиона имеет выраженные колебания, как в течении суток (максимум в утренние часы), так и с возрастом (увеличивается, примерно, с 7-и, и плавно снижается после 30 лет). У женщин показатель также зависит от фазы менструального цикла (максимум в середине) и значительно возрастает при беременности. Определение уровня андростендиона используется для оценки синтеза андрогенов (избытка секреции мужских гормонов) и диагностики различных нарушений функционирования половой и эндокринной систем.
Цены на исследования можно узнать в разделе "Прейскурант" клинической лаборатории. Кровь на исследования принимается ежедневно (кроме воскресенья) с 7 до 11 часов. Строго натощак .
Функции эстрадиола и прогестерона. Синтез эстрогенов и прогестинов
Функции эстрадиола и прогестерона. Синтез эстрогенов и прогестинов
Существуют два типа половых гормонов яичника — эстрогены и прогестины. Наиболее важным из эстрогенов является гормон эстрадиол, а самым важным прогестином является прогестерон. Эстрогены ответственны за осуществление пролиферации и рост специфических клеток организма, которые обеспечивают формирование вторичных женских половых признаков. Основной функцией прогестинов является подготовка матки к беременности и молочных желез — к лактации.
а) Химическая структура половых гормонов. Эстрогены. В норме у небеременной женщины в значительном количестве в яичниках секретируются только эстрогены; очень небольшие количества эстрогенов могут продуцироваться также корой надпочечников. Во время беременности огромные количества эстрогенов начинают секретироваться плацентой (обсуждается в отдельной статье на сайте, просим вас пользоваться формой поиска выше).
У женщины в плазме крови присутствуют в значительных количествах только три эстрогена: -βэстрадиол, эстрон и эстриол, химическая формула которых представлена на рисунке ниже.
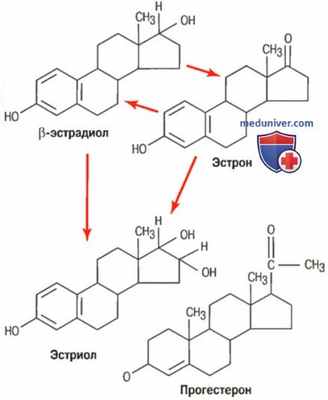
Химические формулы основных женских гормонов
Яичники продуцируют главным образом β-эстрадиол, наряду с которым секретируется в небольшом количестве эстрон, хотя большая часть этого гормона образуется в периферических тканях из андрогенов, секретируемых корой надпочечников и клетками теки яичника.
Эстриол относится к гормонам со слабо выраженными свойствами эстрогена и является производным эстрадиола и эстрона, получаемым из них путем окисления, превращение эстрадиола и эстрона в эстриол осуществляется главным образом в печени.
Эстрогенная активность β-эстрадиола в 12 раз выше, чем у эстрона, и в 80 раз выше, чем у эстриола. Помня об относительно более высокой активности эстрадиола, можно считать, что вклад эстрадиола в создание суммарных эстрогенных эффектов в организме в целом во много раз превышает совместный вклад двух других — эстрона и эстриола. По этой причине β-эстрадиол считают основным эстрогеном, хотя эстрогенными влияниями эстрона не стоит пренебрегать.
б) Прогестины. Едва ли не наиболее важным из всех прогестинов является прогестерон, хотя небольшое количество секретируемого вместе с прогестероном 17-α-гидроксипрогестерона по существу вызывают те же эффекты, что и прогестерон. Из практических соображений обычно прогестерон считают единственно важным прогестином. В организме здоровой небеременной женщины прогестерон секретируется в значительном количестве только во второй половине овариального цикла, в это время прогестерон синтезируется желтым телом.
Как мы увидим в отдельной статье на сайте (просим вас пользоваться формой поиска выше), большое количество прогестерона также производится плацентой во время беременности, особенно после четвертого месяца гестации.
в) Синтез эстрогенов и прогестинов. Все химические формы эстрогенов и прогестерона, показанные на рисунке выше, являются стероидным гормонами. Они синтезируются в яичниках главным образом из холестерола, доставляемого кровью, но небольшое количество может образовываться из ацетил-КоА, множество молекул которого могут объединяться, формируя соответствующие стероидные ядра.
Первоначально во время этого синтеза образуются в основном прогестерон и мужской половой гормон — тестостерон, причем первым образуется тестостерон; затем во время фолликулярной фазы овариального цикла, перед тем как эти два первоначально синтезируемых гормона покинут яичник, почти весь тестостерон и большая часть прогестерона превращаются клетками гранулезы в эстрогены. Во время лютеиновой фазы цикла образуется так много прогестерона, что он не успевает превращаться в эстрогены, и все большее количество прогестерона начинает обнаруживаться в крови в этот период овариального цикла. Количественное поступление в кровоток синтезируемого в яичниках тестостерона соответствует 1/15 количества тестостерона, синтезируемого в семенниках и присутствующего в плазме крови мужчины.
г) Эстрогены и прогестерон транспортируются кровью, связавшись с белками плазмы крови. Как эстрогены, так и прогестерон транспортируются кровью, будучи связанными в основном с альбуминами плазмы и со специфическими эстроген- и прогестеронсвязывающими глобулинами. Взаимодействие гормонов с белками плазмы достаточно непрочное, и они могут быстро высвобождаться и поступать в ткани в течение примерно 30 мин.
Учебное видео анализ на женские половые гормоны в норме и при патологии
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Женская репродуктивная эндокринология
Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему.
В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон, известный также как ГнВГ, и рилизинг-гормон лютеинизирующего гормона (РГЛГ).
Эстрогены и прогестерон , связанные с белками плазмы, циркулируют в кровяном русле. Только свободные эстрогены и прогестерон проявляют биологическую активность. Они стимулируют органы-мишени репродуктивной системы (например, матку, влагалище) и молочные железы. Эти гормоны обычно ингибируют (так называют негативную обратную связь) секрецию гонадотропинов, но в определенных случаях (например, примерно во время овуляции), могут стимулировать ее.
Система ЦНС-гипоталамус-гипофиз-гонады и органы-мишени
Яичниковые гормоны имеют прямое и опосредованное влияние на другие ткани (например, кости, кожу, мышцы).
ФСГ = фолликуло-стимулирующий гормон; ГнВГ = гонадотропин-высвобождающий гормон; ЛГ = лютеинизирующий гормон.
Половая зрелость
Половое созревание – это период последовательного приобретения ребенком физических характеристик взрослого человека, которые определяют состояние зрелости и способность к деторождению. Уровень ЛГ и ФСГ достаточно высок при рождении, затем в течение нескольких месяцев он падает и остается низким вплоть до периода полового созревания. До полового созревания в репродуктивных органах-мишенях происходят незначительные изменения.
Возраст наступления пубертатного периода
Возраст начала пубертатного периода и скорость развития различных его этапов зависят от различных факторов. За последние 150 лет возраст начала полового созревания уменьшился, прежде всего из-за улучшения состояния здоровья и качества пищи, но эта тенденция стабилизировалась. В США средний возраст начала полового созревания составляет 12,5 лет, однако этот показатель варьирует в зависимости от этнической принадлежности ( 1 Справочные материалы по пубертатному периоду Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ).
Половая зрелость у девочек с повышенной массой тела наступает раньше среднего, а у девочек со значительным недобором массы тела и при недостаточном питании –позже среднего ( 2 Справочные материалы по пубертатному периоду Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ). Согласно этим наблюдениям, для полового созревания необходима критическая масса тела или количество жира.
Множество других факторов влияют на момент начала пубертатного периода и на то, как быстро он развивается. К примеру, существуют некоторые данные, свидетельствующие, что ограничение внутриутробного роста, особенно, с последующим перекармливанием, могут способствовать более раннему началу пубертатного периода и более быстрому его развитию ( 3 Справочные материалы по пубертатному периоду Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ). Например, некоторые данные свидетельствуют о том, что у детей, рожденных с низкой для данного гестационного возраста массой, наблюдается более быстрое прогрессирование полового созревания ( 4 Справочные материалы по пубертатному периоду Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ).
Физические изменения при половом созревании
В течение подросткового периода последовательно происходят физические изменения (см. рисунок Пубертатный период— когда развиваются женские половые признаки Пубертатный период - период развития женских половых признаков ).
Менархе (первые месячные) наступает примерно через 2-3 года после начала развития молочных желез. Менструальные циклы обычно нерегулярны после менархе, и может пройти до 5 лет, пока они становятся регулярными. Ускорение роста замедляется после начала менархе. конституционные особенности телосложения изменяются, расширяется область таза и бедер. Увеличивается количество подкожного жира и происходит его накопление на бедрах.
Механизмы, инициирующие половое созревание
Механизмы, инициирующие половое созревание, неясны.
Основными факторами, которые влияют на высвобождение ГнВГ есть нейротрансмиттеры и пептиды (например, гамма-аминомасляная кислота [ГАМК], белая фракция протеина). В детстве эти факторы могут тормозить высвобождение гонадотропин-высвобождающего гормона, а затем инициировать его высвобождение, что вызывает преждевременное половое созревание. В раннем пубертате выброс гипотапамического гонадотропин-высвобождающего гормона становится менее чувствительным к торможению эстрогенами и прогестероном . В результате увеличивается выброс гонадотропин-высвобождающего гормона, который стимулирует секрецию ЛГ и ФСГ, которые, в свою очередь, стимулируют выработку половых гормонов, прежде всего эстрогенов . Эстроген стимулирует развитие вторичных половых признаков.
Рост лобковых и подмышечных волос стимулируется надпочечниковыми андрогенами дегидроэпиандростеронами (ДЭА) и сульфатами ДЭА; производство этих андрогенов увеличивается за несколько лет до полового созревания в период, называемый адренархе.
Пубертатный период - период развития женских половых признаков
Показатели отражают нормальный диапазон значений.
Схематическое изображение стадий I-V созревания молочных желез по Таннеру
Из Marshall WA, Tanner JM: Variations in patterns of pubertal changes in girls. Archives of Disease in Childhood44:291–303, 1969; used with permission.
Схематическое изображение стадий I-V созревания молочных желез по Таннеру
Из Marshall WA, Tanner JM: Variations in patterns of pubertal changes in girls. Archives of Disease in Childhood44:291–303, 1969; used with permission.
Справочные материалы по пубертатному периоду
1. Anderson SE, Must A: Interpreting the continued decline in the average age at menarche: results from two nationally representative surveys of U.S. girls studied 10 years apart. J Pediatr 147 (6):753–60 2005.doi: 10.1016/j.jpeds.2005.07.016
3. Darendeliler F: IUGR: Genetic influences, metabolic problems, environmental associations/triggers, current and future management. Best Pract Res Clin Endocrinol Metab 33 (3):101260, 2019. doi: 10.1016/j.beem.2019.01.001 Epub 2019 Jan 22.
4. Veening MA, van Weissenbruch MM, Roord JJ, de Delmemarre-van Waal HA: Pubertal development in children born small for gestational age. J Pediatr Endocrinol Metab 17 (11):1497–505, 2004. doi: 10.1515/jpem.2004.17.11.1497
5. Sørensen S, Brix N, Ernst A, et al: Maternal age at menarche and pubertal development in sons and daughters: A Nationwide Cohort Study. Hum Reprod 33 (11):2043–2050, 2018. doi: 10.1093/humrep/dey287
6. Eckert-Lind C, Busch AS, Petersen JH, et al: Worldwide secular trends in age at pubertal onset assessed by breast development among girls: A systematic review and meta-analysis. J AMA Pediatr 174 (4):e195881, 2020. doi:10.1001/jamapediatrics.2019.5881
7. Marshall WA, Tanner JM: Variations in patterns of pubertal changes in girls. Arch Dis Child 44:291–303, 1969.
Развитие фолликулов в яичнике
Плод женского пола имеет конечное число предшественников яиц (половых клеток). Герминогенные клетки сперва представляют собой примордиальные оогонии, которые мигрируют из эндодермы желточного мешка в экстраэмбриональной области в недифференцированный генитальный гребень и становятся оогониями. Оогонии дифференцируются в первичные ооциты и заметно пролиферируют за счет митоза (однократное деление на две идентичные диплоидные клетки), в результате чего к 5-му месяцу беременности появляется около 7 млн ооцитов. В течение 3-го месяца беременности у некоторых оогоний начинается мейоз и наступает остановка в профазе мейоза I до полового созревания. Мейоз протекает в две фазы; это приводит к делению на четыре гаплоидные клетки. К 7-му месяцу беременности вокруг всех жизнеспособных герминогенных клеток развивается слой гранулезных клеток, формируя примордиальный фолликул. После 4 месяца гестации оогонии (а позже ооциты) начинают спонтанно погибать, в процессе гибнет около 99,9% оогоний.
В период полового созревания ооцит завершает мейоз I с образованием одного вторичного ооцита и одного полярного тельца; эти клетки задерживаются в метафазе мейоза II.
ФСГ индуцирует рост фолликулов в яичниках. В течение каждого менструального цикла отмечается ускоренный рост 3–30 фолликулов. Обычно в каждом цикле достигает овуляции только один фолликул. Такой доминантный фолликул высвобождает ооцит во время овуляции и вызывает артезию других фолликулов. В результате двух мейотических делений образуется одна яйцеклетка – одна непосредственно перед овуляцией, а вторая – при проникновении сперматозоида. При каждом мейотическом делении выделяются полярные тельца, содержащие избыток генетического материала. С увеличением возраста матери ооциты, длительно существующие в профазе мейоза, могут отвечать за генетические аномалии у плода ( 1 Справочные материалы по развитию фолликула в яичнике Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ).
Справочные материалы по развитию фолликула в яичнике
1. Jones KT: Meiosis in oocytes: Predisposition to aneuploidy and its increased incidence with age. Hum Reprod Update 14:143–158, 2008.
Менструальный цикл
Менструация – это периодические кровянистые выделения с отторженным эндометрием (общепринятое название – месячные или менструальное кровотечение) из матки через влагалище. Это вызвано быстрым снижением выработки яичниками прогестерона и эстрогена , что имеет место во время каждого цикла при отсутствии беременности. Менструация происходит в течение всей репродуктивной жизни женщины.
Нормальная продолжительность менструаций составляет от 4,5 до 8 дней ( 1 Менструальный цикл. Ссылки Гормональная взаимосвязь между гипоталамусом, передней долей гипофиза и яичниками регулирует женскую репродуктивную систему. В гипоталамусе секретируется короткий пептид, гонадотропин-рилизинг-гормон. Прочитайте дополнительные сведения ). Кровопотеря во время менструации составляет в среднем 30 мл (нормальный диапазон – 5–80 мл) и обычно обильная кровопотеря отмечается на 2-й день. Поскольку пациентки не измеряют объем менструальной крови, чрезмерно тяжелые или легкие менструации определяются на основании их ощущений и количества использованных прокладок или тампонов; пропитанные прокладка или тампон поглощают от 5 до 15 мл крови. Обычная менструальная кровь не сворачивается (если кровотечение не очень сильное), вероятно, потому что фибринолизин и другие факторы ингибируют свертывание.
Средняя продолжительность менструального цикла —;28 дней (нормальный диапазон составляет 24–38 дней). Самые длительные периоды между менструациями наблюдаются сразу после наступления менархе и перед менопаузой, когда овуляция происходит нерегулярно. У человека менструация считается регулярной, когда продолжительность самого короткого и самого длинного циклов варьирует от ± 2–20 дней. Продолжительность менструального цикла рассчитывается как число дней от первого дня менструации в одном цикле до первого дня в следующем цикле.
Менструальный цикл можно разделить на фазы. Яичник проходит следующие фазы:
Читайте также:
- Гемангиома височной кости на томограмме
- Плесневые грибы. Пневмомикозы. Аллергический бронхолегочный микоз.
- Травмы скелета. Переломы костей скелета
- Гигантская кондилома Бушке—Левенштейна. Верруциформная эпидермодисплазия Левандовского—Лютца.
- Тактика при торакоабдоминальном ранении - ревизия раны, торакотомия
