Кровоснабжение гипертрофированных отделов сердца. Кровоснабжение сердца при врожденном пороке
Добавил пользователь Алексей Ф. Обновлено: 30.01.2026
Замыкающие артерии в сердце. Гистология замыкающих артерий при пороках сердца
Существование и развитие замыкающих артерий в сердце при врожденных пороках с их резкими нарушениями гемодинамики играет не последнюю роль в регуляции венечного кровообращения порочного сердца, поскольку при возникшем застойном полнокровии избыточное количество крови может удаляться из миокарда сокращениями мощных стенок замыкающих артерий через устья тебезиевых сосудов прямо в полости сердца.
Шонмакерс и Штратман (1955), Шольц, Слепка (1958), Н. В. Архангельская (1960) также находили тебезиевы сосуды, замыкающие артерии и артерио-венозные анастомозы в сердце при врожденных пороках. Роль сосудов Вьессана — Тебезия в норме и патологии изучена Pratt (1898), М. Я. Арьевым (1949), Моравиц и Цан (Morawitz, Zahn, 1912), Краиничиану (1922), Кратц (Kratz, 1927), Н. С. Механик (1941), С. П. Ильинским (1949, 1954), А. И. Озарай (1956), Поулес, Фруетте, Локамм (Poulhes, Frouette, Locamme, 1958), В. Д. Арутюновым (1960), Л. А. Тарасовым (1961).
В результате работ А. В. Рывкинда (1948—1959) известно, что в стенке замыкающей артерии имеется слой мышц, могущий при сокращении полностью суживать просвет сосуда. Замыкающие артерии являются тонко специализированными частями артериальной системы, включенными по ходу артерий мышечного типа, и сообщаются с близлежащими венами, образуя артерио-венозные анастомозы. Несомненна роль замыкающих артерий в регуляции местного кровообращения.
А. В. Рывкинд изучил артерио-венозные анастомозы и замыкающие артерии в основном в легких, плевре и плевральных спайках.
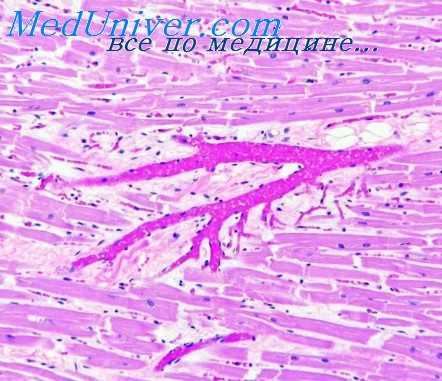
В 6 наблюдениях при тетраде Фалло, в 1 — при пентаде Фалло, в 1 — при врожденном сужении устья аорты, в 1 — при изолированном дефекте межжелудочковой перегородки, в 2 — при изолированном дефекте межпредсердной перегородки, в 1 — при аорто-пульмональном свище, в 1 — при незаращении боталлова протока, в 1 — при изолированном сужении артериального конуса правого дениях (кроме врожденного сужения артериального конуса левого желудочка и трикуспидальной атрезии) было обнаружено ожирение миокарда наиболее гипертрофированного, правого желудочка сердца.
За вычетом наблюдений, в которых имелось тотальное ожирение миокарда всех отделов сердца, в 8 наблюдениях было обнаружено очаговое мелкокапельное ожирение мышечных волокон левого желудочка, в 3 наблюдениях — межжелудочковой перегородки. Ожирение миокарда правого и левого предсердий отмечено только в случаях тотального ожирения всех отделов сердца.
Помимо жировой дистрофии, сопровождавшейся появлением капелек липоидов в саркоплазме мышечных волокон, в 11 наблюдениях обнаружена «суданофилия» мышечных волокон, т. е. интенсивное очаговое окрашивание миокарда Суданом III без появления свободных капель жира в саркоплазме (в 6 наблюдениях — при тетраде и пентаде Фалло, в 1—при изолированном дефекте межпредсердной перегородки, в 1—при изолированном дефекте межжелудочковой перегородки, в 1 — при транспозиции магистральных сосудов, в 1—при незаращении боталлова протока, в 1—при врожденном сужении артериального конуса левого желудочка).
Врожденные пороки сердца
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
Общие сведения
Врожденные пороки сердца - весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Кровоснабжение гипертрофированных отделов сердца. Кровоснабжение сердца при врожденном пороке
В далеко зашедших стадиях гипертрофии миокарда при гипертонической болезни и при ревматизме при наличии кардиосклероза также имеется гипоксия миокарда, однако отсутствует второе условие, необходимое, как мы думаем, для новообразования сосудов — незакончившаяся дифференцировка миокарда. Вот почему при гипертонической болезни и при ревматических пороках сердца не наблюдается такого большого количества сосудов в гипертрофированных отделах миокарда.
Возникает вопрос, почему авторы (Шонмакерс и Штратман, 1955), изучавшие ангиоархитектонику сердца при врожденных пороках, не обратили внимания на увеличение количества интрамуральных сосудистых ветвей. Мы думаем, что эти авторы выбрали не лучшую методику ангиорентгенографического исследования. Для проверки правильности наших наблюдений одни и те же сердца мы пробовали снимать на рентгеновскую пленку, заключенную в кассету с усиливающими вольфраматными экранами, как это делает большинство авторов, и на пленку, помещенную в пакет из черной бумаги при условии увеличенной в 10—15 раз экспозиции, как предложил В. Д. Арутюнов (1961).
При сравнении полученных ангиорентгенограмм оказалось, что на пленке, заключенной в кассету, сеть интрамуральных ветвей значительно реже, а рельеф получившихся сосудов менее четкий, чем на пленке, помещенной в пакет из черной бумаги. Предварительная проверка методик ангиорентгенографии и определила выбор наилучшей из них.
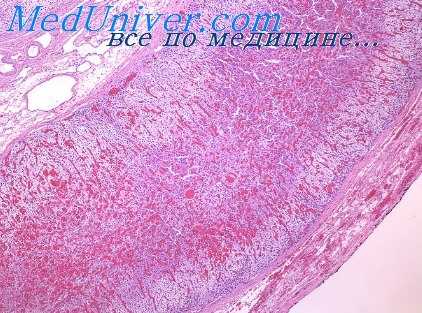
Мы привели ссылки на единичные, найденные нами в литературе, исследования, посвященные изучению сосудов сердца при врожденных пороках с помощью методики ангиорентгенографии. При ознакомлении с работами, авторы которых изучали сосуды сердца не при врожденных пороках сердца, а при гипертрофии другой этиологии, оказалось, что по вопросу о кровоснабжении гипертрофированного сердца до сих пор нет единого мнения.
А. Н. Надежин (1896), Христиан (Christian, 1927), Уорн (Wearn, 1928), Роберте (Roberts, 1941), Гросс и Спарк (Gross a. Spark, 1937), С. С. Вайль (1934—1940) считают, что между ростом гипертрофированных мышечных волокон и увеличением числа сосудов в миокарде нет параллелизма. Рюль (Ruhl, 1938), Линцбах (Linzbach, 1947), Т. Е. Ивановская (1948) обнаружили некоторое увеличение количества капилляров в миокарде, однако считают, что оно недостаточно для повышенной потребности гипертрофированного миокарда в кровоснабжении.
Док (Dock, 1941), Р. М. Коган (1947) полагают, что имеющаяся в здоровом сердце система сосудов вполне достаточна для кровоснабжения гипертрофированного сердца.
Грегг, Притчард, Чапей (Gregg, Pritchard, Shipley, 1943) установили в эксперименте на животных, что сужение легочной артерии приводит к усилению коронарного кровотока, особенно по системе правой коронарной артерии. Однако авторы не обнаружили новообразования сосудов в миокарде (опыты были произведены на половозрелых животных).
Коарктация аорты
Коарктация аорты – врожденный сегментарный стеноз (или полная атрезия) аорты в области перешейка - перехода дуги в нисходящую часть; реже – в нисходящем, восходящем или брюшном отделах. Коарктация аорты проявляется в детском возрасте беспокойством, кашлем, цианозом, одышкой, гипотрофией, утомляемостью, головокружением, сердцебиением, носовыми кровотечениями. При диагностике коарктации аорты учитываются данные ЭКГ, рентгенографии грудной клетки, ЭхоКГ, зондирования полостей сердца, восходящей аортографии, левой вентрикулографии, коронарной ангиографии. Методами хирургического лечения коарктации аорты служат транслюминальная баллонная дилатация, истмопластика (прямая и непрямая), резекция коарктации аорты, шунтирование.
МКБ-10
Коарктация аорты – врожденная аномалия аорты, характеризующаяся ее стенозом, как правило, в типичном месте - дистальнее левой подключичной артерии, в месте перехода дуги в нисходящую аорту. В детской кардиологии коарктация аорты встречается с частотой 7,5%, при этом в 2—2,5 раза чаще у лиц мужского пола. В 60-70% случаев коарктация аорты сочетается с другими врожденными пороками сердца: открытым артериальным протоком (70%), дефектом межжелудочковой перегородки (53%), стенозом аорты (14%), стенозом или недостаточностью митрального клапана (3-5%), реже с транспозицией магистральных сосудов. У части новорожденных с коарктацией аорты выявляются тяжелые экстракардиальные врожденные аномалии развития.
Причины коарктации аорты
В кардиохирургии рассматривается несколько теорий формирования коарктации аорты. Принято считать, что в основе порока лежит нарушение слияния аортальных дуг в периоде эмбриогенеза. Согласно теории Шкоды, коарктации аорты формируется вследствие закрытия открытого артериального протока (ОАП) с одновременным вовлечением прилегающей части аорты. Облитерация Баталлова протока происходит вскоре после рождения; при этом стенки протока спадаются и рубцуются. При вовлечении в данный процесс стенки аорты происходит ее сужение или полное заращение просвета на определенном участке.
По теории Андерсона–Беккера причиной коарктации может служить наличие серповидной связки аорты, которая обусловливает сужение перешейка при облитерации ОАП в области ее расположения.
В соответствии с гемодинамической теорией Рудольфа, коарктация аорты – следствие особенностей внутриутробного кровообращения плода. В период внутриутробного развития через восходящую аорту проходит 50% выброса крови из желудочков, через нисходящую - 65%, в то же время в перешеек аорты поступает только 25% крови. С этим фактом связана относительная узость перешейка аорты, которая при некоторых условиях (при наличии септальных дефектов) сохраняется и усугубляется после рождения ребенка.
Особенности гемодинамики при коарктации аорты
Типичным местом расположения стеноза служит терминальный отдел дуги аорты между артериальным протоком и устьем левой подключичной артерии (область перешейка аорты). В этом месте коарктация аорты выявляется у 90-98% больных. Снаружи сужение может иметь вид песочных часов или перетяжки с нормальным диаметром аорты в проксимальном и дистальном отделах. Внешнее сужение, как правило, не соответствует величине внутреннего диаметра аорты, поскольку в просвете аорты располагается нависающая серповидная складка или диафрагма, которые в некоторых случаях полностью перекрывают внутренний просвет сосуда. Протяженность коарктации аорты может составлять от нескольких мм до 10 и более см, однако чаще ограничивается 1-2 см.
Стенотическое изменение аорты в месте перехода ее дуги в нисходящую часть обусловливает развитие двух режимов кровообращения в большом круге: проксимальнее места препятствия кровотоку имеется артериальная гипертензия, дистальнее – гипотензия. В связи с имеющимися гемодинамическими нарушениями у больных с коарктацией аорты включаются компенсаторные механизмы – развивается гипертрофия миокарда левого желудочка, увеличивается ударный и минутный объем, расширяется диаметр восходящей аорты и ветвей ее дуги, расширяется сеть коллатералей. У детей старше 10 лет в аорте и сосудах уже отмечаются атеросклеротические изменения.
На особенности гемодинамики при коарктации аорты значительное влияние оказывают сопутствующие врожденные пороки сердца и сосудов. Со временем в артериях, задействованных в коллатеральном кровообращении, (межреберных, внутренних грудных, боковых грудных, лопаточных, эпигастральных и т.д.), происходят изменения: их стенки истончаются, а диаметр увеличивается, предрасполагая к формированию престенотических и постстенотических аневризм аорты, аневризм артерий головного мозга и др. Обычно аневризматическое расширение сосудов наблюдается у больных старше 20 лет.
Давление извитых и расширенных межреберных артерий на ребра способствует образованию узур (зазубрин) на нижних краях ребер. Данные изменения появляются у пациентов с коарктацией аорты в возрасте старше 15 лет.
Классификация коарктации аорты
С учетом локализации патологического сужения различают коарктацию в области перешейка, восходящей, нисходящей, грудной, брюшной аорты. Некоторые источники выделяют следующие анатомические варианты порока - предуктальный стеноз (сужение аорты проксимальнее впадения ОАП) и постдуктальный стеноз (сужение аорты дисталтнее впадения ОАП).
По критерию множественности аномалий сердца и сосудов А. В. Покровский классифицирует 3 типа коарктации аорты:
- 1 тип - изолированная коарктация аорты (73%);
- 2 тип – сочетание коарктации аорты с ОАП; с артериальным или венозным сбросом крови (5%);
- 3 тип – сочетание коарктации аорты с другими гемодинамически значимыми аномалиями сосудов и ВПС (12%).
В естественном течении коарктации аорты выделяют 5 периодов:
- I (критический период) - у детей до 1 года; характеризуется симптомами недостаточности кровообращения по малому кругу; высокой смертностью от тяжелой сердечно-легочной и почечной недостаточности, особенно при сочетании коарктации аорты с другими ВПС.
- II (приспособительный период) - у детей от 1 до 5 лет; характеризуется уменьшением симптоматики недостаточности кровообращения, которая обычно представлена повышенной утомляемостью и одышкой.
- III (компенсаторный период) – у детей от 5 до 15 лет; характеризуется преимущественно бессимптомным течением.
- IV (период развития относительной декомпенсации) – у пациентов 15-20 лет; в периоде полового созревания нарастают признаки недостаточности кровообращения.
- V (период декомпенсации) – у пациентов 20-40 лет; характеризуется признаками артериальной гипертензии, тяжелой лево- и правожелудочковой сердечной недостаточности, высокой летальностью.
Симптомы коарктации аорты
Клиническая картина коарктации аорты представлена множеством симптомов; проявления и их выраженность зависят от периода течения порока и сопутствующих аномалий, влияющих на внутрисердечную и системную гемодинамику. У детей раннего возраста с коарктацией аорты могут отмечаться задержка роста и увеличения массы тела. Преобладают симптомы левожелудочковой недостаточности: ортопноэ, одышка, сердечная астма, отек легких.
В более старшем возрасте, в связи с развитием легочной гипертензии, характерны жалобы на головокружение, головную боль, сердцебиение, шум в ушах, снижение остроты зрения. При коарктации аорты нередки носовые кровотечения, обмороки, кровохарканье, чувство онемения и зябкости, перемежающаяся хромота, судороги в нижних конечностях, абдоминальные боли, обусловленные ишемией кишечника.
Средняя продолжительность жизни пациентов с коарктацией аорты составляет 30-35 лет, около 40% больных умирают в критическом периоде (возрасте до 1 года). Наиболее частыми причинами летального исхода в периоде декомпенсации служат сердечная недостаточность, септический эндокардит, разрывы аневризм аорты, геморрагический инсульт.
Диагностика коарктации аорты
При осмотре обращает внимание наличие атлетического типа телосложения (преимущественное развитие плечевого пояса при худых нижних конечностях); усиление пульсации сонных и межреберных артерий, ослабление или отсутствие пульсации на бедренных артериях; повышенное АД на верхних конечностях при снижении АД на нижних конечностях; систолический шум над верхушкой и основанием сердца, на сонных артериях и т. д.
В диагностике коарктации аорты решающую роль играют инструментальные исследования: ЭКГ, ЭхоКГ, аортография, рентгенография грудной клетки и рентгенография сердца с контрастированием пищевода, зондирование полостей сердца, вентрикулография и др.
Электрокардиографические данные свидетельствуют за перегрузку и гипертрофию левых и/или правых отделов сердца, ишемические изменения миокарда. Рентгенологическая картина характеризуется кардиомегалией, выбуханием дуги легочной артерии, изменением конфигурации тени дуги аорты, узурацией ребер.
Эхокардиография позволяет непосредственно визуализировать коарктацию аорты и определить степень стеноза. Детям старшего возраста и взрослым может выполняться чреспищеводная ЭхоКГ.
При катетеризации полостей сердца определяется престенотическая гипертензия и постстенотическая гипотензия, снижение парциального давления кислорода в постстенотическом отделе аорты. С помощью восходящей аортографии и левой вентрикулографии обнаруживается стеноз, оценивается его степень и анатомический вариант. Коронарография при коарктации аорты показана в случае наличия эпизодов стенокардии, а также при планировании операции пациентам старше 40 лет для исключения ИБС.
Коарктацию аорты следует дифференцировать от других патологических состояний, протекающих с явлениями легочной гипертензии: вазоренальной и эссенциальной артериальной гипертензии, аортального порока сердца, неспецифического аортита (болезни Такаясу).
Лечение коарктации аорты
При коарктации аорты возникает необходимость в медикаментозной профилактике инфекционного эндокардита, коррекции артериальной гипертензии и сердечной недостаточности. Устранение анатомического порока аорты проводится только оперативным путем.
Кардиохирургическая операция по поводу коарктации аорты осуществляется в ранние сроки (при критическом пороке - до 1 года, в остальных случаях в возрасте от 1 до 3-х лет). Противопоказаниями к хирургическому лечению коарктации аорты служат необратимая степень легочной гипертензии, наличие тяжелой или некорригируемой сопутствующей патологии, терминальная стадия сердечной недостаточности.
Для лечения коарктации аорты в настоящее время предложено следующие типы открытых операций:
- I. Местно-пластическая реконструкция аорты: резекция стенозированного участка аорты с наложением анастомоза «конец в конец»; прямая истмопластика с продольным рассечением стеноза и сшиванием аорты в поперечном направлении; непрямая истмопластика (с использованием лоскута из левой подключичной артерии или синтетической заплаты, с наложением сонно-подключичного анастомоза).
- II.Резекция коарктации аорты с протезированием: с замещением дефекта артериальным гомотрансплантатом или синтетическим протезом.
- III. Создание обходных анастомозов: обходное шунтирование с использованием левой подключичной артерии, селезеночной артерии или гофрированного сосудистого протеза.
При локальном или тандемном стенозе и отсутствии выраженного кальциноза и фиброза в области коарктации выполняется транслюминальная баллонная дилатация аорты. Послеоперационные осложнения могут включать развитие рекоарктации аорты, аневризмы, кровотечения; разрывы анастомозов, тромбозы реконструированных участков аорты; ишемию спинного мозга, ишемическую гангрену левой верхней конечности и др.
Прогноз коарктации аорты
Естественное течение коарктации аорты определяется вариантом сужения аорты, наличием других ВПС и в целом имеет крайне неблагоприятный прогноз. При отсутствии кардиохирургической помощи 40-55% больных погибает на первом году жизни. При своевременном хирургическом лечении коарктации аорты хороших отдаленных результатов удается достичь у 80-95% больных, особенно если операция проведена в возрасте до 10 лет.
Оперированные больные с коарктацие аорты пожизненно находятся под наблюдением кардиолога и кардиохирурга; им рекомендуется ограничение физической активности и нагрузок, регулярные динамические осмотры для исключения послеоперационных осложнений. Исход беременности после реконструктивных операций по поводу коарктации аорты обычно благоприятный. В процессе ведения беременности для профилактики разрыва аорты назначаются гипотензивные средства, проводится профилактика инфекционного эндокардита.
В рожденные пороки сердца (ВПС) — достаточно распространенная патология среди заболеваний сердечно-сосудистой системы, которая является основной причиной смерти детей первого года жизни. Частота ВПС составляет 30% от всех пороков развития. Лечение врожденных сердечных аномалий возможно только хирургическим путем. Благодаря успехам кардиохирургии стали возможны сложные реконструктивные операции при ранее неоперабельных ВПС. В этих уcловиях основной задачей в организации помощи детям с ВПС является своевременная диагностика и оказание квалифицированной помощи в хирургической клинике.
Основными причинами рождения детей с ВПС являются: хромосомные нарушения - 5%; мутация 1-го гена - 2–3%; влияние внешних факторов (алкоголизм родителей, прием лекарственных препаратов, перенесенные вирусные инфекции во время беременности и т.д.) - 1–2% ;полигенно-мультифокальное наследование - 90%.
Классификация
Встречается более 90 вариантов ВПС и множество их сочетаний. В Институте сердечно-сосудистой хирургии им. А.Н. Бакулева АМН СССР была разработана классификация, основанная на распределении ВПС с учетом анатомических особенностей порока и гемодинамических нарушений.
Для практикующих врачей-кардиологов удобнее пользоваться более упрощенным делением ВПС на 3 группы:
1. ВПС бледного типа с артериовенозным шунтом: дефект межжелудочковой перегородки (ДМЖП), дефект межпредсердной перегородки (ДМПП), открытый артериальный проток (ОАП); открытый атриовентрикулярный канал (АВК).
2. ВПС синего типа с веноартериальным шунтом: транспозиция магистральных сосудов (ТМС), тетрада Фалло (ТФ), триада Фалло, атрезия трикуспидального клапана (АТК) и т.д.
3. ВПС без сброса, но с препятствием на пути кровотока из желудочков (стенозы легочной артерии и аорты). Такое деление охватывает 9 наиболее распространенных ВПС.
Нарушение гемодинамики при врожденных пороках сердца
Не случайно во всех предложенных классификациях большое внимание уделено оценке нарушений гемодинамики при ВПС, так как степень этих нарушений тесно связана с анатомической тяжестью порока, от них зависит тактика медикаментозного лечения и сроки выполнения операции.
ВПС вызывает ряд изменений компенсаторного характера, которые заставляют перестраиваться весь организм ребенка, но при длительном существовании порока процессы компенсации ведут к выраженным деструктивным изменениям органов и систем, что приводит к гибели больного.
В зависимости от состояния малого круга кровообращения в организме больного с ВПС наблюдаются следующие патологические изменения:
• при наличии увеличенного кровотока в легких (пороки бледного типа с артериовенозным шунтом) развивается гиперволемия и гипертензия малого круга кровообращения;
• при наличии обедненного кровотока в легких (пороки синего типа с веноартериальным шунтом) у больного развивается гипоксемия;
• при увеличении кровотока в малом круге кровообращения развивается гиперволемия и легочная гипертензия.
Примерно 50% детей первого года жизни с большим сбросом крови в малый круг кровообращения без хирургической помощи погибают при явлениях сердечной недостаточности. Если ребенок переживает этот критический период, то к году в результате спазма легочных артериол уменьшается сброс крови в малый круг и состояние ребенка стабилизируется, однако это улучшение касается только самочувствия больного, так как одновременно начинают развиваться склеротические процессы в сосудах легких. Существует много классификаций легочной гипертензии. Для практики наиболее удобной является классификация, разработанная в ИССХ им. А. Н. Бакулева АМН СССР (В.И. Бураковский и соавт., 1975). Она основана на величине давления в легочной артерии, степени сброса крови и соотношении общелегочного сопротивления к показателям большого круга кровообращения (табл. 1).
Согласно этой классификации, больные делятся на 4 группы, где I и III стадия разделены на подгруппы А и Б. Больные IА группы имеют небольшие нарушения гемодинамики и нуждаются в наблюдении кардиолога. У больных IБ и II группы ставится вопрос об операции. Легочная гипертензия в этих группах носит функциональный характер.
У больных III группы при большом сбросе крови в малый круг изменения в легочных сосудах значительно более выражены. При IIIА гемодинамической группе возможна радикальная коррекция порока, и давление после операции снижается. В IIIБ и IV группе хирургическое лечение не показано. Дифференциальный диагноз между IIIА и Б группами сложен, и нередко для решения вопроса об операбельности порока необходимо выполнить внутрисосудистое ультразвуковое исследование и/или биопсию легкого для изучения морфологических изменений в легочных сосудах. Для оценки этих изменений наиболее часто используется классификация, предложенная Д. Хитом и Дж. Эдвардсом в 1958 г. (табл. 2).
При цианотических формах ВПС наличие сброса венозной крови в артериальную или смешение крови ведут к увеличению объема крови в большом круге кровообращения и уменьшению в малом, что приводит к снижению насыщения крови кислородом (гипоксемии) и к появлению цианоза кожи и слизистых. Для улучшения доставки кислорода к органам и повышения эффективности вентиляции происходит развитие коллатерального кровообращения между сосудами большого и малого круга кровообращения. Перестройка коллатеральной сети кровообращения происходит в сосудах всех органов. Особенно это выражено в сосудах сердца, легких и головного мозга.
Благодаря компенсаторным механизмам состояние больного с цианотическими формами ВПС, несмотря на тяжелые нарушения гемодинамики, может быть длительно удовлетворительным, но постепенно компенсаторные механизмы истощаются, длительная гиперфункция миокарда приводит к развитию тяжелых необратимых дистрофических изменений в сердечной мышце. Поэтому оперативное вмешательство при цианотических пороках (радикальное или паллиативное) показано в самом раннем детском возрасте.
Диагностика
Первичная диагностика ВПС основывается на данных неинвазивных методов исследования. Большое значение для диагностики имеет целенаправленный сбор анамнеза у родителей ребенка. При бледных пороках сердца необходимо выяснить, часто ли болеет ребенок респираторными инфекциями, были ли у него пневмонии, так как это говорит о большом сбросе крови слева-направо. С другой стороны, прекращение респираторных инфекций у больного с большим сбросом крови в малый круг говорит о начале развития легочной гипертензии. Это должно быть поводом для направления больного к кардиохирургу. Естественное течение ВПС может осложниться развитием инфекционного эндокардита, поэтому необходимо выяснить, бывают ли у ребенка подъемы температуры тела без признаков респираторной инфекции. Следует также выяснить, не было ли у больного синкопальных состояний, судорожного синдрома, которые могут быть следствием аритмий сердца.
При осмотре ребенка с подозрением на ВПС необходимо отметить цвет кожных покровов и слизистых. Цианоз может быть периферическим и генерализованным. Важно отметить наличие или отсутствие цианоза на всех 4 конечностях, так как при некоторых ВПС наблюдается дифференцированный цианоз (предуктальная коарктация аорты, транспозиции магистральных сосудов в сочетании с перерывом дуги аорты). При осмотре грудной клетки необходимо отметить деформацию грудной клетки в области сердца — появление так называемого сердечного горба (по величине и локализации которого можно косвенно судить о сложности ВПС и/или развитии легочной гипертензии).
При пальпации грудной клетки у больного с ВПС можно отметить смещение верхушечного толчка, изменение его площади, наличие “дрожания” над областью сердца. Пальпация позволяет оценить размеры печени и селезенки. Методом перкуссии определяют размеры сердца, печени и селезенки.
Аускультация является наиболее информативным методом физикального обследования больных с ВПС. При аускультации можно отметить изменение тонов сердца (усиление, ослабление или расщепление), появление шумов, а также их локализацию, иррадиацию и место максимального выслушивания. Интенсивность шума не всегда коррелирует с тяжестью порока, например, при ВПС с легочной гипертензией и синих пороках со стенозом легочной артерии эта зависимость носит обратный характер. При аускультации легких можно выявмть признаки застоя в малом круге.
Физикальное исследование дополняется проведением неинвазивного инструментального обследования, которое включает электрокардиографию (ЭКГ), фонокардиографию (ФКГ) и рентгенографию органов грудной клетки.
ЭКГ позволяет судить о гипертрофии различных отделов сердца, патологических отклонениях электрической оси, наличии нарушений ритма и проводимости. Изменения на ЭКГ не являются специфичными для какого-либо порока, но в сочетании с данными, полученными при клиническом обследовании и с помощью других неинвазивных методов, позволяют судить о тяжести порока. Разновидностью метода ЭКГ является холтеровское суточное ЭКГ-мониторирование, которое помогает выявить скрытые нарушения ритма и проводимости.
Следующим неинвазивным методом обследования кардиологических больных является ФКГ, которая воспроизводит данные аускультации сердца и позволяет более детально и количественно оценить характер, продолжительность и локализацию сердечных тонов и шумов.
Рентгенография органов грудной клетки дополняет предыдущие методы и позволяет оценить: состояние малого круга кровообращения (наличие артериального или венозного застоя, снижение наполнения сосудов легких); расположение, форму, размеры сердца и его отдельных камер; изменения со стороны других органов и систем (легкие, плевра, позвоночник, а также расположение внутренних органов).
Сочетание ЭКГ, ФКГ и рентгенография органов грудной клетки позволяет диагностировать большинство изолированных пороков и предположить наличие сложных ВПС.
Наиболее высокоинформативным неинвазивным методом исследования является эхокардиография (ЭХОКГ). С появлением данной методики, особенно двухмерной ЭХОКГ, значительно расширились возможности диагностики ВПС. Этот метод позволяет провести анатомически точную диагностику дефектов перегородок сердца, поражения атриовентрикулярных и полулунных клапанов, размеры и расположение камер сердца и магистральных сосудов, а также оценить сократительную способность миокарда. При определенных пороках (неосложненные ДМПП, ДМЖП, ОАП, частично открытый АВК, коарктация аорты) можно выполнить операцию без проведения катетеризации сердца. Однако в ряде случаев при сложных ВПС и сопутствующей легочной гипертензии необходимо провести катетеризацию сердца и ангиокардиографию, так как эти методы позволяют провести точную анатомическую и гемодинамическую диагностику ВПС. Проведение катетеризации сердца возможно только в условиях специализированной кардиохирургической клиники. В настоящее время при проведении катетеризации сердца в случае необходимости выполняется электрофизиологическое исследование для уточнения механизма аритмий сердца, оценки функции синусового и атриовентрикулярного узлов, а также проводятся различные эндоваскулярные операции: баллонная ангиопластика при стенозах легочной артерии и аорты; эмболизация небольших ОАП, коронаросердечных фистул, аортолегочных коллатералей; баллонная атриосептостомия при простой ТМС и стентирование легочных сосудов при периферических стенозах.
Тактика хирургического лечения
Тактика оказания помощи больным с ВПС строится с учетом течения порока, эффективности консервативного лечения, возможности и риска проведения хирургического лечения. После установления диагноза необходимо решить:
1. Как лечить больного (медикаментозно или хирургически)?
2. Определить сроки выполнения операции.
Ответить на эти вопросы помогает классификация, предложенная J. Kirklin и соавт. (1984).
0-я группа – больные с ВПС, с незначительными нарушениями гемодинамики, которые не нуждаются в операции.
1-я группа – больные, состояние которых позволяет провести операцию в плановом порядке ( через год и более).
2-я группа – больные, которым операция показана в ближайшие 3–6 мес.
3-я группа – больные с тяжелыми проявлениями ВПС, которых необходимо оперировать в течение нескольких недель.
4-я группа – больные, нуждающиеся в экстренной операции (в течение 48 ч после госпитализации).
Наиболее сложная проблема в кардиохирургии – операция у детей первого года жизни с ВПС. Хирургическая летальность в последние годы значительно снижена и отличается от высокой естественной смертности при ВПС. Операция у детей первого года жизни выполняется в том случае, если консервативными методами не удается достичь стабилизации состояния. Большинство неотложных операций выполняются у детей с цианотическими ВПС.
Если у новорожденного с ВПС отсутствуют признаки сердечной недостаточности, цианоз выражен умеренно, то консультация кардиохирурга может быть проведена позднее. Наблюдение за такими детьми осуществляет кардиолог по месту жительства. Такая тактика позволяет провести обследование больного в более благоприятных условиях, снизить риск проведения инвазивных методов исследования и оперативного вмешательства.
В более поздней возрастной группе хирургическая тактика при ВПС зависит от тяжести патологии, предполагаемого прогноза, возраста и массы тела больного. K.Turley и соавт. в 1980 г. предложили разделить ВПС на 3 группы, в зависимости от вида возможной операции.
К 1-й группе относятся такие наиболее часто встречающиеся пороки, как ОАП, ДМЖП, ДМПП, частично открытый АВК, коарктация аорты, стеноз и недостаточность митрального и аортального клапанов. При установлении данных пороков единственным выбором может быть операция. Она может быть отложена, если нарушения гемодинамики нерезко выражены, а возраст ребенка и масса тела слишком малы (более поздний возраст и достаточная масса тела снижают риск выполнения кардиохирургических вмешательств).
Во 2-ю группу входят сложные цианотические пороки, такие, как тетрада Фалло, стеноз легочной артерии, атрезия легочной артерии 1-го типа, транспозиция магистральных сосудов и др. Выбор между радикальной и паллиативной операцией зависит от анатомической тяжести порока, степени гипоксемии и массы тела ребенка.
К 3-й группе относятся ВПС, при которых возможна только паллиативная или гемодинамическая коррекция порока. К ней относятся различные варианты сложных пороков: атрезия трикуспидального и митрального клапанов, двухкамерное сердце, синдром гипоплазии правого и левого сердца, единственный желудочек сердца и др.
Радикальная коррекция простых неосложненных пороков не представляет технических трудностей для специализированной кардиохирургической клиники. При ДМЖП и ДМПП выполняется ушивание или пластика дефектов заплатой, при ОАП - перевязка или пересечение протока. При выраженной гипоксемии первым этапом у больного с ВПС проводится паллиативная операция - наложение различных межсистемных анастомозов. После проведения операции улучшается насыщение крови кислородом, что позволяет ребенку развиваться в более благоприятных условиях. Выполнение двухэтапных операций, по данным различных авторов, не только не увеличивает риск вмешательства, но уменьшает летальность при радикальной коррекции.
При некоторых анатомически сложных ВПС, когда отсутствуют или недоразвиты различные отделы сердца (атрезия трикуспидального и митрального клапанов, единственный желудочек сердца, двухкамерное сердце и т.д.) выполнение радикальной операции не представляется возможным и единственной операцией может быть гемодинамическая коррекция внутрисердечной гемодинамики, которая позволяет разделить артериальные и венозные потоки крови, не устраняя полностью анатомические пороки. К ним относятся различные модификации гемодинамической коррекции по методу Фонтена, Мастарда и Сенинга.
1. Бураковский В.И., Бухарин В.А. Константинов С.А. и др. Врожденные пороки сердца. В кн. Частная хирургия болезней сердца и сосудов / Под ред. В.И. Бураковского и С.А.Колесникова. М.: Медицина, 1967; 315—23.
2. Бураковский В.И., Бухарин В.А., Плотникова Л.Р. Легочная гипертензия при врожденных пороках сердца. М. Медицина, 1975; 247.
3. Амосов Н.М., Бендет Я.А. Терапевтические аспекты кардиохирургии. Киев: Здоровье, 1983; 33—96.
4. Белоконь Н.А., Кубергер М.Б. Болезни сердца и сосудов у детей. Руководство для врачей. В 2 томах. — М. Медицина, 1987; 918.
5. Бураковский В.А., Бухарин В.А., Подзолков В.П. и др. Врожденные пороки сердца. В кн. Сердечно-сосудистая хирургия / Под ред. В.И. Бураковского, Л.А. Бокерия. М. Медицина, 1989; 345—82.
6. Иваницкий А.В., Роль рентгенологического исследования в диагностике пороков сердца у детей. Педиатрия. 1985; 8 (7) 55—7.
7. Н.А.Белоконь, В.П. Подзолков. Врожденные пороки сердца. М. Медицина, 1991; 352.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Читайте также:
