Лечение посттравматической эмпиемы плевры - методы
Добавил пользователь Владимир З. Обновлено: 10.01.2026
Лечение посттравматической эмпиемы плевры - методы
Центральное место в комплексном лечении эмпиемы плевры занимает ранняя и полноценная санация всей плевральной полости, что бывает не так часто, или чаще — ограниченных гнойных полостей. При обнаружении очага гнойной инфекции под контролем УЗИ намечают точку наиболее безопасного и эффективного дренирования и устанавливают в этот очаг двухпросветную силиконовую трубку ТММК 8 мм, несущую 2-3 боковых отверстия, равных диаметру трубки.
В наших наблюдениях в остром периоде развития эмпиемы плевры всем пострадавшим выполняли дренирование плевральной полости с фракционным промыванием и аспирацией содержимого. Видеоторакоскопическая санация полости плевры произведена у 4 пациентов. Показанием к торакотомии, выполненной в трех наблюдениях в остром периоде нагноения, был большого объема свернувшийся гемоторакс спустя 3-4 нед. после ранения, однако на операции были установлены признаки нагноения гемоторакса, что потребовало выполнения плеврэктомии и декортикации легкого.
Показания к операции в срок от 30 до 90 сут установлены лишь у 4 пострадавших (3,8%): в одном наблюдении причиной хронизации гнойного процесса служило инородное тело в полости эмпиемы, в остальных трех — респираторно-плевральные свищи.
Из них у одного пациента со свищом левого главного бронха после пневмонэктомии по поводу огнестрельного ранения корня левого легкого поэтапно выполнена трансстернальная трансперикардиальная окклюзия главного бронха с последующей плеврэктомией и торакопластикой; у другого пострадавшего — торакотомия, плеврэктомия и атипичная резекция легкого; у третьего пациента с трахеоплевральным свищом после цервикоторакального ранения произведена чресшейная медиастинотомия, разобщение свища с использованием грудино-ключично-сосцевидной мышцы. При лечении эмпиемы плевры с бронхоплевральными свищами у 4 пациентов выполнена временная окклюзия бронхов III—IV порядка, а у 2 — торакоскопическая коагуляция свища в полости эмпиемы. Адекватное дренирование полости эмпиемы оказалось достаточным для выздоровления других 5 пациентов с бронхоплевральными свищами, однако продолжительность лечения при этом была в 1,5 раза выше, чем у пострадавших с неосложненной эмпиемой плевры.
Длительность дренирования в среднем составила 27+3,4 дня. Крайне редко, в случаях длительно существующих бронхоплевральных свищей и эмпиемы плевры, когда развивается цирроз доли легкого, и она становится неспособной к расправлению, полости, оставшиеся после плеврэктомии и декортикации, заполняют мышечной тканью на сосудистой ножке. В передних отделах плевральной полости используют большую грудную мышцу, в боковых и задних отделах — переднюю зубчатую мышцу, или широчайшую мышцу спины [Regnard J. F. et al.]|.
С учетом недостаточности фагоцитарного и В-клеточного звеньев иммунной системы, выявленной нами у пострадавших с гнойными осложнениями ранений груди [Абакумов М.М., Булава Г.В.], в комплексном лечении посттравматичекой эмпиемы плевры резко возрастает роль иммунной и детоксикационной терапии.
При наличии фебрильной температуры тела, лейкоцитоза с палочкоядерным сдвигом, высокой СОЭ, 2-3-кратпого повышения уровня циркулирующих иммунных комплексов (ЦИК) на фоне гиперактивации кислородного метаболизма нейтрофилов и существенного дефицита лимфоцитов, необходимо проведение последовательной комплексной инфузионной, трансфузионной и иммунотерапии после дренирования эмпиемы плевры в следующей последовательности:
1) реополиглюкин 400 мл внутривенно (для уменьшения агрегации форменных элементов крови);
2) гемодез 200 мл внутривенно для связывания и выведения токсических веществ;
3) сбалансированные солевые растворы в объеме 1-1,5 л для поддержания реологических свойств крови, увеличения диуреза;
4) свежезамороженную плазму и альбумин для поддержания онкотического давления и детоксикации.
При ареактивном течении эмпиемы наблюдается нормальная или субфебрильная температура, нормальное число лейкоцитов без иалочкоядерного сдвига, лимфопения с преимущественным дефицитом В-лимфоцитов, снижение количества фагоцитирующих нейтрофилов на фоне многократного повышения уровня циркулирующих иммунных компонентов. В таких случаях мы используем внутривенное введение лейкина на протяжении 3-5 дней (ежедневно или через день) в дозе 50-100 мг/кг массы тела.
Препарат растворяют в 400 мл изотонического раствора хлорида натрия и вводят внутривенно в течение 1,5-2 ч Для предупреждения возможной гипертермической реакции за 30 мин до вливания целесообразно подкожно ввести нестероидный противовоспалительный препарат (диклофенак, индометацин).
Летальность при эмпиеме плевры наблюдалась только в остром периоде воспаления (7-32-е сутки после травмы) и составила 13,3% (15 наблюдений из 105). Формирование остаточной сухой полости отмечено у 2 из 90 выживших пострадавших с эмпиемой плевры (2,2%), один пациент переведен в туберкулезный стационар в связи с выявленной активной формой легочного туберкулеза.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лечение свернувшегося гемоторакса - методы
Главной задачей любого метода лечения свернувшегося гемоторакса является ранняя и полная эвакуация патологического содержимого из плевральной полости. Методы лечения свернувшегося гемоторакса представлены в таблице, из которой следует, что у значительной части пострадавших лечение заключалось только в эвакуации жидкостной фракции путем пункции или дренирования плевральной полости на фоне антибактериальной терапии. Как правило, это были пациенты пожилого и старческого возраста, страдающие тяжелыми сопутствующими заболеваниями, с локальной формой свернувшегося гемоторакса и без явлений дыхательной недостаточности.
В этой группе пострадавших формировался ограниченный фиброторакс в результате организации плотной части свернувшегося гемоторакса.
Следует подчеркнуть, что наиболее трудной для диагностики и лечения была фрагментарная форма свернувшегося гемоторакса, поскольку метод УЗИ для визуализации парамедиастинальной и междолевой локализации свертков крови малоинформативен, равно как и для дренирования этих зон под контролем УЗИ. В такой ситуации методом выбора является диагностическая и лечебная видеоторакоскопия, однако ее применение требовало общего обезболивания с раздельной интубацией бронхов, поэтому даже в ранние сроки се выполнение проблематично при наличии пневмонии и гнойного трахеобронхита. В поздние сроки (через 2-3 нед. после травмы) торакоскопия малоэффективна и опасна из-за наличия плотных легочно-плевральных сращений.
По мере накопления опыта в публикациях последних десятилетий возможности торакоскопического вмешательства стали оценивать более сдержанно. В частности, М. A. Rashid отметил опасность выполнения торакоскопических манипуляций при субплевральной гематоме, которую трудно дифференцировать от свернувшегося гемоторакса. Считается, что наилучшим для проведения эффективной торакосконической эвакуации свернувшегося гемоторакса является период со 2-х по 6-е сутки после ранения, так как позже этого срока образуются плотные сращения, которые препятствуют полной ревизии и эвакуации содержимого [Landcrnan R. L. et al.].
Методы лечения свернувшегося гемоторакса
| Методы лечения | % |
| Пункция и дренирование плевральной полости | 40,5 |
| Введение стрептазы | 16 |
| Торакоскопия | 8,5 |
| Торакотомия, плеврэктомия, декортикация | 21,7 |
| Консервативное ведение | 13,3 |
| Всего | 100% |
Однако следует признать, что срок в 2 сут после ранения является слишком ранним для применения торакоскопии, так как свернувшийся гемоторакс возникает обычно не ранее 4-5-х суток после ранения, а следовательно, в первые 3 сут для эвакуации гемоторакса достаточно дополнительного дренирования плевральной полости или просто смены дренажа.
Массивный свернувшийся гемоторакс (более 1500 см 3 ) является жизненным показанием к операции, независимо от стадии его формирования. Неэффективность или частичная эффективность торакоскопии, местного применения фибринолитических препаратов служат показанием к выполнению в срок от 15 до 20 сут после образования свернувшегося гемоторакса торакотомии, если объем свернувшегося гемоторакса превышает 300-500 см3, а следовательно, отрицательным образом сказывается на функции дыхания и является потенциальной причиной развития эмпиемы плевры.
Для выполнения такого рода операции необходимы большой опыт работы хирурга в торакальном отделении, тщательное выполнение аэростаза и контроль за функционированием плевральных дренажей, подключенных к аспирационной системе.
Если операцию производят в поздние сроки, воспалительно измененную париетальную плевру также необходимо удалять для того, чтобы обеспечить прочное слипание ткани легкого с грудной стенкой и предотвратить развитие осумкованных гнойных полостей. Операция заканчивается санацией плевральной полости и установкой дренажей. Дренирование плевральной полости производится в типичном месте — по заднеподмышечной линии в восьмом межреберье.
При нарушении целости легкого следует установить дополнительный дренаж во втором межреберье по среднеключичной линии. Торакотомную рану ушивают с соблюдением принципов асептики.
Необходимо еще раз подчеркнуть, что торакотомия, декортикация легкого и плеврэктомия (даже частичная) являются чрезвычайно травматичными вмешательствами и по возможности их следует избегать, применяя менее агрессивные методы лечения на ранних этапах.
В последнее десятилетие используем видеоассистированную миниторакотомию, которая сочетает в себе достоинства миниинвазивной технологии и возможности мануального разделения плотных сращений с удалением фибрина в стадии организации [Villavincencio R. Т. et al., Eckerberger F.].
Наш опыт насчитывает 25 наблюдений применения классической торакотомии с декортикацией и плеврэктомией и 16 наблюдений видеоассистированной торакотомии. Умерших не было.
В послеоперационном периоде основное внимание должно быть уделено состоянию плевральной полости. Необходим ежедневный контроль за функционированием дренажей, в первые 3-4 сут — контрольные УЗИ. При необходимости данные УЗИ могут быть дополнены и сопоставлены с результатами рентгенологического исследования.
Анализ результатов применения этих препаратов показал, что наиболее эффективным из них является стрептаза (стрептокиназа) — фибринолитический препарат, который способствует превращению плазминогена в плазмин, разрушающий фибрин, фибриноген и некоторые другие белки плазмы крови. При внутривенной инфузии стреитокиназы фибринолитический эффект наблюдается только в течение нескольких часов, однако удлинение тромбинового времени может сохраняться до 24 ч, вследствие одновременного снижения уровня фибриногена и увеличения количества циркулирующих продуктов деградации фибрина и фибриногена. При введении в плевральную полость влияния препарата на свертывающую систему крови не зафиксировано.
В то же время внутриплевральное введение стрептокиназы нередко приводит к сильной боли в груди и гипертермии. Редкие наблюдения острого респираторного дистресс-синдрома, возникающего при введении препарата, некоторые авторы связывают со специфическим анафилактическим действием продуктов фибринолиза на сосуды малого круга кровообращения [Luterman A. et al., Kexstein M. D. et al., Frye D.D. et al.]. Раннее применение стрептокиназы может привести к вторичному кровотечению в плевральную полость [Godley J. P. et al.]. Оптимальным временем применения химического фибринолиза являются сроки от 4 до 10 сут после образования свернувшегося гемоторакса.
В наших 17 наблюдениях мы использовали следующую методику. Порошок стреитазы (стрептокиназы) в дозе 750 тыс. ЕД растворяли в 50 мл изотонического раствора хлорида натрия, добавляли к нему 50 мл 2 % раствора новокаина и вводили через дренаж плевральной полости, стоящий непосредственно в зоне формирования свернувшегося гемоторакса. Так как от локализации дренажной трубки напрямую зависит эффективность введения препарата, ее положение должно быть четко определено и, если нужно, исправлено под контролем УЗИ или КТ.

Для внутриплеврального тромболизиса необходимо использовать стандартную дренажную трубку диаметром не менее 6 мм, так как трубки малого диаметра (Pigtail) не обеспечат надежной эвакуации содержимого плевральной полости после экспозиции препарата, что чревато всасыванием продуктов деградации сгустков и фибрина с гипертермией и эндотоксикозом.
После введения препарата дренаж мы пережимали с экспозицией от 4 до 9 ч, в зависимости от переносимости этой процедуры. Для лучшего контакта лизирующего раствора с тромботическими массами пациент по возможности должен менять свое положение в постели.
По окончании экспозиции дренаж плевральной полости подключали к системе аспирации с разрежением 20-30 см водн. ст. Как правило, одномоментно выделялось от 300 до 1000 мл геморрагического содержимого, после чего выполняли КТ. Если в плевральной полости оставалось плотное содержимое объемом не более 100-150 см3, тромболизис считали завершенным и через 24-48 ч удаляли дренаж. У подавляющего большинства пациентов введение стрептазы было выполнено однократно.
Несмотря на то что мы применяли достаточно высокую дозировку препарата (750 тыс. ЕД против рекомендуемых В. J. Kimbrell и соавт. 250 тыс. ЕД), мы не наблюдали таких осложнений, как вторичное кровотечение, аллергическая реакция. Показатели коагулологии (MHO, протромбиновое время) были в пределах нормы. Примерно 20 % пациентов имели болевые ощущения, максимальные при введении препарата. При использовании раствора новокаина введение было практически безболезненным. Эффективность метода наблюдалась в 87%.
Наличие у 2 пациентов ушитых ран сердца, у 3 — печени, в том числе с наличием под швами гематом (по данным УЗИ и КТ), у 1 — травматического субарахноидального кровоизлияния и у 4 пострадавших пожилого и старческого возраста — последствий нарушения мозгового кровообращения, хронической почечной недостаточности — мы посчитали противопоказанием к применению этого мощного фибринолитического препарата. Противопоказанием является также наличие гастродуоденального кровотечения язвенного или стрессового генеза, геморрагического цистита, беременности.
Всего из 102 больных со свернувшимся гемотораксом умерли 3 (2,9%): одна больная 71 года — от инфаркта миокарда, одна больная 62 лет — от повторного нарушения мозгового кровообращения и один больной 41 года -от сердечной недостаточности на фоне алкогольной кардиомиопатии. Непосредственной связи со свернувшимся гемотораксом летальные исходы не имели.
Таким образом, нами установлено, что причиной свернувшегося гемоторакса после проникающего ранения груди чаще всего является позднее обращение за медицинской помощью и неполноценное дренирование плевральной полости при гемотораксе.
При рентгенологическом исследовании грудной клетки можно только заподозрить свернувшейся гемоторакс. Его наличие подтверждается пункцией плевральной полости. Ультразвуковой метод, являясь неинвазивным, позволяет подтвердить данные рентгенологического исследования, а также осуществлять динамический контроль за состоянием плевральной полости в процессе лечения. Наиболее полноценную информацию, позволяющую выбрать оптимальную лечебную тактику, дает КТ.
В лечение свернувшегося гемоторакса необходимо использовать различные методы в зависимости от состояния пациента, стадии формирования свернувшегося гемоторакса и его объема. Каждый метод имеет ограниченные показания и не является универсальным.
Наряду с мероприятиями, направленными на ликвидацию свернувшегося гемоторакса, и местным лечением его осложнений, комплексное лечение больных должно включать:
1) антибактериальную терапию с применением антибиотиков «легочно-плеврального» спектра действия, а при возникновении гнойных осложнений — с учетом чувствительности выделенных возбудителей;
2) бронхолитические и муколитические препараты, улучшающие дренажную функцию бронхов;
3) неспецифическую и специфическую иммунную терапию.
Накопленный опыт свидетельствует о существенном улучшении результатов лечения больных со свернувшимся гемотораксом при использовании иммунотропных препаратов. Необходимость включения иммунотерапии в комплекс лечебных мероприятий определяется глубиной, направленностью и продолжительностью нарушений иммунного гомеостаза с учетом стадий развития свернувшегося гемоторакса. На стадии формирования свернувшегося гемоторакса применение иммунотропных препаратов является, по сути, профилактическим и преследует цель ускорения процесса иммунореабилитации после травмы и кровонотери.
Относительное число пострадавших, нуждающихся в эти сроки в применении иммунопрепаратов, возрастает по мере увеличения объема острой кровопотери с 24% (кровопотеря в пределах 1500 мл) до 78% (кровопотеря более 3000 мл). Раньше и интенсивнее под влиянием травмы и операции понижается функциональная активность Т-лимфоцитов, что часто сочетается со снижением фагоцитарной активности нейтрофилов, а в случаях массивной кровопотери — и уровня иммуноглобулинов. Это состояние может сохраняться до 28 сут и способствовать развитию гнойного процесса в полости плевры.
Эффективным в эти сроки является применение тимических препаратов или миелопидов в сочетании с донорским нативным или антистафилококковым иммуноглобулином для внутримышечного введения на фоне инфузионно-трансфузионной терапии, объём и качество которой определяются общим состоянием больного. Тактивин или тимоген вводят подкожно ежедневно в течение 5 дней в дозах 10 мкг, а миелопид — по 3-6 мг внутримышечно или подкожно во второй половине дня. Иммуноглобулин для внутримышечного введения назначают ежедневно по 3 мл в течение 3-5 дней. Наиболее прогностически неблагоприятным иммунологическим признаком в плане развития нагноения является продолжающаяся лимфопения с дефицитом основных популяций и дисбалансом субпоиуляций Т-лимфоцитов на фоне снижения резервного бактерицидного потенциала фагоцитирующих клеток по результатам НСТ-теста.
Отсутствие положительной динамики иммунограммы в течение 2 нед. после травмы или операции у пострадавших, не имеющих признаков нагноения, является показанием к проведению иммунотерапии. Наиболее эффективно применение миелопида, в состав которого входят несколько пептидов, обладающих разнонаправленными биологическими функциями (МП-1 усиливает активность Т-хелперов, МП-3 стимулирует активность фагоцитарного звена). Миелопид применяют подкожно или внутримышечно по 6 мг (2 ампулы) ежедневно в течение 5 сут в комплексе с антибиотиками.
Посттравматическая эмпиема плевры - причины, диагностика
В наблюдениях среди гнойных осложнений ранений груди превалирует эмпиема плевры. Известно, что общим свойством серозных оболочек является усиление выделения клетками серозной жидкости в ответ на механическое воздействие или воспаление. Наиболее реактивными в этом смысле являются листки плевры и перикарда. Провоцирующими факторами являются длительная экспозиция крови и воздуха в плевральной полости.
Таким образом, посттравматическая реакция плевральных листков в виде экссудации и выпадения фибрина является закономерной. Небольшое количество экссудата, располагающегося в костодиафрагмальных синусах, вскоре подвергается частично всасыванию, частично организации и нередко остается незамеченным. При накоплении большого объема и блокировании всасывания вследствие воспаления возникает необходимость удаления жидкости путем плевральных пункций, как правило, многократных. В таких случаях речь идет о посттравматическом серозном плеврите, частота которого после проникающих ранений груди достигает 2,5%. Посевы экссудата стерильны, он содержит большое количество белка.
Установить на ранних стадиях факт трансформации серозного экссудативного плеврита в гнойный не всегда удается [Лукомский Г. И., Sunder-Plassman L.]. В наших наблюдениях нагноение серозного плеврита удалось констатировать лишь в 8 наблюдениях (4,3% от числа пациентов с экссудативным посттравматическим плевритом).
По данным других авторов, эмпиема плевры встречается в 0,4-15,2% наблюдений проникающих ранений груди, уровень летальности колеблется от 5 до 30% [Королев Б. А., Тевит Б.М., Лыткин М.И. и др., Авилова О. М., Гетьман В.Г., Бисенков Л.Н., Зубарев П. Н., Aguilar M.M. et al., Mandal А. К. et al., Richardson J. D. et al.].
Установлено, что основными причинами развития эмпиемы плевры при изолированных и сочетанных ранениях груди являются:
1) массивная кровопотеря;
2) длительно существующий свернувшийся гемоторакс;
3) длительное спадение легкого, связанное с повреждением его паренхимы, остаточным пневмотораксом, наличием бронхоплевралыюго свища;
4) наличие в легком и в плевральной полости инородных тел (включая дренажные трубки);
5) повреждения органов пищеварительного тракта (пищевод — при ранениях груди, органы брюшной полости — при сочетанных ранениях);
6) гнойные процессы в грудной стенке (нагноение ран, флегмона, остеомиелит).
Редким осложнением является образование гантелеобразной гнойной полости справа, верхняя часть которой представляет собой ограниченную эмпиему плевры, а нижняя часть — плоской формы поддиафрагмальный абсцесс. Такое гнойное осложнение встречается при нераспознанном правостороннем торакоабдоминальном ранении. При повреждении желчных протоков в отрогах этой полости может содержаться гнойная желчь. М.М. Абакумов за много лет располагает всего двумя такими наблюдениями. Оба пострадавших были переведены в поздние сроки из других лечебных учреждений России (1) и бывшей советской республики (1), нами оперированы и выздоровели.
В диссертационной работе Ш. Н. Даниеляна, основанной на анализе 57 пациентов с эмпиемой плевры после ранений груди, установлено, что основными факторами, способствующими развитию этого осложнения, являются: массивная кровопотеря, а также длительная экспозиция патологического содержимого в плевральной полости в результате позднего обращения пострадавших или в результате неэффективного дренирования плевральной полости, что приводит к возникновению свернувшегося гемоторакса или затяжному течению экссудативного плеврита.
Э.А. Нечаев и соавт. считают одной из причин возникновения эмпиемы плевры использование тонких дренажных трубок для дренирования плевральной полости и отсутствие контроля за их функционированием. Известно, что кровь, оставшаяся в плевральной полости в результате неполноценного дренирования, является контаминированной, что в 4-5% случаев приводит сначала к свернувшемуся гемотораксу и затем — к эмпиеме плевры [Eddy A.S. et al., Etoch S.W. et al.].
В наших наблюдениях в течение первой недели послеоперационного периода эмпиема плевры возникла у 18 пациентов с инфицированием плевральной полости содержимым желудочно-кишечного тракта при торакоабдоминальном ранении (что составило 8% от числа всех гнойных осложнений) и у 42 пострадавших с первичным инфицированием ран при проникающих ранениях груди на фоне кровопотери (18,7%).
Вторичное инфицирование плевральной полости в более поздние сроки отмечено у 29 пациентов со свернувшимся гемотораксом (12,9% от числа всех гнойных осложнений), у 40 пациентов с неоднократным и неэффективным дренированием плевральной полости (17,9 %) и у 19 — с дренированием плевральной полости на протяжении более 7 сут (8,5%). При этом необходимо подчеркнуть, что у всех этих пациентов имелась кровопотеря более 1000 мл.
Посттравматическая эмпиема плевры в большинстве наблюдений является следствием длительно протекающих процессов и не может развиться внезапно. Поэтому изложение в руководствах острого начала с высокой температурой тела, ознобами, потливостью, бледностью кожного покрова, цианозом слизистых оболочек, одышкой и тахикардией свидетельствует о поздней диагностике эмпиемы плевры, когда в плевральной полости имеется не менее 1 л гноя.
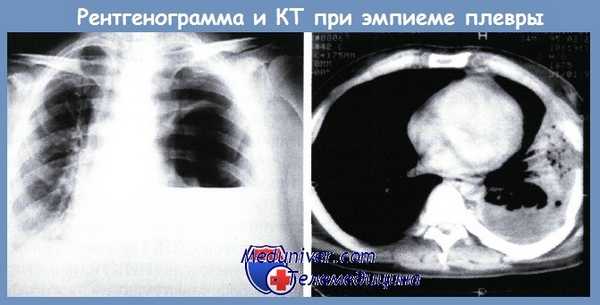
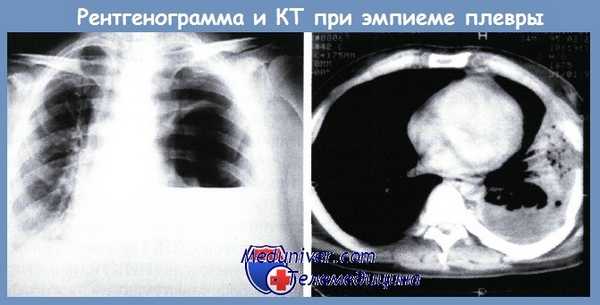
В таких случаях на обзорной рентгенограмме груди в плевральной полости четко виден горизонтальный уровень жидкости.
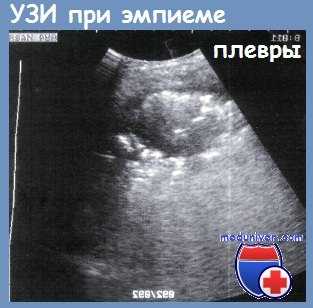
В настоящее время возможности ранней диагностики эмпиемы плевры в значительной мере расширились благодаря применению методов ультразвуковой диагностики и спиральной компьютерной томографии. При УЗИ в плевральной полости определяется эхогенное содержимое с плотными включениями, листки плевры утолщены.
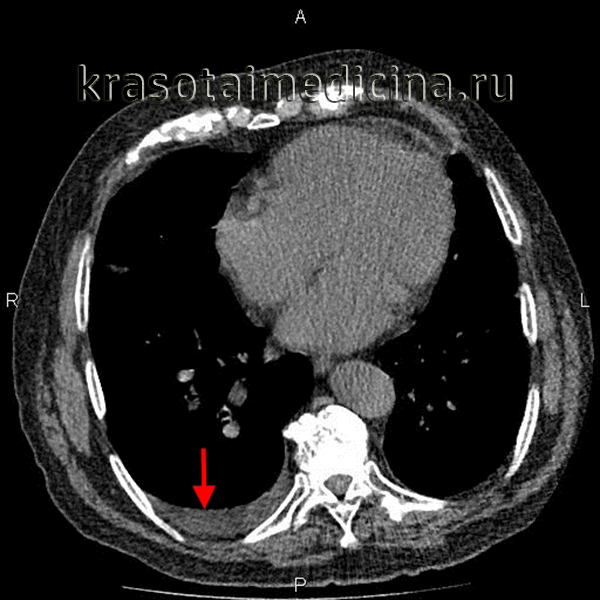
Эмпиема плевры на КТ выглядит как зона плотностью жидкости линзовидной или серповидной формы с четкими границами и с неоднородной структурой за счет участков мягкотканной плотности (фибрин) и плотностью газа. Газ может выявляться как в виде скопления над горизонтальным уровнем жидкости, так и в виде мелких пузырьков. Однако необходимо помнить, что пузырьки газа могут быть не только при эмпиеме плевры, но и без нагноения экссудата, вследствие предшествующих пункций плевральной полости или ее дренирования.
Эмпиема плевры ( Гнойный плеврит , Пиоторакс )
Эмпиема плевры – это воспаление плевральных листков, сопровождающееся образованием гнойного экссудата в плевральной полости. Эмпиема плевры протекает с ознобами, стойко высокой или гектической температурой, обильной потливостью, тахикардией, одышкой, слабостью. Диагностику эмпиемы плевры проводят на основании рентгенологических данных, УЗИ плевральной полости, результатов торакоцентеза, лабораторного исследования экссудата, анализа периферической крови. Лечение острой эмпиемы плевры включает дренирование и санацию плевральной полости, массивную антибиотикотерапию, дезинтоксикационную терапию; при хронической эмпиеме может выполняться торакостомия, торакопластика, плеврэктомия с декортикацией легкого.
МКБ-10
Общие сведения
Термином «эмпиема» в медицине принято обозначать скопление гноя в естественных анатомических полостях. Так, гастроэнтерологам в практике приходится сталкиваться с эмпиемой желчного пузыря (гнойным холециститом), ревматологам – с эмпиемой суставов (гнойным артритом), отоларингологам – с эмпиемой придаточных пазух (гнойными синуситами), неврологам – с субдуральной и эпидуральной эмпиемой (скоплением гноя под или над твердой мозговой оболочкой). В практической пульмонологии под эмпиемой плевры (пиотораксом, гнойным плевритом) понимают разновидность экссудативного плеврита, протекающего со скоплением гнойного выпота между висцеральным и париетальным листками плевры.
Причины
Почти в 90% случаев эмпиемы плевры являются вторичными по своему происхождению и развиваются при непосредственном переходе гнойного процесса с легкого, средостения, перикарда, грудной стенки, поддиафрагмального пространства.
1. Чаще всего эмпиема плевры возникает при острых или хронических инфекционных легочных процессах:
- пневмонии,
- бронхоэктазах,
- абсцессе легкого,
- гангрене легкого,
- туберкулезе,
- нагноившейся кисте легкого,
- спонтанном пневмотораксе,
- экссудативном плеврите и др.
В ряде случаев эмпиемой плевры осложняется течение медиастинита, перикардита, остеомиелита ребер и позвоночника, поддиафрагмального абсцесса, абсцесса печени, острого панкреатита.
2. Метастатические эмпиемы плевры обусловлены распространением инфекции гематогенным или лимфогенным путем из отдаленных гнойных очагов (например, при остром аппендиците, ангине, сепсисе и др.).
3. Посттравматический гнойный плеврит, как правило, связан с травмами легкого, ранениями грудной клетки, разрывом пищевода.
4. Послеоперационная эмпиема плевры может возникать после резекции легких, пищевода, кардиохирургических и других операций на органах грудной полости.
Патогенез
В развитии эмпиемы плевры выделяют три стадии: серозную, фибринозно-гнойную и стадию фиброзной организации.
- Серозная стадия протекает с образованием в плевральной полости серозного выпота. Своевременно начатая антибактериальная терапия позволяет подавить экссудативные процессы и способствует спонтанной резорбции жидкости. В случае неадекватно подобранной противомикробной терапии в плевральном экссудате начинается рост и размножение гноеродной флоры, что приводит к переходу плеврита в следующую стадию.
- Фибринозно-гнойная стадия. В этой фазе эмпиемы плевры вследствие увеличения количества бактерий, детрита, полиморфно-ядерных лейкоцитов экссудат становится мутным, приобретая гнойный характер. На поверхности висцеральной и париетальной плевры образуется фибринозный налет, возникают рыхлые, а затем плотные спайки между листками плевры. Сращения образуют ограниченные внутриплевральные осумкования, содержащие скопление густого гноя.
- Стадия фиброзной организации. Происходит образование плотных плевральных шварт, которые, как панцирь, сковывают поджатое легкое. Со временем нефункционирующая легочная ткань подвергается фиброзным изменениям с развитием плеврогенного цирроза легкого.
Классификация
В зависимости от этиопатогенетических механизмов различают эмпиему плевры:
- метапневмоническую и парапневмоническую (развившуюся в связи с пневмонией),
- послеоперационную
- посттравматическую.
По длительности течения эмпиема плевры может быть острой (до 1 мес.), подострой (до 3-х мес.) и хронической (свыше 3-х мес.). С учетом характера экссудата выделяют гнойную, гнилостную, специфическую, смешанную эмпиему плевры. Возбудителями различных форм эмпиемы плевры выступают неспецифические гноеродные микроорганизмы (стрептококки, стафилококки, пневмококки, анаэробы), специфическая флора (микобактерии туберкулеза, грибки), смешанная инфекция.
По критерию локализации и распространенности эмпиемы плевры бывают:
- односторонними и двусторонними;
- субтотальными, тотальными, отграниченными: апикальными (верхушечными), паракостальными (пристеночными), базальными (наддиафрагмальными), междолевыми, парамедиастинальными.
По объему гнойного экссудата:
- малая - при наличии 200-500 мл гнойного экссудата в плевральных синусах;
- средняя - при скоплении 500–1000 мл экссудата, границы которого доходят до угла лопатки (VII межреберье);
- большая - при количестве выпота более 1 литра.
Пиоторакс может быть закрытым (не сообщающимся с окружающей средой) и открытым (при наличии свищей – бронхоплеврального, плеврокожного, бронхоплевральнокожного, плевролегочного и др.). Открытые эмпиемы плевры классифицируются как пиопневмоторакс.
Симптомы эмпиемы плевры
Острый пиоторакс манифестирует с развития симптомокомплекса, включающего ознобы, стойко высокую (до 39°С и выше) или гектичекую температуру, обильное потоотделение, нарастающую одышку, тахикардию, цианоз губ, акроцианоз. Резко выражена эндогенная интоксикация: головные боли, прогрессирующая слабость, отсутствие аппетита, вялость, апатия.
Осложнения
Вследствие потери белков и электролитов развиваются волемические и водно-электролитные расстройства, сопровождающиеся уменьшением мышечной массы и похуданием. Лицо и пораженная половина грудной клетки приобретают пастозность, возникают периферические отеки. На фоне гипо- и диспротеинемии развиваются дистрофические изменения печени, миокарда, почек и функциональная полиорганная недостаточность. При эмпиеме плевры резко возрастает риск тромбозов и ТЭЛА, приводящих к гибели больных. В 15% случаев острая эмпиема плевры переходит в хроническую форму.
Диагностика
Распознавание пиоторакса требует проведения комплексного физикального, лабораторного и инструментального обследования. При осмотре пациента с эмпиемой плевры выявляется отставание пораженной стороны грудной клетки при дыхании, асимметричное увеличение грудной клетки, расширение, сглаживание или выбухание межреберий. Типичными внешними признаками больного с хронической эмпиемой плевры служат сколиоз с изгибом позвоночника в здоровую сторону, опущенное плечо и выступающая лопатка на стороне поражения.
Перкуторный звук на стороне гнойного плеврита притуплен; в случае тотальной эмпиемы плевры определяется абсолютная перкуторная тупость. При аускультации дыхание на стороне пиоторакса резко ослаблено или отсутствует. Дополняют физикальную картину данные инструментальной диагностики:
- Рентген. Полипозиционная рентгенография и рентгеноскопия легких при эмпиеме плевры обнаруживают интенсивное затенение. Для уточнения размеров, формы осумкованной эмпиемы плевры, наличия свищей выполняют плеврографию с введением водорастворимого контраста в плевральную полость. Для исключения деструктивных процессов в легких показано проведение КТ, МРТ легких.
- Сонография. В диагностике ограниченных эмпием плевры велика информативность УЗИ плевральной полости, которое позволяет обнаружить даже небольшое количество экссудата, определить место выполнения плевральной пункции.
- Оценка экссудата. Решающее диагностическое значение при эмпиеме плевры отводится пункции плевральной полости, с помощью которой подтверждается гнойный характер экссудата. Бактериологический и микроскопический анализ плеврального выпота позволяет уточнить этиологию эмпиемы плевры.
Лечение эмпиемы плевры
Санация плевральной полости
При гнойном плеврите любой этиологии придерживаются общих принципов лечения. Большое значение придается раннему и эффективному опорожнению плевральной полости от гнойного содержимого. Это достигается с помощью дренирования плевральной полости, вакуум-аспирации гноя, плеврального лаважа, введения антибиотиков и протеолитических ферментов, лечебных бронхоскопий. Эвакуация гнойного экссудата способствует уменьшению интоксикации, расправлению легкого, спаиванию листков плевры и ликвидации полости эмпиемы плевры.
Системная терапия
Одновременно с местным введением противомикробных средств назначается массивная системная антибиотикотерапия (цефалоспорины, аминогликозиды, карбапенемы, фторхинолоны). Проводится дезинтоксикационная, иммунокорригирующая терапия, витаминотерапия, переливание белковых препаратов (плазмы крови, альбумина, гидролизатов), растворов глюкозы, электролитов. С целью нормализации гомеостаза, снижения интоксикации и повышения иммунорезистентных возможностей организма выполняется УФО крови, плазмаферез, плазмоцитоферез, гемосорбция.
Физиореабилитация
В период рассасывания экссудата назначаются процедуры, предотвращающие образование плевральных сращений - дыхательная гимнастика, ЛФК, ультразвук, классический, перкуторный и вибрационный массаж грудной клетки.
Хирургическое лечение
При формировании хронической эмпиемы плевры показано хирургическое лечение. При этом может выполняться торакостомия (открытое дренирование), плеврэктомия с декортикацией легкого, интраплевральная торакопластика, закрытие бронхоплеврального свища, различные варианты резекции легкого.
Прогноз и профилактика
Осложнениями эмпиемы плевры могут являться бронхоплевральные свищи, септикопиемия, вторичные бронхоэктазы, амилоидоз, полиорганная недостаточность. Прогноз при эмпиеме плевры всегда серьезный, летальность составляет 5-22%. Профилактика эмпиемы плевры заключается в своевременной антибиотикотерапии легочных и внелегочных инфекционных процессов, соблюдении тщательной асептики при хирургических вмешательствах на грудной полости, достижении быстрого расправления легкого в послеоперационном периоде, повышении общей резистентности организма.
Плеврит
Плеврит – различные в этиологическом отношении воспалительные поражения серозной оболочки, окружающей легкие. Плеврит сопровождается болями в грудной клетке, одышкой, кашлем, слабостью, повышением температуры, аускультативными феноменами (шумом трения плевры, ослаблением дыхания). Диагностика плеврита осуществляется с помощью рентгенографии (-скопии) грудной клетки, УЗИ плевральной полости, плевральной пункции, диагностической торакоскопии. Лечение может включать консервативную терапию (антибиотики, НПВС, ЛФК, физиотерапию), проведение серии лечебных пункций или дренирования плевральной полости, хирургическую тактику (плевродез, плеврэктомию).
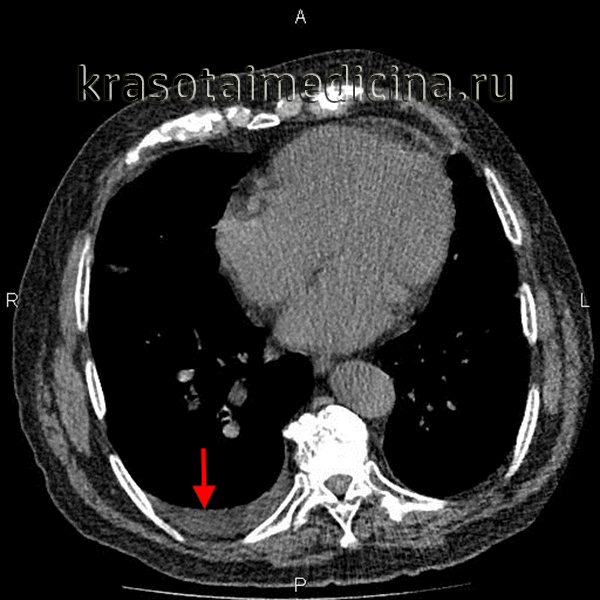
Плеврит – воспаление висцерального (легочного) и париетального (пристеночного) листков плевры. Плеврит может сопровождаться накоплением выпота в плевральной полости (экссудативный плеврит) или же протекать с образованием на поверхности воспаленных плевральных листков фибринозных наложений (фибринозный или сухой плеврит). Диагноз «плеврит» ставится 5-10% всех больных, находящихся на лечении в терапевтических стационарах. Плевриты могут отягощать течение различных заболеваний в пульмонологии, фтизиатрии, кардиологии, онкологии. Статистически чаще плеврит диагностируется у мужчин среднего и пожилого возраста.
Причины плеврита
Зачастую плеврит не является самостоятельной патологией, а сопровождает ряд заболеваний легких и других органов. По причинам возникновения плевриты делятся на инфекционные и неинфекционные (асептические).
Причинами плевритов инфекционной этиологии служат:
- бактериальные инфекции (стафилококк, пневмококк, грамотрицательная флора и др.);
- грибковые инфекции (кандидоз, бластомикоз, кокцидиоидоз);
- вирусные, паразитарные (амебиаз, эхинококкоз), микоплазменные инфекции;
- туберкулезная инфекция (выявляется у 20% пациентов с плевритом);
- сифилис, сыпной и брюшной тифы, бруцеллез, туляремия;
- хирургические вмешательства и травмы грудной клетки;
Плевриты неинфекционной этиологии вызывают:
- злокачественные опухоли плевры (мезотелиома плевры), метастазы в плевру при раке легкого, раке молочной железы, лимфомы, опухоли яичников и др. (у 25% пациентов с плевритом);
- диффузные поражения соединительной ткани (системная красная волчанка, ревматоидный артрит, склеродермия, ревматизм, системный васкулит и др.);
- ТЭЛА, инфаркт легкого, инфаркт миокарда;
- прочие причины (геморрагические диатезы, лейкозы, панкреатит и т. д.).
Механизм развития плевритов различной этиологии имеет свою специфику. Возбудители инфекционных плевритов непосредственно воздействуют на плевральную полость, проникая в нее различными путями. Контактный, лимфогенный или гематогенный пути проникновения возможны из субплеврально расположенных источников инфекции (при абсцессе, пневмонии, бронхоэктатической болезни, нагноившейся кисте, туберкулезе). Прямое попадание микроорганизмов в плевральную полость происходит при нарушении целостности грудной клетки (при ранениях, травмах, оперативных вмешательствах).
Плевриты могут развиваться в результате повышения проницаемости лимфатических и кровеносных сосудов при системных васкулитах, опухолевых процессах, остром панкреатите; нарушения оттока лимфы; снижения общей и местной реактивности организма.
Незначительное количество экссудата может обратно всасываться плеврой, оставляя на ее поверхности фибриновый слой. Так происходит формирование сухого (фибринозного) плеврита. Если образование и накопление выпота в плевральной полости превышает скорость и возможность его оттока, то развивается экссудативный плеврит.
Острая фаза плевритов характеризуется воспалительным отеком и клеточной инфильтрацией листков плевры, скоплением экссудата в плевральной полости. При рассасывании жидкой части экссудата на поверхности плевры могут образовываться шварты - фибринозные плевральные наложения, ведущие к частичному или полному плевросклерозу (облитерации плевральной полости).
Наиболее часто в клинической практике используется классификация плевритов, предложенная в 1984 г. профессором СПбГМУ Н.В. Путовым.
По этиологии:
- инфекционные (по инфекционному возбудителю – пневмококковый, стафилококковый, туберкулезный и др. плевриты)
- неинфекционные (с обозначением заболевания, приводящего к развитию плеврита – рак легкого, ревматизм и т. д.)
- идиопатические (неясной этиологии)
По наличию и характеру экссудата:
- экссудативные (плевриты с серозным, серозно-фибринозным, гнойным, гнилостным, геморрагическим, холестериновым, эозинофильным, хилезным, смешанным выпотом)
- фибринозные (сухие)
По течению воспаления:
По локализации выпота:
- диффузные
- осумкованные или ограниченные (пристеночный, верхушечный, диафрагмальный, костодиафрагмальный, междолевой, парамедиастинальный).
Симптомы плевритов
Сухой плеврит
Как правило, являясь вторичным процессом, осложнением или синдромом других заболеваний, симптомы плеврита могу превалировать, маскируя основную патологию. Клиника сухого плеврита характеризуется колющими болями в грудной клетке, усиливающимися при кашле, дыхании и движении. Пациент вынужден принимать положение, лежа на больном боку, для ограничения подвижности грудной клетки. Дыхание поверхностное, щадящее, пораженная половина грудной клетки заметно отстает при дыхательных движениях. Характерным симптомом сухого плеврита является выслушиваемый при аускультации шум трения плевры, ослабленное дыхание в зоне фибринозных плевральных наложений. Температура тела иногда повышается до субфебрильных значений, течение плеврита может сопровождаться ознобами, ночным потом, слабостью.
Диафрагмальные сухие плевриты имеют специфическую клинику: боли в подреберье, грудной клетке и брюшной полости, метеоризм, икота, напряжение мышц брюшного пресса.
Развитие фибринозного плеврита зависит от основного заболевания. У ряда пациентов проявления сухого плеврита проходят спустя 2-3 недели, однако, возможны рецидивы. При туберкулезе течение плеврита длительное, нередко сопровождающееся выпотеванием экссудата в плевральную полость.
Экссудативный плеврит
Начало плевральной экссудации сопровождает тупая боль в пораженном боку, рефлекторно возникающий мучительный сухой кашель, отставание соответствующей половины грудной клетки в дыхании, шум трения плевры. По мере скапливания экссудата боль сменяется ощущением тяжести в боку, нарастающей одышкой, умеренным цианозом, сглаживанием межреберных промежутков. Для экссудативного плеврита характерна общая симптоматика: слабость, фебрильная температура тела (при эмпиеме плевры – с ознобами), потеря аппетита, потливость. При осумкованном парамедиастинальном плеврите наблюдается дисфагия, осиплость голоса, отеки лица и шеи. При серозном плеврите, вызванном бронхогенной формой рака, нередко наблюдается кровохарканье. Плевриты, вызванные системной красной волчанкой, часто сочетаются с перикардитами, поражениями почек и суставов. Метастатические плевриты характеризуются медленным накоплением экссудата и протекают малосимптомно.
Большое количество экссудата ведет к смещению средостения в противоположную сторону, нарушениям со стороны внешнего дыхания и сердечно-сосудистой системы (значительному уменьшению глубины дыхания, его учащению, развитию компенсаторной тахикардии, снижению АД).
Исход плеврита во многом зависит от его этиологии. В случаях упорного течения плеврита в дальнейшем не исключено развитие спаечного процесса в полости плевры, заращение междолевых щелей и плевральных полостей, образование массивных шварт, утолщение плевральных листков, развитие плевросклероза и дыхательной недостаточности, ограничение подвижности купола диафрагмы.
Наряду с клиническими проявлениями экссудативного плеврита при осмотре пациента выявляется асимметрия грудной клетки, выбухание межреберных промежутков на соответствующей половине грудной клетки, отставание пораженной стороны при дыхании. Перкуторный звук над экссудатом притуплен, бронхофония и голосовое дрожание ослаблены, дыхание слабое или не выслушивается. Верхняя граница выпота определяется перкуторно, при рентгенографии легких или при помощи УЗИ плевральной полости.

В крови определяются повышение СОЭ, нейтрофильный лейкоцитоз, увеличение значений серомукоидов, сиаловых кислот, фибрина. Для уточнения причины плеврита проводится торакоскопия с биопсией плевры.
Лечение плеврита
Лечебные мероприятия при плеврите направлены на устранение этиологического фактора и облегчение симптоматики. При плевритах, вызванных пневмонией, назначается антибиотикотерапия. Ревматические плевриты лечатся нестероидными противовоспалительными препаратами, глюкокортикостероидами. При туберкулезных плевритах лечение проводится фтизиатром и заключается в специфической терапии рифампицином, изониазидом и стрептомицином на протяжении нескольких месяцев.
С симптоматической целью показано назначение анальгетиков, мочегонных, сердечно-сосудистых средств, после рассасывания выпота - физиотерапии и лечебной физкультуры.
При экссудативном плеврите с большим количеством выпота прибегают к его эвакуации путем проведения плевральной пункции (торакоцентеза) или дренирования. Одномоментно рекомендуется эвакуировать не более 1-1,5 л экссудата во избежание сердечно-сосудистых осложнений (вследствие резкого расправления легкого и обратного смещения средостения). При гнойных плевритах проводится промывание плевральной полости антисептическими растворами. По показаниям внутриплеврально вводятся антибиотики, ферменты, гидрокортизон и т. д.
В лечении сухого плеврита помимо этиологического лечения пациентам показан покой. Для облегчения болевого синдрома назначаются горчичники, банки, согревающие компрессы и тугое бинтование грудной клетки. С целью подавления кашля назначают прием кодеина, этилморфина гидрохлорида. В лечении сухого плеврита эффективны противовоспалительные средства: ацетилсалициловая кислота, ибупрофен и др. После нормализации самочувствия и показателей крови пациенту с сухим плевритом назначают дыхательную гимнастику для профилактики сращений в полости плевры.
С целью лечения рецидивирующих экссудативных плевритов проводят плевродез (введение в плевральную полость талька или химиопрепаратов для склеивания листков плевры). Для лечения хронического гнойного плеврита прибегают к хирургическому вмешательству – плеврэктомии с декорткацией легкого. При развитии плеврита в результате неоперабельного поражения плевры или легкого злокачественной опухолью по показаниям проводят паллиативную плеврэктомию.
Малое количество экссудата может рассасываться самостоятельно. Прекращение экссудации после устранения основного заболевания происходит в течение 2-4 недель. После эвакуации жидкости (в случае инфекционных плевритов, в т. ч. туберкулезной этиологии) возможно упорное течение с повторным скоплением выпота в полости плевры. Плевриты, вызванные онкологическими причинами, имеют прогрессирующее течение и неблагоприятный исход. Неблагоприятным течением отличается гнойный плеврит.
Пациенты, перенесшие плеврит, находятся на диспансерном наблюдении на протяжении 2-3 лет. Рекомендуется исключение профессиональных вредностей, витаминизированное и высококалорийное питание, исключение простудного фактора и переохлаждений.
В профилактике плевритов ведущая роль принадлежит предупреждению и лечению основных заболеваний, приводящих к их развитию: острой пневмонии, туберкулеза, ревматизма, а также повышению сопротивляемости организма по отношению к различным инфекциям.
3. Диагностическая тактика у больных с плевритом неясной этиологии: Автореферат диссертации/ Арутюнян А. В. – 2009.
4. Морфогенез и патологическая анатомия неопухолевых экссудативных плевритов Автореферат диссертации/ Фрисс С. А. – 2005.
Читайте также:
- Монотерапия эпилепсии. Политерапия эпилепсии. Побочные эффекты антиэпилептических препаратов.
- Сердечная астма. Причины сердечной астмы.
- Рандомизированные контролируемые исследования в здравоохранении. Квазиэкспериментальные исследования в медицине
- Рентгенограмма, КТ при обструкции пиелоуретерального сегмента
- Симптомы инфекции Clostridium difficile и ее лечение
