Лучевая диагностика рака пищевода
Добавил пользователь Alex Обновлено: 30.01.2026
а) Определения:
• Плоскоклеточный рак: злокачественная трансформация плоского эпителия
• Аденокарцинома: злокачественное перерождение измененного цилиндрического эпителия при синдроме Барретта
б) Визуализация:
1. Общая характеристика:
• Наиболее достоверный признак:
о Стойкое сужение просвета пищевода с наличием патологически измененной слизистой оболочки
• Локализация:
о Средняя треть пищевода (50%), нижняя треть (30%), верхняя треть (20%)
• Морфология:
о Классификация распространенного рака пищевода основывается на макроскопических признаках и данных рентгеновских методов исследования. Выделяют инфильтративный, полиповидный, язвенный и варикозный типы.
• Некоторые другие общие моменты:
о Рак - наиболее частая опухоль пищевода (более чем 95% всех опухолей)
о Плоскоклеточный рак:
- На долю плоскоклеточного рака приходится более 40% рака пищевода в США и до 90% в развивающихся странах:
Наблюдается уменьшение относительной распространенности по сравнению с аденокарциномой
- Вирус папилломы человека является фактором риска рака пищевода:
Особенно в Китае и Южной Африке
- Составляет 1 % раков всех локализаций и 7% рака желудочно-кишечного тракта
- Два главных фактора риска в США: табакокурение и злоупотребление алкоголем
о Аденокарцинома:
- На долю аденокарцином приходится более чем 60% всех случаев рака пищевода в США
- Наблюдается тенденция к увеличению распространенности аденокарциномы по сравнению с плоскоклеточным раком
- В 90-100% возникает на фоне синдрома Барретта
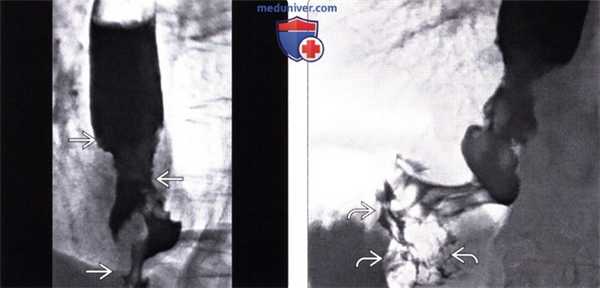
(Слева) На рентгенограмме определяется сужение просвета дистального сегмента пищевода в виде «огрызка яблока». Это переходная зона между проксимальной частью опухоли и неизменной частью пищевода. Слизистая оболочка в области опухоли разрушена, имеет узловатый вид.
(Справа) На рентгенограмме этого же пациента видны узло-видно утолщенные складки слизистой в области кардии, что позволяет предположить распространение опухоли на желудок. Кроме того, можно также предположить распространение рака желудка в дистальные отделы пищевода.
2. Рентгенография при раке пищевода:
• Двойное контрастирование пищевода, рентгенограммы в прямой и боковой проекциях:
о Плоскоклеточный рак пищевода на ранних стадиях:
- Бляшковидные поражения: небольшие полипы на широком основании или вдавление стенки
о Аденокарцинома на ранних стадиях на фоне синдрома Барретта:
- Бляшковидные поражения: полипы на широком основании
- Локализация изменений в стенке пищевода (чаще всего в нижней трети)
о Распространенный плоскоклеточный рак:
- Инфильтративный тип (наиболее частый): неравномерное утолщение стенки, стойкое сужение просвета (стрикутра) с наличием измененной за счет узлов или язв слизистой
- Полиповидный тип: внутрипросветное объемное образование дольчатой формы, с участками некроза и распада
- Язвенный тип: язвы в виде «блюдца» с четкими и ровными краями с рентгеновски прозрачным «ободком» на снимке в боковой проекции, обусловленным наличием опухоли
- Варикозный тип: утолщенные извилистые продольные складки слизистой пищевода, похожие на варикозно измененные вены, обусловлены подслизистым распространением опухоли:
Основное отличие: нет изменений рентгеновской картины при повторных снимках
о Распространенный рак на фоне синдрома Барретта:
- Нельзя отличить от плоскоклеточного рака на основании только рентгеновских методов исследования
- Распространенное поражение инфильтративного характера в дистальных отделах пищевода
о Стойкое сужение просвета пищевода:
- Асимметричный контур: расширение просвета пищевода перед опухолью и резкое его сужение в дистальном сегменте (симптом «мышиного хвоста»)
3. КТ при раке пищевода:
• КТ: стадирование рака пищевода:
о Стадии I и II: локальное утолщение стенки пищевода/неболь-шая внутрипросветная опухоль без инвазии в средостение
о Стадия III: опухоль прорастает за пределы стенки пищевода в средостение:
- Распространение в трахею и бронхи: прорастание в заднюю стенку или ее сдавливание, может быть ателектаз доли легкого
- Распространение в аорту: нечастая находка (до 2%)
- Распространение в перикард: инвазия в перикардиальную клетчатку или объемное воздействие
- Медиастинальная лимфаденопатия: лимфатические узлы могут быть расположены отдельно или сливаться с первичной опухолью
о Стадия IV: опухоль распространяется в средостение и в отдаленные органы:
- Печень, легкие, плевра, надпочечники, почки, лимфоузлы
- Увеличение лимфоузлов под диафрагмой наблюдается в 2/3 всех случаев при раке дистального сегмента пищевода
4. МРТ при раке пищевода:
• Данные, схожие с таковыми при КТ
5. УЗИ при раке пищевода:
• УЗИ без доплерографии:
о Эндоскопическая ультрасонография:
- Наилучший метод исследования для выявления метастазов в регионарных лимфоузлах
- Малигнизированные лимфоузлы: гипоэхогенные с четкими контурами
- Неизмененные лимфоузлы: гиперэхогенные с нечеткими контурами
6. Радионуклидная диагностика:
• ПЭТ:
о ПЭТ с фтордезоксиглюкозой (ФДГ-18):
- Более чувствительный метод по сравнению с КТ в выявлении регионарных и отдаленных метастазов
7. Рекомендации:
• Двойное контрастирование пищевода для обнаружения опухоли
• Эндоскопическая ультрасонография для определения поражения регионарных лимфоузлов
• КТ или ПЭТ для выявления метастазов
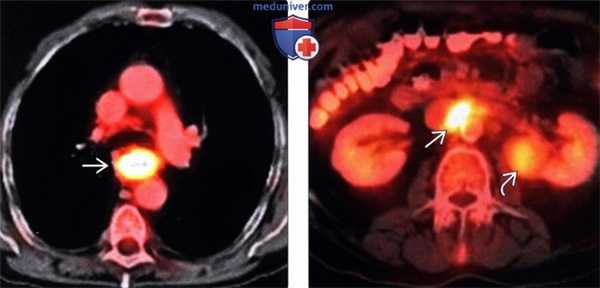
(Слева) На аксиальных ПЭТ/КТ срезах визуализируется очаг гиперфиксации ФДГ, соответствующий первичному раку пищевода.
(Справа) На более каудальных срезах у этого же пациента обнаружен очаг гиперфиксации ФДГ в аортокавальном лимфатическом узле. Кроме того, выявлен очаг накопления ФДГ в объемном образовании левой почки, что свидетельствует о первичном почечноклеточном раке. ПЭТ/КТ самый эффективный метод оценки распространенности поражения, влияющий на принятие итогового решения.
в) Дифференциальная диагностика рака пищевода:
1. Рефлюкс-эзофагит (со стриктурой):
• Плавное концентрическое сужение просвета короткого дистального сегмента пищевода:
о Перистальтика пищевода не изменена при доброкачественных процессах
о Перистальтика отсутствует при стриктуре, обусловленной злокачественной опухолью
• Окончательный диагноз: на основании данных эндоскопической биопсии и анамнеза
2. Доброкачественные интрамуральные опухоли пищевода:
• Лейомиома >> стромальная опухоль ЖКТ
• Края опухоли находятся под прямым или тупым углом по отношению к стенке пищевода
• Дефект наполнения округлой или овоидной формы
• Слизистая оболочка чаще всего ровная, интактная
• Изъязвление слизистой может симулировать аденокарциному
3. Метастазы в стенке пищевода и лимфома:
• Может поражать пищевод непосредственно
• Может быть причиной неравномерного сужения просвета пищевода
• Рак легкого, подтвержденный любым методом диагностики
4. Лучевой эзофагит:
• Неравномерное сужение подвергшегося лучевой терапии отдела пищевода
• Необходимо уточнить, были ли в анамнезе опухоли легкого, средостения и другие опухоли грудной клетки
5. Инородное тело пищевода:
• Плотный кусочек мяса может давать неправильной формы дефект наполнения, похожий на полип
• Не полностью расправленный просвет пищевода ниже места обтурации может быть ошибочно принят за патологическое сужение
• После извлечения инородного тела при рентгенографии пищевода можно обнаружить нормальную рентгеновскую картину, кольца Шацкого или стриктуру
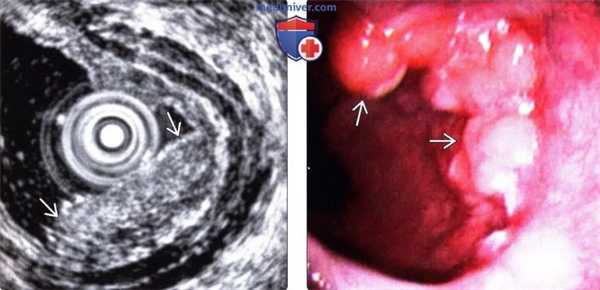
(Слева) При эндоскопической ультрасонографии выявлено внутрипросветное объемное образование, не проникающее через мышечную пластинку (аденокарцинома на стадии Т1а). Внутрипросветная сонография - лучший метод для определения глубины инвазии опухоли.
(Справа) На фотографии, полученной при эндоскопическом исследовании у этого же пациента, видно неправильной формы полиповидное объемное образование в дистальных отделах пищевода. Эта аденоарцинома была оперативно удалена путем эзофагэктомии с перемещением желудка в грудную полость.
г) Патология:
1. Общая характеристика:
• Этиология:
о Плоскоклеточный рак:
- Курение, употребление алкоголя, ахалазия кардии, стриктура нижних отделов пищевода
- Целиакия, опухоли головы и шеи
- Пламмера-Винсона (Plummer-Vinson) синдром, облучение, кератодермия
- Вирус папилломы человека, синергический эффект
о Аденокарцинома:
- Синдром Барретта практически всегда предшествует возникновению аденокарциномы
• Наследственность:
о Генная патология у пациентов в синдромом Барретта может увеличивать риск возникновения аденокарциномы
2. Стадирование, градация и классификация рака пищевода:
• Распространение: контактное, лимфогенное, гематогенное
• Стадирование по шкале TNM: о Стадия 0: рак in situ
о Стадия I: прорастание собственной пластинки или подслизистой основы
о Стадия IIA: прорастание мышечной пластинки и адвентиция
о Стадия IIB: прорастание собственной пластинки, подслизистого слоя, мышечной пластинки, адвентиция и поражение регионарных лимфатических узлов
о Стадия III: прорастание в смежные структуры, поражение регионарных лимфоузлов либо любых других лимфоузлов
о Стадия IV: прорастание всех слоев, поражение регионарных и других лимфоузлов, или наличие отдаленных метастазов
3. Макроскопические и хирургические особенности:
• Инфильтративный, полиповидный, язвенный или варикозный тип опухоли
4. Микроскопия:
• Атипичный плоский эпителий, столбчатый железистый
• Железистый и сквамозный компонент
д) Клинические особенности:
1. Проявления:
• Наиболее частые признаки/симптомы:
о Дисфагия (при приеме плотной пищи), одинофагия (боль при глотании)
• Клинический профиль:
о Пожилые пациенты, имеющие затруднения при проглатывании твердой пищи и потерей веса в анамнезе
• Данные лабораторных исследований:
о ± Гипохромная микроцитарная анемия
о ± Положительный анализ кала на скрытую кровь или снижение уровня альбумина
• Подтверждение диагноза: эндоскопическая биопсия и гистологическое исследование
2. Демография:
• Возраст: обычно старше 50 лет
• Пол:
о Мужчины: женщины = 4:1
• Этническая принадлежность:
о Афроамериканцы > европейцы (2:1)
• Эпидемиология:
о Увеличивается количество случаев заболевания в Турции, Иране, Индии, Китае, Южной Африке, Франции
о В США в последние 20 лет наблюдается резкое увеличение количества аденокарцином пищевода по сравнению с плоскоклеточным раком
3. Течение и прогноз:
• Осложнения:
о Формирование пищеводно-трахеального (бронхиального, перикардиального) свища
• Прогноз:
о Рак на ранних стадиях: пятилетняя выживаемость 90%
о Распространенный рак: пятилетняя выживаемость менее 10%
4. Лечение рака пищевода:
• Основное (направленное на устранение опухоли)
о Оперативное вмешательство, лучевая терапия (до и после операции)
о Часто выполняется эзофагэктомия с интерпозицией желудка:
- По методике Ivor-Lewis или другим (альтернативным)
• Паллиативное
о Оперативное вмешательство, лучевая терапия, химиотерапия
о Лазерная терапия, протезирование пищевода
е) Диагностическая памятка:
1. Следует учесть:
• Диагностические изображения при стриктурах пищевода, обусловленных воспалением и неравномерным утолщением слизистой оболочки, могут быть очень похожими
• Часто необходима эндоскопическая биопсия
2. Советы по интерпретации изображений:
• Неравномерное сужение просвета пищевода на фоне измененной с наличием узлов или изъязвленной слизистой оболочки
• Асимметричный контур: расширение просвета пищевода перед опухолью и резкое его сужение в дистальном сегменте (симптом «мышиного хвоста»)
ж) Список использованной литературы:
1. Karashima R et al: Advantages of FDG-PET/СТ over CT alone in the preoperative assessment of lymph node metastasis in patients with esophageal cancer. Surg Today. ePub, 2014
2. Napier KJ et al: Esophageal cancer: A Review of epidemiology, pathogenesis, staging workup and treatment modalities. World J Gastrointest Oncol. 6(5): 112-20, 2014
3. Lewis RB et al: From the radiologic pathology archives: esophageal neoplasms: radiologic-pathologic correlation. Radiographics. 33(4): 1083-108, 2013
4. Bird-Lieberman EL et al: Early diagnosis of oesophageal cancer. Br J Cancer. 101(1):1-6, 2009
5. Herszenyi L et al: Diagnosis and recognition of early esophageal neoplasia. Dig Dis. 27(1):24-30, 2009
6. Gupta S et al: Usefulness of barium studies for differentiating benign and malignant strictures of the esophagus. AJR Am J Roentgenol. 180(3):737-44, 2003
Лучевая диагностика рака пищевода
Диагностика рака пищевода на рентгенограмме, КТ, МРТ, ПЭТ
а) Терминология:
1. Сокращения:
• Плоскоклеточный рак пищевода (ПРП)
2. Определение:
• Первичное злокачественное новообразование пищевода:
о ПРП и аденокарцинома
б) Лучевые признаки рака пищевода:
1. Основные особенности:
• Локализация:
о Согласно классификации Американского объединенного комитета по изучению рака (AJCC) пищевод с целью стадирования рака пищевода делят на 4 отдела:
- Шейный: от перстнеглоточной мышцы до вырезки грудины Верхний грудной: от верхней апертуры грудной клетки до дуги непарной вены
- Средний грудной: от дуги непарной вены до нижней легочной вены
- Нижний грудной: от нижней легочной вены до нижнего пищеводного сфинктера
- Опухоли пищеводно-желудочного перехода (ПЖП) классифицируют как рак пищевода, если:
Центр новообразования расположен в нижнем грудном отделе пищевода или в ПЖП
Центр новообразования расположен в желудке не далее 5 см от дистальной границы пищевода, и опухоль распространяется на пищевод
• Размер:
о Варьируется от небольшого патологического участка в слизистой до крупного объемного образования
• Особенности рака пищевода:
о Отсутствие серозного слоя стенки пищевода => злокачественное новообразование легко распространяется на прилежащие структуры (трахею, щитовидную железу, аорту)
о Перекрестная сеть лимфатических сосудов пищевода с двунаправленным током лимфы => лимфогенное распространение выше или ниже уровня опухоли
2. Рентгенография рака пищевода:
• Изолированное объемное образование средостения:
о Смещение или выпуклость контура азигоэзофагеального кармана
о Утолщение задней трахеальной полосы в боковой проекции
о Смещение трахеи вперед:
- Опухоль в проксимальных отделах пищевода
- Параэзофагеальная лимфаденопатия
• Дилатация пищевода ± уровень жидкости и газа
• Исследование пищевода с двойным контрастированием:
о Участок слизистой с неровным, узловатым контуром или изъязвлением
о Ограниченная зона уплощения стенки пищевода, ее ригидность
о Неравномерное сужение просвета пищевода, проксимальный и дистальный края резко обрываются
о Крупное объемное образование с дольчатым контуром в просвете пищевода
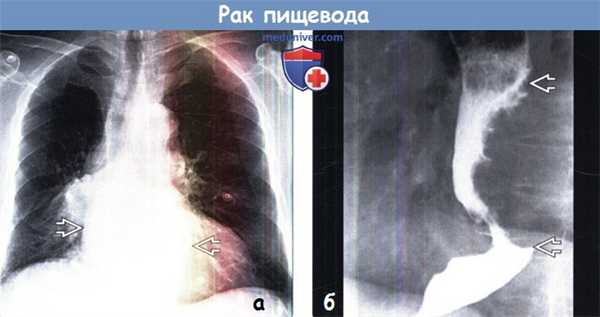
(а) Пациент, страдающий раком пищевода, обратился с жалобами на дисфагию. При рентгенографии органов грудной клетки в ПП проекции в нижних отделах средостения определяется объемное образование, на фоне которого азигоэзофагеальный карман и левый парааортальный контур не визуализируются.
(б) У этого же пациента при рентгеноконтрастном исследовании пищевода в боковой проекции визуализируются расширение проксимальных отделов пищевода и выраженное неравномерное сужение его просвета. Дистальный и проксимальный края суженной части пищевода резко обрываются. Данная картина соответствует объемному образованию в просвете пищевода.
3. КТ рака пищевода:
• Утолщение стенок пищевода:
о Асимметричное или циркулярное
о Не позволяет дифференцировать опухоли на стадии Т1, Т2 и Т3
о Сохранность жировой клетчатки между опухолью пищевода и прилежащими структурами средостения исключает стадию Т4
• Изолированное объемное образование пищевода
• Местная инвазия (Т4):
о Отсутствие жировой клетчатки между пищеводом и аортой или позвоночником
о Трахеоэзофагеальный или бронхоэзофагеальный свищ
о Смещение дыхательных путей, вдавление на их стенках или рост опухоли в их просвет
о Утолщение перикарда, перикардиальный выпот, отсутствие жировой клетчатки между перикардом и пищеводом/опухолью
о Охват аорты на протяжении >90°
• Мультипланарная реконструкция изображений облегчает определение протяженности опухоли в краниокаудальном направлении, что необходимо для планирования хирургического вмешательства или лучевой терапии
• Лимфаденопатия:
о Размер внутригрудных и брюшных лимфатических узлов > 1 см по короткой оси
о Размер надключичных лимфатических узлов>5 мм по короткой оси
о КТ не обладает высокой чувствительностью или специфичностью
• Метастазы:
о Внутригрудные или внегрудные метастазы
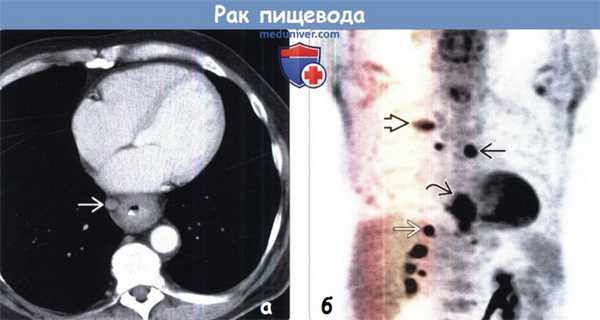
(а) У пациента с аденокарциномой пищевода при КТ с контрастным усилением определяются циркулярное утолщение стенок дистальных отделов пищевода и увеличенный правый параэзофагеальный лимфатический узел.
(б) У этого же пациента при ФДГ-ПЭТ в коронарной плоскости визуализируется интенсивное поглощение ФДГ первичной опухолью, которую сложно отличить от прилежащего параэзофагеального лимфатического узла. Следует отметить наличие лимфаденопатии правой паратрахеальной области и метастазов в заднем отрезке ребра справа и в правом надпочечнике.
4. МРТ рака пищевода:
• При высоком разрешении на Т2ВИ с кардиореспираторной синхронизацией визуализируются слои стенки пищевода
5. Ультразвуковое исследование рака пищевода:
• Эндоскопическое ультразвуковое исследование (ЭУЗИ):
о Визуализация 5 слоев стенки пищевода различной эхогенности:
- Ориентиры для оценки глубины опухолевой инвазии
- Превосходит КТ по возможностям разграничения опухолей стадии Т1, Т2 и Т3
- Под контролем данного метода возможно выполнение тонкоигольной аспирационной биопсии лимфатических узлов
- По сравнению с КТ позволяет с большей точностью выявлять метастазы в лимфатических узлах:
Форма округлая
Гипоэхогенная зона в центре
Контур четко отграничен
о Ограничения: крупные опухоли могут вызывать выраженное сужение просвета пищевода, которое препятствует проведению эндоскопа к месту стеноза
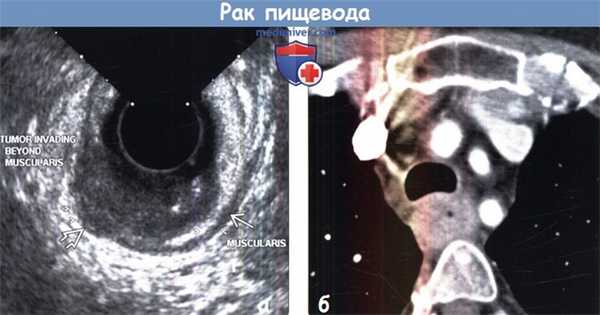
(а) При ЭУЗИ мышечный слой определяется в виде гипоэхогенной полосы. Гипоэхогенное объемное образование пищевода распространяется глубже мышечного слоя в адвентицию, что соответствует стадии опухоли. ЭУЗИ является методом выбора для определения категории Трака пищевода.
(б) У пациента с плоскоклеточной карциномой (ПКК) при КТ с контрастным усилением визуализируются утолщение стенок пищевода и вдавление по задней стенке трахеи, что свидетельствует в пользу инвазии дыхательных путей. В таких случаях для исключения инвазии обычно выполняют бронхоскопию.
6. Методы медицинской радиологии. ПЭТ/КТ:
о По сравнению с КТ позволяет точнее определить проксимальную и дистальную границу опухоли, что важно для планирования лучевой терапии
о По сравнению с ПЭТ позволяет точнее проводить стадирование регионарных лимфатических узлов благодаря установлению локализации очагов поглощения ФДГ вблизи первичной опухоли
о В 5-40% случаев позволяет обнаруживать не выявленные до этого отдаленные метастазы
о При первичном стадировании позволяет в 1,5-8% случаев выявлять синхронное первичное злокачественное новообразование
о Высокая чувствительность при определении рецидивирования опухоли или выявлении метастазов после проведенного лечения
о Позволяет на раннем этапе определить эффективность неоадъювантной терапии
7. Рекомендации к проведению лучевых исследований:
• Оптимальный метод лучевой диагностики:
о ЭУЗИ является методом выбора для определения стадии Т опухоли и обнаружения вовлечения в опухолевый процесс регионарных лимфатических узлов
о КТ после первичной диагностики позволяет выявлять нерезектабельные новообразования на стадии Т4 или обнаруживать метастазы
о ПЭТ /КТ используется для стадирования, рестадирования и выявления синхронной злокачественной опухоли
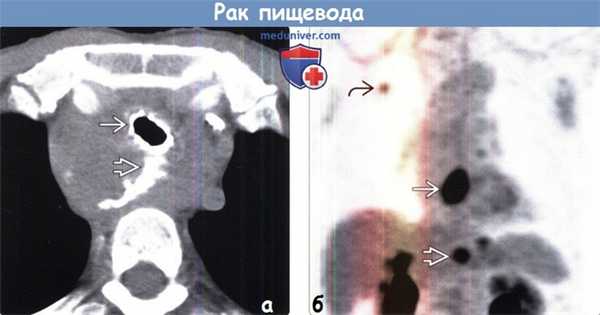
(а) Пациент с крупным образованием (ПРП), расположенным в верхнем грудном отделе пищевода. При КТ с пероральным контрастированием определяется трахеоэзофагеальный свищ (ТЭС). Для сохранения проходимости трахеи и закрытия свища был установлен стент. Рак пищевода является наиболее частой причиной развития ТЭС.
(б) Курильщик с плоскоклеточным раком пищевода (ПРП). При первичном стадировании посредством ФДГ-ПЭТ визуализируется поглощение ФДГ первичной опухолью, увеличенными желудочно-печеночными лимфатическими узлами и первичной аденокарциномой верхней доли правого легкого. ФДГ-ПЭТ облегчает выявление синхронного злокачественного новообразования.
в) Дифференциальная диагностика рака пищевода:
1. Стромальная опухоль пищевода: лейомиома, лейомиосаркома:
• Объемное образование в стенке пищевода, расположенное глубже слизистого слоя
• Может достигать больших размеров, не вызывая дилатации пищевода выше уровня локализации опухоли
• Лейомиома: гомогенная структура при КТ
• Лейомиосаркома: гетерогенная структура при КТ
2. Метастазы в пищеводе:
• Обычно у пациентов с ранее выявленным первичным злокачественным новообразованием:
о Рак молочной железы, легких, желудка
3. Эзофагит:
• Воспаление, обусловленное химиотерапией, лучевой терапией, гастроэзофагеальным рефлюксом, инфекцией
• Протяженный линейный участок накопления ФДГ или протяженное утолщение стенки пищевода в краниокаудальном направлении
г) Патоморфология рака пищевода:
1. Основные особенности:
• Этиология:
о Плоскоклеточная карцинома (ПКК): обычно в проксимальных 2/3 пищевода
- Факторы риска:
Употребление табака
Употребление алкоголя
Нитрозамины в консервированных продуктах
Ахалазия
- Наиболее распространенный повсеместно тип рака пищевода
- В странах северной Америки и Западной Европы уровень заболеваемости снижается; в США плоскоклеточная карцинома (ПКК) встречается реже, чем аденокарцинома:
о Аденокарцинома:
- Факторы риска:
Гастроэзофагеальный рефлюкс и метаплазия Барретта
Курение
Ожирение
- В странах северной Америки и Западной Европы уровень заболеваемости быстро растет
2. Стадирование, определение степени дифференцировки и классификация опухолей:
• Классификация TNM разработана Американским объединенным комитетом по изучению рака (AJCC):
о Категория Т; глубина инвазии стенки пищевода:
- Tis: рак in situ
- Т1: опухоль ограничена слизистым слоем, собственной пластинкой слизистой оболочки или подслизистым слоем
Т2: инвазия мышечной оболочки
Т3: инвазия адвентиции
Т4а: резектабельная злокачественная опухоль с инвазией в прилежащие структуры (плевру, перикард, диафрагму)
Т4b: нерезектабельная злокачественная опухоль с инвазией в прилежащие структуры (аорту, тело позвонка, трахею)
о Категория N; регионарные лимфатические узлы, любые параэзофагеальные лимфатические узлы от шейных до чревных:
N0: в регионарных лимфатических узлах метастазы отсутствуют
N1: метастазы в 1-2 регионарных лимфатических узлах
N2: метастазы в 3-6 регионарных лимфатических узлах
- N3: метастазы не менее чем в 7 лимфатических узлах
о Категория М:
М0: отдаленные метастазы отсутствуют М1: отдаленные метастазы
• Степень дифференцировки:
о G1: высокодифференцированная
о G2: умеренно дифференцированная
о G3: низкодифференцированная
о G4: недифференцированная
• Группировка стадий по категориям Т, N, М, G для ПКК и аденокарциномы отличается:
о Плоскоклеточный рак пищевода (ПРП): группировка стадий зависит в том числе и от локализации опухоли (верхний, средний, нижний отделы пищевода)
3. Макроскопические патоморфологические и хирургические особенности:
• Плоскоклеточная карцинома (ПКК):
о На ранних стадиях ограниченное бляшковидное утолщение слизистого слоя
о Полиповидное объемное образование в просвете пищевода
о Язвенно-некротические дефекты ±эрозирование в дыхательные пути, аорту
• Аденокарцинома:
о На ранних стадиях плоские или приподнятые бляшки
о Узловые объемные образования
д) Клинические аспекты:
1. Проявления:
• Наиболее частые признаки:
о Дисфагия, потеря веса
• Другие симптомы:
о Боль при глотании
о Охриплость: инвазия возвратного гортанного нерва
2. Демографические данные:
• Возраст:
о Средний: 65-70 лет
• Пол:
о М>Ж
3. Естественное течение заболевания и прогноз:
• В 24% случаев опухоль на момент выявления ограничена пищеводом
• В 30% случаев на момент выявления обнаруживают отдаленные метастазы
• Общий показатель пятилетней выживаемости при аденокарциноме < 15%, при плоскоклеточной карциноме (ПКК) еще меньше
4. Лечение:
• Опухоль на стадии Т1N0М0: эндоскопическое терапевтическое или хирургическое лечение
• Опухоль на стадии М0 с более глубоким поражением стенки пищевода или обширным поражением регионарных лимфатических узлов: неоадъювантная химиолучевая терапия с последующим хирургическим вмешательством
• М1: химиотерапия ± лучевая терапия
• Эндоскопические процедуры: при опухоли в слизистом слое на ранних стадиях или в целях паллиативного лечения
о Лазерная терапия
о фотодинамическая терапия
о Радиочастотная абляция
е) Диагностические пункты. Ключевые моменты при интерпретации изображений:
• При дилатации проксимальных отделов пищевода следует изучить его дистальные отделы, с тем чтобы исключить утолщение стенки пищевода или наличие объемного образования
ж) Список литературы:
1. Hong SJ et al: New TNM staging system for esophageal cancer: what chest radiologists need to know. Radiographics. 34(6): 1722-40, 2014
2. Krasna MJ: Radiographic and endosonographic staging in esophageal cancer. Thorac Surg Clin. 23(4):453-60, 2013
Сто оттенков лучевой диагностики: у каждого вида рака — свой «золотой стандарт» исследования
8 ноября — День рентгенолога. В этот день, в 1895 году, немецкий физик Вильгельм Конрад Рентген, проводя очередной эксперимент, открыл рентгеновское излучение. Сегодня это самый доступный и распространенный метод диагностики в мире.
Ни один метод лучевой диагностики не является универсальным, каждый имеет свои преимущества и недостатки, поэтому в реальной клинической практике врачи применяют все возможности медицинской визуализации, обсуждая в рамках мультидисциплинарной команды оптимальный алгоритм обследования пациента. С помощью Сергея Сергеевича Багненко, доктора медицинских наук, профессора, заведующего научным отделением диагностической и интервенционной радиологии НМИЦ онкологии им. Н.Н. Петрова, разбираемся, какие лучевые исследования нужно делать при конкретных онкопатологиях.

Методы лучевого исследования
Принято считать, что всего существует пять методов лучевой диагностики. В целом, деление базируется на видах лучевого воздействия, которое применяется в том или ином случае.
Рентгеновский метод — рентгеновское излучение, ультразвуковое (УЗИ) – ультразвуковые волны, МРТ – электромагнитные колебания, радионуклидный метод (позитронно-эмиссионная томография — ПЭТ, одно-фотонная эмиссионная томография – ОФЭКТ) — гамма и другие виды ионизирующего воздействия. Исключение – компьютерная томография (КТ). Данный вариант лучевой визуализации в своей основе предполагает рентгеновское излучение, и должен был бы относиться к рентгеновскому, однако его появление настолько расширило возможности классической рентгенодиагностики, что в свое время было принято решение вынести КТ в самостоятельный метод.
По большому счету, задачи, которые они выполняют, следующие:
Рентгенодиагностика — оценка состояния костей и органов грудной клетки, как правило, в рамках первичной диагностики, а также желудочно-кишечного тракта, желчных протоков и сосудов, если речь идет о рентген-контрастных методиках.
УЗИ — первичная диагностика практически любой онкопатологии, а также экспертная оценка при злокачественных поражениях щитовидной и паращитовидных желез, наружных половых органах, опухолях мягких тканей, имеющих поверхностное расположение, в том числе патологии молочных желез.
КТ — анализ состояния грудной клетки, скелета и органов живота в рамках предоперационного планирования (инвазия сосудов, поражение лимфатических узлов и пр.)
МРТ — головной, спинной мозг, молочные железы, связки и мышцы, органы малого таза и другие мягкотканные структуры.
Радионуклидный метод — решение отдельных вопросов дифференциальной диагностики (доброкачественный/злокачественный процесс и др.), оценка функционального состояния органов, а также стадирование онкологического заболевания (визуализация отдаленных метастазов и пр.).
Независимо от конкретного варианта лучевой диагностики, нативное исследование (без применения контрастных веществ) изредка может быть оправдано, однако в подавляющем большинстве случаев, особенно, если речь идет об онкопатологии, применение контрастных препаратов является обязательным.
Виды рака и методы лучевой диагностики
Рассмотрим лучевую диагностику по отдельным анатомическим локализациям.
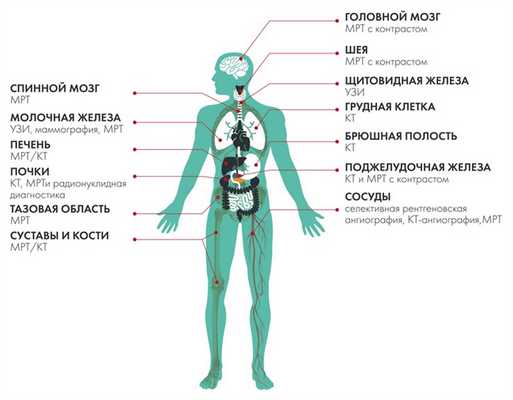
Головной мозг
Основной метод оценки непосредственно вещества головного мозга (в том числе первичных опухолей и метастазов) — МРТ с применением контрастного усиления.
Вопросы стадирования (поиск отдаленных метастазов) лучше всего решаются с помощью ПЭТ, в том числе с метионином.
Компьютерная томография используется как дополнительный метод в случае, если требуется оценка состояния костных структур, а также при наличии абсолютных противопоказаний к МРТ исследованию (наличие металла в теле — например, кардиостимулятора, ферромагнитных инородных металлических соединений: пластины, протезы, импланты и т.п.)
Первичный метод диагностики опухолей шеи — УЗИ.
Экспертная оценка – МРТ с контрастом.
КТ используется, когда необходимо оценить процесс разрушения (деструкции) костной ткани, требуется детальный анализ состояния гортани, а также есть показания к выполнению исследования сосудов (КТ-ангиография).
Радионуклидная диагностика – определение наличия онкологического процесса как такового, а также стадирование заболевания (применяются различные фармпрепараты: 18F-дезоксиглюкоза, метионин и пр.).
Щитовидная железа
Основной метод диагностики опухолевого процесса в щитовидной и паращитовидных железах — УЗИ. Отсутствие лучевой нагрузки, высокая разрешающая способность, а также доступность оборудования являются очевидными достоинствами эхографии. Особенно справедлив данный тезис, если речь идет об УЗИ с контрастным усилением и применением эластографии. Так называемое, мультипараметрическое УЗИ, то есть вариант исследования с включением в процедуру максимально количества различных методик, является наиболее перспективным вариантом реализации сонографической диагностики, особенно при злокачественной патологии.
Радионуклидная диагностика (к примеру, ПЭТ с 18F-DOPA) информативна в рамках подтверждения злокачественного характера имеющегося процесса, а также для выявления отдаленных метастазов.
Грудная клетка
С момента своего открытия (ровно 101 год назад) и по сей день рентгенодиагностика сохраняет свою актуальность (прежде всего, как метод первичной визуализации) в рамках оценки состояния легких и костной ткани. Однако «золотым стандартом» в данных областях заслужено стала КТ, базирующаяся на рентгеновском излучении, но существенно расширившая возможности классической рентгенографии. Компьютерная томография позволяет детально проанализировать состояние органов грудной клетки, оценить стадию и распространенность патологического процесса, вовлечение сосудов и других тканей, ответ на проводимую терапию.
У пациентов с острой патологией (например, реанимационных больных) может быть оправдано применение УЗИ (плевриты и др.).
МРТ эффективно для диагностики нейрогенных образований, которые располагаются в заднем средостении, а также как дополнительный метод диагностики при стадировании других опухолей средостения, например, рака пищевода.
Молочная железа
В настоящее время основными методами исследования молочных желез являются: маммография, УЗИ и МРТ. Все они обладают очевидными достоинствами и активно конкурируют между собой. Классическим вариантом визуализации (широкодоступным и понятным подавляющему большинству специалистов) является рентгеновская маммография.
УЗИ – неинвазивный метод, не предполагающий лучевую нагрузку, обладающий чрезвычайно высокими характеристиками в плане разрешающей способности изображений. Многие учреждения именно сонографический вариант диагностики рассматривают как «золотой стандарт», однако «операторозависимость» (когда два разных специалиста могут по-разному трактовать увиденное), а также невозможность оценить результаты другим специалистом (альтернативное мнение), ограничивают «зону ответственности» ультразвуковой диагностики.
МРТ решает большинство рассматриваемых вопросов, также не предполагает лучевой нагрузки, но имеет определенные ограничения в плане доступности и стоимости процедуры.
Печень
Первичная диагностика – УЗИ.
Экспертная оценка — КТ/МРТ с динамическим контрастированием.
КТ – доступнее, необременительна для пациента (само сканирование происходит за считанные секунды/минуты), позволяет в ходе одного визита исследовать в том числе легкие (что часто требуется в рамках онкоскриннинга).Это более простой, а потому более стандартизированный метод, который позволяет детально оценить состояние сосудов, что крайне важно при предоперационном планировании. Независимо от того, в каком центре проводится исследование, качество собранных данных будет, как правило, на достаточном уровне.
МРТ дает максимум информации в плане выявления и дифференциальной диагностики очаговой патологии печени, особенно если сканирование проводится с гепатотропными контрастными препаратами. Не предполагает лучевой нагрузки (то есть безвредно), а потому может выполняться многократно, в том числе беременным и детям. Однако многое зависит от того, в каком конкретно центре выполнено исследование (аппарато- и операторозависимость), занимает больше времени (сложности при обследовании пожилых, ослабленных пациентов), имеет ограничения в плане исследования легких (МРТ легких обычно не проводится и для их анализа приходится совершить визит в КТ отделение), имеет абсолютные противопоказания (например, металл в теле), уступает КТ в отношении предоперационной оценки.
Поджелудочная железа
По большому счету ситуация аналогична применяемым методам лучевой диагностики печени, однако есть некоторые нюансы. Так, из-за центрального расположения органа в теле визуализация при УЗИ может быть затруднена (тучные пациенты, при метеоризме — вздутие кишечника). Локальные обызвествления значительно лучше выявляются при КТ.
МРТ эффективнее для дифференциальной диагностики выявленных изменений.
Почки
Основные методы диагностики опухоли почки — КТ, МРТ и радионуклидный. Только в совокупности эти три составляющие могут дать врачам-онкологам полную информацию о состоянии органов. Традиционное УЗИ активно применяется для первичной оценки зоны интереса. Большие перспективы связывают с внедрением в клиническую практику УЗИ с контрастным усилением, однако по ряду технических моментов доступность данной методики сейчас ограничена.
Малый таз
«Золотым стандартом» оценки состояния органов малого таза, независимо от пола пациента, считают МРТ. И женские и мужские внутренние половые органы лучше всего оценивать с помощью МРТ с динамическим контрастированием. Впрочем, существуют ситуации, когда КТ может дать ценную дополнительную информацию.
Суставы и кости
В онкологической практике основными методами диагностики опухолей костно-мышечной системы являются МРТ и КТ.
Определенный приоритет имеет МРТ, однако, если требуется детальная оценка структуры кости или речь идет о параметрах деструкции, без КТ не обойтись.
Также в НИМЦ онкологии им. Петрова используется SLOT-рентгенография костей, когда с помощью специальной методики вся конечность, позвоночник или весь скелет целиком визуализируются на одном рентгеновском изображении. Этот метод позволяет точно определить параметры опухоли и соотнести ее с размером кости, что чрезвычайно важно хирургам при планировании вмешательства, подбора протеза или изготовления импланта.
Сосуды
Определенную информацию о состоянии некоторых сосудов можно получить при допплерографическом УЗИ, однако в онкологической практике чаще требуется более детальная информация и приходится прибегать к ангиографическим методикам.
Наиболее информативны – артериография на фоне плоскодетекторной компьютерной томографии (ПДКТ-артериография) и селективная цифровая субтракционная ангиография (ЦСА).
В 2021 году в НМИЦ онкологии им. Н.Н. Петрова в рентгеноперационной отделения рентгенохирургических методов диагностики и лечения был установлен современный ангиографический комплекс Artis Zee Flor (Siemens), позволяющий выполнять весь спектр диагностических и лечебных вмешательств, применяемых в интервенционной онкологии (в том числе с использованием ПДКТ-артериографии, ЦСА, внутрисосудистой и чрескожной 3D навигации). Однако основным недостатком данных методов визуализации является их инвазивность, требующая госпитализации пациентов для проведения вмешательства с соблюдением строгих правил асептики и антисептики.
Поэтому в рутинной практике чаще прибегают к менее инвазивным КТ-ангиографии и неинвазивной МР-ангиографии. Эти варианты визуализации позволяют проследить ход сосудов, выявить наличие тромбов, оценить наличие и степень опухолевой инвазии. КТ быстрее и обеспечивает более высокое пространственное разрешение изображений. Если применение йодсодержащих контрастов противопоказано (аллергические реакции, почечная недостаточность), выполняют магнитно-резонансное исследование. Современные технологии позволяют проводить сканирование с ЭКГ синхронизацией (требуется при изучении сосудов сердца), а также выполнять бесконтрастную МР-ангиографию (без введения контрастных препаратов в сосудистое русло).
Спинной мозг
Основной метод диагностики опухолей в спинном мозге — МРТ с контрастом. Он позволяет определить локализацию патологического процесса (интрамедуллярный или экстрамедуллярный, то есть находящийся в структуре спинного мозга или вне его), оценить его распространённость, вовлечение соседних структур. Если есть противопоказания к МРТ, а также, когда нужно детально разобраться с состоянием расположенных рядом позвонков, проводят КТ.
Пациенту важно помнить, что любые обследования, их последовательность и объем должен назначить врач-онколог. В подавляющем большинстве случаев диагностика нужна не сама по себе, а для планирования лечения, которое будет проводить соответствующий врач. Поэтому «назначенные» самостоятельно процедуры без предварительной консультации со специалистом могут быть абсолютно не информативны, то есть бесполезны, а с учетом возможной лучевой нагрузки даже вредны.


Автор:
Ирина Фигурина
специалист по связям с общественностью НМИЦ онкологии им. Н. Н. Петрова
Оренбургский государственный университет, факультет филологии
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Рак пищевода
Рак пищевода представляет собой опухоль злокачественного характера, происходящую из эпителиальных клеток пищевода. Заболевание берет начало с внутреннего слоя, то есть слизистой оболочки, а затем распространяется наружу, преодолевая подслизистый и мышечный слои.
Существует два основных вида такого заболевания:
- Плоскоклеточный рак. Он возникает из клеток, составляющих слизистую оболочку пищевода. Чаще всего встречается в зоне шеи, а также двух верхних третей грудной клетки.
- Аденокарцинома, другими словами – железистый рак. Чаще всего диагностируется в нижней трети пищевода. Вначале происходит замещение железистого эпителия плоскоклеточным (при пищеводе Барретта).
Статистика
Чаще всего (до 80% случаев) новообразование находится в нижне- и среднегрудном отделах пищевода. С частотой 10-15% случаев диагностируется рак шейного отдела пищевода.
Факторы риска
Основные факторы риска возникновения и развития такой болезни:
- мужской пол, потому что мужчины чаще подвержены вредным привычкам – курению и употреблению спиртного в больших количествах;
- возраст – чем он больше, тем выше риск, лишь 15% пациентов были младше 55-ти лет;
- избыточная масса тела;
- курение и злоупотребление спиртным;
- употребление очень горячих напитков и еды;
- пищевод Барретта (когда в нижней части пищевода возникает клеточное перерождение, вызываемое кислотным повреждением хронической формы);
- рефлюкс;
- ахалазия (когда нарушена запирательная функция отверстия между желудком и пищеводом);
- рубцы в пищеводе, приведшие к его сужению;
- синдром Пламмера-Винсона (для такого синдрома характерна триада, то есть три вида нарушений одновременно: нарушенная глотательная функция, суженный пищевод, железодефицитная анемия);
- контакт с химикатами.
Примерно у 1/3 заболевших диагностирован ВПЧ (вирус папилломы человека).
Риск заболеть этим видом рака можно снизить, если разнообразно питаться, не пить крепкий алкоголь, а при наличии синдрома Барретта отслеживать изменения в слизистой оболочке.
Скрининг этого заболевания не проводится. Однако при повышенном риске появления рака пищевода рекомендуется проходить эндоскопическое исследование, при необходимости с биопсией подозрительной зоны.
Симптомы
Обычно рак пищевода обнаруживается на поздних стадиях, когда терапия уже осложнена, или случайно.
Наиболее частая симптоматика включает следующее:
- Дисфагия. Этот симптом представляет собой нарушенную функцию глотания. Пациенты описывают свое состояние как ощущение «комка в горле». Заболевшие начинают уменьшать порции пищи, избегают твердой еды. На поздних стадиях возможно употребление только жидкой пищи.
- Повышенное слюноотделение. Больше слюны в ротовой полости начинает вырабатываться для того, чтобы помочь продвинуться пищевому комку через суженный просвет пищевода.
- Дискомфорт и боль в грудине. Эти симптомы не всегда относятся к раку пищевода, они могут вызываться межреберной невралгией, стенокардией, гастроэзофагеальным рефлюксом. Поэтому не являются специфическими.
- Снижение массы тела. При затрудненном глотании и общей слабости заболевший человек начинает отказываться от еды, поэтому похудение часто сопровождает рак пищевода.
Есть и более редкие симптомы:
- кашель;
- икота;
- хриплый голос;
- рвота;
- костные боли (при наличии метастазов);
- пищеводное кровотечение (после того как кровь проходит по ЖКТ, стул окрашивается в черный цвет);
- как следствие кровотечения – анемия (человек становится бледным, слабым, быстро утомляется, испытывает постоянную сонливость).
Важно! Наличие подобных симптомов еще не означает рак. Однако нужно обязательно обратиться к врачу и обследоваться.
Классификация рака пищевода
По области возникновения:
- внутригрудной отдел пищевода;
- шейный отдел (от нижней границы перстневидного хряща до входа в грудную полость);
- верхняя грудная зона (от входа в грудную полость до области бифуркации трахеи);
- средняя грудная область (проксимальная часть пищевода распространяется от зоны бифуркации трахеи до соединения пищевода с желудком);
- нижняя грудная область (дистальная часть пищевода примерно 10 см в длине, включая абдоминальную часть пищевода, распространяется от зоны бифуркации трахеи до соединения пищевода и желудка).
По характеру роста опухоли:
- в просвет пищевода (экзофитный);
- язвенный (эндофитный);
- круговая форма (инфильтративный склерозирующий).
По степени дифференцировки новообразования:
- степень не определена – Gx;
- высокодифференцированное образование – G1;
- умеренно дифференцированное – G2;
- малодифференцированное – G3;
- недифференцируемое – G4.

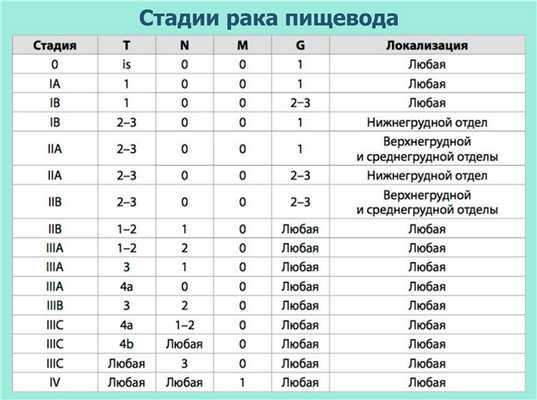
Стадии рака пищевода
Предлагаем ознакомиться с таблицей стадирования заболевания:
Диагностика
Диагностирование осуществляется инструментальными и лабораторными методами.
- Рентгенография с бариевым контрастом. Пациент принимает внутрь сульфат бария, который обволакивает стенки пищевода. Это позволяет увидеть на снимке рельеф стенок и обнаружить сужение просвета. На ранней стадии рак может иметь вид небольших круглых выпуклостей, то есть бляшек. На поздней стадии развития новообразование принимает вид большой опухоли неправильной формы, которая может вызывать сильное сужение пищевода. Рентгенография также позволяет диагностировать трахеопищеводную фистулу, то есть когда из-за разрушения новообразованием стенки пищевода на всю толщину пищевод начинает сообщаться с трахеей.
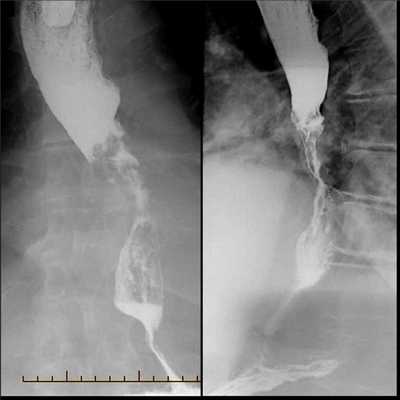
Рентгенодиагностика рака пищевода
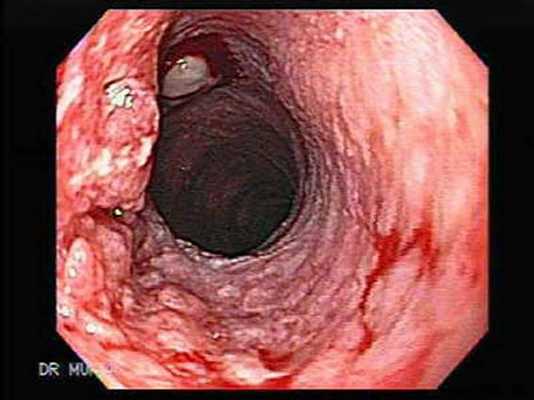
Эндоскопическая картина аденокарциномы
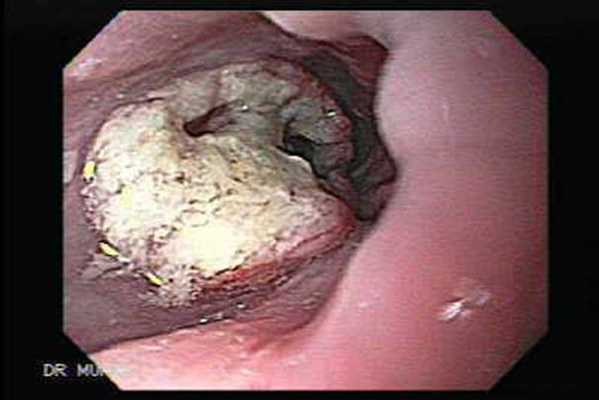
Эндоскопическая картина плоскоклеточного рака
Лабораторные исследования
- Клинический анализ крови. Позволяет выявить анемию, которая возникает из-за кровотечения или скудного рациона.
- Биохимический анализ крови. Он показывает состояние внутренних органов, а именно почек, печени и др.
- Анализ на онкомаркеры СА 19-9, РЭА.
- Исследование биоматериала, взятого во время биопсии. В нем определяют рецепторы белка HER2. При их наличии против новообразования можно использовать таргетную терапию.
Лечение
Основной метод лечения – хирургическая операция, однако комплексный подход позволяет улучшить результаты. Поэтому различные методики комбинируются.
Хирургическое лечение
В ходе операции удаляют пищевод целиком или его часть, все зависит от распространенности и локализации патологического процесса.
Когда опухоль находится в шейном отделе, удаляют большую часть пищевода. После этого желудок поднимают и подшивают к оставшейся части пищевода. Кроме того, вместо удаленной части методом пластической операции может быть использована часть толстой или тонкой кишки. При возможности выполнения резекции шейного отдела пищевода может быть выполнена пластика кишкой с микрососудистым анастомозом сосудов на шее.
При локализации опухоли в шейном отделе пищевода с большим распространением приходится выполнять операцию в объеме: удаления фаринголарингоэктомии с одномоментной пластикой пищевода желудочным трансплантатом, с пришиванием его к корню языка.
Хирургическое вмешательство по удалению части пищевода с последующим замещением трансплантатом может быть проведено открытым способом или методом торакоскопии и лапароскопии.
При любом типе вмешательства удаляют регионарные лимфоузлы, которые потом исследуют в лаборатории методом гистологии. Если в них обнаруживаются раковые клетки, то после операции пациенту прописывают лучевое лечение или химиотерапию в комбинации с ЛТ.
Также существуют паллиативные операции. Их проводят для того, чтобы пациент мог питаться, если из-за опухоли он не может глотать. Этот тип вмешательства называется гастростома, то есть введение через переднюю брюшную стенку в желудок специальной трубки для питания.
Лучевая терапия
Применяется ионизирующее излучение с целью уничтожения клеток новообразования. Такая терапия может проводиться:
- Тем пациентам, которым по состоянию здоровья нельзя делать операцию. В этом случае облучение, обычно вместе с химиотерапией, представляет собой основную методику лечения.
- При локализации опухоли в области шейного отдела пищевода химиолучевая терапия является первым этапом комбинированного метода лечения.
- Перед операцией вместе с химиотерапией. Это нужно, чтобы уменьшить опухоль и обеспечить ее лучшее удаление (называется «неоадъювантная терапия»).
- После хирургического вмешательства вместе с химиотерапией. Таким образом воздействуют на остаточную опухоль, которую нельзя было увидеть во время операции (носит название «адъювантная терапия»).
- Для облегчения симптоматики при распространенном раке пищевода. Позволяет снизить интенсивность болевого синдрома, устранить кровотечение и трудности с глотанием. В данном случае это паллиативная терапия.
Разновидности лучевого лечения:
- Наружное (дистанционное). Источник ионизирующего излучения находится на расстоянии от пациента.
- Контактное (называется «брахитерапия»). Источник излучения эндоскопическим методом размещается как можно ближе к новообразованию. Ионизирующие лучи проходят малое расстояние, поэтому достигают опухоли, но мало затрагивают расположенные рядом ткани. Лечение позволяет уменьшить новообразование и восстановить проходимость.
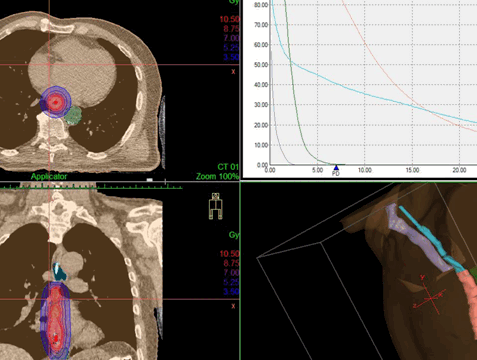
Дозное распределение, получаемое при дистанционной конформной лучевой терапии и внутрипросветной брахитерапии
Химиотерапия
Данная методика представляет собой введение в организм препаратов, затормаживающих жизнедеятельность опухолевых клеток или уничтожающих их. Лекарственные средства принимаются внутрь или вводятся в вену, после чего попадают в кровоток и достигают почти всех областей организма.
Химиотерапия осуществляется циклами. Это связано с тем, что действие препарата направлено на те клетки, которые постоянно делятся. Введение повторяется через определенное число дней, что связано с клеточным циклом. Циклы химиотерапии, как правило, имеют продолжительность 2-4 недели, больным обычно показано несколько циклов.
Как и облучение, химиотерапия показана в адъювантном и неоадъвантном режимах. Также она применяется, чтобы облегчить симптоматику тем больным, у которых рак распространен и не поддается хирургическому лечению.
- «Цисплатин» и «5-фторурацил» («5-FU»);
- «Паклитаксел» и «Карбоплатин»;
- «Цисплатин» совместно с «Капецитабином»;
- схема ECF: «Эпирубицин», «Цисплатин» и «5-FU»;
- схема DCF: «Доцетаксел», «Цисплатин» и «5-FU»;
- «Оксалиплатин» совместно либо с «Капецитабином», либо с «5-FU»;
- «Иринотекан».
Таргетная терапия
Направлена на блокировку роста новообразования путем воздействия на определенные мишени, то есть на те молекулы, которыми определяются деление и рост опухоли. Если в биоматериале, взятом методом биопсии, находят такие белковые молекулы, то может быть эффективна именно таргетная терапия.
Паллиативные методы
При проведении паллиативной терапии применяют следующие методики:
- Бужирование, то есть расширение пищевода.
- Установку стентов эндоскопическим методом. Стенты – это полые цилиндры, которые устанавливаются в просвет пищевода, чтобы обеспечить проходимость пищи.
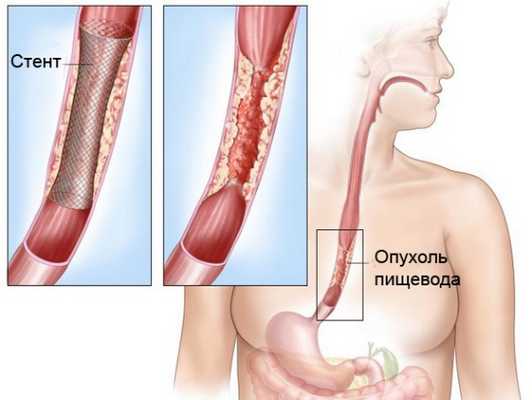
Стентирование рака пищевода
Лечение рака пищевода изменяется в зависимости от стадии
0 стадия
Опухоль на этой стадии – это не истинный рак. В ней содержатся аномальные клетки. Такое состояние называют «дисплазией», это разновидность предраковых заболеваний. Аномальные клетки имеют вид раковых, но встречаются только во внутренней оболочке пищевода (эпителии), они не растут в глубокие слои пищевода.
Обычно применяются эндоскопические методики лечения:
- PDT, или фотодинамическая терапия;
- RFA, то есть радиочастотная абляция;
- EMR, эндоскопическое удаление опухоли слизистой оболочки (после этого обеспечивается длительное наблюдение с применением эндоскопии, чтобы вовремя заметить рецидив, если он возникнет).
I стадия
Новообразование затрагивает мышечную или собственную пластинку слизистой, но не поражает другие органы и лимфоузлы.
- Рак T1. Заболевание на ранней стадии, когда оно находится только в небольшой зоне слизистой и не достигло подслизистой основы (новообразования Т1а), может быть удалено путем эндоскопической резекции в рамках слизистой или подслизистого слоя. Иногда медики рекомендуют хирургически удалить часть пищевода, а затем провести облучение и химиотерапию.
- Рак Т2. Опухоль затрагивает мышечную пластинку слизистой. Таким пациентам перед операцией проводятся химиотерапия и облучение. Исключительно хирургическое удаление рекомендовано, только когда новообразование менее 2 см в размере.
Когда рак локализуется в зоне шеи, вместо операции в качестве основного метода лечения могут быть рекомендованы облучение и химиотерапия.
II и III стадии
На второй стадии опухоль распространяется на главный мышечный слой пищевода либо его наружную оболочку. Также новообразование поражает 1 или 2 расположенных рядом лимфоузла.
При третьей стадии новообразование прорастает на наружную оболочку пищевода, может распространяться на соседние органы, им поражены регионарные лимфоузлы. Рекомендовано комбинированное лечение, которое включает операцию и предваряющие ее химиотерапию либо химиотерапию в сочетании с облучением. Если по состоянию здоровья для пациента есть риск не пережить операцию, то химиотерапия в сочетании с облучением становится основным методом лечения.
IV стадия
Рак затрагивает отдаленные лимфоузлы, есть метастазы в отдаленных органах (легких, печени). На такой стадии основная цель лечения – как можно более долгий контроль над распространением и размером новообразования. Пациентам проводится симптоматическое лечение для облегчения боли, восстановления возможности питаться и др. Применяется лучевая терапия и химиотерапия.
Профилактика
Чтобы предупредить такое заболевание, нужно исключить алкоголь и курение, контролировать массу тела. Если у человека присутствует повышенный риск развития этого типа рака (это такие патологии, как пищевод Барретта, ахалазия кардии, стриктуры пищевода, хронические эзофагит), то он должен регулярно обследоваться с обязательным применением эндоскопии.
Важно! Если рано диагностировать рак пищевода, то его можно вылечить с вероятностью от 85% до 100%.
Когда лечение рака завершено, нужно регулярно проходить контрольные обследования:
- После радикального лечения, сочетающего хирургию, химиотерапию и лучевую терапию: в первые 2 года – каждые 3-6 месяцев, в следующие 3-5 лет – каждые 6-12 месяцев, затем – каждый год.
- Тем, у кого был обнаружен ранний рак и кто подвергся эндоскопическому удалению слизистой: в первый год – каждые 3 месяца эндоскопическое обследование, во 2-й и 3-й годы – каждые полгода, затем – каждый год.


Авторская публикация:
Бекяшева Зоя Салаватовна
Ординатор хирургического отделения опухолей головы и шеи
НМИЦ онкологии им Н.Н. Петрова

Под научной редакцией:
Раджабова Замира Ахмедовна
Заведующий отделением опухолей головы и шеи, врач-онколог, научный сотрудник, доцент, кандидат наук
НМИЦ онкологии им. Н.Н. Петрова
Читайте также:
