МРТ при липомиеломенингоцеле
Добавил пользователь Владимир З. Обновлено: 27.01.2026
На базе НМИЦ детской травматологии и ортопедии им. Г. И. Турнера с 2015 года работает профильный Центр лечения детей с последствиями спинномозговых грыж Spina bifida, где применяется комплексный подход к лечению с участием ортопеда, невролога, нейрохирурга, уролога и психолога.
Предлагаем Вам ознакомиться с описанием патологии и современными методами лечения.
Spina bifida: определение, распространённость заболевания в мире и в России
Spina bifida (рус.: Спина бифида, лат.: Spina bifida, англ.: split spine) – это врождённый порок развития позвоночника и спинного мозга, при котором дуги одного или нескольких позвонков не срослись и в результате чего позвоночник остаётся «расщепленным». В сформированный дефект могут выпячиваться сам спинной мозг или различные структуры спинного мозга и его оболочки. Термин Spina bifida впервые использовал N. Tulp в 1651 году для описания удвоения остистого отростка позвонка как проявления аномалии развития позвоночника, но не спинного мозга. Несмотря на только лишь историческое значение данного термина, он до сих пор применяется для обозначения так называемых спинальных дизрафий – группы заболеваний, проявляющихся нарушением формирования позвоночника и спинного мозга. Спинальный дизрафизм (dys – нарушение + греч. rhaphē – шов), или Spina bifida, принадлежит к группе заболеваний, носящих название «дефекты нейральной трубки» (ДНТ), включающее в себя также аномалии развития головного мозга и черепа.
Другими словами, Spina bifida охватывает группу дефектов развития позвоночника, начиная от достаточно «безобидной» Spina bifida occulta (от латин. «скрытый»), которая обычно не влияет на функции организма, до тяжёлой миеломенингоцеле, которая характеризуется тяжёлыми нарушениями двигательной и чувствительной сферы нижних конечностей, а также органов малого таза – именно с этой формой большинство людей ассоциируют понятие спинно-мозговая грыжа или Spina bifida.
Встречаемость заболевания по данным исследователей в различных странах неодинаковая и составляет от 0,1 до 5 случаев на 1000 новорождённых. В России этот показатель составляет 0,1-0,2 % от числа всех новорождённых детей. В научной литературе встречается мнение, что данный порок развития встречается чаще у девочек.
Как развивается заболевание?
У нормально развивающегося эмбриона человека центральная нервная система, включающая в себя головной и спинной мозг, развивается из слоя клеток, который формируется ко 2 неделе беременности и носит название нервной пластинки. В начале 3 недели развития эмбриона данная пластинка утолщается, образуя продольную борозду. На 4 неделе борозда углубляется и с обеих сторон от неё развиваются складки, которые со временем сливаются и образуют закрытую трубку. Из данной трубки или цилиндра в дальнейшем развивается головной и спинной мозг. Параллельно с этим из зародышевых листков экто- и мезодермы развиваются мышцы, позвоночник и череп. В основе данных процессов лежат сложные механизмы дифференцировки и миграции клеток.
При Spina bifida и любом дефекте нервной трубки определённая часть нервной пластинки не сливается в цилиндр и остаётся дефектной. Если нервная трубка не сформировалась правильно, то и окружающие ткани, включая череп и позвоночник, также будут аномальными. Полости головного мозга вырабатывают церебро-спинальную жидкость, или ликвор, которая омывает и защищает нервные клетки. Данная жидкость в норме циркулирует между головным и спинным мозгом, проходя через большое затылочное отверстие, через которое головной мозг переходит в спинной мозг. Обычно со Spina bifida связана аномалия развития головного мозга и задней черепной ямки или аномалия Арнольда-Киари 2 типа. При данной патологии структуры ствола головного мозга, мозжечка, четвёртого желудочка смещаются в большое затылочное отверстие. При этом может возникнуть расстройство циркуляции ликвора с развитием гидроцефалии и, как следствие, повреждение нервных клеток в результате увеличения внутричерепного давления с возможными осложнениями в виде судорог, спастичности мышц и грозными нарушениями функции ствола головного мозга, где располагаются сердечно-сосудистый и дыхательные центры. Подобное состояние часто требует проведения неотложной хирургической коррекции в виде различных вариантов шунтирования с целью коррекции ликвородинамики.
В зависимости от периода внутриутробного развития и уровня возникновения дефекта нервной трубки будет определяться тяжесть и многообразие клинических проявлений. Так, раннее поражение верхнего конца нервной трубки будет приводить к развитию анэнцефалии (отсутствие головного мозга), а нижнего отдела – к миеломенингоцеле.
Классификация и характеристика наиболее распространённых форм Spina bifida
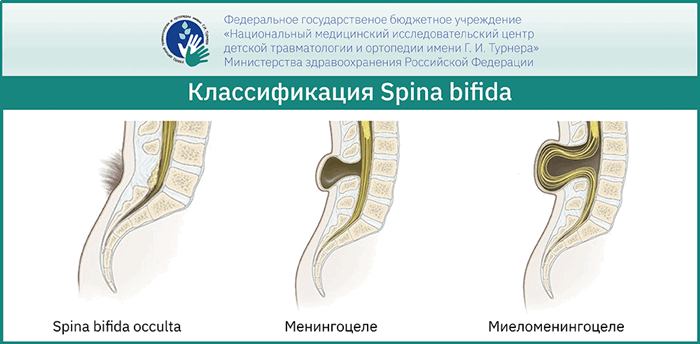
Выделяют открытые и закрытые формы Spina bifida или спинального дизрафизма в зависимости от вовлечённости в патологический процесс кожных покровов и связи структур спинномозгового канала с внешней средой. К открытым формам или Spina bifida относится aperta/cystica, когда в имеющемся дефекте кожных покровов формируется грыжевой мешок, заполненный ликвором. При наличии в грыжевом мешке только лишь твёрдой мозговой оболочки данный подтип Spina bifida aperta носит название менингоцеле, а при наличии в нём самого спинного мозга – миеломенингоцеле, и его корешков – миеломенингорадикулоцеле.
Закрытые формы спинального дизрафизма или Spina bifida occulta не имеют дефекта кожных покровов, но могут проявляться диспластическими изменениями на её поверхности в виде невусов или локального гипертрихоза. К данной форме можно отнести менингоцеле, липомиеломенингоцеле, миелоцистоцеле, липому терминальной нити, Spina bifida posterior, интрадуральную или интрамедуллярную липому, диастематомиелию, дермальный синус, синдром каудальной регрессии и другие.
Наиболее часто встречающейся и тяжёлой формой заболевания является миеломенингоцеле, встречающейся в 75 процентов случаев Spina bifida. Данное состояние является угрожающим для жизни плода и новорождённого ребёнка. Неврологические нарушения будут зависеть от уровня расположения миеломенингоцеле. Чем выше локализация, тем тяжелее нарушения функции органов и систем, находящихся ниже. Как правило, данный дефект наиболее часто локализуется в поясничном отделе и приводит к парезам и параличам нижних конечностей, нарушению мочеиспускания и дефекации. Если грыжа находится в грудных отделах, то неврологические нарушения гораздо более тяжёлые, вплоть до полной неподвижности. Грыжа шейного отдела является показанием к прерыванию беременности.
Менингоцеле встречается в 15-25 процентах случаев и может не иметь дефекта кожи. При этом отсутствие вовлечения в дефект спинного мозга и его компонентов может не приводить к тяжёлому неврологическому дефициту.
Скрытые формы спинального дизрафизма или Spina bifida occulta – наименее тяжёлый вариант заболевания. Может протекать бессимптомно и обнаруживаться случайно при лучевых методах исследования. Иногда может давать неприятные симптомы в виде периодических болей в спине, слабости в ногах или дизурических явлений.
Клинические проявления последствий заболевания Spina bifida
Многообразие последствий заболевания возникает в связи с поражением структур спинного мозга и его корешков, что приводит к нарушению чувствительности нижних конечностей и невозможности совершать активные движения по причине отсутствия иннервации мышц ниже уровня поражения с развитием вялого или периферического паралича.
Уровень поражения определяет количество вовлечённых мышечных групп нижних конечностей и степень двигательных нарушений локомоторного аппарата, проявляющихся от едва заметных нарушений походки до полного отсутствия движений.
Мышечный дисбаланс или полное отсутствие сократительной активности мышц (вялый паралич) вызывают формирование контрактур в суставах конечностей, приводят к развитию костных деформаций, к вывихам и подвывихам в суставах. Наиболее распространёнными ортопедическими проблемами являются вывихи/подвывихи тазобедренных суставов, сгибательные контрактуры в коленных суставах, вывихи костей голени, деформации стоп в виде косолапости, плано-вальгусной деформации, эквинусной деформации, пяточно-вальгусной деформации и т. д.
Сопутствующий порок развития позвоночника может являться причиной тяжёлых деформаций, таких как лордоз пояснично-кресцового отдела позвоночника и кифосколиоз, часто требующих хирургической коррекции.
Данные ортопедические проблемы могут являться причиной нарушения походки, затруднять ношение ортезов, вызывать развитие трофических нарушений кожи нижних конечностей.
Снижение осевой нагрузки и способности к передвижению на фоне нарушенной иннервации конечностей приводит к развитию остеопороза с риском развития патологических переломов костей нижних конечностей.
Нарушение иннервации мускулатуры органов малого таза увеличивает риск инфекций мочевыводящих путей и развития хронической почечной недостаточности.
Причины заболевания Spina bifida
Spina bifida является многофакторным заболеванием, но не имеет достоверной причины возникновения. Повышают вероятность развития Spina bifida следующие факторы:
- генетические;
- алкоголь;
- интоксикации;
- внутриутробная инфекция плода на раннем сроке;
- ионизирующее излучение;
- недостаточность фолиевой кислоты;
- приём противосудорожных препаратов на ранних сроках;
- приём цитостатиков;
- ожирение;
- сахарный диабет с гипергликемией (малокомпенсированный).
Диагностика Spina bifida
Современные методы диагностики позволяют выявить Spina bifida на ранних сроках беременности. Скрининговые УЗИ проводятся женщинам в каждом триместре беременности. В I триместре уже с 12 недели ультразвуковая диагностика может достоверно обнаружить эту патологию.
Комплексные программы скрининга новорождённых проводятся в Консультативно-диагностическом Центре (ул. Лахтинская, д. 12) ФГБУ «НМИЦ детской травматологии и ортопедии им. Г. И. Турнера» Минздрава России.
При подозрении на Spina bifida необходимо провести УЗИ плода c 3D-визуализацией.
При обнаружении Spina bifida проводят сканирование головного мозга на предмет выявления гидроцефалии или кровоизлияний. Также обследуют конечности плода на предмет выявления врождённой сопутствующей патологии.
Дополнительно исследуют сыворотку крови женщины на наличие альфа-фето-протеина и гомоцистеина, но, в настоящее время, в виду распространённости лучевой УЗИ-визуализации данные методы утрачивают своё значение.
Липомиеломенингоцеле (разновидность синдрома фиксированного спинного мозга)
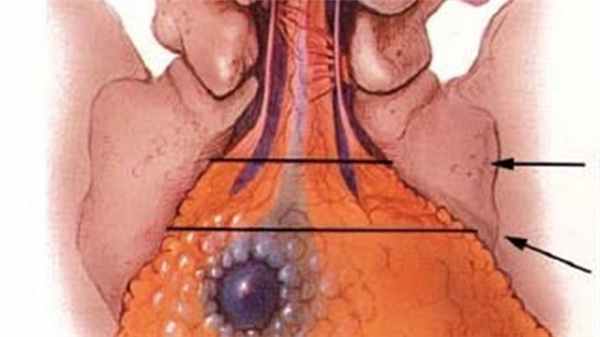
Вариант скрытой формы спинального дизрафизма, при котором в процессе эмбриогенеза не происходит полного разделения между нейроэктодермой и мезенхимальными элементами, формирующими позвоночник и мягкие ткани вокруг нервной трубки. Частота встречаемости составляет 1:4000 новорождённых и составляют 60% от всех липом спинного мозга. В зависимости от анатомических взаимоотношений липом со спинным мозгом выделяют следующие формы (классификация Chapman P): дорзальная липома, каудальная липома, переходная липома. По отношению к твёрдой мозговой оболочке и позвоночного канала разделяют на интрадуральную, интра,-экстрадуральную.
Клиническая картина липомиеломенингоцеле
При рождении в большинстве случаев липомы конуса спинного мозга асимптомы (70%) и проявляются кожными стигмами (признаками) спинального порока развития: подкожная липома, ангиома, гиперпигментация, кожные ямки, ассиметрия ягодичной складки. Наличие или отсутствие неврологической симптоматики зависит от степени вовлечения конуса, корешков конского хвоста и конечной нити в аномалию развития. Периоды возникновения и прогрессирования симптомов заболевания проявляются в периоды активного роста ребёнка с манифистацией симптомов от 0 до 4 лет, в подавляющем большинстве симптомы нейрогенной дисфункции возникают в 1-й год жизни. Неврологическая симптоматика представлена двигательными и чувствительными нарушениями в нижних конечностях, гипотрофией заинтересованных мышц. Длительная нейропатия корешков спинного мозга приводит к деформации стоп, укорочению конечностей, сколиозу позвоночника. Нарушение функции тазовых органов возникает в 30% случаев и в виду возрастных оссобенностей является скрытым.
Диагностика липомиеломенингоцеле
В 60% случаев диагноз липомы спинного мозга можно поставить по кожным признакам спинальных дизрафизмов. МРТ позвоночника и спинного мозга с большой достоверностью позволят выявить липому спинного мозга, определить форму и взаимоотношения жировой ткани по отношению к невральным структурам. На T1 – взвешенных изображениях МРТ для липомиеломенингоцеле характерен гиперинтенсивный сигнал, в режиме Т2 гипо-изоинтенсивность, с исходным расположением в каудальных отделах спинного мозга, распространяющийся в подкожную область через дефект оболочки и незаращенный позвоночный канал. Сопутствующими МРТ находками выявляются сирингомиелия, диастематомия, дермальный синус.
Диагностика скрытых нейрогенных функциональный нарушений является неотъемлемой составляющей при выявлении липом спинного мозга. Субклинические нейрогенные дисфункции выявляемые при электронейромиографии, уродинамических обследования, являются определяющими в сроках проведения оперативного лечения и динамическими критериями эффективности иссечения липом спинного мозга.
Хирургическое лечение липомы спинного мозга
Хирургическое лечение липом спинного мозга является одной из сложных и деликатных в хирургии спинальных дизрафизмов. Максимально радикальное и безопасное иссечение липомы - основа эффективного лечения этой группы детей. Особенно сложны переходные липомы, обрастающие вентральные, сакральные корешки спинного мозга. Ранее хирургическое лечение в первые 6 месяцев жизни позволяет профилактировать прогрессию неврологической симптоматики и ухудшение функции тазовых органов. У асимптомных детей предупреждает развития симптомов натяжения спинного мозга. Хирургическое лечение интрадуральной липомы спинного мозга является единственным методом позволяющим нивелировать компрессию спинного мозга.
Использование мультимодального интраоперационного мониторинга, микрохирургической техники, интраоперационного микроскопа, современных пластических материалов - позволяет малотравматично восстановить анатомические параметры спинного мозга и позвоночного канала, тем самым профилактировать вторичную фиксацию спинного мозга.
"АРБАЛЕТНЫЙ" РАЗРЕЗ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ЛИПОМИЕЛОЦЕЛЕ ПОЯСНИЧНО-КРЕСТЦОВОЙ ЛОКАЛИЗАЦИИ Текст научной статьи по специальности «Клиническая медицина»
СПИННОМОЗГОВАЯ ГРЫЖА / ЛИПОМИЕЛОМЕНИНГОЦЕЛЕ / ДОСТУП / РАЗРЕЗ / ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ / ЖұЛЫН ЖАРЫғЫ / ТіЛіК / ХИРУРГИЯЛЫқ ЕМДЕУ / SPINAL HERNIA / LIPOMYELOMENINGOCELE / ACCESS / INCISION / SURGICAL TREATMENT
Аннотация научной статьи по клинической медицине, автор научной работы — Усманханов О.А., Ахмедиев Т.М., Тухтамуродов Ж.А.
Введение. В связи с естественным стремлением хирургов к повышению радикальности и надёжности при иссечении пояснично-крестцовых липом и сравнительно высоким риском послеоперационных осложнений продолжаются поиски наиболее оптимальных доступов и хирургических приёмов. В статье представлен так называемый «арбалетный» разрез для хирургической коррекции пояснично-крестцовых липом. Материалы и методы: При хирургическом лечении 49 больных с липомами пояснично-крестцовой области «арбалетный» разрез был применён у 33 из них (81,5%). При выборе кожного разреза руководствовались возрастом больного, размерами и локализацией липомы, данными МРТ и МСКТ-миелографии. Выводы: Одним из преимуществ «арбалетного» разреза явилось то, что при существенном повышении радикальности хирургии он обеспечивал минимальную травматизацию спинного мозга и его элементов.
Похожие темы научных работ по клинической медицине , автор научной работы — Усманханов О.А., Ахмедиев Т.М., Тухтамуродов Ж.А.
Интраоперационная ректальная ампулярная манометрия при хирургическом лечении липом конуса спинного мозга у детей
Ортопедические аспекты хирургического лечения больных дегенеративно-дистрофическими заболеваниями пояснично-крестцового отдела позвоночника
Результаты этапного хирургического лечения пациентов с тандем-стенозами шейного и пояснично-крестцового отделов позвоночника
CROSSBOW" INCISION IN SURGICAL TREATMENT LIPOMENINGOCELE IN THE LUMBOSACRAL AREA
Introduction. Due to the natural desire of surgeons to improve the radicality and reliability of the excision of lumbosacral lipomas and the relatively high risk of postoperative complications, the search for the most optimal approaches and surgical techniques continues. The article presents the so-called" crossbow" incision for surgical correction of lumbosacral lipomas. Materials and methods: In the surgical treatment of 49 patients with lipomas of the lumbosacral region, a "crossbow" incision was used in 33 of them (81.5%). The age of the patient, the size and localization of the lipoma, MRI and MSCT myelography data were used to select the skin incision . Summary. One of the advantages of the "crossbow" incision was that with a significant increase in the radicality of surgery, it provided minimal trauma to the spinal cord and its elements.
Текст научной работы на тему «"АРБАЛЕТНЫЙ" РАЗРЕЗ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ЛИПОМИЕЛОЦЕЛЕ ПОЯСНИЧНО-КРЕСТЦОВОЙ ЛОКАЛИЗАЦИИ»
О.А. Усманханов, Т.М. Ахмедиев, Ж.А. Тухтамуродов
Ташкентский педиатрический медицинский институт, г. Ташкент, Узбекистан Республиканский научный центр нейрохирургии, г. Ташкент, Узбекистан
«АРБАЛЕТНЫЙ» РАЗРЕЗ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ЛИПОМИЕЛОЦЕЛЕ ПОЯСНИЧНО-КРЕСТЦОВОЙ ЛОКАЛИЗАЦИИ
Введение. В связи с естественным стремлением хирургов к повышению радикальности и надёжности при иссечении пояснично-крестцовых липом и сравнительно высоким риском послеоперационных осложнений продолжаются поиски наиболее оптимальных доступов и хирургических приёмов. В статье представлен так называемый «арбалетный» разрез для хирургической коррекции пояснично-крестцо-вых липом.
Материалы и методы: При хирургическом лечении 49 больных с липомами пояснично-крестцовой области «арбалетный» разрез был применён у 33 из них (81,5%). При выборе кожного разреза руководствовались возрастом больного, размерами и локализацией липомы, данными МРТ и МСКТ-миелогра-
Выводы: Одним из преимуществ «арбалетного» разреза явилось то, что при существенном повышении радикальности хирургии он обеспечивал минимальную травматизацию спинного мозга и его элементов.
Ключевые слова: спинномозговая грыжа, липомиеломенингоцеле, доступ, разрез, хирургическое лече-
Введение. Сложные формы spina bifida, такие как липомиелоцеле, являются сложной частью вертебро-медуллярной аномалии 4. Сам процесс иссечения липомиелоцеле - кропотливый труд, который требует пристального внимания в плане дефиксации спинного мозга. Существует большой арсенал общепринятых, в определённой степени классических разрезов кожи над липомой: вертикальный срединный (линейный), горизонтальный, окаймляющий, S-образный и другие 5.
Частота послеоперационных осложнений (расхождение швов, ликворея, ликворные подушки, менингит) довольно высокая и колеблется от 15 до 25% случаев [8, 9]. Усугубление неврологического дефицита после хирургии отмечается у 6,316,4% больных 14.
Цель исследования. Определить преимущество использования «арбалетного» разре-
за над линейным, и оценить его возможности для широкого обзора анатомо-топографических отношений костных и невральных структур и стратегии хирургических манипуляций при пояснич-но-крестцовых липомах.
Характеристика собственного материала и методик исследования. По поводу липом пояснично-крестцовой области оперировано 49 больных в возрасте от 3,5 мес. до 38 лет (средний возраст - 8,5 лет). Лиц женского пола преобладала над мужским. Липомы у всех больных располагались экстра-интравертебрально. Латерализация или асимметрия распространения экстраверте-бральной порции липомы отмечена у 13 больных (25 %). У большинства больных с липомами имело место сочетание спинального порока с другими аномалиями (табл. 1). Наиболее частыми спутниками липом были мальформация Арнольда-Киа-ри и сирингомиелия.
НЕЙРОХИРУРГИЯ И НЕВРОЛОГИЯ КАЗАХСТАНА
СОПУТСТВУЮЩИЕ ЛИПОМЕ ДРУГИЕ АНОМАЛИИ ЦНС
Аномалия абс. число (%)
мальформация Арнольда-Киари 24 (44,4%)
Сирингомиелия 12 (25,9%)
Диастематомиелия 6 (12,1%)
дермальный синус 3 (6%)
внутричерепные арахноидальные кисты 2 (4,5%)
Гидроцефалия 1 (2%)
В клинической картине заболевания у пациен- доступ к сакральным отделам позвоночного кана-
тов выявлялись двигательные и чувствительные нарушения, трофические расстройства, нарушения функции тазовых органов (преимущественно по типу недержания мочи), ортопедические нарушения.
Всем больным в качестве рутинного обследования, были выполнены магнитно-резонансные томограммы (МРТ) не только пояснично-крестцо-вой области, но и головного мозга. Большинству больных перед операцией была выполнена муль-тиспиральная компьютерно-томографическая (МСКТ)-миелография. Предоперационная анато-мо-топографическая характеристика липом проводилась на основании клинических, МРТ и МСКТ данных. При изучении взаимоотношения липомы со спинным мозгом отмечено, что дорзальная разновидность липом имелась у 14,8%, каудаль-ная 37%, транзиторная или промежуточная 48,1% пациентов.
Незаращение дужек позвонков (spina bifida) - один из значимых морфологических и рентгенологических признаков липомиелоцеле. Частой находкой у обследованных было одновременное незаращение дужек позвонков L5 и S1 (помимо расщепления дужек соседних позвонков), что обнаружено 63% больных.
Для повышения радикальности и надёжности хирургического лечения липомиелоцеле нами применён и предложен так называемый «арбалетный» разрез кожи, который состоит из двух составляющих компонентов (разрезов). Первый компонент - «купол» в виде дуги огибает межягодичную складку по максимально возможному радиусу удаления от потенциального очага инфицирования. Функциональное предназначение «купола», благодаря своей лоскутной форме, во-первых, обеспечить радикальную резекцию экстраверте-бральных порций липомы, во-вторых, обеспечить
ла. Второй компонент - «шпиль», распространяется от вершины «купола» вверх по срединной линии (рис. 1). При разработке такого разреза мы исходили из потребностей в следующих хирургических действиях: 1) полная резекция отдалённых от средней линии экстравертебральных порций липомы; 2) свобода доступа (при необходимости) к сакральным отделам позвоночного канала; 3) расширение доступа в оральном направлении (по показаниям дополнительная ламинэктомия вышележащих позвонков). Дополнительная ламинэк-томия (арбалетный разрез) с целью расширения обзора и свободы манипуляций на интраверте-бральных структурах выполнена 74% больным. Ламинэктомия в оральном направлении осуществлена у 80%, в каудальном - у 5%, одновременно и в оральном, и в каудальном - у 15%.
После выполнения основного этапа операции, пластика дефекта твёрдой оболочки мозга современными синтетическими материалами произведена у 22% пациентов.
Результаты и их обсуждение.
При выборе разновидности кожного разреза руководствовались возрастом больного, размерами липомы, данными МРТ и МСКТ-миелографии. Арбалетный разрез кожи применен у 33 (81,5%) больных и традиционный линейный у 16 (18,5%) пациентов. При этом линейный разрез применялся только у детей грудного и младшего возраста (максимальный возраст 3,5 года). В этом возрасте липома ещё не «успевала» широко разрастись, и все экстравертебральные порции липомы могли быть свободно удалены из линейного разреза. Наружные размеры липом при применении линейного разреза составляли от 6х5 до 6х7 см, а при применении арбалетного разреза - от 7х7 до 19х12 см.
Широкий доступ при «арбалетном» разрезе обеспечивал всесторонний обзор и свободу манипуляций, полипозиционное выделение апо-невротической и костной частей ворот липомы. Тотальная резекция экстравертебральной части липомы предоставляла свободу действий на апоневрозе паравертебральных мышц (для последующей пластики грыжевых ворот по Бауеру). Дополнительная ламинэктомия, выполненная у % больных, позволяла максимально визуализировать интравертебральные порции липомы, выделить интактные участки твёрдой оболочки мозга, выполнить менингиолиз, миелолиз и ради-кулолиз, а в ряде случаев рассечь терминальную нить. Выделение интактных и «добротных» участков твёрдой оболочки мозга давало возможность в последующем герметично ушить оболочку, либо выполнить её пластику. Пластика грыжевых ворот по Бауеру (мышечно-апоневротическими лоскутами) при «арбалетном» разрезе, так же могла
быть выполнена без особых технических трудностей.
Сравнительный анализ результатов в аспекте возможностей устранения фиксации спинного мозга, свидетельствует не в пользу «арбалетного» разреза (табл. 2). Хотя с другой стороны исключительно при применении арбалетного разреза отмечено улучшение функции тазовых органов. Осложнение в виде псевдоменингоцеле возникло только у 1 больного, хотя это состояние не требовало специального лечения и постепенно регрессировало. Раневой ликвореи не отмечено, и это, на наш взгляд, результат тщательных манипуляций на твёрдой оболочке мозга, а также применения методики длительного наружного дренирования сформированного субдурального пространства. Летальных исходов не было. Представленные цифры свидетельствуют не о преимуществах линейного разреза над «арбалетным», а скорее о грубости морфофункциональных нарушений при липомах больших размеров.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЛИПОМ ПОЯСНИЧНО-КРЕСТЦОВОИ ОБЛАСТИ
«арбалетный» разрез линейный разрез
неврологический статус улучшился 16 2
неврологический статус без изменений 5 3
неврологический статус ухудшился 1 -
первичное заживление раны 20 4
вторичное заживление раны 2 1
Таким образом, выбор хирургического разреза при пояснично-крестцовых липомах в основном зависит от локализации и распространённости процесса. «Арбалетный» разрез эффективен при обширных экстра-, интравертебральных липомах размерами более чем 7х7 см. Авторы далеки от мысли, что предлагаемый разрез является универсальным. При малых размерах экстравертебральной порции липомы вполне достаточен линейный вертикальный разрез. Громоздкость «арбалетного» разреза и продолжительность операции во времени, всё же, на наш взгляд, оправданы конечной целью радикальности и надёжности, так как он позволил свести к минимуму травматичность манипуляций на специфической нервной ткани и оболочках мозга, что в свою очередь предопределяло профилактику возникнове-
ния послеоперационных неврологических выпадений, либо их нарастания и усугубления. Выводы:
При выборе разновидности кожного разреза целесообразно учитывать возраст больного, размеры липомы, данные МРТ и МСКТ-миелографии.
«Арбалетный» разрез при липомиелоцеле обеспечивает свободу манипуляций, как в области грыжевых ворот, так, и за его пределами. Предоставляет широкий доступ к структурам позвоночного канала, максимальную радикальность хирургических приёмов, создаёт благоприятные условия для устранения фиксации спинного мозга, минимальный риск послеоперационных осложнений (в частности инфицирования), в том числе и оптимальное заживление ран.
В дополнительной ламинэктомии с целью расширения обзора и свободы манипуляций
НЕЙРОХИРУРГИЯ И НЕВРОЛОГИЯ КАЗАХСТАНА №3 (56)
на интравертебральных структурах липомиелоце-ле нуждаются 74% больных. Причём в подавляющем большинстве наблюдений ламинэктомия выполняется в оральном от липомы направлении.
Пластика дефекта твёрдой оболочки мозга синтетическим материалом после выполнения основного этапа операции, требуется 22% пациентов.
1. Баиров Г.А., Дорошевский Ю.Л., Немилова Т.К. Атлас операций у новорожденных. // Л. Медицина. - 1984. - 256 с.
2. Дорошенко П.В. Модифицированный пе-реднебоковой ретроперитонеальный доступ к поясничному отделу позвоночника для оперативного лечения больных с компрессиями конского хвоста и поясничных спинномозговых корешков (топографо-анатомическое исследование): Автореф. дис. . канд. мед. наук. - М., 2004 - 21 с.
3. Вецка П., Цеков Хр., Унджия С. Современные проблемы лечения Spina bifida aperta // Вопросы нейрохирургии. - 1988. - Вып. 2. - С. 39-42.
4. Воронов В.Г. Пороки развития спинного мозга и позвоночника у детей. - СПб., 2002. - 399 с.
6. Gallia G.L., Burger P.C., Suk I., Bagley C.A., Wolinsky J-P., Garonzik I.M., Gokaslan Z.L. Concomitant conus medullaris ependymoma and filum terminale lipoma: case report // Neurosurgery. - 2006. - Vol. 58. - P. 1214-1215.
7. Зябров А.А. Синдром фиксированного спинного мозга (клиника, диагностика, хирургическая коррекция, ближайшие и отдаленные результаты) в детском возрасте: Автореф. дис. . канд. мед. наук. - СПб., 2012. - 24 с.
8. Ерофеев Е., Кушель Ю., Озеров С. Осложнения хирургического лечения детей с синдромом
фиксированного спинного мозга // IV съезд нейрохирургов России. - Москва. - 2006. - С. 391-392.
9. Орлов М.Ю. Особенности распространения липом при липоменингоцеле у детей // Бюл. УАН. - 1998. - № 6. - С. 60
10. Орлов Ю.А., Цимейко О.А., Орлов М.Ю. Липоменингоцеле у детей современные возможности диагностики и лечения // Украинский нейрохирургический журнал. - 2001. - № 1. - С. 73-77.
11. Притыко А.Г., Бурков И.В., Николаев С.Н. Диагностика и хирургическое лечение каудаль-ных пороков развития позвоночника и спинного мозга. - Ульяновск: «Симбирская книга», 1999. - 96 с.
12. Слынько Е.И., Золотоверх А.М., Вербова В.В., Пишанов Р.Т. Выбор доступа при удалении опухолей крестца и крестцового канала // Украинский нейрохирургический журнал. - 2011. - № 4. - С. 37-40.
13. Федосеева М.А., Юмашев Г.С., Хасанов М. Аномалии развития поясничного и крестцового отдела позвоночника. - Ташкент: Медицина УзССР, 1986. - 104 с.
14. Хачатрян В.А., Орлов Ю.А., Осипов И.Б., Елик-баев Г.М. Спинальные дизрафии. Нейрохирургические и нейроурологические аспекты. - СПб, «Десятка», 2009. - 304 с.
15. Danish S.F., Samdani A.F., Storm P.B. Use of allogeneic skin graft for the closure of large meningomyeloceles: Technical case report // Neurosurgery - 2006. - Vol. 58. - Suppl 2. - P. 376.
О.А. Усманханов, Т.М. Ахмедиев, Ж.А. Тухтамуродов
Ташкент педиатриялык медициналык институт, Ташкент к. Эзбекстан
Республикалык шлыми нейрохирургия орталыы, Ташкент к., Эзбекстан
БЕЛ-СЕГ1ЗКеЗ ЛОКАЛИЗАЦИЯСЫНДАГЫ ЛИПОМИЕЛОЦЕЛЕН1 ХИРУРГИЯЛЫК ЕМДЕУ КЕЗ1НДЕГ1 АРБАЛЕТТ1К Т1Л1К
Kipicne: Бел-сегiзквз липомаларын алып тастаудык тYбегейлiлiгi мен сенiмдiлiгiн арттыруFа деген хи-рургтердщ умтылысына жэне операциядан кейнп аскынулардык салыстырмалы тYрдегi жоFары каутне байланысты неF¥рлым октайлы жолдар мен хирургиялык эдiстердi iздестiру жалFасып келедК Макалада бел-сегiзквз липомасын хирургиялык тYзетуге арналFан «арбалеттiк» деп аталатын ттк тYрi сипатталады.
Материалдар мен эдктер: Бел-сегiзквз аймаFынык липомасы бар 49 наукастык 33-iнде (81,5%) «ар-балеттк» тiлiк колданылды. Терi тiлiгiн такдау кезiнде наукастык жасы, липоманык квлемi мен орналасу орны, МРТ жэне МСКТ-миелография деректерi басшылыкка алынды.
Корытынды: «Арбалеттiк» тiлiктi колдану кезiнде байкалFан артыкшылыктардык бiрi - хирургиянык тYбегейлiлiгiн айтарлыктай арттырFан кезде ол жулын мен онык элементтерiнiк минималды жаракатын камтамасыз етедi.
Нeгiзгi свздер: жулын жарыFы, липомиеломенингоцеле, тiлiк, хирургиялык емдеу.
O.A. Usmankhanov, T.M. Akhmediev, J.A. Tukhtamuradov
Tashkent Pediatric Medical Institute, Tashkent, Republic of Uzbekistan
Republican Scientific Center of Neurosurgery, Tashkent, Republic of Uzbekistan
"CROSSBOW" INCISION IN SURGICAL TREATMENT LIPOMENINGOCELE IN THE LUMBOSACRAL AREA
Introduction. Due to the natural desire of surgeons to improve the radicality and reliability of the excision of lumbosacral lipomas and the relatively high risk of postoperative complications, the search for the most optimal approaches and surgical techniques continues. The article presents the so-called" crossbow" incision for surgical correction of lumbosacral lipomas.
Materials and methods: In the surgical treatment of 49 patients with lipomas of the lumbosacral region, a "crossbow" incision was used in 33 of them (81.5%). The age of the patient, the size and localization of the lipoma, MRI and MSCT myelography data were used to select the skin incision.
Summary. One of the advantages of the "crossbow" incision was that with a significant increase in the radicality of surgery, it provided minimal trauma to the spinal cord and its elements.
Keywords: spinal hernia, lipomyelomeningocele, access, incision, surgical treatment.
Липома - диагностика, методы лечения
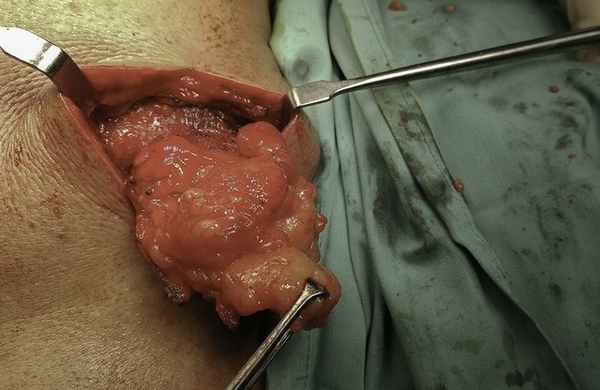
Доброкачественные новообразования, развивающиеся в жировой ткани, прежде всего, кожи, но бывают липомы молочной железы, головного и спинного мозга. Опухоли растут медленно и редко малигнизируются.
Липомы возникают у многих людей, по статистике они есть у каждого сотого человека. Мужчины и женщины одинаково подвержены заболеванию.
Что такое липома?
Липома – это мягкое на ощупь, округлое, заполненное жиром образование, которое чаще всего вырастает под кожей. В быту липомы нередко называют жировиками. В подавляющем большинстве случаев липомы безобидны, их относят к доброкачественным опухолям. На коже липом не бывает, они формируются в жировой ткани кожи или в подкожной клетчатке. Таким образом, липома может возникнуть на любой части тела, где есть жировая ткань. Обычно у человека возникает 1-2 образования. Очень редко встречаются липомы множественные, это состояние называют множественным семейным липоматозом, он чаще возникает у мужчин.
Как липома выглядит?
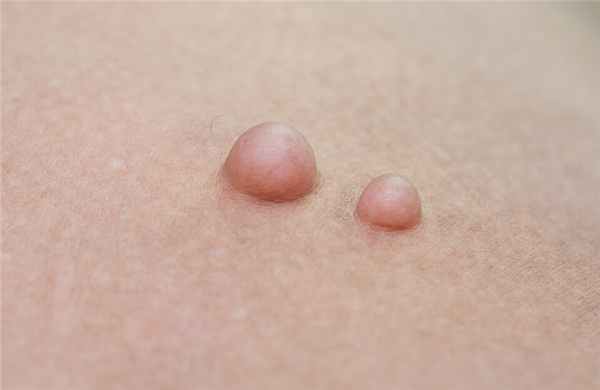
Медленно растущие мягкие образования под кожей — жировики — обычно являются липомами.
Выглядит липома как “шарик” или “комок” под кожей. Величина образования варьирует, оно может быть размером от горошины и до нескольких сантиметров в поперечнике. Липома при пальпации (ощупывании) мягкая, по плотности напоминает резину, не спаяна с нижележащими тканями.
Причины возникновения липомы
Обычно липомы возникают в среднем возрасте – между 40 и 60 годами, у детей это патология встречается редко.
Точные причины появления липом неизвестны. Но они чаще возникают
- у пациентов с редким наследственным заболеванием – синдромом Коудена
- при синдроме Гарднера
- при болезни Маделунга.
Нередко липомы находят у членов одной семьи, т.е. генетическая предрасположенность к ним передается по наследству. Ожирение не приводит к повышенному риску образования липом.
Классификация
По анатомическому признаку липомы подразделяют на:
- липомы головы, лица и шеи, которые, соответственно, располагаются на голове, на лице, на шее
- липомы туловища – на спине, животе
- липомы конечностей – на ногах и руках
- липомы грудной клетки – образованием затронуты легкие
- липомы внутри брюшных органов – новообразования могут затрагивать почки
- липомы семенного канатика
- липомы других локализаций.
Классификация липомы по МКБ-10
По международной классификации болезней липомы относят к разделу D17, т.е. к доброкачественным образованиям жировой ткани.
Механизм образования
Иногда триггером, запускающим образование липомы, считают повреждение кожи. Липома представляет собой новообразование из жировых клеток. Ее рост начинается из одной клетки, которая растет и делится быстрее, чем окружающие ее ткани. Под микроскопом липома представляет собой скопление узелков из зрелых жировых клеток (адипоцитов), разделенных фибромускулярными перегородками. Доброкачественность образования устанавливают при отсутствии атипии ядер или самих клеток.
Симптомы и признаки липом
Липомы растут очень медленно и обычно не вызывают никаких симптомов, кроме уплотнения в виде “шишки” или “шарика” под кожей. Внутренние липомы также обычно ничем себя не проявляют, т.е. бессимптомны.
Липома молочной железы
Липома в молочной железе обычно возникает у женщин после наступления менопаузы. Как правило, это образование размером до 1 см, весом до нескольких граммов. Липому молочной железы размером более 5 см и весом более 500 г называют гигантской.
Основные признаки липомы молочной железы:
- безболезненность
- мягкость на ощупь
- возможность смещения под кожей. Т.е. она не спаяна плотно с окружающими тканями и не изменяет внешний вид кожи над ней.
Так как липомы часто располагаются в толще железы и не имеют никаких симптомов, то их нередко обнаруживают случайно, во время плановой маммографии или УЗИ.
Липома молочной железы не повышает риск рака молочной железы и очень редко трансформируется в злокачественную опухоль.
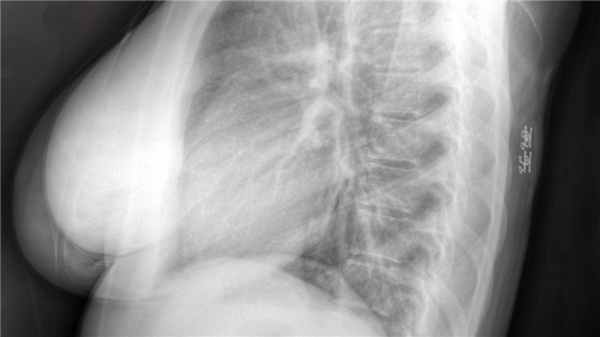
Липома молочной железы. Фото: © Nevit Dilmen / Wikipedia (Creative Commons Attribution-Share Alike 3.0 Unported license)
Липома головного и спинного мозга
Липомы головного мозга также выявляют случайно, когда у пациентов старшей возрастной группы проводят МРТ или КТ мозга по каким-то другим причинам, например, при нарушении когнитивных функций, эпилепсии. Липомы могут быть обнаружены в любом отделе мозга, тем не менее 50% – это перикалозальные липомы, в свою очередь 45% которых ассоциированы с агенезией мозолистого тела. 25% составляют липомы квадригименальной цистерны и 15% – липомы супраселлярной цистерны. Так как липомы мозга не имеют симптомов, хоть и часто сочетаются с какими-то пороками, например, агенезией мозолистого тела, то и лечения они не требуют. Хирургическое лечение сопряжено с большим риском осложнений и не имеет никаких преимуществ. Если возникают гидроцефалия или судорожный синдром, то лечение проводят по общим правилам.
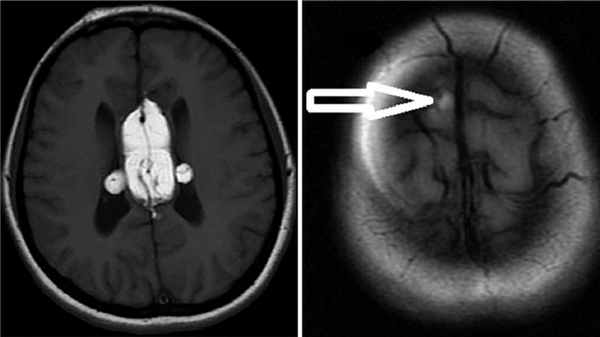
Липома мозолистого тела головного мозга. Фото: Journal of neurosciences in rural practice / Open-i (Attribution-NonCommercial-ShareAlike 3.0 Unported)
Липома у детей
Липомы позвоночника составляют 35% всех новообразований спинного мозга, чаще встречаются у девочек.
Липома спинного мозга подразделяется на несколько клинических вариантов:
- липомиеломенингоцеле. Это врожденная патология, при которой жировые образования расположены вдоль позвоночника и проникают внутрь спинномозгового канала, соединяясь со спинным мозгом. Эта липома внешне выглядит как объемное образование внизу позвоночника. У ⅓ пациентов образование проявляет себя нарушениями мочеиспускания. Реже пациентов беспокоит искривление стоп, боль в спине. Лечение хирургическое.
- липома терминальной нити, при которой жировая ткань расположена в конечной нити спинного мозга. Иногда это состояние рассматривают как синдром натяжения концевой нити. Это редкое заболевание, которое эффективно лечат хирургической операцией, менее опасной, чем в предыдущем случае.
- липома спинного мозга (интрадуральная) встречается редко и составляет 4% от всех липом. Чаще ее выявляют в грудном отделе позвоночника у детей, патологии костей или кожи при ней не бывает. Если вырастает до больших размеров, то проявляет себя симптомами сдавления спинного мозга. Это одно из самых малоизученных новообразований.
Липома у взрослых
Кроме обычных подкожных липом, в зрелом возрасте могут быть:
- Эпидуральный липоматоз, который возникает при избыточном синтезе жира в эпидуральном пространстве, то есть между позвонками и твердой оболочкой спинного мозга. Это нередкое осложнение при синдроме Кушинга, тяжелом ожирении, приеме глюкокортикостероидов. Дебютирует патология синдромом “конского хвоста”, лечат его отменой стероидов или снижением веса.
- Ангиомиолипома, состоящая из аномально разросшихся сосудов и жировой ткани. Чаще всего ее обнаруживают в поясничном или грудном отделах позвоночника. Как правило, возникает в теле одного позвонка и может проявляться болью в спине, так как уменьшает высоту позвонка и приводит к сдавливанию нервных корешков. Образование обычно выявляют случайно у людей в возрасте 30-40 лет. При сильной компрессии, т.е. при сдавливании нервных структур, проводят лечение – пункционную вертебропластику (“цементирование” позвонка). Иногда ангиомиолипому обнаруживают в почке. При небольших размерах (до 1,0-1,5 см) лечения не требует, за образованием наблюдают, периодически выполняя ультразвуковое исследование.
Диагностика липом
Липому под кожей легко диагностируют при осмотре и прощупывании.
Липомы внутри организма выявляют с помощью:
В неясных случаях проводят биопсию, при которой небольшое количество ткани исследуют под микроскопом.
К какому врачу обратиться?
Так как липома может вырасти в любом месте организма, то её диагностируют и лечат врачи разных специальностей. Это зависит от места расположения образования. Липомами на коже занимаются хирург и дерматолог, липомами в области молочной железы – маммолог, липомами мозга или позвоночника – нейрохирург.
В чем отличие атеромы от липомы?
Липома представляет собой образование из жировой ткани, тогда как атерома – это скопление секрета сальной железы из-за закупорки ее протока. Соответственно, атерома не может возникнуть там, где нет сальных желез, т.е. в легких, мозге, брюшной полости, семенном канатике и т.д. Атерома чаще растет на волосистой части головы, имеет тенденцию к воспалению и нагноению, располагается более поверхностно. При воспалении атеромы она увеличивается в размерах, возникает покраснение, чего не бывает при липоме. Для того, чтобы выяснить, что имеется у пациента – атерома или липома – проводят УЗИ.
Методы лечения
Если липомы безболезненны и небольших размеров, то лечения не нужно. Липому молочной железы обычно наблюдают. Для этого маммографию проводят каждые 6 месяцев, и, если образование не растет, его не удаляют.
Надо ли удалять липому?
Вмешательство необходимо, если она:
- сдавливает нервные окончания
- вызывает дискомфорт
- изменяет свою консистенцию или размер
- рецидивирует после удаления
- растет.
Перед удалением внутрь липомы могут вводить кортикостероиды для того, чтобы уменьшить её размер.
Хирургическое удаление липомы
Используют следующие методы удаления:
- Хирургическим путем, когда измененную ткань иссекают скальпелем под местной анестезией. Затем проводят ушивание раны.
- Липосакцию. В липому вводят иглу и с помощью шприца удаляют содержимое.
- Удаление липомы лазером. Этот щадящий метод используют для удаления образований размером более 3 см. При вмешательстве практически нет риска травмирования здоровой ткани и минимальна вероятность кровотечения или инфицирования. После удаления лазером редко возникают шрамы или рубцы.
Лечение липомы народными средствами
Так как липому обычно не нужно лечить, то не стоит пытаться свести ее народными средствами. Прикладывание льда или прогревание бесполезны, так как эти процедуры не влияют на жировую ткань.
Профилактика
Обычно не имеет смысла, так как четкой причины возникновения патологии не выявлено. При эпидуральном липоматозе, причиной которого может быть ожирение, профилактикой считают поддержание нормального веса.
24.07.2012 г. МРТ пояснично-крестцового отдела позвоночника девочка 2 мес Липомиеломенингоцеле. КОНКУРС.
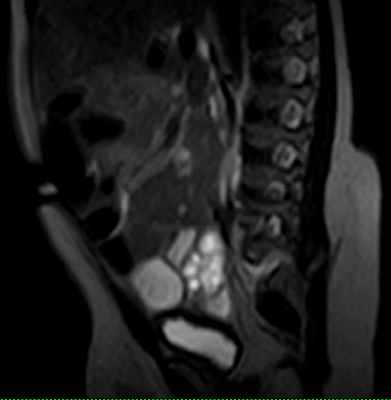
На МРТ пояснично-крестцового отдела определяяетмя подкожная липома , к оторая через дефект (ращепление) дужек сакральных позвонков распространяетя в позвоночный канал, соединяеясь на этом уровне с аномально низко расположеным спинном мозгм (Tethered spinal cord syndrome). Также мы видим выхождение спинного мозга и оболочек через дефект дужек сакральных позввонков. Такая врожденная аномалия развития позвоночника и спинного мозга называется - ЛИПОМИЕЛОМЕНИНГОЦЕЛЕ.(вариант спинального дизарфизма).
Спинальный дизрафизм (от латинского raphe – шов) – это неоднородная многообразная группа врожденных аномалий развития позвоночника и спинного мозга, характеризующаяся расщеплением позвоночника (т.н. spina bifida).
Существует два основных варианта спинального дизрафизма:
-скрытый спинальный дизрафизм (spina bifida occulta), при котором нет нарушения целостности кожных покровов над дефектом позвонков;
-открытое (грыжевое) расщепление позвоночника (spina bifida cystika), при котором имеется явное нарушение целостности кожных покровов над незаращенным участком позвоночника с формированием грыжевого выпячивания, содержимым которого может быть спинной мозг и/или его оболочки.
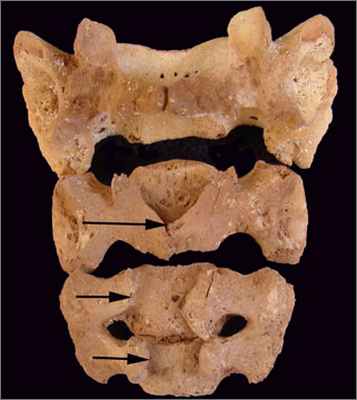
Скрытый спинальный дизрафизм (ССД) встречается чаще всего. Эта форма незаращения позвоночника может не сопровождаться никаким неврологическим дефицитом, если отмечается только расщепление дужки одного-двух позвонков, чаще пятого поясничного (spina bifida L5) и/или первого крестцового (spina bifida S1). У большинства людей с такой формой незаращения позвоночника не наблюдается никаких симптомов или проблем, часто они узнают о своем дефекте случайно при рентгенологическом исследовании позвоночника, проводимом по иным причинам. Вот почему истинная частота ССД неизвестна.
Однако понятие «ССД» включает также такие формы, как миелодисплазия, синдром фиксированного спинного мозга, расщепление спинного мозга, спинальные липомы, дорсальный дермальный синус и др. В этих случаях ССД обычно сопровождается выраженной ортопедо-неврологической симптоматикой: нижним парапарезом (слабостью в ногах), снижением мышечного тонуса, мышечными атрофиями, недержанием мочи и кала, снижением чувствительности в ногах и промежности, деформациями позвоночника (кифоз, лордоз, сколиоз) и ног, паралитической нестабильностью тазобедренных суставов и т.п.
При наличии неврологической симптоматики ССД довольно часто (до 70-80% случаев) сочетается с гидроцефалией – водянкой головного мозга, нередко встречаются сочетания с такими пороками развития, как синдром Арнольда-Киари (низкое расположение полушарий мозжечка) и сирингомиелия (образование полостей спинного мозга). ССД может также иметь кожные проявления: участок избыточного оволосения (гипертрихоз), ангиомы, свищевой ход, подкожная липома, хвостовой придаток («псевдохвостик») или их сочетание.
ССД может проявляться не сразу после рождения ребенка, а отсрочено, при этом неврологические нарушения медленно прогрессируют, и для установления точного диагноза необходимо производить магнитно-резонансную томографию (МРТ) спинного мозга. Медленное прогрессирование симптомов ССД по мере роста ребенка, связано, прежде всего, с т.н. синдромом фиксированного (натянутого) спинного мозга (ФСМ), называемого также синдромом жесткой концевой, или терминальной, нити. Иногда в русскоязычной литературе используется еще термин тетеринг-синдром (от английского tethered cord syndrome – синдром «привязанного» спинного мозга).
ФСМ характеризуется аномально низким (ниже уровня L1-L2) расположением концевой части спинного мозга – конуса. Известно, что спинной мозг по мере внутриутробного развития, а затем и роста ребенка, перемещается в позвоночном канале вверх. Будучи же патологически фиксированным жесткой концевой нитью, спинной мозг не может следовать за растущим позвоночником. У маленьких детей неврологических нарушений может не быть, поскольку спинной мозг хотя и фиксирован, но еще не натянут. Но по мере роста постепенно происходит нарушение кровообращения в нижних отделах спинного мозга в результате его натяжения. Это приводит к появлению боли в пояснице и ногах, нарушению походки и развитию нижнего вялого парапареза, мышечной атрофии, укорочению и деформациям нижних конечностей, нарушениям чувствительности в ногах и промежности, недержанию мочи и кала, развитию сколиоза и другим проблемам.
Расщепление спинного мозга (РСМ) – еще один вариант ССД, который характеризуется наличием внутри спинномозгового канала костной, хрящевой или фиброзной перегородки, которая полностью или частично разъединяет спинной мозг вдоль на две половины (гемихорды). Согласно современной классификации по Pang выделяют расщепление спинного мозга двух типов. При типе I имеется две разделенные перемычкой гемихорды, каждая из которых находится в собственном дуральном мешке, при типе II обе половины спинного мозга заключены в один дуральный мешок и разделены фиброзной перегородкой. Симптоматика при РСМ определяется фиксацией спинного мозга, который патологически удерживается костным, хрящевым или мягкотканым шипом или перемычкой. У 90% больных выявляются кожные признаки ССД, чаще всего, гипертрихоз. Расщепленный спинной мозг хорошо виден на МРТ, но уровень перемычки лучше определять при помощи рентгеновской компьютерной томографии (КТ), которая визуализирует костные структуры.
Одной из форм ССД являются также спинальные липомы (доброкачественные опухоли из жировой ткани). Они могут располагаться интрадурально или быть припаянными к конусу спинного мозга или терминальной нити. Интрадуральные (расположенные внутри твердой мозговой оболочки) липомы в пояснично-крестцовом отделе, так же, как и липомы, инфильтрирующие конечную нить, ведут к патологической фиксации и натяжению спинного мозга. Липомы конуса спинного мозга тоже фиксируют его на нижнепоясничном уровне, и могут сочетаться с подкожным миеломенингоцеле или миелоцистоцеле (см. ниже).
Дорсальный дермальный синус – это порок развития, характеризующийся наличием свищевого хода, который чаще всего располагается в пояснично-крестцовом отделе позвоночника и может доходить до субарахноидального пространства спинного мозга. Свищевой ход выстлан эпителием. Характерным признаком дермального синуса является наличие маленького кожного отверстия, вокруг которого имеется покраснение или избыточное оволосение. Свищевой ход служит проводником инфекции и источником развития менингитов, эпидуральных и субдуральных абсцессов.
Лечение больных с различными формами ССД – хирургическое. Цель операции при синдроме ФСМ – освобождение спинного мозга. В остальных случаях цели и техника оперативного вмешательства зависят от формы ССД. Улучшение неврологических функций или их стабилизация наступает у 90% прооперированных пациентов.
При открытом (грыжевом) расщеплении позвоночника, называемом также спинномозговой грыжей, через дефект кости выбухает состоящий из мозговых оболочек грыжевой мешок различной величины, содержащий или только спинномозговую жидкость – ликвор (менингоцеле), или ликвор и ткань корешков спинномозговых нервов (менингорадикулоцеле), или же, помимо названных компонентов, ткань спинного мозга (миеломенингоцеле). Различают также миелоцистоцеле – локальное расширение центрального канала с выбуханием задней стенки истонченного спинного мозга. Миелоцистоцеле содержит скопившийся в расширенном центральном канале спинного мозга ликвор, окруженный веществом спинного мозга, его оболочками и задними корешками спинномозговых нервов. При спинномозговых грыжах часто отмечается истечение ликвора.
Неврологические нарушения при открытых формах спинального дизрафизма зависят от содержимого грыжевого мешка и его локализации (шейный, грудной или пояснично-крестцовый уровень). Около половины менингоцеле бессимптомны, но в 25% случаев менингоцеле сочетается с гидроцефалией. При миеломенингоцеле частота развития водянки головного мозга составляет около 70-80%. Примерно в таком же проценте случаев миеломенингоцеле локализуется в поясничном и пояснично-крестцовом отделе позвоночника, обусловливая нижний вялый парапарез или полное отсутствие активных движений в нижних конечностях, нарушение чувствительности в ногах и/или тазовые расстройства. При локализации спинномозговой грыжи на шейном уровне в патологический процесс вовлечены и верхние конечности.
Открытые формы спинального дизрафизма – спинномозговые грыжи – не представляют трудности для диагностики и служат объектом хирургического вмешательства. Операция избавляет больных от грыжевого выпячивания, но прогноз менее благоприятен в отношении обратного развития неврологических нарушений, которые являются следствием необратимых изменений спинного мозга и его корешков. После хирургического устранения грыжевого выпячивания может развиться гидроцефалия. У 10-75% детей после коррекции миеломенингоцеле и липомиеломенингоцеле развивается синдром ФСМ.
После хирургического лечения различных форм спинального дизрафизма дети нуждаются в длительном восстановительном лечении и реабилитации.
Подкожная липома, которая проходит через срединный дефект люмбо-сакральной фасции, дужку позвонка, ТМО и соединяется с ненормально низко фиксированным СМ. Соединение может быть терминальным, дорсальным или переходным (между предыдущими двумя формами).
Интрадуральная жировая опухоль также носит название липомы конского хвоста. В дополнение к тому, что конус СМ расположен ненормально низко, он расщеплен по средней линии по задней поверхности обычно на том же уровне, где имеет место расщепление дужек позвонков. Этот дорсальный миелошизис может продолжаться вверх под интактными дужками. Имеется толстая фибро-васкулярная связка, которая соединяется с наиболее ростральной расщепленной дужкой. Эта связка сдавливает мешок менингоцеле и нервную ткань, вызывая перегиб верхней поверхности менингоцеле.
На уровне дорсального миелошизиса ТМО имеет дефект, открывающий плакод. Липома проникает через этот дефект и прикрепляется к дорсальной поверхности плакода; она может распространяться вверх под нормальными дужками и может проникать в центральный канал выше уровня дорсального миелошизиса. Липома отличается от нормальной эпидуральной жировой клетчатки, которая является более рыхлой. САП обычно имеет выпячивание на стороне, противоположной липоме.
В серии наблюдений у детей в 56% случаев липома проявлялась в виде бокового объемного образования, в 32% случаев – нарушениями мочеиспускания, в 10% случаев – деформациями стопы, парализацией или болью в ноге.
Практически все пациенты имеют кожные стигмы, которые сочетаются с расщеплением позвоночника: подкожные жировые комки (расположенные по средней линии и обычно распространяющиеся асимметрично в одну сторону) с/или без ямочек, родимые пятна, участки ненормального оволосения, открытый дермальный синус или кожные подвески. Может быть косолапость стопы.
50% больных могут иметь нормальный неврологический статус (большинство имеют только кожные проявления). Наиболее частым неврологическим нарушением является снижение чувствительности в сакральных дерматомах.
Обзорные спондилограммы пояснично-крестцового отдела в большинстве случаев показывают расщепление дужек (по определению должно быть практически во всех случаях, но в некоторых случаях вместо этого имеет место сегментирование). Также могут быть обнаружены аномальные соединения позвонков и дефекты крестца.
КТ/миелография или МРТ могут выявить ненормально низко расположенный конус. МРТ также показывает жировое объемное образование (высокий сигнал в режиме Т1, низкий в режиме Т2).
Всем пациентам перед операцией необходимо осуществить урологическое обследование для документирования возможных нарушений.
Поскольку симптомы обусловлены (1) фиксацией СМ, особенно в период активного роста и (2) компрессией в результате прогрессирующего накопления жира, особенно в периоды быстрого увеличения веса, целью операции является освобождение фиксированного СМ и уменьшение объема жировой опухоли. Простое косметическое удаление подкожных жировых комков не предотвращает от развития неврологического дефицита и может сделать дальнейшее радикальное восстановление затруднительным или даже невозможным.
Хирургическое лечение показано, когда ребенок достигает возраста 2 мес или в момент установления диагноза, если проявления заболевания возникнут позднее. В дополнение к хирургическому лечению используют мониторинг ВП и лазер. В общем, после хирургического лечения улучшение наблюдается у 19% пациентов, у 75% изменений нет, у 6% наступает ухудшение. Деформации стопы часто прогрессируют независимо от проведенного лечения.
Методика хирургического лечения (с изменениями)
1. мобилизуйте подкожное образование, которое направляется вглубь через глубокую фасцию
2. удалите последнюю неизмененную дужку позвонка (начинайте препарировать со стороны нормальной ТМО)
3. определите фибро-васкулярную связку, которая идет от наиболее рострально расположенной расщепленной дужки
4. пересечение фибро-васкулярной связки освобождает дуральную трубку и устраняет сильный перегиб на верхней поверхности менингоцеле
5. стараясь не повредить задние нервные корешки рассеките ТМО вперед до места соединения ТМО с липомой
6. аналогичным образом действуйте в отношении арахноидальной оболочки
7. продолжайте дуральный/арахноидальный разрезы вокруг всего фиксированного конуса
8. ликвидируйте фиксацию конуса и плакода (рекомендуемая техника мониторинга описана в Синдром фиксированного спинного мозга)
9. субтотальное удаление липомы: липому иссекают насколько это возможно, намеренно оставляя немного жировой ткани позади, чтобы избежать повреждения задней поверхности плакода. Если имеется распространение опухоли по задней поверхности СМ или в центральный канал, то эти части удаляют максимально, насколько это возможно и безопасно
10. плакод превращают в закрытую невральную трубку
11. сшивают края мягкой мозговой оболочки
12. зашивают ТМО (первично, там где это возможно, или с использованием трансплантата широкой фасции бедра, если возникает слишком большое давление на свернутый плакод
Читайте также:
