МРТ при псевдоменингоцеле
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Данный вид обследования позволяет оценить следующие анатомические структуры:
- костный и спинной мозг;
- межпозвоночные диски;
- дугоотростчатые суставы;
- связочный аппарат позвоночника;
- мышцы спины;
- паравертебральные мягкие ткани.
Как правило, чтобы пройти МРТ позвоночника, необходимо направление или рекомендация лечащего врача.
Что показывает МРТ позвоночника
На снимке после сканирования с контрастным веществом можно выявить и изучить нестабильность позвоночника, функционирование сосудов спинного мозга, обнаружить опухоли или метастазы. Сделать МРТ позвоночника необходимо в следующих случаях:
- острая травма любого отдела позвоночника;
- интенсивные боли с онемением конечности;
- необходимость оценить размеры и состояние межпозвоночных грыж и суставов, новообразований, врожденных патологий;
- нарушение функций тазовых органов (недержание мочи, кала);
- головные боли;
- боли в спине неясного характера;
- неврологические расстройства: шум в ушах, головокружение и т. д.;
- подготовка к операциям на позвоночнике.
Заболевания, диагностируемые с помощью МРТ позвоночника:
- врожденные патологии позвоночного столба, в том числе, сосудистые;
- деформация позвоночных дисков;
- доброкачественные и злокачественные новообразования позвоночника, наличие метастазов;
- поражения тканей спинного мозга;
- последствия травм;
- воспалительные заболевания мягких тканей и суставов, для диагностики отклонений в которых также проводится КТ костей и суставов;
- защемление нервных корешков;
- нарушение кровообращения в шейном отделе.
В Центре точной диагностики в СПб можно недорого сделать МРТ поясничного, шейного, грудного, крестцового отделов позвоночника (с захватом 2-3 верхних крестцовых позвонков). Также во время сканирования исследуется крестец с копчиком, оцениваются крестцово-подвздошные суставы. Можно выполнить исследование всех отделов позвоночника.
Показания для МРТ позвоночника
Пройти обследование необходимо:
- Если вас беспокоит боль в спине в покое или при нагрузке;
- Есть подозрение на грыжу межпозвонкового диска;
- Была получена или имеется старая травма позвоночника и спинного мозга;
- Диагностированы неврологические нарушения и корешковый синдром;
- Есть подозрение на опухоль позвонков, спинного мозга или необходим поиск метастазов (выполняется МРТ с внутривенным контрастированием);
- При остром или хроническом воспалении (гнойный спондилодисцит, туберкулез позвоночника, болезнь Бехтерева и т. д).
Противопоказания к МРТ позвоночника
Процедуру не проводят:
- при наличии кардиостимулятора или других электронных устройств;
- стентов;
- несъемных металлических протезов;
- металлических винтов;
- штифтов, фиксирующих кости пластин;
- суставных имплантов.
Ограничением может быть склонность к аллергии (при необходимости ввода контраста), клаустрофобия, психические расстройства.
Подготовка к исследованию
МРТ позвоночника и спинного мозга не требует особой подготовки.
МРТ (магнитно-резонансная томография) позвоночника и спинного мозга – информативный и неинвазивный метод. С его помощью можно оценить состояние костных тканей, суставов, межпозвонковых дисков, мышц спины.
Как делают МРТ позвоночника
В Центре точной диагностики в Сестрорецке созданы комфортные условия для проведения любого вида МРТ или КТ исследования. При сканировании отделов позвоночника и спинного мозга, пациента укладывают на стол томографа, выбирают необходимое положение тела. Затем подвижный стол перемещают в широкую трубу томографа. Пациент должен лежать неподвижно, но в любой момент может связаться с врачом по радиосвязи. Процедура безболезненная, поэтому не требует применения местных или общих обезболивающих средств.
Как долго проходит МРТ позвоночника
Безконтрастный метод обследования одного отдела позвоночника занимает около получаса, контрастный — до 40 минут. Подробный отчет поможет вашему лечащему врачу составить наиболее эффективную схему лечения и реабилитации, в зависимости от выявленных травм и патологий.
Где можно сделать МРТ позвоночника в СПб
Справка по процедуре:
Длительность — 30 мин;
Обследование — в день обращения;
Консультация врача — бесплатно!
Великолепный центр, красиво, чисто, современно, парковка, туалет , Оборудование современное! Благодарность руководству центра и персоналу за работу
МРТ при псевдоменингоцеле
1 Кафедра неврологии и нейрохирургии ФПК и ППС,
Казанский государственный медицинский университет, Казань
2 Межрегиональный клинико-диагностический центр, Казань
Для корреспонденции: Каххаров Руслан Абдуллаевич
ул. Карбышева, д. 12а, г. Казань, 420097; ur.liam@vorahhak.nalsur
Благодарности: профессору Валерию Данилову из Казанского государственного медицинского университета за помощь в подготовке рукописи.
Аномалия (мальформация) Киари — это порок, чаще врожденный, характеризующийся смещением миндалин мозжечка ниже уровня большого затылочного отверстия, что приводит к хроническому сдавлению структур краниовертебрального перехода и нарушению ликвородинамики и кровообращения в данной области (рис. 1) [1, 2].
В настоящее время выделяют 6 типов аномалии (мальформации) Киари (таблица) [1, 3, 4, 5, 6]. Наиболее часто встречаются I и II типы аномалии: I тип — 3,3–8,2 случая на 1000 человек, II тип — 1–2 случая на 1000 человек [1, 7].
Основным методом лечения при наличии показаний (сирингомиелии и прогрессировании клинической симптоматики) является хирургическое лечение.
В 1932 г. C. J. Van Houweninge Graftidijk доложил о первых попытках хирургической коррекции мальформации. Он пытался восстановить цереброспинальный ликвороток на уровне деформации путем резекции излишней части мозжечка или резекции кости по задней поверхности мальформации с рассечением подлежащей твердой мозговой оболочки. Лечение не дало положительных результатов [8, 9, 10]. В 1938 г. Penfield и Coburn описали хирургическую технику резекции нижней порции миндалин мозжечка при аномалии [11]. В дальнейшем с появлением концепций W. J. Gardner и B. Williams хирургическая методика лечения сирингомиелии (рис. 2) и мальформации Киари нашла теоретическое обоснование. Именно имя Gardner'а (или «базисная методика») носит операция, описанная им для коррекции сирингомиелии при мальформации Киари в 1965 г. В различных модификациях она используется и по сей день. Операция включает субокципитальную резекционную трепанацию, ламинэктомию верхних шейных позвонков, рассечение арахноидальных спаек, ревизию отверстия Мажанди и закрытие входа в центральный канал спинного мозга кусочком мышцы. Хирургическое вмешательство предусматривает выравнивание гидродинамического давления ликвора на уровне краниовертебрального перехода [12, 13].
В настоящее время операция Гарднера в ее классическом варианте осуществляется редко. Предложенные модификации данной операции выполняют в двух видах. Первый вид — резекционная трепанация задней черепной ямки, рассечение твердой и арахноидальной мозговых оболочек с резекцией или без резекции миндалин мозжечка с реконструкцией большой затылочной цистерны или без нее. Второй вид — резекционная трепанация задней черепной ямки со вскрытием твердой мозговой оболочки (ТМО) и проведением манипуляций на ней [14, 15, 16, 17].
Выделяют также другие виды хирургического вмешательства: эндоскопическую тривентрикулостомию (ЭТВС), трансоральную декомпрессию и краниовертебральную декомпрессию с окципитоспондилодезом [5].
Выполнение ЭТВС в качестве первого этапа лечения пациентов с мальформацией Киари I типа (МК I) и сопутствующей гидроцефалией в настоящее время признано золотым стандартом, вытеснившим используемые ранее шунтирующие системы. Эффективность процедуры, по мнению исследователей [6], составляет до 95 %. Существует небольшая группа пациентов с МК, страдающих непосредственно от симптомов внутричерепной гипертензии, хирургическое лечение которых может быть ограничено лишь выполнением ЭТВС [6]. Однако большинству пациентов с МК и сопутствующей гидроцефалией в последующем требуется проведение декомпрессии краниовертебрального перехода.
К методике трансоральной декомпрессии у пациентов с мальформацией Киари следует прибегать в случаях выраженной передней компрессии и наличии базилярной инвагинации. У пациентов с комбинацией передней и задней компрессии, по мнению большинства ученых, учитывая травматичность данного метода, целесообразно в качестве первого этапа хирургического лечения прибегнуть к стандартной краниовертебральной декомпрессии с одномоментной стабилизирующей операцией [18].
Одномоментное выполнение краниовертебральной декомпрессии и стабилизирующей операции показано в относительно небольшой группе пациентов с МК I, атлантоаксиальной дислокацией и высоким риском формирования нестабильности шейного отдела позвоночника, выявленных на этапе дооперационного обследования. Провоцирующими факторами для формирования нестабильности шейного отдела у пациентов с МК I являются нарушение иннервации мышц шеи при наличии сирингомиелитической кисты на верхнешейном уровне, фиброзные изменения в мышцах, повторяющиеся их сокращения и растяжения и неадекватное закрытие операционной раны [18, 19].
Цель операции — декомпрессия структур краниовертебрального перехода, результатом которой является устранение нарушений ликвородинамики и кровообращения на данном уровне за счет восстановления оттока ликвора из отверстия Мажанди и большой затылочной цистерны в спинальное субарахноидальное пространство.
Выделяют ряд послеоперационных осложнений, связанных с несостоятельностью пластики твердой мозговой оболочки. В нашем исследовании мы решили остановиться на двух основных — асептическом менингите и псевдоменингоцеле.
Асептический менингит — это воспалительная реакция мозговых оболочек, отличающаяся от гнойного послеоперационного менингита отсутствием выявленного при бактериоскопии пиогенного возбудителя. Данный синдром имеет характерную клиническую картину (гипертермия, менингеальный симптомы, воспалительные изменения в крови и цереброспинальной жидкости), которая существенно не отличается от таковой при гнойном послеоперационном менингите. Синдром асептического менингита сопровождается иммунологическим феноменом послеоперационного транзиторного реактивного воспаления, связанного с активацией лимфоцитов [20].
Псевдоменингоцеле — это патологическое экстрадуральное скопление ликвора в мягких тканях, сообщающееся через дефект ТМО с субдуральным пространством (рис. 3).
Встречается также ряд других послеоперационных осложнений: скопление пластинчатой субдуральной гигромы в области полушарий мозжечка, пневмоцефалия, арахноидит. В связи с сидячим положением пациента во время операции отмечают и такое интраоперационное осложнение как воздушная эмболия.
Цель исследования: определить роль пластики твердой мозговой оболочки при операциях по поводу аномалии (мальформации) Киари.
- уточнить частоту встречаемости различных клинических симптомов при аномалии Киари;
- оценить частоту послеоперационных осложнений в зависимости от вида хирургической техники;
- оценить результаты хирургического лечения при различных вариантах пластики ТМО.
ПАЦИЕНТЫ И МЕТОДЫ
В исследование были включены 34 пациента с аномалией Киари, пролеченные в нейрохирургическом отделении Межрегионального клинико-диагностического центра в период с 2010 по 2014 г.
Для проведения исследования использовали клинический метод, метод предоперационной нейровизуализации, непосредственную интраоперационную визуализацию, ретроспективный анализ.
Всем пациентам проводили неврологический осмотр в дооперационном и раннем послеоперационном периодах с оценкой основных неврологических функций.
Предоперационная визуализация заключалась в МРТ головного мозга с захватом краниовертебрального перехода и в МРТ спинного мозга по длиннику в зависимости от уровня сирингомиелии. МРТ-исследование проводили на томографах Signa HDxt 1,5T (General Electric, США) с напряженностью магнитного поля не менее 1,5 Тл в аксиальной, сагиттальной и коронарной проекциях, а также в режиме гидрографии для оценки ликвородинамики в области краниовертебрального перехода.
Основными критериями диагностики аномалии Киари служили данные нейровизуализации (рис. 4) [21, 22, 23] и клинического обследования, основанного на выявлении характерных клинических синдромов (мозжечкового, гипертензионно-гидроцефального, сирингомиелического, корешкового, бульбарного и синдрома вертебробазилярной недостаточности [24]). На МРТ при МК I в большинстве случаев определяют опущение миндалин мозжечка ниже линии Мак-Рея, сирингомиелию, компрессию ствола головного мозга. При мальформации Киари II типа (МК II) также определяется опущение миндалин мозжечка, Z-образная деформация продолговатого мозга, четверохолмное сращение (клювовидный изгиб в области четверохолмия), удлинение продолговатого мозга, низкое прикрепление головного мозга. При МК II на МРТ встречается гидроцефалия, сирингомиелия в области краниовертебрального перехода, изолированный IV желудочек, церебелломедуллярная компрессия, агенезия/дисгенезия мозолистого тела [5].
Средний возраст исследуемых больных составил 45 лет (от 18 до 69 лет), соотношение между мужским и женским полом — 1 : 3,2 соответственно. Стоит отметить, что наиболее часто хирургическое вмешательство проводили пациентам в возрасте 50–60 лет. Показанием к оперативному вмешательству было прогрессирование неврологической симптоматики.
Операцию проводили в положении больного сидя. Рассечение мягких тканей выполняли по Наффцигеру–Тауну в модификации И. С. Бабчина. На следующем этапе проводили резекцию нижних участков чешуи затылочной кости и ламинэктомию C1, а иногда и C2. По объему дальнейшего вмешательства всех пациентов разделили на две группы.
В первую группу были включены 8 (23,5 %) пациентов, которым ТМО не вскрывали. В этом случае виднелась отчетливая пульсация ТМО.
Пациентам второй группы, представленной 26 (76,5 %) больными, проводили Y-образное вскрытие ТМО. В большинстве случаев ТМО оказывалась утолщенной, не пульсировала. Венозные синусы нередко были расширенными. После рассечения ТМО выполняли осмотр и оценивали уровень опущения миндалин мозжечка, субарахноидального пространства. В случае выраженного спаечного процесса производили ревизию субарахноидального пространства с освобождением от спаек сосудов, продолговатого мозга и миндалин мозжечка. Далее восстанавливали целостность твердой мозговой оболочки путем ее пластики. В зависимости от вида пластики ТМО вторую группу разделили на две подгруппы:
- 2A: 14 (41,2 %) пациентов, вскрытие ТМО с последующей ее пластикой аллотрансплантатом. В качестве аллотрансплантата использовали искусственную ТМО DURAFORM (Codman Neuro, США).
- 2B: 12 (35,3 %) пациентов, вскрытие ТМО с последующей ее пластикой аутотрансплантатом. Аутотрансплантатом выступал ранее выделенный апоневроз затылочных мышц. На этапе доступа рассечение мягких тканей доходило до апоневроза затылочных мышц, далее апоневроз отсекался лоскутом размером 3 × 5 см и откидывался в сторону, основанием лоскут был направлен в сторону затылочных мышц. Таким образом, лоскут оставался на ножке, по средству которой происходило его питание до окончания операции. Далее рассечение происходило линейно, как и в других группах. На этапе пластики питающая ножка отсекалась, и лоскут подшивался к краям вскрытой ТМО. Таким образом, происходило увеличение и большой затылочной цистерны, что приводило к дополнительной декомпрессии краниовертебрального перехода.
Резекцию миндалин мозжечка не проводили ни одному пациенту.
Проанализированы результаты хирургического лечения в раннем послеоперационном периоде. При их сравнении в первую очередь учитывали неврологический регресс, частоту встречаемости послеоперационных осложнений, связанных с несостоятельностью пластики твердой мозговой оболочки, зависимость от варианта пластики ТМО.
Статистическую обработку данных производили с помощью программы Microsoft Office Excel 2010.
При анализе историй болезни пациентов с аномалией Киари была определена частота встречаемости неврологических синдромов, выявленных у них в ходе предоперационного клинического обследования (рис. 5). В большинстве случаев (88,2 %) отмечен мозжечковый синдром. Реже всего (менее чем у половины пациентов) наблюдали бульбарный синдром и синдром вертебробазилярной недостаточности.
При анализе результатов хирургического лечения использовали клинический метод и метод послеоперационной нейровизуализации. При проведении неврологического осмотра учитывали регресс характерной клинической симптоматики, критерием наличия которого были отсутствие жалоб у пациента; улучшение чувствительности по соответствующему дерматому и увеличение силы в конечностях; уменьшение мозжечковой симптоматики и признаков внутричерепной гипертензии.
Результаты лечения оценивали в раннем и отдаленном послеоперационном периодах. Положительные результаты достигнуты у всех больных после осуществления полноценного лечения.
В динамике раньше всех регрессировал гипертензивно-гидроцефальный синдром. В течение первых дней после операции у больных исчезли характерные неврологические симптомы внутричерепной гипертензии. В пределах 3–4 мес. у пациентов наблюдалось полное или частичное исчезновение бульбарного, мозжечкового и сирингомиелического синдромов. Отмечено восстановление чувствительности, мышечной силы. По данным МРТ-исследования, сирингомиелические кисты исчезали в пределах от 6 мес. до 1 года.
Были получены следующие результаты (рис. 6).
В группе пациентов, которым была проведена декомпрессия структур краниовертебрального перехода с последующей пластикой ТМО, у 21 (80,8 %) из 26 пациентов наблюдали регресс неврологических синдромов в течение первых 20 дней со дня операции: в первой подгруппе с пластикой ТМО аллотрансплантатом — у 11 (79 %) из 14 пациентов; во второй подгруппе с пластикой ТМО аутотрансплантатом — у 10 (83 %) из 12 больных. Временной лимит в 20 дней был выбран условно в соответствии результатами полученных в исследовании данных.
В группе пациентов, которым была проведена декомпрессия структур краниовертебрального перехода без вскрытия ТМО, регресс неврологических синдромов в 75 % случаев происходил не ранее, чем через месяц со дня проведения операции. У 2 (25 %) из 8 пациентов основные синдромы регрессировали в пределах первых 20 дней. Послеоперационные осложнения, связанные с несостоятельностью пластики ТМО, в виде асептического менингита и псевдоменингоцеле были выявлены только у пациентов, которым проводили декомпрессию структур краниовертебрального перехода со вскрытием ТМО и последующей ее пластикой аллотрансплантатом (42,9 %). При этом из всех больных данной подгруппы (n = 14) асептический менингит в послеоперационном периоде наблюдали у 5 (35,7 %) пациентов, а псевдоменингоцеле — у 1 (7,1 %).
В подгруппе пациентов, которым выполняли декомпрессию структур краниовертебрального перехода со вскрытием ТМО и последующей ее пластикой аутотрансплантатом, вышеназванных послеоперационных осложнений не наблюдали.
Выявление эффективной методики хирургической коррекции и стандартизация данного метода — это важная задача, так как хирургическое лечение является основным методом лечения больных с данной патологией. Однако решение об объеме хирургического вмешательства в некоторых случаях не может быть стандартизировано, и какие-либо дополнения к основной методике операции должны определяться интраоперационно. Основная цель операции — декомпрессия структур краниовертебрального перехода и восстановление ликвороциркуляции в данной зоне.
В ряде случаев костной декомпрессии бывает вполне достаточно для достижения цели операции. Об этом свидетельствует четкая пульсация ТМО, но единственный критерий не может дать нужной достоверности. Поэтому, по нашему мнению, следует использовать процедуру соматосенсорных вызванных потенциалов интраоперационно. Данный метод дает достаточно достоверную информацию о возможном послеоперацинном регрессе. Свидетельством этому являются полученные нами интраоперационные результаты, а именно положительная динамика у 2 из 8 пациентов, которым не проводили вскрытие ТМО. Данные 2 пациента первой группы демонстрировали наиболее быстрый регресс неврологической симптоматики.
Результаты нашего исследования показывают, что наиболее оптимальным объемом хирургического лечения аномалии Киари I типа является операция со вскрытием ТМО и последующей ее пластикой аутотрансплантатом, что совпадает с данными мировой литературы [25, 26, 27].
На основании результатов хирургического лечения пациентов с аномалией Киари I типа можно заключить, что декомпрессия структур краниовертебрального перехода со вскрытием твердой мозговой оболочки и последующей ее герметизацией аутотрансплантатом является эффективным методом хирургического лечения больных с данной патологией, снижающим риск развития послеоперационных осложнений. Доказательством эффективности данной методики является относительное большинство пациентов с наиболее быстрым регрессом неврологической симптоматики.
КТ или МРТ позвоночника — что эффективней?

Лучевая диагностика является одним из основных диагностических методов, позволяющих получить пространственное представление о строении тела именно благодаря КТ и МРТ. С их помощью врач-рентгенолог имеет возможность разобраться с причинами болевого синдрома (грыжа межпозвонкового диска, опухоль, воспалительный процесс) в любом отделе позвоночника, которые сложно, а иногда и невозможно обнаружить с помощью других методов диагностики.
Компьютерная томография (КТ)
Этот метод основан на измерении ослабления рентгеновского излучения, проходящего через тело человека в различных проекциях. КТ-томограф позволяет получать послойные тонкосрезовые изображения, устраняя их наложение друг на друга. Его чувствительность к мелким изменениям как минимум в 10 раз выше, чем у рентгеновского аппарата. Компьютерная томография быстрая и безболезненная, однако проходить ее часто все же не рекомендуется, поскольку рентгеновское излучение может негативно воздействовать на организм пациента.
Тем не менее, КТ является ведущим методом диагностики заболеваний органов грудной клетки (легких и средостения), забрюшинного пространства, надпочечников. КТ лучше других методов выявляет камни мочевыделительной системы и оценивает деструктивные изменения при костных опухолях любой локализации.
Показания к проведению КТ позвоночника:
- травматическое повреждение дужек тел позвонков и их отростков;
- травматическое повреждение крестца;
- злокачественные и доброкачественные новообразования тел позвонков, дужек и их отростков в случаях, когда МРТ не дает полной картины;
- воспалительные заболевания тел позвонков, дужек и их отростков в случаях, когда МРТ не дает полной картины
- аномалии развития тел позвонков, дужек и их отростков;
- определение степени остеопороза (КТ-денситометрия);
- послеоперационная оценка правильности стояния фиксирующих металлических конструкций после различных операций на позвоночнике.
Как правило, вышеперечисленные показания не требуют введения контрастного препарата.
Компьютерная томография совершенно не подходит для диагностики межпозвонковых грыж шейного и грудного отделов позвоночника. Она может применяться для исследования поясничного отдела, но в этом случае более эффективной будет МРТ. Кроме того, КТ не информативна при диагностике заболеваний спинного мозга и его корешков.
Во всех остальных случаях КТ позвоночника проводится при наличии противопоказаний к МРТ.
Магнитно-резонансная томография (МРТ)
Это высокоинформативный, абсолютно безопасный для здоровья пациента метод лучевой диагностики, позволяющий выявлять и дифференцировать различные патологические процессы, локализованные в костном мозге тел позвонков, эпидуральном клетчаточном пространстве (расположенном между твердой оболочкой спинного мозга и наружной стенкой позвоночного канала и содержащем соединительную ткань и венозные сплетения), дуральном мешке (канале, в котором расположен спинной мозг и защищающая его спинномозговая жидкость), межпозвонковых дисках, околопозвоночных (паравертебральных) мягких тканях. Кроме того, МРТ позвоночника позволяет оценить состояние спинного мозга и его корешков, выявить их повреждение при травме, опухоли, демиелинизирующих или воспалительных заболеваниях. Высокая диагностическая точность и достоверность свойственны методу МРТ при исследовании любого из отделов позвоночника: шейного, грудного и пояснично-крестцового.
Данный вид диагностики наиболее предпочтителен для выявления свежих компрессионных переломов тел позвонков, всегда сопровождающихся отеком костного мозга, исчезновение которого в процессе лечения свидетельствует о консолидации (сращении) компримированного (сжатого) позвонка. МРТ выявляет метастазы в позвоночник, локализованные только в костном мозге и потому не вызывающие разрушения (деструкции) костной ткани, визуализировать которые при помощи КТ или рентгенографии не представляется возможным.
Большое преимущество МРТ — это ее информативность: при сравнительно небольшом количестве противопоказаний она предоставляет полные сведения о состоянии исследуемой области, и чаще всего после ее проведения нет необходимости в дополнительных обследованиях. Помимо всего прочего, МРТ позвоночника не требует специальной подготовки и не имеет побочных эффектов. За одно посещение пациент может провести МР-томографию сразу трех отделов позвоночника либо любого из его отделов. Кроме того, по желанию пациент может пройти МРТ копчика.
Показания к проведению МРТ позвоночника
Как правило, врачи-клиницисты (неврологи, нейрохирурги, терапевты, травматологи) рекомендуют пройти МРТ при болях в спине, независимо от того, какой характер они носят. Следует обратить внимание, что зачастую проблемы с позвоночником могут проявляться не только в виде болевого синдрома, но и сопровождаться нарушением чувствительности (онемением) пальцев, слабостью в руке или ноге, атрофией мышц конечности, головокружением, болью в сердце, задержкой мочеиспускания и другими жалобами.
МРТ позвоночника показана при:
- ДДЗП (дегенеративно-дистрофических заболеваниях позвоночника), самым распространенным из которых является остеохондроз. МРТ выявляет не только само заболевание, но и его осложнения (протрузии и грыжи межпозвонковых дисков, стенозы позвоночного канала, спондилоартрозы дугоотростчатых сочленений и т.д.). Исходя из полученных данных, лечащий врач подбирает наиболее оптимальный метод консервативной (не оперативной) терапии, либо прибегает к хирургическому (оперативному) лечению;
- воспалительных заболеваниях позвоночника (спондилодисцит, туберкулезный спондилит), спинного мозга (поперечный миелит) и корешков (арахноидит);
- сосудистых заболеваниях спинного мозга (кавернозная ангиома);
- врожденных аномалиях спинного мозга (миелоцеле и миеломенингоцеле, гидромиелия, сирингомиелия, диастематомиелии (ращепление спинного мозга);
- подозрении на опухоль: спинного мозга, его корешков или позвоночника;
- травматических повреждениях позвоночника и спинного мозга;
- демиелинизирующих заболеваниях головного мозга, для поиска интрамедуллярных (локализованных в спинном мозге) очагов демиелинизации, а также для оценки динамики или определения активности процесса ранее выявленных очагов;
- оценке постоперационных осложнений (псевдоменингоцеле), определении степени резектабельности, исключении или выявлении продолженного роста опухоли у прооперированных пациентов.
МР-томография позвоночника с контрастом
в одной из серий популярного сериала "Теория большого взрыва" главный герой, гениальный физик Шелдон Купер, дарит девушке МРТ-снимок своего головного мозга с подсвеченной орбитофронтальной корой. Читать далее.
МРТ плечевого сплетения –
метод выбора при диагностике патологических изменений и травм плечевого сплетения в неврологии, травматологии, реабилитации.
Травма или воспаление плечевого сплетения (плексит) может проявлять себя в виде двигательных нарушений или изменений кожной чувствительности в области шеи, надключичной и подключичной областей и верхних конечностей. Чаще всего повреждение плечевого связано с растяжениями и разрывами (бытовая, спортивная, автомобильная травма), с родовой травмой (акушерские параличи у новорожденных), воспалением (сдавление, инфекция, операция). Реже причиной может стать опухоль (нейрофиброма), повреждение оболочки нерва (псевдоменингоцеле).
Принципиально новый уровень диагностики!
МР-томограф SIEMENS MAGNETOM SKYRA 3,0 Тесла
Эксклюзивно только в сети клиник Тонус в Нижегородской области
МРТ плечевого сплетения на аппарате SIEMENS MAGNETOM SKYRA с напряженностью магнитного поля 3,0 Тл: применение инноваций в неврологии, реабилитации, при травме
- Детальная визуализация – эффективная диагностика:
благодаря высокому соотношению сигнал/шум 3,0 Тл МРТ позволяет получать качественные и четкие изображения сложно устроенного плечевого сплетения, его тонких анатомических структур; - При МРТ 3,0 Тл лучше визуализируются патологические изменения в плечевом суставе, которые сопровождают травмы и повреждения плечевого сплетения;
- Первый в Нижегородской области сверхмощный флагманский томограф.
Золотой стандарт аппаратной диагностики!
МР-томограф SIEMENS MAGNETOM AERA 1,5 Тесла
Только в центре лучевой диагностики и эндоскопической хирургии «ТОНУС ПРЕМИУМ»
Сверхпроводящий высокопольный МР-томограф
SIEMENS MAGNETOM ESPREE 1,5 Тесла в медицинском центре “Тонус”
Сверхпроводящий высокопольный МР-томограф SIEMENS MAGNETOM AVANTO 1,5 Тесла в медицинском центре “Тонус” в г. Кстово, ул. Магистральная, д. 57
МРТ плечевого сплетения на томографах SIEMENS с напряженностью магнитного поля 1,5 Тл:
Изображения, полученные при сканировании на 1,5 Тл томографах, отличаются высокой четкостью, что позволяет устанавливать точный диагноз после прицельной детальной диагностики. На сегодняшний день магнитно-резонансная томография плечевого сплетения является безальтернативным методом диагностики патологических изменений и травм плечевого сплетения.
Преимущества магнитно-резонансной томографии при диагностике воспаления или повреждения плечевого сплетения:
К методам исследования анатомии плечевого сплетения относят рентгенографию, миелографию, компьютерную томографию, КТ-миелографию, ангиографию, МР-ангиографию, МРТ плечевого сплетения. На сегодняшний день магнитно-резонансная томография плечевого сплетения является наиболее эффективным методом диагностики повреждений плечевого сплетения среди вышеперечисленных.
МРТ при псевдоменингоцеле
Городская многопрофильная больница №2, Санкт-Петербург;
Кафедра нейрохирургии Санкт-Петербургской государственной академии им. И.И. Мечникова
Отделение нейрохирургии Городской многопрофильной больницы №2, Санкт-Петербург
ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова», Санкт-Петербург;
СПб ГБУЗ «Городская многопрофильная больница №2», Санкт-Петербург, Россия
СПб ГБУЗ «Городская многопрофильная больница №2», Санкт-Петербург, Россия
Случай псевдоменингоцеле с компрессией спинного мозга после удаления менингиомы на уровне Th3-Th4 позвонков
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2015;79(5): 77‑81
Городская многопрофильная больница №2, Санкт-Петербург;
Кафедра нейрохирургии Санкт-Петербургской государственной академии им. И.И. Мечникова
Псевдоменингоцеле - это патологическое экстрадуральное скопление ликвора в мягких тканях, сообщающееся через дефект твердой мозговой оболочки с арахноидальным пространством. Послеоперационное псевдоменингоцеле на грудном уровне с неврологическими проявлениями в форме миелопатии - достаточно редкое явление, в литературе мы обнаружили описание только двух подобных случаев. Описан клинический случай пациентки, оперированной по поводу менингиомы на уровне Th3-Th4 позвонков с развитием псевдоменингоцеле с компрессией спинного мозга.
Городская многопрофильная больница №2, Санкт-Петербург;
Кафедра нейрохирургии Санкт-Петербургской государственной академии им. И.И. Мечникова
Отделение нейрохирургии Городской многопрофильной больницы №2, Санкт-Петербург
ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова», Санкт-Петербург;
СПб ГБУЗ «Городская многопрофильная больница №2», Санкт-Петербург, Россия
СПб ГБУЗ «Городская многопрофильная больница №2», Санкт-Петербург, Россия
Псевдоменингоцеле определяют как патологическое экстрадуральное скопление ликвора в мягких тканях, сообщающееся через дефект твердой мозговой оболочки (ТМО) с арахноидальным пространством [1]. Впервые спинальное псевдоменингоцеле, возникшее вследствие гемиляминэктомии, описано O. Hyndman и W. Gerber в 1946 г. [2]. Выделяют врожденные, травматические и ятрогенные псевдоменингоцеле. Ятрогенные псевдоменингоцеле чаще возникают при непреднамеренных повреждениях ТМО при оперативных вмешательствах на шейном и поясничном уровнях.
Наиболее частое клиническое проявление псевдоменингоцеле — периодическая боль в спине [3]. Реже у пациентов могут быть прогрессирующие неврологические проявления, которые возникают при выпячивании нервных структур через дефект ТМО либо их компрессии.
Псевдоменингоцеле на грудном уровне с компрессией спинного мозга — крайне редкое явление. В доступной нам литературе мы обнаружили только 2 случая псевдоменингоцеле на грудном уровне с неврологическими проявлениями в форме миелопатии [4, 5].
В нашей клинике мы столкнулись лишь однажды с псевдоменингоцеле, которое возникло после удаления экстрамедуллярной опухоли грудного отдела, вызвавшего компрессию спинного мозга с неврологической симптоматикой.
Описание клинического случая
Пациентка В., 66 лет, поступила в клинику с жалобами на боли в межлопаточной области, усиливающиеся при физической нагрузке. Интенсивность боли оценивала в 6—7 баллов по визуально-аналоговой шкале (ВАШ). Боль в межлопаточной области беспокоит в течение 14 лет. При МРТ выявлено экстрамедуллярное объемное образование на уровне Th3—Th4 позвонков слева, с экстра- и интрадуральным компонентом, распространяющееся в межпозвонковое отверстие Th3—Th4 (рис. 1).
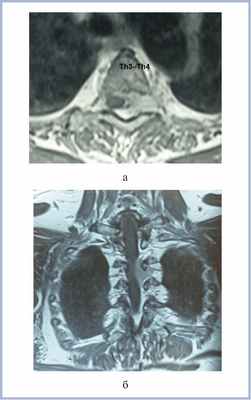
Рис. 1. МР-томограммы (Т1-ВИ с контрастным усилением) пациентки с менингиомой на уровне Th3—Th4 позвонков перед операцией в аксиальной (а) и фронтальной (б) проекциях. Определяется объемное образование (менингиома) на уровне Th3—Th4 позвонков, распространяющееся в межпозвонковое отверстие.
Пациентка неврологически интактна, оценка по шкале Klekamp—Samii [6] — 24 балла (4 балла по показателю «чувствительные нарушения или боль», 5 баллов по остальным показателям).
Выполнено оперативное вмешательство — гемиламинэктомия Th3 позвонка слева, тотальное удаление объемного образования. Макроскопически опухоль представляла собой плотную ткань, «стелющуюся» по ТМО, в виде муфты облегающей корешок Th3 позвонка. Произведено тотальное удаление опухоли вместе с пораженными участками ТМО (матрикс опухоли) и нервным корешком. Пластика дефекта ТМО выполнена с использованием свободного жирового лоскута из ягодичной области. Гистологическое заключение: менинготелиоматозная менингиома.
Ранний послеоперационный период протекал без осложнений, рана зажила первичным натяжением. В неврологическом статусе появилась зона гипестезии в зоне иннервации Th3 корешка слева, в остальном — без нарастания симптоматики. Оценка по шкале Klekamp—Samii при выписке — 24 балла, оценка боли по ВАШ — 4—5 баллов. Выписана из стационара на 7-е сутки послеоперационного периода.
На следующий после выписки день пациентка отметила появление припухлости в области послеоперационного рубца, онемение и слабость в ногах, что послужило причиной для повторной госпитализации в стационар. В неврологическом статусе при поступлении доминирует синдром заднестолбовой атаксии (снижение вибрационной чувствительности с уровня Th5—Th6 позвонков, неустойчивость в позе Ромберга), оценка по шкале Klekamp—Samii 18 баллов. При МРТ верифицирована ликворная киста (псевдоменингоцеле) в зоне оперативного вмешательства, дислоцирующая спинной мозг кпереди (рис. 2).
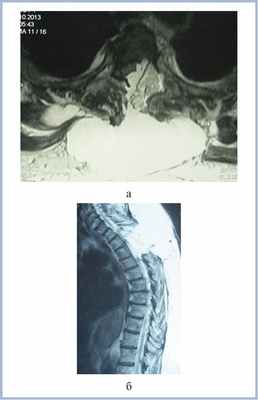
Рис. 2. МР-томограммы пациентки (Т2-ВИ) с менингиомой на уровне Th3—Th4 позвонков перед второй операцией в аксиальной (а) и сагиттальной (б) проекциях. Определяется компрессия спинного мозга жировым лоскутом и ликворной кистой больших размеров.
На 10-е сутки после первой операции выполнено повторное хирургическое вмешательство — пластика дефекта ТМО лоскутом широкой фасции бедра. Произведена дополнительная герметизация ликворных пространств свободным жировым лоскутом и фибриновым клеем. В послеоперационном периоде синдром заднестолбовой атаксии частично регрессировал, при этом пациентка ходила с опорой на ходунки. На 20-е сутки после удаления опухоли и 10-е сутки после герметизации ликворных пространств отмечено усугубление неврологической симптоматики в виде нарастания слабости в нижних конечностях (до 4 баллов в левой ноге и до 3 баллов — в правой), увеличение размеров ликворной кисты в области оперативного вмешательства. При контрольной МРТ верифицировано увеличение размеров ликворной кисты с дислокацией спинного мозга (рис. 3).
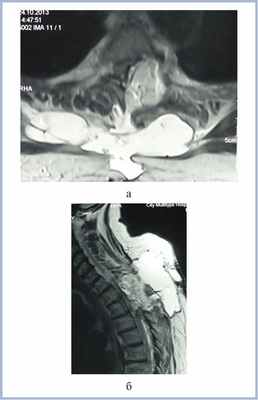
Рис. 3. МР-томограммы (Т2-ВИ) пациентки с менингиомой на уровне Th3—Th4 позвонков перед 3-й операцией в аксиальной (а) и сагиттальной (б) проекциях. Определяется компрессия спинного мозга жировым лоскутом и псевдоменингоцеле больших размеров.
На 20-е сутки после первой операции выполнено очередное (3-е) оперативное вмешательство: наложение дополнительных герметизирующих швов на фасциальную заплату ТМО, удаление из эпидурального пространства жирового лоскута, герметизация ТМО мышечным лоскутом на ножке. В послеоперационном периоде отмечено увеличение силы в ногах до 4 баллов. В удовлетворительном состоянии выписана из стационара при сохраняющихся явлениях заднестолбовой атаксии, оценка по шкале Klekamp—Samii — 18 баллов.
При контрольном осмотре через 5 мес после удаления опухоли несколько улучшилась чувствительность в ногах, ходит с опорой на костыли, оценка по шкале Klekamp—Samii — 19 баллов. Контрольная МРТ пациентки через 5 мес после операции представлена на рис. 4.
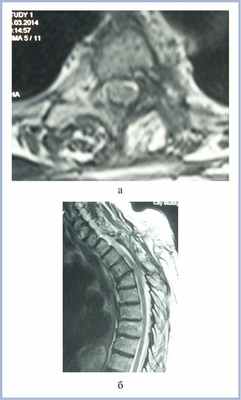
Рис. 4. МР-томограммы (Т2-ВИ) пациентки с менингиомой на уровне Th3—Th4 позвонков в аксиальной (а) и сагиттальной (б) проекциях через 5 мес после операции. Определяется небольшая ликворная киста без компрессии спинного мозга.
Наиболее частые причины компрессии спинного мозга — травмы, опухоли, дегенеративные изменения и воспалительные процессы в позвоночнике. Послеоперационное псевдоменингоцеле, вызывающее компрессию спинного мозга с клиническими проявлениями в форме миелопатии, — крайне редкое явление. Pereira Filho и соавт. [5] описали случай компрессии спинного мозга псевдоменингоцеле через 10 мес после удаления шванномы на уровне Th11—Th12 позвонков, а Mohamed Macki и соавт. (2014) описали подобный случай, проявившийся через 2 мес после дискэктомии на уровне Th10—Th11 позвонков [4].
Псевдоменингоцеле на грудном уровне разделяют на три группы: врожденные, травматические и ятрогенные [7]. Врожденные дефекты ассоциированы с генетическими заболеваниями, такими как синдром Марфана или нейрофиброматоз I типа. Травматические псевдоменингоцеле обычно возникают при травмах плечевого или поясничного сплетений в результате повреждения твердой и арахноидальной оболочек корешковых манжеток. Ятрогенные псевдоменингоцеле встречаются наиболее часто. Они возникают после непреднамеренных повреждений ТМО, либо после операций со вскрытием мозговых оболочек. Большая частота ятрогенных псевдоменингоцеле на поясничном уровне объясняется большим числом поясничных ляминэктомий в сочетании с бо́льшим ликворным давлением по сравнению с грудным и поясничным уровнями.
Истинная частота послеоперационных псевдоменингоцеле неизвестна, так как большинство из них асимптомны [8].
Патофизиология псевдоменингоцеле связана с дефектом ТМО. Если арахноидальная оболочка при этом не повреждена, она может пролабировать в дефект с формированием арахноидального пространства с ликвором. При повреждении одновременно и ТМО, и арахноидальной оболочки ликвор попадает в паравертебральные мягкие ткани и приводит к формированию фиброзной капсулы. Большие дефекты ТМО могут спонтанно закрываться, благодаря сращениям между оболочками и паравертебральными мягкими тканями. Маленькие дефекты, наоборот, несут больший риск формирования псевдоменингоцеле из-за образования клапанного механизма с односторонним током ликвора [9]. По нашему мнению, у описанной пациентки сформировался именно такой механизм компрессии спинного мозга, когда ликвор поступал через отверстие в ТМО в мягкие ткани спины без возможности обратного тока и вызывал компрессию спинного мозга через уложенный свободный жировой лоскут.
Клинические проявления псевдоменингоцеле крайне вариабельны и зависят от вовлечения в процесс подлежащих нервных структур. Как правило, псевдоменингоцеле бессимптомны и представлены флюктуирующим образованием под послеоперационным рубцом. Оно может увеличиваться при кашле, чихании, при этом в полости псевдоменингоцеле будет аккумулироваться еще больше ликвора [10]. У пациентов появляется головная боль, обусловленная ликворной гипотензией. Достаточно часто возвращаются симптомы, имевшие место до операции, боль в спине и корешковые боли.
Диагностика послеоперационных псевдоменингоцеле включает МРТ, КТ-миелографию, ретроградную миелографию. Хотя МРТ является диагностической процедурой выбора, КТ-миелография помогает лучше визуализировать расположение псевдоменингоцеле по отношению к хирургическому дефекту благодаря отчетливой визуализации костных структур.
Лечебные опции при псевдоменингоцеле включают консервативное лечение, эпидуральное введение крови, люмбальный субарахноидальный дренаж и хирургическое лечение. Консервативные мероприятия включают наблюдение, постельный режим, повторные пункции псевдоменингоцеле [11]. Эффективность установки люмбального субарахноидального дренажа в настоящее время спорна. Хирургическое закрытие дефекта ТМО остается единственным окончательным мероприятием при псевдоменингоцеле. Как правило, показаниями для хирургического лечения служат неэффективность консервативных мероприятий, прогрессирование радикулопатии или возникновение миелопатии. В большинстве случаев ТМО может быть герметично ушита, при необходимости герметизации больших дефектов используется фасциальный трансплантат либо другой заменитель ТМО. В нашем случае хирургическое лечение было проведено из-за возникновения признаков миелопатии и компрессии спинного мозга по данным МРТ.
В целях профилактики формирования псевдоменингоцеле важно тщательно герметизировать дефекты ТМО. Для этого накладывают водонепроницаемый шов, при необходимости линию шва дополнительно укрепляют различными герметиками. При невозможности тщательно зашить ТМО применяют различные пластические материалы (аутоплантаты, аллоплантаты, ксеноплантаты, синтетические материалы). В нашей клинике для пластики дефектов ТМО уже более 10 лет мы используем жировой аутотрансплантат, взятый из ягодичной области.
Комментарий
Все спинальные хирурги за свою практику неоднократно сталкиваются с ятрогенным псевдоменингоцеле. Это происходит по причине негерметичного закрытия разреза или повреждения ТМО после удаления опухоли, ревизии спинного мозга, декомпрессии позвоночного канала. В нашей клинике мы уделяем особое внимание закрытию разрезов или дефектов ТМО. В случае несостоятельности швов на ТМО мы используем Тахокомб, иногда в сочетании с фибриновым клеем. Также возможно послойное использование этих материалов: слой Тахокомба на ТМО, область заливается фибриновым клеем, сверху Тахокомб большей площади. При необходимости пациенту устанавливается люмбальный дренаж. В ряде случаев при закрытии дефектов после удаления менингиом с иссечением матрикса применялась резодура (коллагеновый биоматрикс для регенерации твердой мозговой оболочки), которую можно укладывать и подшивать к дефекту ТМО как снаружи, так и изнутри. Эта методика укладки и подшивания резодуры изнутри дурального мешка используется нами при вентрально расположенных дефектах ТМО. При вентрально-латеральных дефектах ТМО мы производим их ушивание изнутри с последующим укрытием Тахокомбом также изнутри дурального мешка. После этого линейный разрез ТМО зашивается обычным способом.
В подавляющем большинстве случаев ятрогенные псевдоменингоцеле не вызывают проводниковой симптоматики. Послеоперационное псевдоменингоцеле, вызывающее компрессию спинного мозга с клиническими проявлениями в форме миелопатии, — крайне редкое явление, требующее повторного хирургического вмешательства. Именно пример клинически значимого послеоперационного псевдоменингоцеле и тактики его лечения приводится в данной статье. В российской литературе мало работ, посвященных осложнениям при спинальных операциях. Поэтому представленная авторами картина осложненного течения хирургического лечения менингиомы спинного мозга является познавательным для хирургов, занимающихся данной проблемой.
Несомненно, что основной акцент должен делаться на профилактике развития послеоперационного псевдоменингоцеле посредством тщательного ушивания ТМО с использованием различных современных герметизирующих материалов.
Читайте также:
