Патогенез язвенного некротизирующего энтероколита (ЯНЭК)
Добавил пользователь Владимир З. Обновлено: 27.01.2026
Энтероколит — это группа заболеваний тонкого и толстого отделов кишечника воспалительно-дистрофического характера. Наряду с дистрофическими изменениями могут наблюдаться дегенеративные и атрофические изменения.
Серьезной патологией новорожденного является некротический энтероколит — воспалительное заболевание кишечника, которое часто осложняется перфорацией кишечника, перитонитом и может иметь летальный исход.
Классификация
Все энтероколиты подразделяются на 2 большие группы:
- по течению заболевания — острые и хронические;
- по этиологическому фактору — инфекционные и неинфекционные.
Инфекционные энтероколиты включают: вирусные, бактериальные, паразитарные энтероколиты, а также заболевания, вызываемые простейшими организмами.
Неинфекционный энтероколит может иметь разную природу.
Клиническая классификация неинфекционного колита включает:
- первичные нарушения пищеварения и всасывания в кишечнике;
- воспалительные и дистрофические патологии кишечника (неспецифический энтерит, эозинофильный гастроэнтерит, синдром экссудативной энтеропатии, неспецифический язвенный колит, болезнь Крона и др.);
- патологии кишечника при иммунодефицитных состояниях;
- функциональные болезни кишечника;
- послеоперационные поражения кишечника;
- сосудистые патологии кишечника;
- дивертикулез толстой кишки;
- аномалии развития кишечника и т.д.
По этиологии среди неспецифических энтероколитов выделяют: медикаментозные, алиментарные, аллергические, токсические, механические, паразитарные, вторичные.
Этиология и патогенез
К развитию энтероколита у детей и взрослых могут привести как внешние, так и внутренние факторы.
Причины энтероколита:
- кишечные инфекции, вызванные вирусами, бактериями, простейшими;
- нарушение питания (в том числе, злоупотребление острой, жирной, копченой пищей, недостаточное или избыточное питание);
- пищевые аллергены;
- злоупотребление алкоголем;
- медикаментозные препараты (длительное употребление антибиотиков);
- кишечные гельминтозы;
- интоксикация производственная;
- радиационные поражения.
В патогенезе заболевания ведущую роль играет изменение основных функций кишечника: секреторной (нарушение пристеночного и полостного пищеварения), двигательной функций и кишечного всасывания.
Причины некротизирующего энтероколита у новорожденных на сегодняшний день до конца не выяснены.
Клинические проявления
Острый энтероколит начинается внезапно и проявляется выраженными клиническими симптомами. При инфекционной природе энтероколита повышается температура, появляются симптомы общей интоксикации. В свою очередь, хронический энтероколит на ранних стадиях болезни протекает с мало выраженной симптоматикой, при затяжном течении развиваются различные осложнения энтероколита, в том числе, опасные для жизни пациента.
Симптомы энтероколита:
- острая боль в животе, которая часто носит схваткообразный характер;
- диспепсические расстройства (тошнота, реже - рвота, метеоризм);
- язык обложен налетом;
- урчание в животе;
- стул зловонный, часто с пузырьками воздуха;
- запор, стул в виде “овечьего кала”;
- снижение аппетита;
- похудание;
- признаки общей интоксикации (головная боль, высокая температура, общая слабость и ноющая боль в мышцах);
- жидкий стул, содержащий непереваренные кусочки пищи и/ или слизь, кровь;
- тенезмы, не исчезающие после акта дефекации.
При аллергическом гастроэнтерите и колите наблюдается связь между гастроинтестинальными симптомами и приемом некоторых продуктов — молока, фруктов и овощей, зерновых продуктов, орехов, грибов и т. д.
Осложнения
При установленном диагнозе и правильно подобранной схеме лечения риски развития осложнений энтероколита минимальны. При запущенном протекании заболевания, неадекватном лечении возможно развитие неблагоприятных последствий.
Последствия энтероколита:
- Анемия
- Синдром мальабсорбции
- Синдром мальдигестии
- Формирование колостомы
Диагностика
При диагностике энтероколита учитываются данные анамнеза, причины, которые могли вызвать поражение кишечника, признаки энтероколита, физикальное обследование, лабораторные данные и инструментальные методы исследования.
При физикальном обследовании диагностируется болезненность при пальпации и боль в околопупочной области, урчание и отхождение большого количества газа при пальпации слепой кишки.
Лабораторные методы исследования:
- общий анализ крови;
- общий анализ мочи;
- биохимический анализ крови;
- кал на скрытую кровь;
- бактериологическое исследование кала;
- копрограмма;
- гистологическое исследование биоптата.
Гастроэнтеролог может назначить дополнительные лабораторные исследования: определение антигена р24 ВИЧ, определение в кале кальпротектина ИФА-методом, определение в кале лактоферрина, исследование кала на гельминты и простейшие, исследование биологического материала на грибы рода Кандида.
Инструментальные исследования энтероколита:
При необходимости проводятся консультации у узких специалистов — отоларинголога, стоматолога, аллерголога.
Дифференциальная диагностика энтероколита необходима с хроническим гастродуоденитом, хроническим панкреатитом, хроническим холециститом, язвенной болезнью.
Лечение
Лечение энтероколита зависит от тяжести течения заболевания и этиологических факторов. При не тяжелом течении и вне обострения проводится амбулаторное лечение. Стационарное лечение показано при осложненной клинической картине, сильной интоксикации, отсутствии эффекта от амбулаторной терапии, при наличии осложнений.
Основная тактика лечения направлена на:
- проведение противовоспалительной терапии;
- устранение болевого синдрома;
- нормализацию нормальной функции кишечника;
- дезинтоксикационную терапию;
- селективную деконтаминацию условно-патогенной и патогенной флоры;
- коррекцию нарушений микробиоценоза;
- поддерживающее лечение;
- симптоматическую терапию.
Немедикаментозное лечение энтероколита включает корректировку питания, физиотерапевтические процедуры, магнитотерапию, рефлексотерапию, процедуры по очищению кишечника.
Медикаментозное лечение включает терапию:
- энтеросорбентами;
- антибиотиками;
- сульфаниламидными средствами;
- противовирусными препаратами;
- спазмолитиками;
- препаратами для нормализации моторики кишечника;
- ферментными препаратами.
При наличии в клинической картине осложнений энтероколита, симптомов диспепсического синдрома назначаются дополнительные лекарственные средства: противогрибковые препараты, ферментативные средства, адсорбенты и др., проводят инфузионную терапию.
Особенности питания при энтероколите:
- свежеприготовленная, химически и механически щадящая пища;
- ограничение углеводов и исключение продуктов, богатых клетчаткой, пряностей, острых, соленых, жареных, копченых продуктов, цельного молока;
- повышение в рационе количества белковых продуктов;
- исключение индивидуально непереносимых продуктов.
Контроль излеченности
После выписки больных энтероколитом рекомендуется наблюдение в клинике в течение первого года — 1 раз в 3 месяца, после этого — каждые полгода.
Целесообразно дважды в год проводить в стационаре курсы противорецидивного лечения энтероколита. При развитии синдрома нарушенного кишечного всасывания особое внимание уделяется диетотерапии.
Снятие с диспансерного учета возможно при условии стойкой ремиссии продолжительностью не менее 2 лет.
Профилактика
Профилактика энтероколита включает ряд мероприятий:
- своевременное лечение и профилактика острых колитов, инфекционных заболеваний;
- диспансеризация реконвалесцентов;
- рациональный режим питания;
- прием антибактериальных средств только под контролем врача;
- регулярная санация ротовой полости.
Статья носит информационно-ознакомительный характер. Пожалуйста, помните: самолечение может вредить вашему здоровью.
Хирургическое лечение осложнений язвенно-некротического энтероколита у новорожденных Текст научной статьи по специальности «Клиническая медицина»
Аннотация научной статьи по клинической медицине, автор научной работы — Гассан Т. А., Исаков Ю. Ф., Красовская Т. В.
Представлен опыт лечения 63 новорожденных с перфоративным перитонитом и динамической непроходимостью на почве язвенно-некротического энтероколита в условиях отделения хирургии новорожденных детской городской клинической больницы №13 им. Н.Ф.Филатова. Рассматриваются вопросы диагностики и хирургической тактики. Анализ результатов лечения указывает на целесообразность лапароцентеза, определяет варианты формирования временных кишечных стом и показания к декомпрессии просвета кишки. Наибольший риск летального исхода имеют глубоконедоношенные новорожденные .
Похожие темы научных работ по клинической медицине , автор научной работы — Гассан Т. А., Исаков Ю. Ф., Красовская Т. В.
Профилактика осложнений путем совершенствования показаний и методов формирования искусственных кишечных свищей у детей
Surgical treatment of complications of ulcerative-necrotic enterocolitis in neonates
The authors present the experience of treating 63 neonates with perforative peritonitis and dynamic ileus related to ulcerative-necrotic enterocolitis at the department of neonate surgery of N.F.Filatov Pediatric Hospital No 13. The problems of diagnosing and surgical tactics are discussed. The analysis of the results of treatment demonstrates the expediency of laparocentesis, determines variants of formation of temporary intestinal stomas and indications for decompression of the intestinal lumen. The greatest risk of a lethal outcome is found in highly immature neonates .
Текст научной работы на тему «Хирургическое лечение осложнений язвенно-некротического энтероколита у новорожденных»
Хирургическое лечение осложнений язвенно-некротического энтероколита у новорожденных
Т.А.Гассан, Ю.Ф.Исаков, Т.В.Красовская
Российский государственный медицинский университет, Москва
Представлен опыт лечения 63 новорожденных с перфоративным перитонитом и динамической непроходимостью на почве язвенно-некротического энтероколита в условиях отделения хирургии новорожденных детской городской клинической больницы №13 им. Н.Ф.Филатова. Рассматриваются вопросы диагностики и хирургической тактики. Анализ результатов лечения указывает на целесообразность лапароцентеза, определяет варианты формирования врёменных кишечных стом и показания к декомпрессии просвета кишки. Наибольший риск летального исхода имеют глубоконедоношенные новорожденные.
Ключевые слова: кишечные стомы, декомпрессия кишечника, новорожденные, язвенно-некротический энтероколит
Surgical treatment of complications of ulcerative-necrotic enterocolitis in neonates
T.A.Gassan, Yu.F.Isakov, T.V.Krasovskaya
Russian State Medical University, Moscow
The authors present the experience of treating 63 neonates with perforative peritonitis and dynamic ileus related to ulcerative-necrotic enterocolitis at the department of neonate surgery of N.F.Filatov Pediatric Hospital No 13. The problems of diagnosing and surgical tactics are discussed. The analysis of the results of treatment demonstrates the expediency of laparocentesis, determines variants of formation of temporary intestinal stomas and indications for decompression of the intestinal lumen. The greatest risk of a lethal outcome is found in highly immature neonates.
Key words: intestinal stomas, intestinal decompression, neonates, ulcerative-necrotic enterocolitis
Язвенно-некротический энтероколит (ЯНЭК) - одно из наиболее тяжелых заболеваний у детей периода новорожденное™. Его этиология до настоящего времени является предметом дискуссии. Риск возникновения ЯНЭК велик у детей, перенесших перинатальную гипоксию, инфузионную терапию и гемотрансфузии, декомпенсацию кровообращения, а также находящихся в токсико-септическом состоянии. Заболевание протекает стадийно. Перитонит является наиболее частым (86,5%) его осложнением [1, 2]. Хирургическое лечение его нередко заканчивается наложением высокой колостомы, а иногда и илеостомы 5. По данным Ю.Ф.Исакова и соавт., операцией выбора является резекция некротизированного участка кишки с выведением двойной кишечной стомы, а при тотальном поражении толстой кишки - выключение ее путем наложения противоестественного заднего прохода на подвздошную кишку [11]. В.Г.Баиров и соавт. при мультилокальном поражении кишечника прибега-
Гассан Татьяна Анатольевна, кандидат медицинских наук, докторант кафедры хирургических болезней детского возраста Российского государственного медицинского университета Адрес: 103001, Москва, ул. Садово-Кудринская, 15 Телефон: (095) 254-0929
Статья поступила 20.11.2002 г., принята к печати 11.03.2005 г.
ют к множественной энтеростомии [12]. Еще ряд авторов указывают на целесообразность подобных паллиативных вмешательств, ссылаясь на выраженные нарушения регионарного кровотока у новорожденных с ЯНЭК 14.
Целью исследования явилось определение оптимальной хирургической тактики лечения и послеоперационного ведения новорожденных с ЯНЭК.
Пациенты и методы
Проведен анализ результатов лечения 63 новорожденных (36 мальчиков, 27 девочек) с хирургическими осложнениями ЯНЭК, поступивших в отделение хирургии новорожденных детской городской клинической больницы №13 им. Н.Ф.Фи-латова за период с 1998 по 2001 гг. Поводом для перевода больных в специализированное отделение явилось резкое ухудшение их состояния: рвота с примесью желчи или кишечного содержимого, вздутие и болезненность живота, напряжение передней брюшной стенки, скудный стул с примесью крови либо его отсутствие, выраженные гемодинами-ческие нарушения - централизация кровообращения, дегидратация, инфекционный токсикоз. При анализе архивного и клинического материала было выявлено, что в 61 % наблюдений ЯНЭК развился у недоношенных детей, родившихся с ге-
стационным возрастом от 26 до 37 нед (преимущественно 32-36 нед) с указанными выше факторами риска. Состояние гипоксии перенесли 30 (47,6%) детей, внутриутробное инфицирование - 11 (17,5%). У 14 (23,7%) новорожденных было перинатальное поражение ЦНС, у 9 - критически низкая масса тела (менее 1000 г). В 2 наблюдениях ЯНЭК сочетался с болезнью Гиршпрунга, в 2 - с дивертикулом Меккеля, у 1 ребенка - с болезнью Дауна, у 5 - с врожденным пороком сердца. Связи заболевания с полом ребенка не выявлено.
Помимо тщательного клинического обследования всем детям при поступлении проводили ультразвуковое исследование и обзорную рентгенографию брюшной полости, а в случае необходимости (4 наблюдения) - контрастное исследование желудочно-кишечного тракта наряду с неинвазивными методами диагностики, у части пациентов выполняли лапароцентез, показанный при подозрении на перфорацию полого органа.
Результаты исследования и их обсуждение
Больные ЯНЭК поступали в сроки, зависевшие от формы течения заболевания. При молниеносной форме (58,7%) на 1-5-е сут жизни развивалась клиническая картина перитонита. Одиннадцать детей поступили на 2-10-е сут жизни с направляющим диагнозом «кишечная непроходимость». У 7 из них при поступлении диагностирована перфорация полого органа, у 2 при операции выявлена предперфорация и у 2 - динамическая непроходимость (2-я стадия заболевания).
При поступлении у детей выявлялись следующие клинические симптомы: сухость языка, западение большого родничка, рвота (45,8%), застойное содержимое желудка (76,3%) или кишечника (23,7%), вздутие живота, отечность, усиление сосудистого рисунка, цианотичный оттенок кожи и напряжение передней брюшной стенки, болезненность при пальпации живота. Меконий после рождения отходил самостоятельно у всех детей. При поступлении стул получали после клизмы в виде кала (мекония, слизи) с кровью, у 9 новорожденных стул полностью отсутствовал.
При обзорной рентгенографии в 68,3% наблюдений выявлен свободный газ в брюшной полости (хотя число случаев перфорации полого органа достигало 76,2%), в 22% была затемнена ее нижняя половина. У 25% больных отмечены уровни жидкости, у остальных газонаполнение кишечника было повышено или неравномерно. Утолщение стенок кишечника определялось у 41,3% больных, пневматоз кишечной стенки и «газ» в портальной системе печени обнаружены только у 4 детей. Контрастное исследование кишечника проведено 4 детям с подозрением на кишечную непроходимость: из них у 2 эвакуация контрастного вещества происходила своевременно, а у 2 - замедленно.
Как показал наш опыт, почти в 8% случаев перфорации кишки рентгенография не выявила свободного газа в брюшной полости. В таких случаях, особенно при затемнении нижней половины брюшной полости в вертикальном положении, утолщении кишечных стенок при рентгенографии или выявлении жидкости в брюшной полости при ультразвуковом исследовании, показан лапароцентез, позволяющий определить хирургическую тактику. Так, примесь мекония или кала в выпоте брюшной полости указывает на перфорацию полого органа и является показанием к лапаротомии, а
прозрачный выпот у больного ЯНЭК позволяет ограничиться интенсивной терапией.
Таким образом, в 68,3% наблюдений показаниями к экстренному оперативному вмешательству послужили клинические проявления перфоративного перитонита, подтвержденные рентгенологическими данными. У 8 пациентов перфорация полого органа была дополнительно подтверждена характером содержимого брюшной полости, полученного путем лапароцентеза, у остальных - клинической картиной перитонита и кишечной непроходимости.
Наиболее часто поражались подвздошная кишка (у 20 пациентов), селезеночный угол (у 9) и поперечный отдел ободочной кишки (у 5). В 8 наблюдениях перфорации кишки были множественными. У всех детей этой группы в ходе операции была выведена кишечная стома. Варианты наложения стомы зависели от характера повреждения кишечной стенки (см. таблицу).
При множественных перфорациях, участках предперфо-раций и нарушениях микроциркуляции формировали двуствольную илеостому выше места поражения (у 23 пациентов). В наблюдениях с единичными перфорациями без нарушения микроциркуляции на переднюю брюшную стенку выводили поврежденный участок в виде двуствольной энтеро-стомы (у 2). При одиночных, но обширных поражениях всей окружности кишки производили резекцию некротизирован-ных участков с формированием двуствольной раздельной (у 11) или одноствольной концевой (у 19) энтеростомы. В 8 наблюдениях через стому интубировали приводящий отдел кишки. Объем оперативного вмешательства обязательно включал также ревизию органов, санацию и дренирование брюшной полости.
В раннем послеоперационном периоде у 20 детей возникли осложнения, связанные с неблагоприятным течением основного заболевания на фоне недоношенности и морфофункциональной незрелости. У 9 из них на 2-5-е сут после операции произошла перфорация приводящей петли кишки
Таблица. Оперативные вмешательства у новорожденных с
Характер и уровень Виды оперативных вмешательств Число
Перфорация Резекция некротизированного участка, 9
толстой кишки одноствольная колостомия
То же, с интубацией просвета 3
Ушивание дефекта, двуствольная 7
энтеростомия выше перфорации
То же, с интубацией просвета 3
Множественная Резекция некротического участка. 4
перфорация ушивание мелких дефектов, одноствольная
толстой кишки илеостомия
То же, раздельная илеостомия 2
То же, двуствольная колостомия 1
Перфорация Ушивание дефекта, двуствольная 11
подвздошной кишки илеостомия выше перфорации
Резекция некротического участка, 8
Резекция, одноствольная илеостома 3
Ушивание перфорации 1
Двуствольная илеостома (место перфорации) 2
Перфорация Резекция, прямой анастомоз 2
тощей кишки Резекция, прямой анастомоз, аппендикостотн (гастростомия) 1 +(1)
Предперфорация Двуствольная илеостомия выше места поражения 5
выше стомы, у 1 - перфорация желудка, в связи с чем при повторном вмешательстве дополнительно сформирована гастростома по Кадеру. В 1 наблюдении развилась ранняя спаечная кишечная непроходимость. У 1 больного осложнилась одноствольная колостома, наложенная на поперечноободочный отдел кишки: на 12-е сут после операции наступило расхождение краев раны и несостоятельность стомы на фоне пареза кишечника и ДВС-синдрома.
Нами отмечено, что повторная перфорация кишки и спаечная кишечная непроходимость были наиболее вероятны у тех больных, которым не проводили интубацию кишки. У 8 новорожденных развившиеся осложнения потребовали релапаротомии. Характер повторного вмешательства определялся индивидуально. Так, при несостоятельности одноствольной колостомы последняя была ликвидирована, сформирован прямой анастомоз с декомпрессией зондом, установленным через анальный проход. Операция по поводу перфорации желудка завершилась ушиванием дефекта, санацией и дренированием брюшной полости. При повторной перфорации подвздошной кишки в 3 случаях ушивали дефект и проводили интубацию кишки через гастростому, вновь сформированную аппендикостому или уже имеющуюся илеостому. В 1 наблюдении был резецирован измененный фрагмент подвздошной кишки, создан прямой анастомоз, декомпрессия которого осуществлялась через аппендикостому. При перфорации селезеночного угла (ранее был сформирован противоестественный задний проход на сигмовидной кишке) выведена одноствольная колостома. При спаечной непроходимости одноствольная колостома была заменена на двуствольную илеостому с интубацией приводящего отдела.
Существенное значение имело и комплексное консервативное интенсивное лечение в раннем послеоперационном периоде, включавшее инфузионную терапию, полное парентеральное питание до восстановления пассажа по приводящему отделу кишки с последующим введением энтерального кормления, а также рациональную антибактериальную терапию. Учитывая общую метаболическую направленность, нарушение ферментативной активности и снижение всасывающей способности тонкой кишки в патологических условиях, целесообразно использование в энтеральном кормлении пациентов специальных элементных смесей. Особую значимость лечебное энтеральное питание имеет в случае развития синдрома короткой кишки. В наших наблюдениях этот синдром развился у 5 больных с обширным поражением тонкой кишки, из них у 4 исход был летальным.
Летальность больных с ЯНЭК составила 34,9%. Почти половина (45,5%) этих детей имели гестационный возраст 27-32 нед и половина - массу тела от 800 до 1500 г. В 9 случаях отмечалось прогрессирующее течение ЯНЭК и перитонита, приведшее к летальному исходу в 8 из них. При патолого-ана-томическом исследовании основными причинами смерти были сепсис, фибринозно-геморрагический перитонит, кровоизлияния в желудочки головного мозга, двусторонняя пневмония.
Показанием к формированию энтеростом является необходимость полного выключения пораженного (дистального) участка кишки с целью создания условий для восстановле-
ния микроциркуляции в ее стенке и заживления ушитых перфораций. При мультилокальном поражении кишечника оправдано выведение нескольких стом для предотвращения развития синдрома короткой кишки.
Возможность развития послеоперационных осложнений значительно снижается при формировании раздельной эн-теростомы в случае резекции некротизированного сегмента и петлевой энтеростомы на расстоянии не менее 15-20 см от места нарушения микроциркуляции.
Анализ результатов хирургического лечения новорожденных с осложненным течением ЯНЭК показал, что интубация приводящего отдела кишки абсолютно показана при парети-ческом расширении просвета кишечника, утолщении кишечных стенок, фибринозных наложениях на висцеральной и париетальной брюшине, а также при ушивании перфораций и формировании кишечных анастомозов.
1. Баиров Г.А., Островский Е.А. Хирургия толстой кишки у детей. Л.: Медицина, 1974; 27-35, 46-7, 81,122,149-55,166-8.
2. Moore T.S. Successful use of the «patch, drain and wait» laparotomy approach to perforated necrotizing enterocolitis: is hypoxia-triggered «good angiogenesis» involved? J Pediatr Surg Int 2000; 16: 356-63.
3. Баиров Г.А., Манкина H.C. Поражение толстой кишки у новорожденных с язвенно-некротическим энтероколитом. В кн.: 8 съезд хирургов Дагестана. Махачкала, 1978; 53-4.
4. Баиров Г.А., Манкина Н.С. Хирургия недоношенных детей. Л.: Медицина, 1987; 106-7,114-5,123-4.
5. Joppich I., Kellnar S. Surgery of atresia of the gastrointestinal tract. J Chir 1996; 67(6): 576-83.
7. Ионушене С.В. Клинико-морфологическое обоснование патогенеза и тактики лечения некротизирующего энтероколита у новорожденных детей. Авто-реф. дисс. . канд. мед. наук. М., 2002; 24.
8. Каншин Н.Н., Каншина О.А. Хирургическое лечение неспецифического язвенного колита у детей. Вестник хирургии 1980; (12): 97-101.
9. Соопе H.J., Eigler P.W. Chirurgische Therapie bei Kolonperforationen. Zbl Chir 1987; 112(14): 914-8.
10. Faching G., Hollwarth M.E., Schmidt B., Mayr J. Surgical strategies in very low birth weight neonates with necrotizing enterocolitis. Acta Paediatr Suppl 1984; 396: 62-4.
11. Исаков Ю.Ф., Степанов Э.А., Красовская T.B. Абдоминальная хирургия детей. М.: Медицина, 1988; 126-43,171-7.
12. Баиров В.Г., Караваева С.А. Об опыте хирургического лечения некротического энтероколита. Актуальные проблемы детской хирургии. Сборник научных трудов. Саратов, 2002; 16-20.
13. Подкаменев В.В., Новожилов В.А., Подкаменев А.В. Регионарный кровоток при хирургических заболеваниях кишечника у новорожденных детей. Неотложные состояния у детей. Материалы VI Конгресса педиатров. М., 2000; 231.
14. Chirdan L.B., Aameh Е.А. Neonatal intestinal perforation in a developing country. J Ann Trop Pediatr 2001; 21(1): 26-8.
15. Fasoli L., Turi R.A., Spitz L., et al. Necrotizing enterocolitis extent of disease and surgical treatment. J Pediatr Surg 1999; 34:1096-999.
Патогенез язвенного некротизирующего энтероколита (ЯНЭК)
Патогенез язвенного некротизирующего энтероколита (ЯНЭК)
Большинство информации о патогенезе язвенного некротизирующего энтероколита (ЯНЭК) основано на данных эпидемиологических исследований, оценке индивидуальных наблюдений и результатах исследований на животных. До сих пор не удалось создать такую модель язвенного некротизирующего энтероколита (ЯНЭК) у животных, которая была бы полностью идентична тому, что наблюдается у недоношенных детей.
Это означает, что на основании современных методов исследования пока можно только предположить тесную взаимосвязь таких факторов, как генетическая составляющая, незрелость кишечника (изначальное состояние иммунитета), микробное окружение и питание.
Генетические факторы язвенного некротизирующего энтероколита (ЯНЭК)
В последнее время с помощью методов логистической регрессии была оценена вероятность семейной и генетической предрасположенности к ЯНЭК, внутрижелудочковым кровоизлияниям и бронхолегочной дисплазии (БЛД). Исследования близнецов подтверждают теорию о семейной природе данных заболеваний.
Учитывая генетическую предрасположенность к указанной патологии, установление чувствительного и специфичного, выполняющего прогностическую функцию генетического маркера было бы полезно в плане профилактики этих состояний. Было выдвинуто предположение о возможной роли в развитии язвенного некротизирующего энтероколита (ЯНЭК) неадекватного врожденного иммунного ответа на бактериальные антигены кишечной микрофлоры.
Были проанализированы одиночные нуклеотидные полиморфизмы CD14, TLR4 и CARD15 у детей с ОНМТ при наличии язвенного некротизирующего энтероколита (ЯНЭК) и без него. В результате связь с повышенным риском возникновения язвенного некротизирующего энтероколита (ЯНЭК) не была подтверждена.
Дополнительная оценка с помощью сложной геномной и протеомической технологии может дать новую важную информацию о маркерах заболевания, что позволит выявлять пациентов из группы высокого риска и придавать профилактическим мероприятиям более индивидуальный характер вместо рутинной профилактики у всех детей.
Незрелость кишечника при язвенном некротизирующем энтероколите (ЯНЭК)
По мере созревания недоношенного ребенка развитие ЖКТ обусловливает более выраженную его способность к перевариванию и всасыванию. Однако кишечник не только участвует в переваривании и всасывании компонентов пищи, но и является одним из наибольших по размеру иммунных органов. Он выполняет важные эндокринную и экзокринную функции и содержит равное по объему спинному мозгу количество нервной ткани.
По мере развития ЖКТ отмечается значительный его рост. Так, в III триместре происходит удвоение длины кишечника плода, а увеличение площади поверхности кишечника идет еще более быстрыми темпами (в основном за счет роста ворсин и микроворсин в течение этого периода). Таким образом, чем больше степень недоношенности ребенка, тем ограниченнее его способность переваривать и усваивать пищу и тем сложнее удовлетворить его повышенную потребность в питании, особенно в стрессовых ситуациях.
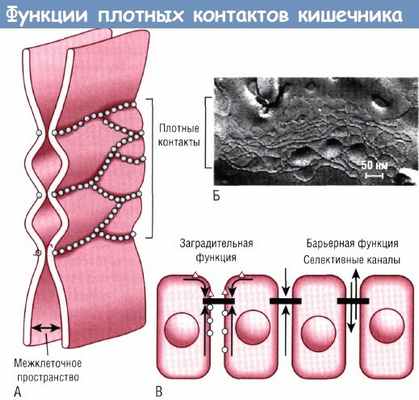
Физико-химические условия и барьерная функция кишечника при язвенном некротизирующем энтероколите (ЯНЭК)
Особенности развития врожденной и адаптивной иммунных систем у новорожденных остаются малоизученными. Некоторые составляющие врожденной иммунной системы не только определяют реакцию на возникающие в неонатальном периоде непродолжительные заболевания, но и имеют значение в дальнейшей жизни. Врожденный кишечный барьер важен в плане профилактики транслокации бактерий и инициации воспалительного ответа, который может влиять не только на кишечник, но и на состояние отдаленных органов, таких как легкие и ЦНС.
Одна из первых линий защиты против попавших в пищеварительный тракт патогенов и токсинов представлена полостным пищеварением в желудке и двенадцатиперстной кишке. Физико-химические особенности незрелого ЖКТ заключаются в сниженной продукции иона водорода в желудке и низкой протеолитической активности ферментов поджелудочной железы.
Вероятно, относительно низкая активность энтерокиназы и низкая активность трипсина подавляют гидролиз токсина, обладающего способностью повреждать кишечник. Таким образом, незрелое полостное пищеварение может предрасполагать к проникновению патогенов извне и их колонизации в дистальных отделах ЖКТ.
Действительно, недавно проведенные исследования подтвердили связь дальнейшего снижения и без того низкой продукции кислоты в желудке при использовании Н2-блокаторов у недоношенных детей с большой частотой возникновения ЯНЭК.
Барьерная функция незрелого кишечника детально обсуждена в отдельной статье на нашем сайте. В этой статье будут кратко представлены те данные о развитии кишечника, которые имеют отношение к ЯНЭК.
Вся информация о барьерной функции и возможном процессе воспаления в кишечнике получена из исследований, проведенных на животных и культурах клеток, но некоторые исследования с участием новорожденных детей также начинают раскрывать неясные моменты. Опыты на животных показали, что слой кишечной слизи у новорожденных недостаточен и отличается по составу от слоя кишечной слизи у взрослых.
Это приводит к большей проницаемости незрелого кишечника для молекул с большой молекулярной массой, а также может усиливать прилипание бактерий к эпителию.
У незрелых новорожденных отмечается большая проницаемость кишечной стенки по сравнению с детьми старшего возраста и взрослыми. При получении идентичного объема молока недоношенные дети, родившиеся на сроке гестации менее 33 нед, имеют более высокую концентрацию бета-лактоглобулина в сыворотке крови по сравнению с доношенными детьми.
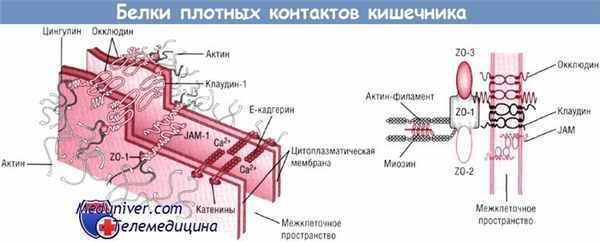
Проницаемость кишечника недоношенного ребенка для интактных углеводных маркеров, например лактулозы, является демонстрацией изменений, связанных с развитием, а именно с повышением проницаемости кишечника по мере его созревания. В настоящее время мало информации о созревании белков плотных контактов (окклюдина и клаудинов), которые составляют основу околоклеточного барьера эпителия.
Если белки плотных контактов более чувствительны к токсинам и другим неблагоприятным факторам в незрелом кишечнике, то стимуляция синтеза белков плотных контактов представляется перспективной целью в плане проведения профилактических или лечебных мероприятий.
Моторика тонкой кишки у недоношенных новорожденных значительно менее скоординирована по сравнению с моторикой у доношенных детей. Эта особенность объясняется значительной незрелостью ЭНС. Малая подвижность кишечника приводит к задержке прохождения пищи, что обусловливает интенсивное размножение бактерий и расширение кишечника из-за обилия газов, являющихся побочными продуктами ферментации.
Похоже, что недостаточная подвижность кишечника, связанная с незрелостью, создает условия, при которых взаимодействие нутриентов, незрелой защиты организма хозяина и других факторов инициирует ряд событий, вызывающих переход микроорганизмов и их токсических продуктов через незрелый барьер слизистой оболочки кишечника. Кульминацией этих процессов является воспалительная реакция, приводящая к ЯНЭК.
Медиаторы воспаления при язвенном некротизирующем энтероколите (ЯНЭК)
Так же, как при сепсисе или респираторном дистресс-синдроме взрослого типа, в патогенезе ЯНЭК присутствует конечная стадия эндогенной продукции медиаторов воспаления, имеющих значение в развитии повреждения кишечника. В общей конечной стадии патогенеза ЯНЭК принимают участие эндотоксин ЛПС, PAF, TNF и другие цитокины вместе с простагландинами, лейкотриенами и оксидом азота.
Некоторые бактерии имеют эндотоксины, которые провоцируют каскад воспалительных реакций, активируя PAF, TNF и IL-1. В этом процессе участвует и IL-8 — очень сильный, притягивающий нейтрофилы хемокин. Недавно было подтверждено участие и других цитокинов, таких как IL-12 и IL-18.
Необходимо лучше понимать процесс каскада воспалительных реакций, поскольку его прерывание или предупреждение его начала с помощью питания или фармакологических средств может быть превентивной мерой в отношении ЯНЭК. Например, было выявлено, что PAF, введенный в аорту взрослых крыс, вызывает некроз кишечника, который можно предупредить предварительным назначением PAF-ацетилгидролазы или усилить ингибитором синтазы оксида азота.
Некоторые нутриенты, такие как омега-3 жирные кислоты, глютамин, аргинин или пробиотические бактерии, также могут играть определенную роль в профилактике ЯНЭК, прерывая или предупреждая каскад воспалительных реакций.
Микрофлора при язвенном некротизирующем энтероколите (ЯНЭК)
Обзор среды микроорганизмов в ЖКТ и ее взаимосвязь с заболеванием подробно изложены Claud и Walker в главе 5, а данная глава содержит лишь краткое обсуждение этого вопроса. ЖКТ человека и других млекопитающих колонизирован огромным количеством микроорганизмов, совокупность которых называют микробиотой. Функцию этих микроорганизмов, представленных в основном комменсалами и симбионтами, только начинают понимать.
В настоящее время известно, что одна из функций этих микроорганизмов заключается в полостном пищеварении не абсорбируемых другим путем углеводов и секреции жирных кислот (например, бутирата), которые участвуют в поддержании функции интестинального барьера и пролиферации. Взаимодействие друг с другом (cross-talk) микробиоты и кишечника приводит к тому, что стимуляция секреции пептидов клетками Панета способствует ангиогенезу и росту, а также создает среду, которая предупреждает размножение потенциально патогенных микроорганизмов.
Существует несколько доказательств необходимости наличия инфекции для развития ЯНЭК. В крови новорожденных с ЯНЭК часто обнаруживают бактерии. Однако спорным остается вопрос, играют ли выделенные бактерии первичную роль в патогенезе ЯНЭК или представляют собой в основном микроорганизмы полости кишечника, которые проникли через поврежденный барьер слизистой.
Большое разнообразие бактерий, ассоциирующихся с ЯНЭК, позволяет предположить, что они являются сопутствующими факторами, которые активируют иной процесс или процессы. Возможно также, что обнаруживаемые при ЯНЭК микроорганизмы обладают пока еще не установленным патогенетическим свойством, из-за которого провоцируется развитие заболевания.
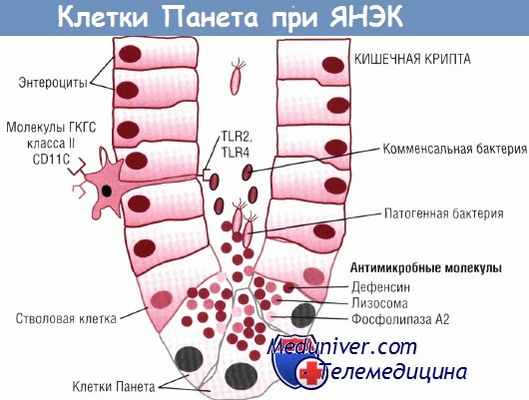
Клетки Панета функционально схожи с нейтрофилами: при взаимодействии с бактериями или их продуктами клетки Панета выделяют в полость крипты антимикробные молекулы. Стволовые клетки постоянно пополняют эпителиальные клетки, которые мигрируют и погибают на верхушке ворсинок. Клетки Панета защищают стволовые клетки, оказывая протективное действие по отношению к обновлению эпителиальных клеток.
TLR — Toll-подобные рецепторы;
ГКГС — главный комплекс гистосовместимости.
В ОИТН большинству детей с выраженной недоношенностью сразу после рождения, согласно алгоритму профилактики или раннего лечения сепсиса, начинают проводить антибактериальную терапию препаратами широкого спектра действия. Это может нарушить процесс колонизации кишечника новорожденного нормальной микрофлорой. Резистентные микроорганизмы, характерные для ОИТН, могут колонизировать кишечники детей в большей степени, чем лактобактерии, бифидобактерии и другие симбиотические бактерии.
Пока неизвестно, играет ли это какую-либо роль в патогенезе ЯНЭК и в какой степени, но некоторые микроорганизмы имеют большую предрасположенность к активации рецепторов поверхности клеток. Эти рецепторы передают сигнализирующие молекулы (например, NFkB) к ядру, которое, в свою очередь, стимулирует провоспалительный ответ посредством синтеза провоспалительных цито- и хемокинов. Более того, опыты на грызунах показали, что введение антибиотиков увеличивает предрасположенность кишечника к геморрагическому колиту и в значительной степени нарушает экспрессию многочисленных генов, связанных с развитием кишечника.
Комменсальная микрофлора может выступать в роли пускового механизма воспалительного ответа кишечника. Эпителий кишечника, отчасти из-за наличия TLR, выступает в роли проводника между полостной микрофлорой и путями передачи клеточного сигнала. TLR — это рецепторы на поверхности клеток, распознающие специфические лиганды микроорганизмов (как патогенов, так и комменсалов).
TLR дают возможность иммунной системе отличать чужеродные агенты и активируют как врожденный, так и адаптивный иммунный ответ. Недавно проведенные исследования позволили предположить, что эпителий и резидентные иммунные клетки не только толерантны к существованию микроорганизмов-комменсалов, но и зависят от них. Это важно для понимания сути не только таких заболеваний в ОИТН, как ЯНЭК, частота которого, согласно недавно проведенным исследованиям, снижается при назначении пробиотиков, но и тех заболеваний, которые встречаются у детей в дальнейшей жизни (например, аллергии и атопии). Более того, вполне возможно, что такие агонисты TLR, как ЛПС, действительно могут выступать в роли полезных терапевтических средств при профилактике ЯНЭК и другой патологии кишечника.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Некротический энтероколит
Некротический энтероколит является приобретенным заболеванием, прежде всего у недоношенных или больных новорожденных, и характеризуется некрозом слизистой оболочки или даже более глубоких слоев кишечника. Его развитие является самой частой опасностью для младенцев со стороны желудочно-кишечного тракта. Симптомы и признаки включают непереносимость пищи, вялость, неустойчивость температуры, непроходимость кишечника, вздутие живота, рвоту с примесью желчи, кровавый стул, редуцирующие вещества в стуле, апноэ и иногда признаки сепсиса. Диагноз клинический; подтверждают методами визуализации. Лечение в первую очередь поддерживающее и включает аспирацию содержимого желудка через назогастральный зонд, парентеральное введение жидкостей, полное парентеральное питание, антибиотики, изоляцию в случае инфекционных заболеваний и иногда хирургическое вмешательство.
Факторы риска
Асфиксия при рождении
Изменение микробиома кишечника (дисбиоз)
Кормление молоком нечеловеческого происхождения
Как правило, присутствуют три кишечных фактора:
Предшествующий ишемический инсульт
Внутрипросветный субстрат (те, энтеральное питание)
Этиология НЭК
Точная этиология некротического энтероколита не выяснена. Однако предрасполагающими факторами являются повышенная проницаемость и недоразвитая иммунная функция незрелого кишечного тракта. Считается, что ишемический инсульт повреждает слизистую оболочку кишечника, что приводит к повышенной проницаемости кишечника и делает его восприимчивым к бактериальной инвазии. Некротический энтероколит редко возникает до начала применения энтерального питания и менее распространен среди младенцев на грудном вскармливании. Однако, как только было начато кормление, в просвете кишечника появляется достаточно субстрата для распространения бактерий, которые могут проникнуть в поврежденную стенку кишечника, вырабатывая газообразный водород. Газ может собираться в кишечной стенке (пневматоз кишечника) или попадать в воротную вену. Дисбактериоз (изменение микробиома кишечника), например, возникающий после лечения антибиотиками или препаратами снижающими кислотность, также может быть способствующим фактором, так как при нем возрастает количество условно-патогенных бактерий.
Первоначальный ишемический инсульт может быть результатом спазма брыжеечных артерий, вызванного бескислородным инсультом, запускающим примитивный дайвинг-рефлекс, который заметно уменьшает кишечный кровоток. Кишечная ишемия может также быть результатом низкого кровотока во время обменного переливания крови, при сепсисе или из-за использования гиперосмолярных смесей. Точно так же врожденный порок сердца с уменьшенным системным кровотоком или насыщением кислородом артериальной крови может привести к кишечной гипоксии/ишемии и предрасполагает к развитию некротизирующего энтероколита.
Некротизирующий энтероколит может возникнуть как группа случаев или как вспышки в отделениях интенсивной терапии новорожденных. Некоторые группы случаев, скорее всего, связаны с конкретными возбудителями (например, с Klebsiella, Escherichia coli, коагулазонегативными стафилококкамиn Pseudomonas, Clostridioides difficile), но тем не менее специфический патоген при этом часто бывает не идентифицирован.
Осложнения некротического энтероколита
Некроз начинается в слизистой оболочке и может прогрессировать до вовлечения стенки кишечника на всю толщину, что приводит к кишечной перфорации Острая перфорация желудочно-кишечного тракта Перфорация может происходить на любом уровне желудочно-кишечного тракта; при этом содержимое желудка или кишечника поступает в полость брюшины. Причины различны. Клинические симптомы развиваются. Прочитайте дополнительные сведенияСимптомы и признаки НЭК
У младенцев могут быть трудности с кормлением, остатки крови и желчи в желудке (после кормления), которые могут перейти в желчную рвоту, кишечная непроходимость проявляется вздутием живота или же большим количеством крови в стуле. Сепсис может проявляться вялостью, нестабильностью температуры, учащенными приступами апноэ и метаболическим ацидозом.
Некротизирующий энтероколит и спонтанная перфорация кишки. MHO
A.
Некротизирующий
энтероколит
(НЭК)
приобретенное
заболевание
у
новорожденных,
представляющее собой конечный этап поражения
кишечника вследствие
сочетания сосудистых и
метаболических
нарушений, развивающихся в
относительно незрелом кишечнике
B. Спонтанная перфорация кишечника является
клиническим синдромом, причина которого в
большинстве случаев неизвестна, с менее агрессивным
течением. Может представлять собой вариант
классического НЭК
или быть следствием других
пороков или системных заболеваний
3. Частота встречаемости
НЭК чаще всего развивается у
недоношеных младенцев
6-10% 70% до 90% у новорожденных с низкой
массой тела
10-25% у доношенных новорожденных
4. Патофизиология.
1.
2.
3.
4.
В настоящее время нет единой объединяющей теории
патогенеза НЭК, которая удовлетворительно объясняет
все клинические наблюдения, связанные с этим
расстройством.
потеря
целостности
слизистой
кишечника
(ишемическая, токсическая).
бактериальная пролиферация, связанная с кормлением
колонизация слизистой кишечника патогенной флорой,
с развитием пневматоза кишечника.
последующий трансмуральный некроз или гангрена
кишки с развитием перитонита..
5. Факторы риска
A. Недоношенность
B. Асфиксия и врожденные пороки сердца приводят к снижению
сердечного выброса и уменьшению перфузии, что ведет к редукции
брыжеечного кровообращения с ишемией кишечника
C. Энтеральное питание
NB! Около
90-95% новорожденных получали энтеральное
питание
1. Энтеральное питание обеспечивает необходимый субстрат для
пролиферации кишечных патогенов.
2. Гиперосмолярная формула питания вызывают изменение
проницаемости слизистой оболочки и ее повреждение.
3. В коммерчески приготовленных формулах и в хранящемся
грудном
молоке
существует
потеря
или
отсутствие
иммунопротекторных факторов.
4. Кормление грудью значительно снижает риск развития НЭК
D. Полицитемия.
E. Заменное переливание Эр-массы .
6. Факторы риска
F. Объемы кормления, сроки энтерального питания
и быстрое продвижение энтеральных кормов. Они,
похоже,
играют
определенную
роль,
но
клинические данные остаются спорными.
G.
Энтеропатогенные
микроорганизмы.
Бактериальные и вирусные патогены, включая
Escherichia
coli,
Klebsiella,
Enterobacter,
Pseudomonas,
Salmonella,
Staphylococcus
epidermidis,
Clostridium
sp,
коронавирусы,
ротавирусы и энтеровирусы, были прямо или
косвенно связаны с культурами крови, стула или
перитонеального пространства.
7. Критерии диагностики
Предварительный диагноз НЭК может быть
выставлен у любого младенца с триадой
симптомов:
1. Неусвояемость питания
2. Вздутие живота
3. Гематохезис
В качестве альтернативы, самые ранние
признаки могут быть идентичны таковым
при неонатальном сепсисе.
8. Клиническая картина
Время начала НЭК изменяется обратно пропорционально
гестационному возрасту.
В группе новорожденных с экстерамально низкой массой тела
клиническая картина неизменно следует за началом энтеральных
кормлений и обычно диагностируется между 14 и 20 днями
У доношенных новорожденных заболевания развивается в течение
первой недели жизни.
Клиническая картина может варьировать от вздутия живота
(наиболее частый ранний признак, отмеченный в 70% случаев),
развитием кишечной непроходимости и увеличением объема
остаточного объема желудочного аспирата или застойного
отделяемого с примесью желчи (2/3 случаев) до явных признаков
шока, мелены, перитонита и перфорации.
Сложными для диагностики являются случаи неспецифических
проявлений: лабильная температура, апноэ, брадикардия или
другие признаки начинающегося септического процесса.
9. Стадия 1. Подозреваемый НЭК
1. Системные признаки неспецифичны,
включая апноэ, брадикардию, летаргию и
температурную нестабильность.
2. Кишечные проявления проявляются в
увеличения остаточного объема желудка и
появление крови в кале.
3. Рентгенологические данные являются
нормальными или неспецифическими.
10. Стадия 2А.
1. Системные признаки сходны с
таковыми в стадии I.
2. Выраженное вздутие живота с или
без напряжения, отсутствие
перистальтики и кровь в стуле.
3. Рентгенографические данные
включают признаки непроходимости,
ограниченный пневматоз кишечной
стенки
11. Стадия 2 Б
1. Ацидоз и тромбоцитопения
2. Отек
и напряжение передней
брюшной
стенки,
отсутствие
инфильтрата в брюшной полости,
расширенные кишечные петли
3.
Распространенный
пневматоз
кишечной стенки, асцит,
газ в
портальной системе.
12. Стадия 3А
1.Респираторный и метаболический ацидоз, апноэ,
требующее проведения ИВЛ, снижение
артериального давления и снижение диуреза,
нейтропения и коагулопатия.
2. Отек передней брюшной стенки
3. Асцит, снижение газонаполнения кишечника,
возможно наличие статической петли кишки.
4. Признаков перфорации кишечника нет
13. Стадия 3В.
1.
2.
3.
Распространенные отеки, ухудшение
лабораторных показателей, рефрактерная
гипотензия, ДВС -синдром и тяжелые
электролитные нарушения
Напряжение и отек передней брюшной стенки
Отсутствие газа в кишечнике, свободный газ в
брюшной полости.
15. Обязательное обследование
16. Рентгенологические исследования
1. Обзорная рентгенография брюшной
полости
Неравномерное газообразование, кишечная
непроходимость, фиксированная петля
тонкой кишки, пневматозкишечной стенки.
б. Подтверждающие симптомы
(1) распространенный интестинальный
пневматоз и (2) газ в портальной системе при
отсутствии пупочного катетера
2. Профильные или снимки в латеропозиции
для выявления пневмоперитонеума.
17. Рентгенографические признаки 1 стадии
Неспецифические рентгенологические
данные:
Исчезновение нормальной симметрии
газонаполнения кишечника
Читайте также:
